1.原理分析 本培养基适合于肠杆菌科的鉴定。用于观察细菌对糖的利用和硫化氢(变黑)的产生。 该培养基含有乳糖、蔗糖和葡萄糖的比例为10:10:1,只能利用葡萄糖的细菌,葡萄糖被分解产酸可使斜面先变黄,但因量少,生成的少量酸,因接触空气而氧化,加之细菌利用培养基中含氮物质,生成碱性产物,故使斜面后来又变红,底部由于是在厌氧状态下,酸类不被氧化,所以仍保持黄色。而发酵乳糖的细菌(e.coli),则产生大量的酸,使整个培养基呈现黄色。如培养基接种后产生黑色沉淀,是因为某些细菌能分解含硫氨基酸,生成硫化氢,硫化氢和培养基中的铁盐反应,生成黑色的硫化亚铁沉淀。2.试验方法 以接种针挑取待试菌可疑菌落或者纯造就物穿刺接种并涂布于斜面置36±1℃造就18-24h观察结果3.化学性质 粉红色粉末,一种鉴别培养基,由牛肉膏、酵母菌膏、卵白胨、 胨、葡萄糖、乳糖、蔗糖、硫酸亚铁、氯化钠、硫代硫酸钠、酚红、琼脂等配合制造而成。易吸湿,加水煮沸熔解后成橘红色半透明液体,pH约7.5,冷至45℃开始凝固。
三糖铁琼脂培养基( l )成分 蛋白胨 20g 硫酸亚铁 0.2g 牛肉浸出粉 5g 硫代硫酸钠 0.2g 乳糖 10g 002%酚磺酞指示液 12.5ml 蔗糖 10g 琼脂 12~15g 葡萄糖 1g 水 1000ml 氯化钠 5g ( 2 )制法 除乳糖、蔗糖、葡萄糖、指示液、琼脂外,取上述成分,混合,加热使溶解,调pH 值使灭菌后为7.3 士0.1 ,加入琼脂,加热溶胀后,再加入其余成分,摇匀,分装,121 ℃ 灭菌15 分钟,制成高底层(2 ~3cm ) 短斜面。( 3 )用途 用于初步鉴别肠杆菌科细菌对糖类的发酵反应和产生硫化氢试验。 方法和结果观察:取可疑菌落或斜面培养物,做高层穿刺和斜面划线接种,置35 ℃ 培养24~ 48 小时,观察结果。培养基底层变黄色为葡萄糖发酵阳性,斜面层变黄色为乳糖、蔗糖发酵阳性;底层或整个培养基呈黑色表示产生硫化氢。
一、目的要求了解合成培养基、半合成培养基和天然培养基的配制原理。 学习和掌握麦芽汁培养基、马铃薯葡萄糖培养基、豆芽汁葡萄糖培养基和察氏培养基的配制方法。二、基本原理 麦芽汁培养基和马铃薯葡萄糖培养基被广泛用于培养酵母菌和霉菌。马铃薯葡萄糖培养基有时也可用于培养放线菌。豆芽汁葡萄糖培养基也是培养酵母菌及霉菌的一种优良培养基。察氏培养基主要用于培养霉菌观察形态用。麦芽汁培养基为天然培养基,马铃薯葡萄糖培养基和豆芽汁葡萄糖培养基二者均为半合成培养基,而察氏培养基则为合成培养基。培养基配方中出现的自然pH系指培养基不经酸、碱调节而自然呈现的pH。 三、实验材料 (一) 药品 葡萄搪、蔗糖、NaN03、K2HP04、KCl、MgSO4·7H2O,FeS04、琼脂。 (二) 仪器 天平、高压蒸汽灭菌锅。 (三) 玻璃器皿 移液管、试管、锥形瓶、烧杯、量筒、培养皿、玻璃漏斗等。 (四) 其他物品 药匙、pH试纸、称量纸、记号笔、棉花、纱布、线绳、塑料试管盖、牛皮纸、报纸、新鲜麦芽汁、黄豆芽、马铃薯等。四、实验内容 (一) 麦芽汁培养基的配制 1.培养基成分 新鲜麦芽汁一般为10-15波林。 2.配制方法 (1) 用水将大麦或小麦洗净,用水浸泡6-12h,置于15℃阴凉处发芽,上盖纱布,每日早、中、晚淋水一次,待麦芽伸长至麦粒的两倍时,让其停止发芽,晒干或烘干,研磨成麦芽粉,贮存备用。 (2) 取一份麦芽粉加四份水,在65℃水浴锅中保温3-4h,使其自行糖化,直至糖化完全(检查方法是取0.5ml的糖化液,加2滴碘液,如无蓝色出现,即表示糖化完全)。 (3) 糖化液用4-6层纱布过滤,滤液如仍混浊,可用鸡蛋清澄清(用一个鸡蛋清,加水20 ml,调匀至生泡沫,倒入糖化液中,搅拌煮沸,再过滤)。 (4) 用波美比重计检测糖化液中糖浓度,将滤液用水稀释到10-15波林,调pH至6.4。如当地有啤酒厂,可用未经发酵,未加酒花的新鲜麦芽汁,加水稀释到10-15波林后使用。 (5) 如配固体麦芽汁培养基时,加入2%琼脂,加热融化,补充失水。 (6) 分装、加塞、包扎。 (7) 高压蒸汽灭菌 100 Pa灭菌20 min。 (二) 马铃薯葡萄糖培养基的配制1.培养基成分 马铃薯 20g 葡萄糖 2 g 琼脂 1.5-2g 水 100ml 自然pH 2.配制方法 (1) 配制20%马铃薯浸汁 取去皮马铃薯200g,切成小块,加水1000ml。80℃浸泡lh,用纱布过滤,然后补足失水至所需体积。100 Pa灭菌20 min。即成20%马铃薯浸汁,贮存备用。 (2) 配制时,按每100 ml马铃薯浸汁加入2g葡萄糖,加热煮沸后加入2g琼脂,继续加热融化并补足失水。 (3) 分装、加塞、包扎。 (4) 高压蒸汽灭菌 100 Pa灭菌20 min。 (三)豆芽汁葡萄糟培养基的配制 1.培养基成分 黄豆芽 10g 葡萄糖 5g 琼脂 1.5-2g 水 100ml 自然pH 2.配制方法 (1) 称新鲜黄豆芽10g,置于烧杯中,再加入100 ml水,小火煮沸30 min,用纱布过滤,补足失水,即制成10%豆芽汁。 (2) 配制时,按每100 ml10%豆芽汁加入5g葡萄糖,煮沸后加入2 g琼脂,继续加热融化,补足失水。 (3) 分装、加塞、包扎。 (4) 高压蒸汽灭菌 100 Pa灭菌20 min。(四)察氏(czapck)培养基的配制1.培养基成分 蔗糖 3g NaN03 0.3g K2HP04 0.1g KCl 0.05g MgSO4·7H2O 0.05 g FeS04 0.001 g 琼脂 1.5-2g 蒸馏水 100ml 自然pH 2.配制方法 (1) 称量及溶化 量取所需水量约2/3左右加入到烧杯中,分别称取蔗糖、NaNO3 、K2HP04 、KCl、MgSO4。依次逐一加入水中溶解。按每100 ml培养基加入1ml 0.1%的FeS04溶液。 (2) 定容 候药品全部溶解后,将溶液倒入量筒中,加水至所需体积。 (3) 加琼脂 加入所需量琼脂,加热融化,补足失水。 (4) 分装、加塞、包扎。 (5) 高压蒸汽灭菌 100 Pa灭菌20 min。
我们测定固体样品中霉菌和酵母菌,刚开始使用“马铃薯葡萄糖琼脂(PDA)”进行测定,由于样品是灰色粉末状,培养了三天后看不出长菌迹象。 同时采用“霉菌酵母菌显色培养基”进行了检测,不到两天就长出蓝绿色圆点,根据说明书说是酵母菌,我又将PDA培养基覆盖到蓝绿色菌的平皿中培养了24小时,长出很多菌,请帮忙分析一下是什么菌?为什么同一样品采用PDA和“显色培养基”进行检测,一个可以检测出霉菌,而另一个检测不出来,很头痛,也不知道怎么判定,求助!
我想要用葡聚糖凝胶色谱来分离纯化半刀豆球蛋白分子量是104000,它本身会结合葡萄糖,那用葡聚糖凝胶色谱还能不能分来,如果不行的话,琼脂糖凝胶可以不?琼脂糖凝胶我还没有用过,所以不知道DEAE琼脂糖凝胶 FF能不能用来分离,谢谢大家了!
据美国物理学家组织网12月27日报道,美国伊利诺伊大学香槟分校食品科学与人类营养系、加州大学劳伦斯伯克利国家实验室和英国石油公司(BP)的科学家表示,他们对酿酒酵母进行了基因改造,新得到的酵母菌株可以发酵葡萄糖、纤维二糖(葡萄糖的前体物,由两个结合在一起的葡萄糖组成)和木糖,能更好更多地把植物发酵成替代燃料乙醇。相关研究发表在最新一期的美国《国家科学院院刊》上。酵母以糖为生,并在这个过程中能产生很多对人来说是“宝物”的废物——乙醇和二氧化碳,因此生物燃料工业也使用酵母将植物糖转变为生物乙醇。然而,大多数酵母无法将植物中的葡萄糖、纤维二糖和木糖这三种糖全部转化成有用的燃料,比如,酿酒酵母能很好地发酵葡萄糖,但对木糖却有心无力,这使得利用酵母制造生物燃料的成本居高不下。之前,科学家对酵母菌种进行基因改造,让其代谢木糖,但速度很慢,效率过低。研究小组成员之一、伊利诺伊大学食品科学和人类营养学教授金泳恕(音译)表示,经过基因改造的酵母无法发酵木糖的主要问题是,它接触木糖之前会吸收所有葡萄糖,酵母表面的葡萄糖转运蛋白更愿意同葡萄糖依附在一起。在此项新研究中,基因改造后的酿酒酵母可以同时将纤维二糖和木糖转化为乙醇。转化效率和转化得到的乙醇数量都提高了一倍,这主要归结于混合发酵的协同作用。金泳恕表示,新酵母菌种将木糖转化为乙醇的效率至少比目前已知酵母菌高20%,使其成为最好的发酵木糖的细菌。研究团队通过对酿酒酵母做出几个关键的改进而获得了这样的结果。首先,他们给予这种酵母一个纤维二糖转运蛋白,这意味着其能将纤维二糖直接带入细胞中,而只有当纤维二糖进入到细胞内部时,它才会被转化为葡萄糖。这种方法可以战胜酿酒酵母本身对葡萄糖的偏好,从而专注于将木糖吸收进酵母细胞中。接着,研究人员将从一个消耗木糖的酵母中提取的3种蛋白质插入酿酒酵母中,由此提高了新酵母菌种代谢木糖的速度和效率。他们也对一种人造的同功酶进行了基因修改,让木糖代谢的正常中间产物木糖醇积聚的数量最少。最后,该研究团队使用“进化工程”让新菌种利用木糖的能力达到最大。研究人员表示,混合发酵的成本优势也很明显,其乙醇产量也高于工业标准,这种研究很快将被商业化。
β-葡聚糖的活性结构是由葡萄糖单位组成的多聚糖,它们大多数通过β-1,3结合,这是葡萄糖链连接的方式。它能够活化巨噬细胞、嗜中性白血球等,因此能提高白细胞素、细胞分裂素和特殊抗体的含量,全面刺激机体的免疫系统。那么,机体就有更多的准备去抵抗微生物引起的疾病。β-葡聚糖能使受伤机体的淋巴细胞产生细胞因子(IL-1)的能力迅速恢复正常,有效调节机体免疫机能。大量实验表明,β-葡聚糖可促进体内IgM抗体的产生,以提高体液的免疫能力。这种葡聚糖活化的细胞会激发宿主非专一性防御机制,故应用在肿瘤、感染病和治疗创伤方面深受瞩目。经特殊步骤萃取且不含内毒素的β-1,3-葡聚糖在美国FDA已认定是一种安全的物质,可添加在一般食品,许多报导显示老鼠口服酵母β-1,3-葡聚糖,可增加强腹膜细胞抗菌之吞噬作用。酵母葡聚糖是存在于酵母细胞壁中的一种具有增强免疫力活性的多糖——β-葡聚糖。β-葡聚糖广泛存在于各种真菌和植物,如香菇、灵芝、燕麦中,是它们发挥保健作用的主要功效物质。而酵母葡聚糖的免疫增强活性更强,并具有改善血脂、抗辐射、改善肠道功能的作用。
1、培养基 除另有规定外,培养基制备的灭菌条件为121℃20分钟。 1.1 营养琼脂培养基与营养肉汤培养基 1.1.1 营养琼脂培养基 胨 10g 琼脂 15~20g氯化钠 5g 肉浸液 1000ml 取胨、氯化钠和琼脂加入肉浸液,加热溶解后,调PH为弱碱性,煮沸、滤清,调节PH值使灭菌后为7.2±0.2,分装,灭菌。 1.1.2 营养肉汤培养基 胨 10g 肉浸液 1000ml氯化钠 5g 取胨和氯化钠加入肉浸液,微温溶解后,调PH为弱碱性,煮沸,滤清,调节PH值使灭菌后为7.2±0.2,分装,灭菌。 1.2 玫瑰红钠琼脂培养基 胨 5g 玫瑰红钠 0.0133g葡萄糖 10g 琼脂 15~20g 磷酸二氢钾 1g 水 1000ml 硫酸镁 0.5g 除葡萄糖、玫瑰红钠外,取上述成分,混合,加热溶化后,滤过,加入葡萄糖、玫瑰红钠,分装,灭菌。 1.3 酵母浸出粉胨葡萄糖琼脂培养基(YPD) 胨 10g 琼脂 15~20g 酵母浸出粉 5g 水 1000ml 葡萄糖 20g 除葡萄糖外,取上述成分,混合,加热溶化后,滤过,加入葡萄糖,分装,灭菌。 1.4 胆盐乳糖培养基(BL) 胨 20g 磷酸二氢钾 1.3g乳糖 5g 牛胆盐(或去氧胆酸钠0.5g) 2g 氯化钠 5g 水 1000ml 磷酸氢二钾 4.0g 除乳糖、牛胆盐外,取上述成分,混合,加热使溶解,调节PH值使灭菌后为7.4±0.2,煮沸,滤清,加入乳糖、牛胆盐,分装,灭菌。 1.5 曙红亚甲蓝琼脂培养基(EMB) 营养琼脂培养基 100ml 曙红钠指示液 2ml20%乳糖溶液 5ml 亚甲蓝指示液 1.3~1.6ml 取营养琼脂培养基,加热溶化后,冷至60℃,按无菌操作加入灭菌的其他3种溶液,摇匀,倾注平皿。 1.6 麦康凯琼脂培养基(MacC) 胨 20g 1%中性红指示液 3ml乳糖 10g 琼脂 15~20g 牛胆盐 5g 水 1000ml 氯化钠 5g 除乳糖、指示液、牛胆盐及琼脂外,取上述成分,混合,加热使溶解,调节PH值使灭菌后为7.2±0.2,加入琼脂,加热溶化后,再加入其余各成分,摇匀,分装,灭菌,冷至约60℃,倾注平皿。 1.7 4-甲基伞形酮葡糖苷酸(4-Methylumbelliferyl-β-D-Glucuronide,MUG)培养基 胨 10g 磷酸二氢钾 0.9g硫酸铵 5g 磷酸氢二钠(无水) 6.2g 硫酸锰 0.5mg 亚硫酸钠 40mg 硫酸锌 0.5mg 去氧胆酸钠 1g硫酸镁 0.1g MUG 75mg 氯化钠
如题,采用平板计数琼脂 菌落总数中到底包不包括酵母菌与霉菌?谢谢
葡萄酒在瓶装时,必须认真考虑葡萄酒是否已经达到了除菌、灭菌的目的。为了准确达到这个目的,就要对瓶装的葡萄酒进行快速而可靠的检验。这里列举了3个检查方法,仅供同行朋友们在实际生产中,根据企业的实际条件进行参考。 一、格森海姆(Geisenheimer)检定法 将被检验的葡萄酒在无菌的条件下,接入与其等量的葡萄汁,便为酵母提供了良好的繁殖条件,酵母开始快速繁殖和发酵。酵母繁殖的速度和发酵的强度,是衡量被检样品染菌的程度。 具体操作如下: 取标准试管3支,分别注入10mL葡萄汁,并加棉塞封口,置于高压灭菌锅中灭菌;将吸管用纸包好,并在160℃下灭菌。然后小心的拔除葡萄酒瓶的软木塞,立即用火焰将瓶口附着的微生物灭除,再用无菌吸管从瓶底吸出10mL被检葡萄酒,移入已灭菌葡萄汁的试管内,每份样品做平行样3支。 若被检的样品活酵母较多,在3—5天内即可检定其发酵度;若酵母较少,发酵需要两倍于此的时间,由此可断定生产线是否处于受控状态,断定瓶装酒出厂后是否会发生浑浊等质量事故。 这个方法十分简便,不需要特别的仪器,对小型葡萄酒厂十分适用,这是其优点。缺点是只能检定出葡萄酒中是否存在酵母菌,无法进行定量分析。 二、薄膜过滤法 借助于不同孔径的过滤片(孔径一般为2微米以下),在无菌条件下过滤被检葡萄酒,分离出酵母及其它微生物,然后对滤片上的微生物进行生长培养,计算出现的菌落数,并进行其它各项必要的检查。 操作方法如下: 将所有参与过滤的仪器、器皿进行彻底消毒,在无菌的条件下进行过滤等操作。在每次分析之前,将过滤器及过滤片置于高压锅内灭菌,用经火焰烧过的镊子取已灭菌的过滤片放入过滤器中。 被检瓶酒在开启前,必须仔细用75%酒精擦拭瓶口,小心地拔除软木塞,勿使开瓶刀穿通软木塞。 开始时先将软木塞拔出四分之三,然后用手轻轻取下软木塞,瓶口在倒酒前先用火焰烧一下,再将葡萄酒一点一点地倒入过滤漏斗中。 过滤结束后,用火焰烧过的镊子在漏斗内取出滤片,置于培养皿中,并摆放平整,倒入适量的酵母培养基(约3mL),然后标明日期和试样编号,置于生物培养箱内,在25℃下培养3—5天。为避免凝结水影响菌落生长,将培养皿反扣于培养箱内。若过滤片上的酵母菌是活的,酵母即进行繁殖,在培养基上会出现菌落。 如果未发现菌落生长,说明被检的葡萄酒是稳定的,不会出现酵母菌引起的浑浊;如果每瓶样有5个以上的菌落出现,说明葡萄酒的除菌或杀菌操作不彻底,葡萄酒有不稳定的因素,应该严格检查生产过程中的每个环节,直到查出原因为止。 这一方法能对瓶装酒内各种微生物进行定量检定,但需要选择适当孔径的滤片和培养基,并由掌握基本微生物学的熟练人员操作。 三、快速检定法 薄膜过滤法可以用显微镜对滤片做仔细检查,迅速检出活酵母;快速检定法则可将死的和活的微生物区别开来,但要求瓶装酒内必须不含其他悬浮物。 在适宜的温度下,于8—14小时内,具有繁殖能力的菌体生长成为微小的菌落,用显微镜观察,可将死的、没有繁殖能力的菌落区别开来。活菌体在培养时会形成小的菌落,死菌体只有单个的存在。
糖是葡萄酒中甜味的主要来源,它们有多种形式。在葡萄植株内——实际上任何植物都是——主要的供能底物是蔗糖 (在动物体内则是葡萄糖)。蔗糖是一种双糖,是单个葡萄糖和单个果糖分子的结合。在葡萄成熟过程中,蔗糖会被分解,所以葡萄醪开始发酵时,葡萄糖和果糖总是以等量存在。葡萄糖、果糖与蔗糖酵母菌(他们拉丁文名字的本义就是"嗜糖真菌")会优先消耗葡萄糖,因此葡萄酒中的残糖通常有 60% 至 70% 是果糖,具体比例取决于葡萄品种和酵母菌株。果糖分子可以与我们味蕾上的甜味受体以更高的效率相互作用,尝起来是葡萄糖的两倍甜。这就食品工业严重地依赖高果糖玉米糖浆的部分原因,而且这种糖浆的生产成本极低。葡萄酒中还含有少量的其他糖,通常可以忽略不计。它们包括纤维二糖、半乳糖和戊糖。戊糖就是五碳糖,如阿拉伯糖、鼠李糖和木糖。由于酵母菌并不会利用它们,它们通常被称为"不可发酵糖"。再加上对人类来说味道不是很甜,所以人们很少讨论它们。
向您介绍葡萄酿酒酵母CEC 目前CEC系列酵母酿造的酒,已经多次在国内外各大赛事中获得金奖、大金奖,相信以后会有更多本土酵母酿制的酒在各大赛事中脱颖而出!

大家好: 按照15版药典,检测阿拉伯胶的“葡萄糖和果糖”项目,结果是硅胶板在喷了显色剂,然后放入烘箱加热后,整个硅胶板都变黑了。.且后面研究发现,直接将显色剂喷到板上,板在烘箱中加热,板就变黑了。求助有此经验的同学,问题会出在哪里?我们自己调查的结果可能是如下几个方面,:1- 硅胶板质量问题(用了2个品牌的板,国药集团和上海信宜的,都出现了这样的问题,可能性小);2- 显色剂有问题(用的都是新开瓶的试剂,可能性小);3- 药典的方法有问题,要求用的硅胶G板,是不是应当用不同的板?附:检验方法葡萄糖和果糖 取本品0.1g ,置离心管中,加1%三氟乙酸溶液2 m l ,强力振摇使溶解,密塞120°C加热1 小时,离心,小心转移上层液至50ml烧杯中,加水10ml减压蒸发至干. 残渣加水0 .1m l及甲醇0.9ml,离心分离沉淀。如有必要,用醇1ml稀释上层清液。另分别取阿拉伯糖、半乳糖、葡萄糖、鼠李糖及木糖对照品各lOmg于lm l水中,用甲醇稀释至10ml,作为对照品溶液。照薄层色谱法(通则0502)试验,吸取上述两种溶液各10μl,分别点于同一硅胶G 薄层板上,以1 .6%磷酸二氢钠溶液-正丁醇-丙酮(10:4 0: 50)为展开剂,展开,取出,晾干,喷以对甲氧基苯甲醛溶液(取对甲氧基苯甲醛0.5ml,加冰醋酸10m丨,甲醇8 5 m l,琉酸5ml,摇匀,即得)至恰好湿润,立即在110C加热10分钟,放冷,立即检视,对照品溶液应显示的5个淸晰分离的斑点,从下到上的顺序依次为半乳糖(灰绿色或绿色)、葡萄糖(灰色)、阿拉伯糖(黄绿色)、木糖(绿灰色或黄灰色)、鼠李糖(黄绿色)。供试品色谱中,在与半乳糖和阿拉伯糖对照品色谱相应的位置之间,不得显灰色或灰绿色斑点。http://ng1.17img.cn/bbsfiles/images/2015/10/201510130951_569848_1835550_3.jpg
在多糖类测定分子量时,计算理论板数用的葡萄糖是药典上的分子量为198的葡萄糖吗?需要先进样测定葡萄糖的理论板数吗? 葡萄糖是小分子的,在凝胶色谱柱上 在最后出峰,与溶剂及小分子物质分不开,如何进行计算理论板数啊???
在发酵生产过程中,种子制备的过程大致可分为两个阶段:(1)实验室种子制备阶段(2)生产车间种子制备阶段 一、实验室种子的制备实验室种子的制备一般采用两种方式:对于产孢子能力强的及孢子发芽、生长繁殖快的菌种可以采用固体培养基培养孢子,孢子可直接作为种子罐的种子,这样操作简便,不易污染杂菌。对于产孢子能力不强或孢子发芽慢的菌种,可以用液体培养法。(一)孢子的制备1,细菌孢子的制备细菌的斜面培养基多采用碳源限量而氮源丰富的配方。培养温度一般为37℃。细菌菌体培养时间一般为1~2天,产芽孢的细菌培养则需要5~10天。2,霉菌孢子的制备霉菌孢子的培养一般以大米、小米、玉米、麸皮、麦粒等天然农产品为培养基。培养的温度一般为25~28℃。培养时间一般为4~14天。3,放线菌孢子的制备放线菌的孢子培养一般采用琼脂斜面培养基,培养基中含有一些适合产孢子的营养成分,如麸皮、豌豆浸汁、蛋白胨和一些无机盐等。培养温度一般为28℃。培养时间为5~14天。(二)液体种子制备1,好氧培养对于产孢子能力不强或孢子发芽慢的菌种,如产链霉素的灰色链霉菌(S. griseus)、产卡那霉素的卡那链霉菌(S. Kanamuceticus)可以用摇瓶液体培养法。将孢子接入含液体培养基的摇瓶中,于摇瓶机上恒温振荡培养,获得菌丝体,作为种子。其过程如下: 试管→三角瓶→摇床→种子罐2,厌氧培养对于酵母菌(啤酒,葡萄酒,清酒等),其种子的制备过程如下:试管→三角瓶→卡式罐→种子罐例如生产啤酒的酵母菌一般保存在麦芽汁琼脂或MYPG培养基(培养基配制:3克麦芽浸出物,3克酵母浸出物,5克蛋白胨,10克葡萄糖和20克琼脂与升水中)的斜面上,于4℃冰箱内保藏。每年移种3-4次。将保存的酵母菌种接入含10ml麦芽汁的500-1000ml三角瓶中,再于25℃培养2-3天后,再扩大至含有250-500ml麦芽汁的500-1000ml三角瓶中,再于25℃培养2天后,移种至含有5-10L麦芽汁的卡氏培养罐中,于15-20℃培养3-5天即可作100L麦芽汁的发酵罐种子。从三角瓶到卡氏培养罐培养期间,均需定时摇动或通气,使酵母菌液与空气接触,以有利与酵母菌的增殖。二、生产车间种子制备实验室制备的孢子或液体种子移种至种子罐扩大培养,种子罐的培养基虽因不同菌种而异,但其原则为采用易被菌利用的成分如葡萄糖、玉米浆、磷酸盐等,如果是需氧菌,同时还需供给足够的无菌空气,并不断搅拌,使菌(丝)体在培养液中均匀分布,获得相同的培养条件。1,种子罐的作用:主要是使孢子发芽,生长繁殖成菌(丝)体,接入发酵罐能迅速生长,达到一定的菌体量,以利于产物的合成。2,种子罐级数的确定种子罐级数:是指制备种子需逐级扩大培养的次数,取决于:(1)菌种生长特性、孢子发芽及菌体繁殖速度;(2)所采用发酵罐的容积。 比如:细菌:生长快,种子用量比例少,级数也较少,二级发酵。 茄子瓶→种子罐→发酵罐霉菌:生长较慢,如青霉菌,三级发酵 孢子悬浮液→一级种子罐(27℃,40小时孢子发芽,产生菌丝 )→二级种子罐(27℃,10~24小时,菌体迅速繁殖,粗壮菌丝体)→发酵罐放线菌:生长更慢,采用四级发酵酵母:比细菌慢,比霉菌,放线菌快,通常用一级种子3,确定种子罐级数需注意的问题(1)种子级数越少越好,可简化工艺和控制,减少染菌机会(2)种子级数太少,接种量小,发酵时间延长,降低发酵罐的生产率,增加染菌机会(3)虽然种子罐级数随产物的品种及生产规模而定。但也与所选用工艺条件有关。如改变种子罐的培养条件,加速了孢子发芽及菌体的繁殖,也可相应地减少种子罐的级数。

β-葡萄糖醛酸酶/芳基硫酸酯酶 被广泛地应用于科研和分析实验室,可同时具备对β-葡萄糖苷酸类固醇类和硫酸酯类物质的酶解/水解能力,对分析物做到最优化的样品前处理,确保最佳的气相色谱GC,液相色谱HPLC,免疫学等其他分析检测。β-葡萄糖醛酸酶典型应用:GBT 22286-2008: 动物源性食品中多种β-受体激动剂残留量的测定液相色谱串联质谱法SNT 1924-2011: 进出口动物源食品中克伦特罗、莱克多巴胺、沙丁胺醇和特布他林残留量的测定 液相色谱-质谱 质谱法农业部1025号公告-18-2008: 动物源性食品中β-受体激动剂残留检测液相色谱-串联质谱法目前可以提供免费试用,如需请发送信息至 luxiaofan@anpelsci.com .最新产品单页献上!!http://ng1.17img.cn/bbsfiles/images/2013/10/201310161017_471135_2655559_3.jpg
单一的甜菊糖苷与瑞鲍迪A或者是纯度高的葡萄糖基甜菊糖苷的基线波动小,分离也不错。但是有时候做比较杂的葡萄糖基甜菊糖苷,会有小杂峰密集出现并带着基线波动。是按照国标方法做的,求方法解决
岛津液相,柱子用[font=&]Bio-Rad Aminex HPX-87H[/font][font=宋体]柱时,葡萄糖和葡萄糖酸在同一个地方出峰。为了得到葡萄糖酸的量,看了一些文献,说可以用紫外检测器来尝试,但是因为体系里还有葡萄糖酸内酯,在紫外检测器上和葡萄糖酸在同一个地方出峰,也不能分离。[/font][font=宋体]求问各位大神用什么柱子和什么方法可以分离体系中有内酯的葡萄糖和葡萄糖酸?感谢[/font]
安捷伦1200,C18柱,想将葡萄糖和葡萄糖酸分开,之前用磷酸二氢钠作流动相,柱温25摄氏度,流速1,可是分离效果不好,出峰时间仅隔0.2分钟,而且每次出峰时间不同,请问是什么问题?有没有朋友做过这两种物质分离的液相,如何选择流动相,设置参数?
找了很久都没找到葡萄糖粉末的折射率只搜到产品信息中文名称 无水葡萄糖 英文名称 Dextrose Anhydrate 中文别名 D-无水葡萄糖 葡萄糖 右旋糖 β-D-无水葡萄糖 CAS RN 50-99-7 EINECS号 200-075-1 分 子 式 C6H12O6 分 子 量 180.15 熔点 150-152 °C(lit.) 比旋光度 52.75 º (c=10, H2O, NH4OH 25 º C) [color=#00008B]折射率 53 ° (C=10, H2O) [/color]储存条件 2-8°C 溶解度 H2O: 1 M at 20 °C, clear, colorless 水溶解性 Soluble 请教各位大侠折射率 53 °是什么意思?用阿贝折射仪测试的结果吗?那该如何换算成折射率呢?
急求木糖和葡萄糖的分析方法,最好是国标,如果没有国标的行业标准的也行。
培养基及成分 1、Acetobacter Medium (醋酸菌培养基) Glucose (葡萄糖) 100g Yeasst extract (酵母膏) 10g CaCO3 20g Agar (琼脂) 15g Distilled water (蒸馏水) 1000ml Adjust (调) pH to 6.8 适用范围:恶臭醋酸杆菌混浊变种 2、 Nutrient Agar (营养肉汁琼脂) Pepton (蛋白胨) 5g Beef extract (牛肉膏) 30g NaCl 5g Agar (琼脂) 15g Distilled water (蒸馏水) Adjust (调) pH to 7.0-7.2 :When cultivation of Bacillus,5mg of to MnSO4.H2O may be added . It is favorable to promote spore formation . 适用范围:产气气杆菌、粪产碱杆菌、蜡状芽孢杆菌、蜡状芽孢杆菌蕈状变种、地衣形芽孢杆菌、巨大芽孢杆菌、多粘芽孢杆菌、尘埃芽孢杆菌、短小芽孢杆菌、嗜热脂肪芽孢杆菌、枯草芽孢杆菌、枯草芽孢杆菌深黑变种、苏云金芽孢杆菌、苏云金芽孢杆菌蜡螟亚种(青虫菌)、苏云金芽孢杆菌戈尔斯德变种、苏云金芽孢杆菌猝倒亚种、产氨短杆菌、黄色短杆菌、谷氨酸棒状杆菌、北京棒杆菌、大肠埃希氏菌(大肠杆菌)、铜绿假单胞菌(绿脓杆菌)、凸形假单胞杆菌、荧光假单胞菌、弯曲假单胞菌、恶臭假单胞菌、假单胞杆菌、藤黄八叠球菌、亚黄八叠球菌、尿素八叠球菌、金黄色葡萄球菌、运动发酵单孢菌 3、Azotobacter Medium (固氮菌培养基) KH2PO4 0.2g K2HPO4 0.8g MgSO4.7H2O 0.2g CaSO4.2H2O 0.1g Na2MoO4.2H2O Trace(微量) Yeast axtract(酵母膏) 0.5g Mannitol(甘露醇) 20g FeCl3 Tract(微量) Distilled water (蒸馏水) 1000ml Agar (琼脂) 15g Adjust (调) pH to 7.2 适用范围:固氮菌、胶质芽孢杆菌 4、Corn Meal Medium (玉米粉培养基) Maize flour (玉米粉) 5g Peptone (蛋白胨) 0.1g Glucose (葡萄糖) 1g Tap water (自来水) 1000ml :Boil the mixture in autoclave at 121℃ for 1 hr. distribute the medium into 18ⅹ18 mm tubes , each contains 10 ml of the liquid , then autoclave at 121℃ for 1 hr . again (15磅蒸煮1小时,分装入18ⅹ18毫米试管,每管深度达6厘米。15磅再次灭菌15小时。) 5、Lactic-bacteria Medium I (乳酸菌培养基 I ) Yeast extract (酵母膏) 7.5g Peptone (蛋白胨) 7.5g Glucose (葡萄糖) 10g KH2PO4 2g Tomato juice (西红柿汁) 100ml Tween (吐温) 80 0.5ml Distilled water (蒸馏水) 900ml pH 7.0 适用范围:植物乳杆菌(胚芽乳杆菌)、嗜热乳酸链球菌 6、Lactic-bacteria Midium Ⅱ (乳酸菌培养基 Ⅱ) Lacto-casein peptone (乳酪蛋白胨) 10g Beef extract (蛋白胨) 10g Yeast extract (酵母膏) 5g Glucose (葡萄糖) 5g Tween (吐温) 80 1g K2HPO4 2g Na-acetate (醋酸钠) 5g Diamine citrate (柠檬酸二胺) 2g MgSO4.7H2O 0.2g MnSO4.H2O 0.05g Distilled water (蒸馏水) 1000m pH 6.5-6.8 适用范围:植物乳杆菌(胚芽乳杆菌) 7、Peotone Glucose Yeast extract Medium PGY (蛋白胨、酵母膏、葡萄糖培养基) Peptone(蛋白胨) 10g Yeast extract (酵母膏) 5g Glucose (葡萄糖) 1g Distilled water (蒸馏水) 1L 8、Glycerol Agar (甘油琼脂) Peptone (蛋白胨) 5g Beef extract (酵母膏) 3g Glycerol (甘油) 20g Top water (自来水) 1000ml Agar (琼脂) 15g pH 7.0-7.2 9、Rhizobium medium (根瘤菌培养基)AS 9 Yeast eztract (酵母膏) 1g Soil eztract (土壤浸提液) 200ml Mannitol (甘露醇) 10g Agar (琼脂) 15g Distilled water (蒸馏水) 800ml pH 7.2 :Soil extract:Suspend 50g finely and dried gardon soil in 200ml of tap water. Autoclave at 121℃ for 1 hr. Decant through cotton-cloth, filler though paper, make up volume to 200ml. Resterilize for 20 minutes at 121℃ , then mixed with othringredients and distributed. (土壤浸提液的制法:取土壤50克,加水200毫升,15磅蒸煮1小时,经滤纸过滤后加水补足到200毫升。) 适用范围:大豆根瘤菌(慢生型)、豇豆慢生根瘤菌、花生根瘤菌、紫云英根瘤菌、 大豆根瘤菌(快生型)、大豆根瘤菌、豌豆根瘤菌、苜蓿根瘤菌、田菁根瘤菌 10、 Mannitol Agar (甘露醇琼脂) Yeast extract (酵母膏) 5g Peptone (蛋白胨) 3g Mannitol (甘露醇) 25g Agar (琼脂) 15g Distilled water (蒸馏水) 1000ml 11、 Glucose Asparagine (葡萄糖、天门冬素琼脂) Glucose (葡萄糖) 10g Asparagine (天门冬素) 0.5g K2HPO4 0.5g Water (水) 1000ml pH 7.2-7.4 适用范围:刺孢小单孢菌绛红变种、紫色小单孢菌(绛红小单孢菌) 12、Gause′s Synthetic Agar (高氏合成一号琼脂) KNO3 1g Soluble starch(可溶性淀粉) 20g K2HPO4 0.5g MgSO4.7H2O 0.5g NaCl 0.5g FeSO4 0.01g Agar (琼脂) 20g water (水) 1000ml pH 7.2-7.4 适用范围:刺孢小单孢菌绛红变种、紫色小单孢菌(绛红小单孢菌)、白黄链霉菌、白色链霉菌、抗生链霉菌、双重轮丝链霉菌、产色链霉菌、烬灰链霉菌、天蓝色链霉菌、灭蚊链霉菌、红霉素链霉菌、青色链霉菌、球孢链霉菌、浅灰链霉菌、灰色链霉菌、吸水链霉菌、淡紫灰链霉菌、黄色长孢链霉菌、藤黄色链霉菌、细黄链霉菌、黑化链霉菌、玫瑰色链霉菌、华美链霉菌、嗜热链霉菌、委内瑞拉链霉菌、紫色直丝链霉菌、紫色链霉菌、绿色链霉菌 13、Wort Agar (麦芽汁琼脂) Dilute the world (without hop) to 12 Brix. Add 15g agar into 1000ml of the diluted word..Melt the agar by heating, then distribute the medium into tubes. Autoclave at 110 for 30 minutes. (将发酵啤酒的原料(未加酒花),稀释至12柏林,加琼脂15克,溶化后分装。15磅灭菌30分钟。) 适用范围:克鲁斯假丝酵母、郎比可假丝酵母、解脂假丝酵母、马其顿假丝酵母、拟热带假丝酵母、粗壮假丝酵母、皱褶假丝酵母、热带假丝酵母、产朊假丝酵母、阿舒假囊酵母、白地霉、果香地霉、地霉属、异常汉逊酵母、异常汉逊酵母变种、阿拉伯糖醇汉逊酵母、施氏汉逊酵母、菅囊
请问[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定葡萄糖 木糖的方法
电泳基本原理 迁移率(或泳动度)是指带电颗粒在单位电场强度下泳动的速度,可用下列公式计算: U =υ/E =(d/t)/(V/l) =dl/Vt U为迁移率(cm2•V-1•min-1);υ为颗粒泳动速度(cm•s-1);E 为电场强度( V•cm-1);d为颗粒泳动的距离(cm);l为滤纸有效长度(cm);V为实际电压(V);t为通电时间(s或min)。通过测量d, l, V, t, 即可计算出被分离物质的迁移率。 1迁移率单位= 10-5 cm2•V-1•min-1在确定的条件下,某物质的迁移率为常数,是该物质的化学特征常数。 颗粒带净电荷多,直径小而接近于球形,则在电场中泳动速度快,反之则泳动速度慢。 迁移率还与分子的形状,介质粘度,颗粒所带电荷有关,迁移率与颗表面电荷成正比,与介质粘度及颗粒半径成反比。 影响琼脂糖电泳迁移的主要因素 电场强度 溶液的pH值 溶液的离子强度 电渗现象 温度的影响 支持物的影响 按分离原理分类: 1.区带电泳 2.移界电泳 3.等速电泳 4.聚焦电泳 按有无固体支持物分类 1. 纸上电泳 2. 醋酸纤维素膜电泳 3. 薄层电泳 4. 非凝胶性支持物区带电泳(支持物有:淀粉、纤维素粉、玻璃粉、硅胶) 5. 凝胶支持区带电泳(淀粉凝胶、聚丙稀酰胺凝胶、琼脂糖凝胶) 影响琼脂糖电泳迁移的主要因素 DNA的大小 DNA的构象 琼脂糖浓度 缓冲液 不同构像质粒 缓冲液 TAE:乙酸盐缓冲液 TBE:硼酸盐缓冲液 TPE:磷酸盐缓冲液 实验操作 1. 用胶带将洗净、干燥的水平板的边缘封住,形成一个胶模并水平放置。 2. 按水平板的长×宽×0.5cm胶厚,量取0.5×TBE,并按0.7%的浓度称取agarose琼脂糖,在微波炉或电炉上加热至全熔(清澈透明)。 3. 等凝胶温度降至大约50-60以下时,加入1 mg/L溴化乙锭(EB)至终浓度为0.5ug/mL ;摇匀并轻快地倒入水平板中,除掉气泡,插入梳子。 4. 凝固后,将梳子轻轻拔出。 5.去掉胶带,将水平板放入加有0.5×TBE电泳缓冲液的电泳槽中,并且使电泳缓冲液高出凝胶约1mm。 6.在parafilm膜上依次加: ddH2O 6ul,上样Buffer 2ul ,DNA 4ul 分别混匀后点样,记录点样次序。 7. 在水平板两边的点样孔中分别加入6 μ l的λΔΝΑ/EcoRI+HindIII marker。 8. 盖好电泳槽盖子,选择适当的电泳电压(≤5V/cm)及电泳方向(DNA阴极阳极),开始电泳。 9. 当色素接近胶的先端,停止电泳,样品在紫外灯下观察、成像℃
中元胶囊中盐酸氨基葡萄糖检测中元胶囊中盐酸氨基葡萄糖检测中元胶囊中盐酸氨基葡萄糖检测中元胶囊中盐酸氨基葡萄糖检测中元胶囊中盐酸氨基葡萄糖检测
[color=#444444]Bio-Rad Aminex HPX-87H(300mm×7.8mm)色谱柱,用0.005mol/L硫酸作为流动相的高效液相测糖浓度,所测葡萄糖、木糖值偏高怎么办?可能是哪些问题呢?求大佬帮助[/color]
我要分离葡萄糖,木糖,阿拉伯糖和半乳糖,我查了一下,说可以用季胺盐硼酸型阴离子树脂来分离,可是那树脂买不到阿。郁闷中。请各位高手帮帮忙,帮我支个招,小妹在此不胜感激阿。
求各位高手帮忙一下,怎样用HPLC分离葡萄糖和葡萄糖酸 或者是葡萄糖和葡萄糖酸钠? 应该用什么样的柱子和检测器呢?拜托拜托!!
一、凝胶制备1. 微波炉溶解琼脂糖时,胶液沸腾冲溢出三角锥瓶微波炉加热时胶液可能发生剧烈沸腾,(1)总液体量不宜超过三角锥瓶的50%容量。(2)2%以上胶液设置中火加热。 (3)胶液剧烈沸腾时,停止加热,移开三角锥瓶,请戴上防热手套,小心摇动三角锥瓶,然后再次加热,胶液沸腾直至胶液清澈,保证琼脂糖完全溶解。 2. 琼脂糖电泳图像背景模糊不清:琼脂糖没有完全溶解会造成电泳图像背景模糊不清。完全溶解的琼脂糖胶液清澈,三角锥瓶内壁应没有粘附琼脂糖颗粒。 3.加热后水分蒸发,如需要应加入热的蒸馏水,补足到原来的重量,摇匀。 二、电泳1. DNA条带模糊,拖尾。 (1)DNA降解。避免核酸酶污染。 (2)DNA上样量过多。减少凝胶中DNA上样量。 (3)电泳缓冲液陈旧:电泳缓冲液多次使用后,离子强度降低,pH值上升,缓冲能力减弱,从而影响电泳效果。建议经常更换电泳缓冲液。 (4)电泳条件不合适。电泳时电压不应超过20 V/cm,温度<30℃,巨大DNA链,温度应<15℃,核查所用电泳缓冲液是否有足够的缓冲能力。 (5)DNA样含盐过高。泳前通过乙醇沉淀去除过多的盐。 (6)有蛋白污染。电泳前抽提去除蛋白。 (7)DNA变性。电泳前勿加热,用20 mM NaCl缓冲液稀释DNA。[/c
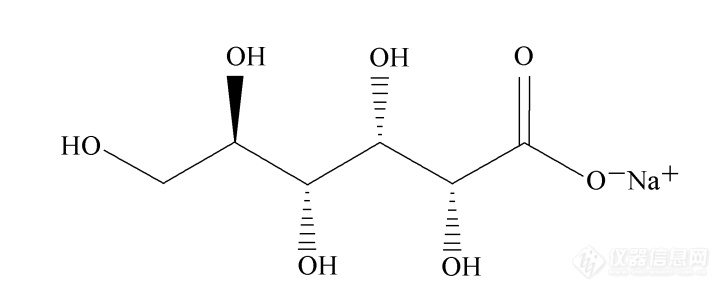
[font='calibri'][size=13px] [/size][/font][font='calibri'][size=14px] [/size][/font][size=29px]葡萄糖酸钠[/size][font='calibri'][size=29px] [/size][/font][font='calibri'][size=21px] [/size][/font][size=21px]林扬[/size][align=center][font='黑体'][size=20px]摘 要 [/size][/font][/align][align=center][font='calibri'][size=18px] [/size][/font][/align][font='黑体']摘要[/font][font='黑体']:[/font]葡[font='黑体']萄糖酸钠的分子式为C[/font][font='黑体'][size=16px]6[/size][/font][font='黑体']H[/font][font='黑体'][size=16px]11[/size][/font][font='黑体']O[/font][font='黑体'][size=16px]7[/size][/font][font='黑体']Na,分子量为218.14。葡萄糖酸钠广泛用于工业中。在食品工业中,葡萄糖酸钠作为食品添加剂,可以赋予食品酸味,增强食品的味道,防止蛋白质变性,改善不良的苦味和涩味,并取代盐来获得低钠,无钠的食品。本文简述了食品添加剂葡萄糖酸钠的理化性质及其主要的生产制备工艺[/font][font='黑体'],[/font][font='黑体']并参照国家标准[/font][font='黑体'],[/font][font='黑体']展示了几种常见的葡萄糖酸钠的检测方法[/font][font='黑体']。[/font][font='黑体']关键词[/font][font='黑体']:葡萄糖酸钠、食品添加剂[/font][font='黑体']、[/font][font='黑体']制备[/font][font='黑体']、[/font][font='黑体']检测[/font][font='calibri'][size=18px] [/size][/font] [font='calibri'][size=18px] [/size][/font][size=18px]引言[/size]葡萄糖酸钠是一种重要的食品添加剂, 在食品中的应用前景广阔,因为其广泛的来源,且无毒性,无潮解性,稳定性和良好的螯合性能,在营养增补剂、食品保鲜剂、品质改良剂等方面有广泛的应用。在2021年8月即将实施的GB1886.320-2021中,国家市场监督总局、国家卫生健康委员会对食品添加剂葡萄糖酸钠的相关指标及检测方法设定了国家标准。[size=18px]1[/size][size=18px].[/size][size=18px]葡萄糖酸钠的理化性质[/size][font='宋体'][size=16px][1][/size][/font][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262015125951_6792_1608728_3.png[/img]分子式:C[font='宋体'][size=16px]6[/size][/font]H[font='宋体'][size=16px]11[/size][/font]NaO[font='宋体'][size=16px]7[/size][/font]分子量:218.14熔点:206-209℃外观:白色结晶颗粒或粉末溶解性:极易溶于水(0.1g/mL),略溶于酒精,不能溶于乙醚比旋光度:[α]D20+11~+13°(c=10,H[font='宋体'][size=16px]2[/size][/font]O)储存条件:低于30℃PH值:7.0-8.0(100g/l,H[font='宋体'][size=16px]2[/size][/font]O,20℃)CAS数据库:527-07-1(CAS Data Base Reference)EPA化学物质信:Sodium gluconate(527-07-1)[size=18px]2[/size][size=18px].[/size][size=18px]葡萄糖酸钠的生产制备[/size][font='宋体'][size=18px][2][/size][/font]葡萄糖酸钠的制备方法主要包括均相化学氧化法,电解氧化法,非均相催化氧化法和生物发酵法。其中,最常用的是非均相催化氧化和生物发酵。非均相催化氧化法受催化剂和催化效率的限制,具有催化剂易中毒,生产效率低,生产成本高的缺点。因此,非均相催化方法不适合在食品工业中生产葡萄糖酸钠[font='宋体'][size=16px][3][/size][/font]。食品级葡萄糖酸钠的制备主要采用的是生物发酵法,生物发酵法所用的菌种主要包括真菌和细菌,另外还有新型的固定化细胞发酵。现目前葡萄糖酸钠生产的方法采用的是酶氧化法生产,其中用到的主要的酶是葡萄糖氧化酶(GOD)。葡萄糖氧化酶主要负责通过葡糖酸和过氧化氢催化葡萄糖的产生。黑曲霉(Aspergillus niger)是GOD的主要生产菌株。在实际生产中,GOD将与过氧化氢酶(CAT)形成复杂的酶系统。CAT主要的功能是使得体系中的H[font='宋体'][size=16px]2[/size][/font]O[font='宋体'][size=16px]2[/size][/font]得以分解。葡萄糖在GOD的作用会氧化为葡萄糖酸,并伴随过氧化氢的释放。过氧化氢具有很强的氧化性,可以降低葡萄糖氧化酶的活性。过氧化氢酶的加入可以快速分解过氧化氢,将过氧化氢分解成水和氧,葡萄糖氧化酶可以继续催化反应。并且可以补充反应所需的氧气,使氧化反应持续进行。在实际生产中,加入一定量的氢氧化钠溶液以维持反应体系的pH值,使反应继续进行。2.1传统生物发酵技术传统的葡萄糖酸钠发酵采用的是黑曲霉菌发酵工艺,该方法是利用黑曲霉为发酵菌株,通过不断向发酵体系内加入氢氧化钠溶液控制pH,并控制一定的温度,氧含量等条件进行发酵。发酵后,通过多种工艺获得产品,如灭菌,脱色,浓缩,结晶,离心和干燥。由于存在传统工艺效率低下,所得产品质量较差等缺陷。目前国内外在传统生物发酵法中的研究主要集中在改良发酵菌种、固定化菌丝体重复利用、改变发酵方式和寻找葡萄糖替代品等方面。 葡萄糖酸钠的生产过程是需氧过程,反应体系中的氧气量对发酵时间和产量有着重要的影响。传统工业生产一般都是通入空气以供应反应所需的氧气,但液体溶氧速率有限,不能及时满足实际生产中所需氧气含量,从而延长了生产时间。H.W. Lee通过加压使得水中溶解氧浓度达到150mg/L,发现葡萄糖酸钠的生产得率大大提高。O.V. Singh对比了液态发酵,表面发酵,半固态发酵和固态发酵对于葡萄糖酸钠生产的影响,证明了固态发酵是最有效的发酵方式。在实际生产中,为了降低生产成本,将尝试寻找低成本碳源作为发酵和生产葡萄糖酸钠的基质,包括玉米淀粉,甘蔗渣,糖蜜等。2.2生物发酵新技术——固定化酶技术[font='宋体'][size=16px][2][/size][/font] 传统的发酵法生产葡萄糖酸钠,会得到大量的细菌或真菌菌丝。这些菌丝会被当做废料处理,而其中往往含有大量的葡萄糖氧化酶。近年来,基于这一问题,国内外学者将目光瞄准酶固定化技术,因此固定化酶技术越来越受到了研究者的关注。固定化酶的研究使得葡萄糖酸钠广泛的应用于工业中成为可能。目前为止,多种酶被成功固定到不同载体上,并且取得了很好的经济效益及应用价值。在食品工业中,使用固定化酶代替游离酶可以提高葡萄糖酸钠的生产效率,降低使用成本,简化纯化过程,并提供高产量和高质量。关于酶固定化技术的早期研究主要选择纤维素,固体玻璃颗粒,多孔玻璃颗粒和镍网。其中,多孔玻璃和纤维素是最广泛使用的固定载体,因为它们的表面积大,因而酶的催化活性相对较高。近年来,固定化技术应用越来越多,酶的固定化技术涉及用高分子材料物理的包埋法,导电高分子共聚法和无机凝胶包埋法。有研究者采用丙烯酸的微粒凝胶和三价金来固定GOD,表现出很好的效果,还有报道关于利用戊二醛交联作用把GOD固定在竹子的内膜上,并取得了一定的成果。现在所使用的固定化载体种类繁多。[size=18px]3.应用[/size][font='宋体'][size=18px][2][/size][/font]目前葡萄糖酸钠作为一种性能良好的食品添加剂,广泛用于食品加工业。同时,它还广泛用于营养补充剂,食品防腐剂,质量改进剂和缓冲剂。 3.1.葡萄糖酸钠调节食品的酸度 在食品中添加酸可以增强食品的安全性,因为酸是防止冷藏食品中微生物污染的主要形式,而与高温或高静水压力处理相结合使用酸可以降低能耗,从而降低成本。然而,在食品或饮料配方中添加酸通常会降低适口性,因为酸性较高,这限制了食品工业更好地利用酸作为防腐剂的能力,将葡萄糖酸钠配制成钠盐混合物(分别加入氯化钠和醋酸钠)后分别作用于柠檬酸、乳酸和苹果酸,发现葡萄糖酸钠混合物对柠檬酸和苹果酸的酸度(PH为4.4)有中度抑制作用,但对乳酸的酸度几乎没有影响。葡萄糖酸钠调节柠檬酸和苹果酸中的pH值,从而有效减少酸味,不会产生过咸的味道,说明葡萄糖酸钠在相对较高的酸水平上能够显著抑制柠檬酸和苹果酸的酸性。在食品工业中,葡萄糖酸钠被广泛用于饮料行业以确保饮料的质量,同时还保护由常规灭菌方法引起的过高温度引起的饮料成分的破坏,并且节省能量。 3.2葡萄糖酸钠代替食盐用于食品工业 相关研究表明中国人均的食盐摄入量是世界平均人均摄入量水平的数倍,体内钠离子含量过高,会导致高血压高血脂等慢性疾病的发生。在关注生活水平和疾病健康的同时,低盐食品引起了广泛关注,成为食品行业的热点。研究表明,每日盐的钠含量是葡萄糖酸钠的四倍,而葡萄糖酸钠的钠分子量仅为10.5%。与常用的低钠盐相比,葡萄糖酸钠的味道差别不大,但具有无刺激性,无苦味和涩味的优点,在实际应用中已成为盐的替代品。目前主要用于食品领域,如无盐产品和面包。研究报道使用葡萄糖酸钠代替盐进行面包发酵,不仅可以发酵低钠面包,还可以在不影响其整体风味和保质期的情况下实现减盐。 3.3葡萄糖酸钠改善食品风味 在食品行业,食品的风味是在感官评价中的重要指标。近年研究发现:葡萄糖酸钠能够改善苦味,葡萄糖酸钠盐对苦味化合物及其二元组合物质的苦味有不同程度的抑制作用。将不同剂量的葡萄糖酸钠盐以及乳酸锌盐均应用于咖啡因发现其能够抑制咖啡因苦味,上述研究说明葡萄糖酸钠对呈苦味的风味物质具有调节作用。另外,有报道表明在肉制品加工过程中添加一定量的葡萄糖酸钠,能较好的改善豆制品当中的大豆腥臭味。有研究发现。在海产品的加工过程中,通常会添加一定量的葡萄糖酸钠来降低鱼臭味,提高食物的食欲,且相比于传统的覆盖方式,成本更加低廉。 3.4葡萄糖酸钠能够改善食品品质 随着生活水平的不断提高,人们对食品的要求也越来越高。作为一种新型食品添加剂,葡萄糖酸钠不仅提高食品的风味,而且还增强了食品的营养特性。与市场上许多食品添加剂相比,它的无毒无害性能已经成为其最大的亮点。将葡萄糖酸钠作为乳酸钙晶体抑制剂在切达干酪中作用,发现葡萄糖酸钠能增加乳酸钙的溶解度,调节切达干酪的PH值,所以葡萄糖酸钠具有增加钙和乳酸盐溶解度的潜力,通过与钙和乳酸盐离子形成可溶性复合物,阻止它们形成乳酸钙晶体,不仅保证其营养,还改善了切达干酪的品质。将葡萄糖酸钠浸泡处理海带后,能够增加其藻酸盐含量,导致表面更软,改善口感。葡糖糖酸钠还具有蛋白变性抑制作用和肌原纤维蛋白溶解作用,在鱼糜中加入葡萄糖酸钠,加热后凝胶体的凝胶强度比未加葡萄糖酸钠的有明显提高,所以葡萄糖酸钠能够改善鱼糜制品的品质。[size=18px][color=#333333][back=#ffffff]4.限量[/back][/color][/size][font='宋体'][size=18px][color=#333333][4][/color][/size][/font]由GB 2760-2014,葡萄糖酸钠可在各类食品中按生产需要适量使用。[size=18px]5.检测[/size]5.1葡萄糖酸钠的定性检测[font='宋体'][size=16px][1][/size][/font]5.1.1钠离子的鉴别方法原理:根据钠离子在无色火焰上燃烧、火焰为亮黄色的现象,鉴别钠离子的存在。测定步骤:称取约1g试样,精确至0.01 g,溶于10 mL水中,用铂丝蘸取盐酸在无色火焰上燃烧至无色,再蘸取试验溶液少许,在无色火焰上燃烧,火焰应呈亮黄色。5.1.2葡萄糖酸的鉴别方法原理:试样在冰乙酸介质中,与苯肼共热,生成黄色葡萄糖酰苯肼结晶。测定步骤:取约0.5 g试样,精确至0.01 g,置于10 mL试管中,加5 mL 水,溶解(必要时加热),加0.7 mL冰乙酸和1 mL苯肼,在水浴上加热30 min,放至室温,用玻璃棒摩擦试管内壁,则析出黄色的结晶。5.2葡萄糖酸钠的定量检测5.2.1常规滴定法方法原理:试样以冰乙酸为溶剂,以结晶紫为指示剂,用高氯酸标准滴定溶液滴定,根据消耗高氯酸标准滴定溶液的体积计算葡萄糖酸钠的含量。分析步骤:称取测定干燥减量后的试样约0.4 g,精确至0.000 1 g,置于250 mL干燥的锥形瓶中,加50 mL冰乙酸(必要时可用电热板稍微加热),加2滴~3滴结晶紫指示液,用高氯酸标准滴定溶液滴定至溶液由紫色经蓝色最后变为绿色即为终点。除不加试样外,使用相同数量的试剂溶液做空白试验。使用时,高氯酸标准滴定液的温度应与标定时的温度相同 若其温度差小于4℃时,应将高氯酸标准滴定溶液的浓度修正到使用温度下的浓度 若其温度差大于4℃时,应重新标定。[img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262015127065_6610_1608728_3.png[/img]5.2.2电位滴定法方法原理:试样以冰乙酸为溶剂,采用电位滴定仪用高氯酸标准滴定溶液滴定,在滴定过程中通过测量电位变化以确定滴定终点﹐并根据消耗高氯酸标准滴定溶液的体积计算葡萄糖酸钠的含量。分析步骤:称取测定干燥减量后的试样约0.4 g,精确至0.000 1 g,置于250 mL,干燥的锥形瓶中,加50 mL冰乙酸(必要时可用电热板稍微加热),采用电位滴定仪用高氯酸标准滴定溶液滴定。除不加试样外,使用相同数量的试剂溶液做空白试验。使用时,高氯酸标准滴定液的温度应与标定时的温度相同 若其温度差小于4℃时,应将高氯酸标准滴定溶液的浓度修正到使用温度下的浓度﹔若其温度差大于4℃时,应重新标定。[img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262015128040_257_1608728_3.png[/img][size=18px]5.3其它可用于定量分析的方法[/size][font='宋体'][size=18px][5][/size][/font]5.3.1 HPLC法准确称取1.5040g于105℃下烘至恒重的葡萄糖酸钠, 用超纯水溶解并定容至 500mL。分别取1, 2, 3, 4, 5, 6, 7, 8, 9mL葡萄糖酸钠溶液用超纯水稀释至15mL。将其分别过0.45μm 滤膜,再超声处理后即可进样,在HPLC仪器上分析,取其中6点做标准曲线。高效液相色谱采用的流动相为甲醇︰水︰1%磷酸 (2︰48︰50), 流速为1.0mL/min,柱温为25℃, 进样量为15μL,检测波长为210nm.葡萄糖酸钠的出峰时间在2.758min, 峰形较好。色谱条件简单,操作简便,线性关系好。缺点是:其中葡萄糖酸钠属于盐类,对色谱柱的影响较大;且高效液相色谱仪器较昂贵。5.3.2 分光光度法准确称取 13.4779g于105℃下烘至恒重的葡萄糖酸钠, 用蒸馏水定容至 50mL。分别取 1, 2,3, 4, 5, 6, 7, 8, 9m L用蒸馏水定容至 25mL,作为标准溶液待用。各取 1mL上述标准溶液 , 加入18mL 1.25mol/L NaOH, 再边缓缓滴加0.10mol/L CuSO[font='宋体'][size=16px]4[/size][/font]溶液边充分搅拌, 直至产生的沉淀不消失。再将螯合后的溶液煮沸 5min,冷却至室温后,过滤, 再用2mL 1.25 mol/L NaOH洗涤滤渣。将收集的滤液用蒸馏水定容至50mL, 得到一系列浓度分别为 1, 2, 3, 4, 5, 6, 7, 8, 9mmol /L的标准溶液。以0.50 mol /L NaOH 为对照,在660nm波长下测其吸光度。该法的线性关系较好, 但该法较繁琐。该法仅适用于葡萄糖酸钠浓度≦10mmol /L的溶液,且当溶液中葡萄糖的量大于3倍葡萄糖酸钠的量时,葡萄糖对其影响较大。在葡萄糖酸钠的制备中,可能葡萄糖为其制备源,葡萄糖的含量较高, 故该法若要用于葡萄糖酸钠的检测还有待改进。5.3.3 旋光度法 准确称取 13.4070g于 105℃下烘至恒重的葡萄糖酸钠 , 用蒸馏水定容至 50mL。分别取 1, 2,3, 4, 5, 6, 7, 8m L用蒸馏水定容至20m L, 以水为空白 , 依法分别测定旋光度 t =20 ±0.5℃,L =2dm, 用同法读取旋光度 5 次, 取其平均数做标准曲线。用旋光法作葡萄糖酸钠标准曲线的线性关系好 , 操作方便,且不需要昂贵的仪器。但该法的抗干扰因素太低,工业生产的葡萄糖酸钠的纯度往往不高 ,含有较多具有旋光性的杂质,故不适用于工业生产葡萄糖酸钠的检测,可用于食品添加剂葡萄糖酸钠的检测。[size=18px][color=#333333][back=#ffffff]6.葡萄糖酸钠的标准[/back][/color][/size][font='宋体'][size=18px][color=#333333][1][/color][/size][/font][color=#333333][back=#ffffff]6.1.感官要求[/back][/color][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262015129311_283_1608728_3.png[/img][color=#333333][back=#ffffff]6.2.物化指标[/back][/color][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262015130223_2270_1608728_3.png[/img][size=18px]总结与展望[/size][size=16px]葡萄糖酸钠被广泛应用于食品工业[/size][size=16px],[/size][size=16px]但对于国内的发展现状[/size][size=16px],[/size][size=16px]无论是生产工艺还是检测方法[/size][size=16px],[/size][size=16px]都有许多有待提高的方面[/size][size=16px]。[/size][size=16px]未来对于食品添加剂葡萄糖酸钠的研究[/size][size=16px],[/size][size=16px]应着眼于开发高效绿色的生产方法[/size][size=16px],[/size][size=16px]进一步完善食品安全标准并确立准确高效的检测手段。同时对葡萄糖酸钠在其他领域的应用价值进行探索,不局限于食品添加剂,拓宽其应用范畴。[/size][size=18px]参考文献 [/size][1]GB 1886.320-2021[2]杜裕芳,左艳娜,胡秋连,郝苗.食品添加剂葡萄糖酸钠的制备方法及其应用研究进展[J].食品界,2019,{4}(08):80-81.[3]黄道震,余丽秀,王桂香,何纪光.葡萄糖酸钠的生产工艺及研究动态[J].河南化工,1999,{4}(05):35-36.[4]GB 2760—2014[5]李艳,肖凯军,王兆梅,陈朝毅,郭祀远.葡萄糖酸钠检测方法研究[J].食品研究与开发,2006,{4}(09):109-112.