请问2010药典中,TOC测定制药用水中的蔗糖对照品,1,4-苯醌对照品如何购买?是直接向中检所购买吗,还是普通的分析纯或者优级纯就可以了?
现在我们公司增加辅料乙醇和醋酸钠的红外检测,需要购买红外乙醇对照品和醋酸钠对照品。请各位大侠提供除了中检所外,能够在一个星期内买到的厂家。谢谢大家了!!!!
本人现在用[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]测硬脂酸镁,为什么对照品溶液中有很多杂峰,我用的正庚烷是色谱纯级别的,还有到最后计算是用不到对照品的浓度,那为什么还要进对照品?请各位老师指点
各位大虾,在做液相时称量对照品真是个头疼的问题。我用的是赛多利斯十万分之一的天平称量,价格贵啊,所以每次称量几毫克,但是天平读数变化好大哦,好一会儿才稳定,咨询买仪器的人家说就是那样,我总觉得不保险啊。这对照品都不准的话,怎么保证结果啊,打算用称量漏斗来称量,这样读数稳定,不会撒到外面,称两三毫克都很稳定,反复试了试重现性还可以,自认为比较可靠。不知道有没有什么问题啊?各位大侠,您们又是怎么做的呢?
化妆品工业高速发展,大大小小的化妆品生产企业遍布各地,近年来,化妆品损害消费者健康的事件时有发生,因此加强对化妆品的监测尤为重要。氢醌和苯酚具有一定的美白作用,但其毒性和刺激性大,故我国卫生标准规定:祛斑类化妆品中禁用氢醌和苯酚。由于此类物质易获得且价格低廉,常被一些化妆品生产厂家用于祛斑类漂白化妆品中,长期使用含量高的氢醌类化妆品会引起皮肤刺激,色素加深甚至出现白斑。苯酚在医疗上常用于消毒,3%~5%水溶液可消毒皮肤,但苯酚对皮肤刺激性很大,可引起刺激损伤。 由于目前只有《化妆品卫生规范》中规定化妆品中苯酚和氢醌的检测,但由于化妆品种类繁多,基体复杂,只通过甲醇、乙醇提取后,上机分析,净化效果不佳,易造成假阳性;迪马科技根据目标物的性质特征,建立了SPE固相萃取柱-ProElut PSA进行前处理净化,高效液相色谱检测化妆品中苯酚和氢醌的解决方案,具有前处理简单,回收率损失少,固相萃取柱净化效果明显、重现性好等优点。 详细解决方案如下:
[align=center][font='times new roman'][size=20px]藤青泡[/size][/font][font='times new roman'][size=20px]腾片[/size][/font][font='times new roman'][size=20px]纯化[/size][/font][font='times new roman'][size=20px]工艺研究[/size][/font][/align][size=16px]由于提取工艺中采用水为溶剂,其极性大,浸出范围广,选择性较差,药材中的有机酸盐、多糖、蛋白质、[/size][size=16px]苷[/size][size=16px]类、黄酮等均能被浸出,所含与疗效无关的成份较多,使浸膏得率偏高,患者每天所需服用量大,顺应性差,因此采用适当的方法进行纯化。[/size][size=16px]本实验采用醇沉的方法对药液进行[/size][size=16px]纯化,沉淀除去[/size][size=16px]药[/size][size=16px]液中的[/size][size=16px]多糖、蛋白质[/size][size=16px]等杂质,[/size][size=16px]以提高有效成分纯度[/size][size=16px]。[/size][size=16px]采[/size][size=16px]用正交试验的方法考察各因素对醇[/size][size=16px]沉结果[/size][size=16px]的影响,筛选最佳醇沉条件。[/size][font='times new roman'][size=20px]仪器与试药[/size][/font][size=16px]([/size][size=16px]1[/size][size=16px])[/size][size=16px]实验仪器[/size][table][tr][td][size=16px]低温冷却液循环泵[/size][size=16px]DLSB-5/20[/size][/td][td][size=16px]郑州长城科技工贸有限公司[/size][/td][/tr][tr][td][size=16px]循环水式多用真空泵[/size][size=16px]SHB -[/size][size=16px]Ⅲ[/size][/td][td][size=16px]郑州长城科技工贸有限公司[/size][/td][/tr][tr][td][size=16px]旋转蒸发仪[/size][size=16px]RE-2000[/size][/td][td][size=16px]上海亚荣生化[/size][size=16px]仪器厂[/size][/td][/tr][tr][td][size=16px]低速多管离心机[/size][size=16px]LXJ-[/size][size=16px]Ⅱ[/size][size=16px]B[/size][/td][td][size=16px]上海飞鸽电器厂[/size][/td][/tr][/table][size=16px]([/size][size=16px]2[/size][size=16px])[/size][size=16px]实验试药[/size][table][tr][td][size=16px]无水乙醇[/size][size=16px] (AR)[/size][/td][td][size=16px]国药集团化学试剂有限公司[/size][/td][/tr][/table][font='times new roman'][size=20px]泡腾片醇沉工艺条件的研究[/size][/font][font='times new roman'][size=18px]醇沉正交试验筛选[/size][/font][size=16px]称取药材藤茶、葛花、青果、甘草各[/size][size=16px]0.5[/size][size=16px]倍处方量,共[/size][size=16px]1[/size][size=16px]份,按[/size][size=16px]“[/size][size=16px]1.2.1[/size][size=16px]”[/size][size=16px]项所筛选的最佳提取工艺[/size][size=16px]A3B1C3[/size][size=16px],即[/size][size=16px]20[/size][size=16px]倍量水、提取[/size][size=16px]0.5h[/size][size=16px]、提取[/size][size=16px]3[/size][size=16px]次,合并[/size][size=16px]3[/size][size=16px]次提取液,分成[/size][size=16px]9[/size][size=16px]份,每份[/size][size=16px]350 ml[/size][size=16px],以提取液浓度([/size][size=16px]A[/size][size=16px]),含醇量([/size][size=16px]B[/size][size=16px]),醇沉时间([/size][size=16px]C[/size][size=16px])为考察因素,按表[/size][size=16px]5[/size][size=16px]的因素水平进行[/size][size=16px]L9[/size][size=21px]([/size][size=16px]3[/size][font='times new roman'][size=16px]4[/size][/font][size=21px])[/size][size=16px]正交试验,并以总黄酮提取量、干浸膏得率为评价指标,考察最佳醇沉工艺条件。[/size][size=16px]醇沉浸膏得率的测定[/size][size=16px]精密量取上述醇沉后药液[/size][size=16px]5 ml[/size][size=16px],参照[/size][size=16px]“[/size][size=16px]1.2.1[/size][size=16px].1”[/size][size=16px]项下的方法测定浸膏得率,结果见表[/size][size=16px]6[/size][size=16px]。[/size][size=16px]醇沉后总黄酮的含量测定[/size][size=16px]对照品溶液的制备:对照品溶液的制备:[/size][size=16px]称[/size][size=16px]芦丁对照品适量,精密称定,加甲醇溶解[/size][size=16px]并定量稀释至每[/size][size=16px]1 ml[/size][size=16px]含[/size][size=16px]0.2 mg[/size][size=16px]的[/size][size=16px]芦丁溶液,[/size][size=16px]制得对照品溶液[/size][size=16px]。[/size][size=16px]供试品溶液[/size][size=16px]的制备:取上述[/size][size=16px]9[/size][size=16px]份醇沉后药液各[/size][size=16px]1 ml[/size][size=16px],置[/size][size=16px]50 ml[/size][size=16px]容量瓶中,并用水稀释至刻度。[/size][size=16px]芦丁对照品标准曲线制备:芦丁对照品标准曲线制备:精密吸取芦丁对照品溶液[/size][size=16px]0.0[/size][size=16px],[/size][size=16px]1.0[/size][size=16px],[/size][size=16px]2.0[/size][size=16px],[/size][size=16px]3.0[/size][size=16px],[/size][size=16px]4.0[/size][size=16px],[/size][size=16px]5.0[/size][size=16px],[/size][size=16px]6.0[/size][size=16px] [/size][size=16px]ml[/size][size=16px],分别置[/size][size=16px]25 ml[/size][size=16px]([/size][size=16px]V[/size][font='times new roman'][size=16px]3[/size][/font][size=16px])量瓶中,加水至[/size][size=16px]6 ml[/size][size=16px],[/size][size=16px]加入[/size][size=16px]1 ml[/size][size=16px]的[/size][size=16px]5%[/size][size=16px][back=#ffffff] NaNO[/back][/size][font='times new roman'][size=16px][back=#ffffff]2[/back][/size][/font][size=16px],[/size][size=16px]混匀,放置[/size][size=16px]6min[/size][size=16px],[/size][size=16px]往容量瓶里加入[/size][size=16px]1 ml[/size][size=16px]的[/size][size=16px]10%A[/size][size=16px]l[/size][size=16px](NO[/size][font='times new roman'][size=16px]3[/size][/font][size=16px])[/size][font='times new roman'][size=16px]3[/size][/font][size=16px],[/size][size=16px]混匀后静置[/size][size=16px]6min[/size][size=16px],加[/size][size=16px]入[/size][size=16px]10[/size][size=16px] ml [/size][size=16px]NaOH[/size][size=16px]试液,[/size][size=16px]混匀,[/size][size=16px]加[/size][size=16px]蒸馏[/size][size=16px]水至刻度,[/size][size=16px]混匀[/size][size=16px],[/size][size=16px]静置[/size][size=16px]15[/size][size=16px]分钟,以[/size][size=16px]0.0 ml[/size][size=16px]对照品溶液制[/size][size=16px]备[/size][size=16px]的溶剂为空白[/size][size=16px]对照[/size][size=16px],[/size][size=16px]在[/size][size=16px]510nm[/size][size=16px]波长下[/size][size=16px]测定[/size][size=16px]各组的[/size][size=16px]吸[/size][size=16px]光[/size][size=16px]度值。[/size][size=16px]以吸光度为纵坐标[/size][size=16px]([/size][size=16px]A[/size][size=16px])[/size][size=16px],浓度为横坐标([/size][size=16px]mg/ml[/size][size=16px]),绘制标准曲线[/size][size=16px], [/size][size=16px]结果见图[/size][size=16px]2.[/size][size=16px]样品测定:[/size][size=16px]精密吸取精密吸取[/size][size=16px]供试溶液[/size][size=16px]8 ml[/size][size=16px]([/size][size=16px]V[/size][font='times new roman'][size=16px]2[/size][/font][size=16px]),至[/size][size=16px]25 ml[/size][size=16px]量瓶中,照[/size][size=16px]“[/size][size=16px]1.2.1[/size][size=16px].2”[/size][size=16px]自[/size][size=16px]“[/size][size=16px]加入[/size][size=16px]5%[/size][size=16px]亚硝酸钠溶液[/size][size=16px]1 ml”[/size][size=16px]起,在波长[/size][size=16px]510nm[/size][size=16px]处分别测定吸收度值,[/size][size=16px][color=#000000]从标准曲线上读出[/color][/size][size=16px][color=#000000]供试品溶液中含总黄酮[/color][/size][size=16px][color=#000000]的浓度[/color][/size][size=16px][color=#000000]([/color][/size][size=16px][color=#000000]C[/color][/size][size=16px][color=#000000])[/color][/size][size=16px][color=#000000],计算样品中总黄酮的含量([/color][/size][size=16px][color=#000000]X[/color][/size][size=16px][color=#000000])。[/color][/size][size=16px]计算方法:[/size][size=16px]参照[/size][size=16px]“[/size][size=16px]1.2.1[/size][size=16px].2”[/size][size=16px]项下的[/size][size=16px]计算方法进行计算。结果见表[/size][size=16px]6[/size][size=16px],表[/size][size=16px]7.[/size][size=16px][color=#000000]图[/color][/size][size=16px][color=#000000]2 [/color][/size][size=16px][color=#000000]芦丁标准品标准曲线[/color][/size][align=center][img]https://ng1.17img.cn/bbsfiles/images/2020/09/202009241153149717_1330_2166779_3.jpeg[/img][/align][align=center][size=16px]表[/size][size=16px]5[/size][size=16px]醇沉正交试验因素水平表[/size][/align][table][tr][td=1,2][align=center][size=16px]水平[/size][/align][/td][td=3,1][align=center][size=16px]因素[/size][/align][/td][/tr][tr][td][align=center][size=16px]A[/size][size=16px]药液相对密度[/size][/align][/td][td][align=center][size=16px]B[/size][size=16px]含醇量[/size][size=16px](%)[/size][/align][/td][td][align=center][size=16px]C[/size][size=16px]醇[/size][size=16px]沉时间[/size][size=16px](h)[/size][/align][/td][/tr][tr][td][align=center][size=16px]1[/size][/align][/td][td][align=center][size=16px]1.0035-1.0039[/size][/align][/td][td][align=center][size=16px]60[/size][/align][/td][td][align=center][size=16px]16[/size][/align][/td][/tr][tr][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]1.0009-1.0016[/size][/align][/td][td][align=center][size=16px]70[/size][/align][/td][td][align=center][size=16px]20[/size][/align][/td][/tr][tr][td][align=center][size=16px]3[/size][/align][/td][td][align=center][size=16px]0.9959-0.9965[/size][/align][/td][td][align=center][size=16px]80[/size][/align][/td][td][align=center][size=16px]24[/size][/align][/td][/tr][/table][size=16px]注:以[/size][size=16px]D[/size][size=16px]因素为误差项[/size][size=16px]采用[/size][size=16px][back=#ffffff]加权平均法对浸膏得率、总黄酮含量进行综合评分,由于[/back][/size][size=16px][back=#ffffff]含量对泡腾[/back][/size][size=16px][back=#ffffff]片疗效的影响较大,因此,分别给予浸膏得率、总黄酮含量[/back][/size][size=16px][back=#ffffff]40%[/back][/size][size=16px][back=#ffffff]、[/back][/size][size=16px][back=#ffffff]60%[/back][/size][size=16px][back=#ffffff]的权重进行分配。浸膏的率越高,患者最终单次的给[/back][/size][size=16px][back=#ffffff]药量越[/back][/size][size=16px][back=#ffffff]多,宜越低越好,故以最低得率[/back][/size][size=16px]18.68[/size][size=16px][back=#ffffff]%[/back][/size][size=16px][back=#ffffff]为最高得分,而总黄酮为主要有效成份,宜越高越好,故以[/back][/size][size=16px]1.625[/size][size=16px][back=#ffffff]为最高得分。以序号[/back][/size][size=16px][back=#ffffff]1[/back][/size][size=16px][back=#ffffff]为例计算综合评分:[/back][/size][size=16px][back=#ffffff]([/back][/size][size=16px]18.680[/size][size=16px][back=#ffffff]/[/back][/size][size=16px]28.002[/size][size=16px][back=#ffffff])*0.4+(1.190/1.625)*0.6=0.706[/back][/size][size=16px][back=#ffffff],同理,可求得其余各综合评分,结果见表[/back][/size][size=16px][back=#ffffff]6[/back][/size][size=16px][back=#ffffff].[/back][/size][align=center][size=16px]表[/size][size=16px]6[/size][size=16px]醇沉正交试验结果([/size][size=16px]n[/size][size=16px]=9[/size][size=16px])[/size][/align][table][tr][td][align=center][font='宋体'][size=16px]序号[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]A[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]B[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]C[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]D[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]浸膏得率[/size][/font][size=16px](%)[/size][/align][/td][td][align=center][font='宋体'][size=16px]总黄酮含量[/size][/font][size=16px](g)[/size][/align][/td][td][align=center][font='宋体'][size=16px]综合评分[/size][/font][/align][/td][/tr][tr][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][size=16px]28.002 [/size][/align][/td][td][align=center][size=16px]1.190 [/size][/align][/td][td][align=center][size=16px]0.706 [/size][/align][/td][/tr][tr][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][size=16px]18.680 [/size][/align][/td][td][align=center][size=16px]0.863 [/size][/align][/td][td][align=center][size=16px]0.719 [/size][/align][/td][/tr][tr][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][size=16px]27.900 [/size][/align][/td][td][align=center][size=16px]1.143 [/size][/align][/td][td][align=center][size=16px]0.690 [/size][/align][/td][/tr][tr][td][align=center][font='宋体'][size=16px]4[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][size=16px]30.799 [/size][/align][/td][td][align=center][size=16px]1.405 [/size][/align][/td][td][align=center][size=16px]0.761 [/size][/align][/td][/tr][tr][td][align=center][font='宋体'][size=16px]5[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][size=16px]30.447 [/size][/align][/td][td][align=center][size=16px]1.370 [/size][/align][/td][td][align=center][size=16px]0.751 [/size][/align][/td][/tr][tr][td][align=center][font='宋体'][size=16px]6[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][size=16px]28.441 [/size][/align][/td][td][align=center][size=16px]1.313 [/size][/align][/td][td][align=center][size=16px]0.747 [/size][/align][/td][/tr][tr][td][align=center][font='宋体'][size=16px]7[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][size=16px]32.887 [/size][/align][/td][td][align=center][size=16px]1.592 [/size][/align][/td][td][align=center][size=16px]0.815 [/size][/align][/td][/tr][tr][td][align=center][font='宋体'][size=16px]8[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][size=16px]31.601 [/size][/align][/td][td][align=center][size=16px]1.582 [/size][/align][/td][td][align=center][size=16px]0.820 [/size][/align][/td][/tr][tr][td][align=center][font='宋体'][size=16px]9[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][size=16px]31.258 [/size][/align][/td][td][align=center][size=16px]1.625 [/size][/align][/td][td][align=center][size=16px]0.839 [/size][/align][/td][/tr][tr][td][align=center][size=16px]K1[/size][/align][/td][td][align=center][size=16px]2.11 [/size][/align][/td][td][align=center][size=16px]2.28 [/size][/align][/td][td][align=center][size=16px]2.27 [/size][/align][/td][td][align=center][size=16px]2.30 [/size][/align][/td][td][/td][td][/td][td][/td][/tr][tr][td][align=center][size=16px]K2[/size][size=16px] [/size][/align][/td][td][align=center][size=16px]2.26 [/size][/align][/td][td][align=center][size=16px]2.29 [/size][/align][/td][td][align=center][size=16px]2.32 [/size][/align][/td][td][align=center][size=16px]2.28 [/size][/align][/td][td][/td][td][/td][td][/td][/tr][tr][td][align=center][size=16px]K3[/size][/align][/td][td][align=center][size=16px]2.47 [/size][/align][/td][td][align=center][size=16px]2.28 [/size][/align][/td][td][align=center][size=16px]2.26 [/size][/align][/td][td][align=center][size=16px]2.27 [/size][/align][/td][td][/td][td][/td][td][/td][/tr][tr][td][align=center][size=16px]R[/size][/align][/td][td][align=center][size=16px]0.12 [/size][/align][/td][td][align=center][size=16px]0.00 [/size][/align][/td][td][align=center][size=16px]0.02 [/size][/align][/td][td][align=center][size=16px]0.01 [/size][/align][/td][td][align=center][font='宋体'][size=16px] [/size][/font][/align][/td][td][align=center][font='宋体'][size=16px] [/size][/font][/align][/td][td][align=center][font='宋体'][size=16px] [/size][/font][/align][/td][/tr][/table][align=center][size=16px]表[/size][size=16px]7 [/size][size=16px]醇沉正交试验方差分析[/size][/align][table][tr][td][align=center][size=16px]方差来源[/size][/align][/td][td][align=center][size=16px]离差平方和[/size][/align][/td][td][align=center][size=16px]自由度[/size][/align][/td][td][align=center][size=16px]F[/size][size=16px]值[/size][/align][/td][td][align=center][size=16px]均方[/size][/align][/td][td][align=center][size=16px]显著性[/size][/align][/td][/tr][tr][td][align=center][size=16px]相对密度[/size][/align][/td][td][align=center][size=16px]0.02185[/size][/align][/td][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]205.2415[/size][/align][/td][td][align=center][size=16px]0.01093[/size][/align][/td][td][align=center][size=16px]**[/size][/align][/td][/tr][tr][td][align=center][size=16px]含醇量[/size][/align][/td][td][align=center][size=16px]0.00003302[/size][/align][/td][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]0.3101[/size][/align][/td][td][align=center][size=16px]0.00001651[/size][/align][/td][td][/td][/tr][tr][td][align=center][size=16px]醇[/size][size=16px]沉时间[/size][size=16px] [/size][/align][/td][td][align=center][size=16px]0.0007093[/size][/align][/td][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]6.6615[/size][/align][/td][td][align=center][size=16px]0.0003547[/size][/align][/td][td][/td][/tr][tr][td][align=center][size=16px]误差[/size][/align][/td][td][align=center][size=16px]0.0001065[/size][/align][/td][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]1.0000 [/size][/align][/td][td][align=center][size=16px]0.00005324[/size][/align][/td][td][/td][/tr][/table][size=16px]由表[/size][size=16px]7[/size][size=16px]可知,以总黄酮含量与水提取液浸膏得率为[/size][size=16px]评价[/size][size=16px]指标,[/size][size=16px]各因素对结果的影响大小为:[/size][size=16px]药液相对密度[/size][size=16px][/size][size=16px]醇[/size][size=16px]沉时间[/size][size=16px][/size][size=16px]含醇量,即主要影响因素是药液相对密度,其次是醇沉时间,[/size][size=16px]含醇量[/size][size=16px]影响[/size][size=16px]最小[/size][size=16px]。[/size][size=16px]以实验[/size][size=16px]结果[/size][size=16px]为参考[/size][size=16px],结合实际[/size][size=16px]生产情况,最终[/size][size=16px]确定[/size][size=16px]醇沉[/size][size=16px]工艺为[/size][size=16px]:药液[/size][size=16px]相对密度为[/size][size=16px]0.9959-0.9965[/size][size=16px],[/size][size=16px]含醇量[/size][size=16px]70%[/size][size=16px],醇[/size][size=16px]沉时间[/size][size=16px]20h[/size][size=16px]。[/size][font='times new roman'][size=18px]醇沉正交验证实验[/size][/font][size=16px]根据以上所选最佳醇沉工艺条件,相对密度为[/size][size=16px]0.9959-0.9965[/size][size=16px],[/size][size=16px]含醇量[/size][size=16px]70%[/size][size=16px],醇[/size][size=16px]沉时间[/size][size=16px]20h[/size][size=16px],平行[/size][size=16px]3[/size][size=16px]份,对醇沉后药液的浸膏得率与总黄酮含量进行测定,按[/size][size=16px]2.2.1[/size][size=16px].2[/size][size=16px]项下的方法计算综合评分后,[/size][size=16px]求平均[/size][size=16px]得分,结果见表[/size][size=16px]8.[/size][align=center][size=16px]表[/size][size=16px]8[/size][size=16px]醇沉正交实验验证结果([/size][size=16px]n[/size][size=16px]=3[/size][size=16px])[/size][/align][table][tr][td][align=center][size=16px]编号[/size][/align][/td][td][align=center][size=16px]浸膏得率[/size][size=16px](%)[/size][/align][/td][td][align=center][size=16px]总黄酮含量[/size][size=16px](g)[/size][/align][/td][td][align=center][size=16px]综合评分[/size][/align][/td][td][align=center][size=16px]平均得分[/size][/align][/td][/tr][tr][td][align=center][size=16px]1[/size][/align][/td][td][align=center][size=16px]27.9[/size][/align][/td][td][align=center][size=16px]1.780[/size][/align][/td][td][align=center][size=16px]0.925[/size][/align][/td][td=1,3][align=center][size=16px]0.918[/size][/align][/td][/tr][tr][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]28.4[/size][/align][/td][td][align=center][size=16px]1.757[/size][/align][/td][td][align=center][size=16px]0.911[/size][/align][/td][/tr][tr][td][align=center][size=16px]3[/size][/align][/td][td][align=center][size=16px]28.4[/size][/align][/td][td][align=center][size=16px]1.776[/size][/align][/td][td][align=center][size=16px]0.918[/size][/align][/td][/tr][/table][size=16px]由表[/size][size=16px]8[/size][size=16px]可知,最佳醇沉工艺的平均得分[/size][size=16px]0.918[/size][size=16px],大于正交设计中的各项综合评分,且评分最高,有较高的准确率,所筛选的醇沉工艺条件基本稳定,可作为[/size][size=16px]藤青泡[/size][size=16px]腾片的醇沉方法。[/size][font='times new roman'][size=20px]小结与讨论[/size][/font][size=16px]通过正交实验,确定最佳醇沉工艺为:将药液浓缩至相对密度为[/size][size=16px]0.9959-0.9965[/size][size=16px],[/size][size=16px]含醇量[/size][size=16px]70%[/size][size=16px],醇[/size][size=16px]沉时间[/size][size=16px]20h[/size][size=16px]。醇沉正交试验过程中,各实验组尽可能采用同一批次的提取液,以排除提取因素对结果的影响,且提取液放置过程会有少许沉淀,取样时应先混匀;测定相对密度时,要待浓缩的药液冷却至室温后再测,因高温会是玻璃比重瓶体积变大,导致结果不准确;加入乙醇的过程中,乙醇的滴加速度以及搅拌速度应当一致,到醇[/size][size=16px]沉时间[/size][size=16px]后,及时分离出沉淀物并用旋转蒸发仪回收乙醇。[/size]
今天我把昨天的两份对照品储备液分别稀释成对照品溶液,顶空进样,但是第一份对照品溶液待测组分未出峰,第2份对照品溶液出峰正常,我想问下隔24小时以后再用待测组分都会挥发完全吗?为什么第二份正常出峰呀?对照品溶液里面的组分分别是乙醇,乙酸乙酯,丙酮,二氯甲烷,水为溶剂
大家经常做气相需要测对照品溶液,有时对照品溶液的出峰面积在不同时期可能差异较大,大家遇到过这样的问题吗?问题:取甲醇、乙酸乙酯、甲苯适量,精密称定,用DMF溶解稀释定容制成每1ml中约含甲醇60ug、乙酸乙酯100ug、甲苯20ug的混合溶液。那么我们实际称取的对照质量应该在什么范围内是可以接受的?因为称量的差异会导致对照品出峰面积的差异。问题:如何能用天平称准对照试剂的量?(有机溶剂甲醇、乙腈、二氯甲烷等)换算成体积量取还是直接称取?
目前国内一些不良化妆品生产企业,为了使化妆品达到较好的祛斑效果,往往会添加氢醌和苯酚, 氢醌和苯酚具有一定的美白作用,但其毒性和刺激性大,故我国卫生标准规定:祛斑类化妆品中禁用氢醌和苯酚。 不过,由于此类物质易获得且价格低廉,常被一些化妆品生产厂家用于祛斑类漂白化妆品中,长期使用含量高的氢醌类化妆品会引起皮肤刺激,色素加深甚至出现白斑。苯酚在医疗上常用于消毒,3%~5%水溶液可消毒皮肤,但苯酚对皮肤刺激性很大,可引起刺激损伤。 目前只有《化妆品卫生规范》中规定化妆品中苯酚和氢醌的检测,但由于化妆品种类繁多而且基体复杂,规定中前处理,只通过甲醇、乙醇提取后,上机分析,净化效果不佳,易造成假阳性; 针对以上问题,迪马科技根据目标物的性质特征,建立了SPE固相萃取柱-ProElut PSA进行前处理净化,高效液相色谱检测化妆品中苯酚和氢醌的解决方案,具有前处理简单,回收率损失少,固相萃取柱净化效果明显、重现性好等优点。详细解决方案如下:1 适用范围该方法适用于祛斑类化妆品和香波中氢醌、苯酚含量的测定。2 样品准备2.1 香波类化妆品(1) 取1 g样品,加入3mL饱和氯化钠溶液,5 mL提取液*,涡旋1 min,6000 rpm下离心2 min,收集上清液;(2) 将下层残留物再用5 mL提取液*重复提取一次,合并两次提取上清液;(3) 将上清液用提取液*定容至10 mL,混匀,供HPLC测定。2.2 乳液、面霜等化妆品(1) 取1 g样品,加入3mL饱和氯化钠溶液,5 mL提取液*,涡旋1 min,6000 rpm下离心2 min,收集上清液;(2) 将下层残留物再用5 mL提取液*重复提取一次,合并两次提取上清液;(3) 将上清液用提取液*定容至10 mL,混匀,取5 mL上清液并加入2.5 mL正己烷,混匀待净化。提取液*:甲基叔丁基醚:正己烷=3:13乳液、面霜等化妆品的SPE柱净化——ProElut PSA 1 g/6 mL (Cat.#:63206)(1)活 化:向柱中加入5 mL甲基叔丁基醚:正己烷=1:1,弃去流出液;(2)上 样:将待净化液加入柱中,弃去流出液;(3)淋 洗:向柱中加入5 mL正己烷,弃去流出液;(4)洗 脱:向柱中加入5 mL甲醇,收集流出液;(5)重新溶解:将洗脱液在40 ℃缓慢通入氮气吹至1 mL,再用二氯甲烷定容至1 mL,供HPLC分析。4 分析条件色谱柱:Diamonsil C18(2),250 mm×4.6 mm,5μm(Cat# 99603)流 速:1.0mL/min检测器:*UV 280nm柱 温:30℃ 进样量: 20 μL流动相:A:水B:甲醇梯度时间(min)010151625A(%)8050308080B(%)2050702020*本方法中,目标化合物是由[color=b
高效液相色谱仪对照品的纯度要求是多少?
百眼藤【英文名】Littleleaf Indianmulberry, Littleleaf Indianmulberry Herb, Root or stem of Littleleaf Indianmulberry【别名】爬山虎、五眼子、泥藤草、鸡眼藤、猪糠藤、爬山虎、咸鱼头、大甘草、小叶羊角藤【来源】药材基源:为双子叶植物药茜草科植物细叶巴戟天的全株。拉丁植物动物矿物名:Morinda parvifolia Bartl.ex DC.采收和储藏:夏、秋季采收,洗净,晒干。【原形态】攀援灌木。小枝顶部被短粗毛。叶对生;叶柄长4-8mm;托叶膜质,长2-3mm;叶片倒卵状椭圆形,稀椭圆形,衡椭圆状长圆形,长2-6cm,宽1-2(-3)cm,先端急尖或钝而具小凸尖,基部楔形,上面无毛,下面脉腋内有短束毛和有时沿主脉上被短粗毛,纸质。花序由2-6个小头状花序组成伞形花序式顶生,小头状花序直径5-8mm,有花4-8朵,着生于长5-10mm的总花梗上;萼简半球形,长约1mm;花冠白色或绿白色,长约5mm,裂片4,几达基部,长圆状披针形,近中部以下密被卷绒毛,顶端内弯。聚合果扁球形,直径8-10mm,熟时红色。花期夏季。【生境分布】生态环境:生于山野灌丛中。资源分布:分布我国南部。【化学成份】全株含蒽醌类成分:百眼藤醌(morindaparvin)A、B,茜草素-1-甲醚(alizarin-1-methyl ether),光泽定-w-乙醚(luicdin-w-ethyl ether),光泽定-w-甲醚(lucidin-w-methyl ether),锈色洋地黄醌醇(digiferruginol),1-羟基-6-或7-羟甲基蒽醌(1-hy-droxy-6-or 7-hydroxymethyl anthraquinone)和2-羟甲基蒽醌(2-hy-droxymethyl anthraquinone)。【药理作用】本品所含成分百契藤醌A对BDF;小鼠体内P388淋巴细胞白血病具有较强的抑制作用。在10mg/(dg·d)剂量下,百眼藤醌A抗小鼠P388淋巴细胞白血病的T/C(治疗动物生存/对照动物生存率)为129%。体外细胞培养试验表明,百眼藤醌A和从百眼藤中新分离出的百眼藤醌B抑制P388淋巴细胞白敌国病组织细胞生长的ED50分别为1.85μg/ml和10.5μg/ml,抑制鼻咽癌(KB)细胞生长的ED50分别为10μg/ml和4.0μg/ml。【性味】甘;凉【归经】肺经【功能主治】清热解毒;散瘀止痛;和胃化湿。主感冒咳嗽;百日咳;消化不良;湿疹;跌打损伤,腰肌劳损【用法用量】内服:煎汤,15-60g。
问下:吸取的对照品无水甲醇、乙醛、乙缩醛是专门的对照品吗?还有用到的50μl、100μl、150μl取样管是微量进样器吗?
【英文名】Littleleaf Indianmulberry, Littleleaf Indianmulberry Herb, Root or stem of Littleleaf Indianmulberry【别名】爬山虎、五眼子、泥藤草、鸡眼藤、猪糠藤、爬山虎、咸鱼头、大甘草、小叶羊角藤【来源】药材基源:为双子叶植物药茜草科植物细叶巴戟天的全株。拉丁植物动物矿物名:Morinda parvifolia Bartl.ex DC.采收和储藏:夏、秋季采收,洗净,晒干。【原形态】攀援灌木。小枝顶部被短粗毛。叶对生;叶柄长4-8mm;托叶膜质,长2-3mm;叶片倒卵状椭圆形,稀椭圆形,衡椭圆状长圆形,长2-6cm,宽1-2(-3)cm,先端急尖或钝而具小凸尖,基部楔形,上面无毛,下面脉腋内有短束毛和有时沿主脉上被短粗毛,纸质。花序由2-6个小头状花序组成伞形花序式顶生,小头状花序直径5-8mm,有花4-8朵,着生于长5-10mm的总花梗上;萼简半球形,长约1mm;花冠白色或绿白色,长约5mm,裂片4,几达基部,长圆状披针形,近中部以下密被卷绒毛,顶端内弯。聚合果扁球形,直径8-10mm,熟时红色。花期夏季。【生境分布】生态环境:生于山野灌丛中。资源分布:分布我国南部。【化学成份】全株含蒽醌类成分:百眼藤醌(morindaparvin)A、B,茜草素-1-甲醚(alizarin-1-methyl ether),光泽定-w-乙醚(luicdin-w-ethyl ether),光泽定-w-甲醚(lucidin-w-methyl ether),锈色洋地黄醌醇(digiferruginol),1-羟基-6-或7-羟甲基蒽醌(1-hy-droxy-6-or 7-hydroxymethyl anthraquinone)和2-羟甲基蒽醌(2-hy-droxymethyl anthraquinone)。【药理作用】本品所含成分百契藤醌A对BDF;小鼠体内P388淋巴细胞白血病具有较强的抑制作用。在10mg/(dg·d)剂量下,百眼藤醌A抗小鼠P388淋巴细胞白血病的T/C(治疗动物生存/对照动物生存率)为129%。体外细胞培养试验表明,百眼藤醌A和从百眼藤中新分离出的百眼藤醌B抑制P388淋巴细胞白敌国病组织细胞生长的ED50分别为1.85μg/ml和10.5μg/ml,抑制鼻咽癌(KB)细胞生长的ED50分别为10μg/ml和4.0μg/ml。【性味】甘;凉【归经】肺经【功能主治】清热解毒;散瘀止痛;和胃化湿。主感冒咳嗽;百日咳;消化不良;湿疹;跌打损伤,腰肌劳损【用法用量】内服:煎汤,15-60g。
大家都用那些容积配置过黄芩苷对照品啊?怎么我们用稀乙醇溶液溶解的时候不易溶解啊,超声半小时还会有很多不容物?
做一个甾体皂苷的含量测定,已经做第4次了,问题始终没解决,遂请教。具体要求如下:色谱条件要求:C8的柱子;流动相是乙腈-水(30:70);检测波长210nm。样品处理:取一定量,加75%乙醇超声10分钟,放冷,补足减失重量,滤过,即可。 对照品也是用75%乙醇溶解。测试经过如下:有同一厂家同一品种不同批号两批样品,用C8的柱子做,计算了下,含量合格,但峰实在太难看。怕峰形太差影响结果的准确性,但只有一根这C8的柱子,只好换根C18的柱子,调整流动相试试;峰形很好,进了一针其中一批的样品,计算了也合格,就编个序列继续做下去了。第四天才发现另一批不合格,只好第五天返工。第二次,问题出现了。返工时,同样的仪器,色谱柱,色谱条件,用原来配的对照品溶液,重新处理样品,不合格的那一批还是不合格,结果比上次测的还低一点,合格的那批也不合格了。又另配了对照品溶液,与之前配的浓度相差不大,但峰面积小多了。但是之前配的对照品峰面积反而变大了,估计是因为流动相微调,把之前没分开的小峰分开了,不至于斜着积分的原因吧。怀疑过对照品峰面积小,是不是冷冻(对照品要求冷冻保存哈)后没放至室温,直接称,导致称不准。样品怀疑过的原因 A:是不是不合格那一批取样量大了,浓度高了,导致过饱和,未全溶 B:样品是不是未混匀,取样代表性不够 C:超声时间,功率是不是有问题,是不是超声发热导致样品降解(对照品要冷冻保存嘛)E:是不是第二次配的溶样溶剂有问题第三次做,更蹊跷了。之前怀疑的样品的原因都排除了。减少,增加取样量;混匀样品;超声不同时间,用不同超声设备(不同功率);超声中换水,防止温度升高,水浴上回流处理样品;重配75%乙醇几次,用无水乙醇配也试了,还换用甲醇,样品溶液居然都没有目标峰。但之前两次配的对照品溶液峰高变化不大,高的还是高,低的还是低。第四次,就是今天。又重配了对照品溶液,换甲醇(色谱纯)溶解,居然对照品也没峰了,用75%乙醇溶解也是。之前配的对照品峰高还是老样子。将第一次配的对照品溶液跟这次提取的测不到目标峰的样品溶液混合,也能出目标峰。这根柱子换走另一个对照品测试,峰好得很。再换另一根柱,走样品和对照品,还是老样子,之前能出的还出,出不了的还是还是出不了。总结:一共配了三次对照品,浓度差异不大,但峰面积在变小,第三次就没了。样品也是,第一次合格的,第二次提取也不合格了,以后干脆目标峰也不出了。 分析:应该不是目标物不稳定的原因,因为第一次配的对照品,隔了一周,峰高依然变化不大,更何况新配的对照品溶液。 几次都是我操作,对照品溶液都超声助溶过,应该也是溶了的。而且用紫外扫过,稀释后吸收值会降低,虽然最大吸收波长在约205nm。其实用甲醇比用75%乙醇溶解要好些,几乎振摇就能溶,用75%乙醇必须稍超声一下。[/fo
中检所提供的乙醇对照品乙醇浓度是多少?
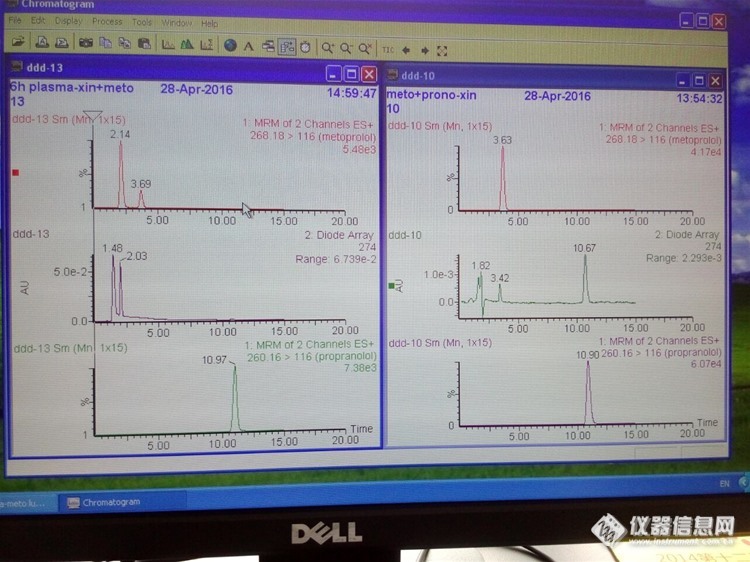
麻烦各位朋友帮忙分析一下了,困扰了我很久了,很多方法都试了,还是那样。情况介绍:流动相为甲醇-乙腈-0.2%甲酸水=10:15:75;样品为琥珀酸美托洛尔灌胃大鼠后血浆样品,图谱ddd-13;样品和对照品均用流动相作溶剂,对照品浓度远大于样品,图谱ddd-10;进样量5ul;MRM扫描。主要问题:质谱图提取后,对照品中美托洛尔是单峰;样品中美托洛尔是双峰,第一个峰的峰面积远大于第二个峰。样品为何会出双峰,真的都是美托洛尔?为何色谱保留时间差别很大?http://ng1.17img.cn/bbsfiles/images/2016/04/201604291443_591954_3099769_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/04/201604291444_591955_3099769_3.jpgfile:///C:\Program Files\Tencent\QQ\Users\540761932\Image\C2C\C8E4ADEAE357ABD265B94368610BE8C5.jpg
已知样品中含有醇类物质,如何使用高校液相色谱测试确定该醇类物质?对照品如何配制?
近日在做一个日本上市缓释制剂的仿制,对其释放度检查标准有些疑问,特别是其供试品的吸收度计算方法很特别,希望园里的老师给分析指点一下,谢谢!释放度的测定取本品,照释放度测定法,采用溶出度测定法第二装置,以Ph1.2盐酸溶液500ml为溶剂,转速为每分钟100转,依法操作,经1小时时,取溶液10ml,过滤,作为供试品溶液(1);弃去上述各容器中的酸液,加已预热至37±0.5℃的Ph7.5磷酸盐缓冲液500ml,继续运转至2小时时,取溶液10ml,过滤,作为供试品溶液(2);并补加同体积的Ph7.5磷酸盐缓冲液,继续运转至5小时时,取溶液10ml,过滤,作为供试品溶液(3);另取对照品约0.1g,精密称定,置50ml量瓶中,加甲醇适量使溶解,并稀释至刻度,摇匀;精密量取此溶液各1ml,置100ml量瓶中,分别加Ph1.2的盐酸溶液和Ph7.5磷酸盐缓冲液稀释至此刻度,摇匀,作为对照品溶液(1)和对照品溶液(2)。照分光光度法,供试品溶液(1)在360nm和450nm波长处测定吸收度,计算吸收度差值;其他各对照品溶液及供试品溶液均在360nm波长处测定吸收度,分别计算不同时间的释放量。
液相色谱检测,产品主峰峰纯度达不到要求,购买的中检所和EP对照品主峰纯度也不行。
我不小心那错了试剂,对照品用甲醇溶解,我拿了分析纯溶解,是否会影响结果?
在检测注射用甲磺酸左氧氟沙星含量时:中间体检测时用紫外检测,成品用的是高效液相检测,之前中间体用原料做工作对照,对照品A值一般在所配浓度下一般为0.39左右,F值在1.26左右,成品没什么问题,可是现在用中检所的对照品,中间体测定时对照品在相同浓度下A值才有0.35左右,这样的话F值就接近1.3了,结果含量就会高很多甚至不合格,但是成品上液相时又是合格的,也就是说对照品应该没问题,是不是中检所的对照品不适合用紫外分光光度法来检测呢?请各位帮忙分析分析,谢谢!!!补充:在这之前,该产品中间体检测都是用中检所的对照品上高效液相测定的,为了节省时间改用了紫外分光光度法检测工艺没改,液相测出来接过肯定会更精确些,但是奇怪的是,同样的对照品中间体检测超标,成品检测合格,不过之前用原料做工作对照检中间体时,成品标示量一般在100%以下,用中检所对照品检测中间体,成品标示量一般在105%,规定上限是110%没我是在想我们的中间体检测方法是不是不太合理制药工艺中没有纯化过程的,但是原料工作对照77.54%,中检所对照品97.3%,都是根据所需浓度换算好了再配制检测的,我是想应该里面所含杂质吸收影响就不明显了吧?您觉得呢?
[size=4]1.所用对照品(标准品)中检所已经发放提供(可参阅中国药典2005年版二部附录ⅩⅤG),且使用方法相同时,应使用中检所提供的现行批号对照品(标准品),并提供其标签和使用说明书,说明其批号,不应使用其他来源者;如使用方法与说明书使用方法不同(如定性对照品用作定量用、效价测定用标准品用作理化测定法定量、UV法或容量法对照品用作色谱法定量等),应采用适当方法重新标定,并提供标定方法和数据;若色谱法含量测定用对照品用作UV法或容量法,定量用对照品用作定性等,则可直接应用,不必重新标定。 2.申报临床研究时,如中检所尚无供应,为不影响注册进度,可先期与中检所接洽制备和标定,申报时提供标定报告、标签(应标明效价或含量、批号、使用效期)和使用说明书;也可与省所合作标定,申报时提供标准品或对照品研究资料,“说明其来源、理化常数、纯度、含量及其测定方法和数据”;标定有困难时,可使用国外药品管理当局或药典委员会发放的对照品(标准品)或国外制药企业的工作对照品(标准品),进行标准制订和其他基础性研究,但应提供其标签(应标明其含量)和使用说明书,能保证其量值溯源性;也可使用国外试剂公司(如sigma公司等)提供的对照品(标准品),但应提供试剂公司该批对照品(标准品)的检测报告(用作含量测定时,应有确定的含量数据),如为高纯度试剂,提供了国外试剂公司检测报告(用作含量测定时,应有确定的含量数据)时,也可使用,并应能保证其量值溯源性,但申请人应及时与中检所接洽对照品(标准品)的标定事宜,临床研究期间完成此工作。 3.直接申报生产品种,如中检所尚无供应,可参照2中要求进行,并提供相应研究资料,但申请人在标准试行期间应与中检所接洽并完成的标定事宜。 4.对照品(标准品)标定的技术要求: 4.1.创新药物 应说明对照品(标准品)原料的制备路线、精制方法、质检报告,提供理化常数和纯度的测定数据及分析结果(包括相关图谱),提供标定方法的研究和验证资料(如与原料药质量研究项下相同,可不再提供)、含量测定数据及经统计分析得到的对照品(标准品)含量结果,并说明进行临床前药学研究、药理毒理学研究所用样品的含量是否用该批对照品(标准品)确定或可用该批对照品(标准品)进行量值溯源。 ●纯度测定方法应选用色谱法,并采用两种以上不同分离机理或不同色谱条件并经验证的色谱方法相互验证比较,同时采用二极管阵列检测器或其它适宜方法检测HPLC法的色谱峰纯度,而后根据测定结果经统计分析确定对照品(标准品)原料的纯度。 ●对于组份单一、纯度较高的药物,对照品(标准品)标定方法宜首选可进行等当量换算、精密度高、操作简便快速的容量法。可根据药物分子中所具有的官能团及其化学性质,选用不同的容量分析方法,但应符合如下条件:(1)反应按一个方向进行完全;(2)反应迅速,必要时可通过加热或加入催化剂等方法提高反应速度;(3)共存物不得干扰主药反应,或能用适当方法消除;(4)确定等当点的方法要简单、灵敏;(5)标化滴定液所用基准物质易得,并符合纯度高、组成恒定且与化学式符合、性质稳定(标定时不发生副反应)等要求。 标定方法的选择要关注如下事项:(1)供试品的取用量应满足滴定精度的要求(消耗滴定液约20ml);(2)滴定终点的判断要明确,提供滴定曲线。如选用指示剂法,应考虑其变色敏锐,并用电位法校准其终点颜色。(3)为排除因加入其它试剂而混入杂质对测定结果的影响,或便于剩余滴定法的计算,可采用“将滴定的结果用空白试验校正”的办法;(4)要给出滴定度(采用四位有效数字)的推导过程。 标定结果要根据3个以上实验室各不少于15组测定结果经统计分析,去除离群值和可疑值后的结果,并报告可信限。 ●如该药物没有可进行等当量换算并符合要求的容量法时,可采用反复纯化的原料,色谱法确定纯度后扣除有关物质、炽灼残渣、水分和挥发溶剂等后的理论含量确定为标准品含量,以此为基准进行对照品(标准品)的换代和量值传递。 ●用于抗生素微生物检定法的第一代基准标准品可参照上述方法标定,如为多组份抗生素,其组份比例应与拟上市产品组份比例一致或接近,或以其中某一组份纯品为基准标准品,但要注意标准品换代时量值传递的恒定。 ●仅用于鉴别定性的化学对照品,注重其结构确证的研究资料,纯度和含量的要求一般可适当降低。 ●杂质对照品,用作限度要求时,应提供其来源(合成路线)、结构确证的研究资料,应具备较高的纯度和含量,并提供纯度和含量的的测定结果,提供质量控制标准。 4.2其他类别药物,可参照4.1要求进行。 ●用于抗生素微生物检定法的标准品须用上市国的国家标准品或原发厂的工作标准品为基准标准品进行标定。标定时采用的原料药应符合相应要求,并提供原料的制备路线、精制方法、质检报告,提供理化常数和纯度的测定数据及分析结果(包括相关图谱)。标定须用现行版中国药典附录收载的“抗生素微生物检定法”-三剂量法,并提供详细的方法学研究,包括检定菌和培养基的选择、剂量和剂距选择、缓冲液选择(如与质量研究项下相同,可不再提供)。每次标定结果均应照“生物检定统计法-量反应平行线测定法(3.3)”法进行可靠性测验及效价计算。按照《药品注册管理办法》,上市药品质量标准所用标准物质均须由中检所负责标定和管理,药品研发过程中,研制单位应注意及时与中检所联系标定事宜,以保证研发工作的连续性。[/size]
近日在做一个日本上市缓释制剂的仿制,对其释放度检查标准有些疑问,特别是其供试品的吸收度计算方法很特别,希望园里的老师给分析指点一下,谢谢!释放度的测定取本品,照释放度测定法,采用溶出度测定法第二装置,以Ph1.2盐酸溶液500ml为溶剂,转速为每分钟100转,依法操作,经1小时时,取溶液10ml,过滤,作为供试品溶液(1);弃去上述各容器中的酸液,加已预热至37±0.5℃的Ph7.5磷酸盐缓冲液500ml,继续运转至2小时时,取溶液10ml,过滤,作为供试品溶液(2);并补加同体积的Ph7.5磷酸盐缓冲液,继续运转至5小时时,取溶液10ml,过滤,作为供试品溶液(3);另取对照品约0.1g,精密称定,置50ml量瓶中,加甲醇适量使溶解,并稀释至刻度,摇匀;精密量取此溶液各1ml,置100ml量瓶中,分别加Ph1.2的盐酸溶液和Ph7.5磷酸盐缓冲液稀释至此刻度,摇匀,作为对照品溶液(1)和对照品溶液(2)。照分光光度法,供试品溶液(1)在360nm和450nm波长处测定吸收度,计算吸收度差值;其他各对照品溶液及供试品溶液均在360nm波长处测定吸收度,分别计算不同时间的释放量。
[size=3][color=#ff6600][url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法检薄荷桉油含片中薄荷脑的含量,仪器条件和操作方法如下[/color]:[/size][size=3][b][font=宋体]色谱条件与系统适用性试验[/font][/b][font=宋体] 采用弹性石英毛细管柱(30m×0.32mm×0.25[/font][/size][font=宋体][size=3]um )(PEG)聚乙二醇为固定液,进样口温度220℃,检测器温度为250℃。分流进样。[/size][/font][font=宋体][size=3]程序升温,初始90℃,保持1分钟,每分钟5℃升至170℃。理论塔板数按薄荷脑峰计[/size][/font][font=宋体][size=3]算应不低于10000。薄荷脑与内标物质峰的分离度应大于4。[/size][/font][size=3][b][font=宋体]校正因子测定[/font][/b][font=宋体] [/font][font=宋体]取水杨酸甲酯适量,加丙酮稀释成每1ml含1.0mg的溶液,摇匀,作为内标溶液。另取薄荷脑对照品适量,加丙酮稀释成每1ml含1.0mg的溶液。精密取内标溶液与对照品溶液各5ml,置25ml量瓶中,加丙酮至刻度,摇匀,精密吸取1μl注入[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url],计算效正因子。[/font][/size][size=3][b][font=宋体]测定法[/font][/b][font=宋体] [/font][font=宋体]取本品20片,精密称定,研细,取粉末适量(约10片量),精密称定,置具塞瓶中,精密加入丙酮25ml,振摇30分钟,滤过,精密量取续滤液10ml与内标溶液5ml,置25ml量瓶中,加丙酮至刻度,摇匀,精密吸取1μl注入[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url],测定,计算,即得。我按上述方法操作,用的机子是岛津GC-14C,柱子是0.53×30的PEG-20M,各气体流量也正常,但在做时发现只有水杨酸甲酯的内标峰出来,保留时间大约在7分钟的样子,而进薄荷脑对照品怎么没有薄荷脑的峰呢?进样品同样没有薄荷脑的峰,只有内标峰,请大家帮帮忙分析一下原因出在哪里?[/font][/size]
液相色谱中怎样设置梯度洗脱?我分析的是双氧水中2-乙基蒽醌和四氢中2-乙基蒽醌的含量,用的溶剂是水和甲醇。
[size=3]不知大家注意没有,在2010年版药典中,特别是UV-Vis测含量,在“对照品溶液的制备”中,往往是准确指出精密称取的对照品的量,例如,2010年版药典一部第5页,人工牛黄中胆酸的含量测定项下,胆酸对照品溶液的制备:取胆酸对照品12.5mg,精密称定,置25ml量瓶中,加60%冰醋酸溶液使溶解,并稀释至刻度,摇匀,即得(每1ml中含胆酸0.5mg)。而,HPLC或GC等测含量,大多的表述是,如同是第5页,八角茴香中反式茴香脑的含量测定,对照品溶液的制备:取反式茴香脑对照品适量,精密称定,加乙醇制成每1ml含0.4mg的溶液,即得。这两种表述有何不同?[/size]
请教各位:在乙醇的气相色谱检验中,对照品溶液制备用到的试剂:甲醇、乙醛、乙缩醛、苯、4-甲基-2-戊醇。这些试剂必须用国家标准品吗?还是能用色谱纯的试剂代替,如果能代替使用,需不需要做相关对比试验,又该怎么进行这些对比试验?谢谢各位大神解答。。。。
【求助】中检所胆固醇对照品要检测胆固醇的含量,但是中检所的胆固醇对照品是用作鉴别的,应该怎么解决这个问题?这样的对照品还能用于含量测定吗?请高手指点,谢谢!
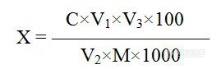
[color=black][b]藤青泡腾片提取工艺研究[/b][/color]藤青泡腾片是以闽产药食资源为基础制成的复方制剂,处方由藤茶、青果、葛花、甘草[font=times new roman]4[/font]味药材组成,具有调节血脂,保护化学性肝损伤的作用。传统中药煎煮繁琐,携带不便,气味较苦,将其制成泡腾片,携带、服用方便,崩解速度快,提高其生物利用度、临床疗效。本处方中各味药的主要有效成份为黄酮,水溶性较好,且二氢杨梅素等在热水中的溶解度大,因此采用水为提取溶液进行加热提取,成本低、实验条件简单。采用正交试验的方法考察各因素对总黄酮、浸膏得率的影响,获得最佳提取工艺。1.1[font=宋体][b]仪器与试药[/b][/font](1)实验仪器[font=times new roman] [/font][table][tr][td]电子分析天平[font=times new roman]XS105[/font][/td][td]METTLER TOLEDO[/td][/tr][tr][td]电子调温电热套[font=times new roman]98-1-B[/font]型[/td][td]天津市泰斯特仪器有限公司[/td][/tr][tr][td]电热恒温水浴锅[font=times new roman]HWS24[/font][/td][td]上海一恒科学仪器有限公司[/td][/tr][tr][td]常压恒温干燥箱[font=times new roman]XMTD-822[/font][/td][td]上海精宏实验设备有限公司[/td][/tr][tr][td]紫外分光光度计[font=times new roman]UV9100[/font][/td][td]北京瑞利分析仪器公司[/td][/tr][tr][td][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url][/color][/url]([font=times new roman]200 μL[/font]、[font=times new roman]1000 μL[/font])[/td][td]GILSON[/td][/tr][/table](2)实验试药葛花[font=times new roman] [/font]产地:安徽[font=times new roman] [/font]北京三和药业有限公司[font=times new roman] [/font]藤茶(产地:广西)、青果(产地:广东)、甘草(产地:甘肃)[table][tr][td]芦丁对照品[/td][td]批号:[font=times new roman]100080-20708[/font]中国[font=宋体]食品[/font]药品[font=宋体]检[/font]定[font=宋体]研究院[/font][/td][/tr][tr][td]甲醇[font=times new roman] (AR)[/font][/td][td]国药集团化学试剂有限公司[/td][/tr][tr][td]亚硝酸钠[font=times new roman](AR)[/font][/td][td]上海联试化工试剂有限公司[/td][/tr][tr][td]硝酸铝[font=times new roman](AR)[/font][/td][td]上海展云化工有限公司[/td][/tr][tr][td]氢氧化钠[font=times new roman](AR)[/font][/td][td]上海联试化工试剂有限公司[/td][/tr][/table] [font=times new roman][size=13px]1.2 [/size][/font][size=13px]泡腾片提取工艺条件的研究[/size]1.2.1[font=宋体][b]正交试验筛选[/b][/font]称取藤茶、葛花、青果、甘草各[font=times new roman]0.5[/font]倍处方量为[font=times new roman]1[/font]份,共[font=times new roman]9[/font]份,以加水量([font=times new roman]A[/font]),提取时间([font=times new roman]B[/font]),提取次数([font=times new roman]C[/font])为考察因素,按表[font=times new roman]1[/font]的因素水平进行[font=times new roman]L9[/font][font=times new roman][size=21px]([/size][/font][font=times new roman]3[/font][font=times new roman]4[/font][font=times new roman][size=21px])[/size][/font]正交试验,根据总黄酮含量、浸膏得率进行评价,考察最佳提取工艺条件。1.2.1.1[font=宋体][b]水提取液浸膏得率的测定[/b][/font]吸取1.2.1项下提取的每份药液[font=times new roman]15 ml[/font],转移到干燥蒸发皿内,置于水浴锅内蒸发水份至流浸膏后,放入烘箱于[font=times new roman]100[/font]℃烘干到恒重,称重,记录结果并计算,结果见表[font=times new roman]2[/font]1.2.1.2[font=宋体][b]水提取液总黄酮的含量测定[/b][/font]对照品溶液的制备:称芦丁对照品适量,精密称定,加甲醇溶解并定量稀释至每1 ml含[font=times new roman]0.2 mg[/font]的芦丁溶液,制得对照品溶液。供试品溶液的制备:取上述[font=times new roman]9[/font]份提取物各[font=times new roman]1[/font] [font=times new roman]ml[/font],于[font=times new roman]50[/font] [font=times new roman]ml[/font]容量瓶中,并用水稀释至刻度。芦丁对照品标准曲线制备:精密吸取芦丁对照品溶液[font=times new roman]0.0[/font],[font=times new roman]1.0[/font],[font=times new roman]2.0[/font],[font=times new roman]3.0[/font],[font=times new roman]4.0[/font],[font=times new roman]5.0[/font],[font=times new roman]6.0[/font] [font=times new roman]ml[/font],分别置[font=times new roman]25 ml[/font]([font=times new roman]V[/font][font=times new roman]3[/font])量瓶中,加水至[font=times new roman]6 ml[/font],加入1 ml的[font=times new roman]5%[/font] NaNO2,混匀,放置[font=times new roman]6min[/font],往容量瓶里加入1 ml的[font=times new roman]10%A[/font]l[font=times new roman](NO[/font][font=times new roman]3[/font][font=times new roman])[/font][font=times new roman]3[/font],混匀后静置[font=times new roman]6min[/font],加入[font=times new roman]10[/font] ml NaOH试液,混匀,加蒸馏水至刻度,混匀,静置[font=times new roman]15[/font]分钟,以[font=times new roman]0.0 ml[/font]对照品溶液制备的溶剂为空白对照,在[font=times new roman]510nm[/font]波长下测定各组的吸光度值。以吸光度为纵坐标[font=times new roman]([/font][font=times new roman][i]A[/i][/font][font=times new roman])[/font],浓度为横坐标([font=times new roman]mg/ml[/font]),绘制标准曲线,结果见图[font=times new roman]1[/font]。样品测定:吸取待测溶液[font=times new roman]10 ml[/font]([font=times new roman]V[/font][font=times new roman]2[/font])于[font=times new roman]25 ml[/font]容量瓶中,照芦丁对照品标准曲线制备自“加入[font=times new roman]1 ml[/font]的[font=times new roman]5%[/font] NaNO2”起,在波长[font=times new roman]510nm[/font]下测定样品的吸光度,([font=times new roman][i]X[/i][/font])。根据标准曲线求出样品中总黄酮的含量[img]https://ng1.17img.cn/bbsfiles/images/2020/09/202009212136303003_5694_2166779_3.png[/img][color=black]结果计算:[/color][color=black] [/color][color=black] [/color][color=black]X—[/color][font=宋体][color=black]试样中总黄酮百分含量,以芦丁[/color][/font][color=black](C[/color][color=black]27[/color][color=black]H[/color][color=black]30[/color][color=black]O[/color][color=black]16[/color][color=black])[/color][font=宋体][color=black]计, [/color][/font][color=black]g/100g[/color][font=宋体][color=black]([/color][/font][color=black]ml[/color][font=宋体][color=black]);[/color][/font][color=black]C—[/color][font=宋体][color=black]标准曲线上读出供试品溶液中总黄酮的浓度,[/color][/font][color=black]mg/ml[/color][font=宋体][color=black];[/color][/font][color=black]V[/color][color=black]1[/color][color=black]—[/color][font=宋体][color=black]试样定容体积,[/color][/font][color=black]ml[/color][font=宋体][color=black];[/color][/font][color=black]V[/color][color=black]2[/color][color=black]—[/color][font=宋体][color=black]吸取供试液体积,[/color][/font][color=black]ml[/color][font=宋体][color=black];[/color][/font][color=black]V[/color][color=black]3[/color][color=black]—[/color][font=宋体][color=black]显色定容体积,[/color][/font][color=black]ml[/color][font=宋体][color=black];[/color][/font][color=black]M—[/color][font=宋体][color=black]试样取样量,[/color][/font][color=black]g(ml)[/color][font=宋体][color=black]。[/color][/font][color=black]结果见表[/color][font=times new roman][color=black]2[/color][/font][color=black],表[/color][font=times new roman][color=black]3. [/color][/font][font=times new roman][color=red] [/color][/font][align=center]表[font=times new roman]1 [/font]提取正交试验因素水平表[/align][table][tr][td=1,2][align=center]水平[/align][/td][td=3,1][align=center]因素[/align][/td][/tr][tr][td][align=center]A[font=宋体]加水量[/font]([font=宋体]倍[/font])[/align][/td][td][align=center]B[font=宋体]提取时间[/font](h)[/align][/td][td][align=center]C[font=宋体]提取次数[/font][/align][/td][/tr][tr][td][align=center]1[/align][/td][td][align=center]10[/align][/td][td][align=center]0.5[/align][/td][td][align=center]1[/align][/td][/tr][tr][td][align=center]2[/align][/td][td][align=center]15[/align][/td][td][align=center]1.0[/align][/td][td][align=center]2[/align][/td][/tr][tr][td][align=center]3[/align][/td][td][align=center]20[/align][/td][td][align=center]1.5[/align][/td][td][align=center]3[/align][/td][/tr][/table]注:以[font=times new roman]D[/font]因素为误差项[color=black]图[/color][font=times new roman][color=black]1[/color][/font][color=black]芦丁标准品标准曲线 [/color][align=center][img]https://ng1.17img.cn/bbsfiles/images/2020/09/202009212136306476_9524_2166779_3.png[/img][size=16px] [/size][/align]采用加权平均法对浸膏得率、总黄酮含量进行综合评估,由于含量对泡腾片疗效的影响较大,因此,分别给予浸膏得率、总黄酮含量[font=times new roman]40%[/font]、[font=times new roman]60%[/font]的权重进行分配。浸膏的率越高,患者最终单次的给药量越多,较低较好,以最低得率[font=times new roman]19.808%[/font]为最高得分,而总黄酮为主要有效成份,宜越高越好,故以[font=times new roman]1.969[/font]为最高得分。以序号[font=times new roman]1[/font]为例计算综合评分:[font=times new roman](19.808/19.808)*0.4+(0.796/1.969)*0.6=0.643[/font],同理,可求得其余各综合评分,结果见表[font=times new roman]2.[/font] 表[font=times new roman]2[/font]提取正交试验结果([font=times new roman][i]n[/i][/font][font=times new roman]=9[/font])[table][tr][td][align=center]序号[/align][/td][td][align=center]A[/align][/td][td][align=center]B[/align][/td][td][align=center]C[/align][/td][td][align=center]D[/align][/td][td][align=center]浸膏得率[font=times new roman](%)[/font][/align][/td][td][align=center]总黄酮含量[font=times new roman](g)[/font][/align][/td][td][align=center]综合评分[/align][/td][/tr][tr][td][align=center]1[/align][/td][td][align=center]1[/align][/td][td][align=center]1[/align][/td][td][align=center]1[/align][/td][td][align=center]1[/align][/td][td][align=center]19.808 [/align][/td][td][align=center]0.796 [/align][/td][td][align=center]0.643 [/align][/td][/tr][tr][td][align=center]2[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]2[/align][/td][td][align=center]2[/align][/td][td][align=center]29.159 [/align][/td][td][align=center]1.109 [/align][/td][td][align=center]0.610 [/align][/td][/tr][tr][td][align=center]3[/align][/td][td][align=center]1[/align][/td][td][align=center]3[/align][/td][td][align=center]3[/align][/td][td][align=center]3[/align][/td][td][align=center]34.835 [/align][/td][td][align=center]1.499 [/align][/td][td][align=center]0.684 [/align][/td][/tr][tr][td][align=center]4[/align][/td][td][align=center]2[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]33.656 [/align][/td][td][align=center]1.490 [/align][/td][td][align=center]0.689 [/align][/td][/tr][tr][td][align=center]5[/align][/td][td][align=center]2[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]1[/align][/td][td][align=center]37.467 [/align][/td][td][align=center]1.854 [/align][/td][td][align=center]0.776 [/align][/td][/tr][tr][td][align=center]6[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]23.851 [/align][/td][td][align=center]0.978 [/align][/td][td][align=center]0.630 [/align][/td][/tr][tr][td][align=center]7[/align][/td][td][align=center]3[/align][/td][td][align=center]1[/align][/td][td][align=center]3[/align][/td][td][align=center]2[/align][/td][td][align=center]40.161 [/align][/td][td][align=center]1.969 [/align][/td][td][align=center]0.797 [/align][/td][/tr][tr][td][align=center]8[/align][/td][td][align=center]3[/align][/td][td][align=center]2[/align][/td][td][align=center]1[/align][/td][td][align=center]3[/align][/td][td][align=center]26.402 [/align][/td][td][align=center]1.099 [/align][/td][td][align=center]0.635 [/align][/td][/tr][tr][td][align=center]9[/align][/td][td][align=center]3[/align][/td][td][align=center]3[/align][/td][td][align=center]2[/align][/td][td][align=center]1[/align][/td][td][align=center]34.196 [/align][/td][td][align=center]1.544 [/align][/td][td][align=center]0.702 [/align][/td][/tr][tr][td][align=center]K1[/align][/td][td][align=center]1.94 [/align][/td][td][align=center]2.13 [/align][/td][td][align=center]1.91 [/align][/td][td][align=center]2.12 [/align][/td][td] [/td][td] [/td][td] [/td][/tr][tr][td][align=center]K2 [/align][/td][td][align=center]2.10 [/align][/td][td][align=center]2.02 [/align][/td][td][align=center]2.00 [/align][/td][td][align=center]2.04 [/align][/td][td] [/td][td] [/td][td] [/td][/tr][tr][td][align=center]K3[/align][/td][td][align=center]2.13 [/align][/td][td][align=center]2.02 [/align][/td][td][align=center]2.26 [/align][/td][td][align=center]2.01 [/align][/td][td] [/td][td] [/td][td] [/td][/tr][tr][td][align=center]R[/align][/td][td][align=center]0.07 [/align][/td][td][align=center]0.04 [/align][/td][td][align=center]0.12 [/align][/td][td][align=center]0.04 [/align][/td][td][align=center] [/align][/td][td][align=center] [/align][/td][td][align=center] [/align][/td][/tr][/table][align=center]表[font=times new roman]3[/font]提取正交试验方差分析[/align][table][tr][td][align=center]方差来源[/align][/td][td][align=center]离差平方和[/align][/td][td][align=center]自由度[/align][/td][td][align=center]F[font=宋体]值[/font][/align][/td][td][align=center]均方[/align][/td][td][align=center]显著性[/align][/td][/tr][tr][td][align=center]加水量[/align][/td][td][align=center]0.007349[/align][/td][td][align=center]2[/align][/td][td][align=center]3.2139[/align][/td][td][align=center]0.003675[/align][/td][td] [/td][/tr][tr][td][align=center]提取时间[/align][/td][td][align=center]0.002731[/align][/td][td][align=center]2[/align][/td][td][align=center]1.1945[/align][/td][td][align=center]0.001366[/align][/td][td] [/td][/tr][tr][td][align=center]提取次数[/align][/td][td][align=center]0.02189[/align][/td][td][align=center]2[/align][/td][td][align=center]9.5733[/align][/td][td][align=center]0.01095[/align][/td][td][align=center]**[/align][/td][/tr][tr][td][align=center]误差[/align][/td][td][align=center]0.002287[/align][/td][td][align=center]2[/align][/td][td][align=center]1.0000 [/align][/td][td][align=center]0.001143[/align][/td][td] [/td][/tr][/table]由表[font=times new roman]3[/font]可知,根据水提取液中总黄酮含量与浸膏得率进行评估,各因素对结果的影响大小:提取次数[font=times new roman][/font]加水量[font=times new roman][/font]提取时间,即主要影响因素是提取次数,其次是加水量,提取时间影响最小。以实验结果为参考,结合实际生产情况,最终确定提取工艺为:加水[font=times new roman]20[/font]倍量,每次提取[font=times new roman]0.5h[/font],提取[font=times new roman]3[/font]次。1.2.2[font=宋体][b]提取正交验证实验[/b][/font]根据以上所选最佳提取工艺条件,加水[font=times new roman]20[/font]倍量,每次提取[font=times new roman]0.5h[/font],提取[font=times new roman]3[/font]次,平行[font=times new roman]3[/font]份,对水提取液的浸膏得率与总黄酮含量进行测定,按[font=times new roman]1.2.1.2[/font]项下的方法计算综合评分后,求平均得分,结果见表[font=times new roman]4.[/font][align=center]表[font=times new roman]4[/font]提取正交实验验证结果([font=times new roman][i]n[/i][/font][font=times new roman]=3[/font])[/align][table][tr][td][align=center]编号[/align][/td][td][align=center]浸膏得率(%)[/align][/td][td][align=center]总黄酮含量(g)[/align][/td][td][align=center]综合评分[/align][/td][td][align=center]平均得分[/align][/td][/tr][tr][td][align=center]1[/align][/td][td][align=center]37.3[/align][/td][td][align=center]2.036[/align][/td][td][align=center]0.833[/align][/td][td=1,3][align=center]0.830[/align][/td][/tr][tr][td][align=center]2[/align][/td][td][align=center]38.1[/align][/td][td][align=center]2.038[/align][/td][td][align=center]0.829[/align][/td][/tr][tr][td][align=center]3[/align][/td][td][align=center]37.4[/align][/td][td][align=center]2.021[/align][/td][td][align=center]0.828[/align][/td][/tr][/table]由表[font=times new roman]4[/font]可知,[font=times new roman]3[/font]份平行实验最终的平均得分为[font=times new roman]0.830[/font],接近于正交设计中的[font=times new roman]A3B1C3[/font]综合评分,且评分最高,有良好的重复性和较高的准确率,所筛选的提取工艺条件基本稳定,可作为藤青泡腾片的提取方法。小结与讨论在提取工艺的探讨过程中,用正交试验的方法研究加水量、提取时间、提取次数对药液浸膏得率和总黄酮含量的影响,获得最适提取条件为:[font=times new roman]20[/font]倍量水,提取[font=times new roman]3[/font]次,每次提取[font=times new roman]0.5h[/font]。试验中发现,青果为橄榄的干燥果实,本处方中用量较少,为方便称取,同时提高没食子酸等有效成份的提取率,宜先将其进行粉碎;藤茶、葛花密度小,提取过程中浮于水面,应将其充分润湿,使其浸没于水中,以免影响各成份的提取率;若直接加热煎煮,提取过程中水分蒸发严重,实验结果重现性差,宜采用冷凝回流的方法进行提取。