
遗传毒性杂质,现在是药学研究的焦点之一。甲磺酸、苯甲磺酸等磺酸盐类物质与微量的低级醇在合成反应中生成烷基磺酸酯类,这些物质可与DNA发生烷基化反应,从而可能成为引发癌症的诱因。欧洲医药评价署、美国食品和药品管理局及国际药品注册协调会议等先后对基因毒性杂质做出限度规定。具体到我们的甲磺酸加贝酯产品,需要对其中的甲磺酸乙酯的限度进行控制。溶液制备:对照品溶液 取甲磺酸乙酯适量,精密称定,用乙腈制成每毫升含1.5μg/ml的溶液,精密移取2ml加入顶空瓶中,加入3ml水,6g碘化钠后,扎盖密封。供试品溶液 取甲磺酸加贝酯适量,精密称定,按供试品100mg与乙腈1ml的比例配制供试品溶液,溶液经超声、波膜过滤处理后,精密移取2ml加入顶空瓶中,加入3ml水,3g碘化钠后,扎盖密封。色谱条件:Agilent 7890色谱仪,顶空进样器,FID检测器;色谱柱,月旭WEL-PEG20M,30m*0.32mm*0.25μm(Cat. NO:01918-32001;Ser. NO:GC20131102);进样口温度为110℃,检测器温度为260℃,氢气流速为30ml/min,空气流速为350ml/min,进样量为1mL,分流比为0.1:1。升温程序,起始温度为40℃,维持10min,然后以20℃/min的升温速率,升温至160℃,维持1min。顶空瓶平衡温度为80℃,平衡时间为30min。结果:对照液色谱图: http://ng1.17img.cn/bbsfiles/images/2014/07/201407021418_503868_1609327_3.jpg其中,时间为1.982min的保留峰为甲磺酸乙酯的衍生物。供试液色谱图:http://ng1.17img.cn/bbsfiles/images/2014/07/201407021538_503896_1609327_3.jpg由色谱图中可以看出,样品中未检出甲磺酸乙酯。讨论:出峰时间非常的快,但是理论塔板数、分离度、对称因子等却非常给力!既得到了良好的分离效果,又尽可能的节约了分析时间。
有没有EDTA络合滴定三氟甲磺酸钪的方法
一下子买不到色谱纯或分析纯的甲磺酸,于是就用了化学纯的甲磺酸,只是背景稍高于以前,分离效果目前也没有什么问题,不知道以后会不会有影响。
在检测甲磺酸酯类物质时,根据欧洲药典方法,选用碘化钠和硫代硫酸钠作为衍生试剂,其中对照溶液的配置方法是称取一定量甲磺酸酯类到5ml容量瓶中,加甲苯稀释定容摇匀,请问甲苯的作用是什么呢

XB-C18之完美收官摘要:对在适宜条件下保存的注射用甲磺酸罗哌卡因进行有关物质检查,用以得到该工艺条件、该存储条件对产品质量的影响,为药品的质量分析提供研究数据。结果表明,该工艺条件下值得的注射液,在改存储条件下保存满足药品的质量要求,该存储条件可以得到质量稳定的产品。关键词:高效液相色谱法、有关物质、检查前言:注射用甲磺酸罗哌卡因注射液,适应症为外科手术麻醉:硬膜外麻醉(包括剖腹产术硬膜外麻醉);局部浸润麻醉。急性疼痛控制:用于术后或分娩镇痛,可采用持续硬膜外输注,也可间歇性用药,局部浸润麻醉。一般的参考用量见下表:http://ng1.17img.cn/bbsfiles/images/2014/12/201412291415_529840_1609327_3.jpg药物的质量评价,一般由鉴别、检查、含量测定几部分组成。其中,有关物质的检查,是现在申报药物资料中的重中之重。本实验就是取批号为JR20121201的注射用甲磺酸罗哌卡因注射液进行有关物质的检查(稳定性长期24月检查)。1.实验部分2.设备和试剂高效液相色谱仪,Agilent1260;VWD检测器。色谱乙腈、色谱异丙醇、磷酸氢二钠、磷酸二氢钠。1.2色谱条件检测波长:240nm;进样量:10μL;流动相:乙腈-磷酸盐缓冲液(pH8.0)(60:40)为流动相;色谱柱:月旭,Ultimate®,XB-C18,4.6*250mm,5μm(Part. No:00201-31043,Seri. No:211303968)。1.3 溶液配制供试液配制:精密量取本品2ml,用异丙醇溶解并定容至10ml。对照液配制:精密量取供试液100μL,用异丙醇稀释并定容至10ml。3.结果与讨论3.1典型色谱图 对照液色谱图:http://ng1.17img.cn/bbsfiles/images/2014/12/201412291414_529837_1609327_3.jpg供试液色谱图:http://ng1.17img.cn/bbsfiles/images/2014/12/201412291415_529838_1609327_3.jpg3.2结果 标准规定,理论塔板数按甲磺酸罗哌卡因峰计算不低于2000,甲磺酸罗哌卡因峰与相邻杂质峰的分离度应符合要求。色谱图的记录时间应至主成分峰保留时间的2倍,供试品溶液的色谱图中如有杂质,量取各杂质的峰的面积之和,不得大于对照溶液主成分峰的面积(1.0%)。而本实验中有关物质的含量见下表:http://ng1.17img.cn/bbsfiles/images/2014/12/201412291415_529839_1609327_3.jpg3.3讨论①. 标准要求理论塔板数以甲磺酸罗哌卡因峰计算不低于2000,而色谱图中任何一个甲磺酸罗哌卡因峰的塔板数都在两万多,是标准的10倍以上,意义自不必说了。②. 从色谱图中的峰型及分离度来看,似乎也不用多说了。③. 从保留时间的差异来看,需要多说吗?
现在我们要用气相检测甲磺酸中的甲磺酸甲酯和甲磺酸乙酯,不知道甲磺酸能不能直接进样? 对柱子和仪器有什么要求不?感谢
2.9 样品中有关物质测定精密量取甲磺酸罗哌卡因注射液1 mL,置20 mL量瓶中,加流动相稀释至刻度,摇匀,作为供试品溶液。精密量取1 mL,置100 mL量瓶中,加流动相稀释至刻度,作为对照溶液。取对照溶液20u L注入液相色谱仪,调节检测灵敏度,使主成分色谱峰的峰高约为[color=#ff7a4e]满量程[/color]的10% ;再精密量取上述两种溶液各20u L 分别进样,记录色谱图至主成分峰保留时间的3倍,供试品溶液的色谱图中如显杂质峰,各杂质峰面积之和不得大于对照溶液主成分峰的峰面积,即规定甲磺酸罗哌卡因注射液样品中的有关物质应不超过1.0%。以上是我从一篇文献里摘出来的关于有关物质测定的步骤。有几点不明白之处,想向朋友们请教一下,这个供试品溶液浓度和对照溶液浓度之间是怎么一个关系?上面说的“[color=#ff9d7d]满量程[/color]”是什么意思啊?
急需甲磺酸丁酯,哪位大虾可以指点从哪里可以购买到,急急!
请问谁有甲磺酸的检测方法,最好是简单的点的,易操作的
求助三氟甲磺酸酐气相测试方法我们用HP-5测试 不知道测试出来的是不是主峰,并且杂质较多,求助测试方法?是否可以做硅化测试?

[align=center][b]甲磺酸伊马替尼片的中试质量研究[/b][/align][align=center]王淑华,臧恒昌[/align](山东大学药学院)[b]摘要:[/b]甲磺酸伊马替尼片是一种小分子靶向抑制剂,用于治疗费城染色体阳性的慢性髓性白血病的慢性期、加速期或急变期和不能切除和/或发生转移的恶性胃肠道间质瘤的成人患者。甲磺酸伊马替尼由瑞士诺华公司2001年在美国首研上市,作为肿瘤的首个靶向治疗药物面世开创了肿瘤分子靶向治疗的新时代,目前已经在全球90多个国家获得批准,美国、欧盟和其它国家还批准甲磺酸伊马替尼片用于胃肠基质瘤患者的治疗。2005年进口到中国,中文商品名是格列卫。本文按照现行药品注册法规的要求对甲磺酸伊马替尼片的制备工艺进行研究,在小试工艺处方的基础上进行中试放大,对粉碎、混合、制粒、总混、压片、包衣的工艺参数进行研究确定,并确定中试设备,用中试产品与格列卫进行全面的质量对比试验,并进行影响因素试验考察10天的研究。开发出与原研药具有相同质量的甲磺酸伊马替尼片,实现甲磺酸伊马替尼片的可工业化生产。[b]关键词:[/b]甲磺酸伊马替尼片;开发;制备工艺;[b]1 实验材料和仪器[/b]1.1实验材料[align=center][img=,572,220]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251640111718_2529_3389662_3.png!w572x220.jpg[/img][/align]1.2实验仪器[align=center][img=,573,287]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251642146696_8860_3389662_3.png!w573x287.jpg[/img][/align][b]2方法与结果 [/b] 研究内容包括中试放大3批,批量为5000片,筛选各项工艺参数、进行影响因素考察、与原研药进行全面的质量对比,最终确定了中试规模的处方、工艺、工艺参数、设备及场所。[b]2.1 中试3批样品的制备[/b]为了充分验证处方及制备工艺的可行性,优化各项工艺参数,中试制备了三批甲磺酸伊马替尼片(批号20111205、20111228、20120104),每批5000片,三批产品处方见表3[align=center][img=,555,295]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251643270416_551_3389662_3.png!w555x295.jpg[/img][/align]制备工艺:取甲磺酸伊马替尼,用万能粉碎机粉碎,筛网目数为100目,粉碎后称取处方量,备用。粉碎过筛后的甲磺酸伊马替尼、微晶纤维素、羟丙甲纤维素、交联聚维酮、二氧化硅和硬脂酸镁分别称取处方量备用;将甲磺酸伊马替尼、微晶纤维素(Ⅰ)、羟丙甲纤维素同置湿法混合制粒机中,混合9min,搅拌转速20Hz,剪切转速30Hz;在HLSG-10型混合制粒机中边搅拌边加入纯化水制软材,搅拌转速15HZ,剪切转速15HZ,时间5min,取出后摇摆制粒机20目筛制粒;湿颗粒置60℃热风循环干燥箱中干燥,至水分为2.5%以下时停止;干燥完的颗粒取出,用摇摆制粒机24目筛整粒;整粒后的颗粒,加入交联聚维酮、微晶纤维素(Ⅱ)和二氧化硅,置SH-20三维混合机中混合,转速为9rpm,时间为20min,然后加入硬脂酸镁,继续混合10min,出料。取样检测中间体含量,计算理论片重;将上述总混粉用ZPW-21B型旋转压片机压片,Ф9mm圆形双凸冲模,控制平均片重为理论片重±3%,硬度50-70N;LDCS型高效包衣机,出风温度:38℃;锅体转速:5-10 rpm;喷液泵转速:5-10 rpm;雾化压力:1100mbar;直喷压力:750mbar;包衣增重2%-4%;用铝塑包装机进行泡罩包装,每板10片。泡罩板外套复合膜袋。[b]2.2 工艺参数的研究2.2.1 原料药的粉碎 [/b]甲磺酸伊马替尼为水中易溶的药物,粉碎的粒度对药物溶出的影响不大,因此,确定使用湿法制粒的常规工艺参数:即万能粉碎机粉碎,筛网为100目,备用。[b]2.2.2 混合[/b]混合采用高效湿法混合制粒机,甲磺酸伊马替尼、微晶纤维素(Ⅰ)、羟丙甲纤维素同置湿法混合制粒机中混合,搅拌转速20Hz,剪切转速30Hz,分别于3min、6min、9min和12min在不同位置取样测定甲磺酸伊马替尼的含量,计算RSD值,结果见表4,中试三批的混合参数见表5。[align=center][img=,583,304]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251644390288_1847_3389662_3.png!w583x304.jpg[/img][/align]结果显示中试样品在6min时,各个位置的含量测定结果已经没有显著差异(RSD<5%),表明这时已经混合均匀,9min和12min时,物料更加均匀(RSD<2%)。为保证工艺操作的可靠性,将中试的混合时间确定为9min。[b]2.2.3 制粒 [/b]20111205批中试样品的制粒过程:在混合制粒机中边搅拌边加入纯化水制软材,搅拌转速15Hz,根据处方筛选的结果,加入的纯化水量应为75ml,制备时先加入50ml,然后开启制粒(剪切),转速15Hz,2min后停机观察,发现软材略干,润湿不够,又加入少许,最终纯化水加入量为65 ml,制粒3min后停机观察,发现软材能够握紧成团,轻压即散,符合要求。出料后,置20目筛摇摆制粒机中制粒,湿颗粒置60℃干燥箱中干燥,至水分为2.5%以下时停止。24目筛摇摆制粒机整粒。20111228,20120104两批样品的制备均按照上述参数执行。最终确定中试的制粒参数为:搅拌转速15HZ,剪切转速15HZ,时间5min。取出后摇摆制粒机20目筛制粒。60℃干燥。水分控制小于2.5%。24目筛整粒。[b]2.2.4 总混 [/b] 由于本品制粒后需要加入较多的粉末,包括交联聚维酮、微晶纤维素、二氧化硅和硬脂酸镁,约占片芯总重的22%,所以保证粉末和颗粒的充分混合就比较关键。结合20111205批中试样品的制备,对总混时间进行了取样验证。将整粒后的颗粒与交联聚维酮、微晶纤维素(Ⅱ)和二氧化硅同置三维混合机中混合20min,转速为9rpm,然后加入硬脂酸镁,继续混合10min。分别于15min、20min、25min和30min在混合机中物料的不同部位取样6份,测定其中甲磺酸伊马替尼的含量,计算RSD值,结果见表6,三批中试批混合参数见表7。[align=center][img=,613,321]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251656004349_7538_3389662_3.png!w613x321.jpg[/img][/align]最终确定的中试混合工艺参数为:将整粒后的颗粒与交联聚维酮、微晶纤维素(Ⅱ)、二氧化硅同置三维混合机中混合20min,转速为9rpm,然后加入硬脂酸镁,继续混合10min。[b]2.2.5 中间体含量测定[/b]总混粉取样,测定其中伊马替尼的含量,按100mg/片计算理论片重,见表8。[align=center][img=,574,92]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251656591680_4007_3389662_3.png!w574x92.jpg[/img][/align][b]2.2.6 压片 [/b]参照原研药,采用Ф9mm浅圆冲压片。单独制备了一批3000片用量的总混粉,分别压制不同硬度范围的甲磺酸伊马替尼片各约800片,以确定合适的硬度,结果见表9~11及图1。[align=center][img=,555,545]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251657410320_9022_3389662_3.png!w555x545.jpg[/img][img=,512,293]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251657512292_1250_3389662_3.png!w512x293.jpg[/img][/align]试验结果显示GYYJ01批的溶出5min明显快于格列卫,10min和15min略快于格列卫,其脆碎度为0.5%,且有裂片和断片出现,脆碎度不合格;GYYJ02批溶出曲线与格列卫基本一致,脆碎度合格;GYYJ03批溶出曲线明显慢于格列卫,脆碎度合格。因此,确定压片硬度应控制在50-70N的范围之内。三批中试样品压片参数见表12。[align=center][img=,573,160]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251658297289_6842_3389662_3.png!w573x160.jpg[/img][/align][b]2.2.7 包衣[/b]取GYYJ02批的素片,进行包衣增重的研究。分别于不同时间取出部分片剂,使得它们具有不同的包衣增重。包衣条件为:取包衣粉,用纯化水配制成固含量为13%的液体,搅拌40分钟,备用;出风温度38℃,锅体转速5-10rpm,喷液泵速度5-10rpm,侧喷压力1100mbar,直喷压力750mbar。结果见表13~14及图2[align=center][img=,596,329]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251659214722_6185_3389662_3.png!w596x329.jpg[/img][img=,532,316]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251659216782_8146_3389662_3.png!w532x316.jpg[/img][/align]试验结果显示3种不同的包衣增重对溶出曲线基本无影响,因此,确定包衣增重的范围为2%~4%。中试3批包衣结果见表15[align=center][img=,593,227]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251700491390_8973_3389662_3.png!w593x227.jpg[/img][/align][b]2.2.8 包装 [/b]包衣片用铝塑包装机包装,成形温度118℃,热封温度120℃。2.2.9 中试研究工艺参数汇总[align=center][img=,533,471]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251701345335_8652_3389662_3.png!w533x471.jpg[/img][/align][b]2.3 三批中试产品数据及与原研药的对比研究[/b]结果见表17~18及图3。[align=center][img=,651,279]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251703255806_9275_3389662_3.png!w651x279.jpg[/img][img=,605,691]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251703354406_5321_3389662_3.png!w605x691.jpg[/img][/align][align=center][img=,554,639]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251705217673_2956_3389662_3.png!w554x639.jpg[/img][img=,537,641]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251705282186_7479_3389662_3.png!w537x641.jpg[/img][/align]试验结果显示20111205、 20111228两批自研产品与原研产品格列卫,在0.1M盐酸、pH6.8磷酸盐缓冲液和pH4.5醋酸盐缓冲液和水等4种溶出介质中15分钟溶出度均超过85%,判定为体外溶出行为一致。三批中试产品的各项质量指标与格列卫一致。[b]2.4 影响因素试验[/b]取20111205批中试样品,置强光照射(照度4500Lx)、高温(60℃)、高湿(RH92.5%和RH75%)条件下各放置10天,分别于0、5、10天检测吸湿增重、性状、溶出度、有关物质、含量等各项指标。同时取对照药(格列卫,100mg),置上述条件下,于0天和10天检查相应的项目,作为对比研究。影响因素试验结果表19。[align=center][img=,565,439]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251706500796_5767_3389662_3.png!w565x439.jpg[/img][/align][align=center][/align]试验结果显示自研产品和进口原研产品在高湿RH75%±5%条件下考察10天,吸湿增重均超过5%,提示产品应注意防潮。自研产品和进口原研产品在其它3个条件下各项指标均保持稳定,无显著变化。[b]2.5 中试研究试验结果[/b]2.5.1 处方(按5000片计),见表20[align=center][img=,567,322]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251708221656_8624_3389662_3.png!w567x322.jpg[/img][/align][b]2.5.2 制备工艺 [/b](1)原辅料的处理取甲磺酸伊马替尼,用万能粉碎机粉碎,筛网目数为100目,粉碎后称取处方量,备用。粉碎过筛后的甲磺酸伊马替尼、微晶纤维素、羟丙甲纤维素、交联聚维酮、二氧化硅和硬脂酸镁分别称取处方量备用。(2)混合将甲磺酸伊马替尼、微晶纤维素(Ⅰ)、羟丙甲纤维素同置湿法混合制粒机中,混合9 min,搅拌转速20Hz,剪切转速30Hz。(3)制粒在HLSG-10型混合制粒机中边搅拌边加入纯化水制软材,搅拌转速15HZ,剪切转速15HZ,时间5min,取出后摇摆制粒机20目筛制粒。(4)干燥湿颗粒置60℃热风循环干燥箱中干燥,至水分为2.5%以下时停止。(5)整粒干燥完的颗粒取出,用摇摆制粒机24目筛整粒。(6)总混整粒后的颗粒,加入交联聚维酮、微晶纤维素(Ⅱ)和二氧化硅,置SH-20三维混合机中混合,转速为9rpm,时间为20min,然后加入硬脂酸镁,继续混合10min,出料。取样检测中间体含量,计算理论片重。(7)压片将上述总混粉用ZPW-21B型旋转压片机压片,Ф9mm圆形双凸冲模,控制平均片重为理论片重±3%,硬度50-70N。(8)包衣 LDCS型高效包衣机,出风温度:38℃;锅体转速:5-10 rpm;喷液泵转速:5-10 rpm;雾化压力:1100mbar;直喷压力:750 mbar;包衣增重2%-4%。(9)包装用铝塑包装机进行泡罩包装,每板10片。泡罩板外套复合膜袋。[b]2.5.3 中试研究场地[/b]固体制剂中试车间[b]2.5.4 中试设备[/b]见表2。[b]2.5.5 质量评价[/b]与原研药格列卫对比研究结果显示,中试产品的各项质量指标与格列卫相当,高温、光照、高湿三种剧烈条件下考察10天后,中试产品的各项质量指标仍与列卫相当,说明自研中试产品与原研产品质量一致。[b]3 结论[/b]因为本品原料是水溶性原料,粒度对溶出度影响不大,所以对原料前处理采用了常规机械粉碎法,过100目筛。物料混合6-12分钟都可以混匀,选择了中间点9分钟作为混合时间。根据实际情况,粘合剂水的用量由小试的2.5g/200片降到了65g/5000片。多批样品颗粒水分都小于2.5%,说明控制2.5%以下的颗粒水分适合本工艺。三批中试结果显示总混30分钟可以保证物料混合均匀。通过溶出曲线和脆碎度两个指标,考察了30-50N、50-70N、70-100N三个硬度范围,结果显示压片硬度范围在50-70N更为合理。包衣环节,考察了包衣增重2.1%、3.2%、4.2%三个梯度,对溶出曲线均无影响,最后确定包衣增重范围是2-4%。本文对甲磺酸伊马替尼片的制备工艺进行研究,用中试产品与格列卫进行全面的质量对比试验,并进行了影响因素试验考察研究,拟开发出与原研药具有相同质量的甲磺酸伊马替尼片,实现甲磺酸伊马替尼片的可工业化生产。
各位高手可有盐酸罗哌卡因红外谱图啊?还有顺便问下,药典上说药品1-2mg氯化钾200mg,其中[color=#d40a00]1-2mg[/color]和[color=#d40a00]200mg[/color]只是个用质量来描述固体样品量的方式吧,概数,无需用天平来称量、量化吧?正如液体样品可用体积的量来描述,L,ml或滴。是这样理解的吧?
请问三氟甲磺酸钠、三氟甲磺酸镨如何检测含量,急需
http://www.3158.com/upfiles4/2010/08/24/15/06/07/6599bb85.jpg请教各位版友,用液相法分析甲磺酸伊马替尼(见上式),其中有个中间体是没有与甲磺酸成盐的成分。在液相的溶液条件下(水相pH2.5),能把这两种物质分开吗?甲磺酸伊马替尼是可以水解的吧?这个中间体和甲磺酸依马替尼会生成同一种物质吗?要是这样的话,那这个中间体就没法分析了吧。谢谢各位版友!
请问三氟甲磺酸钠、三氟甲磺酸镨如何检测含量,急需
http://www.greenherbs.com.cn/bbs/dispbbs.asp?boardid=2&Id=7681612594 七氟醚杂质C Sevoflurane Related Compound C 对照品/标准品1612572 七氟醚杂质 B Sevoflurane Related Compound B 对照品/标准品1612550 七氟醚杂质 A Sevoflurane Related Compound A 对照品/标准品1612540 七氟醚 Sevoflurane 对照品/标准品1612539 盐酸舍曲林 Sertraline Hydrochloride 对照品/标准品1612528 盐酸舍曲林杂质A Sertraline Hydrochloride Related Compound A 对照品/标准品1612517 盐酸舍曲林消旋体混合物 Sertraline Hydrochloride Racemic Mixture 对照品/标准品1612506 L-丝氨酸 L-Serine 对照品/标准品1612426 芝麻油杂质B Sesame Oil Related Compound B 对照品/标准品1612415 芝麻油杂质A Sesame Oil Related Compound A 对照品/标准品1612404 芝麻油 Sesame Oil 对照品/标准品1612029 番泻苷 B Sennoside B 对照品/标准品1612018 番泻苷 A Sennoside A 对照品/标准品1612007 番泻苷 Sennosides 对照品/标准品1611955 硒 蛋氨酸 Selenomethionine 对照品/标准品1611900 盐酸司来吉兰 Selegiline Hydrochloride 对照品/标准品1611004 司可巴比妥 CII Secobarbital CII 对照品/标准品1610090 东莨菪亭 Scopoletin 对照品/标准品1610001 氢溴酸东莨菪碱 Scopolamine Hydrobromide 对照品/标准品1609831 沙奎那韦杂质A Saquinavir Related Compound A 对照品/标准品1609829 甲磺酸沙奎那韦 Saquinavir Mesylate 对照品/标准品1609807 双水杨酯 Salsalate 对照品/标准品1609625 沙美特罗杂质B Salmeterol Related Compound B 对照品/标准品1609614 沙美特罗杂质A Salmeterol Related Compound A 对照品/标准品1609603 昔美酸沙美特罗 Salmeterol Xinafoate 对照品/标准品1609501 水杨酸片 Salicylic Acid Tablets 对照品/标准品1609024 水杨酸杂质B Salicylic Acid Related Compound B 对照品/标准品1609013 水杨酸杂质A Salicylic Acid Related Compound A 对照品/标准品1609002 水杨酸 Salicylic Acid 对照品/标准品1608000 水杨酰胺 Salicylamide 对照品/标准品1607506 连翘粉状贯叶提取物 Powdered St. John's Wort Extract 对照品/标准品1607040 糖精钠 Saccharin Sodium 对照品/标准品1607029 糖精钙 Saccharin Calcium 对照品/标准品1607007 糖精 Saccharin 对照品/标准品1606503 芦丁 Rutin 对照品/标准品1606208 硝酚胂酸 Roxarsone 对照品/标准品1605523 罗哌卡因杂质B Ropivacaine Related Compound B 对照品/标准品1605512 罗哌卡因杂质A Ropivacaine Related Compound A 对照品/标准品1605500 盐酸罗哌卡因 Ropivacaine Hydrochloride 对照品/标准品1604916 罗库溴铵合剂峰的识别 Rocuronium Peak Identification Mixture 对照品/标准品1604905 罗库溴铵 Rocuronium Bromide 对照品/标准品1604870 利凡斯的明杂质B Rivastigmine Related Compound B 对照品/标准品1604869 利凡斯的明杂质A Rivastigmine Related Compound A 对照品/标准品1604814 利托那韦杂质混合物 Ritonavir Related Compounds Mixture 对照品/标准品1604803 利托那韦 Ritonavir 对照品/标准品1604701 盐酸利托君 Ritodrine Hydrochloride 对照品/标准品1604665 利培酮系统适用性试验用混合物 Risperidone System Suitability Mixture 对照品/标准品1604654 利培酮 Risperidone 对照品/标准品1604643 利塞膦酸杂质C Risedronate Related Compound C 对照品/标准品1604632 利塞膦酸杂质B Risedronate Related Compound B 对照品/标准品1604621 利塞膦酸杂质A Risedronate Related Compound A 对照品/标准品1604610 利塞膦酸钠 Risedronate Sodium 对照品/标准品1604600 利美索龙 Rimexolone 对照品/标准品1604508 盐酸金刚乙胺 Rimantadine Hydrochloride 对照品/标准品1604348 利鲁唑杂质A Riluzole Related Compound A 对照品/标准品1604337 利鲁唑 Riluzole 对照品/标准品1604202 醌式利福平 Rifampin Quinone 对照品/标准品1604009 利福平 Rifampin 对照品/标准品1603800 利福布丁 Rifabutin 对照品/标准品1603108 核糖 Ribose 对照品/标准品1603006 维生素B2 Riboflavin (Vitamin B2) 对照品/标准品1602706 利巴韦林 Ribavirin 对照品/标准品1602003 间苯二酚 Resorcinol 对照品/标准品1601849 二类残留溶剂-二甲苯 Residual Solvent Class 2 - Xylenes 对照品/标准品1601827 二类残留溶剂-三氯乙烯 Residual Solvent Class 2 - Trichloroethylene 对照品/标准品1601805 二类残留溶剂-甲苯 Residual Solvent Class 2 - Toluene 对照品/标准品1601780 二类残留溶剂-四氢萘 Residual Solvent Class 2 - Tetralin 对照品/标准品1601770 二类残留溶剂-四氢呋喃 Residual Solvent Class 2 - Tetrahydrofuran 对照品/标准品1601769 二类残留溶剂-二氧噻吩烷 Residual Solvent Class 2 - Sulfolane 对照品/标准品1601747 二类残留溶剂-吡啶 Residual Solvent Class 2 - Pyridine 对照品/标准品1601725 二类残留溶剂-硝基甲烷 Residual Solvent Class 2 - Nitromethane 对照品/标准品1601703 二类残留溶剂-N-甲基吡咯烷酮 Residual Solvent Class 2 - N-Methylpyrrolidone 对照品/标准品1601689 二类残留溶剂-甲基环己烷 Residual Solvent Class 2 - Methylcyclohexane 对照品/标准品1601667 二类残留溶剂-甲基丁基酮 Residual Solvent Class 2 - Methylbutylketone 对照品/标准品1601645 二类残留溶剂- 2-甲氧基乙醇 Residual Solvent Class 2 - 2-Methoxyethanol 对照品/标准品1601623 二类残留溶剂-甲醇 Residual Solvent Class 2 - Methanol 对照品/标准品1601601 二类残留溶剂-己烷 Residual Solvent Class 2 - Hexane 对照品/标准品1601587 二类残留溶剂-甲酰胺 Residual Solvent Class 2 - Formam
各位专家,有做过土壤中乙酸和甲磺酸的吗,跪求经验!

【作者】 管清香; 林天慕; 王恩思;【机构】 吉林大学药学院; 吉林大学生命科学学院;【摘要】 目的:建立测定甲磺酸地拉韦啶薄膜衣分散片含量的方法。方法:采用Diamonsil(TM) C18(150mm×4.6mm,5μm),乙腈-50mmol·L-1pH4.6磷酸二氢钠(55∶45)为流动相,检测波长为300nm。结果:甲磺酸地拉韦啶在12.54~62.70mg·L-1范围内呈良好线性关系(r=0.9999)。低、中、高3种浓度的平均回收率分别为99.5%,99.9%和101.5%(n=3)。结论:本方法简便、快速、专属性强,可用来测定甲磺酸地拉韦啶分散片的含量。 【谱图】
[font=&][color=#333333]欧洲药典中规定用碘化钠对甲磺酸酯进行衍生化,这里的碘化钠可以用碘化钾替代吗?[/color][/font]

10,抽取5个版友);中奖名单:yifan1117(注册ID:yifan1117)捌道巴拉巴巴巴(注册ID:v3082413)20071940xu(注册ID:20071940xu)dyd3183621(注册ID:dyd3183621)zengzhengce163(注册ID:zengzhengce163)http://ng1.17img.cn/bbsfiles/images/2017/02/201702061500_01_1610895_3.jpghttp://ng1.17img.cn/bbsfiles/images/2017/02/201702061500_02_1610895_3.jpg【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================HPLC法测定甲磺酸多拉司琼的含量方法:HPLC基质:动物提取物应用编号:102760化合物:甲磺酸多拉司琼固定相:Diamonsil C18色谱柱/前处理小柱:Diamonsil C18, 250 x 4.6mm色谱条件:色谱柱:Diamonsil C18 250 mm× 4.6 mm, 5μm(Cat#:99903) 流动相: 乙腈- 水- 1mo l # L - 1 甲酸铵( 450:440:110), 用三乙胺调pH 至8.0 流速: 1.0 mL/min 柱温: 室温 进样量: 20μL 检测器: UV 285nm文章出处:中国药房 2007,18(22):1731-1732关键字:甲磺酸多拉司琼, Diamonsil C18, 钻石一代, 高效液相色谱法, HPLC, 含量测定谱图:摘要:目的:建立以高效液相色谱法测定甲磺酸多拉司琼含量的方法。方法:色谱柱为Diamonsil C18,流动相为乙腈-水-1mol.L-1甲酸铵(450∶440∶110),用三乙胺调pH至8.0,流速为1.0mL.min-1,检测波长为285nm,进样量为20μL。结果:甲磺酸多拉司琼检测浓度的线性范围为24~56μg.mL-1(r=0.9996);平均加样回收率为99.67%(RSD=0.74%)。结论:本方法操作简便、灵敏度高、重现性好,可用于甲磺酸多拉司琼的质量控制。http://www.dikma.com.cn/Public/Uploads/images/93-6.JPG
不知道哪位用GC检测过"三甲硅烷基三氟甲磺酸酯(TMSOTf)"?我们曾试过,但好象由于酸性太强,对色谱柱损伤太大,目前不敢再测了.
[color=#444444]请问大家有哪些方法可以衍生甲磺酸烷基酯类化合物,采用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]进行测定。采用碘化钾水溶液衍生时空白有干扰。[/color]
采用RP-HPLC法测定甲磺酸帕珠沙星中有关物质。采用Diamonsil C18 5μm 4.6×200mm;乙腈为流动相A液;取1000mL水加5.76g无水柠檬酸,用三乙胺调pH3.0∶乙腈(95∶5)为流动相B液,进行梯度洗脱,0~30min内A-B的比例由8∶92线性变化到50∶50,检测波长331nm,流速为1.0mL·min-1; 结果:甲磺酸帕珠沙星与中间体及各杂质峰能完全分离。该法准确,专属性好,可用于甲磺酸帕珠沙星有关物质检测。
急需以下化学试剂标准四氢呋喃、吗啉、DMF-DMA、N-甲基哌嗪、甲磺酸、对甲苯磺酸有知道的同志请将结果发送至我的邮箱weiweidou2008@live.cn谢谢大家啦!
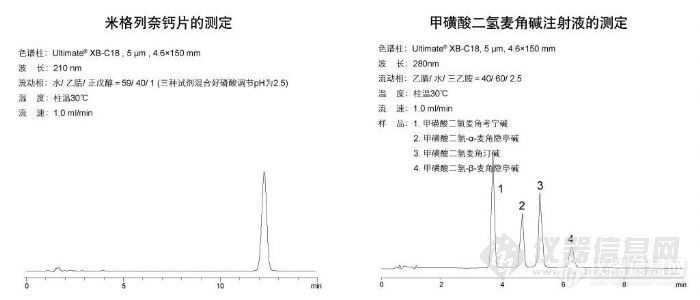
米格列奈钙片测定和甲磺酸二氢麦角碱注射液的测定http://ng1.17img.cn/bbsfiles/images/2009/11/200911021813_180160_1896702_3.jpg
在检测注射用甲磺酸左氧氟沙星含量时:中间体检测时用紫外检测,成品用的是高效液相检测,之前中间体用原料做工作对照,对照品A值一般在所配浓度下一般为0.39左右,F值在1.26左右,成品没什么问题,可是现在用中检所的对照品,中间体测定时对照品在相同浓度下A值才有0.35左右,这样的话F值就接近1.3了,结果含量就会高很多甚至不合格,但是成品上液相时又是合格的,也就是说对照品应该没问题,是不是中检所的对照品不适合用紫外分光光度法来检测呢?请各位帮忙分析分析,谢谢!!!补充:在这之前,该产品中间体检测都是用中检所的对照品上高效液相测定的,为了节省时间改用了紫外分光光度法检测工艺没改,液相测出来接过肯定会更精确些,但是奇怪的是,同样的对照品中间体检测超标,成品检测合格,不过之前用原料做工作对照检中间体时,成品标示量一般在100%以下,用中检所对照品检测中间体,成品标示量一般在105%,规定上限是110%没我是在想我们的中间体检测方法是不是不太合理制药工艺中没有纯化过程的,但是原料工作对照77.54%,中检所对照品97.3%,都是根据所需浓度换算好了再配制检测的,我是想应该里面所含杂质吸收影响就不明显了吧?您觉得呢?
三氟化氮、四氟化碳、六氟化硫,三氟甲磺酸,这些高纯气体怎么分析?跪求分析方法
中检所来源的左卡尼汀对照品,上面的含量为按无水物计,我们现在要用湿计的含量,第一次用时,自己做了一下水分,然后推出湿计的含量,请问一下是不是每次做都要测一下水分,还是同批次做一次就好,求大神们指点。。。
[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url],FID检测器,毛细色谱柱,100%聚乙烯乙二醇分离相,之前检测低浓度乙醇胺可以检测出来,中间进了一次甲磺酸,进了之后就出现基线不稳的情况,老化几次后基线正常,在之后就低浓度的乙醇胺就检测不出来,其他成分均能检测出来,各项设置和之前均不改变,问一下是不是色谱柱出了问题
[color=black]复方盐酸阿替卡因注射液为复方制剂,是盐酸阿替卡因与肾上腺素的灭菌水溶液,作为口腔用局部麻醉剂,适用于涉及切骨术及粘膜切开的外科手术过程。[/color][color=black] [/color][img=,156,99]https://ng1.17img.cn/bbsfiles/images/2019/03/201903211036489419_4502_2297_3.jpg!w156x99.jpg[/img][align=center][/align][align=left][b][color=black]盐酸阿替卡因(Articaine hydrochloride M.W.:320.84)[/color][/b][/align][align=center][b][color=black] [/color][/b][/align][color=black]在现有国家药品标准(YBH17082004-2015Z)分析方法中,流动相添加了离子对试剂-庚烷磺酸钠,并在pH为2.0的强酸条件下进行相应分析,不利于色谱柱的使用寿命。大曹三耀实验室参考USP方法,以冰醋酸水溶液-乙腈作为流动相,选用CAPCELL PAK C18 MGII色谱柱,实现了复方盐酸阿替卡因注射液中盐酸阿替卡因的定量和有关物质的良好分析(复方盐酸阿替卡因注射液由客户提供)。[/color][color=black]CAPCELLPAK C18 MGII[/color][color=black]液相色谱柱,其采用高纯度硅胶作为基质,通过减少硅胶微细孔的数量来增大有效比表面积;并且采用新包被技术Ultimate Polymer Coating,实现了对硅醇基极大程度的封锁,兼具分离性能和普适性能,通用性非常好。[/color][align=left][b][color=#0070c0]实验方法[/color][/b][/align][align=left][img=,500,358]https://ng1.17img.cn/bbsfiles/images/2019/03/201903211037456969_5082_2297_3.jpg!w730x523.jpg[/img][/align][align=left]图1[color=black]盐酸阿替卡因[/color]对照品及供试品溶液[/align][align=left][img=,500,248]https://ng1.17img.cn/bbsfiles/images/2019/03/201903211038541919_2603_2297_3.jpg!w572x284.jpg[/img][/align][align=center][/align][align=center][/align][color=black]为进行有关物质分析,该实验将注射液样品以流动相稀释100倍,作为有关物质供试品溶液,再将该有关物质供试品溶液以流动相进一步稀释100倍,作为自身对照溶液。以冰醋酸水溶液-乙腈作为流动相,选用CAPCELL PAK C18 MGII色谱柱,通过调整流动相比例及柱温,最终在18%乙腈、柱温30℃条件下实现了盐酸阿替卡因供试品溶液及对照品的良好分析。[/color]如图2、3,使用CAPCELL PAK C18 MGII色谱柱进行分析,盐酸阿替卡因和有关物质均能得到良好分析结果,主峰与峰前杂质得到了良好分离,分离度为1.90(见表1)[img=,400,311]https://ng1.17img.cn/bbsfiles/images/2019/03/201903211045536855_9516_2297_3.jpg!w574x447.jpg[/img][img=,400,295]https://ng1.17img.cn/bbsfiles/images/2019/03/201903211045540875_8483_2297_3.jpg!w698x516.jpg[/img][align=left] 图2 [color=black]盐酸阿替卡因[/color]有关物质供试品溶液及空白 图3 自身对照溶液[/align][align=center][/align][align=left]表1 有关物质结果详表[/align][align=left][img=,600,323]https://ng1.17img.cn/bbsfiles/images/2019/03/201903211042513275_6690_2297_3.jpg!w786x424.jpg[/img][/align][align=center][/align]综上实验结果,使用CAPCELL PAK C18 MGII S5 4.6mm i.d.×250 mm色谱柱,以冰醋酸水溶液-乙腈为流动相体系,在30°C柱温条件下,能够实现复方盐酸阿替卡因注射液中盐酸阿替卡因的定量和有关物质的良好分析。[color=black] [/color]