实验室三个人做出的曲线都不一样 各位谁有标准的曲线 上传一个呗 实验方法是水中硫酸盐的检测GB 5750 生活饮用水标准检验法[em0808]
在样品中可能含有间苯二胺和间苯二胺硫酸盐,在相同的流动相下请问间苯二胺硫酸盐与间苯二胺在同一个位置出峰吗?
做了好几次饮用水的硫酸盐标准曲线,在加入硫酸盐标准溶液,3ml,4ml,6ml,8ml,10ml的吸光值都差不多是0.1左右,不知道,问题出来在哪。,就低溶度的有呈现线性相关,刚刚又做了一下,10ml的吸光值为0.1964,8ml的为 0.0744,崩溃
现在有关硫酸盐测试标准有哪些大家能否指点指点。
对苯二胺硫酸盐、间苯二胺硫酸盐、邻苯二胺硫酸盐,用液相色谱C18柱能用吗?应配怎样的流动相? 它们的稀水溶液PH值在2-3左右。我用硫酸调流动相PH到2左右出两个峰。 又用三乙胺调PH到7多点还是两个
标准HJ/T342-2007中铬酸钡分光光度法测水中的硫酸盐标准曲线,最后两个点的吸光度为何上不去,反而比前面的点的吸光度还要低。曲线如下,使用液:(ml)0. 0.25 1.00 2.00 4.00 6 .00 8.00 10.00 吸光度: 0.014 0.024 0.099 0.216 0.418 0.610 0.778 0.658 校正吸光度: 0 0.010 0.085 0.202 0.404 0.596 0.764 请高手指教!
亚硫酸盐 (Sulfites或SulfitingAgents)为使用多年之合法食品添加物,不仅是非常有效的酵素抑制剂、漂白剂、抗氧化剂、还原剂及防腐剂,且价格便宜。亚硫酸盐最早被使用之纪录是在罗马帝国时代,当时是被用於葡萄酒容器之消毒杀菌。 此外,许多食品均含有天然存在之亚硫酸盐,尤其是在各种醱酵食品中。亚硫酸盐具有杀菌功效及强还原力,可将食品的著色物还原漂白,并可抑制氧化作用,防止酵素与非酵素褐变反应。合法添加於食品之亚硫酸盐包括:亚硫酸钠 (Sodium Sulfite,Na2SO3)、亚硫酸钾 (Potassium Sulfite, K2SO3)、亚硫酸氢钠 (Sodium Bisulfite,NaHSO3)、亚硫酸氢钾 (Potassium Bisulfite, KHSO3)、偏重亚硫酸氢钠 (SodiumMetabisulfite, Na2S2O5)、偏重亚硫酸氢钾 (Potassium Metabisulfite, K2S2O5)、低亚硫酸钠(Sodium Hydrosulfite,Na2S2O4)。亚硫酸盐广泛使用於脱水蔬菜、脱水水果、动物胶、糖蜜、糖飴、糖渍果实、虾类、贝类、水果酒、淀粉等產品中,常见市售添加亚硫酸盐的產品则包括:金枣、凤梨乾、脱水香蕉、葡萄乾、杏乾、柿饼、脱水金针、洋菇、笋乾、榨菜、绿豆芽、枸杞等。 二氧化硫是酚氧化酶的化学性抑制剂,同时也会与羰基化合物作用,所以当此类化合物存在时,必须加入过量之二氧化硫与其作用,方能将酚氧化酶之活性去除。以二氧化硫抑制酚氧化酶為一不可逆反应,将过量之二氧化硫去除时(如:漂水过程),酚氧化酶之活性亦无法恢复。但採用漂水过程时,应特别注意可溶性物质之流失,以免影响成品率。 产品内部若有空气存在,少量之氧气亦可造成褐变。因此,使用二氧化硫作為抑制剂时,必须考量二氧化硫之渗透。游离态 (自由态) 之二氧化硫(Free Sulfite) 较亚硫酸盐溶剂所形成之二氧化硫溶液更具有渗透性,亦可使用真空所产生之内外压差将二氧化硫强制渗透进入产品内部。 二氧化硫易溶於水而生成H2SO3,且一旦与硷作用则会转变為SO32-、HSO3-、S2O52-。这些无机亚硫酸盐离子在水溶液中会形成平衡状态,其个别存在之浓度则视pH值而定 (Green, 1976; Joslyn and Braverman, 1954)。其简单化学变化方程式如下: 一般食品之pH范围在3~7左右,大部份之亚硫酸盐是以HSO3-状态存在。唯有在很低之pH值下,SO2才会生成。pH值会影响食品内游离态与结合态 (Combined Sulfites)之亚硫酸盐之比例变化,游离态之亚硫酸盐随pH值降低而增加,若能控制pH值就可以控制食品内之亚硫酸盐残存量 。 亚硫酸盐经氧化后会形成无毒之硫酸盐,而在pH值小於4之食品,其所添加之亚硫酸盐会以SO2形态挥发而散失,尤其是在加热情况下。在许多食品中,仅有一小部份所添加之亚硫酸盐是以游离态之无机亚硫酸盐形态存在。 将亚硫酸盐添加于食品中,其变化之情况系与食品之化学特性、加工方法与程度、储存状态与时间、包装材料之渗透性及亚硫酸盐之添加量等因素相关。亚硫酸盐能与食品中许多成份(还原糖、醛类化合物、酮类化合物及蛋白质等)进行稳定反应,而形成各种型式的结合态亚硫酸盐。此外,在加工处理及贮存过程中,亚硫酸盐非常容易与食品中其他成份產生反应,而形成各种亚硫酸盐之有机化合物,一旦亚硫酸盐与其他有机成份结合后,就失去其特定作用,而使得亚硫酸盐之用量随產品种类而异。 二氧化硫在酸性情况下才会產生漂白及杀菌功效,其二氧化硫含量须在4,000 ppm以上才具有防腐效果。二氧化硫浓度过低时,则无法抑制微生物生长;而当二氧化硫浓度过高时,则果胶质之分解速度加快,致使组织软化,且具有刺激性气味。 亚硫酸盐残留量明显受到食品种类 (成份特性)、加工方法及贮存条件 (温度、时间..等)之影响,因此亚硫酸盐在加工过程之用量与成品之残留量亦非常难订定一合理标準。一般蜜饯业者相信漂水过程可以大幅降低亚硫酸盐残留量,甚至完全除去亚硫酸盐。实际上,漂水过程仅能去除游离态之亚硫酸盐。
大家好 请教个问题 我做液相色谱分析标准曲线,用邻氯苯胺盐酸盐做标准曲线,但是样品是邻氯苯胺硫酸盐,怎么计算邻氯苯胺的含量?谢谢
盐酸副玫瑰苯胺比色法测定亚硫酸盐方法的要点及改进 盐酸副玫瑰苯胺比色法测定食品中的亚硫酸盐残留量是食品卫生理化国标检验方法中的第一法( GB/ T5009. 34 -1996) ,它灵敏、准确,但是它对于水不溶性样品检测时间太长,同时方法未给出关键试剂盐酸副玫瑰苯胺溶液中盐酸浓度范围等,给实际操作带来很大的不便。相据笔者的摸索及实践经验,进行了改进。现报告如下:1 水不溶性固体样品的前处理前处理时间按标准规定水不溶性的固体样品粉碎研磨浸泡至少4h 后才能过滤测定(以使二氧化硫完全被吸收) ,整个实验过程最短也要5h 以上,如果能将水不溶性的固体样品的前处理方法加以改进,实验时间将会大大缩短。笔者用振荡法或超声波法对几种水不溶性固体样品进行不同时间的处理,同时与浸泡法进行了对比,结果见表1。表1 不同前处理方法测定亚硫酸盐残留量(以SO2 计,g/ kg) 结果对比样品名称浸泡5h 超声40min 振荡50min话梅1. 27 1. 28 1. 29情人梅1. 71 1. 75 1. 72话梅肉0. 67 0. 65 0. 69山楂糕0. 12 0. 13 0. 11冬瓜蜜饯0. 77 0. 79 0. 75银耳6. 02 6. 00 5. 95竹笋4. 23 4. 18 4. 20竹荪9. 29 9. 34 9. 32干辣椒0. 080 0. 078 0. 069 对表1 中数字进行统计学处理,浸泡5h 与超声40min 两方法之间经t 检验, P 0. 05 ,两法测定的结果无显著性差异 同时浸泡5h 与振荡50min 两方法之间经t 检验, P 0. 05 ,两法结果也无显著性差异。所以,对于水不溶性的固体样品,可以用超声法(40min) 、或振荡法(50min) 来代替浸泡法进行样品前处理。2 实验关键试剂盐酸副玫瑰苯胺比色法涉及的试剂有多种,其中盐酸副玫瑰苯胺和二氧化硫标准是两个最关键的试剂。2. 1 二氧化硫标准液 二氧化硫标准液容易氧化变质,经实验,新标定的1. 142mg/ ml 二氧化硫标准溶液避光存放冰箱的条件下,可稳定一个月,一个月后必须重新标定。实验结果见表2。表2 二氧化硫标准贮备液存放时间对吸光度值的影响时间1μgSO2标准吸光度2μgSO2标准吸光度4μgSO2标准吸光度一个月前配制0. 002 0. 030 0. 076新配制0. 034 0. 067 0. 1412. 2 盐酸副玫瑰苯胺溶液 盐酸副玫瑰苯胺溶液中的盐酸浓度对实验结果影响非常大,酸度大,比色颜色浅,灵敏度低 酸度低,比色颜色深,灵敏度高,同时空白值也高。但标准方法中未给出调节盐酸副玫瑰苯胺溶液颜色的盐酸用量范围,仅仅指出用肉眼观察颜色变化(由红变黄) ,在实际操作中笔者曾几次因显色剂酸度问题导致实验失败。所以有必要找到一个合适的盐酸副玫瑰苯胺溶液盐酸酸度范围,使实验空白值低、灵敏度又满足要求,为此笔者进行了不同盐酸浓度下标准和空白吸光度值的对比实验,结果见表3 和图1。表3 盐酸副玫瑰苯胺溶液中盐酸的浓度与吸光度的关系盐酸浓度(mol/ L)显色剂颜色空白吸光度4.μgSO2标准吸光度减空白后吸光度0. 20 浅黄色0. 298 0. 459 0. 1610. 30 黄色0. 338 0. 372 0. 0340. 40 黄色0. 251 0. 303 0. 0520. 50 黄色0. 089 0. 254 0. 1650. 60 黄色0. 076 0. 230 0. 1540. 70 黄色0. 062 0. 202 0. 1400. 80 黄色0. 054 0. 186 0. 1320. 90 黄色0. 046 0. 168 0. 1221. 00 黄色0. 043 0. 158 0. 115 注:表2 中盐酸的浓度是指加到盐酸副玫瑰苯胺溶液中盐酸的用量换算之后的浓度。图1 中标准吸光度为减去空白吸光度后的值。图1 不同酸度的盐酸副玫瑰苯胺溶液对空白和标准吸光度值测定的影响0 6 7 中国卫生检验杂志2003 年12 月第13 卷第6 期 Chinese Journal of Health Laboratory Technology 20031December1131No16© 1995-2005 Tsinghua Tongfang Optical Disc Co., Ltd. All rights reserved.2. 2. 1 从图表中可以看出盐酸副玫瑰苯胺溶液中盐酸介质的浓度在0. 50mol/ L、0. 60mol/ L 时灵敏度高,但空白值也高(0.089、0. 076) ,盐酸副玫瑰苯胺溶液中盐酸介质的浓度在0.70mol/L - 1. 0mol/ L 之间空白吸光度较低(0. 062 - 0. 043) 并且灵敏度较高,所以配制0. 02 %的盐酸副玫瑰苯胺使用溶液时,可吸取0. 1 %盐酸副玫瑰苯胺溶液20ml 后直接加入一定量的(1/ 1) 盐酸使盐酸的浓度为0. 70mol/ L - 1. 0mol/ L 之间即可使用。实践证明使用同一个合适酸度的盐酸副玫瑰苯胺溶液,用新标定的标准溶液做标准曲线,环境条件、仪器条件相对稳定的前提下,可以使用相对较长一段时间(更换盐酸副玫瑰苯胺溶液时,再重新标定标准溶液,绘制新的标准曲线) 。2. 2. 2 0. 20mol/ L 空白及标准吸光度较0. 30mol/ L 的空白及标准吸光度高,是因为在反应体系中由于酸度的降低,盐酸副玫瑰苯胺本身结构改变颜色发生变化所致。3 标准曲线线性范围国标方法中规定标准曲线的线性范围是从0 - 4μg 二氧化硫,经过实验线性范围可延伸到10μg 二氧化硫,结果见表3。表3 盐酸副玫瑰苯胺比色法测定二氧化硫残留量标准曲线标准含量(μg) 0. 00 0. 40 0. 80 1. 20 1. 60 2. 00 3. 00 4. 00 6. 00 8. 00 10. 00吸光度值0. 000 0. 012 0. 027 0. 040 0. 061 0. 067 0. 107 0. 141 0. 222 0. 292 0. 368 线性范围的扩大对于高含量样品可减少稀释带来的误差。本文根据笔者的实际经验和摸索,对盐酸副玫瑰苯胺比色法测定食品中的亚硫酸盐残留量提出了改进意见,会给实际操作者带来一定的益处。参考文献[1 ] 中华人民共和国国家标准,食品卫生检验方法,理化部分,食品中亚硫酸盐残留量的测定方法GB/ T5009. 32 - 1996.(收稿日期:2003206230)
水质 硫酸盐的测定 火焰[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]分光光度法Water quality-Determination of sulphate-Flame atomic absorption spectrophotometric methodGB 13196—911 主题内容与适用范围1.1 本标准规定了间接测定水中可溶性硫酸盐的火焰[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]分光光度法。 1.2 本标准适用于地表水、地下水及饮用水可溶性硫酸盐的测定。1.3 本标准的最低检出浓度为0.4mg/L,测定上限当取样量为10mL时,是30mg/L。当取样虽为1mL时,则是300mg/L。水样适当稀释,测定范围还可以扩大。1.4 Pb2+和PO43-对测定产生于扰,但10μg以下的Pb2+或PO43-可允许存在。2 原理在水-乙醇的氨性介质中,硫酸盐与铬酸钡悬浊液反应。反应式如下:SO42-+BaCrO4→BaSO4↓+CrO42-用[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]法测定反应释放出的铬酸根,即可间接算出硫酸盐的含量。所用火焰。为空气-乙炔富燃性黄色火焰,测定波长为359.3nm。3 试剂除非另有说明,分析时均使用符合国家标准或专业标准分析纯试剂,去离子水或同等纯度的水。3.1 盐酸(HCl):ρ=1.19g/mL。3.2 冰乙酸(CH3COOH):ρ=1.05g/mL。3.3 氢氧化铵(NH4OH):ρ=0.880g/mL。3.4 无水乙醇(CH3CH2OH)。3.5 氢氧化铵溶液:1+1。用氢氧化铵(3.3)配制。临用时现配。3.6 混合酸溶液:盐酸(3.1)0.42mL,冰乙酸(3.2)14.7mL混合,用水稀释至200mL。3.7 钙溶液:1mg/mL。称0.28g氯化钙(CaCl2)溶于100mL水中,摇匀。3.8 铬酸钡悬浊液:称0.5g铬酸钡(BaCrO4)溶于200mL。混合酸溶液(3.6)中,贮于聚乙烯瓶中。用前振摇。3.9 硫酸盐标准溶液,SO42-:100mg/L。准确称取无水硫酸纳(Na2SO4,在105℃烘2h)0.0740g,用适量水溶解,转入500mL容量瓶中,用水稀释至标线,摇匀。4 仪器一般实验室仪器和4.1 [url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]分光光度计。4.2 铬空心阴极灯。4.3 乙炔的供气装置。4.4 空气压缩机,加除油、水及杂质装置。4.5 过滤器,见下图。过滤装置图1-抽滤瓶;2—10mL比色管;3-带砂芯的玻璃过滤器;4-比色管塞;5-胶盖;6-0.45μm滤膜;7-接抽气泵5 采样及样品水样采集后,立即用0.45μm滤膜抽滤除去悬浮物,贮存于聚乙烯瓶中。6 步骤6.1 试料取10mL水样置于25mL比色管中,如硫酸根含量大于30mg/L,可适量少取样品,然后加水至10mL。6.2 测定6.2.1 前处理:在试料(6.1)中,依次加入铬酸钡悬浊液(3.7)2mL,氢氧化铵溶液(3.5)1mL,钙溶液(3.6)1mL,无水乙醇(3.4)8mL,加水至标线,摇匀。放置30min后,用0.45μm滤膜抽滤(装置见图1)于10mL干燥比色管中,备测。6.2.2 测定:遵照仪器使用说明书调节仪器至最佳工作条件,测定滤液的吸光度。6.3 校准曲线的绘制在一组25mL比包管中,加入硫酸盐标准溶液0,0.50,1.00,1.50,2.00,2.50,3.00mL,然后按步骤(6.2.1)进行前处理,并按(6.2.2)中的条件测定其吸光度。用减去空白的吸光度与相对应的硫酸盐浓度(mg/L)绘制校准曲线。7 分析结果的表述7.1 硫酸盐含量,由下式给出:式中:c——试样中硫酸盐的浓度,mg/L;c/——由样准曲线上查得的浓度,mg/L;V——所取试样的体积,mL;25——比色管的体积,mL。7.2 硫酸盐含量,用回归方程计算。8 精密度和准确度八个实验室测定了三个不同浓度水平的统一样品,硫酸盐含量分别为:4.83,10.5,25.7mg/L。8.1 重复性重复性相对标准倡差分别为:3.69%、3.65%和2.65%。8.2 再现性再现性相对标准偏差分别为:7.98%、3.84%和4.07%。8.3 准确度相对误差分别为:+1.45%、-2.86%和-1.56%。附加说明:本标准由国家环境保护局科技标准司标准处提出。本标准由中国环境监测总站负责起草。本标准主要起草人刘京、魏复盛。本标准委托中国环境监测总站负责解释。
食品中亚硫酸盐的测定方法中华人民共和国国家标准【GB/T 5009.34—1996】食品中亚硫酸盐的测定方法 1 主题内容与适用范围 本标准规定了食品中亚硫酸盐的测定方法。 本标准适用于食品中亚硫酸盐残留量的测定。 第一篇 盐酸副玫瑰苯胺法(第一法) 2 原理 亚硫酸盐与四氯汞钠反应生成稳定的络合物,再与甲醛及盐酸副玫瑰苯胺作用生成紫红色络合物,与标准系列比较定量。本方法最低检出浓度为1mg/kg。 3 试剂 3.1 四氯汞钠吸收液:称取13.6g氯化高汞及6.0g氯化钠,溶于水中并稀释至1000mL,放置过夜,过滤后备用。 3.2 氨基磺酸铵溶液(12g/L)。 3.3 甲醛溶液(2g/L):吸取0.55mL无聚合沉淀的甲醛(36%),加水稀释至100mL,混匀。 3.4 淀粉指示液:称取1g可溶性淀粉,用少许水调成糊状,缓缓倾入100mL沸水中,随加随搅拌,煮沸,放冷备用,此溶液临用时现配。 3.5 亚铁氰化钾溶液:称取10.6g亚铁氰化钾[K4Fe(CN)63H2O],加水溶解并稀释至100mL。 3.6 乙酸锌溶液:称取22g乙酸锌[zn(CH3COO)22H2O]溶于少量水中,加入3mL冰乙酸,加水稀释至100mL。 3.7 盐酸副玫瑰苯胺溶液:称取0.1g盐酸副玫瑰苯胺(C19H18N2Cl4H2O;p-rosanilinenhydrochlo-ride)于研钵中,加少量水研磨使溶解并稀释至100mL。取出20mL,置于100mL容量瓶中,加盐酸(1+1),充分摇匀后使溶液由红变黄,如不变黄再滴加少量盐酸至出现黄色,再加水稀释至刻度,混匀备用(如无盐酸副玫瑰苯胺可用盐酸品红代替)。 盐酸副玫瑰苯胺的精制方法:称取20g盐酸副玫瑰苯胺于400mL水中,用50mL盐酸(1+5)酸化,徐徐搅拌,加4~5g活性炭,加热煮沸2min。将混合物倒入大漏斗中,过滤(用保温漏斗趁热过滤)。滤液放置过夜,出现结晶,然后再用布氏漏斗抽滤,将结晶再悬浮于1000mL乙醚-乙醇(10∶1)的混合液中,振摇3~5min,以布氏漏斗抽滤,再用乙醚反复洗涤至醚层不带色为止,于硫酸干燥器中干燥,研细后贮于棕色瓶中保存。 3.8 碘溶液[c(1/2I2)=0.1mol/L]。 3.9 硫代硫酸钠标准溶液[c(Na2S2O35H2O)=0.1mol/L]。 3.10 二氧化硫标准溶液:称取0.5g亚硫酸氢钠,溶于200mL四氯汞钠吸收液中,放置过夜,上清液用定量滤纸过滤备用。 吸取10.0mL亚硫酸氢钠一四氯汞钠溶液于250mL碘量瓶中,加100mL水,准确加入20.00mL碘溶液(0.1mol/L),5mL冰乙酸,摇匀,放置于暗处2min后迅速以硫代硫酸钠(0.1mol/L)标准溶液滴定至淡黄色,加0.5mL淀粉指示液,继续滴至无色。另取100mL水,准确加入碘溶液20.0mL(0.1mol/L)、5mL冰乙酸,按同一方法做试剂空白试验。 计算: 式中:X1——二氧化硫标准溶液浓度,mg/mL; V1——测定用亚硫酸氢钠-四氯汞钠溶液消耗硫代硫酸钠标准溶液体积,mL; V2——试剂空白消耗硫代硫酸钠标准溶液体积,mL; c——硫代硫酸钠标准溶液的摩尔浓度,mol/L; 32.03——与每毫升硫代硫酸钠[c(Na2S2O35H2O)=1.000 mol/L标准溶液相当的二氧化硫的质量,mg。 3.11 二氧化硫使用液:临用前将二氧化硫标准溶液以四氯汞钠吸收液稀释成每毫升相当于2μg二氧化硫。 3.12 氢氧化钠溶液(20g/L)。 3.13 硫酸(1+71)。 4 仪器 分光光度计。 5 分析步骤 5.1 样品处理 5.1.1 水溶性固体样品如白砂糖等可称取约10.00g均匀样品(样品量可视含量高低而定),以少量水溶解,置于100mL容量瓶中,加入4mL氢氧化钠溶液(20g/L),5min后加入4mL硫酸(1+71),然后加入20mL四氯汞钠吸收液,以水稀释至刻度。 5.1.2 其他固体样品如饼干、粉丝等可称取5.0~10.0g研磨均匀的样品,以少量水湿润并移入100mL容量瓶中,然后加入20mL四氯汞钠吸收液,浸泡4h以上,若上层溶液不澄清可加入亚铁氰化钾溶液及乙酸锌溶液各2.5mL,最后用水稀释至100mt刻度,过滤后备用。 5.1.3 液体样品,口葡萄酒等可直接吸取5.0~10.0mL样品,置于100mL容量瓶中,以少量水稀释,加20mL四氯汞钠吸收液,摇匀,最后加水至刻度,混匀,必要时过滤备用。 5.2 测定 吸取0.50~5.0mL上述样品处理液于25mL带塞比色管中。 另吸取0、0.20、0.40、0.60、0.80、1.00、1.50、2.00mL二氧化硫标准使用液(相当于0、0.4、0.8、1.2、1.6、2.0、3.0、4.Oμg二氧化硫),分别置于25mL带塞比色管中。 于样品及标准管中各加入四氯汞钠吸收液至10mL,然后再加入1mL氨基磺酸铰溶液(12g/L)、1mL甲醛溶液(2g/L)及1mL盐酸副玫瑰苯胺溶液,摇匀,放置20min。用1cm比色杯,以零管调节零点,于波长550nm处测吸光度,绘制标准曲线比较。 5.3 计算 式中:X2——样品中二氧化硫的含量,g/kg; A1——测定用样液中二氧化硫的含量,μg; m1——样品质量,g; V3——测定用样液的体积,mL。 结果的表述:报告算术均值的3位有效数字。 5.4 允许差 相对相差≤10%。 第二篇 蒸馏法(第二法) 6 原理 在密闭容器中对样品进行酸化并加热蒸馏,以释放出其中的二氧化硫,释放物用乙酸铅溶液吸收。吸收后用浓盐酸酸化,再以碘标准溶液滴定,根据所消耗的碘标准溶液量计算出样品中的二氧化硫含量。本法适用于色酒及葡萄糖糖浆、果脯。 7 试剂 7.1 盐酸(1+1):浓盐酸用水稀释1倍。 7.2 乙酸铅溶液(20g/L):称取2g乙酸铅,溶于少量水中并稀释至100mL。 7.3 碘标准溶液[c(1/2I2=0.01mol/L)]:将碘标准溶液(0.1mol/L)用水稀释10倍。 7.4 淀粉指示液(10g/L):称取1g可溶性淀粉,用少许水调成糊状,缓缓倾入100mL沸水中,随加随搅拌,煮沸2min,放冷,备用,此溶液应临用时新制。 8 仪器 8.1 全玻璃蒸馏器。 8.2 碘量瓶。 8.3 酸式滴定管。 9 分析步骤 9.1 样品处理 固体样品用刀切或剪刀剪成碎末后混匀,称取约5.00g均匀样品(样品量可视含量高低而定)。液体样品可直接吸取5.0~10.0mL样品,置于500mL圆底蒸馏烧瓶中。 9.2 测定 9.2.1 蒸馏:将称好的样品置入圆底蒸馏烧瓶中,加入250mL水,装上冷凝装置,冷凝管下端应插入碘量瓶中的25mL乙酸铅(20g/L)吸收液中,然后在蒸馏瓶中加入10mL盐酸(1+1),立即盖塞,加热蒸馏。当蒸馏液约200mL时,使冷凝管下端离开液面,再蒸馏1min。用少量蒸馏水冲洗插入乙酸铅溶液的装置部分。在检测样品的同时要做空白试验。 9.2.2 滴定:向取下的碘量瓶中依次加入10mL浓盐酸、1mL淀粉指示液(10g/L)。摇匀之后用碘标准滴定溶液(0.01mol/L)滴定至变蓝且在30s内不褪色为止。 9.3 计算 式中:X3——样品中的二氧化硫总含量,g/kg; A2——滴定样品所用碘标准滴定溶液(0.01mol/L)的体积,mL; B——滴定试剂空白所用碘标准滴定溶液(0.01mol/L)的体积,mL; m2——样品质量,g; 0.032——与1mL碘标准溶液[c(1/2I2)=1.000mol/L]相当的二氧化硫的质量,g。 附加说明: 本标准由卫生部卫生监督司提出。 本标准第一法由北京市卫生防疫站、广东省卫生防疫站、卫生部食品卫生监督检验所负责起草。 本标准第二法由卫生部食品卫生监督检验所、北京市卫生防疫站、山东省食品卫生监督检验所、河北省卫生防疫站、北京市崇文区卫生防疫站负责起草。 本标准由卫生部委托技术归口单位卫生部食品卫生监督检验所负责解释。
急求铬酸钡法测硫酸盐的标准曲线!!谢谢啊
求助食品中亚硫酸盐检测标准

需要测定供试品中的硫酸盐含量,下面是药典上的标准,请大家帮忙看看,然后请教几个问题:1. 过程中保持pH为11的操作如何实现?还需要用pH计指示么?如果低于10.5,还需要加入氨水?2. 这个测定的原理不清楚,看了看书还不明白,请教一下,该反应用酞紫指示剂主要指示的是什么物质的pH变化范围?3. 测定结果使用空白消耗的滴定液数-供试品消耗的滴定液数的原理是什么?氯化钡起到什么作用?4. 标准里面使用EDTA.2Na作为滴定液,为什么还写“每1ml氯化钡滴定液(0.1mol/L)相当于9.606mg的硫酸盐”?为什么不是“每1mlEDTA.2Na滴定液(0.05mol/L)相当于9.606mg的硫酸盐”?5. 我们测定过程中,紫色始终不消退,是何原因?而即使很早加入乙醇(刚开始滴定1~2ml),溶液立刻由紫色变为无色,没有中间蓝紫色的过程,请问可能是什么原因?6. 加入的乙醇作用是什么呢?非常感谢![img]http://ng1.17img.cn/bbsfiles/images/2008/08/200808301456_106457_1621520_3.jpg[/img]
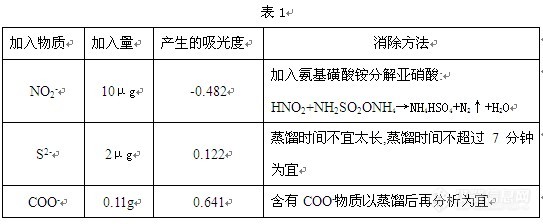
[color=#d40a00][size=2]维权声明:本文为[color=#ba4b01]abcdefghijkl123[/color][/size][color=#d40a00][size=2]原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。[/size][/color]对于一些样品中亚硫酸盐含量的测定,你们是如何测定的,如何提高样品检测的准确性啊[/color] 食品中亚硫酸盐的检测方法国标为GB/T5009.34-2003。本文主要阐述了食品中亚硫酸盐的四种检测方法,并通过选取了有代表的样品将这四种检测方法与国标法进行了比较和探讨。从而证实了这四种检测方法对食品中亚硫酸盐的准确定量具有一定的实践指导意义。 亚硫酸及其盐类是广泛使用的食品添加剂,具有漂白、脱色、防腐及抗氧化等作用。国标GB/T5009.34-2003规定了食品中的亚硫酸盐检测方法:第一法为盐酸副玫瑰苯胺比色法及第二法蒸馏后碘量滴定法。但随着食品添加剂滥用现象严重,着色剂、食品中未知成分干扰等因素,采用GB/T5009.34-2003中规定的方法检测食品中亚硫酸盐仍存在着检测误差和很多的技术盲点,并特别选取了几种有代表性的食品来分析其亚硫酸盐含量,并做比较,认为有必要对其国标法进行改进和深入探讨。 一、检测方法: 第一法 盐酸副玫瑰苯胺法(蒸馏后比色法) 1.原理:亚硫酸盐与四氯汞钠反应生成稳定的络合物,再与甲醛和盐酸副玫瑰苯胺生成紫红色的络合物,比色定量。 2.试剂 2.1 盐酸副玫瑰苯胺:称取精制提纯(或进口分装)试剂盐酸副玫瑰苯胺10mg,加1+1盐酸15mL,用水溶解定容至50mL,该试剂保存于冰箱,1周内稳定。 2.2 氨基磺酸铵: 12g/L 2.3 甲醛: 2g/L 2.4 SO2标准贮备液配制: 先测定固体试剂NaHSO3中SO2的纯度,而后根据已知SO2的纯度,直接称取NaHSO3配成SO2标准溶液,使用时无需再进行标定。这样标定之后的固体NaHSO3试剂可使用1年,用0.1moL/LNaOH溶液配成1000μg/mL贮备液,该贮备液于冰箱内至少稳定1个月。 2.5 SO2标准使用液配制:临用前用四氯汞钠吸收液稀释成2μg/mL的标准使用液。 3.方法 试样处理:在密闭容器中加1+1盐酸对试样进行酸化并加热蒸馏,释放出的SO2以四氯汞钠作为吸收液,定容至一体积,吸取一定量的试液分析。后面步骤及计算同GB/T5009.34-2003第一法。 4.方法探讨 4.1 干扰物质及消除方法见表1[img]http://ng1.17img.cn/bbsfiles/images/2010/08/201008091755_235403_2961690_3.jpg[/img] 4.2 COO- 干扰测定,会与盐酸副玫瑰苯胺形成紫红色络合物,典型样品如味精(谷氨酸钠分子结构中含有COO-),须采用蒸馏后比色,可排除此干扰,否则数据严重虚高。 4.3含硫基食品(如大蒜、萝卜、姜、辣椒、木耳等)蒸馏时间不超过7分钟为宜,蒸馏时间过长,则硫基化合物开始馏出,必要时对蒸馏装置进行改进,否则会干扰测定,数据虚高。 4.4 比色法适用于SO2含量低于0.1g/kg试样的检测。 第二法 蒸馏后碱滴定法 1原理 亚硫酸盐在酸性条件下用碱中和,加热,亚硫酸盐被过氧化氢吸收,用碱中和并滴定至终点,根据消耗标液用量计算其含量。 H2O2+H2SO3→H2SO4+H2O H2SO4+2NaOH→Na2SO4+2H2O 2试剂: 2.1 盐酸1+1 2.2 过氧化氢1+10 2.3 氢氧化钠标准溶液 0.05moL/L 2.4 甲基红-亚甲基蓝指示剂 3步骤 蒸馏过程同第一法,另在接收器内加入过氧化氢(1+10)20mL,加指示剂1滴,用0.05moL/L NaOH标液中和至灰绿色终点,作为吸收液,蒸馏至一定体积后,取下吸收液,再加一滴指示剂,用0.05moL/L NaOH标液滴定至灰绿色为终点。 4计算公式 X(g/kg)=C*V*32/m X:样品中二氧化硫的含量, g/kg C: 0.05moL/L NaOH标液浓度 V:滴定过氧化氢吸收液至终点时NaOH标液消耗毫升数 32:与1mLNaOH标液相当的二氧化硫的毫克数 5方法讨论 5.1该法与国标第二法相比,方法灵敏度更高,选择性相对更强,所须药品更简单,易于操作。 5.1该法适用于二氧化硫含量在0.1 g/kg以上试样的检测。 第三法 盐酸副玫瑰苯胺比色法(加过氧化氢) 适用范围:当检测带色的发酵酒、蒸馏后馏出液含有颜色、红糖等样品时,按GB/T5009.34-2003第一法,样品比色管均呈现一定量底色而干扰测定,使得SO2测得数据虚高,采用加入H2O2法消除呈色物质的背景干扰可得较为满意结果。 1. 原理:H2O2将SO2氧化成硫酸后,不与显色剂盐酸副玫瑰苯胺显色,且在波长550nm下不产生吸光度,呈色物质所产生的吸光度作为底液,予以扣除。 2.试剂 2.1 0.3% H2O2 2.2 其它试剂同本文第一法 3. 步骤:样品不须蒸馏,同GB/T5009.34-2003第一法处理。 显色:同GB/T5009.34-2003第一法,只是在测定样品时,须同时吸取2份样液于A、B管中,A管加0.2mL水,B管则加入0.2mL0.3% H2O2,它们所产生的吸光度相减所得的吸光度(A-B)作为样液中SO2所产生的吸光度,代入计算。 第四法 [url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法 1.原理:试样中的亚硫酸在20%磷酸酸性条件下,于90℃水浴中通氮曝气分离,收集在三乙醇胺溶液中,用IC测定。 2.试剂 2.1 亚硫酸标准溶液:按本文第一法配制成100μg/mLSO32-标准原液。用时用吸收液将原液稀释成0.1-4.0μg/mLSO32-使用液 2.2 吸收液:10克三乙醇胺加水溶解至1L 2.3 1%氨基磺酸铵 2.4 洗脱液:3.71克碳酸钠和3.36克碳酸氢钠加水溶解至1L,用时用水稀释10倍,碳酸钠和碳酸氢钠的浓度分别为3.5mmoL/L和4.0mmoL/L 2.5 净化剂163.3克十二烷基苯磺酸加水溶解至1L,用时用水稀释10倍 2.6 2,4-二硝基苯肼(2,4-DNP)液:1克2,4-DNP加40%磷酸溶解至100mL 3.仪器及测定条件: 3.1 ICS-1500[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url]:美国戴安公司 3.2 亚硫酸收集装置 3.3 色谱柱:IonPac AS14分析柱, 250mm×4mm 3.4 洗脱剂:3.5mmoL/LNa2CO3/4.0mmoL/LNaHCO3 洗脱剂流速:2.0mL/min 3.5 净化剂:50mmoL/L十二烷基苯磺酸,净化剂流速:2.0mL/min 3.6 检测器:抑制型电导检测器 3.7 温度:40℃ 3.8 进样量:100μL 4.操作方法 4.1 试验溶液的制备:取10mL 吸收液加入A吸收管内,5mL2,4-DNP液加入联接SO2收集装置的B管内。取1~5克试样放入已通氮脱气10分钟的40mL20%磷酸和1mL氨基磺酸铵溶液的曝气瓶内,立即接好收集装置。曝气瓶于90℃水浴中以800mL/min流速通氮曝气40min,所得吸收液即为试验溶液。用水代替试样同上操作,得到的吸收液为空白试验溶液。 4.2 测定:取100μL试验溶液和空白试验溶液注入IC内测定亚硫酸离子的峰面积,根据预先用标准溶液(0.1-4.0μg/mLSO32-)作成的标准曲线计算试样中二氧化硫含量。 5 说明:本法标准曲线,亚硫酸在0.1-4.0μg/mL范围内呈线性关系,检出限为0.2mg/kg。1000mgCl-、SO42-、NO3-、甲酸、乙酸、丙酸、乙醇、10mg甲醛、糠醛、二甲基硫醚、二甲基二硫醚、甲硫醇钠、丙烯基异硫氰酸盐及0.1mgS2-对1μg/mL亚硫酸无干扰。NO2-、乙醛、苯甲醛有严重负干扰,但NO2-干扰用氨基磺酸铵,醛类干扰用2,4-DNP消除。 二、总结: 1.本文介绍的四种检测方法与国标法比较结果见表2。由表可见,对于一些颜色较浅的食品如白木耳、粉丝、白糖、竹荪等,这些检测方法与国标法相一致,但一些颜色较深的样品和含有羧基的样品,干扰因素较大,用国标法检测本来不含有SO2的样品,却也测出了较高的值。而用本文介绍的检测方法可得较为满意的数值。[img]http://ng1.17img.cn/bbsfiles/images/2010/08/201008091756_235404_2961690_3.jpg[/img] 2. 样品制备时,尤其是干类果实的个体差异较大,故要注意样品的均质化。 3. 这四种的检测方法,可根据样品的实际情况,结合采用其中的检测方法进行食品中亚硫酸盐含量的测定。
自来水的硫酸盐用环境标准碘量法一般能有多大?
生活饮用水 硫酸盐 铬酸钡分光光度法 (热法)问题1:按照标准加入1mg/ml的硫酸盐标准溶液0,,0.25,0.5,1,3,5,7,10ml,加纯水至50ml。后按步骤进行,使用(1+1)氨水使溶液成柠檬黄色后要移入50ml具塞比色管中加水至刻度吗问题2:是使用慢速定量滤纸还是慢速定性滤纸(该标准要求慢速定量,但我看到有人用慢速定性)问题3:空白值0.025(在440nm出用1cm比色皿),但后面的吸光度不成正比,曲线老是没有线性,请教,有没有人做出来啊,有没有什么需要注意的地方
哪位大侠有食品中亚硫酸盐限量标准?
有一份井水,我们用热法铬酸钡分光光度法测定硫酸盐,怎么硫酸盐一点也没有啊,做不出来。样品加标后测定也没有含量,回收率为零,不知是么回事?标准系列是用纯水配的,作出来了。做了这么多年水样,还是第一次碰到过这种事。有一个现象是,水样在酸性条件下加铬酸钡时颜色没有变化,正常时会有一点变红,重铬酸根离子的颜色。样品测定时氯离子含量很高,达4万多,钙离子含量也很高,500多,单位mg/L。
目前在做食品中亚硫酸盐测定 采用GB 5009.34四氯汞钠-盐酸副玫瑰苯胺法测定,想请问各位大虾废液怎么处理的。。网上有文献报道采用甲醛吸收法测定食品中亚硫酸盐,但是所做结果回收率很低,请高手指点。。。
有没有哪位有20左右和30左右的硫酸盐的标准样品的真值?
请问GSB-1196-2000 201925硫酸盐的标准值是多少?GSB-1195-2000 201834氯化物的标准值是多少?谢谢了先!!!
急需GB13196-91 水质 硫酸盐的测定标准,哪位有的话请传一份给我,谢谢!
[em09511]做了几次硫酸盐的标准曲线但都不是很理想,不知道问题出在哪里?感觉铬酸钡的影响挺大,是不是在吸取时浓度差异太大了。要如何吸取才能避免这一问题啊,还有就是铬酸钡悬浊液的配置是不是也有影响啊!加热时间有影响吗?其他还有什么影响因素啊?
我要配置含有硫酸盐0.1%的标准比浊液,该如何配置?用什么来配?
科里有六支硫酸盐单标的标准样品,是为了计量认证练习而在环保部标样研究所买的,以前都是使用无机盐ABC混合标样的。前段,同事想做下这个项目的练习,刚一加了指示剂还没滴定就变颜色了,仔细看了一下说明书,原来只可以用比色法,这也怪我了,没仔细看说明书,在购买之前,没有问仔细,可是如果想生产这种单标的标准物质,为什么不能多考虑一下呢,因为某种项目的分析方法并不只有一种啊。
亚硫酸盐 (Sulfites或SulfitingAgents)为使用多年之合法食品添加物,不仅是非常有效的酵素抑制剂、漂白剂、抗氧化剂、还原剂及防腐剂,且价格便宜。亚硫酸盐最早被使用之纪录是在罗马帝国时代,当时是被用於葡萄酒容器之消毒杀菌。此外,许多食品均含有天然存在之亚硫酸盐,尤其是在各种醱酵食品中。亚硫酸盐具有杀菌功效及强还原力,可将食品的著色物还原漂白,并可抑制氧化作用,防止酵素与非酵素褐变反应。合法添加於食品之亚硫酸盐包括:亚硫酸钠 (Sodium Sulfite,Na2SO3)、亚硫酸钾 (Potassium Sulfite, K2SO3)、亚硫酸氢钠 (Sodium Bisulfite,NaHSO3)、亚硫酸氢钾 (Potassium Bisulfite, KHSO3)、偏重亚硫酸氢钠 (SodiumMetabisulfite, Na2S2O5)、偏重亚硫酸氢钾 (Potassium Metabisulfite, K2S2O5)、低亚硫酸钠(Sodium Hydrosulfite,Na2S2O4)。亚硫酸盐广泛使用於脱水蔬菜、脱水水果、动物胶、糖蜜、糖飴、糖渍果实、虾类、贝类、水果酒、淀粉等產品中,常见市售添加亚硫酸盐的產品则包括:金枣、凤梨乾、脱水香蕉、葡萄乾、杏乾、柿饼、脱水金针、洋菇、笋乾、榨菜、绿豆芽、枸杞等。
硫酸盐检测方法详解 硫酸盐在地壳中是一种丰富的组份,由于石膏、硫酸钠及某些页岩的溶出,使水中含量 甚高。硫化矿经氧化使矿山排水含硫酸盐很高,含硫有机物及排放工业废水均为硫酸盐的 来源,天然水中的浓度可由数mg/L至数千mg/L。水中的亚硫酸盐可氧化为硫酸盐,而硫酸 盐在缺氧的条件下可还原为硫化物。 饮用水中硫酸盐浓度过高,易使锅炉和热水器结垢,产生不良的水味。当硫酸盐浓度为 300-400mg/L时,多数饮用者开始察觉有味。在有镁离子或钠离子存在时,硫酸盐超过 250mg/L时有轻泻作用。根据饮用者味觉的敏感度,味觉阈为300~1000mg/L。WHO基于 味觉的考虑,饮水中硫酸盐控制浓度为400mg/L。 测定硫酸盐的方法有称量法、EDTA容量法、硫酸钡比浊法、硫酸苯肼法、亚甲蓝比色法、 络合比色法、甲基麝香草酚蓝自动比色法、难溶性钡盐比色法、[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]间接法及[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url] 法等。称量法为经典方法,手续繁琐且不能测定浓度低于lOmg/L的硫酸盐,目前在常规分 析中已较少应用。硫酸钡比浊法可测40mg/L以下的硫酸盐,但反应条件苛刻,近年来对加 入试剂的方式加以改进,获得较好精密度。[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法是目前测定硫酸盐较好的方法,但设 备较昂贵,尚不能在基层水质分析室推广使用。难溶性钡盐比色法,属于这类方法的有铬酸 钡比色法、钼酸钡法、二羟甲苯醌(DHTQ)钡比色法及四氯化醌酸钡比色法。我国幅员辽阔, 各地天然水中所含硫酸盐浓度差别很大,可由数mg/L至数百mg/L,因此所选用的分析方法 应能满足多种情况的需要。 水样保存:ISO规定,硫酸盐水样在冷藏条件下可稳定7~28天。北京市卫生防疫站把 自来水及清洁地面水在4℃及30℃下保存37天,硫酸盐浓度并无明显变化,在冷藏条件所 得结果与ISO基本一致,见表17.1。 1.5.2过滤:在水质分析中,常用滤纸、玻璃砂芯滤器、古氏坩埚等过滤水样。 (1)滤纸分为定性滤纸与定量滤纸,用棉花等纤维制成。常用的有直径为5.5,7,9,12.5 及15cm等规格。 ①定性滤纸:定性滤纸含硅、铁、铅等杂质,灼烧后灰分多,供一般过滤用,不能用于常规 定量分析及微量金属分析。常用的定性滤纸分快速、中速及慢速三种。 ②定量滤纸:分为单洗及双洗两种。单洗定量滤纸已经过盐酸处理,除去铁及无机盐等 杂质,但灼烧后灰分仍较高,不适合精密分析用。双洗定量滤纸是用盐酸和氢氟酸处理过 的,除去了硅酸盐、金属等杂质,并用纯水洗净。每一小张滤纸灼烧后,灰分一般0.01mg,但因厂牌、批号不同,铅、铁等杂质的含量也有差异,用于测定微量金属,使用前还需用稀盐 酸、稀硝酸及纯水依次洗涤。定量滤纸分快速、中速、慢速三种;过去称为白带、蓝带与红带, 孔径分别为80-120,30-50和1~3μm。 滤纸的选择应根据沉淀粒度而定。过滤细微沉淀(如硫酸钡)不能用孔径大的滤纸,大 颗粒沉淀亦不能用慢速滤纸。选择滤纸大小系根据沉淀量而不依溶液体积多少,沉淀的体 积不能超过滤液容积的一半。如溶液体积大而沉淀又少时要用小滤纸。对微量分析尽可能 用较小的滤纸,以减少由滤纸沾污而引起的误差。 根据滤纸的大小选择合适的漏斗,放入的滤纸应比漏斗边缘约低1cm,不容许高出漏 斗,以免因张力作用,使沉淀溢出漏斗而损失。折叠滤纸时应避免沾污滤纸,这对微量分析 更为重要。强酸或强碱溶液不能用滤纸过滤。
想问下饮用水的硫酸盐做曲线的时候应该注意一些什么,我做出来的硫酸盐不成曲线,试剂和标准溶液都是从新配置的,求回复
二氧化硫的问题用GB/T 5009.34中蒸馏法测定食品中亚硫酸盐时,蒸馏过程中有的食品会产生大量的泡沫,请问用什么消泡剂可以消除?