最近做食品中维生素B1的检测,依据GB5009.84-2016,高效液相,按要求配制的一系列浓度的标准液,竟然会有过载的现象,各个浓度峰面积也大概高了一倍,不知道是怎么回事,请有经验的专家帮忙解答就下3.3 标准品维生素B1 标准品:盐酸硫胺素(C12H17ClN4OSHCl)),CAS:67-03-8,纯度≥99.0%。3.4 标准溶液配制3.4.1 维生素B1 标准储备液(500μg/mL):准确称取经五氧化二磷或者氯化钙干燥24h的盐酸硫胺素标准品56.1mg(精确至0.1mg),相当于50mg硫胺素、用0.01mol/L盐酸溶液溶解并定容至100mL,摇匀。置于0℃~4℃冰箱中,保存期为3个月。3.4.2 维生素B1 标准中间液(10.0μg/mL):准确移取2.00 mL 标准储备液,用水稀释并定容至100mL,摇匀。临用前配制。3.4.3 维生素B1 标准系列工作液:吸取维生素B1 标准中间液0μL、50.0μL、100μL、200μL、400μL,800μL,1000μL,用水定容至10mL,标准系列工作液中维生素B1 的浓度分别为0μg/mL,0.0500μg/mL,0.100μg/mL,0.200μg/mL,0.400μg/mL,0.800μg/mL,1.00μg/mL。临用时配制。
维生素B1是维生素中发现最早的一种。由嘧啶环和噻唑环通过亚甲基结合而成的一种B族维生素。为白色结晶或结晶性粉末;有微弱的特臭,味苦,有引湿性,露置在空气中,易吸收水分。在碱性溶液中容易分解变质。酸碱度在3.5时可耐100℃高温,酸碱大于5时易失效。遇光和热效价下降。故应置于遮光,凉处保存,不宜久贮。 在酸性溶液中很稳定,在碱性溶液中不稳定,易被氧化和受热破坏。还原性物质亚硫酸盐、二氧化硫等能使维生素B1失活。(摘自百度百科) 购买回的维生素B1(盐酸硫胺)纯度标准物质(BW3600,中国计量科学研究所)给出的均匀性检验和稳定性考察的前处理条件是105℃干燥至恒重后称取一定量,加入盐酸水溶液溶解,过滤上机测定。而在GB/T 14700-2002《饲料中维生素B1的测定》标准(本法用的反相HPLC)中,标准储备液是称取一定量,用25%乙醇溶液超声溶解。在GB/T5009.84-2003《食品中硫胺素(维生素B1)的测定》标准中,称取经氯化钙干燥24h的一定量硫胺素,溶于0.01mol/L中。在中国兽药典、中国药典中,维生素B1用的是约0.1mol/L盐酸溶液溶解,而其中检验干燥失重时,用的也是105℃。 疑问:根据第一段说法,VB1并不耐热,为何要用105℃? GB/T 14700-2002中用乙醇溶液溶解,储备液能保证稳定,不选用盐酸溶液,是否更便于HPLC测试?
最近准备做维生素A,GB5009.82-2016中在标准溶液配制和分析结果表述中都是用维生素A表述的,分别用“准确称取25.0mg维生素A标准品”“X——试样中维生素A的含量,维生素A单位为微克每百克(μg/100g)”表述;我们买的标品是维生素A醋酸酯;我们的检验报告单又以“维生素A(以视黄醇计)”体现。我查到1IU维生素A=0.3μgRE 1IU维生素A=0.344μg维生素A醋酸酯等换算关系,但在实验过程中究竟该如何处理这些关系了,比如要准确称取25.0mg的维生素A标准品,那我该称多少的维生素A醋酸酯;维生素A醋酸酯需不需要皂化;维生素A又称视黄醇,那检验报告单中维生素A(以视黄醇计)作何理解,视黄醇和视黄醇当量有何异同;标准品和对照品有何异同等。拜托吧里大神赐教啊,万分感谢
维生素B1(硫胺硝酸盐) 标准品CDCT-C17455500 CAS 532-43-4 纯品型,有证书,0.25g价格 360RMB因有效期将近,03/2014,现5折清仓,库存有限,可直接回复联系我,也可联系安谱总部 021-54890099
要做维生素A,文献说要甲醇溶解标准品,可惜根本不容,谁做过,帮忙下,怎么溶解。用液相做
我们要开展婴幼儿乳制品中维生素类的测定,维生素A的标准好象有好几种,好象有维生素A乙酸酯、维生素A酸等等,请哪位高手给点意见,具体应该买哪种?
根据GB 5413.9-2010中附录A的方法校正维生素D的浓度,用乙醇来溶解,但是没有颜色显示,我用1000ug/ml和10ug/ml的标准储备液测出来的吸光度值差不多,是不是还应该有步骤啊?请专家帮忙指正。
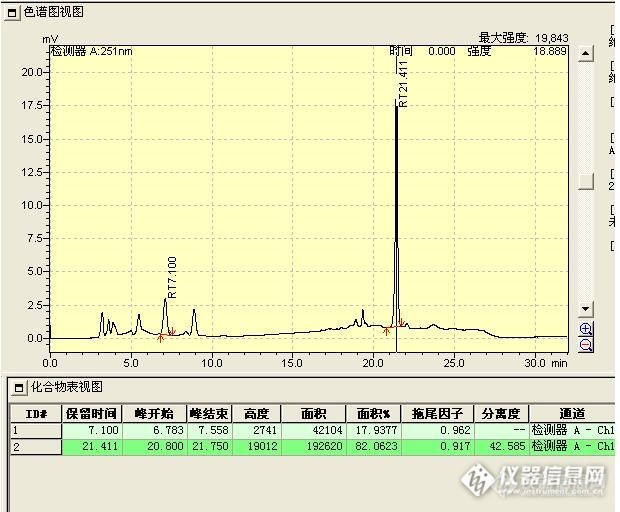
前段时间拿到一个饲料样品,要检测饲料中维生素A和维生素K3,看标准两者用的流动相都是甲醇-水,第一反映就是不是可以梯度洗脱同时测定两个成分,采用定时变换检测波长的方法实现检测。结果很失败,在此分享一下分析过程。 先看标准方法: GB/T 17817-2010 饲料中维生素A的测定 高效液相色谱法[img=,682,136]http://ng1.17img.cn/bbsfiles/images/2017/09/201709292030_01_1638724_3.png[/img][img=,690,336]http://ng1.17img.cn/bbsfiles/images/2017/09/201709292030_02_1638724_3.png[/img] GB/T 7294-2009 饲料添加剂亚硫酸氢钠甲萘醌(维生素K3)[img=,690,506]http://ng1.17img.cn/bbsfiles/images/2017/09/201709292024_01_1638724_3.png[/img] GB/T 18872-2002 饲料中维生素K3的测定 高效液相色谱法 维生素K3的检测原理是在碱性条件下,水溶性的亚硫酸氢钠甲萘醌脱去亚硫酸氢钠生成脂溶性的甲萘醌,用三氯甲烷萃取,吸取适量经甲醇稀释后上机检测。[img=,680,508]http://ng1.17img.cn/bbsfiles/images/2017/09/201709292025_01_1638724_3.png[/img]一、第一次实验:按标准维生素K3的提取过程太麻烦了,且三氯甲烷并不是随便可以买到,那能不能像维生素A一样直接甲醇提取后检测?1、查维生素K3(亚硫酸氢钠甲萘醌)理化特性:易溶于水和热乙醇,难溶于冰乙醇,不溶于苯和乙醚,水溶液PH4.7-7.常温下稳定,遇光易分解。看下面的结构式:[img=,247,199]http://ng1.17img.cn/bbsfiles/images/2017/09/201709292009_01_1638724_3.png[/img]看性质肯定可以溶解在90%甲醇-水里,取亚硫酸氢钠甲萘醌适量,在棕色容量瓶中90%甲醇溶解后上机检测。2、结果出峰极快,受亚硫酸根强极性基团的影响,维生素K3在反相色谱上完全不保留且峰形很差,说明不能直接提取后上机检测,第一次以失败告终。[img]http://ng1.17img.cn/bbsfiles/images/2017/09/201709081927_01_1638724_3.jpg[/img]二、第二次实验:老实的按标准方法(GB/T 18872-2002 饲料中维生素K3的测定 高效液相色谱法)?显然不好,还是不能同时测定维生素A和维生素K3,能不能碱性条件下脱亚硫酸氢钠后纯甲醇提取后上机检测呢?1、由于维生素A的提取方法是65度纯甲醇超声提取30分钟,那么就先取适量维生素A和维生素K3置100mL棕色容量瓶中,由于手上没有氢氧化铵,所以加入5mL碳酸钠溶液代替,加入后超声振摇1min,即有白色沉淀析出(可能是碳酸钠与甲萘醌的混合物),立即加入80mL甲醇,65度超声提取30分钟,过滤取,取滤液稀释至合适浓度上机检测。2、结果几乎无甲萘醌峰出现,观察提取液的颜色,基本可以确定是甲萘醌都氧化成了[color=#cc0000]羟基苯醌[/color]。如下呈褐色的滤液。第二次失败。[img=,602,337]http://ng1.17img.cn/bbsfiles/images/2017/09/201709292059_01_1638724_3.png[/img] 还有一个原因是用甲醇提取与用三氯甲烷提取有明显的区别,是甲醇与碳酸钠溶液是有一定互溶性的,而三氯甲烷与碳酸钠溶液不互溶。甲醇的碳酸钠溶液可能也会促进甲萘醌的破坏。三、第三次实验1、实验方法:维生素A与维生素K3分别按标准方法提取,再吸取甲萘醌的三氯甲烷溶液适量置提取好的维生素A提取液中,混匀,上机检测,梯度洗脱程序如下:[img=,509,384]http://ng1.17img.cn/bbsfiles/images/2017/09/201709292142_01_1638724_3.png[/img]2、结果甲萘醌与维生素A可以实现分离与同时检测,但每针的分析时间太长,与分别单独检测维生素A与维生素K3,每针分析时间只要10分钟相比,没有优势,如果还要同时分析维生素D与维生素E的话,分析时间就会更长,另外也有可能存在提取维生素A时有少量甲萘醌生成,造成结果偏高的误差。其它实验证明维生素A、D、E可能在98%甲醇下同时分析。至此,第三次实验也算失败。[img=,620,512]http://ng1.17img.cn/bbsfiles/images/2017/09/201709300842_01_1638724_3.jpg[/img] 维生素K3(7.1min)与维生素A(21.4min)同时检测图谱[img=,581,500]http://ng1.17img.cn/bbsfiles/images/2017/09/201709300842_02_1638724_3.jpg[/img] 维生素A样品图谱(98%甲醇等度洗脱)[img=,588,492]http://ng1.17img.cn/bbsfiles/images/2017/09/201709300842_03_1638724_3.jpg[/img] 维生素K3样品图谱(80%甲醇等度洗脱) 综上,本次最终还是选择按标准方法分别检测维生素A与维生素K3,在检测维生素K3由标准方法的旋转振荡器改为普通摇床振荡。这次的经验告诉我,要改进方法真的不容易,进行方法开发前一定要充分了解待测组分的理化性质,充分理解参考文献的检测原理与注意事项。看到亚硫酸根有没有人会考虑使用离子对试剂四丁基氢氧化铵和四丁基溴化铵的,估计也是不行的,碱性条件下会水解。
常常看到一个小小的维生素E标准品,竟然有好多相关标准品,如维生素E/生育酚、α-维生素E、β-维生素E、γ-维生素E和δ-维生素E、维生素E乙酸酯、维生素E棕榈酸酯、维生素E琥珀酸酯、DL-α-维生素E 标准品、DL-α-维生素E醋酸酯 标准品,太多了,我要做食品里面的维生素E的含量检测,到底要选哪个是合适的?http://simg.instrument.com.cn/bbs/images/brow/em09506.gif
维生素C是一种已糖醛基酸,有抗坏血病的作用,所以被人们称做抗坏血酸,主要为还原型及脱氢型两种,广泛存在于植物组织中,新鲜的水果、蔬菜,特别是枣、辣椒、苦瓜、柿子叶、猕猴桃、柑橘等食品中含量较多。它是氧化还原酶之一,本身易被氧化,但在有些条件下又是一种抗氧化剂。维生素C(还原型)纯品为白色无臭结晶,熔点190~192℃,溶于水或乙醇中,不溶于油剂。在水溶液中易被氧化,在碱性条件下易分解,在弱酸条件中较稳定,维生素C开始氧化为脱氢型抗坏血酸(有生理作用)。如果进一步水解则生成2,3-二酮古乐糖酸,失去生理作用。根据它具有的还原性质可以测定维生素C的含量。常用的测定方法有(1)2,6-二氯靛酚法 (还原型VC)(2)2,4-二硝基苯肼法 (总VC)(3)碘酸法(4)碘量法(5)荧光分光光度法一、2,6-二氯靛酚滴定法1、原理:还原型抗坏血酸还原染料2,6-二氯靛酚,该染料在酸性中呈红色,被还原后红色消失。还原型抗坏血酸还原2,6-二氯靛酚后,本身被氧化成脱氢抗坏血酸。在没有杂质干扰时,一定量的样品提取液还原标准2,6-二氯靛酚的量与样品中所含维生素C的量成正比。2、试剂⑴ 1%草酸溶液:称取10g草酸,加水至1000ml;⑵ 2%草酸溶液:称20g草酸,加水至1000ml;⑶ 维生素C标准液:准确称20mgVC溶于1%草酸中,并稀释至100ml,吸5ml于50ml容量瓶中,加入1%草酸至刻度,此溶液每毫升含有0.02mgVC;⑷ 0.02%2,6-二氯靛酚溶液:称取2,6-二氯靛酚50mg,溶于200ml含有52mg碳酸氢钠的热水中,冷却后,稀释至250ml,过滤于棕色瓶中,贮存于冰箱内,应用过程中每星期标定一次。[font=宋
[size=5]超临界流体色谱同时测定维生素B2,B3和烟酰胺来源: 作者:郭亚东 摘要:采用超临界流体色谱同时定量测定维生素制剂中维生素B2(核黄素)、维生素B3(烟酸)和烟酰胺的含量。在CO2流动相中添加15%(体积分数)的甲醇(含0.1%二乙胺),于填充柱上分离,检测波长为268nm。上述3种维生素在测定范围内,其浓度与相应的峰面积呈良好的线性关系(r0.999),平均回收率为97.3%~102.3%;5 min即可完成分析。其日内和日间峰面积测定的相对标准偏差(RSD)小于1.5%。该方法简便,样品前处理简单,可用于上述3种维生素的快速分析。关键词:超临界流体色谱;核黄素;烟酸;烟酰胺;维生素制剂水溶性维生素对人们的生长发育和健康有着重要作用。人们除了从水果和蔬菜中摄取外,还从添加了维生素的食品和复合维生素制剂中补充人体的需要,因此有必要建立快速、稳定的分析方法用于其含量的测定。对维生素制剂中维生素B2(核黄素)、维生素B3(烟酸)和烟酰胺测定的方法主要是高效液相色谱法。采用该方法虽可取得较好的结果,但其分析时间长,样品前处理麻烦。毛细管电泳、胶束电动毛细管电泳等方法也可用于其含量测定。本文建立了用超临界流体色谱同时测定这3种维生素的方法,该方法样品前处理简单、分析时间短、分离好,结果令人满意。1 实验部分1.1 仪器与试药超临界流体色谱仪:Gilson Model SF3系统(英国)。核黄素和烟酰胺对照品购自Lancaster化学公司(英国),烟酸购自Acros公司(英国),甲醇为高效液相色谱纯,二乙胺为分析纯,CO2为超临界流体色谱纯。1.2 色谱条件色谱柱:Cyano(5μm,4.6mm i.d.×250mm,英国);柱温:50℃;紫外检测器配有高压检测池,其检测波长为268nm;进样装置:带有10μL进样阀的自动进样器;流动相操作压力:20MPa。2 结果与讨论2.1 流动相组成对分离的影响只用CO2或者CO2加甲醇作流动相时,这3种维生素不能完全分开;当在甲醇中加入少量二乙胺后,其分离情况得到大大改善。表给出了当流动相的流速一定,在CO2中分别添加10%和15%(均为体积分数)的甲醇,并在这两种体积分数下的甲醇中各分别添加0.1%和0.5%(均为体积分数)的二乙胺时上述3种维生素的保留时间,可见流动相中甲醇和二乙胺的含量对保留时间的影响很大。本文将l5%的甲醇(含有0.1%的二乙胺)添加到CO2中作流动相,可使3种维生素的同时分析在短时间内完成,分离结果令人满意。2.2 流动相流速对分离的影响当流动相组成为CO2加l5% 的甲醇(含有0.1% 的二乙胺)时,将流动相流速从2.0 mL/min提高到3.0 mL/min,对这3种维生素的色谱峰形和分离情况都没有太大的影响,最后出峰的维生素B2的保留时间仅从5.11min降为3.37min。本文采用2.5mL/min的流速进行分析。[/size]
那儿有a β γ δ维生素E和三烯酚的标准买啊?E
维生素B6测定中吡哆辛(吡哆醇),吡哆醛,吡哆胺三种混标进样后,就出现了一个 吡哆胺的峰,其他两个的峰,不知道是为什么?我单个的标准品也进了就是那个两个没有峰,请帮助我分析一下原因?
按国标方法标定维生素A、D、E的标准溶液时,标定结果总是不稳定,即使是新配的标准溶液也一样,大家有没有遇到同样的情况,请高手指点指点!
[align=center][b]BP 2015方法|复合维生素注射液的定量分析(1)[/b][/align][align=right][b]——维生素B1、维生素B6及烟酰胺的分析[/b][/align][align=right][/align][align=center][b][color=#FFD500]复合维生素注射液[/color][/b][/align][color=#3E3E3E] [/color][color=#3E3E3E]用于营养不良及因缺乏维生素B类所引起疾患的辅助治疗,如厌食、脚气病、糙皮病等。[/color][color=#3E3E3E] [/color][b][color=#FFD500]维生素B1[/color][/b][color=#3E3E3E]又称硫胺素,是碳水化合物代谢所需辅酶的重要组成成分。[/color][b][color=#FFD500]维生素B6[/color][/b][color=#3E3E3E]为多种酶的辅基,参与氨基酸及脂肪的代谢。[/color][b][color=#FFD500]烟酰胺[/color][/b][color=#3E3E3E]为辅酶[/color][color=#3E3E3E]Ⅰ[/color][color=#3E3E3E]及[/color][color=#3E3E3E]Ⅱ[/color][color=#3E3E3E]的组分,为脂质代谢、组织呼吸的氧化作用和糖原分解所必需。[/color][b][color=#FFD500]右泛醇[/color][/b][color=#3E3E3E](D-泛醇)又称原维生素B5,进入人体内能转化为泛酸,进而合成辅酶A,促进人体蛋白质、脂肪、糖类的代谢,保护皮肤和粘膜,改善毛发光泽,防止疾病的发生。[/color][color=#3E3E3E] [/color][color=#A0A0A0](以上列出组分为配方中部分成分,本数据仅介绍前三种化合物的分析,下期将介绍右泛醇的分析数据)[/color]———————————————————————————————————————————————————————客户提供了复合维生素注射液样品及维生素B[sub]1[/sub]、维生素B[sub]6[/sub]和烟酰胺对照品溶液,并反馈在现有条件下使用C[sub]18[/sub]柱对注射液中维生素B[sub]1[/sub]、维生素B[sub]6[/sub]和烟酰胺进行定量分析时,[color=red]烟酰胺出现杂质干扰,无法准确定量。[/color]客户希望本实验室参考BP2015英国药典方法,筛选合适的色谱柱对复合维生素注射液中的维生素B[sub]1[/sub]、维生素B[sub]6[/sub]和烟酰胺进行定量分析。[img=,670,223]http://ng1.17img.cn/bbsfiles/images/2018/06/201806281004332417_4281_2222981_3.png!w670x223.jpg[/img]依据BP 2015方法,流动相中添加了二乙胺和庚烷磺酸钠,本实验室分别尝试了中等极性的CAPCELL PAK C[sub]18[/sub] MGII、高极性的CAPCELL PAK C[sub]18[/sub] AQ、高碳载量的SUPERIOREX ODS以及低极性的CAPCELL PAK C[sub]18[/sub] UG120色谱柱分别对注射液样品进行分析。如图1,对几款柱子分析所得结果对比后发现,能在纯水相条件下稳定使用的高极性色谱柱[color=#ff0000][b]CAPCELL PAK C[sub]18[/sub] AQ[/b][/color]所得分离效果最佳,其中,[color=#0070C0]烟酰胺与前后杂质分离度在[/color][b][color=#0070C0]0.9[/color][/b][color=#0070C0]以上[/color],满足BP方法中不低于[b]0.8[/b]的分离度要求。[align=center][img=,540,396]http://ng1.17img.cn/bbsfiles/images/2018/06/201806281005340074_3856_2222981_3.png!w540x396.jpg[/img][/align][align=center]图1 CAPCELL PAK C[sub]18[/sub] AQ色谱柱分析所得结果[/align]注:峰上标数字为分离度,下同。[img=,544,239]http://ng1.17img.cn/bbsfiles/images/2018/06/201806281006125064_2880_2222981_3.png!w544x239.jpg[/img]就该结果与客户沟通,客户希望对液相条件进行适当调整,[color=red]在满足英国药典要求的基础上,进一步实现烟酰胺与其前后杂质之间的基线分离。[/color]首先,我们考察柱温对分离的影响——分别在30°C、35°C、40°C柱温条件下考察分离效果,发现仍在原条件,即30°C条件下分离效果最佳;进一步,尝试调整流动相中有机相的比例,将原条件中各10%的甲醇和乙腈均降低至6%,如图2,[color=#ff0000]烟酰胺与其先后杂质峰之间分离度均在1.70以上,能够得到基线分离的良好结果。[/color][color=#ff0000][/color][align=center][color=#ff0000][img=,555,408]http://ng1.17img.cn/bbsfiles/images/2018/06/201806281006565267_3403_2222981_3.png!w555x408.jpg[/img][/color][/align][align=center]图2 CAPCELL PAK C[sub]18[/sub] AQ色谱柱分析所得结果(调整条件)[/align][align=center][img=,534,371]http://ng1.17img.cn/bbsfiles/images/2018/06/201806281007412274_7213_2222981_3.png!w534x371.jpg[/img][/align][align=center]图3 CAPCELL PAK C[sub]18[/sub] AQ色谱柱分析所得结果(调整条件)局部放大图[/align][img=,546,244]http://ng1.17img.cn/bbsfiles/images/2018/06/201806281007256127_6260_2222981_3.png!w546x244.jpg[/img]综上实验结果,使用能在纯水相条件下稳定使用的高极性色谱柱[b][color=red]CAPCELL PAK C[sub]18[/sub] AQ[/color][/b] S5 4.6 mm i.d. × 250 mm,依据BP 2015英国药典方法,通过调整流动相中有机相比例,能够实现复合维生素注射液中维生素B[sub]1[/sub]、维生素B[sub]6[/sub]和烟酰胺及杂质的良好分离及准确定量分析。[align=right] [/align][align=right][/align][align=right] [/align][align=right]三耀精细化工品销售(中国)有限公司技术开发部[/align][align=right]地址:北京经济技术开发区宏达南路5号宏达利德工业园1栋418室[/align][align=right]邮编:100176[/align]
哪位大侠有国外检测维生素(主要是B族维生素)的标准的麻烦传个上来,小弟急用
维生素C能增加“好”胆固醇的水平,促进胆固醇代谢,并可抑制胆固醇合成酶的活性,降低胆固醇合成速率,从而达到控制血脂的目的。新鲜果蔬富含维生素C,比如猕猴桃、鲜枣、青椒、绿叶菜等。
检测VB1,根据5413.11-2010,标准品称相当于硫胺素50mg,我们用的标准品是硝酸硫铵(分子量327.37)或盐酸硫铵。硫胺素的分子量是300.81,换算系数应该是327.37/300.81=1.088,在网上查的换算系数是:1mg硫胺素=1.3379mg维生素B1盐酸盐,1mg硫胺素=1.2336mg维生素B1硝酸盐。我该用哪个呢?谢谢了!
维生素的标准谱图,不知道哪里有???
请问测试维生素K1有什么标准?
如题,求液相维生素A标准品的配制方法

10,抽取5个版友);中奖名单:999youran(注册ID:999youran)mengzhaocheng(注册ID:mengzhaocheng)m3071659(注册ID:m3071659)莫名其妙(注册ID:moyueqiu)dyd3183621(注册ID:dyd3183621)http://ng1.17img.cn/bbsfiles/images/2016/05/201605061502_592486_1610895_3.pnghttp://ng1.17img.cn/bbsfiles/images/2016/05/201605061502_592487_1610895_3.png积分奖励:所有回答正确的版友奖励10个积分(幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================水溶性维生素方法:HPLC基质:标准溶液应用编号:101062化合物:吡哆胺;乳清酸;维生素C;吡哆醛;吡哆醇;烟酰胺固定相:Diamonsil C18(2)色谱柱/前处理小柱:Diamonsil C18(2) 5u 150 x 4.6mm色谱条件:流动相: 甲醇:10 mM HCOONH4(pH=3.0)= 5:95 流速: 1.0 mL/min 温度: 室温 检测器: UV 254 nm文章出处:AN: D1109关键字:水溶性维生素,HPLC,吡哆胺;乳清酸;维生素C;吡哆醛;吡哆醇;烟酰胺,Diamonsil C18(2),钻石二代谱图:http://ng1.17img.cn/bbsfiles/images/2016/05/201605061009_592439_1610895_3.jpg图例:1. 吡哆胺; 2. 乳清酸; 3. 维生素C; 4. 吡哆醛; 5. 吡哆醇; 6. 烟酰胺
谁有维生素A、D、E标准溶液标定特别精准的方法,指点下吧。。。。
在检测纯牛奶中维生素B6时,依据GB 5009.154-2016 《食品安全国家标准 食品中维生素B6的测定》测定纯牛奶中维生素B6,仪器条件中流动相为甲醇50ml,辛烷磺酸钠2g、三乙胺2.5ml,用水定容到1000ml后,用冰乙酸调pH至3.0±0.1。色谱柱为C18,250mm*4.6mm,5μm,检测波长:激发波长293nm,发射波长395nm,流速:1.0ml/min,进样体积:10μl,柱温:30℃。检测图谱如下:[img=,553,170]https://ng1.17img.cn/bbsfiles/images/2024/03/202403181704021615_4430_2888412_3.png[/img]只有吡哆醇和吡哆醛有目标峰,吡哆胺没有出峰,第一感觉就是分析时间短,样品没走完,于是将检测时间延长至45min时,吡哆胺仍无目标峰。首先检查一下仪器方法的参数设置没有问题,然后重新处理了样品,再次上机,查看结果,还是不行。难道是仪器的问题吗?于是换了个项目上机测试,出峰正常。然后又换回去,再次测试还是不出峰。哎,换个柱子试试吧。可是换完柱子依旧没有出峰。最后只能拿到另一台仪器上机检测了,让人崩溃的是,没有出峰…这下就比较头疼了,看来方法有点问题啊,需要改变一下。为了调试方便,决定将国标中给定的流动相中甲醇单独分开,流动相为A和B,A为辛烷磺酸钠2g、三乙胺2.5ml,用水定容到1000ml后,用冰乙酸调pH至3.0±0.1,B为纯甲醇。上机测试,终于出峰了,但是峰型不是太好。不过没关系,出峰总比不出好。继续寻找合适的流动相比例,调整A和B的比例,反复测试,最终确定流动相比例为A:B=80:20,吡哆醇、吡哆醛和吡哆胺目标峰均出峰。[img=,554,216]https://ng1.17img.cn/bbsfiles/images/2024/03/202403181704020362_8441_2888412_3.png[/img]看来平时要多注意一下流动相这个问题了!哈罗德科技团队
维生素B是某些维生素的总称,是一个庞大的维生素家族,它们常常来自于相同的食物来源,如酵母等。它包含十几类,下面就简单的介绍一下人体所需几种维生素B。一) 维生素B1它是水溶性维生素。和所有 B 族维生素一样,多余的 B1 不会贮藏于体内,而会完全排出体外。所以,必须每天补充。生理功能: 维生素B1的需要量与机体热能总摄入量成正比,故维生素B1的供给量以每4.2MJ(1000kcal)热能供给多少来表示,据此,我国的推荐维生素B1供给量为0.5mg/4.2MJ。 食物来源:二) 维生素B2它是在自然界分布广泛的一种维生素。是哺乳动物必需的营养物。生理功能:①促进发育和细胞的再生。②促使皮肤、指甲、毛发的正常生长。③帮助消除口腔内、唇、舌的炎症。④增进视力,减轻眼睛的疲劳。⑤和其他的物质相互作用来帮助碳水化合物、脂肪、蛋白质的代谢。食物来源:成年人每日吃1两动物肝或 2斤黄豆或3棵生菜或3-4只香菇即可满足需要。三) 维生素B3生理功能:它的效用是促进消化系统的健康,减轻胃肠障碍;使皮肤更健康;预防和缓解严重的偏头痛;促进血液循环,使血压下降;减轻腹泻现象。四) 维生素B5 一种水溶性B族维生素,由2,4-二羟基-3,3-二甲基丁酸与β-丙氨酸用酰胺键连接构成。在动植物中广泛分布,故名泛酸。生理功能:1、制造及更新身体组织。2、帮助伤口愈合。3、制造抗体,抵抗传染病。4、防止疲劳,帮助抗压。5、缓和多种抗生素副作用及毒素。6、舒缓恶心症状。食物来源:牛奶、豆浆。工作压力较大及闷闷不乐的人应该尝试多食用,它有助于心情愉悦。五) 维生素B6 维生素B6(Vitamin B6)又称吡哆素。是一种水溶性维生素,遇光或碱易破坏,不耐高温。生理功能:维生素b6是人体脂肪和糖代谢的必需物质,女性的雌激素代谢也需要维生素b6,因此它对防治某些妇科病大有益处。许多女性会因服用避孕药导致情绪悲观、脾气急躁、自感乏力等,每日补充60毫克就可以缓解症状。还有些妇女患有经前期紧张综合征,表现为月经前眼睑、手足浮肿、失眠、健忘,每日吃50~100毫克维生素b6后症状可完全缓解。食物来源:富含b6的食物有金枪鱼、瘦牛排、鸡胸肉、香蕉、花生、牛肉等。在动物性及植物性食物中含量均微,酵母粉含量最多,米糠或白米含量亦不少,其次是来自于肉类、家禽、鱼,马铃薯、甜薯、蔬菜中。。 除此之外,维生素B7、B9、B12,以及维生素B族的胆碱和肌醇通常也归为人类必需维生素。[/font
在检测维生素E和维生素A时,遇到一个棘手的问题。标准品是膏状的,标示为不少于100mg/每瓶,为了配制标准工作液,是直接吸标准品称量配制,还是配制后标定,还是全部配制? 希望有这方面经验的老师,帮忙解答下。
一、保健食品中脂溶性维生素分析方法概况 保健食品中添加有维生素A、维生素D、维生素E、维生素K和b-胡萝卜素,一般情况下后两者使用相对较少 。鉴于脂溶性维生素的特点和样品基质情况,样品一般需要在皂化后经有机溶剂提取后测定。 1.维生素A 一般添加视黄醇醋酸酯和视黄醇棕榈酸酯两者之一或两种均添加。通常情况下成分复杂的样品需采用皂化反应后测定其中的视黄醇。成分相对简单的片剂和胶囊样品可采用溶剂提取直接测定视黄醇醋酸酯或视黄醇棕榈酸酯。奶粉等产品可以使用胰酶或蛋白酶处理,溶剂提取后测定视黄醇醋酸酯或视黄醇棕榈酸酯。 2.维生素E 一般情况下添加的是a-维生素E。成分相对简单的样品可采用溶剂提取直接测定。多数样品需要在皂化反应后测定其中的维生素E。 同时分析维生素E 4种结构并包括内标物,可使用如下正相柱: (1)Nucleosil-NH2 4.6×250mm, 5μm,正己烷:二恶烷=85:15,295nm (2)Zorbax SIL 4.6×250mm, 5μm,正己烷:二恶烷:异丙醇=985:10:5,295nm (3) Lichrosorb-NH2 4.0×250mm,5μm,正己烷:异丙醇=99:1,295nm (4) YMC-Pac A-600 (NH2),3μm,正己烷:异丙醇=98:2 Ex:290nm Em:325nm 3.维生素D 一般情况下添加的是维生素D2和维生素D3中之一。目前维生素D的分析尚不如维生素A和维生素E成熟,主要原因为含量低,前处理过程损失多,与维生素E较难分离。现在采取的方法是采用乙腈+甲醇+水=25+75+4作为流动相,根据样品中维生素D的情况,选择维生素D2和维生素D3互为内标。维生素D的分析对于色谱柱的要求较高,一般来讲250mm长度的Zobax SB-C18 比较适合分析要求。 4.b-胡萝卜素 b-胡萝卜素一般出现在植物性保健食品中,分析方法相对成熟。目前我们将维生素E、番茄红素和b-胡萝卜素通过采用不同的波长达到一次性分析的目的。样品采用二氯甲烷进行提取,分析过程需要加入抗氧化剂BHT对组分进行保护。 流动相为甲醇:乙腈=50:50 色谱柱:Supelcosil RP C18 5.α-胡萝卜素 α-胡萝卜素目前也出现在保健食品中已有应用,初步将其与b-胡萝卜素一同分析。样品采用丙酮进行提取。 流动相为甲醇:甲基叔丁基醚:水=310:76:14 色谱柱:Symmetry C18 检测波长:450nm 二.保健食品中水溶性维生素分析方法概况 目前建立并推广了一套的系统分析方法,通过选用多波长离子对高效液相色谱分析可以解决维生素B1、维生素B6、烟酸、烟酰胺、维生素C的分析。生物素、泛酸、叶酸需采用单独的高效液相色谱分析条件。维生素B2采用荧光分光光度法分析。 1.维生素B1(盐酸硫胺、硝酸硫胺) 分析维生素B1可采用盐酸苯海拉明作为内标。样品采用甲醇+水+磷酸提取。 流动相为硫酸月桂酯钠溶液(5g/530mL):乙腈:磷酸=530:470:0.4 色谱柱:m-Bondapak C18或TSK Gel-C18 检测波长:260nm 2.维生素B1(呋喃硫胺) 有报道,呋喃硫胺是维生素B1的活性结构,在韩国、日本等产品中使用呋喃硫胺与盐酸硫胺、硝酸硫胺的色谱行为有较大区别。 流动相为甲醇:水:乙酸:PigB6=450:530:20:20 色谱柱:m-Bondapak C18 检测波长:280nm 3.维生素B6(吡哆醇)、烟酸、烟酰胺 分析维生素B6、烟酸、烟酰胺可采用愈创木酚甘油醚作为内标。样品采用甲醇+水+磷酸提取。 流动相为1-癸烷磺酸钠溶液(1.22g/850mL):乙腈:磷酸=850:150:0.4 色谱柱:m-Bondapak C18或TSK Gel-C18 在维生素类保健食品中烟酸应用极少,基本上添加的均为烟酰胺。 检测波长:280nm 功能性饮料中添加的咖啡因和苯甲酸也可以同时检测。根据大量实验认为液体类样品应使用TSK Gel-C18,固体样品两者皆可。 4.维生素C 除颜色较深、含量较低、天然植物干制品外,一般样品中的维生素C均可以采用碘溶液滴定法进行测定。利用高效液相色谱法测定维生素C可利用维生素B6(吡哆醇)、烟酸、烟酰胺流动相体系,因维生素C色谱保留时间较短,可以将降低其中乙腈的比例至5%。提取溶剂尽可能使用水,以避免在前面出现倒峰影响定量结果的准确。 检测波长:254nm 5.维生素B2 有关维生素B2的色谱分析方法有报道,但在实际样品分析过程中因保留时间较短且与其它峰难以较好分离,故采用将其转化为光黄素后进行荧光分光光度法分析。 6.泛酸(维生素B3) 泛酸采用液相色谱分析法进行检测,样品用水提取即可。 流动相:0.02M磷酸二氢钾溶液:乙腈=95:5,pH=3.0 色谱柱: m- Bondapak C18 300mm 检测波长:200nm 7.生物素 生物素的分析正在初步摸索阶段,目前采用pH=3.5 0.25M磷酸盐缓冲溶液:甲醇=77:23的流动相,检测波长200nm。 目前的需要解决的问题是保留时间较长,大约在30min左右;此外灵敏度较低。 8.叶酸 叶酸一般使用弱碱性水溶液提取,为保证提取效果可以在50℃水浴中加热10min。 流动相:磷酸二氢钾缓冲溶液:甲醇=460:40,pH=6.0 色谱柱: m- Bondapak C18 300mm 检测波长:280nm 叶酸的研究方向:通过大量实际样品检测研究,发现在虫草等天然产物中存在与叶酸色谱保留时间完全一致的物质;不少样品中叶酸含量较低,拟采用固相萃取等技术作为前处理手段。 9.维生素B12 维生素B12的化学分析目前还是一个难题,对于含量较高,组成简单的原料和添加剂进行高效液相色笱单的原料和添加剂进行高效液相色失杂的多种维生素样品的分析方法正在摸索之中。 维生素B12的研究进展:虽然维生素B12有3个特征波长,但样品在不经处理的情况下也很难分析;在溶液中钴胺素很容易出现氰钴胺素、甲钴胺素、羟钴胺素等几种形式共存的现象。为避免出现上述问题,更好地去除样品中的干扰杂质并对样品中的维生素B12进行富集,目前采用加入表面活性物质、盐析、有机溶剂萃取等方法去除杂质,再通过固相萃取法进行富集的手段。 三、类维生素分析方法概况 1.肉碱(维生素BT) 肉碱若采用分光光度法检测比较繁杂,高效液相色谱法测定相对简单。利用高效液相色谱法测定肉碱同样利用维生素B6(吡哆醇)、烟酸、烟酰胺流动相体系,因肉碱色谱保留时间虽比维生素C长但相对仍较短,因此流动相可以同维生素C一样。提取溶剂尽可能使用水或pH=5~6的水,以避免在前面出现倒峰影响定量结果的准确。 检测波长:210nm 2.辅酶Q10 对于维生素类样品中辅酶Q10的检测采用液相色谱分析法。样品中辅酶Q10使用正己烷作为提取溶剂。 色谱柱:TSK Gel-C18 流动相:乙腈+四氢呋喃+水=55+40+5 检测波长:280nm 3.肌醇 对于维生素类样品中肌醇的检测建立了一套衍生化-气相色谱分析法。样品中肌醇经过提取,彻底去除水分后进行衍生化,正己烷提取后进行气相色谱分析。 衍生化试剂:三甲基氯硅烷:六甲基二硅氨烷:二甲基甲酰胺=1:2:8 色谱柱:BP-5弹性石英毛细管柱, 25m×0.32mm 色谱条件:载气 50mL/min 尾吹气 50 mL/min 氢气 40 mL/min 空气 500 mL/min 分流比 1:50 四、需要解决的问题及展望 1.解决样品前处理技术 (1)不少油性胶囊样品中加入了水溶性维生素,如何应用前处理手段解决提取、净化问题。 (2)对于含量较低的样品如何应用固相萃取等手段。 (3)对于目前原料微囊化制作技术如何应对。 2.解决色谱多组分分析技术 在目前现有的多组分分析技术的基础上,如何能将维生素B1并入维生素B6系列之中或创建新的流动相体系,再囊括维生素B2和叶酸等是今后研究的重要方面。 3. 解决分析过程快速化 在目前大量样品检测的基础上应归纳总结出样品前处理方法指南,确定样品组成和前处理方法之间的关系。
大家好,我是一名新手,正在做维生素A,D,E,图是跑出来了,但是不知道如何做标准曲线图,知道的说一下,提供一下方式方法,本人学习一下,谢谢,是通过表格还是在仪器软件上做,有做过的可以加微信交流一下:ycxzql1989.谢谢各位朋友了。
最近做维生素E,它的旋光度测定是这样的取维生素E胶丸的内容物适量(约相当于维生素E400mg),精密称定,置150mL具塞圆底烧瓶中,加无水乙醇25mL使溶解,加硫酸乙醇溶液(1 7)20mL,水浴回流3小时,放冷,用硫酸乙醇溶液(1 72)定量转移至200mL量瓶中并稀释至刻度,摇匀。精密量取100mL置分液漏斗中,加水200mL,用乙醚提取2次(75mL,25mL),合并乙醚液,加铁氰化钾氢氧化钠溶液50mL,振摇3分钟;取乙醚层,用水洗涤4次,每次50mL,弃去洗涤液,乙醚液经无水硫酸钠脱水后,置水浴中减压或在氮气流下蒸干至7~8mL时,停止加热,继续挥干乙醚,残渣立即加异辛烷溶解并定量转移至25mL量瓶中,加异辛烷稀释至刻度,照比旋度项小的方法测定,比旋度(按d-α-生育酚计)不得低于+24°(天然型)。那结果是用固体公式算的还是液体公式,如果是固体的话,c项应该是100ml所含的溶质,那这里却是定容到25ml,应该怎么换算!
如题,是用来做液相的标准曲线的,主要检测饲料里的维生素。有没有价个适中的推荐几个!!谢谢