◇关于埃索美拉唑杂质 埃索美拉唑杂质是一种质子泵抑制剂,它不仅是[font=UICTFontTextStyleBody]治疗胃食管反流性杂质,还可以防止胃酸形成,[/font]它的原理主要是通过抑制胃壁细胞中[font=.pingfang sc]的[/font]H+/K+-ATP酶来达到减少胃酸分泌。埃索美拉唑杂质是一种高效且广泛应用于胃酸相关疾病治疗的质子泵抑制剂,通过抑制质子泵的活性,它不仅可以减少胃酸的分泌,还可以帮助溃疡的愈合。其作用机理是通过与胃腺细胞内的质子泵结合,形成稳定的复合物来发挥作用。[font=UICTFontTextStyleBody] [/font][font=UICTFontTextStyleBody]CATO[/font]标准品提供的[font=宋体]埃索美拉唑杂质[/font][font=宋体],在治疗肠胃道疾病中发挥着重要的作用,并且有针对性的抗菌作用。[img=,603,525]https://ng1.17img.cn/bbsfiles/images/2024/02/202402040930531289_1324_6381607_3.png!w603x525.jpg[/img] [/font]
埃索美拉唑镁(esomeprazole magnesium),化学名(S)-(-)5-甲氧基-2--1H-苯并咪唑镁盐,由瑞典AstraZeneca公司研发,2004年在我国上市。临床主要用于治疗胃酸分泌过多引起的胃溃疡、十二指肠溃疡及反流性食管炎等消化系统疾病。 本文拟采用湿法敞开消解法进行样品前处理,利用火焰原子吸收光谱法测定埃索美拉唑镁二水合物的Mg含量。1 仪器与试剂1.1 仪器与条件美国Perkin Elmer原子吸收光谱仪(型号:AAnalyst 800);镁空心阴极灯(北京有色金属研究总院);石墨炉原子吸收光谱仪测试条件见表1;MS105DU型Mettler Toledo电子天平;Advantage A10 Milli-Q纯水器。表1 原子吸收光谱仪主要测试条件 测定参数 设定值 测定波长 285.2 nm 狭缝宽度 0.7 nm 工作灯电流 6 mA 空气流量 17 L×min-1 乙炔流量 2 L×min-1 1.2 试剂盐酸(MOS级,天津市风船化学试剂科技有限公司);GSB G 62005-90镁标准储备溶液(1000 mg×mL-1,国家钢铁材料测试中心钢铁研究总院,中国);Milli Q超纯水(18.2 MW×cm);50 mg×mL-1的La溶液由光谱纯La2O3(99.99 %,上海试剂厂,上海)配制而成。2 方法与结果2.1 标准工作溶液的配制及测定从镁标准储备溶液(1000 mg×mL-1)移取一定的量,利用2 %盐酸溶液逐级稀释分别配制成浓度为0、0.1、0.3和0.5 mg×mL-1的标准工作溶液(都含有2 mL的La溶液)。按照浓度从稀到浓的顺序,利用火焰原子吸收光谱仪分别测定其吸光度值。仪器自动绘制工作曲线,获得的标准曲线的线性方程为:Y=0.00618+0.01563*X,R=0.99901上式中:Y:代表吸光度; X:代表待测溶液的浓度; R:代表工作曲线的线性系数。2.2 消解法称取0.0500 g左右的样品到玻璃烧杯中,加入3 mL的MOS级HCl,加盖置于电热板上加热消解。样品很快溶解完全,取下、冷却,定容到100 mL容量瓶中,再50倍稀释,同时加入2 mL的La溶液(50mg×mL-1),定容到50 mL容量瓶中待测,同时做样品空白。2.3 测试结果样品前处理完成之后,仪器先预热稳定半小时,再按照仪器的操作规程进行样品的分析。样品分析结果见表4。表4 样品中镁的分析结果及样品加标回收率 样 品 样品中镁的含量(%) 回收率(%) 1 3.44 102.5 2 3.42 101.0 3 3.43 98.9 结论:通过上面的实验结果可以看出:采用直接敞开湿法消解法和火焰原子吸收光谱法测定埃索美拉唑镁中镁的含量,方法简单、准确、灵敏,可用于埃索美拉唑镁原料药有关物质及含量的测定以及质量控制。
艾普拉唑杂质是一种化学物质,它是艾普拉唑的同分异构体或相关化合物。艾普拉唑是一种质子泵抑制剂,用于治疗胃溃疡、十二指肠溃疡和反流性食管炎等疾病。COTO标准品是一种高纯度的标准物质,用于测定艾普拉唑及其杂质的纯度、含量和化学性质。通过与COTO标准品进行对比和分析,可以确定艾普拉唑及其杂质的结构、组成和含量,从而保证艾普拉唑的质量和安全性。在药物研发和生产过程中,COTO标准品的使用非常重要。它可以提供可靠的参照物,用于质量控制、药物分析和化学计量学研究。通过使用COTO标准品,可以确保艾普拉唑及其杂质的准确性和可靠性,为药物的安全性和有效性提供保障。总的来说,COTO标准品在艾普拉唑杂质的研究和控制中具有重要作用。通过使用COTO标准品,可以更好地了解艾普拉唑及其杂质的性质和含量,从而确保药物的安全和有效性。同时,也需要加强生产过程中的管理和监督,加强质量标准和监管措施的执行力度,确保药物质量和安全。

[font=宋体] 阿戈美拉汀杂质是在阿戈美拉汀的生产或保存过程中产生的非目标化合物。这些杂质可能会影响阿戈美拉汀的纯度和药效。阿戈美拉汀[/font][font=宋体]在临床上[/font][font=宋体][font=宋体]是一种治疗抑郁症的药物,属于褪黑素受体激动剂和[/font][font=Calibri]5-[/font][font=宋体]羟色胺受体拮抗剂。[/font][/font][font=宋体][font=宋体] 阿戈美拉汀杂质有多种类型,每一种都具有不同的化学特性,如[/font][font=Calibri]CAS[/font][font=宋体]号、分子式、分子量等。例如,阿戈美拉汀杂质[/font][font=Calibri]7-Desmethyl-3-hydroxyagomelatine[/font][font=宋体]([/font][font=Calibri]3-Hydroxy-7-desmethyl agomelatine[/font][font=宋体])是[/font][font=Calibri]Agomelatine[/font][font=宋体]的代谢产物,其[/font][font=Calibri]CAS[/font][font=宋体]号为[/font][font=Calibri]166526-99-4[/font][font=宋体],纯度为[/font][font=Calibri]98%[/font][font=宋体],具有特定的化学结构和性质。另一种阿戈美拉汀杂质是[/font][font=Calibri]AgoMelatine DiMer Urea[/font][font=宋体],其[/font][font=Calibri]CAS[/font][font=宋体]号为[/font][font=Calibri]185421-27-6[/font][font=宋体]。[/font][font=Calibri]CATO[/font][font=宋体]标准品提供的阿戈美拉汀全套的杂质[/font][/font][font=宋体],[/font][font=宋体]这些杂质对于药物的纯度和稳定性研究至关重要,也是药物研发过程中不可或缺的一部分[/font][font=宋体]。[img=,606,514]https://ng1.17img.cn/bbsfiles/images/2024/02/202402182106267012_9724_6381607_3.png!w606x514.jpg[/img][/font][font=宋体][color=#05073b][back=#fdfdfe] 广州[/back][/color][/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]佳途科技[/back][/color][/font][font=宋体][color=#05073b][back=#fdfdfe]股份有限公司[/back][/color][/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]深知药物研发与质量控制的重要性[/back][/color][/font][font=宋体][font=宋体],[/font][font=Calibri]CATO[/font][font=宋体]标准品厂家,提供阿戈美拉汀全套[/font][/font][font=宋体]的[/font][font=宋体]杂质,为客户提供更加精准、可靠的分析标准品,助力药物研发事业的快速发展[/font][font=宋体],[/font][font=宋体]以满足客户在药物研发和质量控制方面的需求。[/font]
102%(对照为奥美拉唑钠),后来领导指示我们用奥美拉唑对照再来用液相检测奥美拉唑钠,含量又和奥美拉唑钠对照算出来的结果差很多(奥美拉唑钠和奥美拉唑的转换系数考虑在内了),大家帮忙分析一下是什么原因啊
[b]问题:[b][b][b][/b][/b]艾司奥美拉唑镁肠溶片的检测,流动相是?[/b]答案:流动相: A:水-磷酸盐缓冲溶液-乙腈(80:10:10) B:乙腈-磷酸盐缓冲溶液-水(80:1:19)=======================================================================【活动内容】1、每个工作日上午10:00左右发布一个关于应用数据库的应用问答题,版友根据题目给出自己理解的答案。2、每个工作日下午15:10公布参考答案。【活动奖励】幸运奖:抽奖软件,当天随机抽取3个或5个回答正确的版友ID号(最后一个ID号,截止至下午15:00),每人奖励[color=#ff0000]2钻石币[/color](抽奖人数≤10,抽取3个版友;抽奖人数>10,抽取5个版友);中奖名单:lijing320323(注册ID:lijing320323)999youran(注册ID:999youran)dahua1981(注册ID:dahua1981)PAEs(注册ID:v2911392)吕梁山(注册ID:shih20j07)[img=,690,388]https://ng1.17img.cn/bbsfiles/images/2018/09/201809041504163298_6848_1610895_3.png!w690x388.jpg[/img][img=,690,388]https://ng1.17img.cn/bbsfiles/images/2018/09/201809041504189792_3148_1610895_3.png!w690x388.jpg[/img]积分奖励:所有回答正确的版友奖励[color=#ff0000]10个积分[/color](幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次[/b][align=left][color=#ff0000][b]PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。[/b][/color][/align][align=left][color=#ff0000][b] 下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。[/b][/color][/align][align=center]=======================================================================[/align]方法:HPLC基质:药品应用编号:103783化合物:艾司奥美拉唑色谱柱:[url=http://www.dikma.com.cn/product/details-855.html]Platisil ODS 5μm 250 x 4.6mm[/url]样品前处理:有关物质供试品:精密称取20mg样品置于100mL容量瓶中,加10mL甲醇,振摇,加20mL磷酸盐缓冲溶液(每1000mL水中加入磷酸钠0.0137mol和磷酸氢二钠0.0551mol),超声使其溶解,用水稀释到100mL,混匀,过滤,取续滤液。色谱条件:色谱柱: Platisil ODS 250*4.6 mm,5 μm(Cat#:99503)流动相: A:水-磷酸盐缓冲溶液-乙腈(80:10:10) B:乙腈-磷酸盐缓冲溶液-水(80:1:19)磷酸盐缓冲溶液:1000mL水+磷酸二氢钠0.0052mol+磷酸氢二钠0.0315mol流速: 1.0 mL/min柱温: 30 ℃检测器: 302nm进样量: 20uL文章出处:天津应用实验室关键字:艾司奥美拉唑镁肠溶片、Platisil ODS、99503、HPLC摘要:Platisil ODS检测艾司奥美拉唑镁肠溶片。图谱:[img]http://www.dikma.com.cn/u/image/2017/01/05/1483598227111770.jpg[/img][img]http://www.dikma.com.cn/u/image/2017/01/05/1483598227527569.jpg[/img][img]http://www.dikma.com.cn/u/image/2017/01/05/1483598227109068.jpg[/img]
全球首个每日一次给药的蛋白酶抑制剂锐艾妥(阿扎那韦)日前被中国国家食品药品监督管理局批准在中国上市。锐艾妥是由百时美施贵宝公司自主研发的新型蛋白酶抑制剂,具有持续强效抑制HIV病毒、低耐药、用药方便、对脂肪代谢副作用小等特点。 蛋白酶是HIV病毒复制所必需的物质,而蛋白酶抑制剂能有效阻断HIV蛋白酶的合成。作为一种强效的蛋白酶抑制剂,锐艾妥与其他抗病毒药物联合应用于艾滋病的抗病毒治疗,在从未接受过抗病毒治疗的初治患者中,临床试验研究至今,耐药率只有2%。自2003年6月在美国获准上市,截止到2006年底,仅在美国就已有约13万名患者受益于锐艾妥。 “在抗病毒初治的艾滋病患者中,含有锐艾妥的方案疗效相当于目前的标准治疗方案,但是锐艾妥由于每日一次给药、对脂肪代谢副作用小、耐药率低、且与其他蛋白酶抑制剂无交叉耐药等特点,使其更具优势。”中国疾病预防控制中心性病艾滋病预防控制中心主任、锐艾妥在中国的临床试验主要研究者张福杰医生说。 “在抗病毒经治患者中,锐艾妥需要与利托那韦联合使用,与目前的标准治疗方案,如克力芝相比,疗效相当;而锐艾妥在现有蛋白酶抑制剂中对脂肪代谢的副作用最小。”对脂肪代谢的副作用增大可引起患者血脂升高,可能增加心血管疾病的危害性。 据张福杰医生介绍,在中国,每年大约新增5000至10000名从未接受过治疗的HIV/AIDS病人,政府免费诊治的病人数已超过36000人,并以每年6000人左右的速度递增,其中约20%的患者对一线的治疗方案产生耐药而需要二线治疗药物。 “百时美施贵宝公司是全球三大抗艾药物研发和生产厂商之一。继在中国上市抗艾药物赛锐特TM(司坦夫定)和惠妥滋(去烃肌苷)后,我们很高兴今天又能上市代表全球范围内最新医学成果的抗艾新药锐艾妥。”百时美施贵宝公司(中国)总裁柯彼呐先生说,“希望这一创新药物能够为更多的中国艾滋病患者提供更好的治疗选择。” 据联合国艾滋病规划署和世界卫生组织的最新统计,自世界上首例艾滋病于1981年6月被美国疾病控制中心(CDC)确认以来,截止2003年,艾滋病已在全球范围内夺走约3000万人的生命,而HIV感染的成人及儿童已逾4000万人,每年新增500多万HIV感染病例。若不能有效的预防控制,预计20年后HIV感染者将达2亿人。 自我国在1985年发现首例艾滋病人以来,据卫生部发表的通报显示,截止2006年10月31日,全国历年累计报告艾滋病达183,733例,其中艾滋病病人40,667例;死亡12,464例。 关于锐艾妥 一项对锐艾妥II和III期试验的关键数据的分析显示,锐艾妥除了在血脂代谢方面具有独特的优点外,还有独特的耐药性表现。资料表明,如果初治患者中出现锐艾妥耐药性,总会发生特异性的I50L突变。这种特异突变导致病毒对锐艾妥的敏感性下降,与其他蛋白酶抑制剂无交叉耐药,且在体外对其他蛋白酶抑制剂的敏感性增强。对于首次用药的患者,先用锐艾妥保留未来使用其他蛋白酶抑制剂的可能性。 一项III期研究(AI424-034)的结果显示,在初治患者中,经过48周的治疗后,锐艾妥+拉米夫定+齐多夫定(n=405)的抗病毒疗效与SUSTIVA(依发韦仑)+拉米夫定+齐多夫定的标准治疗方案(n=405)相似。 另一项III期试验(AI424-045)中,比较了增强的锐艾妥300mg+两种核苷类逆转录酶抑制剂(NRTIs)的联合用药方案(n=120)和用利托那韦增强的洛匹那韦+两种NRTIs的联合用药方案(n=120)在接受过治疗的患者中的应用。在这项研究中,含有增强的锐艾妥的治疗方案不亚于标准治疗方案克力芝方案(洛匹那韦/利托那韦),且含有锐艾妥的治疗方案脂肪代谢的副作用明显少于克力芝方案。对于抗病毒初治患者,锐艾妥的推荐用量为400mg(两粒200mg的胶囊),每天一次,餐后给药,与其他抗逆转录病毒药物联用。更多信息请登录www.reyataz.com 查阅完整的处方药资料。 锐艾妥不能治愈HIV或阻止HIV的传播。
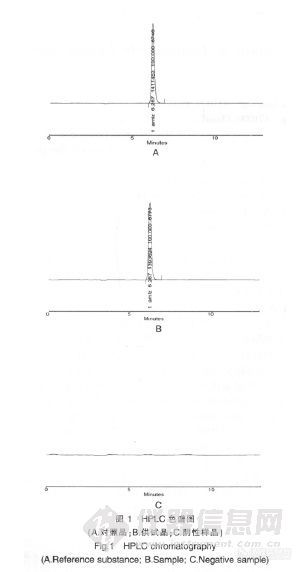
作者:孙蕊;刘世超; (河南省洛阳市中心医院药剂科;河南省洛阳市妇女儿童医疗保健中心药剂科;)摘要:目的:建立高效液相法测定奥美拉唑镁肠溶片含量的方法。方法:采用Diamonsil-C18(4.6 mm×150 mm,5μm)色谱柱;流动相:甲醇-水-磷酸-三乙胺(65∶35∶0.12∶0.3);检测波长:302 nm;流速:1.0 ml/min。结果:奥美拉唑镁在13.3182~31.0758μg范围内与峰面积呈良好的线性关系(r=0.999 0),平均回收率为101.14%,RSD=1.64%。结论:本法简便、准确、重现性好,可用于奥美拉唑镁肠溶片的质量控制。谱图:http://ng1.17img.cn/bbsfiles/images/2012/08/201208201413_384697_1606903_3.jpg
问题: 请问各位老师,有做过艾司奥美拉唑原料有关物质的吗?交流一下好吗?谢谢!艾司奥美拉唑钠有关物质
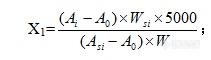
[align=center]奥美拉唑成品中杂质的质量检测[/align][align=center][b]摘要:目的:[/b]在对奥美拉唑原料药中引入的基因毒性杂质,即4-甲氧基-2-硝基苯胺和4-甲氧基-邻苯二胺设定质量检测方法,并进行方法验证。同时,对合成工艺中引入的残留溶剂进行质量检测,确保奥美拉唑成品的质量安全。[b]方法:[/b]在对4-甲氧基-2-硝基苯胺和4-甲氧基-邻苯二胺进行质量检测中,采用液相色谱的方法,并对其进行限度验证;而对残留溶剂采用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url],利用内标法进行质量检测。[b]结果:[/b]本研究对两种基因毒性杂质及残留溶剂的检测是可行有效的,有利于对奥美拉唑原料药的质量监控,同时为后续对奥美拉唑质量标准的制定提供理论依据。[b]关键词:[/b]奥美拉唑;质量标准;毒性杂质;残留溶剂[/align][b]Abstract Objective[/b]: Themass detection is set in the introduction of genotoxic impurities into theomeprazole APIproducts, namely 4-methoxy-2-nitroaniline and4-methoxy-o-phenylenediamine, and the method was verified.At the same time, the quality of theresidual solvent introduced in the synthesis process is checked to ensure thequality and safety of the omeprazole.[b]Methods:[/b]In the mass detection of4-methoxy-2-nitroaniline and 4-methoxy-o-phenylenediamine, the method of liquidchromatography is used, and the limit is verified the residual solvent aretested by the gas chromatogram and internal standard method for quality.[b]Results:[/b]This study is feasible and effective for the detection of twogenotoxic impurities and residual solvents, which is the benefit of qualitymonitoring of omeprazole APIproducts, and provides a theoretical basis forthe subsequent development of omeprazole quality standards.[b]Keywords:[/b] Omeprazole Quality standard Genotoxicimpurities Residual solvents随着人们平时工作、学习等压力的不断增加,导致消化类疾病患病率不断上升,而在中国,发病率已达到20%左右[sup][/sup]。用于治疗消化类疾病的药物也逐步成为生活中的常用药,其发展市场也在不断扩大。在消化系统溃疡类疾病的临床治疗中,质子泵抑制剂类药物因其具有良好的治疗效果,市场销售份额高达58%[sup][/sup]。而奥美拉唑是质子泵抑制剂类的代表药物,通过抑制胃酸分泌,用于治疗胃溃疡、十二指肠溃疡等疾病。但长期服用奥美拉唑存在着潜在风险,可能会引起心脏类疾病等。且其生产过程引入的有机杂质、基因毒性杂质、无机杂质或残留的有机溶剂等均对人体健康有一定危害。因此,建立奥美拉唑引入杂质或残留有机溶剂的质量检测方法是十分有必要的,严格控制质量标准,把控药品市场质量安全。[b]1 仪器与材料1.1 实验仪器[/b]高效液相色谱仪(THERMO SCIENYIFIC, Mltimate3000);电子天平(METTLER-TOLEDO、BP-210S) [url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url](Agilent 6890N)顶空进样器(Agilent 7694E)[b] 1.2 实验试剂[/b][align=center][b]表1-1 实验所需试剂[/b][/align] [table][tr][td=2,1] [align=center][b]实验试剂[/b][/align] [/td][td] [align=center][b]厂家[/b][/align] [/td][/tr][tr][td=2,1] [align=center]磷酸二氢钾[/align] [/td][td] [align=center]莱阳经济技术开发区精细化工厂[/align] [/td][/tr][tr][td=2,1] [align=center]氢氧化钾[/align] [/td][td] [align=center]国药集团[/align] [/td][/tr][tr][td=2,1] [align=center]乙腈[/align] [/td][td] [align=center]Fisher Scientific[/align] [/td][/tr][tr][td=2,1] [align=center]4-甲氧基-2-硝基苯胺[/align] [/td][td] [align=center]北京百灵威科技有限公司[/align] [/td][/tr][tr][td=2,1] [align=center]4-甲氧基-邻苯二胺[/align] [/td][td] [align=center]Alfa Aesar[/align] [/td][/tr][tr][td=2,1] [align=center]奥美拉唑[/align] [/td][td] [align=center]寿光富康制药有限公司[/align] [/td][/tr][tr][td=1,6] [align=center]分析纯[/align] [/td][td] [align=center]丙酮[/align] [/td][td] [align=center]西陇化工股份有限公司[/align] [/td][/tr][tr][td] [align=center]甲醇[/align] [/td][td] [align=center]Fisher Scientific[/align] [/td][/tr][tr][td] [align=center]苯[/align] [/td][td] [align=center]天津富宇化工有限公司[/align] [/td][/tr][tr][td] [align=center]甲苯[/align] [/td][td] [align=center]莱阳经济技术开发区精细化工厂[/align] [/td][/tr][tr][td] [align=center]二氯甲烷[/align] [/td][td] [align=center]天津科密欧化学试剂有限公司[/align] [/td][/tr][tr][td] [align=center]DMA[/align] [/td][td] [align=center]Sigma-Aldrich[/align] [/td][/tr][/table][b]2 基因毒性杂质的检验方法的设定及方法学验证[/b]来源于起始物料苯并咪唑的合成路线的基因毒性杂质[sup][/sup]不适用于药典各论方法检测此类物质,在药典规定的波长无吸收。因此,采用液相色谱方法,对奥美拉唑成品中的4-甲氧基-2-硝基苯胺和4-甲氧基-邻苯二胺进行限度检测和控制。[b]2.1色谱条件[/b]色谱柱:ODS-3,5μm,4.6×250mm;检测波长分别设定为4-甲氧基-2-硝基苯胺(230nm)及4-甲氧基-邻苯二胺(210nm);流速为1.0ml/min;进样量为80μl;柱温为30℃。[b]2.2 溶液配制[/b]1) 流动相:溶解6.8g的磷酸二氢钾用纯化水溶解并稀释至1000ml,用氢氧化钾调节pH至6.5,和乙腈按(73:27)混合。2) 对照溶液:取4-甲氧基-2-硝基苯胺和4-甲氧基-邻苯二胺各16mg,精密称定置于200ml容量瓶中,用流动相溶解并稀释至刻度,准确量取1ml此溶液用流动相稀释至100ml,再量取1ml用流动相稀释至50ml。3) 奥美拉唑供试液:称取奥美拉唑样品100mg,精密称定置于50ml容量瓶中,用流动相溶解并稀释至刻度。注:计算奥美拉唑中的4-甲氧基-2-硝基苯胺和4-甲氧基-邻苯二胺含量都不得超过8ppm。[b]2.3质量检测方法验证[/b]通过限度验证,即该方法的专属性、系统适应性、检测限以及样品测定,是否符合验证可接受的标准,来判断该方法是否符合标准,可用于杂质测定。[b]2.3.1 专属性[/b]1) 溶液配制定性溶液:取4-甲氧基-2-硝基苯胺和4-甲氧基-邻苯二胺各16mg,精密称定置于200ml容量瓶中,用配制完毕的流动相溶解并稀释至刻度,准确量取1ml此溶液用流动相稀释至100ml,再稀释1ml用流动相稀释至50ml。2) 测定取流动相作为空白、定性溶液进样,记录色谱图,数据和结果。3) 数据与结果[align=center][b]表2-1专属性测试数据和结果[/b][/align] [table][tr][td] [align=center][b]项目[/b][/align] [/td][td] [align=center][b]4-甲氧基-2-硝基苯胺峰面积(230nm)[/b][/align] [/td][td] [align=center][b]4-甲氧基-邻苯二胺峰面积(210nm)[/b][/align] [/td][/tr][tr][td] [align=center]空白[/align] [align=center]溶液[/align] [/td][td] [align=center]未检出[/align] [/td][td] [align=center]未检出[/align] [/td][/tr][tr][td] [align=center]定性[/align] [align=center]溶液[/align] [/td][td] [align=center]8550[/align] [/td][td] [align=center]12258[/align] [/td][/tr][/table][align=center][b]表2-2信噪比测试数据和结果[/b][/align] [table=100%][tr][td] [align=center][b]杂质[/b][/align] [/td][td] [align=center][b]信噪比[/b][/align] [/td][/tr][tr][td] [align=center]4-甲氧基-2-硝基苯胺峰面积(230nm)[/align] [/td][td] [align=center]0[/align] [/td][/tr][tr][td] [align=center]4-甲氧基-邻苯二胺峰面积(210nm)[/align] [/td][td] [align=center]0[/align] [/td][/tr][/table][b]2.3.2系统适用性试验[/b]1) 溶液制备贮备液:取4-甲氧基-2-硝基苯胺和4-甲氧基-邻苯二胺各16mg,精密称定置于200ml容量瓶中,用流动相溶解并稀释至刻度,准确量取1ml此溶液用流动相稀释至100ml。杂质溶液:用流动相稀释1ml贮备液到50ml或用专属性定性溶液及图谱。分离度:称取埃索美拉唑镁或奥美拉唑镁样品100mg,精密称定置于50ml容量瓶中,用流动相溶解后准确加入1ml贮备液并用流动相稀释至刻度。2) 测定以方法规定的色谱条件,取杂质溶液、分离度溶液分别进样,记录色谱图,数据和结果。3) 数据与结果[align=center][b]表2-3 系统适用性性测试结果[/b][/align] [table=562][tr][td] [align=center][b]溶液[/b][/align] [align=center][b]名称[/b][/align] [/td][td] [align=center][b]峰面积1[/b][/align] [/td][td] [align=center][b]峰面积2[/b][/align] [/td][td] [align=center][b]峰面积3[/b][/align] [/td][td] [align=center][b]峰面积4[/b][/align] [/td][td] [align=center][b]峰面积5[/b][/align] [/td][td] [align=center][b]峰面积6[/b][/align] [/td][td] [align=center][b]峰面积平均值[/b][/align] [/td][td] [align=center][b]RSD[/b][/align] [/td][/tr][tr][td] [align=center]4-甲氧基-2-硝基苯胺峰面积(230nm)[/align] [/td][td] [align=center]8427[/align] [/td][td] [align=center]8425[/align] [/td][td] [align=center]8481[/align] [/td][td] [align=center]8533[/align] [/td][td] [align=center]8483[/align] [/td][td] [align=center]8460[/align] [/td][td] [align=center]8468.17[/align] [/td][td] [align=center]0.48%[/align] [/td][/tr][tr][td] [align=center]4-甲氧基-邻苯二胺峰面积(210nm)[/align] [/td][td] [align=center]11701[/align] [/td][td] [align=center]11539[/align] [/td][td] [align=center]11086[/align] [/td][td] [align=center]11043[/align] [/td][td] [align=center]10548[/align] [/td][td] [align=center]10679[/align] [/td][td] [align=center]11099.33[/align] [/td][td] [align=center]4.11%[/align] [/td][/tr][/table][align=center][b]表2-4 奥美拉唑和4-甲氧基-邻苯二胺分离度测试结果[/b][/align] [table=100%][tr][td] [align=center][b]名称[/b][/align] [/td][td] [align=center][b]保留时间[/b][/align] [/td][td] [align=center][b]分离度[/b][/align] [/td][/tr][tr][td] [align=center]相邻杂质峰[/align] [/td][td] [align=center]3.813[/align] [/td][td] [align=center]-[/align] [/td][/tr][tr][td] [align=center]4-甲氧基-邻苯二胺峰面积(210nm)[/align] [/td][td] [align=center]4.736[/align] [/td][td] [align=center]2.16[/align] [/td][/tr][tr][td] [align=center]相邻杂质峰[/align] [/td][td] [align=center]5.248[/align] [/td][td] [align=center]1.69[/align] [/td][/tr][/table][align=center][b]表 2-5奥美拉唑和4-甲氧基-2-硝基苯胺分离度测试结果[/b][/align] [table=100%][tr][td] [align=center][b]名称[/b][/align] [/td][td] [align=center][b]保留时间[/b][/align] [/td][td] [align=center][b]分离度[/b][/align] [/td][/tr][tr][td] [align=center]相邻杂质峰[/align] [/td][td] [align=center]23.168[/align] [/td][td] [align=center]-[/align] [/td][/tr][tr][td] [align=center]4-甲氧基-2-硝基苯胺峰面积(230nm)[/align] [/td][td] [align=center]26.908[/align] [/td][td] [align=center]3.32[/align] [/td][/tr][tr][td] [align=center]相邻杂质峰[/align] [/td][td] [align=center]29.467[/align] [/td][td] [align=center]2.85[/align] [/td][/tr][/table][b]2.3.3检测限[/b]1) 溶液制备按照选择项下贮备溶液的配制方法配制溶液,并将标准溶液逐步稀释,得到适当浓度的溶液。2) 测定在色谱条件下,取溶液进样,记录色谱图。当待测组分的信噪比大于2时,对应的浓度为该组分的最小检测浓度。3) 数据与结果4-甲氧基-2-硝基苯胺检测限0.00256 μg/ml,LOD=1.28ppm,S/N=2.22 4-甲氧基-邻苯二胺检测限0.00256μg/ml,LOD=0.000128,S/N=2.[b]2.3.4样品检测[/b]1) 溶液配制根据已设定检测方法已将溶液配制完毕。2) 测定分别取三批样品按照溶液的配制方法,配制供试液进样,记录色谱图。3) 数据与结果[align=center][b]表2-6 奥美拉唑样品检测结果[/b][/align] [table=102%][tr][td] [align=center][b]批号[/b][/align] [/td][td] [align=center][b]4-甲氧基-2-硝基苯胺(230nm)[/b][/align] [/td][td] [align=center][b]4-甲氧基-邻苯二胺(210nm)[/b][/align] [/td][/tr][tr][td] [align=center]20150401[/align] [/td][td] [align=center]未检出[/align] [/td][td] [align=center]未检出[/align] [/td][/tr][tr][td] [align=center]20150402[/align] [/td][td] [align=center]未检出[/align] [/td][td] [align=center]未检出[/align] [/td][/tr][tr][td] [align=center]20150403[/align] [/td][td] [align=center]未检出[/align] [/td][td] [align=center]未检出[/align] [/td][/tr][/table][b]3残留溶剂的检测方法的设定[/b]在《中国药典》[sup][/sup]规定的奥美拉唑中各论残留溶剂的检测方法的基础上,进行修正,更改部分参数,选用内标法对残留溶剂进行检测,有利于快速检验及产品及时入库。[b]3.1 色谱条件[/b]1) [url=https://insevent.instrument.com.cn/t/Mp]气相[/url]部分色谱柱:Agilent DB-624, 0.32mm×30m,膜厚1.8μm;柱温先以50 ℃保持5分钟,后以20℃/min升温到200℃保持4分钟;进样口温度为200℃; 分流比为1:1;检测器为FID,其温度为300℃;载气设定为氮气;柱流量则为3.0ml/min。2) 顶空部分顶空瓶平衡温度98℃,平衡时间20min;定量环温度115℃,体积1ml;传输管线温度为130℃。[b]3.2 溶液配制[/b]1) 苯贮备液:精密称取苯0.02g于已加入少量DMA的100ml容量瓶中,用DMA稀释至刻度,摇匀。2) 标准贮备液:精密称取丙酮0.15g,甲醇0.1g,二氯甲烷0.01g,甲苯0.03g,于已加入少量DMA的100ml容量瓶中,在此容量瓶中加入1ml准确量取的苯贮备液,用DMA稀释至刻度,摇匀。3) 标准溶液:精密量取标准溶液贮备液5.0ml于50 ml容量瓶中,用DMA稀释至刻度,混合均匀。4) 供试溶液:精密称定样品0.5g于20ml顶空瓶中,用5ml DMA溶解。[b]3.3 检测方法[/b]1) 按照[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]部分和顶空部分的操作条件设定操作方法。取标准溶液顶空进样,记录色谱图(主要组分出峰顺序依次为甲醇、丙酮、二氯甲烷、苯、甲苯)。注:计算相邻组分之间的分离度R,均应不小于1.5;取6份标准溶液,连续进样,计算各溶剂峰面积的RSD,应不大于10%。2) 先将空白溶液、6份标准溶液和样品溶液各5ml置于顶空瓶中,密封。取空白溶液进样,记录图谱,再取6份标准溶液,记录色谱图,进行系统适用性试验和标准校正,最后取供试溶液进样,记录图谱。计算公式如下式(2-1):[align=center][img=,211,60]https://ng1.17img.cn/bbsfiles/images/2019/07/201907241130224283_2738_3389662_3.png!w211x60.jpg[/img];[/align][align=center][img=,187,81]https://ng1.17img.cn/bbsfiles/images/2019/07/201907241130597462_639_3389662_3.png!w187x81.jpg[/img][/align]注:X[sub]1[/sub]:残留甲醇、甲苯、二氯甲烷、丙酮的量,ppm X[sub]2[/sub]:残留苯的量,ppm Ai:供试溶液的图谱中溶剂(i)的峰面积;A[sub]0[/sub]:空白溶液的图谱中溶剂(i)的峰面积;A[sub]si[/sub]:标准溶液的图谱中溶剂(i)的峰面积;W:样品的称量,g;W[sub]si[/sub]:溶剂(i)的称重,g。[b]3.4 检测结果[/b][align=center][b]表3-1 奥美拉唑残留溶剂检验结果[/b][/align] [table][tr][td=1,2] [align=center][b]项目[/b][/align] [/td][td=1,2] [align=center][b]标准[/b][/align] [/td][td=1,2] [align=center][b]方法[/b][/align] [/td][td=3,1] [align=center][b]奥美拉唑检验批号[/b][/align] [/td][/tr][tr][td] [align=center][b]A-51511507002[/b][/align] [/td][td] [align=center][b]A-51511507003[/b][/align] [/td][td] [align=center][b]A-51511507004[/b][/align] [/td][/tr][tr][td=1,5] [align=center]残留溶剂检验[/align] [/td][td] [align=center]丙酮不得超过1500ppm[/align] [/td][td=1,5] [align=center]内控[/align] [/td][td] [align=center]309ppm[/align] [/td][td] [align=center]396ppm[/align] [/td][td] [align=center]423ppm[/align] [/td][/tr][tr][td] [align=center]二氯甲烷不得超过100ppm[/align] [/td][td] [align=center]未检出[/align] [/td][td] [align=center]未检出[/align] [/td][td] [align=center]未检出[/align] [/td][/tr][tr][td] [align=center]甲醇不得超过500ppm[/align] [/td][td] [align=center]115ppm[/align] [/td][td] [align=center]129ppm[/align] [/td][td] [align=center]122ppm[/align] [/td][/tr][tr][td] [align=center]甲苯不得超过300ppm[/align] [/td][td] [align=center]未检出[/align] [/td][td] [align=center]未检出[/align] [/td][td] [align=center]未检出[/align] [/td][/tr][tr][td] [align=center]苯不得超过1ppm(LOQ)[/align] [/td][td] [align=center]未检出[/align] [/td][td] [align=center]未检出[/align] [/td][td] [align=center]未检出[/align] [/td][/tr][/table][b]4小结[/b]本研究对治疗胃溃疡的一线药物奥美拉唑进行质量检验方法的研究。通过分析其合成过程中引入的杂质,创新性的提出原料药中可能存在的基因毒性杂质4-甲氧基-2-硝基苯胺、4-甲氧基-邻苯二胺,同时对生产过程引入的残留有机溶剂进行质量监控。根据ICH的指南Q2A和Q2B的要求,采用液相色谱,对奥美拉唑成品中的4-甲氧基-2-硝基苯胺和4-甲氧基-邻苯二胺进行限度检测,并对检测方法进行了专属性、系统适应性、检测限,样品测定等方面的限度验证。限度验证结果均应符合标准,说明该检测方法符合测定的准确性、可靠性和灵敏度的要求,能够进行该杂质的测定。且使用该方法进行三种批号的奥美拉唑基因毒性杂质检验时,均未发现存在4-甲氧基-2-硝基苯胺和4-甲氧基-邻苯二胺。说明现有的工艺可有效除去原料药中引入的这两种基因毒性杂质,可不放入日常质量监控之中。同时,在对奥美拉唑合成工艺中残留的有机溶剂的质量检测研究中,进行检测时,发现,其药品中检测出少量的丙酮和甲醇,但均在质量标准规定以内,未检测出二氯甲烷、甲苯、苯,说明选用的三批奥美拉唑成品药均符合药品质量标准。而在检测中,本研究创新性使用不同于中华人民共和国药典中的N ,N-二甲基甲酰胺(DMF),而选择易于冲洗的N ,N-二甲基乙酰胺(DMA)做溶媒,易冲洗干净,且不影响公司内其它产品的检测,与中华人民共和国药典方法相比,大大缩短检验样品的时间,中华人民共和国药典方法单个样品的检测时间为65min,内控的方法仅为36.5min,对工业化规模生产来说,快速检测样品既经济又能保证产品及时入库。[b]参考文献[/b] AnaLuisa Correia, Mina J Bissell. The tumor microenvironment is a dominantforceinmulti drμg resistance.Drμg Resist Update. 2012, 15(6):39-49. Shaojun Shi, ΜlrichKlotz,Protonpump inhibitors: an update of their clinical us and pharmacokinetics .EurJ Clin Pharmacol, 2008, 64(30): 935-951. ICHVALIDATION OF ANALYTICAL PROCEDURES: TEXT AND METHODOLOGY Q2 (R1) Current Step4 version (Complementary Guideline on Methodology dated 6 November 1996incorporated in November 2005). 国家药典委员会.中华人民共和国药典.二部.北京:中国医药科技出版社, 2015: 1412.
他达拉非杂质是一种化学物质,它是他达拉非的同分异构体或相关化合物。他达拉非是一种磷酸酯酶抑制剂,用于治疗男性勃起功能障碍。COTO标准品是一种高纯度的标准物质,用于测定他达拉非及其杂质的纯度、含量和化学性质。通过与COTO标准品进行对比和分析,可以确定他达拉非及其杂质的结构、组成和含量,从而保证他达拉非的质量和安全性。在药物研发和生产过程中,COTO标准品的使用非常重要。它可以提供可靠的参照物,用于质量控制、药物分析和化学计量学研究。通过使用COTO标准品,可以确保他达拉非及其杂质的准确性和可靠性,为药物的安全性和有效性提供保障。总的来说,COTO标准品在他达拉非杂质的研究和控制中具有重要作用。通过使用COTO标准品,可以更好地了解他达拉非及其杂质的性质和含量,从而确保药物的安全和有效性。同时,也需要加强生产过程中的管理和监督,加强质量标准和监管措施的执行力度,确保药物质量和安全。
各位好: 急求此份美國防火标准 NFPA 260 (UFAC Class 1) ,谢谢大家的帮助.
各有关单位: 根据《食品安全法》及其实施条例的规定,我委组织拟订了《食品安全国家标准食品营养强化剂 葡萄糖酸镁》等9项食品安全国家标准(征求意见稿),现向社会公开征求意见。请于2016年3月30日前登录食品安全国家标准管理信息系统(http://bz.cfsa.net.cn/cfsa_aiguo)在线提交反馈意见。 附件: 1.《食品安全国家标准 食品营养强化剂 葡萄糖酸镁》(征求意见稿)及编制说明 2.《食品安全国家标准 食品营养强化剂 5’单磷酸胞苷》(征求意见稿)及编制说明 3.《食品安全国家标准 食品营养强化剂 醋酸视黄酯(醋酸维生素A)》(征求意见稿)及编制说明 4.《食品安全国家标准 食品营养强化剂 D-泛酸钠》(征求意见稿)及编制说明 5.《食品安全国家标准 食品营养强化剂 多聚果糖》(征求意见稿)及编制说明 6.《食品安全国家标准 食品营养强化剂 低聚果糖》(征求意见稿)及编制说明 7.《食品安全国家标准 食品营养强化剂 氯化锌》(征求意见稿)及编制说明 8.《食品安全国家标准 食品营养强化剂 乙酸锌》(征求意见稿)及编制说明 9.《食品安全国家标准 食品营养强化剂 海藻碘》(征求意见稿)及编制说明

[font=宋体]◇培美曲塞杂质[/font][font=宋体][font=宋体] 培美曲塞杂质是在培美曲塞的生产或保存过程中产生的非目标化合物。培美曲塞杂质有多种类型,每一种都具有不同的化学特性,如[/font][font=Calibri]CAS[/font][font=宋体]号、分子式、分子量等。例如,培美曲塞杂质[/font][font=Calibri]D[/font][font=宋体]([/font][font=Calibri]Pemetrexed Impurity D[/font][font=宋体])的[/font][font=Calibri]CAS[/font][font=宋体]号为[/font][font=Calibri]155405-79-1[/font][font=宋体],英文名称为[/font][font=Calibri]Pemetrexed Impurity D[/font][font=宋体],别名包括培美曲塞[/font][font=Calibri]EP[/font][font=宋体]杂质[/font][font=Calibri]D[/font][font=宋体]、培美曲塞杂质[/font][font=Calibri]04[/font][font=宋体](单体)等。培美曲塞杂质[/font][font=Calibri]10[/font][font=宋体]的[/font][font=Calibri]CBNumber[/font][font=宋体]为[/font][font=Calibri]CB02508197[/font][font=宋体],分子式为[/font][font=Calibri]C19H17N5O5[/font][font=宋体],分子量为[/font][font=Calibri]395.37[/font][font=宋体]。培美曲塞杂质[/font][font=Calibri]12[/font][font=宋体]的[/font][font=Calibri]CAS[/font][font=宋体]号为[/font][font=Calibri]155405-79-1[/font][font=宋体],英文名称为[/font][font=Calibri]Pemetrexed Impurity 12[/font][/font][font=宋体]。[/font][font=宋体][font=Calibri] CATO[/font][font=宋体]标准品提供的培美曲塞全套的杂质[/font][/font][font=宋体],[/font][font=宋体]这些杂质对于药物的纯度和稳定性研究至关重要,也是药物研发过程中不可或缺的一部分[/font][font=宋体]。[/font][img=,610,513]https://ng1.17img.cn/bbsfiles/images/2024/02/202402182201065910_2598_6381607_3.png!w610x513.jpg[/img][font=宋体][color=#05073b][back=#fdfdfe] 广州[/back][/color][/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]佳途科技[/back][/color][/font][font=宋体][color=#05073b][back=#fdfdfe]股份有限公司[/back][/color][/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]深知药物研发与质量控制的重要性[/back][/color][/font][font=宋体][font=宋体],[/font][font=Calibri]CATO[/font][font=宋体]标准品厂家,提供培美曲塞全套[/font][/font][font=宋体]的[/font][font=宋体]杂质,为客户提供更加精准、可靠的分析标准品,助力药物研发事业的快速发展[/font][font=宋体],[/font][font=宋体]以满足客户在药物研发和质量控制方面的需求[/font][font=宋体]。[/font]

今天收到客户一个实验,检测奥美拉唑镁肠溶片,溶出度实验,样品中有一个杂质未分开,希望安排售前实验,进行色谱柱的筛选。以辛烷基硅烷键和硅胶为填充剂,流动相是0.01M磷酸氢二钠(磷酸调pH=7.6)-乙腈=75:25,波长302nm,要求奥美拉唑峰与杂质I分离度大于2.0.下面是客户做的结果,实验室色谱柱筛选工作正在进行中……http://ng1.17img.cn/bbsfiles/images/2016/03/201603071349_586166_1987954_3.png
哪里有还原型辅酶Q10的有证标准品啊?
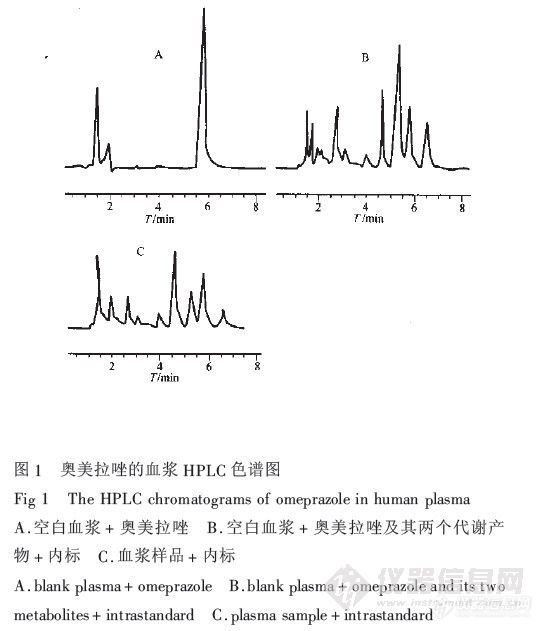
奥美拉唑肠溶胶囊人体相对生物利用度王平全,安富荣,刘振,左明,秦绮 ( 上海第二医科大学仁济医院临床药理药学研究室,上海 复旦大学医学院药物分析教研室,上海) 目的:建立测定奥美拉唑血药浓度的反相高效液相色谱法,并测定奥美拉唑肠溶胶囊的人体相对生物利用度。方法:色谱柱:Diamonsil C18( 150mmx4.6mm,5um);流动相:醋酸铵缓冲液(0.1mol/l,ph7.0),乙腈A甲醇(60:35:5);流速:1.2ml/min;检测波长:UV302nm。以内标法定量,内标物为对羟基苯甲酸乙酯。进行人体随机交叉自身对照试验,血样以二氯甲烷一次提取,测定奥美拉唑肠溶胶囊的相对生物利用度。结果:血药浓度测定的线性范围为:0.004-5.0ug/ml,回归方程为Y=3.0218C-0.0079(r=0.9998,n=7),最低检测浓度为2.5ng/ml(s/n=3),平均方法回收率为102.60%,日内、间精密度均小于5%。结论:方法简便,准确,灵敏,可用于奥美拉唑血药浓度的测定。两种制剂具有生物等效性,试验胶囊的相对生物利用度为(100.4+-13.8%)。 奥美拉唑肠溶胶囊;反相高效液相色谱法;血药浓度;生物利用度http://ng1.17img.cn/bbsfiles/images/2012/07/201207241851_379461_2355529_3.jpg
测酶活时,标准曲线一定要自己做吗? 看到论坛上有人给出曲线了,如果实验的步骤和药品的用量一样的话,能直接用那条曲线吗?因为自己做的时候,相关系数不高,实验的有些步骤是让师妹师弟做的,不知道问题在哪里
国家食品标准-这次怎么没更新测定无机砷啊,为啥???测定铅的和SE的都更新了,没更新无机砷的,奇怪???
如题,我们做了很长时间,不同的人,不同的仪器做这个标准品,都回收不回来。有没版友有同样情况的啊?NIST 610 Trace Elements in Glass:Nominal 500mg/Kg
一 煤油的分类: 1.航空煤油(Aviation Krosine ) 航空煤油也称喷气燃料(Jet Fuel),用于航空涡轮喷气发动机(航空然气涡轮发动机),馏程为60-280℃,要求烯经和芳烃含量少,稳定性好;要求发热值高,密度大,在高空飞行时,体积热值比质量热值重要;要求结晶点和冰点低,高空飞行时,在-40℃的低温下,不得析出冰和蜡。 2.普通煤油 ①灯用、取媛用和炊事用煤油 馏程为170 -280℃,有时统称为灯用煤油,主要用于煤油灯,可用作喷灯、汽灯和煤油炉的燃料。以采用深度精制的无色透明产品为宜。尽量减少灯芯积炭,不产生令人讨厌的气味,不污染室内空气。 ②动力用煤油 动力用煤油主要用作拖拉机等的燃料。动力用煤油不需要像灯用煤油那样深度精制,甚至含有320℃的高馏分也无妨。但相对于柴油而言,便用量正在逐渐减少。目前在国外,如日本常用于渔船上的热球式发动机作燃料。使用煤油做燃料的点火花式发动机则主要用于农业,采用水冷方式,压缩比为4左右。 ③信号灯用煤油 这是一种相对比较古老的油种.其设置场所的温度较高,因此闪点比一般煤油要高;但用于高寒地区,则需具备较低的凝点。 ④溶剂用煤油 煤油作为溶剂有多种用途:印刷油墨、油漆、清漆溶剂,铺路沥青稀释溶剂,杀虫剂和农药溶剂等。与工业溶剂油相比,主要是馏程范围窄。作为医药工业和油漆工业的溶剂。由于不允许含有过多的胶质、烯烃和芳烃,一般由馏程180-310℃的直馏馏分精制而成。另外,也可用来清洗机械零件。 二 煤油的检测标准汇总: GB/T 259 石油产品水溶性酸及碱测定法 GB/T 260 石油产品水分测定法 GB/T 261 石油产品闪点测定法(闭口杯法)(GB/T261 1983.neq ISO 2719:1973) GB/T 265 石油产品运动枯度测定法和动力粘度计算法 GB/T 380 石油产品硫含位测定法(燃灯法) GB/T 382 煤油烟点测定法 GB/T 511 石油产品和添加剂机械杂质测定法(重量法) GB/T 1792 馏分燃料中硫醇硫侧定法(电位滴定法) GB/T 1884 原油和液体石油产品密度实验室测定法(密度计法))(GB/T1884-2000, eqv ISO3675:1998) GB/T 1885 石油计量表(GB/T1885 -1998,eqv ISO 91-2:1991) GB/T 2430 喷漆燃料冰点测定法(GB/T 2430 -1981.eqv ISO 3013:1974) GB/T 3555 石油产品赛波特颜色测定法(赛波特比色计法) GB/T 4756 石油液体手工取样法(GB/T 4756-1998,egv ISO 3170:1988) GB/T 5096 石油产品铜片腐蚀试验法 GB/T 6536 石油产品蒸馏测定法 GB/T 11130煤油然烧性测定法 GB/T 11140石油产品硫含量测定法(X射线光谱法) GB/T 17040石油产品硫含盆测定法(能量色散X射线荧光光谱法) SH 0164 石油产品、包装贮运及交货脸收规则 SH/T 0178 煤油燃烧性测定法(点灯法) SH/T 0253 轻质石油产品中总硫含里测定法(电量法) SH/T 0604 原油和石油产品密度测定法(U形振动管法) (SH/T 0604-2000, eqv ISO 12185:1996) SH/T 0689 轻质烃及发动机燃料和其他油品的总硫含世侧定法(萦外荧光法) SH/T 0770 航空燃料冰点测定法(自动相转化法)
哪位朋友有GB/T16865-1997 变形铝镁及其合金加工制品拉伸试验用试样 标准?谢谢!
环境标准《水质 总大肠菌群、粪大肠菌群和大肠埃希氏菌的测定 酶底物法》已编制完成,目前开始征求意见,附件是该标准的征求意见稿。
1、问:欧、美对五金电镀层进行盐雾测试是否有明确的标准? 答:有的,包括ASTM B117 BS EN ISO 9227 和 GB/T 10125。2、问:针对DIY产品有哪些安全测试要求及标准?消费者组装是否要做滥用测试(年龄段5+)? 答:若DIY产品属于玩具,将以玩具的安全标准作为参考;关于消费者组装后是否要做滥用测试,需要看清楚它的说明书,写清楚该DIY玩具是成人组装还是儿童组装。若为成人组装,滥用测试将在组装后进行,以评估它的安全性;若为儿童组装的DIY玩具,则在组装前及组装后均需做滥用测试。3、问:欧盟进口的玩具电镀层不允许镀镍,请问目前镀蓝锌的六价铬是否符合其他无镍等要求? 答:该问题里混淆了两个不同的要求,第一个要求是无镍要求或release nickle的测试,第二个要求是重金属铬元素的测试。无镍要求或release nickle的要求是针对金属材料的,而该金属材料可能是使用在玩具上的,并且该部分是与儿童皮肤长期接触,这样才有无镍或release nickle的要求;至于镀蓝锌的成份,因有六价铬成份,可符合无镍或release nickle的要求,因为是玩具的一部分并且含有铬元素,但未必符合EN71-3的要求。4、问:ASTM滑板的测试标准是什么? 答:ASTM滑板测试标准是ASTM F2264H03,这是关于走动或脚动的滑板车测试要求,CPSC及ASTM委员会正在考虑及建议出台一项新的关于电动滑板的测试标准。5、问:如果在一个背袋内装玩具,袋上背带的长度大于14 inch,且带上有可调节的扣,如何让带的长度符合标准要求? 答:如果玩具是一个背袋内装玩具,袋上背带的长度需符合玩具袋上的所有要求,再加上带、绳、橡皮筋的要求。6、问:对于包装类材料(玩具包装)是否需要符合RoHS及EN 71标准? 答:玩具上的包装材料不需要符合RoHS及EN 71标准。EN71标准已豁免了玩具包装材料的测试,而包装材料有另一个要求:欧洲是94/62/EEC。7、问:是否所有的玩具都需做尖点及利边测试? 答:所有玩具都需做尖点及利边测试,根据美国的要求,供0至8岁儿童玩耍的玩具,都需做尖点及利边测试,而欧洲则规定所有年龄的玩具都需符合这两项要求。8、问:请问EN71-3中将有可能限制的20种重金属是哪些? 答:正在讨论中的EN71-3的修改,将增加/改动的有:9、问:对于EN71-3中的修正系数,是所有的测试数据都要修正还是只在限值上下才需对检测结果进行修正?在检测报告中需不需要体现是修正值? 答:对于EN71-3中的修正系数,所有的测试数据都是要修正的;修正后再参照EN71-3的要求以作为结论评估;在所有报告中都需要体现所有修正值,这是标准上规定的。而有些实验室会在当测试数据接近标准要求时才做修正,这样做可节省时间。10、问:对于SGS的化学检测,现在很多时候都是写成 答:SGS的化学测试的报告里,很多时候都写成~mg/kg,但如果客人的要求是需要出具测试数据时,站在技术层面上来说,这些测试数据提供出来是没有意思的,因为我们所写的~mg/kg,基于该测试里的不准确度、标准上写的不准确度及在整个流程里所检测的准确度而评估出来的。11、问:对于ASTM F963-0中,提到儿童时尚饰物的金属部件Total pb0.06%,但儿童金属时尚饰物175ug即可,这句话怎么理解? 答:在ASTM F963-07中,没有提到儿童饰物的重金属要求,儿童饰物的铅含量要求在加州65的要求里,Total pb0.06%是指总铅含量,儿童饰物175ug是指可溶性铅释出含量,若是评估Total pb0.06%的总铅含量,是不需要做额外的铅的释出含量来评估该产品是否合格;若Total pb超过0.06%,就需做可释出铅含量测试,此时175ug就是该项目的要求。12、问:磁铁要求中没有提长方形的尺寸要求,是否豁免长方形磁铁?或另有标准要求? 答:关于长方形的磁铁,在ASTM F963-07版里并没有提及是危险磁铁。从安全的角度考虑,如是长方磁铁且是小部件,磁通量超过50单位的,都应该算是危险磁铁。据我所知,欧盟正研究修正EN71-1,而法国已将所有小型磁铁列为不可接受的。 13、问:ASTM中关于铅的含量有两个指标:90(S)及600(T),如何理解这两个指标? 答:S代表可溶性,该可溶性是指在特定条件下,在0.07摩尔浓度的稀盐酸和37 摄氏度下,抽取两小时的结果;而600(T)的要求是指铅的总含量。14、问:关于ASTM F963-07标准:绳带及橡皮筋,描述:要有需要,设计的绳带及橡皮筋长度长于10"的,应加上一个“易开的装置”,并保持端开的两端长度小于12"(最 好在10内)。我想了解的是:一是可否加两个“易开的装置”?二是如果加两个“易开的装置”,在一个装置断开后,另一个装置未断开,但未断开装置一端长度超过12",是否还需再测试? 答:问题1:如果有需要,可加一个以上的“易开装置”;问题2:第二个需再进行测试,因为真正做测试时,每个易开装置是分开独立做测试的。15、 问:针对玩具产品出口中常提到的自我宣告,是否自我说明?有什么好处? 答:我们所说的“自我宣告”即是“自我说明”,它的好处有:根据标准的规定,对照玩具指令88/378/EEC,每间工厂针对每个产品应出具“自我说明”或“自我宣告”文件,以声称每一类产品都符合标准。当然,“自我说明”或“自我宣告”的背后需有一份测试报告支持,或技术文件来支持。具备以上文件后,可帮助我们说服买家及海关,说明进口的产品是安全及合格的。16、 问:关于ASTM F963-07中对磁玩具的要求,其中提到磁通量大于50,列为危险磁石,那么工厂如何测量磁通量? 答:可参考ASTM F963-07版第 8条里的说明,测试方法可通过一个磁通量测试仪或高斯测试仪来进行测试。17、问:磁铁及带磁性的玩具要求是否针对所有年龄层的玩具? 答:有。0~3岁绝对不可含有危险磁铁;3~8岁,当接收玩具时有危险磁铁的,则必须有警告语。3~8岁,当接收玩具没有危险磁铁,但通过滥用测试后产生危险磁铁的,是绝对不允许的。18、 问:关于ASTM磁铁,3~8岁,当玩具接收时含有危险磁铁,有警告语则可以接受,滥用后出现的危险磁铁,加警告语不行吗?(标准写的是不可接受) 答:根据ASTM 危险磁铁新标准,供3~8岁儿童玩耍的玩具,当玩具接收时含有危险磁铁是可以加警告语的,且产品仍然可以售卖;当玩具接收时无危险磁铁,但经过滥用测试后而产生有危险磁铁时是不可以加警告语的。据了解,对于该说明ASTM将再作修订。19、问:有毒PVC(含P)啤出的胶盆,用来盛装其它物料,是否有影响?(P的迁移) 答:若该胶盆不是作为饮料用的,一般正常情况下不受影响。若胶盆不属于儿童用品,是没有问题的。20、问:关于半球形玩具:开口直径64~102mm与新增的64~102mm内部尺寸有什么区别?怎么描述? 答:根据新修订,64~102mm是指内部尺寸的要求。该说明只是补充ASTM F963-03版的不足,并没有特别增加的要求。21、 问:含铅中对印刷品如胶袋警语、说明书、彩盒等可有要求? 答:有。因为这些印刷品属于94/62/EEC或美国CONEG的要求,也包括总铅含量的要求。22、问:我们出货前都会在SGS做EN62115(如带电)和EN71-1,2&3测试,我们的玩具覆盖的品种很多,从毛公仔、手枪、水枪、机器人、拼图到车仔、玩具电话、GAMES和一些儿童乐器。美泰事件后,欧美对铅超标问题很看重,我想请教一下我们的测试内容是否足够?EN71-3能否测出铅的超标?如不能,请问还需要些什么测试? 答:一般情况下,当生产过程里没有交叉污染及人为错误时,所提到的测试内容是足够的。EN71-3的含铅量,因为是可溶性含铅量,而定位定在90ppm、90mg/kg,这个可以作为参考;若没有超标,产品是可以评估为安全的,以上提及的测试基本可以满足欧洲的要求,但对于新的中国海关的CIQ要求,针对每一批玩具上所用的油漆都需要加做总铅含量测试。23、问:ASTM关于溜溜球:什么叫选择适当的弹性系数绳子?弹性系数如何界定? 答:讲义里提及的弹性系数是指有弹性的材料,如橡皮筋、弹簧等有弹性系数的指标。通过系数指标选择一些弹性较小的弹性材料或橡皮筋来作为溜溜球的材料。24、问:8岁以上则没有要求。 问:百密有一疏,万一玩具发生责任事故或者被强制召回,还有什么事后防御措施吗? 保险能保吗? 答:若玩具发生责任事故或者被强制召回,事后是没法防御的。但事前可防御,除做好一系列的质量控制的系统、程序、测试、检验之外,保险也是另一个可考虑的防御措施以上供参考!谢谢!
加拿大发布允许食品中使用菌黑曲霉派生磷脂酶A2的临时营销售批准来源:厦门WTO工作站 2009年10月21日,加拿大发布G/SPS/N/CAN/399号通报,加拿大卫生署拟制定有关用于生产面包、面粉、全麦粉、非标准面包品、非标准整蛋、非标准蛋黄及转基因蛋黄素内的菌黑曲霉PLA-54[Aspergillus niger (PLA-54)]派生磷脂酶A2的临时营销售批准。 加拿大卫生署收到一份要求准用一种转基因菌黑曲霉杆菌派生的,携带该酶的猪胰基因编码的磷脂酶提案。磷脂酶属粗分类脂肪酶。现有数据评估支持由转基因菌黑曲霉派生的这种磷脂酶A2是安全有效的。因此,加拿大卫生署拟议修改食品药物法规,准许这种黑曲霉派生磷脂酶A2按药品生产质量管理规范(GMP)用于生产面包、面粉、全麦粉、非标准面包品、非标准整蛋、非标准蛋黄及转基因蛋黄素。作为改善协调机制应答能力的手段之一,在履行修改法规协调程序的同时,特发布临时营销许可,准许按GMP要求直接使用这种磷脂酶A2;且准许销售用上述物质制作的食品。 有关此项的最终规定将在12-18个月内批准并生效。通报评议截止日期为2009年12月24日。
用没食子酸标准曲线测茶多酚标准品为什么实际值比理论值还高,是我计算的问题吗,按照国标计算的
求助欧美旅行箱包的标准,类似国内QB/T 2155 旅行箱包的标准。目前网上没有搜索到,或者企业标准(如新秀丽)也可。
β-Glucuronidase/aryl sulfatase β-葡萄糖醛酸酶\芳香基硫酸酯酶( 葡萄糖苷酸酶/硫酸芳酯酶 ) 标准品——检瘦肉精等用的除了北京希凯创新科技有限公司提供,还可以从哪里购买么?
每进一次标准品,峰面积不一样,什么原因?同一标准品,并且面积越来越大,进样也没隔太长时间
每进一次标准品,峰面积不一样,什么原因?同一标准品,并且面积越来越大,进样也没隔太长时间