
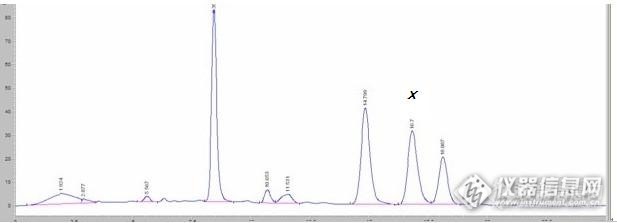
RT, 按药典上的方法测枇杷叶中的两种果酸含量(药典只要求两种果酸含量总合大于0.7%),一直不能把齐墩果酸和熊果酸完全分离,即使对照品也是这样情况;在进行峰面积处理时候,两个这样叠加的峰面积是不是全部加和了?还是有部分被遗漏了?这样做出来的含量达到了药典标准,只是不太清楚这样的结果到底能不能要?PS:今天试验了甲醇90水10冰醋酸0.03三乙胺0.06,还是这样的结果...太无奈了,分离不开下图是对照品峰形:http://ng1.17img.cn/bbsfiles/images/2013/05/201305142346_440065_2459406_3.jpg

个人在工作的小心得,请各位老师多多指点HPLC法测定山楂中熊果酸含量 摘要:目的:建立山楂中熊果酸含量测定HPLC方法。方法:采用高效液相色谱法检测熊果酸含量,以甲醇-水(20:80)为流动相,检测波长为210nm,流速为10ul。结果:标准曲线的绘制及线性范围得熊果酸线性回归方程为y=22.3880x+1.2043,相关系数r为0.9998,表明熊果酸在1~60μg/ml范围内呈现良好线性关系。精密度RSD为1.09%,重复性RSD为1.83%,表明该方法重现性良好。72小时内稳定性试验熊果酸峰面积RSD为1.10%,表明该样品溶液的稳定性良好。结论:熊果酸可作为山楂质量控制指标之一,本方法简便、准确、灵敏度高、重现性好,可作为山楂中熊果酸的含量测定方法,可有效控制山楂的内在质量。关键词:山楂;熊果酸;质量标准;HPLC 山楂又名山里红、红果。蔷薇科(Rosaceae)植物山楂CrataeguspinnatifidaBge.的果实。具有开胃消食、化滞消积、活血散瘀、化痰行气的功效。常用于肉积停乳,胃脘胀满,泻痢腹痛,瘀血经闭,痛经,产后淤血腹痛,心腹刺痛,胸痹心痛,疝气疼痛,高血脂症等。山楂中含多种化学成分,如金丝桃甙、槲皮素、山楂酸、柠檬酸、熊果酸、齐墩果酸等。在《中国药典》2015年版一部山楂项下仅有对山楂性状、显微薄层定性鉴别和有机酸枸橼酸含量滴定方法。为建立山楂HPLC方法,本文选择山楂中熊果酸为目标成分,采用高效液相色谱法,为山楂中药材质量控制提供科学依据,达到有效控制山楂中药材质量的目的。熊果酸为山楂中的主要活性成分,具有抗高血脂、降血糖、镇静、抗炎、抗菌等多种药理作用,熊果酸还具有明显的抗氧化功能。2015年版药典山楂项下未对其熊果酸建立含量测定。1、仪器及试药1.1仪器 Agilent 1260高效液相色谱仪(四元梯度系统),紫外检测器,色谱柱为ZorbaxSB-C18(4.6×250mm,5μm),Agilent Cary60紫外可见分光光度计,KQ5200DB型数控超声波清洗器(昆山市超声仪器有限公司),98-1-B型电子调温电热套(天津市泰斯特仪器有限公司),IKA KS4000i恒温摇床。http://ng1.17img.cn/bbsfiles/images/2016/09/201609090957_608958_2984502_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/09/201609090957_608959_2984502_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/09/201609090957_608960_2984502_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/09/201609090957_608961_2984502_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/09/201609090957_608963_2984502_3.jpg1.2试药 熊果酸对照品:(中国食品药品检定研究院,批号:110742-201212,供含量测定用);山楂药材(经检验为药典品种的市售样品)2、方法与结果2.1山楂中熊果酸测定 本文采用高效液相色谱法测定山楂中熊果酸的含量,为山楂药材质量控制提供科学依据。2.1.1检测波长测定 取熊果酸对照品,加甲醇溶解并制备成一定浓度的溶液,以甲醇为空白溶剂,经Agilent Cary60紫外可见分光光度计测定其最大吸收波长,结合现有文献资料报道,最后确定检测波长为210nm。2.1.2流动相优化 在文献资料中,有用乙腈-水-磷酸、甲醇-磷酸盐缓冲液、乙腈-甲醇-0.5%醋酸铵等系统作为流动相,但经实验考察后发现,这些系统存在或可能分析时间过长,或样品分离效果欠佳等因素。经实验摸索后发现,以甲醇-水系统可以很好的避免影响因素。2.1.3色谱条件 以甲醇-水(80:20)为流动相,检测波长为210nm,柱温40℃,进样量为10μl。经测定,分离度均大于2.0%,理论塔板数均在6000以上。http://ng1.17img.cn/bbsfiles/images/2016/09/201609090840_608927_1669358_3.jpg2.1.4熊果酸对照品储备溶液的制备 精密称取熊果酸对照品0.01272g,置10ml容量瓶中,加甲醇溶解至刻度,摇匀,即得对照品储备液(浓度约1.0mg/ml)。2.1.5供试品溶液的制备 取本品粉末(过2号筛)0.5g,精密称定,置锥形瓶中,精密加入甲醇50ml,称定重量,浸泡1h,超声30min,放冷,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。2.1.6标准曲线的绘制及线性范围 精密量取上述对照品储备液,置量瓶中,分别制备1、2、5、10、20、60μg/ml的标准溶液,用2.1.3项下的色谱条件绘制标准曲线,得熊果酸线性回归方程为y=22.3880x+1.2043,相关系数r为0.9998,表明熊果酸在1~60μg/ml的浓度范围内呈现良好的线性关系。2.1.7供试品溶液制备方法的优化 2.1.7.1取本品粉末(过2号筛,下同)0.5g,精密称定,置锥形瓶中,精密称定,精密加入甲醇50ml,称定重量,浸泡1h,水浴锅加热回流30min,放冷,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。 2.1.7.2取本品粉末0.5g,精密称定,置锥形瓶中,精密加入甲醇50ml,称定重量,浸泡24h,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。 2.1.7.3取本品粉末0.5g,精密称定,置锥形瓶中,精密加入甲醇50ml,称定重量,浸泡1h,超声30min,放冷,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。 经测定,方法3的提取效率明显优于方法1、2,在结合实际工作中的可操作性和提取率,最后确定方法3作为最终的提取方法。2.2精密度试验 取10μg/ml熊果酸对照品溶液,按上述色谱条件进样,重复进样6次,测得RSD为1.09%,表明仪器性能良好。2.3重复性试验 取同一批山楂样品5份,按上述样品制备项下方法,依法操作制备样品溶液。平行测定5次,结果熊果酸的平均含量为0.57%,RSD为1.83%。表明该方法重现性良好。2.4稳定性试验 取同一批山楂制备的样品溶液,在常温下放置,分别于0、6、24、48、72h分别测定1次,结果RSD为1.10%,表明该样品溶液的稳定性良好。2.5回收率试验 精密称取已知熊果酸的山楂样品约0.5g,共5份,分别精密加入对照品溶液(熊果酸浓度为0.05088mg·ml-1)10ml,按上述样品制备方法制备加样回收供试品溶液并注入高效液相色谱仪,计算平均回收率,结果(见表1)http://ng1.17img.cn/bbsfiles/images/2016/09/201609090847_608932_1669358_3.jpg3、讨论 山楂作为常用的中药材(饮片)之一,在2015年版药典收录的方法中,未采用HPLC或者更先进的方法测定其活性成分的含量。本实验方法刚好弥补了这个空缺,更好的体现中药现代化要与时俱进的要求,更符合中国中药标准现代化的要求。本方法操作简便,较更好的鉴别山楂内在质量的优劣,可以替代熊果酸薄层鉴别,更具有科学性。参考文献:国家药典委员会.中华人民共和国药典(一部).北京:化学工业出版社,2015:31国家药典委员会.中华人民共和国药典.一部.北京:化学工业出版社,2010:30南京中医药大学.中药大辞典(上册).上海:上海科学技术出版社,1986:170中药大辞典(上册).上海科学技术出版社,中华人民共和国药典2010版,1986:170.李贵海,孙敬勇,张希林,等.山楂降血脂有效成分的实验研究.中草药,2002,333(1):50.熊斌,雷志勇,陈虹.熊果酸药理学的研究进展.国外医学药学分册,2004,6(31):133.5中国药典62010年版一部国家药典委员会.中华人民共和国药典.一部.北京:化学工业出版社2005:198.曾
齐墩果酸和熊果酸是一个物质吗?我用C18的柱子,流动相为乙腈:水=90:10,流速1.0ml/min,进样20ul,两个对照品在一个位置出峰了
色谱条件与系统适用性试验 用十八烷基硅烷健合硅胶为填充剂;甲醇-乙腈-0.1%冰醋酸(83:5:12)为流动相;检测波长210nm。理论板数按熊果酸峰计算应不低于2000。对照品溶液的制备 分别取齐墩果酸和熊果酸对照品适量,精密称定,加甲醇分别制成每1ml含齐墩果酸0.1 mg和每1ml含熊果酸0.24mg的溶液,摇匀,即得。供试品溶液的制备 取本品粉末1g,精密称定,置索氏提取器中,加乙醚适量,浸泡过夜,加热回流8小时,提取液挥干乙醚,残渣加甲醇适量使溶解,转移至5ml量瓶中,加甲醇稀释至刻度,摇匀,用微孔滤膜(0.45μm)滤过,取续滤液,即得。 用以上方法测得的对照品峰:齐墩果酸与熊果酸分离不开,保留时间很近,请问应该怎样做才有好的效果?谢谢
【作者中文名】谭承佳; 张艺; 马家骅; 王毓杰;【作者单位】绵阳师范学院; 成都中医药大学药学院;【论文摘要】目的从醋柳黄酮中提取分离熊果酸并建立其含量测定方法。方法采用硅胶柱层析从醋柳黄酮氯仿浸提物中分离得到化合物,经1H-NMR、~(13)C-NMR鉴定为熊果酸;采用Diamonsil~(TM)(钻石)C~(18)(250×4.6mm,5μm),甲醇-8mmol·L~(-1)四丁基溴化铵溶液-三乙胺(90:10:0.2)为流动相,流速1mL·min~(-1),紫外检测波长210nm,柱温40℃。结果熊果酸的标准曲线线性范围为0.59~8.85μg(r=0.9996,n=5);平均加样回收率为97.11%,RSD=1.20%(n=6)。结论该法简便、准确,重复性好,适用于醋柳黄酮中熊果酸的定量分析。
[color=#444444]现有一样品中同时含有齐墩果酸、熊果酸;基本上文献上所有的色谱条件均试过、药典上的方法也试过;始终分不开;哪位有靠谱的液相条件呢?实在不行特殊的柱子、特殊的条件能分开也行啊;我用的是二极管检测器;求高人指点[/color]
高效液相色谱法测定促进消化片中熊果酸的含量 本所研制的促进消化片由山楂、麦芽、鸡内金、莱菔子等药味组成,具有清胃消食之功效。用于脾胃虚弱所致的食积,症见不思饮食、嗳腐酸臭、脘腹胀满;消化不良见上述证候者。其中君药为山楂。 中药山楂是蔷薇科山楂或山里红的干燥成熟果实。具有消食健脾,行气散瘀功效,用于肉食积滞,胃脘账满,泻痢腹痛,瘀血经闭,产后瘀阻,心腹刺痛,疝气作痛;高血脂症。主产山东、河北、河南、辽宁、山西等省,多为栽培。 随着中药现代化发展战略的提出,为控制产品质量,确保临床疗效,对中药的鉴别和检查提出了很高的要求。本文采用高效液相色谱法对方中山楂的有效成分熊果酸进行含量测定,为建立促进消化片的质量标准提供依据。材料与方法1 仪器与材料安捷伦1200 配紫外检测器循环水式真空泵(河南郑州)旋转蒸发仪(东京理化)紫外可见分光光度计(瓦里安)SZ-97A自动三重水蒸馏器(上海亚荣生)电子天平(万分之一,梅特勒托利多)超声波清洗机(昆山)熊果酸对照品(中国药品生物制品检定所),促进消化片(本所自制),阴性对照(自制),甲醇(分析纯、色谱纯,国药)2 方法2.1 色谱条件色谱柱为依利特 (250mm×4.6mm,5μm);流动相为甲醇-水:醋酸(65∶34:1);检测波长210nm;体积流量1mL﹒min-1;柱温38℃;进样量20μl。理论塔板数按熊果酸峰计算,应不低于3000。2.2 溶液的配制2.2.1对照品贮备液的制备精密称取于五氧化二磷干燥器中减压干燥24小时的熊果酸10.56mg,溶于适量甲醇,移至50mL容量瓶中,加甲醇定容,制成每1mL含熊果酸0.2112mg的溶液,作为熊果酸对照品贮备液。2.2.2对照品溶液的制备精密量取熊果酸对照品贮备液1mL置5mL容量瓶中,加甲醇定容,制成每1mL含熊果酸0.04224mg的溶液,作为熊果酸对照品溶液。2.2.3供试品溶液的制备取100片促进消化片粉碎过120目筛,精密量取粉末1g,甲醇超声提取30分钟,过滤,滤液水浴蒸干后,残渣加适量甲醇,超声处理30 min,转入50 mL容量瓶中,加甲醇定容,摇匀,以0.45[/size
苹果酸标准品那里能提供呀?知道的朋友联系我。谢谢!xq.shi@126.com
大家好!请问如何分离分离熊果酸和齐墩果酸,它们为同分异构体, 都是属于三萜类, 我试过加冰乙酸和三乙胺等, 仍不能良好分离,分离度均在0.9左右, 请各位大侠赐教! 救命啊!
如何分离熊果酸和齐墩果酸
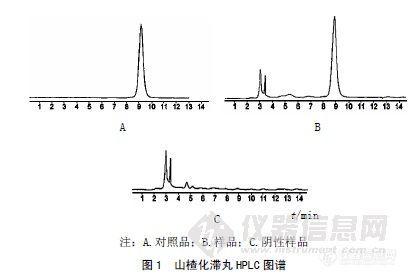
作者:蔡俊安;(河南百年康鑫药业有限公司;)摘要:目的采用高效液相色谱法建立山楂化滞丸中熊果酸的含量测定方法。方法采用高效液相色谱法,Diamonsil ODS1 C18柱,以乙腈-水-磷酸(85∶14.95∶0.05)为流动相,流速为1.0 mL/min,检测波长为210 nm。结果熊果酸在0.512 6~10.252μg范围内呈良好线性,回归方程为Y=28 451.85X+759.46,r=0.999 8。平均加样回收率为98.9%,RSD=1.13%(n=6)。结论本方法简便、准确,专属性强,测定结果重复性好,为山楂化滞丸中熊果酸的定量分析提供了有效方法。谱图:http://ng1.17img.cn/bbsfiles/images/2012/08/201208061435_381906_1606903_3.jpg
专家,您好,我最近在做关于中药材的含量测定,主要成分是齐墩果酸和熊果酸,开始用液相做的时候,这两个物质的峰分的比较开,分离度在1.7,但是后来越做越差,分离度也越来越小,我想问一下您是什么原因。期间我换过流动相,调过比例,都测不出来了。
熊果酸是粗品原料,要测它的较精确含量。之前做了几组,直接取粗品0.05g熊果酸于100ml甲醇中,结果主峰无法分离,出现两个峰重叠,管子用的是C18的,215nm的检测波长,流动相是甲醇:0.05%醋酸溶液=88:22,流速是1ml/min,不知道对不对啊,是不是方法有问题?有没有别的方法?求大神赐教!
问题: 群里有没有做过齐墩果酸和熊果酸的老师 我再网上找的方法 他的子离子只有一个 这样不便于定性 有没有那位老师知道它的定性和定量离子对吗
[size=4]在用分光光度法测试灵芝的醇提物中总三萜含量时,大多数文献都以齐墩果酸为标准品,请问一下为什么?有没有依据?因为我觉得从不同原料中提取出来的三萜类物质差异可能较大,都用齐墩果酸来做标准品是否合适? 怎么来判断或者用什么实验来证明用齐墩果酸为标准品测试三萜含量是可行的?谢谢![/size]
食品安全国家标准 食品添加剂 L-苹果酸
对超声波辅助提取枇杷叶中的熊果酸进行较为系统的研究。选择乙醇体积分数、提取时间、液固比、提取次数、物料的粒子大小5 个影响因素,运用均匀设计法安排实验,以高效液相色谱测定熊果酸的含量。以提取率为实验指标,用自主提出的可视分析方法对多维空间实验数据进行分析,并且以20 倍原料量进行了尚佳工艺放大实验。最终确定最佳工艺范围为乙醇体积分数80%~100%、提取时间50~65min 和80~100min,提取次数1 次。此类提取中,液固比和物料的粒子大小对提取率影响复杂。

[align=center][img=,600,409]https://ng1.17img.cn/bbsfiles/images/2019/09/201909111728013818_3460_932_3.jpg!w690x471.jpg[/img][/align]今天为您带来月旭Ultimate XS-C18色谱柱对木瓜中齐墩果酸、熊果酸成分的测定效果。[align=center][b]色谱条件[/b][/align]色谱柱:月旭Ultimate XS-C18(4.6×250mm,5μm)。流动相:甲醇/水/冰醋酸/三乙胺=265/35/0.1/0.05;检测波长:210nm;柱温:17℃;流速:1.0ml/min;进样量:20μL。[align=center][b]谱图和数据[/b][/align]1、对照溶液[align=center][img=,600,311]https://ng1.17img.cn/bbsfiles/images/2019/09/201909111728337178_6950_932_3.jpg!w690x358.jpg[/img][/align][align=center][img=,600,78]https://ng1.17img.cn/bbsfiles/images/2019/09/201909111728382728_9024_932_3.jpg!w690x90.jpg[/img][/align]2、样品图[align=center][img=,600,313]https://ng1.17img.cn/bbsfiles/images/2019/09/201909111728443893_5279_932_3.jpg!w690x360.jpg[/img][/align][align=center][img=,600,78]https://ng1.17img.cn/bbsfiles/images/2019/09/201909111728462678_7811_932_3.jpg!w690x90.jpg[/img][/align][align=left]3、齐墩果酸[/align][align=center][img=,600,313]https://ng1.17img.cn/bbsfiles/images/2019/09/201909111728526008_4574_932_3.jpg!w690x361.jpg[/img][/align][align=center][img=,600,66]https://ng1.17img.cn/bbsfiles/images/2019/09/201909111728583858_2430_932_3.png!w690x77.jpg[/img][/align]4、熊果酸[align=center][img=,600,313]https://ng1.17img.cn/bbsfiles/images/2019/09/201909111729046793_5613_932_3.jpg!w690x361.jpg[/img][/align][align=center][img=,600,65]https://ng1.17img.cn/bbsfiles/images/2019/09/201909111729084088_4008_932_3.png!w690x75.jpg[/img][/align][b]结论[/b]使用月旭Ultimate XS-C18(4.6×250mm,5μm),在此色谱条件下,能满足检测需求。
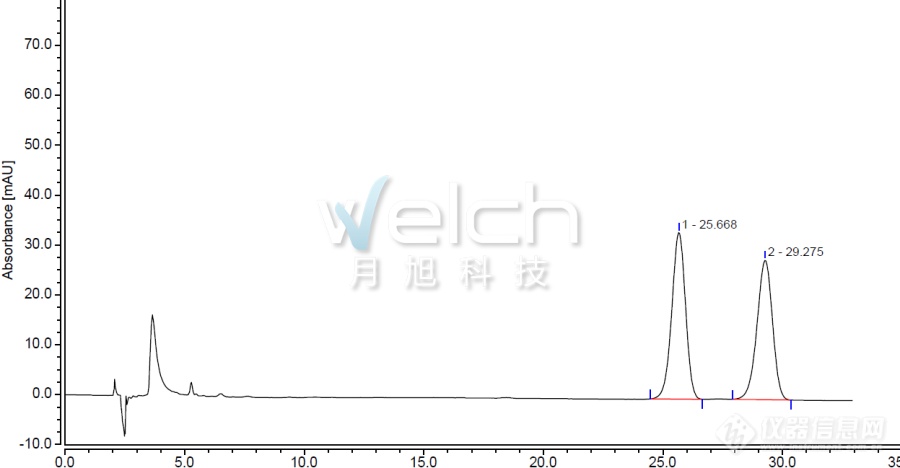
[color=#333333]今天为您带来月旭Ultimate XS-C18色谱柱对木瓜中[/color][color=#333333]齐墩果酸、熊果酸[/color][color=#333333]成分的测定效果。[/color][color=#333333][/color][color=#333333][b]色谱条件[/b][/color][color=#333333][/color]色谱柱:月旭Ultimate XS-C18(4.6×250mm,5μm)。流动相:甲醇/水/冰醋酸/三乙胺=265/35/0.1/0.05;检测波长:210nm;柱温:17℃;流速:1.0ml/min;进样量:20μL。[b]谱图和数据[/b][color=#333333][b][color=#333333]1、对照溶液[/color][/b][/color][align=center][color=#333333][b][img=,690,358]https://ng1.17img.cn/bbsfiles/images/2019/02/201902251715419094_6619_932_3.png!w690x358.jpg[/img][/b][/color][/align][align=center][color=#333333][b][img=,690,90]https://ng1.17img.cn/bbsfiles/images/2019/02/201902251715424933_8502_932_3.png!w690x90.jpg[/img][/b][/color][/align][align=center][color=#333333][b][/b][/color][/align][align=left][b]2、样品图[/b][/align][align=center][color=#333333][b][img=,690,360]https://ng1.17img.cn/bbsfiles/images/2019/02/201902251715428714_1404_932_3.png!w690x360.jpg[/img][/b][/color][/align][align=center][color=#333333][b][img=,690,90]https://ng1.17img.cn/bbsfiles/images/2019/02/201902251715432174_4788_932_3.png!w690x90.jpg[/img][/b][/color][/align][align=center][color=#333333][b][/b][/color][/align][align=left][b]3、齐墩果酸[/b][/align][align=center][color=#333333][b][img=,690,361]https://ng1.17img.cn/bbsfiles/images/2019/02/201902251715435974_6950_932_3.png!w690x361.jpg[/img][/b][/color][/align][align=center][color=#333333][b][img=,690,77]https://ng1.17img.cn/bbsfiles/images/2019/02/201902251715439594_8746_932_3.png!w690x77.jpg[/img][/b][/color][/align][align=center][color=#333333][b][/b][/color][/align][align=left][b]4、熊果酸[/b][/align][align=center][color=#333333][b][img=,690,361]https://ng1.17img.cn/bbsfiles/images/2019/02/201902251715442574_4489_932_3.png!w690x361.jpg[/img][/b][/color][/align][align=center][color=#333333][b][img=,690,75]https://ng1.17img.cn/bbsfiles/images/2019/02/201902251715446654_9441_932_3.png!w690x75.jpg[/img][/b][/color][/align][align=center][color=#333333][b][/b][/color][/align][align=left][color=#333333][b][color=#333333][b]结论[/b][/color][/b][/color][/align][align=left][color=#333333][color=#333333]使用月旭Ultimate XS-C18(4.6×250mm,5μm),在此色谱条件下,能满足检测需求。[/color][/color][/align]
各位高手:小弟刚接触薄层扫描,我在做六位地黄丸中熊果酸的扫描时候发现,斑点的颜色很快变化。扫描过程中就是对同一点的扫描数值上的差距也很大。怎么解决?我用的是cs930。请给点建议
测熊果酸在开始的有一个很大的负峰和一个正峰,猜测正峰是甲醇,到底是什么原因呢?标品怎么不出峰,我在220nm处也试了,都不合适!具体是什么原因,求指教条件是:流动相为甲醇:0.5%冰醋酸=90:10,进样量20微升,流速0.8ml/min,C18反相柱,熊果酸我查了文献大部分都是在210nm处测的,我也是这样测的,但为什么没有峰出现呢?

重赏之下,必有莽夫! 前段时间,本人做一中药复方中齐墩果酸的含测条件摸索,因为方法和操作的错误,导致了保留时间的大转移。实验做了三天才有点道道。下面一一给大家介绍。(唉,本人的实验能力还是太差了,学习啊。)一.样品分子结构http://ng1.17img.cn/bbsfiles/images/2010/04/201004181824_213006_1760187_3.jpg http://ng1.17img.cn/bbsfiles/images/2010/04/201004181825_213007_1760187_3.jpg齐墩果酸,CAS号:508-02-1 熊果酸,CAS号: 77-52-1它们两个是同分异构体。出峰顺序为:齐墩果酸,熊果酸。二.样品来源某中药复方颗粒剂,君药中含有齐墩果酸等化学成分,具有与复方相似的药理作用。于是,我们拟对齐墩果酸的含测条件进行摸索。样品处理为:取药材60%、70%、80%、92%、95%的醇提取液,水浴蒸干,加甲醇定容;取颗粒甲醇超声的续滤液,分别10000r/min离心10min后,取上清液注入高效液相色谱仪。齐墩果酸对照品来源于中国药品生物制品检定所。三.色谱条件:Agilent1100(四元泵、柱温箱、自动进样器、紫外检测器),月旭XB-C18,5μm,4.6*250mm,伊利特ODS2,5μm,4.6*250mm,柱温25℃,流速1ml/min,流动相为甲醇:0.1%磷酸(80:20)检测波长为210nm,进样量:10μl。色谱条件一共摸了三天,下面一一给大家介绍。齐墩果酸保留时间大转移(第一天)查阅资料得知,有人曾做过君药中齐墩果酸的含测。我们就先采用他的方法。甲醇:0.1%磷酸80:20。1ml/min。25℃。210nm。10μl。我们先用月旭柱,XB-C18,5μm,4.6*250mm。先随便找了一个以前师兄师姐配的齐墩果酸对照品,浓度未知,连续进了两针,图谱如下:http://ng1.17img.cn/bbsfiles/images/2010/04/201004181836_213013_1760187_3.jpg 图1http://
我最近做木通的含量测定,对照品是齐墩果酸,甲醇溶解,流动相按药典标准是甲醇:水:冰醋酸:三乙胺(87:13:0.04:0.02),结果对照品就是有个杂峰重叠,不知道怎么处理,知道的告诉我,谢谢
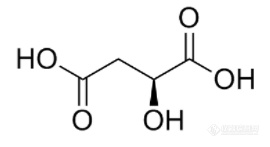
食品添加剂:L-苹果酸 沈皖豫摘要:L-苹果酸是一种四碳酸,广泛存在于自然界中。L-苹果酸是生物体内代谢的中间产物,可以通过发酵法、固定化细胞法、提取法和化学合成法等方法制取得到。L-苹果酸有多种快速检测含量的方法,根据国标和药典的标准,有滴定法、比旋光度法等方法。此外,作为食品添加剂,L-苹果酸的限量有多种方式,如测定溶液澄清度、检测灼烧残渣及检测杂质离子(或分子)含量。因其具有多种优点,L-苹果酸广泛应用于食品行业、医药行业、日化行业、化工行业,并具有保健功能。0. 前言[align=justify]L-苹果酸的CNS号为01.104,是国际上公认的一种安全性食品添加剂,其酸味持久柔和,既是一种优良的酸味剂,又具有重要的生理功能,可加强机体基础代谢,对提高机体健康水平有所裨益,已广泛应用于食品、日化、医药、养殖等行业。1. L-苹果酸的理化性质[align=justify]L-苹果酸的学名为L-羟基丁二酸,分子式为C4H6O5,相对分子质量为134.09[1],是手性苹果酸的一种,L-苹果酸是苹果酸在自然界的存在形式,其分子结构式可见图1。[img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107161807300897_3417_1608728_3.png[/img]图1 L-苹果酸结构式[align=justify]L-苹果酸为白色的结晶或结晶粉末,无臭,具有特殊的刺激性酸味,酸味较柠檬酸强20%(与其他果酸酸味度对比可见表1),呈味缓慢,保留时间较长,爽口但微有苦涩感。L-苹果酸的相对密度为1.595,熔点约100 ℃,分解点为140 ℃,比旋光度为-2.3°(8.5 g / 100 mL 水)。L-苹果酸的等量的左旋体和右旋体异构体混合得外消旋体,密度为1.601,熔点131-132 ℃,分解点为150 ℃[2]。表1 L-苹果酸与其他果酸酸味度的关系[img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107161807302456_8027_1608728_3.png[/img][align=justify]由于L-苹果酸含有羟基和羧基,故其易溶于水和乙醇,1 g L-苹果酸可分别溶于0.8 mL 水和1.4 mL 乙醇,微溶于乙醚,且溶解度随着温度升高而增大,水溶液为强酸性,1 %的水溶液的pH为2.40。L-苹果酸在水中可分两步电离,其中K1=3.9×10-4,K2=7.5×10-6。此外,L-苹果酸还能与醇类、浓硫酸、苯酚过氧化氢、三氯乙醛及醋酸铅发生反应,并能与β- 萘酚、间苯萘酚及2,7- 萘二酚作用,使溶液呈现出不同的颜色[3]。[align=justify]苹果酸是苹果的一种成分,人每日由蔬菜、水果摄取的苹果酸为1.5-3.0 g左右,从未发现不良反应,毒性极低。按日本食品添加剂标准,苹果酸应符合下列质量指标:含量 ≥ 99.0 %(质量),溶状、水溶液澄清,熔点127-130 ℃,重金属 ≤ 0.002 %(质量),氯化物 ≤ 0.0035 %(质量),铁 ≤ 0.004 %(质量),灼烧残留物 ≤ 0.05 %(质量)。按美国食用化学品法典(1983)规定,苹果酸应符合下列质量指标:含量 ≥ 99.5 %(质量)。熔点130-132 ℃,灰分 ≤ 0.1 %(质量),重金属(以Pb计) ≤ 0.002 %(质量),砷(以As计) ≤ 0.0003 %(质量),铅 ≤ 0.001 %(质量),富马酸 ≤ 0.5 %(质量),顺丁烯二酸 ≤ 0.05 %(质量),水不溶≤ 0.1 ‰(质量)。依据中国食品安全国家标准,苹果酸应符合的质量标准可见表2。表2 L-苹果酸的理化指标(GB 1886.40-2015)[img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107161807304868_8925_1608728_3.png[/img][align=justify]2. L-苹果酸的生产2.1 L-苹果酸的生理来源L-苹果酸作为人体代谢过程产生的重要有机酸,是三羧酸循环(TCA循环)(图2)及其支路乙醛酸循环(图3)代谢过程中的重要中间产物,也是CO2固定反应的中间产物。可以迅速通过细胞膜进入线粒体内,直接参与线粒体能量代谢。同时,L-苹果酸还是苹果酸天冬氨酸穿梭的组成部分,对胞液和线粒体之间还原当量(NADH)的转移起着重要的作用(图4)。胞质中的NADH在脱氢酶的作用下,使草酰乙酸还原成苹果酸,后者通过线粒体内膜上的α-酮戊二酸转运蛋白(OMC)进入基质,在基质脱氢酶的作用下重新生成草酰乙酸和NADH,NADH进入电子呼吸链生成ATP,而基质内生成的草酰乙酸经谷草转氨酶的作用生成天冬氨酸,后者经酸性氨基酸转运载体(AGC)转运出基质再转变成草酰乙酸,继续进行穿梭。此外,L-苹果酸还可以减少机体组织内自由基的产生或加速自由基的清除,缓解体力疲劳,增加机体耐力[4]。[img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107161807305868_3179_1608728_3.png[/img]图2 三羧酸循环产生苹果酸中间产物过程[img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107161807307206_3230_1608728_3.jpeg[/img]图3 乙醛酸循环产生苹果酸中间产物过程[img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107161807308173_5082_1608728_3.jpeg[/img]图4 苹果酸天冬氨酸穿梭示意图2.2 L-苹果酸的工业生产由于L-苹果酸属于发酵生产的产品,安全性能有保障,因此,国际市场上需求量快速增加。世界苹果酸主要生产国有美国、[url=https://baike.so.com/doc/3872656-4065468.html]加拿大[/url]、日本等,世界总产量每年约为10万吨,其中L-苹果酸产量每年约为4万吨,而世界市场潜在需求量达到每年6万吨,可见市场发展空间之大。日本是世界主要的L-苹果酸生产国与出口国。目前,L-苹果酸的生产方法已由早期的单一的提取法发展到以下几种方法:提取法、化学合成法、一步发酵法、二步发酵法、固定化酶或细胞转化法。2.2.1 发酵法苹果酸发酵工艺主要有三种,分别是一步发酵法、两步发酵法和酶法转化法。不同的苹果酸发酵工艺要采用不同的工艺。一步法发酵工艺采用的微生物有黄曲霉、米曲霉和寄生曲霉;两步法及混合发酵法采用的有华根酶、无根根酶、短乳杆酶、膜醭毕赤酵母;酶法转化有短乳杆菌、大肠杆菌、产氨短杆菌和黄色短杆菌。一步发酵又称为直接发酵法,其利用的微生物最大的特点,是三羧酸循环中苹果酸到草酰乙酸这一步的苹果酸脱氢酶缺失或处于低水平,使得苹果酸得以积累。这些菌株大多具有糖化淀粉的能力,可以直接利用淀粉质原料,原料来源十分丰富,发酵工艺条件温和,产品为L型,因此一步发酵法与其他方法相比更具优势。两步发酵法也是用糖类为原料,采用两种不同功能的微生物,其中一种先将糖质或其他原料转化生成富马酸,即延胡索酸,另一种微生物将富马酸转化成L-苹果酸,如先用根酶发酵成富马酸(或富马酸-苹果酸混合物),再由酵母或细菌转化成苹果酸[5]。两种微生物可先后加入,也可同时加入。由于两步法涉及到两种微生物,培养条件要求比较严格,发酵周期较长,产酸率相对较低,副产物较多,当前规模生产较少。发酵法的工艺流程图可见图4。[img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107161807309140_6935_1608728_3.png[/img]图4 发酵法制备L-苹果酸的工艺流程示意图酶法转化法是用富马酸(盐)或马来酸为原料,用微生物酶(包括全细胞)转化成苹果酸,发酵方法利用了微生物酶的立体异构专一性,生产的都是L-苹果酸,是生物体内存在和可利用的构型(图5)。[img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107161807310356_7095_1608728_3.png[/img]图5 酶法转化法过程2.2.2 固定化细胞法此工艺一般包括两步,一是固定化细胞的制备:将产酶菌株培养成熟后,收集菌体细胞,包埋菌体,制备固定化酶或细胞,用于生产L-苹果酸,通常在37 ℃ 条件下运行,转化半衰期可达160天左右;二是L-苹果酸制备:先将富马酸和CaCO3反应转化成为富马酸钙,再经转化柱作用生成苹果酸钙,经提取得L-苹果酸。目前这种方法生产L-苹果酸的转化率可达到98 % 以上。固定化细胞法具有比表面积大、包容量大、孔道阻力小的高效膜状载体,图6为固定化细胞法制备苹果酸的工艺流程。[img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107161807311323_8948_1608728_3.png[/img]图6 固定化细胞法制备L-苹果酸的工艺流程示意图2.2.3 提取法由于L-苹果酸在水中的溶解度很大,采用提取法得到L-苹果酸时具有很大的难度,目前各工厂常用的提取方法为硫酸酸解法及有机溶剂萃取法两类。有机溶剂萃取法采用乙醚将发酵液中的苹果酸转入有机相中,蒸除乙醚后获得结晶。因乙醚消耗量较大,故成本较高。硫酸酸解法[6]的步骤是用浓硫酸将在发酵液中已形成的苹果酸钙酸解成苹果酸,稀苹果酸经减压浓缩并制成50 % 浓缩液或粗制苹果酸晶体,其具体步骤如图7所示。[img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107161807312651_6756_1608728_3.png[/img]图7 硫酸酸解法提取苹果酸的流程示意图硫酸酸解法的优点是操作简便、原材料成本低廉。但也存在缺点,如苹果酸母液中的Ca2+成分较高,因硫酸钙溶解度高达0.106 g,会严重妨碍苹果酸结晶,此外,母液中过量的H2SO4,在浓缩过程中极易引起苹果酸碳化。鉴于此,可将使用草酸全部或部分代替硫酸,这样既提高了脱钙效率,又避免在浓缩过程中母液碳化,最终能获得好的结晶。2.2.4 化学合成法在催化剂存在下,苯氧化生成富马酸或马来酸,然后加压与水蒸汽共热形成DL-苹果酸;也可以糠醛为原料,经双氧水处理,在超声波作用下转变而成。生产的DL-苹果酸经拆分、提取获得L-苹果酸[7]。这种方法由于生产工艺比较复杂,工艺条件要求高,分离精制技术难度大,加之原料为化工产品,应用受到限制,目前较少采用。3. L-苹果酸的检测L- 苹果酸具有生物活性,是一种国际上公认安全的食品添加剂。与传统酸味剂柠檬酸相比,苹果酸具有酸味柔和爽口、热量低等优点,更符合高品位饮食文化要求。随着食品和医药领域的发展,其应用领域正不断扩展,L-苹果酸的快速检测也不断地深入。本标准中所用的试剂和水在未注明其他要求时,均指分析纯试剂和GB/T 6682[8]规定的三级水。试验中所用的标准滴定溶液、杂质测定用标准溶液、制剂及制品,在没有注明其他要求时,均按GB/T 601[9]、GB/T 602[10]和GB/T 603[11]的规定制备。试验中所用溶液在未注明用何种溶剂配制时,均指水溶液。3.1 L-苹果酸的鉴别国标规定的L-苹果酸的鉴别方法所需的试剂为:氨水溶液(2+3)、对氨基苯磺酸溶液(10 g/L)、亚硝酸钠溶液(200 g/L)、氢氧化钠溶液(40 g/L)。称取0.5 g 试样,精确至0.01 g,置于50 mL 试管中,加入10 mL 水溶解。用氨水溶液中和至中性,加入1 mL 对氨基苯磺酸溶液,在沸水浴中加热5 min。加入5 mL 亚硝酸钠溶液,再置于水浴加热3 min 后,加入5 mL 氢氧化钠溶液,试验溶液应立呈现红色。3.2 滴定法检测L-苹果酸含量以酚酞为指示剂,用氢氧化钠标准滴定溶液滴定试样水溶液,根据氢氧化钠标准溶液的用量,计算以C4H6O5计的总酸含量的L-苹果酸。本法所用的试剂为:无二氧化碳的水、氢氧化钠标准滴定溶液(c(NaOH)=1.0 mol/L)、酚酞指示剂(10 g/L)。称取2.0 g 试样,精确至0.0002 g,加20 mL 无二氧化碳的水溶解,加2滴酚酞指示剂,用氢氧化钠标准溶液滴定至微红色,保持30 s 不褪色为终点。在测定的同时,按与测定相同的步骤,对不加试样而使用相同数量的试剂溶液做空白试验。L-苹果酸(C4H6O5)的质量分数ω=。式中:V1 ——试样消耗氢氧化钠标准滴定溶液的体积,单位为毫升(mL)V0 ——空白试验消耗氢氧化钠标准滴定溶液的体积,单位为毫升(mL)1000 ——换算系数c ——氢氧化钠标准滴定溶液的浓度,单位为摩尔每升(mol/L)M ——L-苹果酸的摩尔质量,单位为克每摩尔(g/mol),[M(?C4H6O5)=67.04]m ——试样的质量,单位为克(g)3.3 比旋光度法检测L-苹果酸含量称取4.25 g 试样,精确至0.001 g,加入20 mL 水溶解,移至50 mL 容量瓶,用水稀释至刻度,摇匀。其检测方式按GB/T 613[12]规定施行。比旋光度αm(20 ℃,D),以“(°)dm2kg-1”表示,αm(20 ℃,D)=。式中:α ——测得的旋光角,单位为度(°)L ——旋光管的长度,单位为分米(dm)ρα ——溶液中有效组分的质量浓度,单位为克每毫升(g/mL)3.4 Goodban法检测L-苹果酸含量该法使用的试剂为:98 % 硫酸(不含硝酸)、2,7-萘二酚溶液(1 g 2,7-萘二酚溶于100 mL 上述硫酸中)。取1 mL 样品溶液(控制苹果酸含量在5-80 μg)置于25×200 mm 具塞比色管中,沿管壁缓慢加入6 mL 98 % 硫酸,然后加入0.1 mL 2,7-萘二酚溶液,100 ℃ 水浴加热20 min,冷却至室温后,在390 nm 处比色测定。浓硫酸与2,7-萘二酚共热后,可产生有色物质。此法需同时以水样做空白,以供调零使用。根据在390 nm 处测定的吸光度数值,可从标准溶液样品中查得L-苹果酸的含量[13]。3.5 高压液相色谱法检测L-苹果酸含量样品处理后,注入反向化学键合色谱体系,用0.5 % (NH4)2HPO4为流动相。经紫外检测器(214 nm)或示差折射检测器测定和与标准进行对比定量。4. L-苹果酸的限量4.1 食品添加剂L-苹果酸的限量标准作为食品添加剂,L-苹果酸以其爽口味道和无毒性有很大的优势,广泛应用于各类食品中。如:乳及乳制品、脂肪,油和乳化脂肪制品、冷冻饮品、水果,蔬菜,豆类,食用菌,藻类,坚果及籽类、可可制品,巧克力和巧克力制品、糖果、粮食和粮食制品、焙烤食品、肉及肉制品、水产及其制品、蛋及蛋制品、甜味料、调味品、特殊膳用食品、饮料类、酒类,等等。在以上食品中,L-苹果酸皆可适量添加。4.2 L-苹果酸的限量方法4.2.1 溶液的澄清度将试样溶解后,与标准比浊溶液进行比较。本法所用的试剂为:硝酸溶液(1+2)、糊精溶液(20 g/L)、硝酸银溶液(20 g/L)、盐酸标准溶液(c(HCl)=0.1 mol/L)、浊度标准溶液(含氯0.01 mg/mL。量取c(HCl) 0.1 mol/L 盐酸标准滴定溶液14.1 mL±0.02 mL,置于50 mL 容量瓶中,稀释至刻度;量取该溶液10 mL±0.02 mL 于1000 mL容量瓶中,加水稀释至刻度,摇匀)。称取约1.0 g试样,精确至0.01 g,置于比色管中,加入20 mL 水溶解,作为试样溶液;取另一支比色管,准确加入0.5 mL浊度标准溶液,加水至20 mL,加1 mL 硝酸溶液、0.2 mL 环糊精溶液及1 mL硝酸银溶液,摇匀,避光放置15 min,作为标准比浊溶液。在无阳光直射情况下,轴向及侧向观察,试样溶液的浊度不大于标准比浊溶液的浊度,即为通过试验。4.2.2 灼烧残渣的测定称取2.5 g 试样,精确至0.0001 g,按GB/T 9741[14]标准施行。取两次平行测定结果的算数平均值为测定结果,两次平行测定结果的绝对差不大于0.02 %。4.2.3 硫酸盐(以SO4计)的测定在酸性(盐酸)溶液中,试样中的硫酸盐和氯化钡生成硫酸钡白色沉淀,与标准比浊溶液进行比较,做限量检测。所用试剂有:盐酸溶液(1+4)、氯化钡溶液(250 g/L)、硫酸盐(SO4)标准溶液(0.1 mg/mL)。称取1 g 试样,精确至0.01 g,置于50 mL 比色管中,同时量取2 mL±0.02 mL 硫酸盐(SO4)标准溶液置于另一支50 mL比色管中。两支比色管中分别加入0.5 mL 盐酸溶液、1 mL 氯化钡溶液,用水稀释至刻度,摇匀。放置10 min 后观察,试样溶液产生的浊度不深于标准比浊溶液的浊度,即为通过试验。4.2.4 氯化物(以Cl计)的测定所用试剂为氯化物(Cl)标准溶液(0.1 mg/mL)。称取1 g 试样,精确至0.01 g。量取0.4 mL 氯化物(Cl)标准溶液(含氯化物0.04 mg)制备限量标准液。样品所呈浊度不得大于标准。按GB/T 9729[15]标准施行。4.2.5 富马酸或马来酸的测定用高效液相色谱法,在选定的工作条件下,通过色谱柱使试样中各组分分离,用紫外吸收检测器检测,用外标法定量,计算试样中富马酸和马来酸的含量。称取0.2 g 试样,精度至0.0002 g,置于50 mL 容量瓶中,用磷酸溶液稀释至刻度,摇匀,经0.45 μm 滤膜过滤,再经超声波脱气处理。富马酸或马来酸的质量分数ω=。式中:A1——试样溶液色谱图中待测物质的峰面积m2——标准溶液中富马酸或马来酸的进样量,单位为微克(μg)A2——标准溶液色谱图中富马酸或马来酸的峰面积m3——试样的进样量,单位为微克(μg)4.2.6 钙法测定取本品1.0 g,加水10 mL 使溶解,加5 % 醋酸钠溶液20 mL,摇匀,取15 mL,加2 mol/L 醋酸溶液1 mL,摇匀,作为供试品溶液;另取标准钙溶液(精密称取碳酸钙2.50 g,置1000 mL 量瓶中,加5 mol/L 醋酸溶液12 mL,加水适量使溶解并稀释至刻度,摇匀,作为钙贮备溶液。临用前,精密量取钙溶液贮备液1 mL,置100 mL 容量瓶中,加水稀释至刻度,摇匀,每1 mL 中含Ca 10 μg/10.0 mL,加2 mol/L 醋酸溶液1 mL 与水5 mL,摇匀,作为对照品溶液。取醇制标准钙溶液(临用前,精密量取钙溶液贮备液10 mL,置100 mL 量瓶中,用乙醇稀释至刻度,摇匀。每1 mL 中含Ca 0.1 mg/0.2 mL,置纳氏比色管中,加4 % 草酸铵溶液1 mL,1分钟后,加入供试品溶液,摇匀,放置15分钟后,与同法制成的对照液比较,不得更浓(0.02%)[16]。5. L-苹果酸的应用随着各领域行业的发展,L-苹果酸已广泛应用于多个领域,如食品领域用作食品添加剂、医药行业、日化行业、化工行业,等等。5.1 L-苹果酸用于食品行业[17]L-苹果酸为天然果汁的重要成分,与柠檬酸相比,具有酸度大、但味道柔和(具有较高的缓冲指数)、具特殊香味、不损害口腔与牙齿、代谢上有利于氨基酸吸收、不积累脂肪等优点,是新一代的食品酸味剂,被生物界和营养界誉为“最理想的食品酸味剂”。L-苹果酸是人体必需的一种有机酸,也是一种低热量的理想食品添加剂。当50 % 的L-苹果酸与20 % 柠檬酸共用时,可呈现出强烈的天然果实风味。在各种清凉饮料中,应用L-苹果酸配制的软饮料解渴爽口,有苹果酸味,接近天然果汁。国内一些大型食品公司,如娃哈哈集团、健力宝集团在饮料中使用L-苹果酸。L-苹果酸是生物体中三羧酸循环的中间体,口感接近天然果汁并具有天然香味,与柠檬酸相比,产生的热量更低,口味更好,因此广泛应用于酒类、饮料、果酱、口香糖等多种食品中,是目前世界食品工业中用量最大和发展前景较好的有机酸之一。5.1.1 L-苹果酸作酸味调节剂L-苹果酸口感接近天然苹果的酸味,已广泛用于高档饮料、食品等行业,已成为继柠檬酸、乳酸之后用量排第三位的食品酸味剂。用L-苹果酸配制的饮料更加酸甜可口,有接近天然果汁的风味。苹果酸与柠檬酸配合使用,可以模拟天然果实的酸味特征,使口感更自然、协调、丰满。清凉饮料、粉末饮料、乳酸饮料、乳饮料、果汁饮料中均可添加苹果酸改善其口感和风味。苹果酸常与人工合成的二肽甜味剂阿斯巴甜(ASPARTME)配合使用,作为软饮料的风味固定剂添加。100 g 苹果酸比100 g 柠檬酸几乎要强1.25倍,或者说80 g 的苹果酸和100 g 的柠檬酸形成的酸味强度是相当的,因此要达到相同的酸味强度,使用L-苹果酸可以减少20 % 的用量,对于一些食品加苹果酸可以节省白糖10 % 到20 %,由于它的酸味刺激效果优于柠檬酸,而且美国FDA(食品和药物管理局)已限制柠檬酸在儿童和老年食品中的应用,所以,近几年来L-苹果酸在食品工业上的应用已逐渐取代柠檬酸。5.1.2 L-苹果酸的发酵功能L-苹果酸是生物体三羧酸循环的中间体,可以参与微生物的发酵过程,可以作为微生物生长的碳源,因此可以用于食品发酵剂。如可以做酵母生长促进剂,也可以加入发酵乳中。5.1.3 L-苹果酸的凝胶作用当有一定量的果胶和糖时,酸是凝胶形成的关键条件。浓缩果汁的生产要防止产生絮凝和凝块,就要控制有果胶引起的凝聚的条件。L-苹果酸有使果胶产生凝胶的作用,因此可以用来制作果糕、果冻凝胶态的果酱和果泥等。5.1.4 L-苹果酸作保鲜剂L-苹果酸可广泛地用于食品保鲜剂。微生物需要在一定酸碱度的环境中才能正常地进行生长繁殖,如果环境中的pH值不适宜,则可能影响细胞表面的带电性质,从而引起膜的通透性能的变化,影响细胞的正常代谢。酸类对微生物的作用,不仅与氢离子的浓度成正比,而且与有机酸兼有的抗氧化作用、酸的阴离子及未电离的分子有关。苹果酸在中性条件下电离而在酸性条件下不电离,但酸性条件下的杀菌能力却比中性条件大100倍以上,主要是因为分子状态的有机酸更容易透过细胞膜起作用,而离子状态的酸不易透过细胞。另外还可以促进蛋白质的热变性。L-苹果酸可以抑制酶促褐变。切割蔬菜是国外兴起的一种新型蔬菜加工产品,因其具有方便性,快捷性等特点,受到人们的日益青睐。马铃薯是我国一种重要的经济作物,它的褐变引起了人们的关注。苹果酸可以降低pH值,产生螯合作用,以抑制酚氧酶的活力,防止褐变,另外也对其他一些原因的褐变起抑制作用。5.1.5 L-苹果酸作除腥除臭剂L-苹果酸可用作除臭剂,可去除鱼腥,体臭。用于食品贮藏,在牛奶中加入L-苹果酸,还可改善质量。5.1.6 L-苹果酸作面食强化剂L-苹果酸对面食具有强化效果。它可以使面筋蛋白质中的二硫基团增多,蛋白质分子变大,形成大分子网络结构,增强面团的透气性、弹性和韧性。另外,面粉中含有半胱氨酸和胱氨酸,它们是蛋白酶激活剂,L-苹果酸可以使这两种氨基酸丧失激活蛋白酶的能力,阻止蛋白酶分解面粉中的蛋白质。另外还可以对面粉进行漂白,提高蛋白质的黏结作用。5.1.7 L-苹果酸的减盐作用L-苹果酸可用于制作咸味食品,减少食盐用量。如苹果酸钠咸度适中,常可用来制作带盐咸味的食物。苹果酸可形成许多衍生物,应用苹果酸的某些盐类代替食盐浸渍咸菜时,其咸味在仅有食盐七分之一到五分之一的情况下,浸渍效果却是食盐的两倍。同时可以作为肾炎患者的食盐代用品,在豆浆中添加苹果酸钙盐,可有效地改善其口感和风味。5.1.8 L-苹果酸的保护维生素C、保色作用果蔬中所含的色素的色调,往往受到酸碱度的影响,在一些变色反应中,酸往往是起到很重要作用的成分。如叶绿素在酸性环境中会变成黄褐色的脱镁叶绿素;花色素在酸性到中性的范围变化时,会由红色逐渐趋向紫色;单宁物质在酸性下会形成粉红色的“红粉”,等等。因此L-苹果酸可以用作一些食品的保色剂,比如可以做天然果子露保色剂。5.1.9 L-苹果酸的抗氧化、抑制油脂酸败作用L-苹果酸有较好的抗氧化能力。食品中脂类的氧化会导致酸败、蛋白质破坏和色素氧化,使食品的感官性质下降、营养价值降低、货架期缩短。添加食品抗氧化剂可延缓氧化、延长货架期、保持食品的色香味和营养价值。5.2 L-苹果酸用于医药行业[18][color=#000000]L[/color][color=#000000]-[/color][color=#000000]苹果酸可以用于治疗肝病、贫血、免疫力低下、尿毒症、高血压、肝衰竭等多种疾病,并能减轻抗癌药物对正常细胞的毒害作用;还可用于制备和合成驱虫剂、抗牙垢剂等。[/color]在各种片剂、糖浆中,配以苹果酸可以呈现水果味,并有利于在体内的吸收和扩散,它常配入[url=https://baike.so.com/doc/6978231-7200932.html]复合氨基酸[/url]注射液中,以提高氨基酸的利用率。它的钠盐是治疗肝功能不全特别是高血压症的有效药物。L-苹果酸钾是良好的钾补充药,它能保持人体水分平衡,治疗水肿、高血压和脂肪积聚症等。5.3 L-苹果酸用于日化行业[color=#000000]L[/color][color=#000000]-[/color][color=#000000]苹果酸可以配制多种香精、香料,用于多种日用化工产品,如牙膏、洗发香波等;与柠檬酸相比,L[/color][color=#000000]-[/color][color=#000000]苹果酸其酸味柔和别致,因此国外将其用于替代柠檬酸作为新型洗涤助剂,用于合成高档特种洗涤剂。[/color][color=#000000]如[/color]L-苹果酸锌可用于牙膏中,作为抗菌斑斑剂和抗牙结石剂,合成香料配方等。在护肤方面,[color=#000000]L[/color][color=#000000]-[/color][color=#000000]苹果酸中含有天然的润肤成分,能够很容易地溶解粘结在干燥鳞片状的死细胞之间的[/color][color=#000000]“[/color][color=#000000]胶粘物[/color][color=#000000]”[/color][color=#000000],从而可以清除皮肤表面皱纹,[/color]温和地去除老废多余的角质,加强肌肤代谢,[color=#000000]使皮肤变得嫩白、光洁而有弹性,因此在化妆品配方中备受青睐[/color][color=#000000]。此外,利用[/color]苹果萃取液,能够有效减淡皱纹及紧致肌肤,有唤醒疲倦肌肤,让暗淡的肌肤变得均匀明亮的效果。如金缕梅萃取有控油、镇静、安抚,帮助肌肤再生的功能;蛇麻草萃取有深层滋润,防止肌肤老化的效果。苹果紧致毛孔收缩水具有调理肌肤油脂分泌,加强毛孔细致度的功效,很适合毛孔粗大型肌肤。5.4 L-苹果酸用于化工行业L-苹果酸可用作除垢剂、荧光增白剂的合成原料之一。添加到虫胶清漆或其它清漆中,可防止漆面结皮,用该种酸生产的聚脂树脂和醇酸树脂是有特殊用途的塑料。5.5 L-苹果酸的保健功能L-苹果酸为机体[url=https://baike.so.com/doc/1202812-1272296.html]三羧循环[/url]的重要中间产物,且机体内只有L-苹果酸脱氢酶,所以从结构和实际生理环境来看,都必须利用L-苹果酸。美国已明确规定在婴幼儿食品、饮料、药品中,不能使用DL-苹果酸而必须使用L-苹果酸。就食品对维持生命的作用来看,其实质是参与[url=https://baike.so.com/doc/5366466-5602178.html]新陈代谢[/url]和能量转化。蛋白质、脂类、[url=https://baike.so.com/doc/5682009-5894684.html]糖类[/url]等,最后都要经过三羧循环氧化供能,这是转化过程的最后一步,也是最为重要的一步,关系到人体生理机能是否正常。由此食品与健康可有机地统一起来。而苹果酸的保健功效就在于防止人体由于L-苹果酸的缺乏导致三羧循环不正常,导致代谢失调。L-苹果酸具有生理活性,广泛地存在于生物体内,但是其含量的多少因人而异。L-苹果酸及相关产品在食疗方面具备的保健功效如下。由于苹果酸在物质代谢途径中所处的特殊位置,其可直接参与人体代谢,被人体直接吸收,实现短时间内向[url=https://baike.so.com/doc/546630-578663.html]肌体[/url]提供能量,消除疲劳,起到抗疲劳、迅速恢复体力的作用。可利用苹果酸的抗疲劳、护肝、肾、心脏作用,开发保健饮料。L-苹果酸使得代谢正常运行,从而各种营养物质得以顺利分解,促进食物在人体内吸收代谢。因其低热量,可有效地防止肥胖,可以起到减肥的作用。在药物中添加苹果酸可增加其稳定性,促进药物在人体的吸收和扩散。复合氨基酸输液生产中,利用L-苹果酸这一功能来调节pH值,同时作为混合氨基酸输液组分之一,可提高氨基酸利用率,用于治疗尿毒症、高血压等和减少抗癌药物对正常细胞的侵害,用于癌症放、化疗后的辅助药物,用于烧伤治疗可以促进伤口愈合。L-苹果酸可以促进氨代谢,降低血氨浓度,对[url=https://baike.so.com/doc/4135609-4335187.html]肝脏[/url]有保护作用,是治疗肝功能不全、肝衰竭、肝癌尤其是肝功能障碍导致的高血氨症的良药。L-苹果酸作为治疗心脏病基础液成分之一,用于K+、Mg2+的补充,保持心肌的能量代谢,对心肌梗塞的缺血性心肌层起到保护作用。L-苹果酸是[url=https://baike.so.com/doc/3719782-3908677.html]乳酸[/url]钙注射液的[url=https://baike.so.com/doc/5341992-5577435.html]稳定剂[/url],也可作为抗癌药的前体及用作动物生长促进剂。L-苹果酸酸度大、味道柔和、香味独特;苹果酸的腐蚀破坏作用比较弱,相应的牙釉质磨损体积损失较小,有不损害口腔和牙齿等特点。故有抗牙垢的功能。可以改善脑组织的能量代谢,调整脑内神经递质,有利于学习记忆功能的恢复,对学习、记忆有明显的改善作用。褪黑素(MT)是主要由松果腺分泌的吲哚类激素,具有多种生物活性。大量的动物实验和临床研究表明,褪黑素具有良好的镇静催眠作用。褪黑素催眠作用与谷氨酸脱羧酶有关,而L-苹果酸是一个比较理想的[url=https://baike.so.com/doc/7867049-8141144.html]谷氨酸脱羧酶[/url]抑制剂。因此L-苹果酸或许可以减少睡眠、提高兴奋度。L-苹果酸对人体[url=https://baike.so.com/doc/4766467-4982095.html]血管[/url]内皮细胞有保护作用,对损伤内皮细胞效应具有抵抗作用。6. 总结与展望L-苹果酸是一种具有良好口感、热量低、、无毒性、有生理活性的四碳酸,作为食品添加剂广泛应用于食品工业领域,且在医疗、日化、化工行业中也有着重要的作用。现今,作为食品添加剂,L-苹果酸以其优越性已逐渐代替柠檬酸,产量日益增长,仅次于柠檬酸和乳酸。其添加在食品中含量适量,且已有较为成熟的快速检测和限量方法。日前,提取法和一步发酵法仍是L-苹果酸的主要生产方法。因L-苹果酸的优势和广泛应用,其制取方法仍有待改善,在应用领域也需不断拓宽深化。参考文献:[color=#333333][back=#ffffff][1][/back][/color][color=#333333][back=#ffffff] [/back][/color][color=#333333][back=#ffffff]GB 1886.40-2015[/back][/color][color=#333333][back=#ffffff] [/back][/color][color=#333333][back=#ffffff]食品安全国家标准 食品添加剂 L-苹果酸[/back][/color][color=#333333][back=#ffffff].[/back][/color][color=#333333][back=#ffffff][2] [/back][/color][color=#333333][back=#ffffff]国家药典委员会. 中华人民共和国药典[M]. 北京:中国医药科技出版社, 2015.[/back][/color][color=#333333][back=#ffffff][3] [/back][/color][color=#333333][back=#ffffff]吴清平,周小燕.L-苹果酸研究进展[J].微生物学通报,1990,(01):30-33.DOI:10.13344/j.microbiol.china.1990.01.010 [/back][/color][color=#333333][back=#ffffff][4] [/back][/color][color=#333333][back=#ffffff]L-苹果酸的生理特性及应用进展[J].饮料工业,2020,23(04):74-77.[/back][/color][5] [color=#333333][back=#ffffff]王锐清.L-苹果酸的生产及应用研究进展[J].化工时刊,2002(05):1-7.[/back][/color][color=#333333][back=#ffffff][6] 冯大炎,张林普.L-苹果酸发酵与提取的研究初报[J].发酵科技通讯,1991(04):17-21.[/back][/color][color=#333333][back=#ffffff][7] [/back][/color][color=#333333][back=#ffffff]刘建军,姜鲁燕,赵祥颖,李丕武,田延军,张家祥.L-苹果酸的应用及研究进展[J].中国食品添加剂,2003(03):53-56+52.[/back][/color][color=#333333][back=#ffffff][8] [/back][/color][url=http://std.samr.gov.cn/gb/search/gbDetailed?id=71F772D774B1D3A7E05397BE0A0AB82A][color=#333333][back=#ffffff]GB/T?6682-2008[/back][/color][/url][color=#333333][back=#ffffff] [/back][/color][color=#333333][back=#ffffff]分析实验室用水规格和试验方法[/back][/color][color=#333333][back=#ffffff].[/back][/color][color=#333333][back=#ffffff][9] [/back][/color][url=http://std.samr.gov.cn/gb/search/gbDetailed?id=71F772D816D7D3A7E05397BE0A0AB82A][color=#333333][back=#ffffff]GB/T?601-2016[/back][/color][/url][color=#333333][back=#ffffff] [/back][/color][color=#333333][back=#ffffff]化学试剂 标准滴定溶液的制备[/back][/color][color=#333333][back=#ffffff].[/back][/color][color=#333333][back=#ffffff][10] [/back][/color][url=http://std.samr.gov.cn/gb/search/gbDetailed?id=71F772D79132D3A7E05397BE0A0AB82A][color=#333333][back=#ffffff]GB/T?602-2002[/back][/color][/url][color=#333333][back=#ffffff] [/back][/color][color=#333333][back=#ffffff]化学试剂 杂质测定用标准溶液的制备[/back][/color][color=#333333][back=#ffffff].[/back][/color][color=#333333][back=#ffffff][11] [/back][/color][url=http://std.samr.gov.cn/gb/search/gbDetailed?id=71F772D79131D3A7E05397BE0A0AB82A][color=#333333][back=#ffffff]GB/T?603-2002[/back][/color][/url][color=#333333][back=#ffffff] [/back][/color][color=#333333][back=#ffffff]化学试剂 试验方法中所用制剂及制品的制备[/back][/color][color=#333333][back=#ffffff].[/back][/color][color=#333333][back=#ffffff][12] [/back][/color][url=http://std.samr.gov.cn/gb/search/gbDetailed?id=71F772D76EA4D3A7E05397BE0A0AB82A][color=#333333][back=#ffffff]GB/T?613-2007[/back][/color][/url][color=#333333][back=#ffffff] [/back][/color][color=#333333][back=#ffffff]化学试剂 比旋光本领(比旋光度)测定通用方法[/back][/color][color=#333333][back=#ffffff].[/back][/color][color=#333333][back=#ffffff][13] [/back][/color][color=#333333][back=#ffffff]尹志梅,杨青,吴秀敏,徐谦.L-苹果酸定量检测方法[J].中国酿造,1999(04):33-34.[/back][/color][color=#333333][back=#ffffff][14] [/back][/color][url=http://std.samr.gov.cn/gb/search/gbDetailed?id=71F772D777B3D3A7E05397BE0A0AB82A][color=#333333][back=#ffffff]GB/T?9741-2008[/back][/color][/url][color=#333333][back=#ffffff] [/back][/color][color=#333333][back=#ffffff]化学试剂 灼烧残渣测定通用方法[/back][/color][color=#333333][back=#ffffff].[/back][/color][color=#333333][back=#ffffff][15] [/back][/color][url=http://std.samr.gov.cn/gb/search/gbDetailed?id=71F772D7684DD3A7E05397BE0A0AB82A][color=#333333][back=#ffffff]GB/T?9729-2007[/back][/color][/url][color=#333333][back=#ffffff] [/back][/color][color=#333333][back=#ffffff]化学试剂 氯化物测定通用方法[/back][/color][color=#333333][back=#ffffff].[/back][/color][color=#333333][back=#ffffff][16] [/back][/color][color=#333333][back=#ffffff]国家药典委员会.[/back][/color][color=#333333][back=#ffffff] [/back][/color][color=#333333][back=#ffffff]中国药典[M].[/back][/color][color=#333333][back=#ffffff] [/back][/color][color=#333333][back=#ffffff]北京:中国医药科技出版社[/back][/color][color=#333333][back=#ffffff],[/back][/color][color=#333333][back=#ffffff]2020[/back][/color][color=#333333][back=#ffffff].[/back][/color][color=#333333][back=#ffffff][17] [/back][/color][url=http://www.foodbk.com/wiki/%E8%8B%B9%E6%9E%9C%E9%85%B8][color=#333333][back=#ffffff]食品百科全书 - 苹果酸 (foodbk.com)[/back][/color][/url][color=#333333][back=#ffffff][18] [/back][/color][color=#333333][back=#ffffff]张居尚,杨新文,雷萍,孙悦迎,张文隽,张慧.利用苹果渣发酵生产L-苹果酸工艺研究[J].食品科学,2009,30(02):127-129. [/back][/color]
[color=#444444]要定标准检测坚果大豆,杏仁,碧根果酸价,过氧检测,样品需要去多少克?[/color]
用0.02moL/L磷酸二氢钠作流动相测有机酸,苹果酸标品有两个峰(保留时间2.4和4.0),而柠檬酸标品保留时间4.1,柠檬酸与苹果酸第二个峰分不开,看文献上说第一个峰是天然存在的L型苹果酸,第二个峰可能由于苹果酸原样品中含有苹果酸衍生物。那测样品怎么定量呢?哪位朋友能帮忙回答下
采用gc-ms测试有机酸,现手上只有丙二酸、草酸、柠檬酸、苹果酸和己二酸(内标)标准品,由于时间关系来不及买其他有机酸标准品,那么该如何计算检索到样品中的硬脂酸,油酸等其它有机酸?请老师指点!
1.测果树中的有机酸,标准品该怎么选择,应该选DL型吗?2.测DL苹果酸会出现两个峰,应该选择哪一个?最高的峰吗?
请教大家哪些公司卖的有机酸(草酸,酒石酸,丙二酸,苹果酸,柠檬酸,琥珀酸)比较靠谱?之前找代购的标准品不纯单标都有多个特别大的杂峰,完全不能用,跪求靠谱的有机酸购买途径~非常感谢!
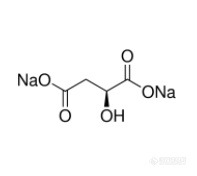
[align=center][font='黑体'][size=21px]L-[/size][/font][font='黑体'][size=21px]苹果酸钠[/size][/font][/align][align=center][font='宋体'][size=18px]陈 超 凡 [/size][/font][/align][align=center][size=18px] [/size][/align][align=center][size=18px]2021[/size][size=18px]年7月[/size][size=18px]21[/size][size=18px]日[/size][/align][align=left][size=21px]理化性质[/size][/align][align=left]1.名称:L-羟基二丁酸钠[/align][align=left][/align][align=left][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262015519693_5947_1608728_3.png[/img] 2.分子式:C[font='等线'][size=18px]4[/size][/font]H[font='等线'][size=18px]4[/size][/font]Na[font='等线'][size=18px]2[/size][/font]O[font='等线'][size=18px]5’[/size][/font][size=18px]H[/size][font='等线'][size=18px]2[/size][/font][size=18px]O[/size][/align][align=left][/align][align=left]3.结构式:[/align][align=left][/align][align=left][/align][align=left] 有一个手心中心,该手性中心为L构型,是苹果酸钠的一个对映异构体。[/align][align=left]4.相对分子质量: 178.05[/align][align=left]5.性状:为白色结晶性粉末或块状物[/align][align=left]6.感官要求:[img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262015520590_9570_1608728_3.png[/img][/align][align=left]7.理化要求:[img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262015521400_1216_1608728_3.png[/img][/align][align=left][size=21px]制备[/size][/align][align=left]L-苹果酸和碳酸钠反应,经结晶、干燥制得的食品添加剂L-苹果酸钠。L-苹果酸的制备方法有以下几种方法:[/align][align=left][font='等线'][size=16px]1. [/size][/font][font='等线'][size=16px]L-苹果酸[/size][/font][font='等线'][size=16px]钠[/size][/font][font='等线'][size=16px]的[/size][/font][font='等线'][size=16px]生产工艺流程:[/size][/font][font='等线'][size=16px]L-苹果酸钠的生产工艺流程图如下: [/size][/font][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262015522191_3600_1608728_3.png[/img][/align][align=left]关键控制点: [/align][align=left](1)中和反应:L-苹果酸和碳酸钠发生中和反应,生产L-苹果酸钠。 投料比例:1.7:1.35,温度50~60℃,pH 6.8~7.2 [/align][align=left](2)过滤:温度50~60℃,溶液澄清 [/align][align=left](3)浓缩:二效蒸汽浓缩,温度 70 ~ 80℃、真空 -0.04~-0.06MPa,混合汽温度80~90℃、一效物料浓度40%,二效物料浓缩至比重142g/cm[font='等线'][size=16px]3[/size][/font] (60℃)出料。 [/align][align=left](4)结晶:温度20℃ [/align][align=left]2.微生物发酵法: [/align][align=left]一步发酵法:菌种有黄曲霉、米曲霉、寄生曲霉等,均以包括葡萄糖在内的多种糖为底物产生L-苹果酸。[/align][align=left]两步发酵法:由华根霉或少根根霉将葡萄糖生物合成富马酸,再由膜醭毕赤酵母、普通变形菌、芽孢杆菌或掷孢酵母等将富马酸转化为L-苹果酸。 一步发酵法较多地采用黄曲霉,它能利用葡萄糖、麦芽糖、蔗糖、果糖及淀粉等多种糖质原料产生L-苹果酸。但培养基较复杂,发酵过程常有富马酸等其他有机酸产生,给分离提纯带来困难,难于得到高纯度的晶体,再加上产酸低,对糖转化率低 (30%~40%),周期长(最少也需5天),故至今在国内外均未实现工业化生产。[/align][align=left]两步发酵法的第一步,先用根霉将糖类发酵生成富马酸,即富马酸发酵,这里的糖较多的使用葡萄糖,葡萄糖可由淀粉经双酶水解而得。[/align][align=left]第二步是在前面所产的富马酸中接入酵母菌或细菌进行发酵,将富马酸转化为L-苹果酸,即转化发酵。采用这种方法,苹果酸对糖转化率最高可达60%以上,但是毕竟发酵周期太长,前后加起来要8~9天。虽然两步法与一步法一样,国内外学者正在不断地探索,取得了一些有价值的进展,但至今仍然未见工业化生产的报道。[/align][align=left]3.固定细胞转换法:该方法是首先大量培养富马酸酶活力高的菌体,收集菌体后用卡拉胶等适当的载体进行固定,然后装入柱式反应器,以富马酸钠盐为底物,流经反应器,由固定化细胞中的富马酸酶的催化作用,很容易将富马酸转化为L-苹果酸,且几乎无副产物,转化率高达95%以上。此法与上述两种方法相比,简单、 经济、高效,于是成了工业化生产的首先方法[/align][align=left]4. 酶促转化直接生产L-苹果酸钠:(1)将富马酸和选自碳酸氢钙、氢氧化钙和碳酸钙中的一种或多种钙盐加入水中并搅 拌混匀以进行中和反应,待所述中和反应完成后,任选调节反应体系的pH值为6 .5-7 .0,得 到富马酸钙悬浊液; (2)向步骤(1)得到的所述富马酸钙悬浊液中加入延胡索酸水合酶催化制剂进行酶促 反应,生成L-苹果酸钙悬浊液,其中,所述延胡索酸水合酶催化制剂选自延胡索酸水合酶或 者表达所述延胡索酸水合酶的重组工程菌,所述延胡索酸水合酶为FUMA、FUMC或它们的混 合物; (3)向步骤(2)得到的所述L-苹果酸钙悬浊液中加入碳酸钠以进行中和反应,待所述中 和反应完成后,得到L-苹果酸钠和碳酸钙的混合物; (4)将步骤(3)得到的所述混合物进行固液分离,得到L-苹果酸钠的上清液以及作为沉 淀物的碳酸钙,其中,将所述L-苹果酸钠的上清液进行处理制得固体的L-苹果酸钠,将所述 碳酸钙回收以在步骤(1)中作为钙盐循环使用。[/align][align=left][font='等线'][size=16px]5[/size][/font][font='等线'][size=16px].[/size][/font][font='等线'][size=16px]细胞转化法:[/size][/font][font='等线'][size=16px][color=#333333]将从土壤中分离得到的Aspergillus wentii属菌株在糖30g/L,磷酸氢二铵3g/L,硫酸铵2g/L,氯化钾2g/L,硫酸镁1g/L,富马酸钠5g/L的培养液中培养48小时,过滤分离出细胞。在60-70℃下配制2%的卡拉胶溶液,降温到50℃时将分离出的细胞按10%(w/w)加入,搅拌均匀后倒入盘子中凝固,制成5mm×5mm×5mm的固定化细胞。然后装入8cm×60cm的玻璃柱。将1.4M的富马酸钠溶液以1000ml/h的速度流经固定化细胞柱,得到L-苹果酸盐和富马酸盐混合溶液。[/color][/size][/font][/align][align=left][font='等线'][size=16px][color=#333333](2)取1000ml经步骤(1)得到的混合液,其中含L-苹果酸钠186g,富马酸钠56g。将溶液加热到60℃,搅拌下加入170g(摩尔比1.05∶1)富马酸,搅拌反应3.5小时,PH=3.2,冷却到15~20℃,过滤,滤饼用少量水洗,然后用NaOH中和至PH=7-8供细胞转化用。所得滤液980ml,含富马酸单钠40g。加热至85℃,通过1500ml 001x7强酸性阳离子交换柱(直径6cm,高60cm),收集淋洗液经减压浓缩,L-苹果酸浓度增加到40%时,冷却到10~15℃,过滤回收富马酸。滤液进一步减压浓缩到L-苹果酸浓度至80~82%,冷却到15℃,结晶出91gL-苹果酸,母液中含有46gL-苹果酸,母液可循环使用。L-苹果酸收率相当于97%。[/color][/size][/font][/align][align=left][/align][align=left][size=21px]应用[/size][/align][align=left][font='等线'][size=16px]苹果酸作为功能性酸味剂广泛用于饮料及食品工业。苹果酸的酸味持久,其酸味比柠檬酸强20%,不仅能保持天然果汁的风味,与合成甜味剂合用还可消除后苦味,可部分或全部代替柠檬酸用于饮料、食品的酸味调节。另外,L-苹果酸是人体三羧酸循环的重要枢纽之一,具有许多独特的生理功能。天然构型的L-苹果酸在细胞能量产生过程中发挥着十分重要的作用。同时在生物体内以络合形式贮存和运输金属离子,因此,L-苹果酸钙可用于预防和治疗因缺钙而引起的老年性骨质疏松。L-苹果酸还用于鲜肉的加工和保存,可加速肉的熟化和起保鲜作用。L-苹果酸能诱导皮肤细胞的分裂,改善皮肤组织的生长,因而可用于化妆品工业。由于柠檬酸会诱导脂肪酸的合成,在食品饮料中使用L-苹果酸可以减少脂肪合成,苹果酸有减肥的功能。近年来还发现L-苹果酸具有保肝,解毒及抗抑郁症的作用,是具有巨大应用前景的功能性添加剂。[/size][/font][/align][align=left][font='等线'][size=16px]L-苹果酸中含有天然的润肤成分,可以清除皮肤表面皱纹,使皮肤变得嫩白、光洁而有弹性,因此在化妆品配方中备受青睐;L-苹果酸可以配制多种香精、香料,用于多种日用化工产品,如牙膏、洗发香波等;国外将其用于替代柠檬酸作为新型洗涤助剂,用于合成高档特种洗涤剂。L-苹果酸可用于药物制剂、片剂、糖浆中,还可以配入氨基酸溶液中,能明显提高氨基酸的吸收率;L-苹果酸可以用于治疗肝病、贫血、免疫力低下、尿毒症、高血压、肝衰竭等多种疾病,并能减轻抗癌药物对正常细胞的毒害作用;还可用于制备和合成驱虫剂、抗牙垢剂等。另外L-苹果酸还可以作为工业清洗剂、树脂固化剂、合成材料增塑剂、饲料添加剂等。[/size][/font][/align][align=left]L-苹果酸钠是苹果酸钠的一种光学异构体,除旋光性之外,其理化性质和DL-苹果酸钠相同。同时L-苹果酸钠还可以直接参与生物体的新陈代谢,因此,相比于DL-苹果酸钠,L-苹果酸钠对人体健康更加有益。它作为酸度调节剂、食品调味剂、保鲜代盐剂、水分保持剂得到广泛应用。[/align][align=left]使用L-苹果酸钠的必要性如下:[/align][align=left] (1)美国FDA已开始限制柠檬酸及DL-苹果酸在老年人、肝肾功能障碍患者和儿童食品中使用。 [/align][align=left](2)根据联合国食品添加剂委员会JECFA的数据,苹果酸钠的ADI值为无限定(no specified)。目前,L-苹果酸、dl-苹果酸、dl-苹果酸钠均已是食品添加剂,且属于无毒物质。与dl-苹果酸钠相比,L-苹果酸钠具有重要的生理功能,可直接进入三羧酸循环,参与人体代谢,对人体的健康有益,同时还避免了D-苹果酸钠在人体的残留。因此,L-苹果酸钠也属于无毒物质,人体摄入是安全的。 (3)随着生物技术的发展,酶法转化生产L-苹果酸钠的成本和dl-苹果酸钠的成本正在逼近,使得L-苹果酸钠的大量使用成为了可能。此外,dl-苹果酸钠中含有50%的D-苹果酸钠不会被人体吸收,因此,理论上讲,当达到相同的使用效果时,L-苹果酸钠的用量仅需dl-苹果酸钠用量的一半。[/align][align=left]在水产品中的应用:水产品具有低脂肪、高蛋白的特点,是合理膳食结构中不可缺少的重要部分,已成为人们摄取动物性蛋白质的重要来源,并且鱼、虾、蟹等水产品肉质鲜美,风味独特,深受广大消费者的青睐。但是由于水产品容易腐败变质,在加工或储藏过程中必须加强水产品的保鲜。通常需要做抑菌抗菌处理。以金枪鱼、扇贝、虾仁的加工处理为例:[/align][align=left][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262015523169_2920_1608728_3.png[/img](1)pH调整剂配方[/align][align=left][/align][align=left](2)加工工艺[img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262015524276_6168_1608728_3.png[/img][/align][align=left][/align][align=left][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262015525511_8120_1608728_3.png[/img](3)结果分析[/align][align=left][/align][align=left] 比较以上实验结果可以看出,添加一定量的pH调整剂处理能够减少水产品中的微生物数量,抑制细菌的生长繁殖,尽可能保持水产品的新鲜度。[/align][align=left]在果蔬腌制品中的应用:目前腌制食品企业往往在研制食品中添加各种食用酸,且把减盐增酸作为今后酱腌菜发展的方向。酸度调节剂能降低腌渍剂的pH值,抑制微生物的生长繁殖,对产品的储藏极为有利。再腌渍液中添加食醋、柠檬酸、苹果酸等酸度调节剂能使腌渍液的pH值下降,从而达到抑制微生物生长繁殖的目的,同时起到调味的作用。为了保持pH值在一个稳定的范围内,通常加入一定比例的有机酸盐。苹果酸用于腌菜中能够起到缓冲和调味的作用,从而既可以使腌渍菜保持较低的pH值,便于保鲜和货架期的延长,又可以酸味,赋予腌渍菜良好的口味和清爽的口感。[/align][align=left]以酸辣白菜的腌渍过程,来说明L-苹果酸钠的应用效果:[/align][align=left](1)加工方法 配方:白菜10kg,食盐1.5kg,白糖0.25kg,干辣椒0.1kg,菜籽油0.2kg,生姜丝0.2kg,酸味料(L-苹果酸、 L-苹果酸钠等)。 制作方法: 白菜洗净,切成3cm长、1cm宽,加盐后搅拌均匀,1h后去除盐水加糖、酸味料,并与经过油炸过的生姜丝、干辣椒丝搅拌均匀,腌制1天即可。 (2)结果分析 改变酸味料中L-苹果酸和L-苹果酸钠的比例,分析不同比例条件下腌菜的口味,结果如下:[img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262015526527_5962_1608728_3.png[/img] 由此可以看出,苹果酸钠用于腌渍菜中,能够起到缓冲和调味作用,从而既可使腌渍菜保持较低的pH值,便于保鲜和货架期的延长,又可调节酸味,赋予腌渍菜良好的口味和清爽的口感。[/align][align=left]果味饮品方面:L-苹果酸钠既可以与柠檬酸钠、DL-苹果酸钠、L-酒石酸钠等常规食品添加剂混合使用,也可以替代或部分替代上述传统食品添加剂。以某种果醋饮料为例,说明L-苹果酸钠的应用效果。[/align][align=left](1)工艺流程 取某种果味饮料A,加入一定量的L-苹果酸钠,制得饮料B,分别对饮料A和饮料B进行感官评价,具体方法见下表。[img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262015527279_4600_1608728_3.png[/img][/align][align=left]实验结果以每个评价项目的有效评分总和除以有效人员,得出每个项目的平均得分,得分越高说明该添加剂对酸度和风味影响越大,评价结果见下表。[img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262015528294_7217_1608728_3.png[/img][/align][align=left]因此,添加L-苹果酸钠的饮料B在酸味和风味表达上明显优于不添加L-苹果酸钠的饮料A。[/align][align=left][size=21px]限量[/size][/align][align=left]苹果酸,于1967年在美国食品和药品管理局登记,是国际上公认的安全、无毒无害的食用有机酸。而作为苹果酸的钠盐,苹果酸钠同样安全无毒,在食品中使用绝对安全可靠,可以作为食品添加剂用于各类食品中对人类健康不会产生危害,其ADI值为无限定。[/align][align=left][/align][align=left][size=21px]质量指标[/size][/align][align=left] 中华人民共和国国家标准:根据中华人民共和国国家标准要求,食品调加剂L-苹果酸应符合以下技术指标:[/align][align=left][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262015529257_8172_1608728_3.png[/img][/align][align=left][/align][align=left][size=21px]检测[/size][/align]1.鉴别试验:试剂和材料:对氨基苯磺酸;(1+1)盐酸溶液;乙酸钴-双氧铀溶液:称取4g乙酸双氧铀,置于50mL乙酸溶液(60g/L)中,加热使溶解 称取20 g乙酸钴,同样置于50 mL 乙酸溶液(60 g/L)中 在温热状态下将两溶液混合,冷却至约20 °C并保持2 h,过滤,即得;亚硝酸钠溶液:200 g/L;氢氧化钠溶液:40 g/L(1)溶解性试验:称取1 g试样,精确至0.01 g,用水溶解并稀释至10 mL,溶液应澄清。(2)钠盐试验:铂丝用盐酸溶液湿润后,蘸取试样,在无色火焰中燃烧,火焰应显亮黄色。称取1 g试样,精确至0.01 g,用适量的水溶解,加1 mL盐酸溶液,用水稀释至20 mL。取1 mL该溶液,加5 mL乙酸钴-双氧铀溶液,振摇,有黄色沉淀产生。(3)苹果酸盐试验:称取 1 g 试样,精确至 0.01 g,加适量的水溶解并稀释至 20 mL。取试样溶液 5mL 放入瓷蒸发皿中, 加对氨基苯磺酸 10 mg,在水浴上加热数分钟,加亚硝酸钠溶液 5 mL,略加热,滴加氢氧化钠溶液使成碱性,应显红色。2. L-苹果酸钠(以C[font='等线'][size=16px]4[/size][/font]H[font='等线'][size=16px]4[/size][/font]Na[font='等线'][size=16px]2[/size][/font]O[font='等线'][size=16px]5[/size][/font]计)含量的测定 (1)试剂和材料:冰乙酸;高氯酸标准滴定溶液: c(HClO4) =0.1 mol/L;结晶紫指示液:2 g/L[align=left](2)分析步骤:[color=#000000]称取 [/color][color=#000000]0.15 g [/color][color=#000000]干燥后的试样,精确至 [/color][color=#000000]0.000 1 g[/color][color=#000000],加 [/color][color=#000000]30 mL [/color][color=#000000]冰乙酸溶解,用高氯酸标准滴定溶液滴定。用电位计指示终点。当用指示剂判断终点时,加几滴结晶紫指示液,溶液由紫色经过蓝色变为绿色即为终点。在测定的同时[/color][color=#000000], [/color][color=#000000]按与测定相同的步骤[/color][color=#000000], [/color][color=#000000]对不加试样而使用相同数量的试剂溶液做空白试验。 [/color][/align][align=left][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262015530218_6149_1608728_3.png[/img][color=#000000](3)结果计算:[/color][color=#000000]L-苹果酸钠(以C4H4Na2O5计)的质量分数 w1 ,按公式计算[/color][color=#000000]:[/color][/align][align=left][color=#000000]式中:[/color][/align][align=left][color=#000000]v0——空白试验消耗高氯酸标准滴定溶液的体积,单位为毫升(mL) [/color][/align][align=left][color=#000000]v1——试样消耗高氯酸标准滴溶液的体积,单位为毫升(mL) [/color][/align][align=left][color=#000000]c ——高氯酸标准滴溶液浓度的准确数值,单位为摩尔每升(mol/L) [/color][/align][align=left][color=#000000]M ——苹果酸钠的摩尔质量的数值,单位为克每摩尔(g/mol)[M(C[/color][font='等线'][size=16px][color=#000000]4[/color][/size][/font][color=#000000]H[/color][font='等线'][size=16px][color=#000000]4[/color][/size][/font][color=#000000]Na[/color][font='等线'][size=16px][color=#000000]2[/color][/size][/font][color=#000000]O[/color][font='等线'][size=16px][color=#000000]5[/color][/size][/font][color=#000000])]=89.03) [/color][/align][align=left][color=#000000]m ——试样的质量,单位为克(g) [/color][/align][align=left][color=#000000]1000——换算因子。[/color][/align][align=left][color=#000000]3.比旋光度测定:[/color][/align][align=left][color=#000000]比旋光度的测定,[/color][color=#000000]称取4.25g实验室样品,精确至0.001g,加入20 mL水溶解,移至50 mL容量瓶中,用水稀释至刻度,摇匀。 比旋光度am(20℃,D)数值以“(°)?dm2?kg-1”表示,按照公式计算:[/color][/align][align=left][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262015531018_5551_1608728_3.png[/img][/align][align=left] 式中: a—测得的旋光角,单位为度(°); l—旋光管的长度,单位为分米(dm); Pa—溶液中有效组分的质量浓度,单位为克每毫升(g∕mL)。[/align][align=left][/align][align=left][color=#000000]4[/color][color=#000000].干燥减量的测定:[/color][/align][align=left][color=#000000](1)分析步骤:[/color][color=#000000]称取 4 g 试样,精确至 0.000 2 g,置于已烘至质量恒定的称量瓶中,在 120 °C±2 °C的恒温干燥箱中 干燥 2 h,调整温度至 160 °C±2 °C,再干燥 2 h,取出,置于干燥器中冷却至室温,称量。[/color][/align][align=left][color=#000000](2)结果计算:[/color][color=#000000]干燥减量的质量分数 ,按公式计算:[/color][/align][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262015531685_128_1608728_3.png[/img]式中:m——干燥前试样的质量,单位为克(g) m1——干燥后试样的质量,单位为克(g)。5.富马酸和马来酸含量的测定:(1)方法提要:用高效液相色谱法,在选定的工作条件下,以磷酸氢二铵溶液为流动相,用高压输液泵将流动相泵入 C18色谱柱使试样溶液中各组分进行分离,用紫外检测器进行检测,由数据处理系统记录和处理色谱信号。(2)试剂和材料:水:符合GB/T 6682-2008的一级水;富马酸:色谱纯;马来酸:色谱纯(3)仪器和设备:高效液相色谱仪,带脱气装置,配备紫外检测器。(4)参考色谱条件: 流动相:取磷酸氢二铵20 g,加入约900 mL水溶解后,用磷酸调节溶液的pH为2,然后用0.45 μm的滤膜过滤,再定容至1000 mL。 色谱柱:C18,填料孔径12 nm,填料粒径5 μm,柱长250 mm,柱内径4.6 mm,或其他等效色谱柱。 流速:0.8 mL/min。 柱温:40 °C 波长:210 nm。 进样量:20 μL。(5)分析步骤: 工作曲线的绘制:按表 A.1 中 DL-苹果酸、马来酸和富马酸浓度标准系列,配制出两种不同浓度的混合标准溶液,按照 浓度和峰面积绘制工作曲线,各物质的保留时间参照表 A.2。[img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262015532765_2322_1608728_3.png[/img][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262015533938_371_1608728_3.png[/img] 试样溶液的制备;称取0.5 g试样,精确至0.000 2 g,于100 mL容量瓶,加少量水溶解并稀释至刻度,混匀。色谱分析前 用0.45μm微孔滤膜过滤。 测定:在规定的色谱条件下,取标准溶液和试样溶液各20 μL分别注入液相色谱仪,在工作曲线上查得试液 中富马酸或马来酸的浓度。 结果计算:富马酸或马来酸含量的质量分数以 w3 计,按公式计算:[img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262015534637_2124_1608728_3.png[/img]式中:c ——测定得到的试样中富马酸或马来酸的浓度,单位为毫克每升(mg/L) m ——试样的质量,单位为克(g) 100——试样的定容体积,单位为毫升(mL) 1000——换算因子。实验结果以平行测定结果的算术平均值为准。在重复性条件下获得的两次独立测定结果的绝对差值不 大于其算术平均值的 10%。[size=21px]参考文献[/size]【1】一种L-苹果酸钠的直接酶促转化生产方法。周铁成,王云山,王自强,冯晓东,赵晶。国家专利,申请号 201710208506.5。【2】中华人民共和国国家标准 GB13737-2008。