[color=#d40a00][size=3]《药品红外光谱集》第四卷(2010)全书电子版下载地址:[/size][/color][url=http://www.instrument.com.cn/download/shtml/156129.shtml][color=#d40a00][size=3]http://www.instrument.com.cn/download/shtml/156129.shtml[/size][/color][/url][color=#d40a00][size=3]zwyu更新:近日搞到了电子版,非常高兴。本来想马上传到资料中心的,但一搜索,原来资料中心已经早有了,是我OUT了。。。[/size][/color]《药品红外光谱集》第一(1995)、二(2000)、三卷(2005)卷想必大家都见过了,也搞到过电子版的了。随着2010版药典的实施,《药品红外光谱集》第四卷也即将出炉,先给大家一个四卷品目,尝尝鲜。等正式推出后,有谁搞到了电子版,莫忘共享一下,嚯嚯。附上之前历卷《药品红外光谱集》的内容提要和具体出版日期:《药品红外光谱集》(1990) 作者:中华人民共和国卫生部药典委员会 出版社:北京:化学工业出版社,1990年11年第一版 ISBN:7-5025-0750-7/R.6 内容提要: 本书收藏药品的红外光谱图共582幅,包括《中华人民共和国药典》(1990年版)、卫生部部颁药品标准以及全国各省、市、自治区地方药品标准中收藏的各类药品的红外光谱图。今后,《中华人民共和国药典》及《中华人民共和国卫生部药品标准》不再收藏红外光谱图,凡以红外光谱法作为鉴别和检查的药品,一律以本书收藏的红外光谱图作为对照图谱。本书是上述各药品标准不可缺少的配套用书,对药品分析和检验工作有很大的实用价值。本书也可供有机化学、有机分析专业人员参考。《药品红外光谱集》第一卷(1995) 【作 者】: 中华人民共和国卫生部药典委员会编 【页 数】: 710 【出版社】: 化学工业出版社 【主题词】: 药物分析:光谱分析 红外光谱法 光谱图 【ISBN号】: 7-5025-1550-X 【出版日期】: 1996 【原书定价】: 98.00 内容提要: 本书是专门配合1995年版药典编汀出版的,共收载685种药品的红外光谱图,凡1995年版药典采用红外分光光度法鉴别的药品,均以本书收载的图谱作为标准对照图谱;书中还收载了卫生部药品标准和全国各省(自治区、直辖市)地方药品标准采用的标准红外图谱;本图谱采用中英文对照排版。 本书在1990年版基础上,作了大量修汀和补充,是执行上述药品标准的必须工具书,对药品分析、检验工作有很大实用价值。 本书还可供药品科研、有机化学、有机分析专业技术人员参考。《药品红外光谱集》第二卷(2000) [作者]:国家药典委员会编 [出版社]:北京:化学工业出版社,2000年6月第一版 [ISBN]:7-5025-2898-9/R.70 [定价]:95元内容提要: 本书是专门配合1995年版药典编汀出版的,第一卷收载了685种、第二卷收载了208种药品的红外光谱图。凡1995年版药典采用红外分光光度法鉴别的药品,均以本书收载的图谱作为标准对照图谱;书中还收载了卫生部药品标准和全国各省(自治区、直辖市)地方药品标准采用的标准红外图谱;本书采用中英文对照,书后附有中文名索引、英文名索引及分子式索引。 本书在1990年版基础上,作了大量修改和补充,是执行上述药品标准的必须工具书,对药品分析、检验工作有很大实用价值。 本书还可供药品科研、有机化学、有机分析专业技术人员参考。《药品红外光谱集》第三卷(2005) [作者]:国家药典委员会编 [出版社]:北京:化学工业出版社,2005年6月第一版 [ISBN]:7-5025-7225-2 [定价]:100元 内容提要: 红外光谱法是有机化合物分析中广泛应用的方法。由于红外光谱的高度专属性,在药品检验中,红外光谱法常与其他理化方法联合使用,作为有机药品重要的鉴别方法。鉴于有机药品品种不断增加,特别是许多药品化学结构比较复杂或相互之间化学结构差异较小,当用颜色反应、沉淀、结晶形成或紫外-可见分光光度法等常用方法不足以相互区分时,红外光谱法更是行之有效的鉴别手段。 本书为《药品红外光谱》第三卷(2005),共收载药品红外光谱图210幅(其中172个为新品种,38个老品种重新绘制了图谱)。凡在《中华人民共和国药典》和国家药品标准中收载红外鉴别或检查的品种,除特殊情况外,本光谱集均有相应收载,以供比对。《中华人民共和国药典》和国家药品标准中不另收载红外光谱图。其他光谱图可供药品检验中作对照用。[color=#d40a00][size=6][color=#fe2419]zwyu按:[/color][/size][/color]近日发现[url=http://www.antpedia.com/][color=#0365bf]分析测试百科网[/color][/url]大量盗用咱们仪器信息网的帖子,我随便搜了一下,我这个帖子,被[color=#f10b00][size=4]连一个标点符号都不改[/size][/color]的盗用在[url=http://www.antpedia.com/viewspace-64666][color=#0365bf]http://www.antpedia.com/viewspace-64666[/color][/url],我的贴子“【分享】17个红外分光光度计的标准操作规程(SOP),总有一个你需要的”([url=http://bbs.instrument.com.cn/shtml/20100504/2536227][color=#0365bf]http://bbs.instrument.com.cn/shtml/20100504/2536227[/color][/url]),被[color=#d40a00][size=4]连标点符号、字体大小、颜色都不改[/size][/color]的盗用在[url=http://bbs.antpedia.com/viewthread.php?tid=27317][color=#0365bf]http://bbs.antpedia.com/viewthread.php?tid=27317[/color][/url]。其实大家的资料大多都是网上找的,共享一下无可厚非,甚至是值得小小赞赏一下的。可像这样赤裸裸的野蛮盗用,没有丝毫提及本人或广大仪器信息网网友原创性工作(资料本身不是原创的不假,但是谁敢说我前边码的那些个字不是原创性工作?我把这些文字、标点、字号、颜色有机的组合在一起不是原创性工作?)的做法,我只能是鄙视,鄙视,再鄙视。。。怪不然现在国家在搞“绿书签行动”!网络上混日子的,可能做不到完全避免盗版的问题;可是,请哪怕是加上一行小字[color=#f10b00][size=1]“引自XXX”[/size][/color]!?再懒一些的或者自己记不得出处的,也请加上“转帖”或“ZT”字样吧。
今天收到《药品红外光谱集》第三卷(2005)。在前言中有一些沿革的介绍。1. 1985年,药典会编制出版了《药品红外光谱集》1985年版,收集绘制了国产药品红外光谱图423幅;2. 1990年,出版了《药品红外光谱集》1990年版,共收载了582幅图谱;3. 为适应光谱集编制工作的延续性,经编审组研究决定,分卷出版《药品红外光谱集》,1995年出版了第一卷,收载了光栅型红外分光光度计绘制的药品红外光谱图共685幅;4. 2000年出版了第二卷,新收载药品红外光谱图208幅,并全部改由傅立叶红外光谱仪绘制;5. 2005年出版第三卷,共收载药品红外光谱图210幅(172个新品种,38个老品种重新绘制)。采用不同型号的傅立叶红外光谱仪录制,再用伯乐win-IR软件统一格式化。
我按药典的配制方法:取碱式品红0.2g,加热水100ml溶解后,放冷,加亚硫酸钠溶液 (1→10)20ml、盐酸2ml,用水稀释至200ml,加活性炭0.1g,搅拌并迅速滤过,放置1小时以上,即得。 本液应临用新制。我配了好多次配出的都是黄色的。请教各路神仙,问题出在哪里?我用焦亚硫酸钠和无水硫酸钠都试过了,都不行。在加入亚硫酸钠溶液后一会儿就出现很多沉淀,加入盐酸后沉淀都消失了。此时产生的沉淀是什么?我配这个试剂是为了检测白蜂蜡的丙三醇与其他多元醇项目丙三醇和其它多元醇 取本品0.20g加氢氧化钾乙醇溶液(取氢氧化钾3g,加水5ml使溶解,加乙醇至100ml,摇匀,即得)10ml,加热回流30分钟,取出,加稀硫酸50ml,放冷,滤过,用稀硫酸洗涤容器和滤器,合并洗液和滤液,置同一100ml量瓶中,加稀硫酸稀释至刻度,摇匀,作为供试品溶液。取10ml纳氏比色管两支,甲管中精密加入供试品溶液1ml,加0.05mol/L高碘酸钠溶液0.5ml,混匀,放置5分钟,再加品红亚硫酸试液1.0ml,混匀,不应出现沉淀;然后将试管置40℃温水中。在水温下降过程中不断旋转试管,观察10~15分钟;乙管中精密加入0.001%丙三醇的稀硫酸溶液1ml,与甲管同时依法操作,甲管中显出的颜色与乙管比较,不得更深。(以丙三醇计,不得过0.5%)加入我配的品红亚硫酸钠样品盒对照就会出现沉淀。不知产生的是什么沉淀?问题出在何处?当我加两毫升品红亚硫酸溶液时沉淀消失,这又是为什么?我已经被这个实验困了好久了,请教大家,帮帮忙啊,感激不尽!
只看到一个会议纪要,来源:药典委员会附件1:《药品红外光谱集》第五卷编委会会议纪要根据药典委员会工作安排,我委于2010年6月23~24日在北京召开了《药品红外光谱集》(第五卷)编委会工作会议。国家药典委员会王平副秘书长、药典委员会资深委员、第四卷主编凌大奎、中国药品生物制品检定所、总后药检所等15个药检所技术负责人及药典会负责人共计20余人参加了会议。首先,王平副秘书长对前一阶段工作进行了回顾,他指出:红外协作组在过去的两年里顺利开展并完成了《药品红外光谱集》(第四卷)的工作,为《中国药典》2010年版(二部)做出了成绩。第四卷中原料药和制剂的红外工作开展的很有声色,该卷的工作在以原料为重点的基础上,另外开展了70多种制剂的红外鉴别研究工作,最终有32个制剂品种的红外鉴别被收入到《中国药典》2010年版(二部)中。他进一步强调了《药品红外光谱集》专题协作组工作的重要性,要求红外协作组各成员所首先要将红外协作组工作做在平常,使红外光谱集的工作常态化、规范化,成为一种经常性的工作;其次要加强制剂和药用辅料的红外鉴别工作,推动和促进更多制剂红外鉴别收入药典的工作,通过提高制剂标准的专属性,来控制掺伪假药,更好地发挥红外专属性鉴别作用。随后,资深药典委员凌大奎对红外光谱的技术要求逐一进行了详细的介绍和讲解,对编写高水平的《药品红外光谱集》起到了重要的指导作用。本次会议经过认真讨论,确定了《药品红外光谱集》(第五卷)任务分工,并对现版《药品红外光谱集》中存在问题及后续工作进行了研究,为编制好《药品红外光谱集》(第五卷)工作奠定了基础。现将会议内容纪要如下:1.讨论并修订了药品红外光谱集编写细则(见附件1);2.对红外对照图谱存在问题的品种,会议决定由药典委员会再次统一发文征集意见,安排落实任务; 3.确定了《药品红外光谱集》(第五卷)的品种名单(见附件2)并落实了任务分工。各协作单位在绘制标准光谱时应遵照药品红外光谱集编写细则执行,特别在提交光谱时,应附编写细则中不同制样条件下绘制的光谱
做个试验 想要盐酸贝那普利的对照品图,还有说两个光谱一致的依据是什么,全波数都对上? 包括指纹区?
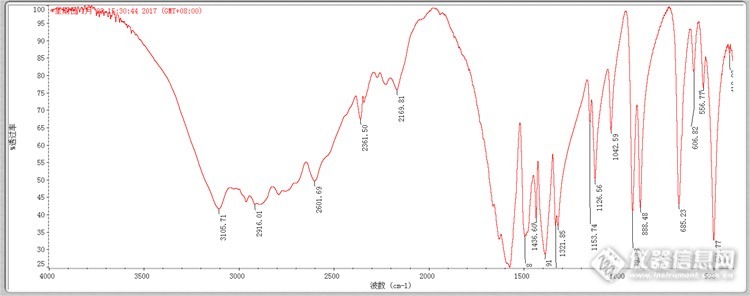
请教各位高手:红外对标准品有没有什么要求?我在检测中国药典上的药品甘氨酸时,用购买的标准品扫出的图谱和《药品红外光谱集》上的标准图谱不像,反而是改用分析纯级的试剂甘氨酸扫出的图谱和标准图谱更像,这正常吗?会是什么原因导致的呢?
各位大侠您们好: 谁能告诉我,所测的样品图谱该如何与对照图谱(药品红外光谱集)比较呢?必须每一个峰(含小峰)的波数都一致吗?还是只比较几个强峰就可以来判定结果了呢?另外峰的强度该如何判定呢?强度的范围是多少?谢谢![em06] [em61]
申请食品添加剂新品种必须是确认的单一物质吗?可以将某种生化提取物申请食品添加剂新品种吗?
第一条 为加强食品添加剂新品种管理,根据《食品安全法》和《食品安全法实施条例》有关规定,制定本办法。第二条 食品添加剂新品种是指:(一)未列入食品安全国家标准的食品添加剂品种;(二)未列入卫生部公告允许使用的食品添加剂品种;(三)扩大使用范围或者用量的食品添加剂品种。第三条 食品添加剂应当在技术上确有必要且经过风险评估证明安全可靠。第四条 使用食品添加剂应当符合下列要求:(一)不应当掩盖食品腐败变质;(二)不应当掩盖食品本身或者加工过程中的质量缺陷;(三)不以掺杂、掺假、伪造为目的而使用食品添加剂;(四)不应当降低食品本身的营养价值;(五)在达到预期的效果下尽可能降低在食品中的用量;(六)食品工业用加工助剂应当在制成最后成品之前去除,有规定允许残留量的除外。第五条 卫生部负责食品添加剂新品种的审查许可工作,组织制定食品添加剂新品种技术评价和审查规范。第六条 申请食品添加剂新品种生产、经营、使用或者进口的单位或者个人(以下简称申请人),应当提出食品添加剂新品种许可申请,并提交以下材料:(一)添加剂的通用名称、功能分类,用量和使用范围;(二)证明技术上确有必要和使用效果的资料或者文件;(三)食品添加剂的质量规格要求、生产工艺和检验方法,食品中该添加剂的检验方法或者相关情况说明;(四)安全性评估材料,包括生产原料或者来源、化学结构和物理特性、生产工艺、毒理学安全性评价资料或者检验报告、质量规格检验报告;(五)标签、说明书和食品添加剂产品样品;(六)其他国家(地区)、国际组织允许生产和使用等有助于安全性评估的资料。申请食品添加剂品种扩大使用范围或者用量的,可以免于提交前款第四项材料,但是技术评审中要求补充提供的除外。第七条 申请首次进口食品添加剂新品种的,除提交第六条规定的材料外,还应当提交以下材料:(一)出口国(地区)相关部门或者机构出具的允许该添加剂在本国(地区)生产或者销售的证明材料;(二)生产企业所在国(地区)有关机构或者组织出具的对生产企业审查或者认证的证明材料。第八条 申请人应当如实提交有关材料,反映真实情况,并对申请材料内容的真实性负责,承担法律后果。第九条 申请人应当在其提交的本办法第六条第一款第一项、第二项、第三项材料中注明不涉及商业秘密,可以向社会公开的内容。食品添加剂新品种技术上确有必要和使用效果等情况,应当向社会公开征求意见,同时征求质量监督、工商行政管理、食品药品监督管理、工业和信息化、商务等有关部门和相关行业组织的意见。对有重大意见分歧,或者涉及重大利益关系的,可以举行听证会听取意见。反映的有关意见作为技术评审的参考依据。第十条 卫生部应当在受理后60日内组织医学、农业、食品、营养、工艺等方面的专家对食品添加剂新品种技术上确有必要性和安全性评估资料进行技术审查,并作出技术评审结论。对技术评审中需要补充有关资料的,应当及时通知申请人,申请人应当按照要求及时补充有关材料。必要时,可以组织专家对食品添加剂新品种研制及生产现场进行核实、评价。需要对相关资料和检验结果进行验证检验的,应当将检验项目、检验批次、检验方法等要求告知申请人。安全性验证检验应当在取得资质认定的检验机构进行。对尚无食品安全国家检验方法标准的,应当首先对检验方法进行验证。第十一条 食品添加剂新品种行政许可的具体程序按照《行政许可法》和《卫生行政许可管理办法》等有关规定执行。第十二条 根据技术评审结论,卫生部决定对在技术上确有必要性和符合食品安全要求的食品添加剂新品种准予许可并列入允许使用的食品添加剂名单予以公布。对缺乏技术上必要性和不符合食品安全要求的,不予许可并书面说明理由。对发现可能添加到食品中的非食用化学物质或者其他危害人体健康的物质,按照《食品安全法实施条例》第四十九条执行。第十三条 卫生部根据技术上必要性和食品安全风险评估结果,将公告允许使用的食品添加剂的品种、使用范围、用量按照食品安全国家标准的程序,制定、公布为食品安全国家标准。第十四条 有下列情形之一的,卫生部应当及时组织对食品添加剂进行重新评估:(一)科学研究结果或者有证据表明食品添加剂安全性可能存在问题的;(二)不再具备技术上必要性的。对重新审查认为不符合食品安全要求的,卫生部可以公告撤销已批准的食品添加剂品种或者修订其使用范围和用量。第十五条 本办法自公布之日起施行。卫生部2002年3月28日发布的《食品添加剂卫生管理办法》同时废止。
根据《食品安全法》及其实施条例、《食品添加剂新品种管理办法》和《食品添加剂新品种申报与受理规定》的要求,为规范食品添加剂新品种许可管理,现公告如下: 一、关于技术必要性材料 申请食品添加剂新品种的,应当提交以下技术必要性证明材料: (一)食品添加剂的功能类别及作用机理; (二)在拟添加的食品中添加与否的效果对比; (三)与同一功能类别的食品添加剂使用效果的对比资料; (四)其他有关技术上确有必要的资料。 申请食品用香料新品种的,可免于提交上述第(二)、(三)项资料。 二、关于食品添加剂质量规格要求 申请的食品添加剂新品种,如无现行有效食品添加剂产品标准的,应当提交以下质量规格材料: (一)食品添加剂产品标准的文本(包括鉴别、主要技术指标要求及相应的检验方法); (二)编制说明; (三)与国际组织和其他国家(地区)相关标准的比较; (四)检验方法的验证情况。 三、关于食品添加剂现场审核 由承担食品添加剂新品种安全性评审的机构挑选2-3名专家,对食品添加剂新品种研制及生产现场进行现场核实、评价: (一)研制单位的基本情况; (二)生产所用的原料、来源和投料记录; (三)按照申报资料的工艺流程图核查样品的生产工艺过程及记录; (四)如需对检验结果进行验证检验的,抽取样品进行验证检验。 (五)对申请扩大食品添加剂使用范围和用量的,可根据具体情况组织现场审核工作。 四、关于验证食品添加剂新品种产品标准 对尚无相应产品标准的食品添加剂新品种,承担食品添加剂新品种安全性评审的机构应当在申请者提交资料基础上,组织对产品标准(包括鉴别、主要技术指标要求及相应的检验方法)进行验证,验证结果作为食品安全风险评估的依据。 五、关于食品添加剂新品种公告内容 卫生部根据食品添加剂技术上必要性和食品安全风险评估结果,对符合食品安全要求的,依法决定准予许可并公布食品添加剂新品种、使用范围和用量,同时公布食品添加剂新品种的质量规格要求,作为企业组织生产的依据。在相应的食品安全国家标准出台后,食品添加剂质量规格要求即时作废。 六、关于鼓励对食品添加剂新品种提出建议 申请食品添加剂新品种受理后,卫生部将通过卫生部网站(www.moh.gov.cn)、食品安全综合信息网(www.nfsiw.gov.cn)和食品安全国家标准网(www.chinafoodsafety.net)等公布相关信息,公开征求社会各界、各有关部门和相关行业组织意见,欢迎对食品添加剂新品种管理提出意见和建议。 特此公告。 二〇一一年十一月二十五日
关于批准聚偏磷酸钾作为食品添加剂新品种等的公告 中华人民共和国国家卫生和计划生育委员会2013-08-26 2013年 第2号根据《中华人民共和国食品安全法》和《食品添加剂新品种管理办法》的规定,经审核,现批准聚偏磷酸钾为食品添加剂新品种,硬脂酰乳酸钠等7种食品添加剂扩大使用范围、用量,增补已批准食品添加剂低聚果糖的质量规格要求。特此公告。附件: 1.食品添加剂新品种聚偏磷酸钾.doc 2.硬脂酰乳酸钠等7种扩大使用范围、用量的食品添加剂.doc 3.增补食品添加剂低聚果糖的质量规格要求.doc 国家卫生计生委 2013年7月30日
很多很多礼品可以换了,无限次数,而且有新品,没有积分了 换不了
关于批准酸式焦磷酸钙等3种食品添加剂新品种等的公告 中华人民共和国国家卫生和计划生育委员会2013年第9号根据《中华人民共和国食品安全法》和《食品添加剂新品种管理办法》的规定,经审核,现批准酸式焦磷酸钙等3种食品添加剂新品种,4-氨基-5,6-二甲基噻吩并嘧啶-2(1H)-酮盐酸盐等2种食品用香料新品种, L-半胱氨酸盐酸盐等2种食品添加剂扩大使用范围、用量。特此公告。国家卫生和计划生育委员2013年6月5日
[color=#333333]对照品与标准品概念[/color][color=#333333]对照品与标准品是2个不同的概念,中国药典凡例中已有明确的定义:对照品系指用于鉴别、检查、含量测定和校正检定仪器性能的标准物质,而标准品系指用于生物检定、抗生素或生物药品中含量或效价测定的标准物质,以效价单位(U)表示.文献中常将2种概念混淆,认为对照品就是标准品,是1种物质2种提法而已[1,2],造成错误的原因,可能是有的药品既有对照品,又有标准品.例如,当用微生物法测定头孢克罗效价时,用头孢克罗标准品,用HPLC或UV法测定时,则用对照品;非那西丁当用作熔点校准物质时,用熔点标准品,测定含量时,用对照品.即使是同一种物质的标准品和对照品,它们的规格、标定方法以及用途都可能是不同的.[/color]
[b]关于食品添加剂新品种氨基乙酸(羟基乙腈法)等的公告 2017年第3号 根据[b]《食品安全法》[/b]规定,审评机构组织专家对食品添加剂新品种氨基乙酸(羟基乙腈法)、食品用香料新品种乙基芳樟基醚和食品添加剂β-胡萝卜素扩大使用范围的安全性评估材料审查并通过。 特此公告。 附件:1. [url=http://file2.foodmate.net/wenku/20170321113512288.docx]食品添加剂新品种氨基乙酸(羟基乙腈法)[/url] 2. [url=http://file2.foodmate.net/wenku/20170321113830207.docx]食品用香料新品种乙基芳樟基醚[/url] 3. [url=http://file2.foodmate.net/wenku/20170321113946516.docx]食品添加剂β-胡萝卜素扩大使用范围[/url][/b][align=right] 国家卫生计生委[/align][align=right] [/align][align=right] 2017年3月8日[/align]
[b]关于食品添加剂新品种碳酸铵、6-甲基庚醛等9种食品用香料新品种和焦亚硫酸钠等2种食品添加剂扩大使用范围的公告(2017年第1号) 根据[b]《食品安全法》[/b]规定,审评机构组织专家对食品添加剂新品种碳酸铵、6-甲基庚醛等9种食品用香料新品种和焦亚硫酸钠等2种食品添加剂扩大使用范围的安全性评估材料审查并通过。 特此公告。 附件: 1. [url=http://file2.foodmate.net/wenku/20170228w60.pdf]食品添加剂新品种碳酸铵[/url] 2.[url=http://file2.foodmate.net/wenku/20170228w60.pdf]6-甲基庚醛等9种食品用香料新品种[/url] 3. [url=http://file2.foodmate.net/wenku/20170228w60.pdf]焦亚硫酸钠等2种食品添加剂扩大使用范围[/url]备注:食品添加剂新品种:碳酸铵食品用香料新品种 :6-甲基庚醛N-(2-异丙基-5-甲基环己基)环丙基甲酰胺4-羟基-4-甲基-5-己烯酸γ-内酯糠基2-甲基-3-呋喃基二硫醚4-癸烯酸2-(4-甲基-5-噻唑基)乙醇丙酸酯4,5-辛二酮5-羟基癸酸乙酯己二酸二辛酯食品添加剂扩大使用范围:焦亚硫酸钠葡萄糖酸-δ-内酯[/b][align=right] 国家卫生计生委[/align][align=right] [/align] 2017年2月6日[b][/b]
对照品:用于鉴别、检查、含量测定和校正检定仪器性能的标准物质;对照品由国家药品检定机构审查认可,其标准应不低于制品的质量标准。 标准品:用于生物检定、抗生素或生物药品中含量或效价测定的标准物质,以效价单位(U)表示。 对照品与标准品概念不清?对照品与标准品是2个不同的概念,中国药典凡例中已有明确的定义:对照品系指用于鉴别、检查、含量测定和校正检定仪器性能的标准物质。标准品:用于生物检定、抗生素或生物药品中含量或效价测定的标准物质,以效价单位(U)表示。文献中常将2种概念混淆,认为对照品就是标准品,是1种物质2种提法而已,造成错误的原因,可能是有的药品既有对照品,又有标准品。 例如:当用微生物法测定头孢克罗效价时,用头孢克罗标准品,用HPLC或UV法测定时,则用对照品;非那西丁当用作熔点校准物质时,用熔点标准品,测定含量时,用对照品。即使是同一种物质的标准品和对照品,它们的规格、标定方法以及用途都可能是不同的。
我配置出来的品红-亚硫酸溶液总是黄色的,放置几天表面会有油状的悬浮物,到底怎样才能配置出无色的品红-亚硫酸溶液呢?急!求解啊!!!
原文:[url]http://www.moh.gov.cn/publicfiles/business/htmlfiles/mohzcfgs/s3576/201004/46908.htm[/url][size=5]中华人民共和国卫生部令 [/size]第73号《食品添加剂新品种管理办法》已于2010年3月15日经卫生部部务会议审议通过,现予以发布,自发布之日起施行。部 长 陈 竺二○一○年三月三十日食品添加剂新品种管理办法第一条 为加强食品添加剂新品种管理,根据《食品安全法》和《食品安全法实施条例》有关规定,制定本办法。第二条 食品添加剂新品种是指:(一)未列入食品安全国家标准的食品添加剂品种;(二)未列入卫生部公告允许使用的食品添加剂品种;(三)扩大使用范围或者用量的食品添加剂品种。第三条 食品添加剂应当在技术上确有必要且经过风险评估证明安全可靠。第四条 使用食品添加剂应当符合下列要求:(一)不应当掩盖食品腐败变质;(二)不应当掩盖食品本身或者加工过程中的质量缺陷;(三)不以掺杂、掺假、伪造为目的而使用食品添加剂;(四)不应当降低食品本身的营养价值;(五)在达到预期的效果下尽可能降低在食品中的用量;(六)食品工业用加工助剂应当在制成最后成品之前去除,有规定允许残留量的除外。第五条 卫生部负责食品添加剂新品种的审查许可工作,组织制定食品添加剂新品种技术评价和审查规范。第六条 申请食品添加剂新品种生产、经营、使用或者进口的单位或者个人(以下简称申请人),应当提出食品添加剂新品种许可申请,并提交以下材料:(一)添加剂的通用名称、功能分类,用量和使用范围;(二)证明技术上确有必要和使用效果的资料或者文件;(三)食品添加剂的质量规格要求、生产工艺和检验方法,食品中该添加剂的检验方法或者相关情况说明;(四)安全性评估材料,包括生产原料或者来源、化学结构和物理特性、生产工艺、毒理学安全性评价资料或者检验报告、质量规格检验报告;(五)标签、说明书和食品添加剂产品样品;(六)其他国家(地区)、国际组织允许生产和使用等有助于安全性评估的资料。申请食品添加剂品种扩大使用范围或者用量的,可以免于提交前款第四项材料,但是技术评审中要求补充提供的除外。第七条 申请首次进口食品添加剂新品种的,除提交第六条规定的材料外,还应当提交以下材料:(一)出口国(地区)相关部门或者机构出具的允许该添加剂在本国(地区)生产或者销售的证明材料;(二)生产企业所在国(地区)有关机构或者组织出具的对生产企业审查或者认证的证明材料。第八条 申请人应当如实提交有关材料,反映真实情况,并对申请材料内容的真实性负责,承担法律后果。第九条 申请人应当在其提交的本办法第六条第一款第一项、第二项、第三项材料中注明不涉及商业秘密,可以向社会公开的内容。食品添加剂新品种技术上确有必要和使用效果等情况,应当向社会公开征求意见,同时征求质量监督、工商行政管理、食品药品监督管理、工业和信息化、商务等有关部门和相关行业组织的意见。对有重大意见分歧,或者涉及重大利益关系的,可以举行听证会听取意见。反映的有关意见作为技术评审的参考依据。第十条 卫生部应当在受理后60日内组织医学、农业、食品、营养、工艺等方面的专家对食品添加剂新品种技术上确有必要性和安全性评估资料进行技术审查,并作出技术评审结论。对技术评审中需要补充有关资料的,应当及时通知申请人,申请人应当按照要求及时补充有关材料。必要时,可以组织专家对食品添加剂新品种研制及生产现场进行核实、评价。需要对相关资料和检验结果进行验证检验的,应当将检验项目、检验批次、检验方法等要求告知申请人。安全性验证检验应当在取得资质认定的检验机构进行。对尚无食品安全国家检验方法标准的,应当首先对检验方法进行验证。第十一条 食品添加剂新品种行政许可的具体程序按照《行政许可法》和《卫生行政许可管理办法》等有关规定执行。第十二条 根据技术评审结论,卫生部决定对在技术上确有必要性和符合食品安全要求的食品添加剂新品种准予许可并列入允许使用的食品添加剂名单予以公布。对缺乏技术上必要性和不符合食品安全要求的,不予许可并书面说明理由。对发现可能添加到食品中的非食用化学物质或者其他危害人体健康的物质,按照《食品安全法实施条例》第四十九条执行。第十三条 卫生部根据技术上必要性和食品安全风险评估结果,将公告允许使用的食品添加剂的品种、使用范围、用量按照食品安全国家标准的程序,制定、公布为食品安全国家标准。第十四条 有下列情形之一的,卫生部应当及时组织对食品添加剂进行重新评估:(一)科学研究结果或者有证据表明食品添加剂安全性可能存在问题的;(二)不再具备技术上必要性的。对重新审查认为不符合食品安全要求的,卫生部可以公告撤销已批准的食品添加剂品种或者修订其使用范围和用量。第十五条 本办法自公布之日起施行。卫生部2002年3月28日发布的《食品添加剂卫生管理办法》同时废止。
今天国家局的专家们对我们进行工艺核查,问我们对照品的领用问题,一开口对照品有效期是多长?(不涉及特殊品种)未用完的对照品要不要进行再标定?多长时间标定?怎么保证未领用已开口的对照品的含量?企业对照品管理办法是否经过验证?
用比色法测环氧己烷残留量,其中品红-亚硫酸溶液的配制:称取0.1g品红,加入120mL热水溶解,冷却后加入10%亚硫酸钠溶液20mL,盐酸2mL置于暗处。试液应无色。可是我配制后发现有微红色,重配了一遍(品红热水溶解后进一步过滤了一下),仍旧带微红色,是怎么回事啊?有做过的请帮忙指点一下吧,谢谢!PS:我使用的品红为碱性的,酸也是强酸!那么,问题出在哪呢?
正在做一个6类化药,对照品中检院有提供;为了省钱,在中检院购买了一支对照品(100mg ),用来标定购买的原料药(GMP厂家提供)作为工作对照品;标定方法:按原料药质量标准全检,HPLC外标法标定含量(没做结构鉴定); 已经使用工作对照品做完了含量和溶出度的方法验证;问题来了: 1.在中检院可以提供对照品的情况下,可以使用自己标定的工作对照品么?(CDE审评三部张哲峰的文章:“不应使用其他来源者”,这话的意思是必须在中检院购买?); 2.如果可以使用工作对照品,那么,这样简单标定就可以使用了么? 3.如果不能使用工作对照品,那现在的情况下怎么补救? 请各位指教,谢谢!
[font=宋体]实验室新配置了对照品,对于对照品这方面的管理体系目前是没有的,现在有个疑问是实验室配制的对照品还需不需要使用部门去验收,制定期间核查计划的话,是新配一批就更新补充计划,还是可以笼统的写,不体现批号,一年只写一次?[/font]
各位大神,请教一个小白的问题,关于HPLC中对照品的配制。外标法测定麦芽糖浓度。麦芽糖对照品是99%纯度的一水合物,请教问题是:真空干燥24h后,对照品中的一水合物的水是否会被去除掉,称量的时候是按一水合物的分子量计算来称量,还是按没有水的纯麦芽糖分子量来称量比如要求称1g就在天平称1g?
标准对照品有没有出问题的,做了多年的能力验证了,是不是遇到过对照品的问题呢???
[size=5][b]食品添加剂新品种管理办法 [/b][/size][font=仿宋_GB2312][font=宋体][font=仿宋_GB2312][/font][/font][/font][align=center][font=宋体][size=4](卫生部令第73号)[/size][/font][/align][font=仿宋_GB2312]《食品添加剂新品种管理办法》已于2010年3月15日经卫生部部务会议审议通过,现予以发布,自发布之日起施行。[/font][font=仿宋_GB2312]部 长 陈 竺[/font][font=仿宋_GB2312]二○一○年三月三十日[/font][font=黑体]第一条[/font][font=仿宋_GB2312] [/font][font=仿宋_GB2312]为加强食品添加剂新品种管理,根据《食品安全法》和《食品安全法实施条例》有关规定,制定本办法。[/font][font=黑体]第二条[/font][font=仿宋_GB2312] [/font][font=仿宋_GB2312]食品添加剂新品种是指:[/font][font=仿宋_GB2312](一)未列入食品安全国家标准的食品添加剂品种; [/font][font=仿宋_GB2312](二)未列入卫生部公告允许使用的食品添加剂品种;[/font][font=仿宋_GB2312](三)扩大使用范围或者用量的食品添加剂品种。[/font][font=黑体]第三条[/font][font=仿宋_GB2312] [/font][font=仿宋_GB2312]食品添加剂应当在技术上确有必要且经过风险评估证明安全可靠。[/font][font=黑体]第四条[/font][font=仿宋_GB2312] [/font][font=仿宋_GB2312]使用食品添加剂应当符合下列要求:[/font][font=仿宋_GB2312](一)不应当掩盖食品腐败变质;[/font][font=仿宋_GB2312](二)不应当掩盖食品本身或者加工过程中的质量缺陷;[/font][font=仿宋_GB2312](三)不以掺杂、掺假、伪造为目的而使用食品添加剂;[/font][font=仿宋_GB2312](四)不应当降低食品本身的营养价值;[/font][font=仿宋_GB2312](五)在达到预期的效果下尽可能降低在食品中的用量;[/font][font=仿宋_GB2312](六)食品工业用加工助剂应当在制成最后成品之前去除,有规定允许残留量的除外。[/font][font=黑体]第五条[/font][font=仿宋_GB2312] [/font][font=仿宋_GB2312]卫生部负责食品添加剂新品种的审查许可工作,组织制定食品添加剂新品种技术评价和审查规范。[/font][font=黑体]第六条[/font][font=仿宋_GB2312] [/font][font=仿宋_GB2312]申请食品添加剂新品种生产、经营、使用或者进口的单位或者个人(以下简称申请人),应当提出食品添加剂新品种许可申请,并提交以下材料:[/font][font=仿宋_GB2312](一)添加剂的通用名称、功能分类,用量和使用范围;[/font][font=仿宋_GB2312](二)证明技术上确有必要和使用效果的资料或者文件;[/font][font=仿宋_GB2312](三)食品添加剂的质量规格要求、生产工艺和检验方法,食品中该添加剂的检验方法或者相关情况说明;[/font][font=仿宋_GB2312](四)安全性评估材料,包括生产原料或者来源、化学结构和物理特性、生产工艺、毒理学安全性评价资料或者检验报告、质量规格检验报告;[/font][font=仿宋_GB2312](五)标签、说明书和食品添加剂产品样品;[/font][font=仿宋_GB2312](六)其他国家(地区)、国际组织允许生产和使用等有助于安全性评估的资料。[/font][font=仿宋_GB2312]申请食品添加剂品种扩大使用范围或者用量的,可以免于提交前款第四项材料,但是技术评审中要求补充提供的除外。[/font][font=黑体]第七条[/font][font=仿宋_GB2312] [/font][font=仿宋_GB2312]申请首次进口食品添加剂新品种的,除提交第六条规定的材料外,还应当提交以下材料:[/font][font=仿宋_GB2312](一)出口国(地区)相关部门或者机构出具的允许该添加剂在本国(地区)生产或者销售的证明材料;[/font][font=仿宋_GB2312](二)生产企业所在国(地区)有关机构或者组织出具的对生产企业审查或者认证的证明材料。[/font][font=黑体]第八条[/font][font=仿宋_GB2312] [/font][font=仿宋_GB2312]申请人应当如实提交有关材料,反映真实情况,并对申请材料内容的真实性负责,承担法律后果。[/font][font=黑体]第九条[/font][font=仿宋_GB2312] [/font][font=仿宋_GB2312]申请人应当在其提交的本办法第六条第一款第一项、第二项、第三项材料中注明不涉及商业秘密,可以向社会公开的内容。[/font][font=仿宋_GB2312]食品添加剂新品种技术上确有必要和使用效果等情况,应当向社会公开征求意见,同时征求质量监督、工商行政管理、食品药品监督管理、工业和信息化、商务等有关部门和相关行业组织的意见。[/font][font=仿宋_GB2312]对有重大意见分歧,或者涉及重大利益关系的,可以举行听证会听取意见。[/font][font=仿宋_GB2312]反映的有关意见作为技术评审的参考依据。[/font][font=黑体]第十条[/font][font=仿宋_GB2312] [/font][font=仿宋_GB2312]卫生部应当在受理后60日内组织医学、农业、食品、营养、工艺等方面的专家对食品添加剂新品种技术上确有必要性和安全性评估资料进行技术审查,并作出技术评审结论。对技术评审中需要补充有关资料的,应当及时通知申请人,申请人应当按照要求及时补充有关材料。[/font][font=仿宋_GB2312]必要时,可以组织专家对食品添加剂新品种研制及生产现场进行核实、评价。[/font][font=仿宋_GB2312]需要对相关资料和检验结果进行验证检验的,应当将检验项目、检验批次、检验方法等要求告知申请人。安全性验证检验应当在取得资质认定的检验机构进行。对尚无食品安全国家检验方法标准的,应当首先对检验方法进行验证。[/font][font=黑体]第十一条[/font][font=仿宋_GB2312] [/font][font=仿宋_GB2312]食品添加剂新品种行政许可的具体程序按照《行政许可法》和《卫生行政许可管理办法》等有关规定执行。[/font][font=黑体]第十二条[/font][font=仿宋_GB2312] [/font][font=仿宋_GB2312]根据技术评审结论,卫生部决定对在技术上确有必要性和符合食品安全要求的食品添加剂新品种准予许可并列入允许使用的食品添加剂名单予以公布。[/font][font=仿宋_GB2312]对缺乏技术上必要性和不符合食品安全要求的,不予许可并书面说明理由。[/font][font=仿宋_GB2312]对发现可能添加到食品中的非食用化学物质或者其他危害人体健康的物质,按照《食品安全法实施条例》第四十九条执行。[/font][font=黑体]第十三条[/font][font=仿宋_GB2312] [/font][font=仿宋_GB2312]卫生部根据技术上必要性和食品安全风险评估结果,将公告允许使用的食品添加剂的品种、使用范围、用量按照食品安全国家标准的程序,制定、公布为食品安全国家标准。[/font][font=黑体]第十四条[/font][font=仿宋_GB2312] [/font][font=仿宋_GB2312]有下列情形之一的,卫生部应当及时组织对食品添加剂进行重新评估:[/font][font=仿宋_GB2312](一)科学研究结果或者有证据表明食品添加剂安全性可能存在问题的; [/font][font=仿宋_GB2312](二)不再具备技术上必要性的。[/font][font=仿宋_GB2312]对重新审查认为不符合食品安全要求的,卫生部可以公告撤销已批准的食品添加剂品种或者修订其使用范围和用量。[/font][font=黑体]第十五条[/font][font=仿宋_GB2312] [/font][font=仿宋_GB2312]本办法自公布之日起施行。卫生部2002年3月28日发布的《食品添加剂卫生管理办法》同时废止。[size=3]来源:[/size][url=http://www.moh.gov.cn/publicfiles/business/htmlfiles/mohzcfgs/s3576/201004/46908.htm][size=3]http://www.moh.gov.cn/publicfiles/business/htmlfiles/mohzcfgs/s3576/201004/46908.htm[/size][/url][/font]
请问各位老师做异丙醇和蔗糖红外鉴别用的什么对照品,中检院的对照品没说可以用于红外鉴别能用吗
做甲醇的时候要用到碱性品红做显色剂,可是买了几家的效果都不好,所以上来求助下大家,看看拿里有卖好的
石蕊,甲基橙,酚酞,品红是怎么变色的?
2016年 第14号 根据《食品安全法》规定,审评机构组织专家对食品用香料新品种9-癸烯-2-酮、茶多酚等7种食品添加剂扩大使用范围和食品营养强化剂钙扩大使用范围的安全性评估材料审查并通过。 特此公告。 附件:1. 食品用香料新品种9-癸烯-2-酮 2. 茶多酚等7种食品添加剂扩大使用范围 3. 食品营养强化剂钙扩大使用范围国家卫生计生委2016年11月1日