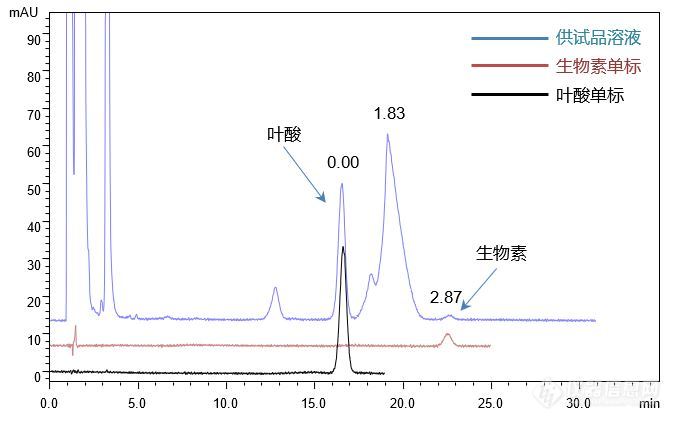
[align=center][b]注射用水溶性维生素的分析(2)[/b][/align][align=center][b]——叶酸,生物素[/b][/align]客户提供了注射用水溶性维生素粉针剂及对照品(叶酸,生物素),要求本实验室依据客户所提供方选择合适色谱柱,满足方法中对叶酸,生物素及其前后相邻杂质的分离要求,进而达到准确定量的目的。首先,依据客户提供的色谱条件我们尝试了使用中等极性色谱柱CAPCELL PAK C18 MGII S5 4.6 mm i.d. × 150 mm(A4AB 07251),分析对照品溶液与供试品溶液,结果如图1所示,对照品溶液中叶酸及生物素得到了良好的分离结果;在分析供试品溶液时,叶酸与其后杂质峰能够得到分离度为1.83的良好分离结果。[align=center][img=,673,421]http://ng1.17img.cn/bbsfiles/images/2018/01/201801110920_3890_2222981_3.jpg!w673x421.jpg[/img][/align][align=center]图1 CAPCELL PAK C[sub]18[/sub] MGII(150 mm)分析对照品及供试品溶液结果[/align]注*峰上所标数字为分离度,下同。[img=,673,298]http://ng1.17img.cn/bbsfiles/images/2018/01/201801110920_2922_2222981_3.jpg!w673x298.jpg[/img]为提高分离能力,使叶酸峰与其后杂质峰分的更远,我们尝试将色谱柱长度由150 mm换为250 mm,再一次分析供试品及对照品溶液,结果发现叶酸和生物素保留时间均明显延长,叶酸峰由16.97 min延长到29.03 min,此时叶酸峰与其后相邻杂质峰能够得到更好的分离,分离度为4.23,但同时也发现生物素峰被包于杂质峰中(如图2)。[align=center][img=,690,437]http://ng1.17img.cn/bbsfiles/images/2018/01/201801111011_6191_2222981_3.jpg!w690x437.jpg[/img][/align][align=center]图2 CAPCELL PAK C[sub]18[/sub] MGII(250 mm)分析对照品及供试品溶液结果[/align][align=left][img=,668,303]http://ng1.17img.cn/bbsfiles/images/2018/01/201801111011_2127_2222981_3.jpg!w668x303.jpg[/img][/align][align=left][/align][align=left]为使客户有更多色谱柱选择,本实验室也尝试了高碳载量的SUPERIOREX ODS色谱柱对对照品溶液及供试品溶液进行分析,同样能够得到待测组分与前后杂质峰的良好分离,分离度均在2.0以上;同时,我们也发现在分析供试品时,由于供试品中复杂基质的影响,叶酸峰会出现一定的拖尾现象(如图3)。[/align][align=left][/align][align=center][img=,619,394]http://ng1.17img.cn/bbsfiles/images/2018/01/201801111012_1478_2222981_3.jpg!w619x394.jpg[/img][/align][align=center] 图3 SUPERIOREX ODS分析对照品及供试品溶液结果[/align][align=center][/align][align=left][img=,687,297]http://ng1.17img.cn/bbsfiles/images/2018/01/201801111012_3462_2222981_3.jpg!w687x297.jpg[/img][/align][align=center][/align][align=left]我们也尝试使用可以在100%水系流动相下使用的高极性AQ色谱柱分析供试品溶液及对照品溶液,发现由于整体保留时间过长而使得生物素峰被包于杂质峰中,因此,我们尝试缩短整体保留时间,在药典规定范围内,提高流动相中有机相比例,将流动相比例由磷酸二氢钾缓冲溶液-乙腈(93:7)调整为(91:9),最终发现供试品中叶酸和生物素也能够与其相邻杂质峰取得良好分离结果,且分离度更佳(见图4)。[/align][align=left][/align][align=center][img=,655,416]http://ng1.17img.cn/bbsfiles/images/2018/01/201801111020_155_2222981_3.jpg!w655x416.jpg[/img][/align][align=center]图4 CAPCELL PAK C[sub]18 [/sub]AQ S3分析对照品及供试品溶液结果[/align][align=left][img=,661,296]http://ng1.17img.cn/bbsfiles/images/2018/01/201801111021_778_2222981_3.jpg!w661x296.jpg[/img][/align][align=left][/align][align=left]综上实验结果,使用中等极性的[b]CAPCELL PAK C[sub]18[/sub] MGII S5[/b] 4.6mm i.d. × 150 mm(A4AB 07251)和高碳载量的[b]SUPERIOREX ODS S5[/b] 4.6 mm i.d. × 150 mm(AZAB 12684)色谱柱,在客户原条件下,均能够实现叶酸、生物素及其相邻杂质间的良好分离;[/align][align=left]使用高极性[b]CAPCELL PAK C[sub]18[/sub] AQ S3[/b] 4.6 mmi.d. × 150 mm(A7AB 02100)色谱柱,在药典规定流动相可调整范围内,将流动相中磷酸盐缓冲液和乙腈比例调整为91 / 9(原条件为93 / 7),也可实现注射用水溶性维生素中叶酸和生物素及相邻杂质的良好分离。[/align]
分享标准,均自网络收集,上传者不保证资料完整性以及版权。下载仅供研究,请勿用于其他用途。研究完毕请及时删除,若有正版需求,请联系出版单位。GB 5413.19-2010 婴幼儿食品和乳品中游离生物素的测定
本人急需氘代生物素作为内标,不知道在哪里可以买到,请高手指点!感谢!
[b][font=宋体]一、引言[/font][/b][font=宋体] [/font][font=宋体]在生物学和医学的研究中,抗体标记技术已成为一种重要的研究手段。其中,生物素标记抗体凭借其独特的优势,在许多领域中得到了广泛应用。本文将详细介绍生物素标记抗体的原理、应用及发展前景。[/font][font=宋体] [/font][b][font=宋体]二、生物素标记抗体的原理[/font][/b][font=宋体] [/font][font=宋体][font=宋体]生物素,又称维生素[/font][font=Calibri]H[/font][font=宋体],是一种存在于自然界中的小分子有机物质。它可以通过化学反应与抗体结合,生成生物素标记抗体。这一过程通常是在抗体的氨基基团上连接一个生物素衍生物,形成共价键。这种连接方式不会改变抗体的免疫活性,同时使得生物素标记抗体能够与相应的抗原结合。[/font][/font][b][font=宋体] [/font][font=宋体]三、生物素标记抗体的应用[/font][/b][font=宋体] [/font][font=宋体]免疫分析:生物素标记抗体在免疫分析中发挥了重要作用。通过将生物素标记抗体与相应的抗原结合,可以实现对抗原的灵敏检测。这种方法被广泛应用于生物学、医学及食品安全等领域。[/font][font=宋体]蛋白质组学研究:在蛋白质组学研究中,生物素标记抗体可用于蛋白质的分离和纯化。通过生物素标记抗体与抗原的特异性结合,可以从复杂的蛋白质混合物中分离出目标蛋白质。[/font][font=宋体]细胞生物学研究:生物素标记抗体在细胞生物学研究中具有广泛的应用价值。例如,通过生物素标记抗体追踪细胞内蛋白质的分布和动态变化,有助于深入了解细胞的生命活动。[/font][font=宋体]疾病诊断与治疗:生物素标记抗体在疾病诊断和治疗中也发挥了重要作用。例如,针对癌症的免疫治疗中,生物素标记抗体可以用于识别和攻击癌细胞,从而达到治疗目的。[/font][font=宋体] [/font][b][font=宋体]四、发展前景[/font][/b][font=宋体] [/font][font=宋体]随着生物学和医学技术的不断进步,生物素标记抗体的应用前景日益广阔。未来,随着技术的不断创新和完善,生物素标记抗体的性能将得到进一步提升,从而推动其在更多领域中的应用。同时,随着人类对生命现象认识的深入,将有更多具有挑战性的研究课题需要借助生物素标记抗体这一强大工具。[/font][b][font=宋体] [/font][font=宋体]五、结语[/font][/b][font=宋体] [/font][font=宋体]生物素标记抗体作为一种重要的研究手段,在生物学、医学及其他相关领域中发挥着不可或缺的作用。随着技术的不断进步和应用领域的拓展,我们有理由相信,生物素标记抗体的未来将更加光明,为人类探索生命奥秘提供更多可能性。[/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供[url=https://cn.sinobiological.com/category/biotinylated-protein-elite][b]生物素标记蛋白[/b][/url]相关产品,详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/category/biotinylated-protein-elite[/font][/font][b][font=宋体] [/font][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b]

http://ng1.17img.cn/bbsfiles/images/2012/11/201211201436_405528_2518341_3.jpg其一款婴儿奶粉在香港被查出生物素含量不达标,可导致婴儿脱发、皮疹等,香港食环署已建议停售,至此相关奶粉的事件已经成为常态新闻了,三聚氰胺、婴儿提早发育、还有婴儿脱发等等,这些让人触目惊心的新闻背后到底有多少不可告人的秘密?根据食环署近日公布的一份报告,明治细仔奶粉0-12个月(850克)的生物素含量只有0.81微克/100千卡,低于食品法典委员会标准。风险评估发现,如根据标签上的喂哺建议,其生物素摄入量将低于世界卫生组织建议的摄入量5微克/日。而另一款和光堂的初生婴儿奶粉为0.68微克/100千卡,同样低于食品法典委员会标准。食物安全中心发言人表示,膳食生物素缺乏症是非常罕见的,未曾在母乳喂养的婴儿出现。但是如果零至6个月大婴儿长期只单纯靠上述奶粉摄取生物素,不排除对健康有不良影响。生物素缺乏的婴儿可能会出现脱发、皮疹、肌肉张力低、嗜睡等症状。你家的孩子现在吃的是什么奶粉?奶瓶塑化剂事件刚过,奶粉生物素问题又来了,怎样才能给自己孩子的健康给一个安全的保障?奶粉中生物素含量应该怎么来测定?奶粉生物素含量国家标准有哪些?生物素的物性是什么?为什么会引起婴儿脱发?
最近用陆桥的微孔板做生物素,结果简直惨不忍睹,3个平行偏差好大,标曲去了好多点才勉强到0.99,质控样的平行也很差,值也做不准,一次偏大一次又偏小。请老师指导该怎么做
[font=宋体][font=宋体]生物素[/font][font=Calibri]-[/font][font=宋体]亲和素系统 [/font][font=Calibri](biotin-avidin system[/font][font=宋体],[/font][font=Calibri]BAS)[/font][font=宋体],是[/font][font=Calibri]70[/font][font=宋体]年代后期应用于免疫学,并得到迅速发展的一种常用的生物反应放大系统。它具有高度特异性、敏感性、稳定性的特点,两者的亲和常数([/font][font=Calibri]K=1015 mol/L[/font][font=宋体])比抗原[/font][font=Calibri]-[/font][font=宋体]抗体([/font][font=Calibri]K=105[/font][font=宋体]~[/font][font=Calibri]1011 mol/L[/font][font=宋体])至少高[/font][font=Calibri]1[/font][font=宋体]万倍,是目前已知强度最高的非共价作用,这使得生物素标记的蛋白成为研究蛋白质相互作用和筛选抗体或小分子潜力药物的强大工具。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州开发了丰富的生物素标记蛋白产品,拥有[/font][font=Calibri]Avi-tag[/font][font=宋体]定点标记和化学标记两种类型的生物素标记蛋白,覆盖细胞治疗、抗体药、疫苗等热门靶点。产品具有高批间一致性、高活性等优势,适用于[/font][font=Calibri]ELISA[/font][font=宋体]、[/font][font=Calibri]Biopanning[/font][font=宋体]、[/font][font=Calibri]SPR / BLI[/font][font=宋体]等实验。下面为大家提供生物素蛋白标记常见问题及注意事项:[/font][/font][font=宋体] [/font][font=宋体][b]生物素蛋白标记常见问题:[/b][/font][font=宋体] [/font][font=宋体][font=Calibri]1[/font][font=宋体]、什么是生物素标记蛋白[/font][font=Calibri]?[/font][/font][font=宋体][font=宋体]在生物化学中,生物素化蛋白质就是生物素与蛋白质等大分子物质共价结合的产物。生物素[/font][font=Calibri]-[/font][font=宋体]亲和素亲和常数至少比抗原[/font][font=Calibri]-[/font][font=宋体]抗体高一万倍[/font][font=Calibri],[/font][font=宋体]是目前发现的自然界中具有最强亲和力的物质。因此,生物素[/font][font=Calibri]-[/font][font=宋体]亲和素系统已被广泛地应用于免疫诊断技术。生物素化蛋白的出现,也为类似于[/font][font=Calibri]WB[/font][font=宋体]实验简化了流程,提高了效率。此外,由于生物素的小尺寸([/font][font=Calibri]MW = 244.31g / mol[/font][font=宋体]),不太影响蛋白质本身的天然功能。所以它同时具备了高亲和力、高特异性、高灵敏度的优点。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2[/font][font=宋体]、生物素标记蛋白有哪些应用?[/font][/font][font=宋体][font=宋体]生物素标记蛋白广泛的应用在生物技术的众多领域。如透析,将具有特殊结构的亲和分子制成固相吸附剂放置在层析柱中,当要被分离的蛋白混合液通过层析柱时,与吸附剂具有亲和能力的蛋白质就会被吸附而滞留在层析柱中。那些没有亲和力的蛋白质由于不被吸附,直接流出,从而与被分离的蛋白质分开,然后选用适当的洗脱液,[/font] [font=宋体]改变结合条件将被结合的蛋白质洗脱下来。怎么释放所需蛋白呢?这需要非常严苛的条件(例如,[/font][font=Calibri]pH=1.5[/font][font=宋体]的 [/font][font=Calibri]GuHCl[/font][font=宋体]),这种极端条件下的蛋白是会变性的。如果需要分离标记的蛋白质,最好用亚氨基生物素标记的蛋白质。该种生物素在碱性条件下与抗生物素蛋白结合紧密,但是在降低[/font][font=Calibri]pH[/font][font=宋体]以后,亲和力降低。因此亚氨基生物素标记蛋白可以通过降低[/font][font=Calibri]pH([/font][font=宋体]约[/font][font=Calibri]pH=4)[/font][font=宋体]从柱子上释放。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]免疫检测中的应用:在常规[/font][font=Calibri]ELISA[/font][font=宋体]原理的基础上,结合生物素[/font][font=Calibri](B)[/font][font=宋体]与亲和素[/font][font=Calibri](A)[/font][font=宋体]间的高度放大作用,而建立的一种检测系统。生物素很易与蛋白质[/font][font=Calibri]([/font][font=宋体]如抗体等[/font][font=Calibri])[/font][font=宋体]以共价键结合。这样,结合了酶的亲和素分子与结合有特异性抗体的生物素分子产生反应,既起到了多级放大作用,又由于酶在遇到相应底物时的催化作用而呈色,达到检测未知抗原[/font][font=Calibri]([/font][font=宋体]或抗体[/font][font=Calibri])[/font][font=宋体]分子的目的。 这可以用于通过荧光或电子显微镜定位的[/font][font=Calibri]ELISA[/font][font=宋体]测定,[/font][font=Calibri]ELISPOT[/font][font=宋体]测定,[/font][font=Calibri]western[/font][font=宋体]印迹和其他免疫分析方法。[/font][/font][font=宋体] [/font][font=宋体][b]生物素标记注意事项:[/b][/font][font=宋体] [/font][font=宋体][font=Calibri]1[/font][font=宋体]、依抗原或抗体分子所带可标记基团的种类(氨基、醛基或巯基)以及分子的酸碱性,选择相应的活化生物素和反应条件;[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2[/font][font=宋体]、标记反应时,活化生物素与待标记抗原或抗体应有适当的比例;生物素:[/font][font=Calibri]IgG [/font][font=宋体]用量比[/font][font=Calibri](mg/mg)[/font][font=宋体]宜为[/font][font=Calibri]2:1, IgG[/font][font=宋体]应用浓度[/font][font=Calibri]0.5~5[/font][font=宋体]μ[/font][font=Calibri]g/ml [/font][font=宋体]生物素[/font][font=Calibri]1~3[/font][font=宋体]个[/font][font=Calibri]/Ag[/font][font=宋体],[/font][font=Calibri]3~5[/font][font=宋体]个[/font][font=Calibri]/Ab[/font][font=宋体];[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]3[/font][font=宋体]、为减少空间位阻影响,可在生物素与被标记物之间加入交联臂样结构;[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]4[/font][font=宋体]、生物素与抗原、抗体等蛋白质结合后,不影响后者的免疫活性;标记酶时则结果有不同。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][font=宋体]更多关于[url=https://cn.sinobiological.com/category/biotinylated-protein-elite][b]生物素标记蛋白[/b][/url]详情可以参看:[/font][font=Calibri]https://cn.sinobiological.com/category/biotinylated-protein-elite[/font][/font][font=宋体] [/font]
婴幼儿食品中B12 叶酸 泛酸 生物素有没有不用微生物法的其他检测方法?望老师不吝赐教
[color=#444444]先已合成的生物素的中间体:双苄基生物素和双苄烯生物素的液相色谱峰重叠,有何办法能将两峰分开。[/color][color=#444444]采用的色谱条件是:C18柱,流动相是磷酸盐缓冲溶液:乙腈=60:40,流速1ml/min, 波长210 nm[/color]
VitaFast Vitamin B7 生物素试剂盒简单易用,采用微生物方法,在微孔板中定量检测食品和药品中的生物素总量(包括添加和原生生物素)。AOAC – RI认证的样品: 婴幼儿配方乳粉、谷类食品、药丸、散剂、果汁和牛奶
玉米浆前处理求教测玉米浆中生物素含量,由于含量低,需要浓缩并除去蛋白等杂质,怎么处理才能使生物素的损失最小?
叶酸生物素有色谱方法检测吗?望老师不吝赐教
[color=#444444]用微生物法检测维生素B12,生物素,叶酸,德国拜发的试剂盒,那个方法确认怎么做[/color]
我们实验室用VitaFast的试剂盒检测乳粉中的生物素,之前一直以来做出来的数据还不错,但最近一段时间总是黑暗孵育24h后每个孔都混浊了,就连空白对照也混浊了,我们分析了原因,考虑是不是培养基污染了?还是加样的时候污染了?我们重新配制了新的培养基,重复做了几次,总是出现偶尔正常,偶尔被污染的状况,但是B12和叶酸却没有这样的事情发生,我们也问过试剂公司,他们说其它购买的使用者没有出现像我们一样的情况~~~~~ 我们也重新拿了新购买未开封的试剂盒重复去检测了,所有的枪头也是用原装的,滤膜是用0.22um的。但还是偶尔出现全板被污染的情况,偶尔又是正常的,实在搞不懂是因为什么原因?希望大家有经验的帮帮忙,我们要怎么做才能找到被污染的原因,排除污染源,看看是哪个环节出了问题,谢谢大家!
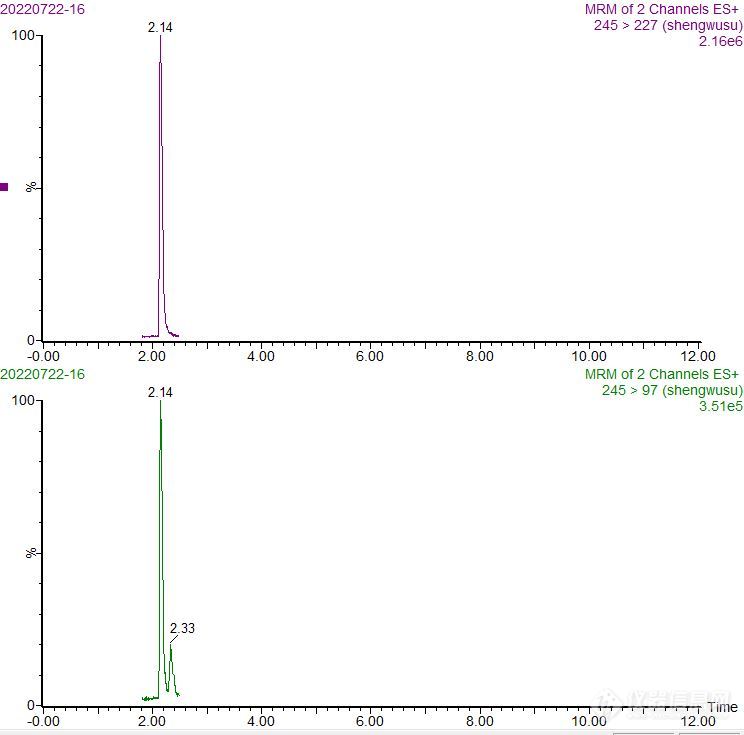
[size=16px]超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法测定奶粉中生物素的含量[/size][align=center][size=16px]户江涛[/size][/align][align=center][size=16px](黑龙江省农垦科学院测试化验中心,黑龙江 佳木斯 154007 )[/size][/align][size=16px]摘要:采用超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法建立了检测奶粉中生物素含量的分析方法,对试样提取、净化条件,流动相、色谱柱和质谱条件进行了优化,结果表明该方法与国标微生物法对同一样品检测得到的生物素含量基本一致,但检测所需时间大大减少,且抗干扰能力、精密度均比微生物法高,特别适和大批量奶粉中生物素含量检测。关键词:超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱;奶粉;生物素生物素又称维生素B7,是生物体内羧基转化酶作用的一种辅酶,在人体生长、代谢、发育过程中发挥着重要的作用。人类自身不能合成生物素,需从膳食中获得,而奶粉是人类(特别是婴幼儿)获取生物素的重要途径,准确测定奶粉中生物素含量有重要意义。目前国家标准规定的生物素测定方法《GB 5009.259-2016 食品安全国家标准 食品中生物素的测定》为微生物法。该方法需要购买特定菌种,成本较高,且菌种难保存、易受污染,实验操作复杂、费时费力、技术难度大、对检验人员和实验室要求较高,且容易受到基质干扰、检测结果重复性较差。同时奶粉成分复杂,所含生物素含量极低,一般为十几个微克/100克。因此,制定一种准确、高效、便捷、灵敏度高的生物素测定方法迫在眉睫。基于高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]的分离能力和质谱的高灵敏度、高选择性,采用[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]串联质谱测定法具有前处理简单、分析速度快,适用的基质范围广、实用性强,可以为奶粉中生物素含量的测定提供一种有效的检测手段。本文建立的超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法测定奶粉中生物素含量[color=black]的方法前处理过程简便、分析时间短、灵敏度高、抗干扰能力强,特别适用于大批量奶粉样品中生物素[/color]含量的检测。1 实验部分1.1 材料与试剂[color=black]生物素(纯度[/color][font=宋体][color=black]≥[/color][/font][color=black]99%,Sigma公司);婴儿配方乳粉定量分析质控样品(BQC1051147452,北京普天同创生物科技有限公司);乙腈、甲酸(色谱纯,Fisher公司);Prime HLB固相萃取柱(200 mg,3 mL,[/color][font=宋体]Waters[/font][color=black]公司);0.2 um有机系滤膜;实验用水为Millipore纯水仪制备。[/color]1.2 仪器与设备UPLC XEVO TQ-S超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]串联质谱仪(Waters公司);涡旋振荡器。1.3 [color=black]生物素[/color]标准储备液的配置称取一定量生物素[color=black]标准品[/color],用50%乙醇-水溶液配置成质量浓度为100 ug/mL标准储备液,于2~4℃冰箱保存(有效期1个月),待用;临用前将溶液回温至室温,并吸取一定体积储备液用水逐级稀释成所需浓度的标准工作液。1.4 样品前处理准确称取1.00 g(精确到0.01 g)奶粉试样于50 mL离心管中,加入10.00 mL纯水涡旋混匀2 min,然后加入10.00 mL乙腈,涡旋混匀1 min,然后在离心机中以15000 r/min离心5 min,取出后吸取2 mL上清液置于[color=black]Prime HLB固相萃取柱中,使其自然流出弃去最初几滴,然后用玻璃试管接取流出液约1 mL涡旋混匀,[/color]过0.22[font=宋体]u[/font]m有机系微孔滤膜后供UP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS分析测定。1.5 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]及质谱条件[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]:色谱柱:Waters HSS [font=times new roman]T3(1.8 μm,100mm×2.1mm);柱温:30℃[/font];流速:[font=times new roman]0.3 [/font]mL/min;进样量:[font=times new roman]2[/font] [font=times new roman]μL;流动相A:乙腈;流动相B:0.1%的甲酸水溶液。梯度洗脱程序:0~0.5min,10% A;0.5~3. 0 min,10%~100% A;3. 0 ~4. 0 min,100%A,4 ~4.1min,100% A~10% A,4.1 ~5.0min 10% A。[/font]质谱:离子源:电喷雾离子源( ESI [sup]+[/sup] ) ;扫描方式:正离子扫描;检测方式:多反应监测( MRM);毛细管电压:3.2 kv;离子源温度:150℃;去溶剂气温度:500℃;去溶剂气流量:1000 L /h;定性、定量离子对及碰撞能量见表1。[/size][align=center][size=16px]表1生物素的质谱参数[/size][/align][table][tr][td][align=center][size=16px]分析物[/size][/align][/td][td][align=center][size=16px]锥孔电压/V[/size][/align][/td][td][align=center][size=16px]母离子/(m/z)[/size][/align][/td][td][align=center][size=16px]子离子/(m/z) [/size][/align][/td][td][align=center][size=16px]碰撞能量/V[/size][/align][/td][/tr][tr][td][size=16px]生物素[/size][/td][td][align=center][size=16px]30[/size][/align][size=16px][/size][/td][td][align=center][size=16px]245[/size][/align][size=16px][/size][/td][td][align=center][size=16px]227﹡[/size][/align][align=center][size=16px]97[/size][/align][size=16px][/size][/td][td][align=center][size=16px]13[/size][/align][align=center][size=16px]25[/size][/align][size=16px][/size][/td][/tr][/table][size=16px]﹡为定量离子2 结果与讨论2.1 色谱质谱条件及前处理过程的优化流动相的选择:对比了酸性体系(0.1%甲酸水溶液)与甲醇、乙腈的流动相体系组合,结果发现生物素在乙腈体系中响应值比甲醇更好一些,故本研究采用0.1%甲酸水溶液+甲醇流动相体系。色谱柱的选择:比较了[font=宋体]Waters [/font]BEH C[sub]18[/sub](1.7 μm,50mm×2.1mm)和[font=宋体]Waters [/font]HSS T[sub]3[/sub](1.8 μm,100mm×2.1mm)两种不同填料的分析柱,实验时发现目标物在这两款色谱柱上响应值差不多,但目标物在BEH C[sub]18[/sub]上保留时间比HSS T[sub]3[/sub]要短,考虑到生物素本身属于水溶性维生素,极性较强,若出峰太早可能造成奶粉中一些极性强的基质随目标物一起共流出进而干扰目标物测定,因此本方法采用了HSS T[sub]3[/sub]色谱柱。质谱参数优化:将1.0 mg/L 生物素标准溶液直接注射到质谱中,在正离子模式下进行母离子全扫描,发现目标物各自对应的准分子离子峰[M+H][sup]+[/sup]具有很好的响应,然后在分别进行子离子全扫描,各得到两对丰度高、干扰小的子离子对进行MRM监测,最终确定的质谱条件见表1,相应的色谱质谱图见图1、图2。前处理过程优化:生物素属于水溶性维生素,用纯水作为提取试剂可以得到很好的提取效果。但实验过程中发现,用纯水将奶粉溶解后整个溶液呈乳白色,只通过离心方式很难去除其中大量的蛋白、脂肪等杂质,需要对提取液进行除蛋白操作。通过考察乙酸铅、三氯乙酸、乙腈等几种常用的沉淀蛋白方法,综合考虑在去除蛋白的同时要尽可能减少其它杂质的引入,因此本方法采用乙腈除蛋白的方式,比较了几种不同水/乙腈比例,最终选定水/乙腈(1:1体积比)达到最优的实验效果。对于脂肪的去除则选用了目前较流行的[color=black]Prime HLB固相萃取柱通过式方法,即提取液通过Prime HLB时脂肪等大分子保留在SPE小柱上,目标物不保留以达到去除脂肪等杂质的目的,[/color]综合以上因素本实验最终采用了1.4的前处理方法。[/size][align=center][size=16px][img]https://ng1.17img.cn/bbsfiles/images/2022/10/202210071506558084_124_1729077_3.jpg[/img][/size][/align][align=center][size=16px]图1 [color=black]生物素[/color]标准溶液(10 ng/mL)MRM色谱图[/size][/align][size=16px][/size][align=center][size=16px][img]https://ng1.17img.cn/bbsfiles/images/2022/10/202210071506561980_1283_1729077_3.jpg[/img][/size][/align][align=center][size=16px]图2 奶粉样品中[color=black]生物素[/color]MRM色谱图[/size][/align][size=16px][color=black]2.2 线性范围和定量限[/color][color=black]吸取不同体积的生物素标准储备液(1.3),用[/color]纯水[color=black]分别配置不同浓度的[/color]上机标准溶液,以各自定量离子的峰面积(或与内标峰面积比值)为Y对应质量浓度X([color=black]m[/color]g/L)做标准曲线,得到的线性方程和相关系数见表2;以10倍信噪比(S/N)计算得到生物素的定量下限,结果见表2。表2 生物素标准溶液的线性方程、相关系数和定量下限(LOQ)[/size][table][tr][td][align=center][size=16px]分析物[/size][/align][/td][td][align=center][size=16px]线性范围/(ng/mL)[/size][/align][/td][td][align=center][size=16px]线性方程[/size][/align][/td][td][align=center][size=16px]R[/size][/align][/td][td][align=center][size=16px]LOQ/(ug/100g)[/size][/align][/td][/tr][tr][td][align=center][size=16px]生物素[sub] [/sub][/size][/align][/td][td][align=center][size=16px]0.2~50[/size][/align][size=16px][/size][/td][td][align=center][size=16px]Y=3078.1X-106.32[/size][/align][size=16px][/size][/td][td][align=center][size=16px]0.9993[/size][/align][size=16px][/size][/td][td][align=center][size=16px]0.5[/size][/align][/td][/tr][/table][size=16px][color=black]2.3回收率和精密度[/color][color=black]生物素在奶粉中天然存在[/color],选取已知生物素含量的奶粉作为基质进行加标。具体添加水平为:[color=black]0.5,5,50[/color] ug/100g。[color=black]每个[/color]水平重复6次,[color=black]同时做该奶粉的本底实验。[/color]按照1.4前处理方法处理后上机检测,回收率计算结果(扣除空白后)见表3。结果表明,该方法生物素的平均回收率为87.2%~110%,相对标准偏差(RSD,n=6)为2.3%~5.2%,均满足实验要求。[/size][align=center][size=16px]表3 奶粉生物素的加标回收率和相对标准偏差(n=6)[/size][/align][table][tr][td][align=center][size=16px]分析物[/size][/align][/td][td][align=center][size=16px]添加水平(ug/100g)[/size][/align][/td][td][align=center][size=16px]回收率/%[/size][/align][/td][td][align=center][size=16px]相对标准偏差/%[/size][/align][/td][/tr][tr][td][align=center][size=16px]生物素[/size][/align][size=16px][sub] [/sub][/size][/td][td][align=center][size=16px]0.5[/size][/align][align=center][size=16px]5[/size][/align][align=center][size=16px]50[/size][/align][/td][td][align=center][size=16px]86.8[/size][/align][align=center][size=16px]93.2[/size][/align][align=center][size=16px]91.6[/size][/align][size=16px][/size][/td][td][align=center][size=16px]4.6[/size][/align][align=center][size=16px]3.3[/size][/align][align=center][size=16px]2.1[/size][/align][size=16px][/size][/td][/tr][/table][size=16px][color=black]2.4实际样品分析[/color][color=black]为进一步验证该方法的准确性,采用本方法和《[/color]GB 5009.259-2016[color=black]》微生物法同时对北京普天同创生物科技有限公司的奶粉质控样品BQC1051147452生物素含量进行检测,结果见表4[/color]。由表4可知,UP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS法测定结果与国标方法的结果基本一致,无显著性差异,但前者所需时间更短,精密度更好。[/size][align=center][size=16px]表4 奶粉质控样品[color=black]BQC1051147452[/color]生物素的测定结果[/size][/align][table][tr][td][align=center][size=16px]检测方法[/size][/align][/td][td][align=center][size=16px]特性值区间(ug/100g)[/size][/align][/td][td][align=center][size=16px]测定平均值(n=6)[/size][/align][/td][td][align=center][size=16px]相对标准偏差/%(n=6)[/size][/align][/td][/tr][tr][td][size=16px]UP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS法微生物法[sub] [/sub][/size][/td][td][align=center][size=16px]15.6~22.4[/size][/align][align=center][size=16px]15.6~22.4[/size][/align][size=16px][/size][/td][td][size=16px]18.718.1[/size][/td][td][align=center][size=16px]2.5[/size][/align][size=16px] 4.6[/size][/td][/tr][/table][size=16px]3 结语本文建立了超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法(UP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS)测定奶粉中[color=black]生物素[/color]含量的分析方法。该方法具有较高的灵敏度、准确度和精密度,前处理步骤简单,分析速度快,特别适合大批量样品的检测。参考文献:[1] GB 5009.259-2016 食品安全国家标准 食品中生物素的测定.[2] 薛霞, 赵慧男, 魏莉莉, 等. 超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法测定蜂蜜中五种水溶性维生素的含量[J]. 食品与发酵工业. 2021,47(12) : 250-256.[3] 李佳兴, 周利, 金艳, 等. 超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法测定枸杞子中8种水溶性维生素[J]. 食品科技. 2018,43(11) : 336-341.[/size]
[b][font=宋体][color=#060607]前言[/color][/font][/b][font=宋体][font=宋体]在生物医学研究领域,蛋白质的功能性鉴定及其在各种生物过程中的作用机制一直是科研人员关注的焦点。近年来,质谱技术因其高分辨率和高灵敏度在蛋白质组学研究中发挥着越来越重要的作用。然而,传统的质谱策略在鉴定具有特定生物功能的蛋白质亚群时,常常受到标记物与非标记物区分困难的限制。为了解决这一问题,科学家们开发了一种名为[/font][font=宋体]“直接检测含生物素标签的蛋白质”([/font][font=Calibri]Direct Detection of Biotin-containing Tags, DiDBiT[/font][font=宋体])的新技术,显著提高了生物素化蛋白质的直接检测效率。[/font][/font][font=Calibri] [/font][b][font=宋体][font=Calibri]DiDBiT[/font][font=宋体]技术检测方法[/font][/font][/b][font=宋体][font=Calibri]DiDBiT[/font][font=宋体]主要是利用质谱技术([/font][font=Calibri]MS/MS[/font][font=宋体])来直接检测含生物素的肽段,无需额外的实验步骤即可直接鉴定生物素化蛋白质。与传统的生物素蛋白质鉴定方法相比,[/font][font=Calibri]DiDBiT[/font][font=宋体]技术显著提高了检测的灵敏度和效率。[/font][font=Calibri]DiDBiT[/font][font=宋体]技术通过优化样品的预处理和质谱分析步骤来提高生物素化肽段的检测灵敏度。首先对细胞裂解物进行蛋白质消化,然后使用[/font][font=Calibri]NeutrAvidin[/font][font=宋体]珠子富集含生物素的肽段,最后进行质谱分析。这种方法的关键在于通过降低样品复杂性,提高了生物素标记肽段的检出率。[/font][/font][font=Calibri] [/font][b][font=宋体][font=Calibri]DiDBiT[/font][font=宋体]技术的应用[/font][/font][/b][font=Calibri]Lucio Matias[/font][font=宋体][font=宋体]等人采用[/font][font=Calibri]DiDBiT[/font][font=宋体]技术,在啮齿动物的神经系统中标记新合成的蛋白质,结果表明使用[/font][font=Calibri]DiDBiT[/font][font=宋体]技术提高了生物素标记新合成蛋白质的检测,与传统方法相比,检测灵敏度提高了约[/font][font=Calibri]20[/font][font=宋体]倍。他们还成功地应用[/font][font=Calibri]DiDBiT[/font][font=宋体]技术在成年大鼠视网膜中直接检测新合成的蛋白质,显示出前所未有的时间分辨率,短至[/font][font=Calibri]3[/font][font=宋体]小时。[/font][/font][font=宋体][font=宋体]此外,[/font][font=Calibri]DiDBiT[/font][font=宋体]技术具有高度的灵活性和可扩展性。它可以与其他蛋白质组学技术相结合,如蛋白质相互作用研究、蛋白质翻译后修饰分析等,从而为我们提供更为全面和深入的蛋白质功能信息。[/font][/font][font=宋体][font=Calibri]DiDBiT[/font][font=宋体]技术的应用展示了其在蛋白质组学研究中的广泛潜力,尤其是在快速鉴定特定细胞类型或生物学状态下新合成蛋白质的能力。此技术不仅提高了实验的准确性和效率,而且通过直接检测生物素化肽段,显著简化了实验流程,降低了实验的复杂性和成本。[/font][/font][font=Calibri] [/font][b][font=宋体]结论[/font][/b][font=宋体][font=Calibri]DiDBiT[/font][font=宋体]技术提供了一种强大的工具,用于在复杂生物样本中直接鉴定和分析含生物素的蛋白质。这种高灵敏度和高分辨率的策略适用于广泛的生物标记策略和样本准备,显著提高了从样本中区分真实候选物和污染物的能力。此技术特别适用于含量较少的生物素化蛋白质的研究,为蛋白质组学和细胞生物学提供了新的研究工具。[/font][/font][font=Calibri] [/font][font=宋体]本篇文章由义翘神州编辑整理,同时义翘神州提供[/font][url=https://cn.sinobiological.com/category/biotinylated-protein-elite][u][font=宋体][color=#0000ff][b]生物素标记蛋白[/b][/color][/font][/u][/url][font=宋体],更多详情可以点击查看![/font][font=宋体]参考文献:[/font][font=宋体][font=Calibri]Schiapparelli LM, McClatchy DB, Liu HH, Sharma P, Yates JR 3rd, Cline HT. Direct detection of biotinylated proteins by mass spectrometry. J Proteome Res. 2014 13(9):3966-3978. doi:10.1021/pr5002862[/font][/font]
玉米浆前处理求教测玉米浆中生物素含量,由于含量低,需要浓缩并除去蛋白等杂质,怎么处理才能使生物素的损失最小?
有朋友做D-泛酸钙或生物素吗?请问出峰时间大概在几分钟?谢谢我用的是WATERS1525型,紫外检测器,碳十八柱.3.9*150.我做了,D-泛酸钙在两分钟有一倒峰连着一个正峰,四分钟有一个正峰.标准品也是这样的.我就不知道哪个才是正确的峰.所以想请教有没有做过的是怎么确定的?
[font=宋体][font=宋体]义翘神州开发了丰富的生物素标记蛋白产品,拥有[/font][font=Calibri]Avi-tag[/font][font=宋体]定点标记和化学标记两种类型的生物素标记蛋白,覆盖细胞治疗、抗体药、疫苗等热门靶点。产品具有高批间一致性、高活性等优势,适用于[/font][font=Calibri]ELISA[/font][font=宋体]、[/font][font=Calibri]Biopanning[/font][font=宋体]、[/font][font=Calibri]SPR / BLI[/font][font=宋体]等实验。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]Avi-Tag[/font][font=宋体]生物素标记蛋白:[/font][/font][font=宋体][font=Calibri]Avi-tag[/font][font=宋体]重组蛋白融合一个额外的[/font][font=Calibri]15[/font][font=宋体]个氨基酸序列,即[/font][font=Calibri]Avi-tag[/font][font=宋体],通常连接至蛋白的[/font][font=Calibri]N-[/font][font=宋体]或[/font][font=Calibri]C-[/font][font=宋体]末端。 [/font][font=Calibri]Avi-tag[/font][font=宋体]肽段被大肠杆菌生物素连接酶[/font][font=Calibri]BirA[/font][font=宋体]所识别,[/font][font=Calibri]BirA[/font][font=宋体]连接酶通过酶促反应将生物素连接到[/font][font=Calibri]Avi-tag[/font][font=宋体]序列内的单个赖氨酸残基。因此,[/font][font=Calibri]Avi[/font][font=宋体]标签蛋白以特定位点的方式进行生物素化,从而实现标记均一。 这使固定在亲和素包被表面的蛋白方向具有一致性,并且由于[/font][font=Calibri]Avi[/font][font=宋体]标签位于蛋白的末端,因此对蛋白活性的影响通常很小,有助于保持生物素化的蛋白与未标记的蛋白保持相同的特性。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]生物素与链霉亲和素[/font][font=Calibri]/[/font][font=宋体]亲和素([/font][font=Calibri]SA[/font][font=宋体])之间的强非共价相互作用,具有高灵敏度和高特异性。义翘神州开发了多种[/font][font=Calibri]Avi-tag[/font][font=宋体]生物素标记的重组蛋白。[/font][/font][font=宋体] [/font][font=宋体]产品优势:[/font][font=宋体][font=宋体]? 高生物活性,经[/font][font=Calibri]ELISA[/font][font=宋体]、[/font][font=Calibri]SPR[/font][font=宋体]、[/font][font=Calibri]BLI[/font][font=宋体]等验证[/font][/font][font=宋体][font=宋体]? 多种属,覆盖细胞治疗、抗体、[/font][font=Calibri]Fc[/font][font=宋体]受体等热门靶点[/font][/font][font=宋体]? 高批间一致性[/font][font=宋体] [/font][font=宋体] [/font][font=宋体]化学标记生物素蛋白:[/font][font=宋体][font=宋体]化学标记法,是将蛋白[/font][font=Calibri]N-[/font][font=宋体]末端游离胺基及内部的赖氨酸侧链上的胺基与生物素分子结合,通常一个蛋白质分子会被标记上多个生物素分子。化学标记法具有灵敏度高、[/font][font=Calibri]tag free[/font][font=宋体]等特点,是常用的生物学方法之一。[/font][/font][font=宋体] [/font][font=宋体]产品优势:[/font][font=宋体]? 高信号强度,每个蛋白分子通常平均含有多个生物素,有助于对其检测。[/font][font=宋体]? 标记方法简单,检测灵敏度高。[/font][font=宋体][font=宋体]? 高生物活性,[/font][font=Calibri]ELISA[/font][font=宋体]、[/font][font=Calibri]SPR[/font][font=宋体]等验证,批间一致性高[/font][/font][font=宋体] [/font][font=宋体]生物素标记蛋白应用:[/font][font=宋体][font=Calibri]1[/font][font=宋体]、用于生物素标记的三种天然产物分子探针的设计与合成研究[/font][/font][font=宋体]从中药中提取分离得到的天然产物具有结构多样、药理作用广泛的特点,常被用来作为先导化合物开发新药,因此需要对其具体作用机制进行研究。天然产物药理作用广泛对应着多靶点的特性,但其靶标蛋白的难以确定也阻碍了人们对其的进一步研究与开发。[/font][font=宋体] [/font][font=宋体][font=宋体]基于亲和性蛋白组学分析方法([/font][font=Calibri]Affinity-based Protein Profiling,ABPP[/font][font=宋体])是基于活性小分子与靶标蛋白之间的亲和作用,在活性小分子上引入报告基团,利用亲和层析技术可以将靶标蛋白进行分离的一种方法,其作为一种十分有效的工具被广泛应用于天然产物靶标蛋白的发现。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]选取三个从中药中提取分离得到的活性天然小分子,设计合成相应的小分子探针,旨在为它们靶标蛋白的发现以及作用机制的研究提供一个有效的工具,具体内容如下:[/font][font=Calibri]1[/font][font=宋体]、对目前主要的用于天然小分子的靶标蛋白鉴定方法进行了介绍,且着重介绍了[/font][font=Calibri]ABPP[/font][font=宋体]方法及其在天然产物靶标蛋白鉴定的应用。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2[/font][font=宋体]、以薯蓣皂苷元和生物素为原料,经过酯化、酰胺化、取代、水解反应等步骤分别合成含有长臂亲脂性链和亲水性链的薯蓣皂苷元生物素标记探针[/font][font=Calibri]3[/font][font=宋体]和[/font][font=Calibri]8,[/font][font=宋体]并以[/font][font=Calibri]MTT[/font][font=宋体]法对其进行抗肿瘤活性评价。实验得到的探针分子、重要中间体用[/font][font=Calibri]MS[/font][font=宋体]、[/font][font=Calibri]1H-NMR[/font][font=宋体]、[/font][font=Calibri]13C-NMR[/font][font=宋体]表征,确认所得化合物结构与目标化合物一致。细胞活性实验结果表明合成的探针分子[/font][font=Calibri]3[/font][font=宋体]和[/font][font=Calibri]8[/font][font=宋体]具有与薯蓣皂苷元相当的抗肿瘤活性,且对探针分子标记的靶标蛋白进行电泳分析,发现了三条薯蓣皂苷元可能特异性作用的蛋白条带,这些结果都为后续薯蓣皂苷元抗肿瘤靶标蛋白的发现奠定基础。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]更多详情可以关注义翘神州[url=https://cn.sinobiological.com/category/biotinylated-protein-elite][b]生物素标记蛋白[/b][/url][/font][font=Calibri]https://cn.sinobiological.com/category/biotinylated-protein-elite[/font][/font]
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=54229]食物中生物素(维生素H)的测定方法[/url]
有没有在做婴幼儿奶粉中生物素、叶酸、VB12的测定的啊,有用试剂盒的吗?用试剂盒做的数据准不准的啊
最近经常做复合维生素片剂中的维生素,其他的维生素还好,用国标的方法都能做出来,就是生物素和维生素B12不太好做,国标中是微生物法,我学化学的,不会做,参考的很多液相测定方法检测限都达不到,大家是怎么做的,有没有用荧光检测器做的
[font=宋体]求助,奶粉中检测项目:亚油酸、烟酸、叶酸、泛酸、生物素、胆碱、肌醇、牛磺酸、左旋肉碱是属于添加剂还是营养强化剂啊[/font]
对照品:用于鉴别、检查、含量测定和校正检定仪器性能的标准物质;对照品由国家药品检定机构审查认可,其标准应不低于制品的质量标准。 标准品:用于生物检定、抗生素或生物药品中含量或效价测定的标准物质,以效价单位(U)表示。 对照品与标准品概念不清?对照品与标准品是2个不同的概念,中国药典凡例中已有明确的定义:对照品系指用于鉴别、检查、含量测定和校正检定仪器性能的标准物质。标准品:用于生物检定、抗生素或生物药品中含量或效价测定的标准物质,以效价单位(U)表示。文献中常将2种概念混淆,认为对照品就是标准品,是1种物质2种提法而已,造成错误的原因,可能是有的药品既有对照品,又有标准品。 例如:当用微生物法测定头孢克罗效价时,用头孢克罗标准品,用HPLC或UV法测定时,则用对照品;非那西丁当用作熔点校准物质时,用熔点标准品,测定含量时,用对照品。即使是同一种物质的标准品和对照品,它们的规格、标定方法以及用途都可能是不同的。
[color=#333333]对照品与标准品概念[/color][color=#333333]对照品与标准品是2个不同的概念,中国药典凡例中已有明确的定义:对照品系指用于鉴别、检查、含量测定和校正检定仪器性能的标准物质,而标准品系指用于生物检定、抗生素或生物药品中含量或效价测定的标准物质,以效价单位(U)表示.文献中常将2种概念混淆,认为对照品就是标准品,是1种物质2种提法而已[1,2],造成错误的原因,可能是有的药品既有对照品,又有标准品.例如,当用微生物法测定头孢克罗效价时,用头孢克罗标准品,用HPLC或UV法测定时,则用对照品;非那西丁当用作熔点校准物质时,用熔点标准品,测定含量时,用对照品.即使是同一种物质的标准品和对照品,它们的规格、标定方法以及用途都可能是不同的.[/color]
在抗生素类的标准物质使用时,经常会遇到标准品和对照品的概念。关于这二者的区别,现在比较流行的说法是在做HPLC时使用的标准物质应为对照品。摘录典型观点如下:[B]“标准品都是按效价单位(或μg)计,以国际标准品进行标定。标准品的标示量是按生物活性来计算的,不是按纯度来标示,此种标示法对单组分或多组分物质均适用,尤适用于多组分物质,如乙酰螺旋霉素标准品,是由4种有效成分组成,若欲于一个纯度来标示其含量是不可能的,但用效价(即生物活性)来标示是可行的;对照品的标示量则必定是某单一组分的纯度指标。所以日常工作中,标准品和对照品在定量时是不可相互替代的。以罗红霉素为例,现今是国家标准品与对照品并存,以抗生素微生物检定法测其含量时,必须使用罗红霉素标准品;但以HPLC法测定其含量时,又必须使用罗红霉素对照品,不可混淆。”[/B]但是我见过一些行业标准,比方说HPLC测土霉素残留中,在说到标准液的配制时,写得就是“土霉素标准品”。难道这里面的“标准品”是“对照品”的错误用法?[em0716] 请大家发表一下看法

随着多肽在生物医药领域越来越广泛和深入的应用,标记和修饰性的多肽种类的需求越来越多,质量需求也越来越高。稳定同位素标记就是其中典型的一种。稳定同位素标记示踪,可以实现肽类代谢途径研究,能够随时追踪含有同位素标记的多肽在体内或体外位置及数量的变化情况。同位素标记具有高灵敏度、定位简单、定量准确等优点,使得同位素修饰在医学及生物化学领域得到越来越广泛的关注。目前我们公司合成的同位素标记多肽主要为C13,N15两种同位素标记的多肽,通过直接在肽链中引入同位素标记的氨基酸达到有效标记整条肽链的目的,常用的同位素标记的氨基酸有Tyr,Thr,Lys,Arg,Glu等。同位素标记的多肽与普通肽的区别在于其结构中某一个或几个氨基酸中的C被C13取代或者N被N15取代。[align=center][img=,422,228]https://ng1.17img.cn/bbsfiles/images/2019/01/201901151433525331_7755_3531468_3.jpg!w422x228.jpg[/img][/align]专业的团队,一流的合成纯化技术,严谨的工作态度,严格的质量要求,是我们能够满足客户对同位素标记多肽的不同纯度要求的重要保障。与此同时,同位素标记多肽的原料(同位素标记的氨基酸)价格昂贵,使得我们合成成本高,这就直接导致了这种多肽价格的高昂,秉着客户至上,竭力满足客户需求的经营理念,我们国肽生物提供微克,毫克到千克级别的质量服务。成功案例:序列WVQTLSEQVQEELLSSQVTQELHPLC分析:[align=center][img=,562,236]https://ng1.17img.cn/bbsfiles/images/2019/01/201901151434210520_3873_3531468_3.jpg!w562x236.jpg[/img][/align]MS分析:[align=center][img=,562,256]https://ng1.17img.cn/bbsfiles/images/2019/01/201901151434419961_6047_3531468_3.jpg!w562x256.jpg[/img][/align]合肥国肽生物官网:http://www.bankpeptide.com[img=,690,163]https://ng1.17img.cn/bbsfiles/images/2019/01/201901151435146731_1710_3531468_3.jpg!w690x163.jpg[/img]
[align=center][font=DengXian]维生素的生物可利用性[/font][/align]1 [font=DengXian]维生素生物可利用性的含义[/font][font=DengXian]维生素的生物可利用性([/font]Bioavailabilityof vitamin[font=DengXian])是指人体摄入的维生素经肠道吸收并在体内被利用的程度。包含两方面含义即吸收与利用。因此,在评价维生素营养完全性时除考虑摄入的食品中维生素的含量和不同化学结构的鉴定外,更重要的应考虑摄入食品中维生素的生物可利用性。[/font]2 [font=DengXian]影响维生素生物可利用性的因素[/font]1[font=DengXian]、消费者本身的年龄、健康以及生理状况等;[/font]2[font=DengXian]、膳食的组成影响维生素在肠道内运输的时间、黏度、[/font]pH[font=DengXian]及乳化特性等;[/font]3[font=DengXian]、同一种维生素构型不同对其在体内的吸收速率、吸收程度、能否转变成活性形式以及生理作用的大小产生影响;[/font]4[font=DengXian]、维生素与其他的组分的反应如维生素与蛋白质、淀粉、膳食纤维、脂肪等发生反应均会影响到其在体内的吸收与利用;[/font]5[font=DengXian]、维生素的拮抗物也影响维生素的活性,从而降低维生素的生物可利用性。例如,硫胺素酶可切断硫胺素代谢分子,使其丧失活性;抗生物素蛋白与代谢物结合,使生物素失去活性;双香豆素具有与维生素[/font]K[font=DengXian]相似的结构,可占据维生素[/font]K[font=DengXian]代谢物的作用位点而降低维生素[/font]K[font=DengXian]的生物可利用性;[/font]6[font=DengXian]、食品加工和贮存也影响到维生素的生物可利用性。[/font]
食品微生物检测实验室必须要有单独的阳性对照室吗?检测项目:菌落总数、大肠、霉菌和酵母菌。
[font=&][color=#333333]对照品系指用于鉴别、检查、含量测定和校正检定仪器性能的标准物质。[/color][/font][font=&][color=#333333]标准品系指用于生物检定、抗生素或生物药品中含量或效价测定的标准物质,以效价单λ(U)表示。[/color][/font][font=&][color=#333333]如果还是感觉不甚明了,是否标准品只用于生物方面?是否化学方面只能称对照品?标准品有什?要求?对照品有什?要求?[/color][/font][font=&][color=#333333]国家药品标准品、对照品系指国家药品标准中用于鉴别、检查、含量测定、杂质和有关物质检查等标准物质,它是国家药品标准不可分割的组成部分。国家药品标准物质是国家药品标准的物质基础,它是测量药品质量的基准;也是做为校正测试仪器与方法的物质标准;在药品检验中,它是确定药品真α优劣的对照,是控制药品质量必不可少的工具。[/color][/font][font=&][color=#333333]目前,中国药品生物制品检定所已能提供各类国家标准物质1242种,其中中药化学对照品288种,对照药材400种,两者占总数的一半以上。[/color][/font][font=&][color=#333333]国家标准品及生物参考品系指用于鉴别、检查含量或效价测定的标准物质,其制备与标定应符合“生物制品国家标准物质制备和标定规程”要求,并由国务院药品监督管理部门指定的机构分发。企业工作标准品或参考品必须经国家标准品或参考品标化后方能使用。[/color][/font][font=&][color=#333333]对照品系指用于生物制品理化等方面测定的特定物质,由生产单λ采用与制品生产工艺相同的方法制备。对照品应尽可能与制品原液配方一致,稳定性较差的,可加不含对测定有干扰物质的适宜的稳定剂。对照品由国家药品检定机构审查认可,其标准应不低于制品的质量标准。[/color][/font][font=&][color=#333333]标准品、对照品:是指用于鉴别、检查、含量测定的标准物质,均由国务院药品监督管理部门指定的单λ制备、标定和供应。标准品系指用于生物测定、抗生素或生化药品中含量或效价测定的标准物质,一国际标准品进行标定;对照品出另有规定外,按干燥进行计算后使用。[/color][/font][font=&][color=#333333]标准品和对照品均附有使用说明书,质量要求,有效期和装量等。[/color][/font][font=&][color=#333333]生物制品标准物质系指用于生物制品效价、活性或含量测定的或其特性鉴别、检查的生物标准品或生物参考物质。[/color][/font]转自:食品伙伴网