分享一个检测标准,GB29681-2013 《食品安全国家标准 牛奶中左旋咪唑残留量的测定 高效液相色谱法》 。本标准适用于牛奶中左旋咪唑残留量检测,检测限为2.5μg/kg,定量限为5μg/kg。
欧盟建议修改杀菌剂咪唑菌酮的最大残留限量2010年10月18日,欧盟建议修改杀菌剂咪唑菌酮(fenamidone)在荷兰芹中的最大残留量限量标准,由0.02 mg/kg(定量限)修改为2mg/kg。
毕业在即,毕业论文中涉及2-丙基苯并咪唑的红外标准图谱图,望各位朋友帮帮忙了!本人将万分感谢!如果哪位朋友能找到,请发到我的邮箱,piao23luo◎163.com,谢谢拉!
本人最近在开发硝基咪唑的方法,主要是甲硝唑、二甲硝唑及其他们的代谢产物。但是不管自己优化,还是照搬标准中的参数,四种物质的响应都不好。尤其是两种代谢产物,5ppb才勉强到5*10的四次方,而空白都有接近4次方,标准品是用1:9的甲醇-甲酸水配的,流动相是甲醇-甲酸水,机器是thermo的TSQ,公司要求最低要做到0.05ppb,希望大家能给我点意见。
GB 29681-2013 食品安全国家标准 牛奶中左旋咪唑残留量的测定 高效液相色谱法
有谁做过咪唑烷基脲的检测吗?有方法吗?急求! 化妆品中咪唑烷基脲检测方法征求意见稿里的方法可用吗
请教大家我用国标方法做4-甲基咪唑,回收率只有20%是什么原因?我的过程是:取15mL5mg/L的4-甲基咪唑标准品,加1mol/L的碳酸钠5mL, 混匀,加入20mL80:20的三氯甲烷和乙醇混合物,摇荡提取,弃去水层,再用20mL50mM的甲烷磺酸液提取,过滤上机,可是为什么回收率这么差呢?
使用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]技术测硝基咪唑及其代谢物 使用内标法 在做液相优化的时候标准品和内标物的峰没有办法分开 内标物和标准品的需要完全分开吗
默克密理博应用实验室 2013-07-15近日,百事可乐的产品在美国10个州中被爆出4-甲基咪唑(4-Methylimidazole)严重超标。4-甲基咪唑是一种有机中间体,主要用于合成大宗胃药西咪替丁,也可用作环氧树脂固化剂和金属表面防护剂等。可乐中的4-甲基咪唑是在以亚硫酸铵为原料生产焦糖色素时产生的。 4-甲基咪唑白色至类白色结晶粉末,易溶于水和乙醇,有腐蚀性,是一种能诱发肿瘤的化学物质。http://blog.merckmilliporechina.com/editor/upload/image/4C619C0F_7B615A74.PNG默克密理博致力于分析方法的开发,为客户提供简便、快速的解决方案。4-甲基咪唑及其异构体2-甲基咪唑均有较强极性,适合使用默克密理博的两性离子型亲水作用色谱柱(ZIC®-HILIC)分离。本实验采用默克密理博两性离子型(ZIC®-HILIC)色谱柱直接分析甲基咪唑的液相色谱方法。该方法前处理简单,不需要衍生化,也不需要添加离子对试剂。1 材料试剂1.1 对照品:4-甲基咪唑,2-甲基咪唑。1.2 色谱柱:ZIC®-HILIC 250-4.6mm 5um 200Å(默克密理博,货号:1.50458.0001)1.3 乙腈(默克密理博,货号:1.00030.4008)1.4 甲醇(默克密理博,货号:1.06007.4008)1.5 磷酸二氢钾(默克密理博,货号:1.04873.1000)1.6 可口可乐及百事可乐样品1.7 实验用为为超纯水(默克密理博Milli-Q Advantage)1.8 PVDF0.22um针头过滤器(默克密理博,货号:SLGV033NB)1.9 标准溶液配制:使用70%乙腈溶液,分别配制1mg/ml的4-甲基咪唑,2-甲基咪唑对照品原液。取两个对照品原液,1:1混合、稀释、定容,成,得100ug/ml的混合对照品母液。混合母液用70%乙腈溶液配制浓度为0.
2013年10月16日,农业部网站发布消息称,《牛奶中左旋咪唑残留量的测定 高效液相色谱法》等29项标准业经食品安全国家标准审评委员会审定通过。并经农业部、卫生和计划生育委员会审查批准,发布为中华人民共和国食品安全国家标准,自2014年1月1日起实施。 迪马科技在国标基础上对牛奶中左旋咪唑残留量的测定方法进行了优化,取得了优异的回收率结果和重现性,下面为详细解决方案,与大家分享
GB/T29667-2013化妆品用防腐剂 咪唑烷基脲
美国一家机构检测可口可乐,发现含有致癌物质4-甲基咪唑(简称:4-MEI),这种与啮齿动物患肺癌有关的化学物质被曝出现在可乐配方焦糖色素中。 因为涉及到饮料业巨头,此事一经曝光,引起广泛关注。 我国的“中国饮料工业协会”也发表声明,表明立场,全文如下: 为提高饮料产品的食品安全性、及时与企业、媒体及消费者保持沟通,我协会一直高度关注“焦糖色中4甲基咪唑”的有关动态,就目前我协会掌握和了解的情况,我国饮料中所含的焦糖色不会致癌,可安全饮用。具体说明如下: 1、无论国外还是国内,焦糖色被允许用于饮料等食品。在我国焦糖色被GB2760《食品安全国家标准 食品添加剂使用标准》和国家标准GB8817《食品添加剂焦糖色》双重管理。在GB2760《食品安全国家标准 食品添加剂使用标准》中,焦糖色可以使用于包括饮料在内的十几种食品中。 2、因工艺的不同,在焦糖色生产过程中可能会产生微量的4-MEI。该成分是在焦糖等食品的加热、烘烤和烹饪过程中形成的。在世界范围内,含有焦糖色的众多食品和饮料中都可能有微量的4-MEI。 3、国际公共健康组织,如欧洲食品安全委员会(EFSA)、加拿大卫生部等,已经证实焦糖色以及包含的微量4-MEI,对包括可乐在内的饮料和食品是安全的。 4、中国饮料工业协会相信饮料企业在严格执行GB2760《食品安全国家标准 食品添加剂使用标准》和GB8817《食品添加剂 焦糖色》、确保饮料质量合规及消费安全的同时,将积极引进国内外的先进技术、提高技术水平。 中国饮料工业协会 2013年8月9日看来焦糖色素中含有4-MEI,是肯定的,但是很微量。一些本来无毒的物质,在加热,烘烤等处理后,也可能会产生对人体有害的物质。这个应该是无法避免的。
请问食品中4-甲基咪唑用GCMS怎样做?
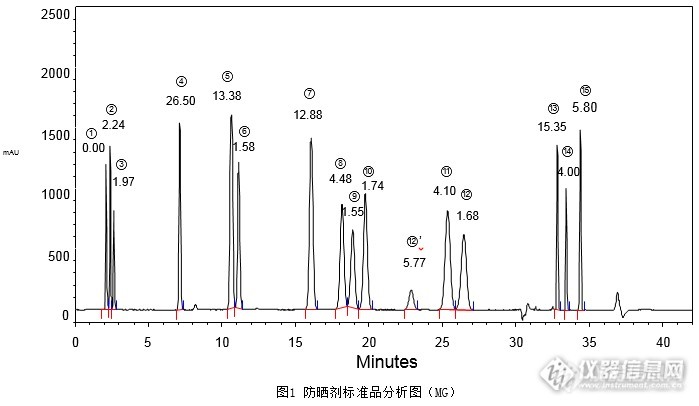
[align=center][b]2015版《化妆品安全技术规范》防晒剂检验方法[/b][/align][align=center][b]苯基苯并咪唑磺酸等15种组分-二元梯度法[/b][/align][align=center][b] [/b][/align]在2015版《化妆品安全技术规范》防晒剂检验方法中,第一法对15种防晒剂的分析为三元梯度方法,此法要求仪器配备三元泵,且四氢呋喃会对PEEK基材的管路和仪器有溶胀作用,所以该方法在实际操作上会受到一定的限制;而第二法将15种防晒剂分为两组,在不同流动相条件下分别检测,较为费时费力,且前12种防晒剂峰未能达到基线分离。基于以上情况,本次实验采用二元梯度方法,对15种防晒剂标准品进行同时分析,既可在常规二元泵系统进行实验,也可免去分组分析的繁琐。本实验混合标准溶液按照《化妆品安全技术规范》配制,分别使用资生堂CAPCELLPAK C[sub]18[/sub] MG S5 4.6 mm i.d. × 250 mm和CAPCELL PAK C[sub]18[/sub] MGII S5 4.6 mm i.d.× 250 mm色谱柱进行分析,结果如图1和图2所示,两款色谱柱在二元梯度条件下均可使15种防晒剂峰实现基线分离。[img=,690,400]http://ng1.17img.cn/bbsfiles/images/2017/08/201708230913_01_2222981_3.png[/img][img=,690,366]http://ng1.17img.cn/bbsfiles/images/2017/08/201708230913_02_2222981_3.png[/img]1:苯基苯并咪唑磺酸; 2:二苯酮-4和二苯酮-5; 3:对氨基苯甲酸; 4:二苯酮-3; 5:对甲氧基肉桂酸异戊酯6:4-甲基苄亚基樟脑; 7:PABA乙基己酯; 8:丁基甲氧基二苯甲酰基甲烷; 9:奥克立林;10:甲氧基肉桂酸乙基己酯; 12’:峰12的同分异构体; 11:水杨酸乙基己酯; 12:胡莫柳酯;13:乙基己基三嗪酮; 14:亚甲基双-苯并三唑基四甲基丁基酚; 15:双-乙基己氧苯酚甲氧苯基三嗪(按出峰顺序)[img=,629,207]http://ng1.17img.cn/bbsfiles/images/2017/08/201708230913_03_2222981_3.png[/img]
焦糖色中4-甲基咪唑的测定是采用薄层色谱法,可是最近我在测定样品时,根据标准方法进行操作,却没有标准样品点却没有显色。不知道哪位同仁做过这个检测,烦请帮忙!
最近要开展测烤鳗中甲苯咪唑残留的检测,请问有国标法或是SN法吗?我的Email:capinter@163.com,谁手头有能发一份给我吗?,先谢过了~~~
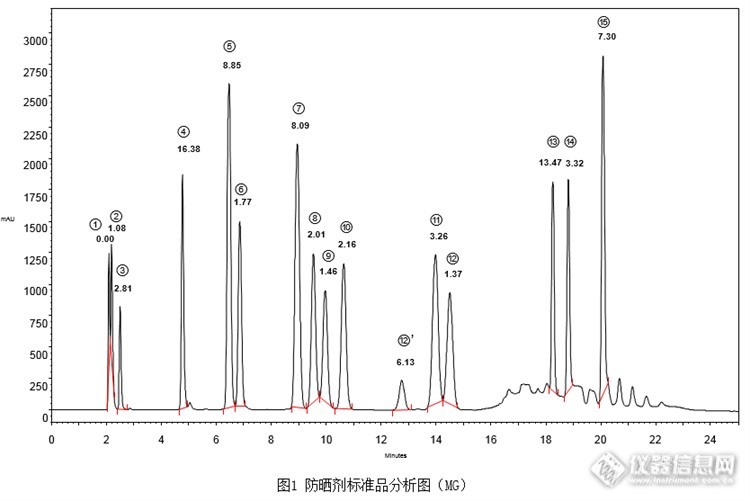
[align=center][b]2015版《化妆品安全技术规范》防晒剂检验方法-苯基苯并咪唑磺酸等15种组分[/b][/align][align=center][b]第一法(高效液相色谱-二极管阵列检测器法)[/b][/align]本次实验按照2015版《化妆品安全技术规范》中防晒剂检验方法的第一法(高效液相色谱-二极管阵列检测器法),对苯基苯并咪唑磺酸等15种防晒剂进行同时分析。15种防晒剂标准品按照《化妆品安全技术规范》配制成混合标准溶液,分别使用CAPCELL PAK C18 MG S5 4.6 mm i.d. × 250 mm,CAPCELL PAK C18 MGII S5 4.6 mm i.d. × 250 mm,CAPCELL PAK ADME S5 4.6 mm i.d. ×250 mm,CAPCELL PAK C18 AQ S5 4.6 mm i.d. × 250 mm以及SUPERIOREX ODS S5 4.6 mm i.d. × 250 mm五款色谱柱对混合标准溶液进行分析。其中,MG和MGII色谱柱得到相对较好结果,但两款色谱柱原流动相条件下,个别峰未实现基线分离。结果如图1、图2。[img=,690,460]http://ng1.17img.cn/bbsfiles/images/2017/08/201708170930_01_2222981_3.png[/img][img=,690,432]http://ng1.17img.cn/bbsfiles/images/2017/08/201708170930_02_2222981_3.png[/img]1:苯基苯并咪唑磺酸; 2:二苯酮-4和二苯酮-5; 3:对氨基苯甲酸; 4:二苯酮-3; 5:对甲氧基肉桂酸异戊酯6:4-甲基苄亚基樟脑; 7:PABA乙基己酯; 8:丁基甲氧基二苯甲酰基甲烷; 9:奥克立林;10:甲氧基肉桂酸乙基己酯; 12’:峰12的同分异构体; 11:水杨酸乙基己酯; 12:胡莫柳酯;13:乙基己基三嗪酮; 14:亚甲基双-苯并三唑基四甲基丁基酚; 15:双-乙基己氧苯酚甲氧苯基三嗪(按出峰顺序)[img=,690,304]http://ng1.17img.cn/bbsfiles/images/2017/08/201708170930_03_2222981_3.png[/img]为得到更好的分离效果,使用1支更新的MGII色谱柱,在原流动相条件基础上,对梯度进行调整,结果如图3所示。各峰分离度得到明显改善,但峰11和峰12分离度为1.43,仍未达到基线分离。[img=,690,425]http://ng1.17img.cn/bbsfiles/images/2017/08/201708170933_01_2222981_3.png[/img]1:苯基苯并咪唑磺酸; 2:二苯酮-4和二苯酮-5; 3:对氨基苯甲酸; 4:二苯酮-3; 5:对甲氧基肉桂酸异戊酯6:4-甲基苄亚基樟脑; 7:PABA乙基己酯; 8:丁基甲氧基二苯甲酰基甲烷; 9:奥克立林;10:甲氧基肉桂酸乙基己酯; 12’:峰12的同分异构体; 11:水杨酸乙基己酯; 12:胡莫柳酯;13:乙基己基三嗪酮; 14:亚甲基双-苯并三唑基四甲基丁基酚; 15:双-乙基己氧苯酚甲氧苯基三嗪(按出峰顺序)[img=,690,292]http://ng1.17img.cn/bbsfiles/images/2017/08/201708170933_02_2222981_3.png[/img]继续调整梯度条件,分析结果如4所示。在此条件下,各峰实现基线分离,得到良好分析结果。[img=,690,421]http://ng1.17img.cn/bbsfiles/images/2017/08/201708170935_01_2222981_3.png[/img]1:苯基苯并咪唑磺酸; 2:二苯酮-4和二苯酮-5; 3:对氨基苯甲酸; 4:二苯酮-3; 5:对甲氧基肉桂酸异戊酯6:4-甲基苄亚基樟脑; 7:PABA乙基己酯; 8:丁基甲氧基二苯甲酰基甲烷; 9:奥克立林;10:甲氧基肉桂酸乙基己酯; 12’:峰12的同分异构体; 11:水杨酸乙基己酯; 12:胡莫柳酯;13:乙基己基三嗪酮; 14:亚甲基双-苯并三唑基四甲基丁基酚; 15:双-乙基己氧苯酚甲氧苯基三嗪(按出峰顺序)[img=,690,307]http://ng1.17img.cn/bbsfiles/images/2017/08/201708170937_01_2222981_3.png[/img]接下来将色谱柱更换为MG色谱柱,在调整后的梯度条件下进行分析,结果如图5所示,同样可得到良好的分析结果。[img=,690,419]http://ng1.17img.cn/bbsfiles/images/2017/08/201708170938_01_2222981_3.png[/img]1:苯基苯并咪唑磺酸; 2:二苯酮-4和二苯酮-5; 3:对氨基苯甲酸; 4:二苯酮-3; 5:对甲氧基肉桂酸异戊酯6:4-甲基苄亚基樟脑; 7:PABA乙基己酯; 8:丁基甲氧基二苯甲酰基甲烷; 9:奥克立林;10:甲氧基肉桂酸乙基己酯; 12’:峰12的同分异构体; 11:水杨酸乙基己酯; 12:胡莫柳酯;13:乙基己基三嗪酮; 14:亚甲基双-苯并三唑基四甲基丁基酚; 15:双-乙基己氧苯酚甲氧苯基三嗪(按出峰顺序)[img=,690,291]http://ng1.17img.cn/bbsfiles/images/2017/08/201708170940_01_2222981_3.png[/img]
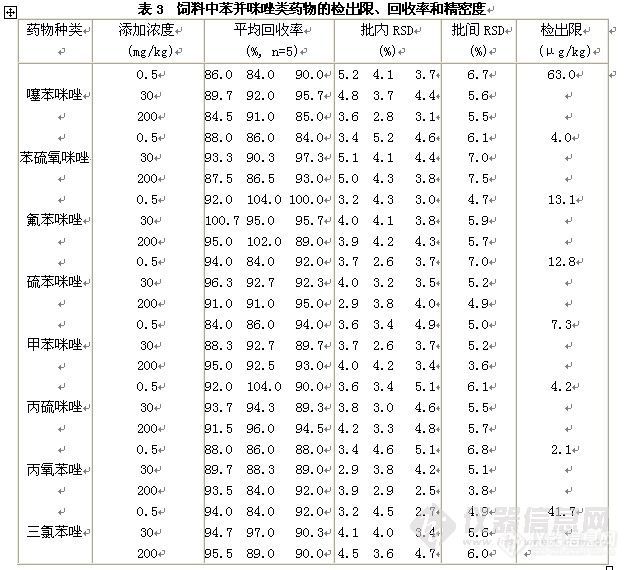
液相色谱串联质谱法测定饲料中8种苯并咪唑类药物摘 要 建立了同时测定饲料中8种苯并咪唑类药物(噻苯咪唑、丙硫咪唑、硫苯咪唑、苯硫氧咪唑、氟苯咪唑、甲苯咪唑、丙氧苯唑和三氯苯唑)的液相色谱串联质谱分析方法。饲料样品直接用酸化乙腈提取,提取液用甲酸溶液稀释后直接进行分析。分析时采用XBridgeTM C18色谱柱,以甲酸溶液-乙腈体系进行梯度洗脱,MRM方式测定,基质外标法定量。苯并咪唑类药物在0.02~10 mg L-1浓度范围内呈良好的线性,线性相关系数均大于0.990,苯并咪唑类药物在饲料样品中最低检测限为2.1~63.0μg/kg。饲料中苯并咪唑类药物在0.50~200 mg/L范围内的回收率为84.0%~104%之间,相对标准偏差(RSD)均小于10%。 关键词 苯并咪唑类药物;液相色谱串联质谱法;饲料 苯并咪唑类药物(benzimidazoles, BMZs)属于广谱、高效、低毒抗蠕虫药,由于对胃肠线虫具有很强的驱杀作用,至今仍在广泛使用。但由于BMZs在实验动物和靶动物显示致畸和致突变作用,目前使用的BMZs多数是食品残留中重要的监控对象,且BMZs在体内转化的代谢产物仍具有毒理作用,所以我国以及联合国粮农组织、欧盟、美国、日本等国家和组织都将苯并咪唑类药物列入限制使用的兽药药物,并制订出各种苯并咪唑类药物在不同动物体内(肌肉、组织、奶等)的最高残留限量。饲料安全直接关系到动物性食品的安全,考虑到苯并咪唑类药物经常被添加到饲料中使用,故很有必要进行饲料中苯并咪唑类药物的分析研究。 目前对于动物组织中苯并咪唑类药物的分析方法较多,而饲料中苯并咪唑类药物分析方法国内未见发表,国外也较少,涉及的种类也较少,最多的仅有5种药物。动物组织和饲料中BMZs分析涉及的主要分析手段有:酶联免疫吸附法( ELISA) 、气相色谱-质谱法(GC-MS)、高效液相色谱法(HPLC)及高效液相色谱串联质谱法(HPLC-MS/MS),高效毛细管电泳法(HPCE)。考虑到苯并咪唑类药物在我国使用情况,本研究选择了8种常用苯并咪唑类药物,考虑到LC-MS/MS法灵敏度高的特点,样品酸化乙腈提取后直接稀释后进行液相色谱串联质谱分析。1 材料与方法1.1 仪器与试剂 Waters 2695 Quattro MicroTM API高效液相色谱串联质谱仪(美国Waters公司),配置电喷雾离子源;固相萃取仪(美国Supelco 公司);Sigma离心机。噻苯咪唑和丙硫咪唑标准品(Accustandard 公司);硫苯咪唑、苯硫氧咪唑、氟苯咪唑、甲苯咪唑、丙氧苯唑和三氯苯唑标准品(Dr. Ehrenstorfer)。乙腈、二甲亚砜和甲酸为色谱纯(Fisher公司)。1.2 仪器条件 XBridgeTM C18色谱柱(150 mm×2.1 mm,内径3.5 μm);流动相A为0.1%甲酸溶液,B相为乙腈,梯度洗脱条件:B相在1.0 min内从15%线性增加到25%,再在2.5 min内线性增加到95%,保持3.5 min,然后在0.1 min内降至15%,保持4.9 min;流速:0.3 mL/min;进样量:10 µL;柱温:30℃。 质谱条件:ESI源正离子模式电离;多反应监测(MRM);毛细管电压:3.0 KV;萃取锥孔电压:20 V;RF透镜电压:0.5 V;离子源温度:110 ℃;脱溶剂气温度:350 ℃;锥孔气流速:50 L/h;脱溶剂气流速:600 L/h;倍增器电压:650 V;二级碰撞气:氩气;其它条件详见表1。http://ng1.17img.cn/bbsfiles/images/2010/11/201011301506_262957_1759541_3.jpg1.3 样品处理 称取2g试样(精确到0.01g)于50 mL离心管中,加入20 mL0.5 %甲酸乙腈,涡旋1 min,然后超声提取10 min,以5000 r/min的速度离心5 min后吸取1.0 mL上清液于5 mL刻度试管中,加入3 mL0.1 %甲酸溶液于试管中,混匀后过0.22 μm滤膜,进行液相色谱串联质谱分析。1.4 线性实验 准确称取各10.0 mg BMZs标准品于相应的10mL容量瓶中,噻苯咪唑、甲苯咪唑、丙氧苯唑和丙硫咪唑用二甲亚砜溶解并定容至刻度,其余4种BMZs用甲醇:二甲亚砜(2:3 v/v)溶解并定容至刻度,即得均为1000 mg/L标准储备液。分别吸取1.0 mL各标准储备液于同一10mL容量瓶中,用甲醇稀释至刻度,即得100 mg/L的混合标准工作液。分别准确移取苯并咪唑类药物混合标准中间液适量,配制浓度为0.2.、0.8、2.0、10.0、40.0和100.0 mg/L的系列标准溶液,吸取0.1 mL于5 mL刻度试管中,再吸取空白试料提取液0.9 mL于该5 mL刻度试管中,加入3 mL0.1%甲酸溶液后混匀过膜,进行上机测定,以定量离子对峰面积为纵坐标,标准溶液浓度为横坐标,绘制基质校准标准曲线。2 结果与分析2.1 液相色谱质谱分析 苯并咪唑类药物色谱分析时,通常采用反相分离体系,主要有三类流动相体系:离子增强体系,pH2~3,一般使用乙腈-磷酸或磷酸盐体系;离子抑制流动相体系,pH5~7;离子对流动相体系,离子增强流动相中加入阴离子对试剂。对于多组分苯并咪唑类药物液相色谱质谱分析时,通常采用离子增强体系进行梯度洗脱,如0.1%甲酸溶液-乙腈体系,因为该体系和纯水-乙腈体系相比色谱峰的拖尾现象得到了明显改善。 苯并咪唑类药物属弱碱性物质,中等极性,在酸性条件下很容易质子化,于是本方法选择ESI+进行分析。以乙腈/0.1%甲酸溶液(3:7,v/v)为溶解液,用蠕动泵(20μL/min)对苯并咪唑类药物的质谱条件进行优化。经过优化的条件为:毛细管电压:3.0KV;离子源温度:110℃;脱溶剂气温度:350℃;锥孔气流速:50L/h;脱溶剂气流速:600L/h。其它条件详见表1。2.2 提取净化方法的选择和优化 [font=宋体
如题,我按照国标GB/T 22994-2008做左旋咪唑。发现问题如下1、换了两个样品都发现含有少量待测物,含量范围在0.1~2.0ppb。左旋是否普遍存在于奶制品中?那我方法检测限应该怎么做呢?2、样品空白加标回收效果还好,但样品加标回收率很低,是否表示基质对目标物的离子化有影响?
本公司天然食用香料产品被检出含有咪唑,大概几个PPM,对方单位用的是极性柱子HP-Innowax,全扫加离子选择,内标法。现在我方只有HP-5MS,没有标样,全扫描未发现咪唑,全扫描出不来,离子选择能出的来吗?请问老师,是否是柱子的问题,或是方法的问题?还有谁知道咪唑是什么东西,怎么会跑到香料中了,本产品纯天然提取,未添加任何禁用物,查了资料,似乎是胶水固化剂类的东西,有没有可能是从包装桶中进入到产品中?
跪求EN 14333.1-2004无脂食品.苯并咪唑杀菌剂carbendazim、噻唑苯并咪唑和苯菌灵的测定方法,中文英文的都行,E-mail:grant_su@sina.com
求助各位大神 现在化妆品咪唑烷基脲用什么方法定量检测,2010年的化妆品中咪唑烷基脲的检测方法 征求意见稿中的方法能用吗
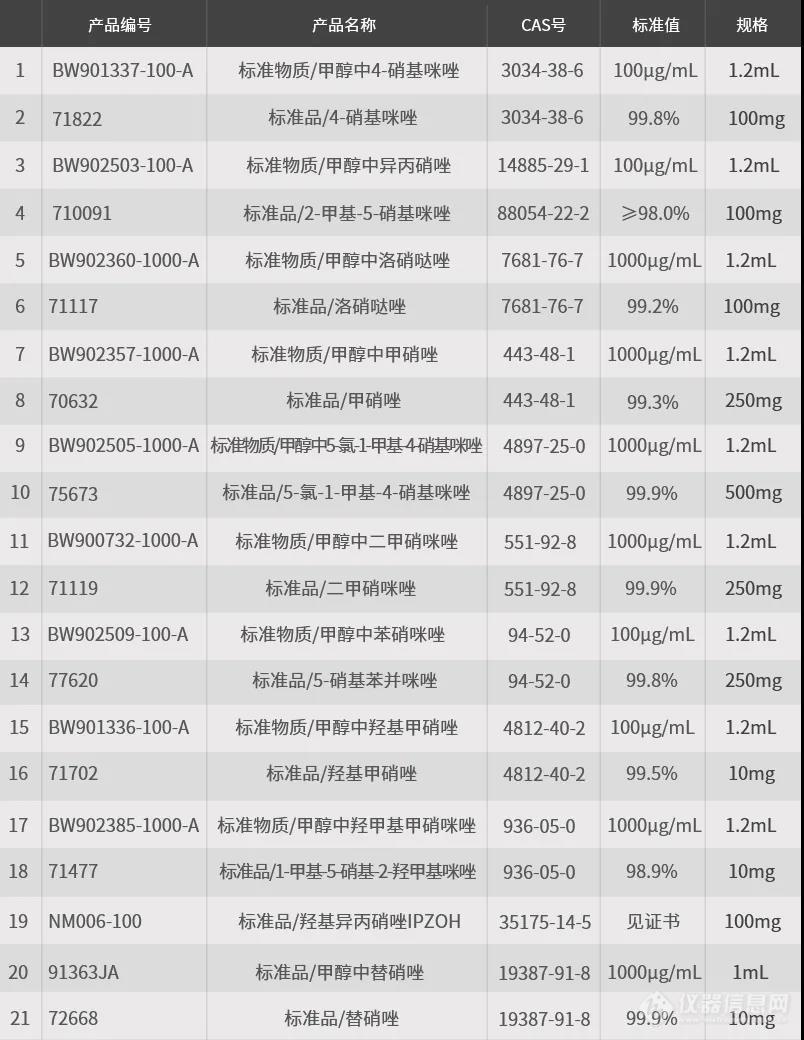
[b][font=宋体]硝基咪唑的危害及检测目的[/font][/b][font=Calibri][font=宋体]硝基咪唑类药物[/font][/font][font=宋体]([/font][font='Times New Roman']nitroimidazole,NMZs[/font][font=宋体])[/font][font=Calibri][font=宋体]是一类具有抗原虫感染和抗厌氧菌的硝基杂环类抗菌药物[/font][/font][font=宋体],[/font][font=Calibri][font=宋体]其具有抗菌和抗原虫作用[/font][/font][font=宋体]。[/font][font=Calibri][font=宋体]近年来作为饲料添加剂广泛应用于畜牧业生产中[/font][/font][font=宋体],[/font][font=Calibri][font=宋体]同时也是一种生长促进剂[/font][/font][font=宋体],[/font][font=Calibri][font=宋体]以促进畜禽的生长及改善饲料[/font][/font][font=宋体]的[/font][font=Calibri][font=宋体]转换率[/font][/font][font=宋体]。[/font][font=Calibri][font=宋体]由于这类化合物含有的硝基杂环类[/font][/font][font=宋体]物质[/font][font=Calibri][font=宋体]具有潜在致癌、致畸和致突变作用[/font][/font][font=宋体],[/font][font=Calibri][font=宋体]因此欧美等发达国家已禁止在食源性动物中使用硝基咪唑类药物[/font][/font][font=宋体]。[/font][font=Calibri][font=宋体]我国也对硝基咪唑类药物进行了严格的限制[/font][/font][font=宋体],[/font][font='Times New Roman']2020[/font][font=宋体]年[/font][font=Calibri][font=宋体]生效实施的[/font][/font][font='Times New Roman']GB 31650-2019[/font][font=Calibri][font=宋体]《食品安全国家标准[/font][/font][font=宋体] [/font][font=Calibri][font=宋体]食品中兽药最大残留限量》中仅规定了甲硝唑和地美硝唑[/font][/font][font=宋体]两[/font][font=Calibri][font=宋体]种物质允许作治疗[/font][/font][font=宋体]使[/font][font=Calibri][font=宋体]用[/font][/font][font=宋体],[/font][font=Calibri][font=宋体]但不得在动物性食品中检出[/font][/font][font=宋体];同年[/font][font=Calibri][font=宋体]农业[/font][/font][font=宋体]农村[/font][font=Calibri][font=宋体]部[/font][/font][font=宋体]公告第[/font][font=宋体]250[/font][font=宋体]号,[/font][font=Calibri][font=宋体]将[/font][/font][font=宋体]洛硝达唑、替硝唑[/font][font=Calibri][font=宋体]列入《食品动物中禁止使用的药品及其他化合物清单》中[/font][/font][font=宋体]。[/font][font=宋体]本文阐述了如何将[/font][font=宋体]硝基咪唑类化合物[/font][font=宋体]从样品基质中分离提取出来,并经过净化后,转化成[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用仪[/color][/url]可以检测的形式。以提取、净化为重点,依据国标[/font][font=宋体]GB/T 21318-2007[/font][font=宋体],为检测人员和相关领域研究人员提供一定的参考。[/font][b][font=宋体]检测项目:[/font][/b][font=宋体]硝基咪唑类原药及代谢产物[/font][b][font=宋体]应用范围:[/font][/b][font=宋体][font=宋体]猪肉[/font]/[font=宋体]鸡肉[/font][font=Calibri]/[/font][font=宋体]牛肉[/font][font=Calibri]/[/font][font=宋体]猪肝[/font][font=Calibri]/[/font][font=宋体]鸡肝[/font][font=Calibri]/[/font][font=宋体]牛肝[/font][font=Calibri]/[/font][font=宋体]猪肾[/font][font=Calibri]/[/font][font=宋体]牛肾[/font][font=Calibri]/[/font][font=宋体]鱼肉[/font][font=Calibri]/[/font][font=宋体]奶粉[/font][font=Calibri]/[/font][font=宋体]蜂蜜[/font][/font][b][b][font=宋体][font=宋体]液相色谱[/font]-质谱/质谱法[/font][font=宋体]方法原理:[/font][/b][font=宋体]样品中残留的[/font][font=宋体]8[/font][font=宋体]种硝基咪唑、[/font][font=宋体]2[/font][font=宋体][font=宋体]种代谢物用甲醇[/font]-[font=宋体]丙酮均质或超声波提取,经乙酸乙酯液液分配,以凝胶色谱([/font][/font][font=宋体]GPC[/font][font=宋体])净化,再经固相萃取([/font][font=宋体]SPE[/font][font=宋体][font=宋体])净化,采用液相色谱[/font]/[font=宋体]串联质谱确证,外标法定量测定。[/font][/font][font=宋体]前处理仪器:[/font][/b][font=宋体]凝胶色谱仪(配有馏份收集浓缩器);组织捣碎机;均质器;超声波发生器;旋转蒸发器;高速[/font][font=宋体]离心机;[/font][font=宋体]氮吹仪;固相萃取装置;具塞锥形瓶([/font][font='Times New Roman']250 mL[/font][font=宋体]);分液漏斗([/font][font='Times New Roman']250 mL[/font][font=宋体]);浓缩瓶([/font][font='Times New Roman']50 mL[/font][font=宋体]、[/font][font='Times New Roman']250 mL[/font][font=宋体])。[/font][b][font=宋体]检测仪器:[/font][font='Times New Roman'][url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS+ESI[/font][font=宋体]源[/font][font=Calibri] [/font][font=Calibri] [/font][font=Calibri] [/font][font=宋体]前处理方法[/font][font='Times New Roman']1.[/font][font=宋体]提取[/font][font=宋体]肌肉组织、脏器组织样品及水产品[/font][/b][font=宋体]准确称取约[/font][font=宋体]20 g[font=宋体]样品(精确至[/font][font=Times New Roman]0.1 g[/font][font=宋体])[/font][/font][font=宋体]于[/font][font='Times New Roman']250 mL[/font][font=宋体]具塞锥形瓶中,加入[/font][font=宋体]10 g[font=宋体]硅藻土([/font][font=Times New Roman]80[/font][font=宋体]目[/font][/font][font=宋体]~[/font][font=宋体]120[font=宋体]目)与样品充分混匀,再依次加入[/font][/font][font=宋体]5 mL[font=宋体]饱和氯化钠水溶液和[/font][font=Times New Roman]70 mL[/font][font=宋体]甲醇[/font][font=Times New Roman]-[/font][font=宋体]丙酮([/font][font=Times New Roman]3+1[/font][font=宋体]),高速均质提取[/font][font=Times New Roman]3 min[/font][font=宋体]。将提取液移入离心管中,于[/font][/font][font=宋体]10000 r/min[/font][font=宋体]离心[/font][font=宋体]2[/font][font=宋体] min[font=宋体],将上层[/font][/font][font=宋体]提取液移入[/font][font='Times New Roman']250 mL[/font][font=宋体][font=宋体]浓缩瓶中。残渣每次再用[/font]50 mL[font=宋体]甲醇[/font][font=Times New Roman]-[/font][font=宋体]丙酮([/font][font=Times New Roman]3+1[/font][font=宋体])重复提取两次,合并提取液。[/font][/font][b][font=Calibri] [/font][font=宋体]蜂蜜、乳及乳制品样品[/font][/b][font=宋体]准确称取约[/font][font=宋体]20 g[font=宋体]样品(精确至[/font][font=Times New Roman]0.1 g[/font][font=宋体])[/font][/font][font=宋体]于[/font][font='Times New Roman']250 mL[/font][font=宋体]具塞锥形瓶中,[/font][font=宋体]加入[/font][font=宋体]10 mL[font=宋体]饱和氯化钠水溶液和[/font][font=Times New Roman]70 mL[/font][font=宋体]甲醇[/font][font=Times New Roman]-[/font][font=宋体]丙酮([/font][font=Times New Roman]3+1[/font][font=宋体]),超声波提取[/font][font=Times New Roman]30 min[/font][font=宋体]。移入离心管中,于[/font][/font][font=宋体]10000 r/min[/font][font=宋体]离心[/font][font=宋体]2[/font][font=宋体] min[font=宋体],将上层[/font][/font][font=宋体]提取液移入[/font][font='Times New Roman']250 mL[/font][font=宋体][font=宋体]浓缩瓶中。残渣每次再用[/font]50 mL[font=宋体]甲醇[/font][font=Times New Roman]-[/font][font=宋体]丙酮([/font][font=Times New Roman]3+1[/font][font=宋体])重复提取两次,合并提取液。[/font][/font][b][font='Times New Roman'] [/font][font=宋体]2.[font=宋体]液液分配[/font][/font][/b][font=宋体]将提取液于[/font][font=宋体]40[/font][font=宋体] ℃水浴中旋转浓缩至只剩水相,并转移至[/font][font='Times New Roman']250 mL[/font][font=宋体][font=宋体]分液漏斗中,加入[/font]50 mL[font=宋体]饱和氯化钠水溶液和[/font][/font][font='Times New Roman']25 mL[/font][font=宋体][font=宋体]乙酸乙酯,振摇[/font]3 min[font=宋体],静置分层,收集乙酸乙酯相。水相再用[/font][/font][font=宋体]20 mL[font=宋体]乙酸乙酯重复提取两次,合并乙酸乙酯相。经无水硫酸钠柱脱水,收集于[/font][/font][font='Times New Roman']250 mL[/font][font=宋体]浓缩瓶中,[/font][font=宋体]于[/font][font=宋体]40[/font][font=宋体] ℃水浴中旋转浓缩至近干,加入[/font][font='Times New Roman']5 mL[/font][font=宋体][font=宋体]乙酸乙酯[/font]-[font=宋体]环己烷([/font][font=Times New Roman]1+1[/font][font=宋体])溶解残渣,并用[/font][font=Times New Roman]0.45 [/font][/font][font='Times New Roman']μm[/font][font=宋体]滤膜过滤,待净化。[/font][b][font='Times New Roman'] [/font][font=宋体]3[/font][font='Times New Roman'].[/font][font=宋体]净化[/font][font=宋体]凝胶色谱([/font][font='Times New Roman']GPC[/font][font=宋体])净化[/font][font=宋体]凝胶色谱净化条件如下:[/font][/b][font=宋体][font=宋体]净化柱:[/font]700 mm[font=宋体]×[/font][font=Times New Roman]25 mm[/font][font=宋体],[/font][font=Times New Roman]Bio Bcads S X3[/font][font=宋体],或相当者;[/font][/font][font=宋体][font=宋体]流动相:乙酸乙酯[/font]-[font=宋体]环己烷([/font][font=Times New Roman]1+1[/font][font=宋体]);[/font][/font][font=宋体][font=宋体]流速:[/font]4.7 mL/min[font=宋体];[/font][/font][font=宋体][font=宋体]样品定量环:[/font]5.0 mL[font=宋体];[/font][/font][font=宋体][font=宋体]预淋洗体积:[/font]50 mL[font=宋体];[/font][/font][font=宋体][font=宋体]洗脱总体积:[/font]210 mL[font=宋体];[/font][/font][font=宋体][font=宋体]开始弃去体积:[/font]90 mL[font=宋体];[/font][/font][font=宋体][font=宋体]收集体积:[/font]90 mL[font=宋体];[/font][/font][font=宋体][font=宋体]最后弃去体积:[/font]30 mL[font=宋体]。[/font][/font][b][font=宋体]凝胶色谱净化步骤如下:[/font][/b][font=宋体][font=宋体]将[/font]5 mL[font=宋体]待净化液按照凝胶色谱净化条件进行净化,合并馏份收集器中的收集液于[/font][/font][font='Times New Roman']250 mL[/font][font=宋体]浓缩瓶中,于[/font][font='Times New Roman']4[/font][font=宋体]0[/font][font=宋体] ℃水浴中旋转浓缩至近干,加入[/font][font=宋体]5 mL[font=宋体]甲醇以溶解残渣,待净化。[/font][/font][b][font=宋体] [/font][font=宋体]固相萃取([/font][font='Times New Roman']SPE[/font][font=宋体])净化[/font][/b][font=宋体]使用前用[/font][font=宋体]5 mL[font=宋体]甲醇预淋洗[/font][font=Times New Roman]C18[/font][font=宋体]固相萃取柱([/font][font=Times New Roman]1 g[/font][font=宋体],[/font][font=Times New Roman]6 mL[/font][font=宋体]),将[/font][font=Times New Roman]5 mL[/font][font=宋体]溶解液倾入[/font][font=Times New Roman]C18[/font][font=宋体]固相萃取柱中,以[/font][font=Times New Roman]1 mL/min[/font][font=宋体]的速度收集流出液,再用[/font][font=Times New Roman]10 mL[/font][font=宋体]甲醇进行洗脱。收集全部洗脱液于[/font][font=Times New Roman]50 mL[/font][font=宋体]浓缩瓶中,于[/font][/font][font='Times New Roman']4[/font][font=宋体]0[/font][font=宋体] ℃水浴中旋转浓缩至干。用甲醇溶解并定容至[/font][font=宋体]1.0 mL[font=宋体],经[/font][font=Times New Roman]0.45 [/font][/font][font='Times New Roman']μm[/font][font=宋体]滤膜过滤后,供[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]测定和确证。[/font][b][font=宋体] [/font][font=宋体]国标解读及注意事项[/font][/b][font='Times New Roman']1.[/font][font=宋体]硝基咪唑标准物质用甲醇配成[/font][font=宋体]1000[/font][font='Times New Roman'] μg/[/font][font=宋体]mL[font=宋体]的标准[/font][/font][font=宋体]储备液,在[/font][font='Times New Roman']0[/font][font=宋体] [/font][font=宋体]~[/font][font='Times New Roman']4[/font][font=宋体] ℃条件下避光保存,可使用[/font][font='Times New Roman']12[/font][font=宋体]个月。[/font][font=宋体]2.[/font][font=宋体]如果有条件,建议凝胶色谱净化系统中配合使用紫外检测器,准确监测目标化合物及杂质的流出情况。[/font][b][font=宋体]3[/font][font='Times New Roman'].[/font][font=宋体][font=宋体]固相萃取净化过程中,[/font]C18[font=宋体]柱作为净化柱使用,注意上样过程中就需要收集流出液,再和洗脱液进行合并。[/font][/font][font=宋体]4.[/font][font=宋体]国标方法中使用基质添加标准曲线,外标法进行回收率的校正。注意做肉类样品的基质添加标准曲线前,先进行洗涤,然后加标,再进行后续提取净化等流程。[/font][font='Times New Roman']5.[/font][font=宋体]建议使用硝基咪唑标准物质相对应的同位素内标,进行回收率的校正。[/font][font=Calibri] [/font][font=Calibri] [/font][font=宋体]参考文献[/font][/b][font=宋体]GB/T 21318-2007 [/font][font=宋体]动物源食品中硝基咪唑残留量检验方法[/font][align=center][font=Calibri] [/font][/align][align=center][img=,554,]https://ng1.17img.cn/bbsfiles/images/2020/10/202010301416299459_3472_3793_3.png!w554x415.jpg[/img][font=Calibri] [/font][/align][align=center][/align][align=center][/align][font=宋体][/font][align=center][font=宋体]图[/font][font=宋体]1 [/font][font=宋体]肌肉组织、脏器组织样品及水产品中硝基咪唑残留量测定的前处理流程图[/font][/align][align=center][/align][align=center][/align][align=center][img=,554,]https://ng1.17img.cn/bbsfiles/images/2020/10/202010301416169976_4411_3793_3.png!w554x415.jpg[/img][/align][font=宋体][/font][align=center] [/align][align=center][font=宋体]图[/font][font=宋体]2 [/font][font=宋体]蜂蜜、乳及乳制品样品中硝基咪唑残留量测定的前处理流程图[/font][/align][font=宋体][/font][font=宋体][/font][align=center][b][font='Times New Roman'][font=宋体]表[/font][/font][font='Times New Roman']1 [/font][font='Times New Roman'][font=宋体]硝基咪唑标准物质信息表[/font][/font][/b][/align][align=center][font=宋体][img=,690,]https://ng1.17img.cn/bbsfiles/images/2020/10/202010301416445861_6609_3793_3.jpg!w690x892.jpg[/img][/font][/align]
GB/T29668-2013化妆品用防腐剂 双(羟甲基)咪唑烷基脲
各位老师,现在实验室在做氯丙醇脂肪酸酯,参照标准[font=Verdana, Arial][color=#333333][back=#f4f1e2]GB 5009.191-2016 食品安全国家标准 食品中氯丙醇及其脂肪酸酯含量的测定。其中衍生剂七氯丁酰基咪唑需要用气密针吸取,但操作过程中衍生剂容易变成白色固体,用气密针吸不起来,所以改成[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url]吸,但好像衍生效果不好。请教各位是不能用[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url]吸吗?为什么标准中规定要用气密针?万分感谢[img]https://simg.instrument.com.cn/bbs/images/default/em09512.gif[/img]。[/back][/color][/font]
求芝麻酚,咪唑和二甲苯麝香检测的标准。国标,国外的都可以,主要是标准!谢谢!
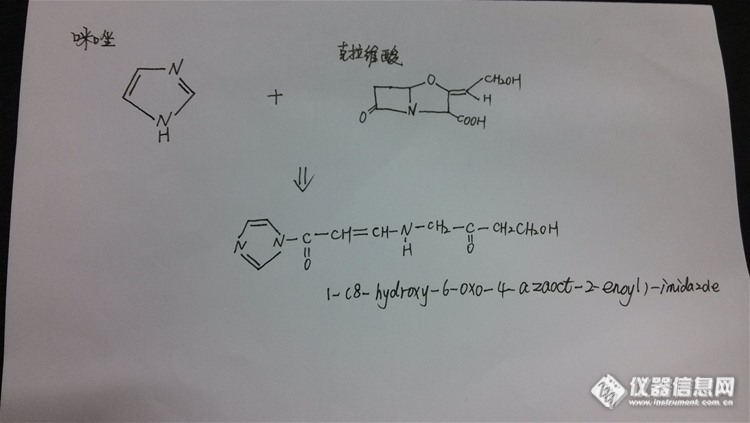
根据国外文献报道,血浆中克拉维酸的高效液相检测方法中常用咪唑衍生化试剂进行衍生以增强其紫外吸收。现在有个问题:衍生化后的咪唑色谱峰对咪唑衍生产物色谱峰有干扰,调节pH值及流动相比例未见效。我将反应式和液相条件列出来,请大家帮忙看看,如何改变液相条件以实现两者分离,感激不尽。 液相检测条件:C18(250mm长柱); 流动相:0.05M硫酸二氢钠溶液(pH调至2.2):乙腈=98:2; 柱温:40℃; 流速:0.6ml/min 克拉维酸衍生反应(文献报道4体积的克拉维酸加1体积的咪唑,具体摩尔比不明):http://ng1.17img.cn/bbsfiles/images/2014/05/201405101115_499105_1625629_3.jpg
近年来乳制品的质量安全问题时有发生,给消费者的生命安全和财产安全带来巨大损害。默克密理博作为色谱领域的鼻祖,一直在为广大消费者的食品安全分析检测贡献自己的一份力量。默克密理博的应用团队也不断为客户开发出安全可靠的分析检测方法。该贴将给大家分享牛奶中左旋咪唑残留量的测定方法。
有网友问:做4-甲基咪唑不出峰。如何解决。
大家好: 我现在有个离子液体样品,里面含有大概1%的N-甲基咪唑量,因为用气相色谱做这个样品对柱子有损坏作用,现在想通过液相色谱法对N甲基咪唑做定量分析。我公司有安捷伦的液相色谱,柱子是C18的,检测器有紫外和视差检测器。我们自己通过液相实验后分析不出样品中的N甲基咪唑,但进纯样N甲基咪唑后有信号峰出现。想求教下大家有什么好方法能分析出离子液体样品中的N甲基咪唑。