泛酸钠有关物质检测实验按要求色谱条件为柱OSDC8流动相磷酸氢二钾——磷酸二氢钾缓冲液为流速0.8检测波长222nm在低浓度对照液中,泛酸钠主峰出峰时间13min,11min出现相当于主峰面积3/4的负峰在高浓度供试品中(供试品与对照品浓度相差100倍),负峰任存在,但面积变化不大,主峰前沿出现小的肩峰。做了空白实验,没有负峰存在,以前从没有出现这种情况,决定调节流动相继续做做看。请问负峰是否要算为杂质峰?
代朋友咨询下:[size=4] 做乳品产品的时候,加的配料是抗坏血酸钠和泛酸钙,在营养成分标签上是标抗坏血酸和泛酸,如果需要一个检测方法来检测VC和泛酸的含量,选用的标准是什么?国家标准测 维生素C (GB5413.18) 和 泛酸(GB5413.17)的标准可以用来测以抗坏血酸钠和泛酸钙为配料的产品的VC和泛酸的含量吗?谢谢![/size]
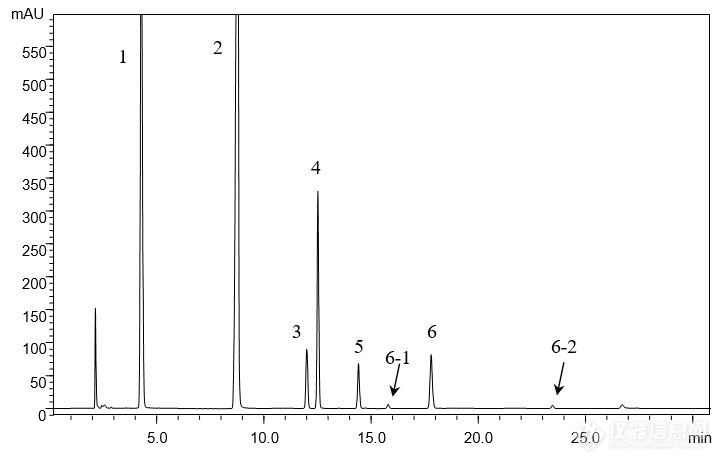
[align=center][b]注射用水溶性维生素的分析(1)[/b][/align][align=center][b]——维生素C钠、烟酰胺、泛酸钠、盐酸吡哆辛、硝酸硫胺、核黄素磷酸钠[/b][/align][align=center][b][/b][/align][align=left]客户提供了注射用水溶性维生素粉针剂及对照品(维生素C钠、烟酰胺、泛酸钠、盐酸吡哆辛、硝酸硫胺、核黄素磷酸钠),要求本实验室依据客户所提供方法筛选合适色谱柱,实现粉针剂中各组分物质的良好分离,同时满足方法中对分离度及理论塔板数的要求。[/align][align=left][/align][align=left]首先,依据客户提供的色谱条件,对对照品溶液进行分析。尝试使用不同填料类型的色谱柱,包括CAPCELL PAK C[sub]18[/sub] MGII,AQ S5,AQ S3,SUPERIOREX ODS,CAPCELL PAK ADME及PFP色谱柱。[/align][align=left][/align][align=left]由于不同色谱柱的分离选择性不同,最终发现CAPCELL PAK C[sub]18 [/sub]MGII色谱柱在完全按照客户提供方法的前提下能够得到最佳分离结果,对照品溶液中各组分均能够得到良好分离(如图1),分离度均在3.0以上,满足客户1.5要求;理论塔板数按核黄素计为103983,满足客户大于15000的要求(见表1)。[/align][align=left][/align][align=center][img=,690,443]http://ng1.17img.cn/bbsfiles/images/2018/01/201801041022_5661_2222981_3.jpg!w690x443.jpg[/img][/align][align=center]图1 CAPCELL PAK C[sub]18[/sub] MGII分析对照品溶液结果[/align][align=center] 1. 维生素C钠 2. 烟酰胺 3. 泛酸钠 4. 盐酸吡哆辛 5. 硝酸硫胺 6, 6-1, 6-2 核黄素磷酸钠[/align][align=left][img=,690,270]http://ng1.17img.cn/bbsfiles/images/2018/01/201801041022_1444_2222981_3.jpg!w690x270.jpg[/img][/align][align=left][/align][align=left][/align][align=center]表1 CAPCELL PAK C[sub]18 [/sub]MGII分析对照品溶液结果详表[/align][align=center][img=,458,316]http://ng1.17img.cn/bbsfiles/images/2018/01/201801041022_2894_2222981_3.jpg!w458x316.jpg[/img][/align][align=center][/align][align=center]在上述色谱条件下,继续使用CAPCELL PAK C[sub]18[/sub] MGII色谱柱对粉针剂供试品溶液进行分析,各待测组分及相邻杂质均能够得到良好分离,结果见图2、图3及表2。[/align][align=center][/align][align=center][img=,682,427]http://ng1.17img.cn/bbsfiles/images/2018/01/201801041023_7282_2222981_3.jpg!w682x427.jpg[/img][/align][align=center]图2 CAPCELL PAK C[sub]18[/sub] MGII分析供试品及空白溶液结果[/align][align=center]1. 维生素C钠 2. 烟酰胺 3. 泛酸钠 4. 盐酸吡哆辛 5. 硝酸硫胺 6, 6-1, 6-2 核黄素磷酸钠[/align][align=center][/align][align=left][img=,690,200]http://ng1.17img.cn/bbsfiles/images/2018/01/201801041023_5300_2222981_3.jpg!w690x200.jpg[/img][/align][align=left][/align][align=center][img=,690,455]http://ng1.17img.cn/bbsfiles/images/2018/01/201801041024_9636_2222981_3.jpg!w690x455.jpg[/img][/align][align=center]图3 CAPCELL PAK C[sub]18[/sub] MGII分析供试品溶液结果放大图[/align][align=center] [/align][align=center]表2 MGII分析供试品溶液结果详表[/align][align=center][img=,487,538]http://ng1.17img.cn/bbsfiles/images/2018/01/201801041024_7687_2222981_3.jpg!w487x538.jpg[/img][/align][align=center][/align]
如题。这个问题最近是我在整理SOP的时候参照国标发现的一个不解的问题。按照国标GB/T22246-2008上的描述。配置一个泛酸钙的标准曲线,进样品,出峰时间应该是泛酸钙的,那么最终测量的是泛酸钙。泛酸和泛酸钙不为同一种东西,且泛酸钙稳定为原料首选,泛酸不稳定。问题来了,既然测量的物质和对照品都为泛酸钙,为什么公式中计算泛酸含量的时候不需要换算,而泛酸钙的含量测定需要换算。
请教:注射用水溶性维生素中关于烟酰胺、等5项的液相检测方法其标准为烟酰胺、盐酸吡哆辛、硝酸硫胺、泛酸钠、维生素C钠和核黄素磷酸钠 照高效液相色谱法(中国药典1995年版二部附录Ⅴ D)测定。 色谱条件与系统适用性试验 用氨基键合多孔硅胶为填料,以(0.02mol/L)磷酸二氢钾溶液-乙腈(27:73),用10%盐酸溶液调节pH为5.3的溶液为流动相,流速为1.5ml/min,检测波长:烟酰胺、盐酸吡哆辛、硝酸硫胺、泛酸钠、维生素C钠为214nm;核黄素磷酸钠用萤光检测λEX=445nm、λEM=520nm。各组分的分离度应符合要求。 对照品溶液的制备 (1)取烟酰胺对照品约150mg、硝酸硫胺对照品约12mg、盐酸吡哆辛对照品约18mg、泛酸钠对照品约62mg,分别精密称量置50ml量瓶中,加水溶解并稀释至刻度摇匀,精密量取2ml置50ml量瓶中,用流动相稀释至刻度,摇匀,即为对照品溶液(Ⅰ),此溶液置暗处充氮气于零下20℃可保存1个月。(2)取维生素C钠对照品约425mg、核黄素磷酸钠对照品约19mg,精密称定,置50ml量瓶中加水溶解并稀释至刻度摇匀,精密量取2ml置50ml量瓶中,用流动相稀释至刻度,摇匀即为对照品溶液(Ⅱ),此溶液必须临用新鲜配制,并于零下20℃保存,用前放置至室温。 等容混合对照品溶液(Ⅰ)和对照品溶液(Ⅱ)即为对照品溶液。 供试品溶液的制备 取装量差异项下的内容物约2瓶重量,精密称定,置100ml量瓶中,加水溶解并稀释至刻度,摇匀,精密量取15ml置200ml量瓶中,用流动相稀释至刻度。 测定法 取对照品溶液和供试品溶液各10μl,交替注入液相色谱仪,测定,用外标法计算各组分含量,即得。目前存在问题用紫外检测的分不开5种组分,大家有什么好办法,谢谢
现在我们公司增加辅料乙醇和醋酸钠的红外检测,需要购买红外乙醇对照品和醋酸钠对照品。请各位大侠提供除了中检所外,能够在一个星期内买到的厂家。谢谢大家了!!!!
样品为复方维生素,其中一项是核黄素磷酸钠,没找到核黄素磷酸钠的对照品,故用的核黄素对照品样品制备:先用水溶,然后用流动相稀释,流动相弱酸性做出的结果比标示量低了很多啊用核黄素对照品代替核黄素磷酸钠对照品,请问结果可信吗?
按照泛酸钙残留溶剂标准:配制成含二氯甲烷36ppm,三氯甲烷3.6ppm,三氯乙烯4.8ppm,二氧六环22.8ppm,苯0.12ppm的水溶液,精密取5ml于顶空瓶加无水硫酸钠1g密封摇匀作为对照液精密取样品0.3g置顶空瓶精密加水5ml与无水硫酸钠1g密封摇匀,作为供试液顶空温度90℃ 平衡30分钟。SE54柱 柱温45℃ 载气为氦气 3.5psi或4.5ml/min FID检测器 残留溶剂应符合规定问题一:我手头有SE54两根 30m*0.25mm*0.25μm 和30m*0.53mm*1.00μm根据标准是0.53mm 可是0.25mm分离度会好些 不知道如何选择?问题二:标准没有提到分流比,那该怎么设好呢?这个苯的标准是最低的≤0.0002% 应该属于痕量分析了。痕量分析似乎0.53mm更合适

http://ng1.17img.cn/bbsfiles/images/2014/05/201405311512_500963_1609327_3.gif 泛酸钙,为维生素类药物,是辅酶A的组成部分。蛋白质、脂肪、糖在体内的代谢不能缺少辅酶A。在混旋泛酸钙中,只有右旋体具有维生素活性,。用于维生素B缺乏症及周围神经炎,以及手术后的肠绞痛。与维生素C合用可治疗播散性红斑狼疮。主要用于医药、食品添加剂及饲料添加剂,是人体和动物维持正常生理不可缺少的微量物质。除特殊营养食品外,使用量须在1%(以钙计)以下。奶粉强化时为10mg/100g;烧酒、威士忌酒中添加0.02%可增强风味;蜂蜜中添加0.02%可防止冬季结晶;可缓冲咖啡因及糖精等的苦味。色谱条件:Agilent1260液相色谱仪,紫外检测器,月旭Ultimate® XB-C18色谱柱(p/N: 00201-31043,S/N:211303968),流动相为乙腈-水-磷酸(50:950:1),检测波长为210nm,流速1.0ml/min,进样量为10μL。溶液配制:对照品溶液:称取泛酸钙对照品12.5mg,精密称定,置于25ml量瓶中,制成浓度约为0.5mg/ml的溶液;供试品溶液:称取该营养乳剂5ml,加5ml3%的偏磷酸溶液,混匀,在8000rad/min的离心机中离心5min,取上清液用0.45μm的滤膜滤过,即得。空白溶液:取不含泛酸钙的营养乳剂5ml,加5ml3%的偏磷酸溶液,混匀,在8000rad/min的离心机中离心5min,取上清液用0.45μm的滤膜滤过,即得。结果:对照品溶液色谱图:http://ng1.17img.cn/bbsfiles/images/2014/06/201406061216_501362_1609327_3.jpg供试品溶液色谱图:http://ng1.17img.cn/bbsfiles/images/2014/06/201406061216_501363_1609327_3.jpg空白溶液色谱图:http://ng1.17img.cn/bbsfiles/images/2014/05/201405311513_500964_1609327_3.jpg讨论:对于体系很复杂的营养乳剂来说,寻找合适的分析方法的任务非常艰巨。在该营养制剂中,水溶性维生素的种类比

[align=center][b][font=宋体]乳制品微生物法检验泛酸过程及注意事项[/font][/b][/align][font=宋体][b]微生物法测定原理:[/b][/font][font=宋体][font=宋体]泛酸是植物乳杆菌生长所必需的营养素[/font][font=Calibri],[/font][font=宋体]在一定控制条件下[/font][font=Calibri],[/font][font=宋体]将植物乳杆菌液接种至含有试样液的培养液中[/font][font=Calibri],[/font][font=宋体]培养一定时间后测定透光率[/font][font=Calibri]([/font][font=宋体]或吸光度值[/font][font=Calibri]),[/font][font=宋体]根据泛酸含量与透光率[/font][font=Calibri]([/font][font=宋体]或吸光度值[/font][font=Calibri])[/font][font=宋体]的标准曲线计算出试样中泛酸的含量。[/font][/font][b][font=宋体][font=Calibri]1.[/font][/font][font=宋体]试管处理[/font][/b][font=宋体][font=宋体]所用试管使用前洗刷干净[/font][font=Calibri],[/font][font=宋体]用水煮沸 [/font][font=Calibri]30min ,[/font][font=宋体]沥干后放入盐酸浸泡液中浸泡 [/font][font=Calibri]2h ,[/font][font=宋体]经 [/font][font=Calibri]170[/font][font=宋体]℃ 烘 [/font][font=Calibri]3h [/font][font=宋体]后使用。[/font][/font][b][font=宋体][font=Calibri]2.试[/font][/font][font=宋体]液配制[/font][/b][font=宋体][font=宋体]乙酸溶液[/font][font=Calibri]( 0. 2mol/ L ):[/font][font=宋体]吸取 [/font][font=Calibri]11.8mL [/font][font=宋体]冰乙酸[/font][font=Calibri],[/font][font=宋体]用水稀释至 [/font][font=Calibri]1000mL ,[/font][font=宋体]混匀。[/font][/font][font=宋体][font=宋体]乙酸钠溶液[/font][font=Calibri]( 0. 2mol/ L ):[/font][font=宋体]称取 [/font][font=Calibri]27.2g [/font][font=宋体]三水合乙酸钠[/font][font=Calibri],[/font][font=宋体]加水溶解并稀释至[/font][font=Calibri]1000mL[/font][font=宋体],混匀。[/font][/font][font=宋体][font=宋体]氢氧化钠溶液[/font][font=Calibri]( 1mol/ L ):[/font][font=宋体]称取 [/font][font=Calibri]40g [/font][font=宋体]氢氧化钠[/font][font=Calibri],[/font][font=宋体]加水溶解并稀释至 [/font][font=Calibri]1000mL ,[/font][font=宋体]混匀[/font][/font][font=宋体]氢氧化钠溶液[/font][font=Calibri]( 0.1mol/ L ):[/font][font=宋体]称取 [/font][font=Calibri]4g [/font][font=宋体]氢氧化钠[/font][font=Calibri],[/font][font=宋体]加水溶解并稀释至 [/font][font=Calibri]1000mL ,[/font][font=宋体]混匀。[/font][font=宋体][font=宋体]生理盐水[/font][font=Calibri]:[/font][font=宋体]称取 [/font][font=Calibri]9g [/font][font=宋体]氯化钠[/font][font=Calibri],[/font][font=宋体]加水溶解并稀释至 [/font][font=Calibri]1000mL ,[/font][font=宋体]混匀。临用前预先灭菌[/font][font=Calibri],[/font][font=宋体]于 [/font][font=Calibri]121[/font][font=宋体]℃ 高压灭菌 [/font][font=Calibri]10min [/font][font=宋体]后备用。[/font][/font][font=宋体][font=宋体]乙醇溶液[/font][font=Calibri]( 20% ):[/font][font=宋体]量取 [/font][font=Calibri]200mL [/font][font=宋体]无水乙醇与 [/font][font=Calibri]800mL [/font][font=宋体]水混匀。[/font][/font][b][font=宋体][font=Calibri]3.[/font][/font][font=宋体]标准溶液的配制[/font][/b][font=宋体][font=宋体]泛酸标准储备溶液[/font][font=Calibri]( 40. 0 [/font][font=宋体]μ [/font][font=Calibri]g / mL ):[/font][font=宋体]精确称取 [/font][font=Calibri]43. 5mg [/font][font=宋体]预干燥至恒重的 [/font][font=Calibri]D- [/font][font=宋体]泛酸钙[/font][font=Calibri],[/font][font=宋体]加水溶解并转移至 [/font][font=Calibri]1000mL [/font][font=宋体]容量瓶中[/font][font=Calibri],[/font][font=宋体]加 [/font][font=Calibri]10mL [/font][font=宋体]乙酸溶液[/font][font=Calibri], 100mL [/font][font=宋体]乙酸钠溶液[/font][font=Calibri],[/font][font=宋体]用水定容至刻度。储存于棕色瓶中[/font][font=Calibri],[/font][font=宋体]加入 [/font][font=Calibri]3 [/font][font=宋体]滴 [/font][font=Calibri]~5 [/font][font=宋体]滴甲苯[/font][font=Calibri],[/font][font=宋体]于 [/font][font=Calibri]2[/font][font=宋体]℃[/font][font=Calibri]~4[/font][font=宋体]℃ 冰箱中可保存 [/font][font=Calibri]2 [/font][font=宋体]年。[/font][/font][font=宋体][font=宋体]泛酸标准中间液[/font][font=Calibri]( 1. 00 [/font][font=宋体]μ [/font][font=Calibri]g / mL ):[/font][font=宋体]准确吸取 [/font][font=Calibri]25. 0mL [/font][font=宋体]泛酸标准储备溶液置于 [/font][font=Calibri]1000mL [/font][font=宋体]容量瓶中[/font][font=Calibri],[/font][font=宋体]加入 [/font][font=Calibri]10mL [/font][font=宋体]乙酸溶液[/font][font=Calibri],100mL [/font][font=宋体]乙酸钠溶液[/font][font=Calibri],[/font][font=宋体]用水定容至刻度。加入 [/font][font=Calibri]3 [/font][font=宋体]滴 [/font][font=Calibri]~5 [/font][font=宋体]滴甲苯于 [/font][font=Calibri]2[/font][font=宋体]℃[/font][font=Calibri]~4[/font][font=宋体]℃ 冰箱中可保存 [/font][font=Calibri]1 [/font][font=宋体]年。[/font][/font][font=宋体][font=宋体]泛酸标准工作溶液[/font][font=Calibri]( 20ng / mL ):[/font][font=宋体]准确吸取 [/font][font=Calibri]2. 00mL [/font][font=宋体]泛酸标准中间溶液置于 [/font][font=Calibri]100mL [/font][font=宋体]容量瓶中[/font][font=Calibri],[/font][font=宋体]用水定容至刻度[/font][font=Calibri],[/font][font=宋体]混匀。临用前现配。[/font][/font][b][font=宋体][font=Calibri]4.[/font][/font][font=宋体]储备菌种的制备[/font][/b][font=宋体][font=宋体]将菌种植物乳杆菌转接至琼脂培养基中[/font][font=Calibri],[/font][font=宋体]在 [/font][font=Calibri]37[/font][font=宋体]℃±[/font][font=Calibri]1[/font][font=宋体]℃ 恒温箱中培养 [/font][font=Calibri]20h~24h ,[/font][font=宋体]连续传种 [/font][font=Calibri]2 [/font][font=宋体]次 [/font][font=Calibri]~3 [/font][font=宋体]次。取出后放入 [/font][font=Calibri]2[/font][font=宋体]℃[/font][font=Calibri]~4[/font][font=宋体]℃ 冰箱作为储备菌株保存。每月至少传代一次[/font][font=Calibri],[/font][font=宋体]不宜超过 [/font][font=Calibri]25 [/font][font=宋体]代。试验前将储备菌株接种至琼脂培养基中[/font][font=Calibri],37[/font][font=宋体]℃±[/font][font=Calibri]1[/font][font=宋体]℃ 恒温培养箱中培养 [/font][font=Calibri]20h~24h [/font][font=宋体]以活化菌株[/font][font=Calibri],[/font][font=宋体]用于接种液的制备。[/font][/font][font=宋体]注[/font][font=Calibri]:[/font][font=宋体]保存数周以上的储备菌株[/font][font=Calibri],[/font][font=宋体]不能立即用作接种液制备[/font][font=Calibri],[/font][font=宋体]试验前宜连续传种 [/font][font=Calibri]2 [/font][font=宋体]代 [/font][font=Calibri]~3 [/font][font=宋体]代以保证细菌活力。[img=,690,179]https://ng1.17img.cn/bbsfiles/images/2023/07/202307011013288710_507_2227357_3.png!w690x179.jpg[/img][/font][font=宋体][b][font=Calibri]5.[/font][font=宋体]接种液的制备[/font][/b][/font][font=宋体]试验前一天[/font][font=Calibri],[/font][font=宋体]取 [/font][font=Calibri]2mL [/font][font=宋体]泛酸标准工作溶液和 [/font][font=Calibri]4mL [/font][font=宋体]泛酸测定用培养液混匀[/font][font=Calibri],[/font][font=宋体]分装于 [/font][font=Calibri]2 [/font][font=宋体]支 [/font][font=Calibri]5mL [/font][font=宋体]离心管中[/font][font=Calibri],[/font][font=宋体]塞好棉塞[/font][font=Calibri],[/font][font=宋体]于[/font][font=Calibri]121[/font][font=宋体]℃ 高压灭菌 [/font][font=Calibri]10min [/font][font=宋体]后即为种子培养液。冷却后用接种环将活化的菌株转种至[/font][font=Calibri]2 [/font][font=宋体]支种子培养液中[/font][font=Calibri],[/font][font=宋体]于 [/font][font=Calibri]37[/font][font=宋体]℃±[/font][font=Calibri]1[/font][font=宋体]℃ 恒温培养箱中培养 [/font][font=Calibri]20h~24h [/font][font=宋体]。[/font][font=宋体][font=宋体]取出后[/font] [font=Calibri]3000r / min [/font][font=宋体]离心 [/font][font=Calibri]10min ,[/font][font=宋体]弃上清液[/font][font=Calibri],[/font][font=宋体]无菌操作下用已预先灭菌的生理盐水淋洗 [/font][font=Calibri]2 [/font][font=宋体]次[/font][font=Calibri], 3000r / min [/font][font=宋体]离心 [/font][font=Calibri]10min ,[/font][font=宋体]弃上清液。再加入[/font][font=Calibri]3mL [/font][font=宋体]灭菌生理盐水[/font][font=Calibri],[/font][font=宋体]振荡混匀[/font][font=Calibri],[/font][font=宋体]制成接种液[/font][font=Calibri],[/font][font=宋体]立即使[/font][/font]用。[font=宋体][font=宋体][font=Calibri]8.[/font][font=宋体]标准系列管:[/font][/font][/font][table][tr][td][font=宋体][font=宋体]泛酸标准工作溶液[/font][font=宋体]/mL[/font][/font][/td][td][font=宋体]0[/font][/td][td][font=宋体]0.5[/font][/td][td][font=宋体]1[/font][/td][td][font=宋体]1.5[/font][/td][td][font=宋体]2.0[/font][/td][td][font=宋体]2.5[/font][/td][td][font=宋体]3[/font][/td][td][font=宋体]3.5[/font][/td][td][font=宋体]4[/font][/td][td][font=宋体]4.5[/font][/td][td][font=宋体]5[/font][/td][/tr][tr][td][font=宋体][font=宋体]加水量[/font][font=宋体]/mL[/font][/font][/td][td][font=宋体]5[/font][/td][td][font=宋体]4.5[/font][/td][td][font=宋体]4[/font][/td][td][font=宋体]3.5[/font][/td][td][font=宋体]3[/font][/td][td][font=宋体]2.5[/font][/td][td][font=宋体]2[/font][/td][td][font=宋体]1.5[/font][/td][td][font=宋体]1[/font][/td][td][font=宋体]0.5[/font][/td][td][font=宋体]0[/font][/td][/tr][tr][td][font=宋体][font=宋体]泛酸测定用培养基[/font][font=宋体]/mL[/font][/font][/td][td][font=宋体]5[/font][/td][td][font=宋体]5[/font][/td][td][font=宋体]5[/font][/td][td][font=宋体]5[/font][/td][td][font=宋体]5[/font][/td][td][font=宋体]5[/font][/td][td][font=宋体]5[/font][/td][td][font=宋体]5[/font][/td][td][font=宋体]5[/font][/td][td][font=宋体]5[/font][/td][td][font=宋体]5[/font][/td][/tr][/table][font=宋体][font=Calibri][b]9.[/b][/font][font=宋体][b]灭菌:[/b]将所有测定管塞好棉塞[/font][font=Calibri],[/font][font=宋体]于 [/font][font=Calibri]121[/font][font=宋体]℃ 高压灭菌 [/font][font=Calibri]10min [/font][font=宋体]。[/font][/font][font=宋体][font=宋体]接种和培养:待测定系列管冷却至室温后[/font][font=Calibri],[/font][font=宋体]在无菌操作条件下向每支测定管滴加接种液 [/font][font=Calibri]50 [/font][font=宋体]μ [/font][font=Calibri]L [/font][font=宋体]。塞好塞子[/font][font=Calibri],[/font][font=宋体]置于[/font][font=Calibri]37[/font][font=宋体]℃±[/font][font=Calibri]1[/font][font=宋体]℃ 恒温培养箱中培养 [/font][font=Calibri]16h~20h ,[/font][font=宋体]直至达到最大混浊度[/font][font=Calibri],[/font][font=宋体]即再培养 [/font][font=Calibri]2h [/font][font=宋体]后透光率[/font][font=Calibri]([/font][font=宋体]或吸光度值[/font][font=Calibri])[/font][font=宋体]无明显变化。另准备一支标准 [/font][font=Calibri]0 [/font][font=宋体]管[/font][font=Calibri]([/font][font=宋体]含 [/font][font=Calibri]0ng [/font][font=宋体]泛酸[/font][font=Calibri])[/font][font=宋体]不接种作为 [/font][font=Calibri]0 [/font][font=宋体]对照管。[/font][/font][font=宋体][font=宋体]测定:将培养好的标准系列管、试样管用漩涡混匀器混匀。用厚度为[/font] [font=Calibri]1cm [/font][font=宋体]比色杯[/font][font=Calibri],[/font][font=宋体]于[/font][font=Calibri]550nm [/font][font=宋体]处[/font][font=Calibri],[/font][font=宋体]以未接种的 [/font][font=Calibri]0[/font][font=宋体]对照管调节吸光度值为 [/font][font=Calibri]0,[/font][font=宋体]依次测定标准系列管、试样管的吸光度值。[/font][/font][font=宋体]如果[/font][font=Calibri]0 [/font][font=宋体]对照管有明显的细菌增长[/font][font=Calibri],[/font][font=宋体]或者与[/font][font=Calibri]0[/font][font=宋体]对照管相比[/font][font=Calibri],[/font][font=宋体]标准[/font][font=Calibri]0[/font][font=宋体]管透光率在 [/font][font=Calibri]90% [/font][font=宋体]以下[/font][font=Calibri]([/font][font=宋体]或吸光度值在 [/font][font=Calibri]0.2 [/font][font=宋体]以上[/font][font=Calibri]) [/font][font=宋体]或标准系列管透光率最大变化量 [/font][font=Calibri]40% ([/font][font=宋体]或吸光度值变化量 [/font][font=Calibri]0.4 ,[/font][font=宋体]说明可能有杂菌或不明来源的泛酸混入[/font][font=Calibri],[/font][font=宋体]需重做试验。[b][font=宋体][font=Calibri]10.[/font][font=宋体]标准曲线[/font][/font][/b][font=宋体][font=宋体]以标准系列管泛酸含量为横坐标[/font][font=Calibri],[/font][font=宋体]每个标准点透光率[/font][font=Calibri]([/font][font=宋体]或吸光度值[/font][font=Calibri])[/font][font=宋体]均值为纵坐标[/font][font=Calibri],[/font][font=宋体]绘制标准曲线。[/font][/font][b][font=宋体][font=Calibri]11.[/font][font=宋体]试样结果计算[/font][/font][/b][font=宋体][font=宋体]从标准曲线查得试样管中泛酸的相应含量[/font][font=Calibri]([/font][font=宋体]ρ[/font][font=Calibri]x ),[/font][font=宋体]如果每个试样的[/font][font=Calibri]4 [/font][font=宋体]支试样系列管中有 [/font][font=Calibri]3 [/font][font=宋体]支以上泛酸含量[/font][font=Calibri]10ng~80ng[/font][font=宋体]范围内[/font][font=Calibri],[/font][font=宋体]且计算每毫升试样稀释液中泛酸浓度[/font][font=Calibri]([/font][font=宋体]ρ[/font][font=Calibri]),[/font][font=宋体]各管之间相对偏差小于 [/font][font=Calibri]15% ,[/font][font=宋体]则可继续进行结果计算[/font][font=Calibri],[/font][font=宋体]否则需重新取样测定。[/font][/font][img=,690,183]https://ng1.17img.cn/bbsfiles/images/2023/07/202307011017210504_285_2227357_3.png!w690x183.jpg[/img][b]最后一张附图是梯度生长的后的状态,供大家实验参考。[/b][font=宋体] [/font][/font][font=宋体] [/font]
[align=center][font=DengXian]泛酸[/font][/align][font=DengXian]广泛存在于自然界,又称遍多酸。泛酸在肉、肝脏、肾脏、水果、蔬菜、牛奶、鸡蛋、酵母、全麦和核果中含量丰富,未发现人类泛酸缺乏症。动物性食品中的泛酸大多呈结合态。[/font][font=DengXian]它由β[/font][font=DengXian]—氨基丙酸与α、γ[/font][font=DengXian]—二羟基[/font]-[font=DengXian]β,[/font][font=DengXian]β—二甲基丁酸以肽键相连的酸性物质。[/font][font=DengXian]泛酸呈浅黄色粘稠油状物,能溶于水、醋酸乙酯、冰醋酸等,略溶于乙醚、戊醇,几乎不溶于苯、氯仿,具有右旋光性。[/font][font=DengXian]泛酸呈浅黄色粘稠油状物,能溶于水、醋酸乙酯、冰醋酸等,略溶于乙醚、戊醇,几乎不溶于苯、氯仿,具有右旋光性。[/font]

GB 5009.210-2016 食品安全国家标准 食品中泛酸的测定-ADME良好数据泛酸又称维生素B5为维生素类药物,是辅酶A的组成部分,也是营养补充剂。主要用于医药、食品添加剂及饲料添加剂,是人体和动物维持正常生理不可缺少的微量物质。http://ng1.17img.cn/bbsfiles/images/2017/04/201704050958_03_2222981_3.png在上一帖中,我们使用C18 MGII色谱柱对泛酸进行了分析,由于泛酸流动相条件为高水相(95%),因此在C18 MGII色谱柱上保留时间较短(约5min)。在此,我们使用表面极性更高的ADME色谱柱对泛酸进行分析,以实现更强的保留(约6min,见图1)。本实验按照《食品安全国家标准食品中泛酸的测定》(GB 5009.210-2016)(该标准代替GB/T 5009.210—2008《食品中泛酸的测定》),使用资生堂 CAPCELL PAK ADME S5; 4.6mmi.d ×250mm色谱柱,对泛酸标准品进行检测分析,并对标准曲线进行考察。http://ng1.17img.cn/bbsfiles/images/2017/04/201704050958_01_2222981_3.pnghttp://ng1.17img.cn/bbsfiles/images/2017/05/201705020914_02_2222981_3.pnghttp://ng1.17img.cn/bbsfiles/images/2017/05/201705020914_01_2222981_3.png泛酸标准曲线的制作配制10 µg/mL, 20 µg/mL, 40 µg/mL, 80 µg/mL, 160 µg/mL, 320 µg/mL系列标准工作液进行标准曲线的制作。以峰面积为纵坐标,标准工作液浓度为横坐标,绘制标准曲线。由图2所示,泛酸在10µg/mL—320µg/mL浓度范围内线性良好,相关系数R2=0.9993。结论综上所述,使用资生堂CAPCELL PAK ADME S5; 4.6mm i.d.×250mm色谱柱按照《食品安全国家标准 食品中泛酸的测定》(GB 5009.210-2016)对泛酸标准品进行分析,可得到良好线性,且峰形良好。表面极性更高的ADME色谱柱较MGII色谱柱,保留时间延长约1.2min,在实际样品的分析中可以期待与基质得到更好的分离效果。注: 图中色谱峰线条不平滑是由于图像在复制过程中解像度问题引起的。
请问有谁做过[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测辛酸钠有关物质的实验吗?您做的对照溶液的信噪比大概是多少?谢谢!请问辛酸钠有关物质检查法 中 供试品溶液中的溶剂是什么?每次试验前需要先进一针溶剂吗?是不是要根据信噪比的要求来调节纵坐标的范围 使对照溶液的主成分峰的峰高约为满量程的10-25% ?
保健食品中泛酸钙的测定 GB/T 22246-2008 即维生素B5与大家分享
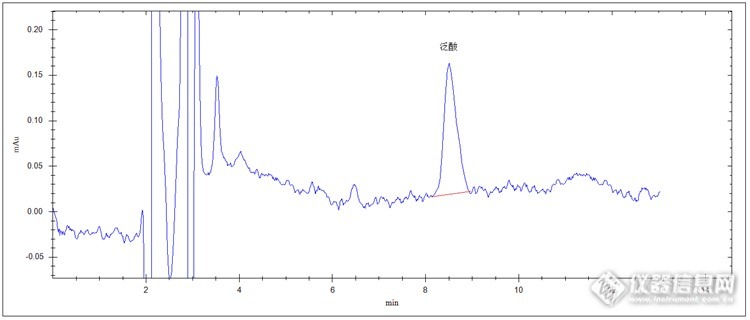
食品中泛酸高效液相色谱检测 泛酸是一种一种营养成分,是多维营养片中的主要成分之一,可用于预防因缺乏B族维生素而引起的各种疾病。它同时也是一种药物成分,多维片等多种药物成分之一,可用于预防和治疗因缺乏B族维生素而引起的多种疾病,多维片为维生素类非处方药药品。样品前处理 提取液制备:准确称取2.58g磷酸二氢钾,加纯净水约1900ml溶解,磷酸调PH值至3.0,精密加入100ml甲醇。 样品溶液制备:取适量多维营养片充分粉碎,准确称取该粉末0.2g于50ml具塞试管中,准确加入25ml以上提取液,具塞密封,超声处理15min,恒温摇床70℃ 10min,常温静置放冷,加提取液至50ml,0.45um微膜滤过,待测。 该前处理方法也可作为多维片中泛酸检测前处理方法。色谱条件检测器:紫外检测器色谱柱:C18色谱柱(250mm X 4.6mm,5um)检测波长:230nm流动相:乙腈:0.05mol/L磷酸二氢钾水溶液(PH约为6.0)=5:95(V:V)流速:1.0ml/min柱温:30℃进样量:20ul标准品色谱图(2.5ppm、5.0ppm、10.0ppm、20.0ppm、40.0ppm、80.0ppm):http://ng1.17img.cn/bbsfiles/images/2014/12/201412162024_527415_2498430_3.pnghttp://ng1.17img.cn/bbsfiles/images/2014/12/201412162024_527416_2498430_3.pnghttp://ng1.17img.cn/bbsfiles/images/2014/12/201412162024_527417_2498430_3.pnghttp://ng1.17img.cn/bbsfiles/images/2014/12/201412162024_527418_2498430_3.pnghttp://ng1.17img.cn/bbsfiles/images/2014/12/201412162024_527419_2498430_3.pnghttp://ng1.17img.cn/bbsfiles/images/2014/12/201412162024_527420_2498430_3.pnghttp://ng1.17img.cn/bbsfiles/images/2014/12/201412162026_527422_2498430_3.png多维营养片色谱图:http://ng1.17img.cn/bbsfiles/images/2014/12/201412162026_527423_2498430_3.pnghttp://ng1.17img.cn/bbsfiles/images/2014/12/201412162026_527424_2498430_3.png重复性比较色谱图: http://ng1.17img.cn/bbsfiles/images/2014/12/201412162027_527425_2498430_3.png最小检出限色谱图:http://ng1.17img.cn/bbsfiles/images/2014/12/201412162027_527426_2498430_3.png结果该方法检测该样品中泛酸含量,分离度好,色谱峰形漂亮,各项指标均优良。结果表明标准品中泛酸浓度在0.1-300ug/ml范围内有良好的线性关系,相关系数r=0.999以上,平均回收率为95%以上[/
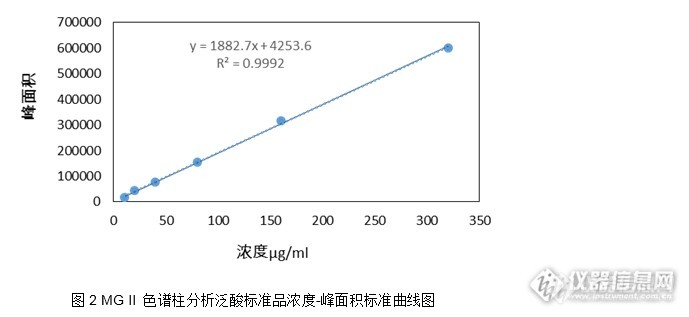
GB 5009.210-2016 食品安全国家标准 食品中泛酸的测定泛酸(Pantothenic acid)又称维生素B5,为维生素类药物,是辅酶A的组成部分,也是营养补充剂。主要用于医药、食品添加剂及饲料添加剂,是生物体维持正常生理不可缺少的微量物质。http://ng1.17img.cn/bbsfiles/images/2017/05/201705020908_01_2222981_3.png本实验按照《食品安全国家标准食品中泛酸的测定》(GB 5009.210-2016)(该标准代替GB/T 5009.210—2008《食品中泛酸的测定》),使用资生堂 CAPCELL PAK C18 MGII S5; 4.6mm i.d ×250mm色谱柱,对泛酸标准品进行检测分析,并对标准曲线进行考察。http://ng1.17img.cn/bbsfiles/images/2017/04/201704050945_01_2222981_3.png泛酸标准曲线的制作配制10 µg/mL, 20 µg/mL, 40µg/mL, 80 µg/mL, 160 µg/mL, 320 µg/mL系列标准工作液进行标准曲线的制作。以峰面积为纵坐标,标准工作液浓度为横坐标,绘制标准曲线。由图2所示,泛酸在10µg/mL—320µg/mL浓度范围内线性良好,相关系数R2=0.9992。http://ng1.17img.cn/bbsfiles/images/2017/05/201705020909_02_2222981_3.pnghttp://ng1.17img.cn/bbsfiles/images/2017/05/201705020909_01_2222981_3.png结论综上所述,使用资生堂CAPCELL PAK C18 MG II S5; 4.6mm i.d. × 250mm色谱柱按照《食品安全国家标准 食品中泛酸的测定》(GB 5009.210-2016)对泛酸标准品进行分析,可得到良好线性。注: 图中色谱峰线条不平滑是由于图像在复制过程中解像度问题引起的。
分享标准,均自网络收集,上传者不保证资料完整性以及版权。下载仅供研究,请勿用于其他用途。研究完毕请及时删除,若有正版需求,请联系出版单位。GB 5413.17-2010 婴幼儿食品和乳品中泛酸的测定
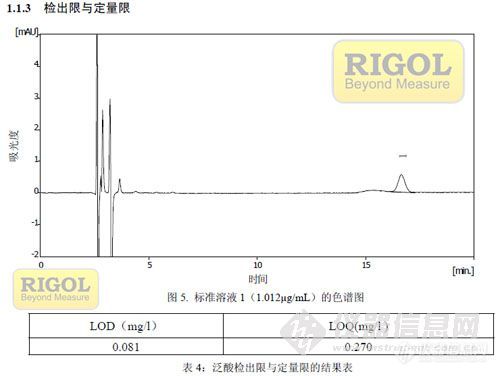
【文章来源】北京普源精电科技有限公司(RIGOL) http://www.instrument.com.cn/netshow/SH101945/index.asp【摘要】 本文根据中华人民共和国国家标准GB5413.17-2010食品安全国家标准婴幼儿食品和乳品中泛酸的测定第二法高效液相色谱法对品牌A婴儿配方奶粉和品牌B生产的牛奶中泛酸进行含量测定及方法学验证。实验结果为:品牌A婴儿配方奶粉和品牌B牛奶以泛酸峰计理论塔板数分别为12263和11423,泛酸含量分别为35.650 mg/Kg 和3.699mg/Kg,回收率分别为101.3%和97.8%,泛酸的线性范围为1.012μg/mL~12.144μg/mL (r=0.9999)。实验结果表明:采用RIGOL L-3000高效液相系统进行乳制品中泛酸含量测定,能完全满足中华人民共和国国家标准GB5413.17-2010方法规定要求,数据结果准确,重现性好。 完整应用文档,请点击如下链接下载 ======================= 点击打开链接 ====================== 针对大家所关心的问题,RIGOL应用中心会持续为大家开展分析http://simg.instrument.com.cn/bbs/images/brow/em09511.gif========================================================部分谱图:http://ng1.17img.cn/bbsfiles/images/2011/01/201101061317_272267_2222707_3.jpghttp://ng1.17img.cn/bbsfiles/images/2011/01/201101061317_272268_2222707_3.jpg欢迎大家积极讨论哈~~http://simg.instrument.com.cn/bbs/images/brow/em09510.gifRIGOL L-3000的其它相关应用文献: 1、HPLC法测定牛奶中山梨酸和苯甲酸的含量 2、HPLC法测定清火栀麦片中栀子苷的含量 3、HPLC法测定牛黄上清片中栀子苷的含量 4、HPLC法测定牛奶中牛磺酸的含量 5、高效液相色谱法测定茶叶中的茶多酚 6、高效液相色谱法测定穿心莲片中内酯的含量 7、高效液相色谱法测定三颗针药材中盐酸小檗碱的含量 8、高效液相色谱法测定天麻钩藤颗粒中黄芩苷的含量
给位大神求帮我分析一下顶空进样测苯,苯对照品的溶剂是90%乙醇,加了10mg 的无水碳酸钠,三针对照总会有一针峰面积较小(只有一半),是什么原因?
近年来乳制品的质量安全问题时有发生,给消费者的生命安全和财产安全带来巨大损害。默克密理博作为色谱领域的鼻祖,一直在为广大消费者的食品安全分析检测贡献自己的一份力量。默克密理博的应用团队也不断为客户开发出安全可靠的分析检测方法。该贴将给大家分享婴幼儿食品和乳品中泛酸的测定方法。
各位大侠,谁那里有硝酸钠水溶液与波美度的对照表啊?有的话请发份给我,谢谢。急。。。。
请教:注射用水溶性维生素中关于烟酰胺、等5项的液相检测方法其标准为烟酰胺、盐酸吡哆辛、硝酸硫胺、泛酸钠、维生素C钠和核黄素磷酸钠 照高效液相色谱法(中国药典1995年版二部附录Ⅴ D)测定。 色谱条件与系统适用性试验 用氨基键合多孔硅胶为填料,以(0.02mol/L)磷酸二氢钾溶液-乙腈(27:73),用10%盐酸溶液调节pH为5.3的溶液为流动相,流速为1.5ml/min,检测波长:烟酰胺、盐酸吡哆辛、硝酸硫胺、泛酸钠、维生素C钠为214nm;核黄素磷酸钠用萤光检测λEX=445nm、λEM=520nm。各组分的分离度应符合要求。 对照品溶液的制备 (1)取烟酰胺对照品约150mg、硝酸硫胺对照品约12mg、盐酸吡哆辛对照品约18mg、泛酸钠对照品约62mg,分别精密称量置50ml量瓶中,加水溶解并稀释至刻度摇匀,精密量取2ml置50ml量瓶中,用流动相稀释至刻度,摇匀,即为对照品溶液(Ⅰ),此溶液置暗处充氮气于零下20℃可保存1个月。(2)取维生素C钠对照品约425mg、核黄素磷酸钠对照品约19mg,精密称定,置50ml量瓶中加水溶解并稀释至刻度摇匀,精密量取2ml置50ml量瓶中,用流动相稀释至刻度,摇匀即为对照品溶液(Ⅱ),此溶液必须临用新鲜配制,并于零下20℃保存,用前放置至室温。 等容混合对照品溶液(Ⅰ)和对照品溶液(Ⅱ)即为对照品溶液。 供试品溶液的制备 取装量差异项下的内容物约2瓶重量,精密称定,置100ml量瓶中,加水溶解并稀释至刻度,摇匀,精密量取15ml置200ml量瓶中,用流动相稀释至刻度。 测定法 取对照品溶液和供试品溶液各10μl,交替注入液相色谱仪,测定,用外标法计算各组分含量,即得。目前存在问题用紫外检测的分不开5种组分,大家有什么好办法,谢谢
请教:注射用水溶性维生素中关于烟酰胺、等5项的液相检测方法其标准为烟酰胺、盐酸吡哆辛、硝酸硫胺、泛酸钠、维生素C钠和核黄素磷酸钠 照高效液相色谱法(中国药典1995年版二部附录Ⅴ D)测定。 色谱条件与系统适用性试验 用氨基键合多孔硅胶为填料,以(0.02mol/L)磷酸二氢钾溶液-乙腈(27:73),用10%盐酸溶液调节pH为5.3的溶液为流动相,流速为1.5ml/min,检测波长:烟酰胺、盐酸吡哆辛、硝酸硫胺、泛酸钠、维生素C钠为214nm;核黄素磷酸钠用萤光检测λEX=445nm、λEM=520nm。各组分的分离度应符合要求。 对照品溶液的制备 (1)取烟酰胺对照品约150mg、硝酸硫胺对照品约12mg、盐酸吡哆辛对照品约18mg、泛酸钠对照品约62mg,分别精密称量置50ml量瓶中,加水溶解并稀释至刻度摇匀,精密量取2ml置50ml量瓶中,用流动相稀释至刻度,摇匀,即为对照品溶液(Ⅰ),此溶液置暗处充氮气于零下20℃可保存1个月。(2)取维生素C钠对照品约425mg、核黄素磷酸钠对照品约19mg,精密称定,置50ml量瓶中加水溶解并稀释至刻度摇匀,精密量取2ml置50ml量瓶中,用流动相稀释至刻度,摇匀即为对照品溶液(Ⅱ),此溶液必须临用新鲜配制,并于零下20℃保存,用前放置至室温。 等容混合对照品溶液(Ⅰ)和对照品溶液(Ⅱ)即为对照品溶液。 供试品溶液的制备 取装量差异项下的内容物约2瓶重量,精密称定,置100ml量瓶中,加水溶解并稀释至刻度,摇匀,精密量取15ml置200ml量瓶中,用流动相稀释至刻度。 测定法 取对照品溶液和供试品溶液各10μl,交替注入液相色谱仪,测定,用外标法计算各组分含量,即得。目前存在问题用紫外检测的分不开5种组分,大家有什么好办法,谢谢
有朋友做D-泛酸钙或生物素吗?请问出峰时间大概在几分钟?谢谢我用的是WATERS1525型,紫外检测器,碳十八柱.3.9*150.我做了,D-泛酸钙在两分钟有一倒峰连着一个正峰,四分钟有一个正峰.标准品也是这样的.我就不知道哪个才是正确的峰.所以想请教有没有做过的是怎么确定的?
做氯霉素滴眼液有关物质:流动相:以含0.1%庚烷磺酸钠溶液(取0.1%庚烷磺酸钠溶液500ml与二甲基酰胺5ml、冰醋酸0.5ml,混匀)-乙腈(72:28)(药典为75:25)为流动相 柱子:Hypersil Bos C18 5μm尺寸:4.6×250mm庚烷磺酸钠 天津傲然精细化工研究所对硝基苯甲醛 Fluka Chemie GmbH CH-9471 Buchs结果对硝基苯甲醛一项对照品与样品的保留时间相差1.5min,氯霉素二醇物一致.请问与什么因素有关?与改变流动相比例有关系吗?流动相中二甲基甲酰胺、冰醋酸起什么作用?
求助:中药口服液质量标准制定的一些问题 第一次做新药,是一个中药复方口服液,主要成分中含有氢溴酸东蒗菪碱,质量标准制定如下: 5.1.1色谱条件 色谱柱:Promosil C18(250×4.6mm,5洀,博纳艾杰尔公司);流动相:0.07mol/L磷酸钠溶液 (用磷酸调 pH值至6.0,含0.0175mol/L十二烷基硫酸钠)-乙腈 (2:1);流速:0.8ml/min;检测波长:216nm;柱温:25℃;进样量:10ul。理论塔板数按氢溴酸东莨菪碱峰计算应不低于10000。 5.1.2 供试品和对照品溶液的制备 5.1.2.1 对照品溶液 精密称取氢溴酸东莨菪碱10.18mg,置10ml容量瓶中,加0.07mol/L磷酸钠溶液(用磷酸调pH至6.0)使溶解,并稀释至刻度,摇匀,制成每1ml含1.018mg的溶液(东莨菪碱重量=氢溴酸东莨菪碱/1.445)。 5.1.2.2 供试品溶液 精密量取本品溶液5ml,置锥形瓶中,加入2mol/L盐酸溶液30ml,超声处理(功率250W,频率40kHz)30分钟,放冷,滤过,滤渣和滤器用 2mol/L盐酸溶液分数次洗涤,合并滤液和洗液,用浓氨试液调节pH值至9,用三氯甲烷振摇提取4次,每次30ml,合并三氯甲烷液,回收容剂至干,残渣用0.07mol/L磷酸钠溶液(用磷酸调pH至6.0)溶解并移至5ml量瓶中,稀释至刻度,摇匀,即得。 5.1.3 阴性对照品溶液的制备 按处方比例及工艺,制备缺洋金花的阴性样品,再按供试品溶液的制备方法制备不含洋金花的阴性样品溶液。 5.1.4 测定方法 精密吸取上述对照品溶液与供试品溶液各10u1,分别注入液相色谱仪(自动进样仪),测定峰面积,以外标法计算含量。 5.1.5 系统适用性试验 分别吸取对照品溶液、供试品溶液及阴性品溶液10ul注入高效液相色谱仪,阴性对照品在氢溴酸东莨菪碱峰位置处无吸收峰,即其它成分对测定无干扰,氢溴酸东莨菪碱峰与其它组分峰基线分离良好。 5.1.6 线性试验 精密称取氢溴酸东莨菪碱对照品10.16mg,置25ml量瓶中,加0.07mol/L磷酸钠溶液(用磷酸调pH至6.0)溶解并稀释至刻度,摇匀。精密吸取0.5、1.0、1.5、2.0、2.5、3.0ml,分别置10ml量瓶中,加0.07mol/L磷酸钠溶液(用磷酸调pH至6.0)溶解并稀释至刻度,摇匀。按上述色谱条件测定,分别进样10ul,测得峰面积积分值。以对照品的浓度为横坐标,峰面积积分值为纵坐标,绘制标准曲线,得回归方程为:A=1.3×107C-9243.77,相关系数r:=0.9997。表明进样量在0.2032~1.2192ug范围内呈良好线性关系。 5.1.7 稳定性试验 精密量取供试品溶液5ml,按供试品(批号:2009010501)溶液制备方法制成供试品溶液,间隔一定时间(0,4,8,12,24,48h)重复进样,每次进样10ul,测得峰面积的RSD为1.78%,表明该溶液在48小时基本稳定。 5.1.8 精密度试验 精密吸取上述对照品溶液10ul,重复进样6次,测定东莨菪碱的峰面积,结果 RSD%为0.58%(n=6)。表明本方法精密度良好。 5.1.9 重复性试验 精密量取供试品溶液(批号:2009010501)5ml,按供试品溶液制备方法平行制得6份供试品溶液,分别测定东莨菪碱的含量,结果RSD为1.42%(n=6)。表明本方法有较好的重复性 。 5.1.10 加样回收率试验 5.1.10.1 对照品溶液的制备 精密称取氢溴酸东莨菪碱对照品约7.8mg,置100ml的容量瓶内,加0.07mol/L磷酸钠溶液(用磷酸调pH至6.0)使溶解,并稀释至刻度,即得。 5.1.10.2 采用加样回收率测定方法,精密量取已知含量的样品2.5ml,精密加入上述对照品溶液2.5ml/2ml/3ml,按供试品溶液制备方法平行制得6份供试品溶液,依法测定,结果平均回收率为106.7%,RSD为1.42%。 回收率=(测的东莨菪碱含量—样品中东莨菪碱含量)/加入东莨菪碱量 因为是第一次作含量测定,有许多不明白之处,中药质量标制定准指导原则也说得不清不楚,许多都是按照自己理解摸索来的。 通过测定样品的平均含量为0.077mg/ml。线性试验是根据样品的平均含量,以样品的平均含量为中间值,制定的线性取样范围。 根据加样回收中对照品加入量与样品含量之和在线性范围的原则,按照80%,100%,120%的原则加入对照品,但是结果很不理想,加样回收率超过了200%,不知道是什么方面的原因,很着急,请大家帮忙分析一下,找出有错误的地方,我马上更改。
对照品溶液与供试品溶液需使用相同的顶空条件,因为样品瓶中有气-液或气-固两相,甚至气-液-固三相共存。顶空气体中各组分的含量既与其本身的挥发性有关,又与样品基质有关。特别是那些在样品基质中溶解度大(分配系数大)的组分,“基质效应”更为明显。这是顶空进样的一大特点,即顶空气体的组成与原样品中的组成不同,这对定量分析的影响尤为严重。因此,对照品不能仅用待测物的标准品配制,还必须有与原样品相同或相似的基质,否则,定量误差将会很大。实际应用中一些消除或减少基质效应的方法:a、利用盐析作用即在水溶液中加入无机盐(如过饱和硫酸钠溶液)来改变挥发性组分的分配系数;b、在有机溶液中加入水相,这可以减小有机物在有机溶剂中的溶解度,增大其在顶空气体中的含量;c、调节溶液的pH 对于碱和酸,通过控制pH可使其解离度改变,或使其中待测物的挥发性变得更大,从而有利于分析;d、降低样品浓度也是减小基质效应的常用方法,但其代价是减低了灵敏度;e、固体样品中挥发物的扩散速度很慢,往往需要很长时间才能达到平衡。尽量采样全溶的样品溶液,有利于缩短平衡时间;f、其他消除基质效应的技术,如全挥发技术等
三黄片的实验条件:乙腈:水(1:1)(每1000ml中加磷酸二氢钾3.4g,十二烷基硫酸钠1.7g)流动相,波长265nm,对照品的峰面积不稳定,每五针的RSD值大于2%。且样品的峰面积稳定是什么原因?对盐酸小檗碱发生变化。对照品的溶剂是甲醇。
婴幼儿食品中B12 叶酸 泛酸 生物素有没有不用微生物法的其他检测方法?望老师不吝赐教
有人参加了奶粉中泛酸的能力验证吗?