如何检测石油醚,乙酸甲酯和丙酮???石油醚本身就有几个峰,要做内标法找不到对照品。用异丙醇或正丙醇做内标物可以嘛?哪个好一些?DB-WAX柱子?进样口、柱温、检测器温度如何??谢谢
由于尸体腐败可能会产生乙醇,一般尸体腐败产生乙醇的同时平行产生正丙醇,其正丙醇的浓度是鉴别乙醇是否是死后新生的重要指标。查了下有论文写到这方面,说是研究认为如果血中乙醇含量在正丙醇含量的20倍以内,则可以认定为死后产生的乙醇,否则系生前摄入乙醇。想问下,有谁知道20倍的数据是从哪里来的吗?是有什么标准上面明确写明的吗?
大家好,我想问下正丙醇与四氟丙醇2种溶剂的混合液,怎么检测含量?用气相还是用液相?
向各位求教正丙醇的检测方法,不只是纯度,最好能有这方面的国标就更好了!谢谢!
大家好.我今天查了一下溶剂手册发现上面写着正丙醇的紫外截止吸收波长为210nm,但在我今天在230nm处分析时,发现化学纯的正丙醇有很大的吸收,而且杂峰还比较的多.请问这是怎么回事?[em0715]
尸体在一定条件下,会出现腐败分解反应,这会导致其产生正丙醇、乙醇等物质。在这种情况下,测其血液中的乙醇是不准确的,那么要如何得到乙醇含量的准确值或者其下限?
尸体在出现腐败分解反应后,会产生正丙醇、乙醇等物质,血样中乙醇受其影响会升高或下降,那么是否会丢失呢?如果是没有饮酒史的人是否会“凭空”产生乙醇?如果会“凭空”产生乙醇,那是溺水死亡的,导致其产生的概率是否会大呢?
为什么在用旋转蒸发仪的时候,有时会加正丙醇来防止爆沸,原理是什么呀?
[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]用顶空做样品中的残留溶剂,但是我们先通过检测试过,样品里面没有(也就是检不出)正丙醇的残留,但领导要求还是要做验证,证明你的方法是合适的,请大家帮忙看看应该怎么验证,还有验证的项目有哪些?方案是怎么样的?
[table=100%][tr][td]使用岛津[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]GC-2014c TCD检测器, 之前用这个柱子检测过乙醇/水体系和乙二醇/水体系,检测乙醇/水时操作条件为 进样口250° 柱温80°(保留时间30min) TCD检测器250°,检测乙二醇/水体系进样口250° 柱温175°(保留时间30min) 检测器250°。现仍想用此柱子检测正丙醇/水体系,但是不知道柱温怎么设置,正丙醇沸点97.1°,水沸点100°。我测试过如下条件:1.进样口250,柱温60(保留时间30min)检测器250,此条件在1min左右出现两个峰,第一个正丙醇峰未走完接着就出现水峰。并且峰型很不好,倾斜的很严重。2.进样口250,柱温100(保留时间30min)检测器250,此条件只出现一个峰,峰型很好。3.其他 就是柱温 75 °,85°也是连峰,正丙醇峰走完最高点刚往下走了一点点就开始出水峰 。请问各位高手 我该怎么设定 条件?[/td][/tr][/table]
旋转蒸发时加入正丙醇的作用是什么
大家好,请问假如我的流动相用的是分析纯的试剂能作液相色谱的流动相吗?比如说我们要使用的流动相是正丙醇和水。我能用分析纯的正丙醇吗?
HP-5柱子怎么老化?能不能测丙酮,正丙醇等原料?
哪可买到色谱纯正丁醇,异丁醇,异戊醇,2-甲基丁醇,正丙醇标样?
GAT 1073-2013 方法测定样品中的乙醇、甲醇、正丙醇、乙醛、丙酮、异丙醇和正丁醇,用的是DB-ALC柱子,请问大家有没这款柱子证书上的TIC图呢?或者自己分析以上目标物的TIC图。。若有,请回复一下,,谢谢
哪可买到色谱纯正丁醇,异丁醇,异戊醇,2-甲基丁醇,正丙醇标样?
正丙醇与乙酸乙酯分离不开是什么原因?
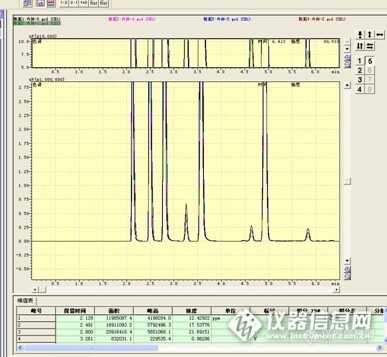
求助一下, ,我这个用程序升温法测甲醇,丙酮,正丙醇(内标) 丁醇 ,丁酯。 110℃ 2.5min 然后25℃/min升到160℃,并保持1min ,,为嘛每次都有三个小峰。如下图片
我在GDX-102气象色谱柱(热导池法)上测混合物(含乙酸。乙醇。正丙醇。异丁醇。异戊醇。乙酸乙酯。乙酸正丙酯。乙酸异丁酯。乙酸异戊酯),请问专家:怎样控制气象色谱的操作条件能把这些混合物各自的含量测出来,而且峰形较好
我们单位买了一台GC-14C[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url],当时没有调试,我用PEG-20M分离甲醇,乙醇,正丙醇分离度不好,柱效也达不到,请专家指点一下问题在那?
请问如何用高效液相色谱法(采用AGP手性色谱柱)检查酒石酸托特罗定左旋异构体?流动相中有少量磷酸盐,能否只用15%的正丙醇水溶液冲洗该手性色谱柱(Chiral-AGP)?谢谢!
液相以前一直做反相的,有一次调到正相后,从正相调回反相对照品十几针都不平衡,曾用异丙醇和乙腈冲洗系统

空气中异丙醇的测定方法 (一)聚乙二醇6000柱(直接进样)见正丙醇的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法(一)。(二)FFAP柱(溶剂解吸进样)1 原理空气中异丙醇用活性炭管采样后,用异丁醇的二硫化碳溶液解吸,经FFAP柱分离,用氢焰离子化检测器检测。以保留时间定性,峰高定量。2 仪器2.1 活性炭管:在长80mm、内径3.5~4.0mm、外径6mm的玻璃管中,分前后、两段装入150mg20~40目椰子壳活性炭,前段100mg,后段50mg,中间用玻璃棉或聚氨酯泡沫塑料隔开,两端用玻璃棉固定,套上塑料帽备用或熔封后保存。在装管前,应先将活性炭于300~350℃通氮气处理4h。2.2 采样泵,0~1L/min。2.3 微量注射器,100,10,1微升。2.4 具塞试管,5ml。2.5 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url],氢焰离子化检测器,0.41ng异丙醇给出的信噪比不低于3∶1。色谱柱:柱长2m,内径3~4mm,不锈钢柱。FFAP:Chromosorb W AW担体=10∶100柱温:70℃汽化室温度:180℃检测室温度:180℃载气(氮气):35ml/min3 试剂3.1 异丙醇,色谱纯。3.2 解吸溶剂:1%(V/V)异丁醇的二硫化碳溶液。3.3 FFAP,色谱固定液。3.4 Chromosorb WAW担体,60~80目。4 采样在采样现场打开活性炭管,50mg端接采样泵并垂直放置,以0.2L/min的速度抽取2L空气。采样后将管的两端套上塑料帽,1周内分析。5 分析步骤5.1 对照试验:将未采过样的活性炭管(2.1,数量为样品总数1/10,至少为1支)按照样品的处理操作同样处理作为空白对照。5.2 样品处理:将活性炭管中的两段活性炭分别倒入具塞试管(2.4)中,加1ml解吸溶剂(3.2),密塞,不时振摇,解吸1h。5.3 标准曲线的绘制:于50ml量瓶中,先加入少量解吸溶剂(3.2),用1ml刻度吸管准确量取一定量异丙醇(于20℃时1ml异丙醇的质量为0.7851g)加入量瓶中,再加解吸溶剂(3.2)至刻度,配成一定浓度的贮备液。临用前,取一定量贮备液用解吸溶剂(3.2)稀释成浓度为1.0、2.0、4.0、10微克/?l的标准溶液。取1微升进样,测量保留时间及峰高。每个浓度重复3次,取峰高的平均值。以异丙醇的含量对峰高作图,绘制标准曲线。保 留时间为定性指标。5.4 测定:取1微升解吸溶液进样,用保留时间定性,用峰高定量。异丙醇色谱图见图35。[img]http://ng1.17img.cn/bbsfiles/images/2007/05/200705201517_52394_1625938_3.jpg[/img]6 计算X=(C1+C2)*1000/V0式中:X——空气中异丙醇的浓度,mg/m3;C1、C2——分别为从标准曲线上查出的炭管前、后段中异丙醇的含量,微克;V0——标准状况下的样品体积,L。7 说明7.1 本法的检测限为4.1×10-4?g(进样1?l液体样品);测定范围为10~5000mg/m3;当异丙醇浓度为492.5、985、1970、4925mg/m3时,变异系数分别为2.0%、2.4%、1.8%、2.4%。7.2 活性炭对异丙醇有理想的现场采样效率。100mg活性炭对异丙醇的穿透容量为9.12mg。实验条件下解吸效率平均为97.8%。 7.3 采样后将活性炭管两端套上塑料帽,于室温下贮存,至少可稳定1周。为保存更长时间,可将采样管两端熔封或低温冷藏。为避免活性炭管吸附其它有机蒸气,最好放于密闭容器中。7.4 现场湿度过大,以致在活性炭管中形成雾滴时,将严重影响采样的可靠性。此时应连接适宜的干燥管以降低湿度。7.5 采样现场共存醋酸乙酯、乙醇、苯等保留时间与异丙醇相近的物质时干扰测定。此时可通过变更色谱条件来排除。7.6 当使用不同厂家、不同型号、不同批号的活性炭时,应重新测定穿透容量和解吸效率。
各位老师,本人是个新手,不知如何做乙醇和异丙醇的残留量测定。本人现有条件如下:1.仪器:GC900A型[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url](上海科创)2.工作站:国产大连工作站3.色谱柱:极性色谱柱,固定液为聚乙二醇(PEG-20M)的毛细管柱4.检测的为2005年版药典第三类试剂:乙醇和异丙醇药典规定为0.5%我想请教的问题是:1.如何配制对照品溶液?2.操作方法如何?[em04] [em07]
[align=center][b]食品中3-氯丙醇测定方法简介[/b][/align][align=center][b] [/b][/align]氯丙醇最初是在酱油中被发现的,传统方法制作酱油这些调味品过程中,添加不安全的酸来水解植物蛋白时能够产生一定量的氯丙醇。而氯丙醇在食品中分游离态和酯态两种形态,食用油中的氯丙醇主要是以氯丙醇酯的形式存在,且主要是3-氯丙醇酯,很少以游离的形式出现(20 μg/kg)。鉴于氯丙醇的危害性严重,许多国家制定了限量标准来控制食品中该污染物的含量,食品中氯丙醇的残留量仅限于酸水解蛋白调味品,而食用油脂中氯丙醇的残留量并没有限量规定。目前,食用油脂中3-MCPD酯的检测方法分为间接法和直接法。间接法指将各3-氯丙醇酯(sn-1,3-氯丙醇单酯、sn-2,3-氯丙醇单酯和3-氯丙醇双酯)通过酯交换反应转化为游离态的3-MCPD,且该方法已经被广泛应用。直接法为不破坏3-MCPD酯的结构而直接检测其含量,目前多数是采用固相萃取柱净化、色谱分离质谱检测。两种分析方法都有自己的不足之处,间接法只能测定油脂中3-MCPD酯的交换产物3-MCPD的总量,不能区分油脂中原有的3-MCPD酯是单酯还是双酯,且间接法中的碱水解法会使得3-MCPD和缩水甘油互相转化,而酸水解法酯交换时间需16h,比较耗时。直接法测定需要通过高分辨率质谱仪,仪器价格昂贵,且需要各种3-MCPD酯的标准品,检测成本高。 2017年欧盟发布了食品中缩水甘油酯(GE酯)的限量要求,具体内容如下:面向消费者上市销售或用于普通食品配料的植物油脂(除婴幼儿食品和加工谷物制品)最大残留量为1000 μg/kg;用作婴幼儿食品和加工谷物制品的植物油脂配料最大残留量为500 μg/kg;而婴儿配方、较大婴儿配方和婴幼儿特殊医学用途配方食品分为粉体和液体两种形式,最大残留量分别为75 μg/kg和10 μg/kg(2019年6月30日前),50μg/kg和6.0 μg/kg(2019年7月1日后)。但是目前并没有相应的方法标准能够将缩水甘油酯的检测限降到欧盟的限量要求,因此,建立低含量缩水甘油酯检测方法至关重要。
目的:建立一个[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]条件同时分离测定环孢素A中乙醇及丙二醇的含量。方法:以GDX-101为固定相,柱长为2 m,进样口温度为210 ℃,检测器为280 ℃,柱温采用程序升温,氮气为载气,以二甲基亚砜为溶剂,以正丙醇为内标。结果:乙醇及丙二醇进样量分别在2.0~6.0 μg,1.0~3.0 μg,其峰面积与浓度呈良好的线性关系,加样回收率分别为99.9%(RSD<0.8%,n=5),101.4%(RSD<1.1%,n=5),精密度良好。结论:此[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]条件可同时测定环孢素A中乙醇及丙二醇的含量,方法简便准确。关键词 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法 乙醇 丙二醇 环孢素A山地明(环孢素A)为诺华制药有限公司的产品,是一种免疫抑制剂,用于器官移植和骨髓移植中的抑制排斥现象以及自身免疫疾病。厂方质量标准中乙醇及丙二醇的含量采用石英毛细管柱测定,此种色谱柱在国内使用不普及,我们经多次试验,摸索出一较好的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]条件,适用于国内检测,即以GDX-101为固定相,柱长为2 m,采用氢离子火焰检测器,进样口温度为210 ℃,检测器为280 ℃,柱温采用程序升温,氮气为载气,以二甲基亚砜为溶剂,以正丙醇为内标,可同时分离测定环孢素A中乙醇及丙二醇的含量,改进后的方法,乙醇与正丙醇的分离度为3.1,丙二醇与正丙醇的分离度为5.0,符合中国药典1995年版中乙醇量度检查的分离度要求[1],操作简便,结果准确可靠。1 仪器与试药 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]:SP-6890 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]柱:玻璃柱,长2 m,固定相为GDX-101。 乙醇、异丙醇、丙二醇均为[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]纯,二甲基亚砜为色谱纯。 样品:环孢素A胶囊(山地明),由诺华公司提供,批号为187MFD0797;241MFD0797;166MFD0797;483MFD0797;477MFD0797。 标准贮备液及内标贮备液:精密称取[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]级的乙醇及丙二醇2.50及1.25 g分置50 mL容量瓶中,加二甲基亚砜至刻度,摇匀,作为标准贮备液;精密量取正丙醇5.0 mL置50 mL量瓶中,加二甲基亚砜至刻度,摇匀,作为内标贮备液。2 试验方法与结果2.1 色谱条件 采用GDX-101为固定相,柱长为2 m,氮气为载气,采用氢离子火焰检测器,进样口温度为210 ℃,检测器为280 ℃,柱温采用程序升温,即初始为165 ℃,保持12 min,以40 ℃。min-1升至280 ℃,并保持20 min,检测器温度为280 ℃,进样量为2 μL。2.2 分离度试验 称取乙醇、丙二醇及正丙醇各50 mg置同一50 mL量瓶中,加二甲基亚砜至刻度,摇匀,进样2 μL,按上述色谱条件试验,记录色谱图,见图1-A,乙醇、丙二醇及正丙醇的保留时间分别为1.15,2.22,7.54 min,计算乙醇与正丙醇及丙二醇与正丙醇的分离度,其分离度分别为3.1和5.0。图1 分离度色谱(A)及样品测定(B)色谱图1.乙醇 2.正丙醇 3.丙二醇 4.二甲基亚砜2.3 线性范围及标准曲线 分别精密量取乙醇和丙二醇标准贮备液1.0,1.5,2.0,2.5,3.0 mL,分别置50 mL量瓶中,并分别加入内标贮备液1.0 mL,使乙醇终浓度为1.0,1.5,2.0,2.5,3.0 mg.mL-1,丙二醇的终浓度为0.5,0.75,1.0,1.25,1.5 mg.mL-1,分别进样2 μL,以乙醇及丙二醇的进样量为横坐标,以它们的峰面积与内标峰面积之比为纵坐标,分别进行线性回归,结果线性关系良好,乙醇、丙二醇回归方程分别为:A=8.935×103C+7.858×102 r=0.998 8A=8.086×103C-1.649×102 r=0.999 92.4 精密度试验 用乙醇与丙二醇浓度分别2.0及1.0 mg.mL-1的溶液,重复进样5次,结果乙醇与丙二醇的RSD分别为0.7%和1.0%,精密度良好。2.5 回收率试验 采用加样回收法,取已知乙醇与丙二醇含量的样品2粒,用二甲基亚砜溶解,置50 mL量瓶中,精密加入内标贮备液1.0 mL,并加二甲基亚砜至刻度,摇匀,精密量取此溶液4.0,4.5,5.0,5.5,6.0 mL,分别加入乙醇与丙二醇的浓度分别为2.0 mg.mL-1及1.0 mg.mL-1的标准溶液6.0,5.5,5.0,4.5,4.0 mL,混匀,量取混匀后的溶液2 μL,注入[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url],测定这5份溶液的乙醇和丙二醇含量,计算回收率,乙醇的平均回收率为99.9%(RSD<0.8%,n=5),丙二醇的平均回收率为101.4%(RSD<1.1%,n=5)。2.6 样品的测定 取乙醇和丙二醇标准贮备液2.0 mL,内标贮备液1.0 mL,并加二甲基亚砜至刻度,摇匀,作为对照品溶液;取环孢素A胶囊2粒,置50 mL量瓶中,用二甲基亚砜溶解,精密加入内标贮备液1.0 mL,并加二甲基亚砜至刻度,摇匀,作为样品溶液;分别量取对照品溶液和样品溶液各2 μL,注入[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url],按上述色谱条件测定,以内标法计算含量,即得;见图1-B。2.7 对比试验结果 取环孢素A样品5批,用改进后的方法测定样品中乙醇和丙二醇的含量,与厂方测定数据相比,结果基本吻合,见表1。表1 乙醇和丙二醇对比试验结果(%) 批号 本法结果 厂方测定数据 乙醇 丙二醇 乙醇 丙二醇 187MFD0797 101.0 106.3 100.5 105.0 241MFD0797 99.2 99.2 100.6 100.6 166MFD0797 101.7 102.7 101.3 103.0 483MFD0797 98.8 96.8 99.3 97.2 477MFD0797 99.1 98.1 98.9 97.7 3 讨论3.1 本法与原厂方方法相比,方法更为简便,条件普及,有利于对样品质量的控制。3.2 原厂方标准在测定乙醇含量时,以正丁醇为溶剂,由于正丁醇的保留时间与丙二醇过于接近,分离度达不到要求,本法采用二甲基亚砜为溶剂,不影响样品的溶解,同时使丙二醇与二甲基亚砜的分离度符合定量分析的要求。3.3 曾用固定相为GDX-401的[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]柱进行检测,乙醇与正丙醇得到完全分离,但丙二醇与溶剂峰重叠,分离度达不到要求。3.4 采用程序升温,可使溶剂出峰时间加快,缩短分析时间。王俊秋(北京市药品检验所 北京 100035)庞青云(北京市药品检验所 北京 100035)余立(北京市药品检验所 北京 100035)参考文献1,中国药典.1995.二部:附录44
最近接了一个环评单子,检测要求为,监测一次最大值异丙醇,这个应该采样频次为多少
请教各位谁知道哪里能买到棉酚标准品和3-氨基-1-丙醇?谢谢!急用
各位: 一月初有一个风险监测的比对,要求做食品中的氯丙醇,大家有参加比对的么?能不能交流一下。
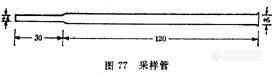
空气中二氯丙醇的测定方法 变色酸比色法 1 原理二氯丙醇水解后,经高碘酸氧化生成甲醛。甲醛与变色酸作用生成紫色化合物,比色定量。2 仪器2.1 采样管(图77)。2.2 抽气机。2.3 流量计,0~1L/min。2.4 具塞比色管,25ml,10ml。2.5 分光光度计。3 试剂3.1 硅胶:40~60目硅胶,用混合酸(硫酸与硝酸等体积混合)在沸水浴上回流加热处理2h。水洗至中性,在110℃干燥4h,然后在200℃活化4h,贮于干燥器内备用。[img]http://ng1.17img.cn/bbsfiles/images/2007/05/200705201424_52378_1625938_3.jpg[/img]3.2 碳酸钠(Na2CO3)溶液,10g/L。3.3 高碘酸钾溶液,15g/L:称取1.5g高碘酸钾,溶于100ml3+2硫酸中。3.4 亚硫酸钠溶液,100g/L。3.5 硫酸,?20=1.84g/ml。3.6 变色酸溶液,20g/L。临用前配制。3.7 标准溶液:于25ml量瓶中加入约10ml碳酸钠溶液(3.2),准确称量,滴入2滴二氯丙醇,再准确称量,两次称量之差即二氯丙醇的质量,加碳酸钠溶液(3.2)至刻度,充分混合,计算1ml溶液中二氯丙醇的含量。临用前用碳酸钠溶液(3.2)稀释成50?g/ml二氯丙醇标准溶液。4 采样于采样管中先投入一个玻璃珠,使其恰好堵在采样管的下端狭窄部位,然后装入3g硅胶,以0.5L/min的速度抽取5L空气(采样管始终保持垂直位置)。5 分析步骤5.1 对照试验:同采样,于采样管中装入硅胶带至现场,但不抽取空气,照样品分析。5.2 样品处理:将采样管中的硅胶移入25ml比色管中,加10ml碳酸钠溶液(3.2),盖上磨口塞(不要塞严),放在沸水浴中加热90min,放冷,取2ml上清液于10ml比色管中。5.3 标准曲线的绘制:按表71配制标准管。向标准管中各加入0.2ml高碘酸钾溶液(3.2),混匀,放置30min,加入0.2ml亚硫酸钠溶液(3.4),振摇(此时溶液应为无色,如残有黄色可再补加一滴亚硫酸钠溶液),沿管壁徐徐加入3ml硫酸(3.5)及0.6ml变色酸溶液(3.6),混匀,放在沸水浴中加热20min,放冷,加水稀释至10ml,混匀,于波长570nm下比色。以二氯丙醇含量对吸光度作图,绘制标准曲线。5.4 测定:样品管操作同标准管,以现场对照管调仪器零点比色。由标准曲线上查出二氯丙醇的含量。6 计算表71 二氯丙醇标准管的配制[img]http://ng1.17img.cn/bbsfiles/images/2007/05/200705201425_52379_1625938_3.jpg[/img]X=5C/V0式中:X——空气中二氯丙醇的浓度,mg/m3;C——所取样品溶液中二氯丙醇含量,微克;V0——标准状况下的样品体积,L。7 说明7.1 本法检测限为1微克/2ml。二氯丙醇浓度为1.5、10、20微克/2ml时,变异系数分别为1.4%、2.6%、2.3%。7.2 采样速度为0.5~1.0L/min时,硅胶对二氯丙醇的采样效率接近100%。