求助,关于银杏叶提取物的总银杏酸含量测定。请问各位有没有做过的,我怎么做了几次都做不出来呢。条件都是按照药典要求做的,对照品都不出峰。我都要疯了。有谁做过帮忙分析一下或者上传一张图谱,谢谢。
各位大神,请教一下用高效液相做欧前胡素的阴性对照,然后在和欧前胡素对照品溶液出峰时间差半分钟地方出现一个峰,请问各位老师这算阴性有干扰么?
大家在做总银杏叶酸时,如何称取对照品A和B的,图谱里有几个峰呢?多长时间出?用的什么色谱柱呢?问题有点多,希望有兴趣的来讨论下
[color=#333333]HPLC法在做欧前胡素的阴性对照,然后在和欧前胡素对照品溶液出峰时间差半分钟地方出现一个峰,请问各位老师这算有干扰么?[/color]
硝酸铝显色法测银杏提取物总黄酮含量,以芦丁为对照,紫外波长扫描结果显示芦丁对照品在500nm左右有最大吸收峰,而供试品在400-600nm范围内均无最大吸收峰,而是呈上升趋势。特此求助,谢谢!
大肠埃希氏菌在KF上不生长,作为阴性对照他后续可以不用做么?还是需要用适宜培养基培养后后续实验用。
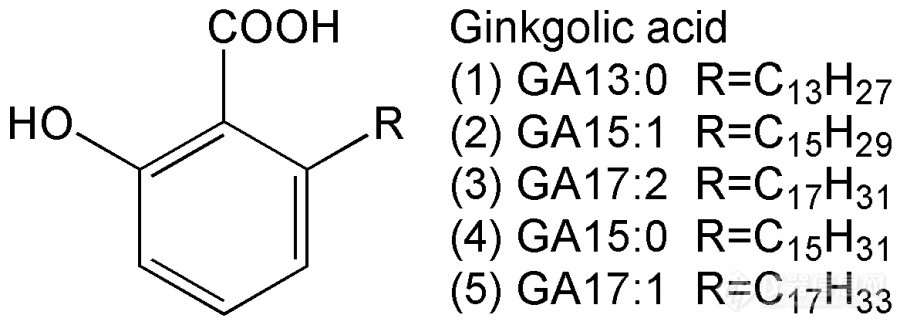
[b]1 引言[/b] 银杏叶提取物是目前临床广泛应用的天然产物药。西方学术界对该药物的成分和疗效也广泛接受。目前银杏叶提取物执行的标准基本上都源自德国EGB-761,其中除规定有效成分含量外,还对银杏酸含量进行了限定。按欧盟药典【European Pharmacopoeia 8.0.Monograph: Ginkgo dry extract. Refined and quantified. [b]2008[/b]】、美国药典【United States Pharmacopeia.Thirty-seventh Revision: Powdered Ginkgo Extract. [b]2015[/b].】要求,总银杏酸含量不得超过5 mg/Kg。我国执行的标准略为宽松,2015版药典【中华人民共和国药典[b]2015[/b], 一部:416-417页】规定总银杏酸含量不得超过10 mg/Kg。.[img=,690,248]http://ng1.17img.cn/bbsfiles/images/2018/07/201807292217347240_855_2204387_3.jpg!w690x248.jpg[/img][b]图1银杏酸的结构式.[/b] 银杏酸的分子结构如图1其中GA13:0、GA15:1、GA17:2是药典规定需要检测的项目。银杏酸的色谱分离并无难点,但是要测定银杏叶提取物中的银杏酸却存在两方面的问题:一是银杏酸限量很低,几乎接近仪器检出限;二是体系中共存的黄酮、内酯、糖类、蛋白质等成分复杂,基体干扰严重。目前通行的检测方法有欧盟药典法、中国药典旧版(2010版)方法、中国药典2015版方法,对比见表1。[img=,690,306]http://ng1.17img.cn/bbsfiles/images/2018/07/201807292218248285_199_2204387_3.png!w690x306.jpg[/img] 色谱分离方面,各种方法均采用反相色谱,条件略有差异,但无本质不同。提取方面,欧盟药典采用甲醇溶剂,提取较为完全,但共存的大量极性组分也一起提取进入溶液中,形成严重的基体干扰。而我国2010版药典方法采用石油醚提取,极性组分溶解少、干扰有所降低,但石油醚对极性试样的浸润性和渗透性不好,提取不完全,因此出现结果偏低的现象。相关研究人员【姚建标, 等.药物分析杂志, [b]2015[/b], 35 (11): 2041-2044.】借鉴了欧盟药典的提取方法提出了2015版药典方法,但是将试样量从0.5g增加到2g。增加样品量是为了弥补检测灵敏度的不足,因为2015版药典方法采用的紫外检测波长为310nm,这一波长下银杏酸的吸收强约为210nm下的五分之一。当然,在310nm下共存杂质的吸收更小、色谱基线漂移的问题也有所缓解,但是取样量增大使得更多的基体杂质进入色谱柱,基体干扰问题有增无减。. 众所周知,通过液液萃取、固相萃取等前处理手段可以起到减少基体干扰、富集目标物的作用,相关研究也有一定报道【Stefan U, Iuliana D S, Victor D,Andrei M. [i]J. Liq. Chromatogr. R. T.[/i], [b]2010[/b], 33 (1): 133-149. Ji W, Ma X, XieH, Chen L, Wang X, Zhao H, Huang L. [i]J.Chromatogr. A[/i], [b]2014[/b], 1368 (1):44-51.】。但是这些前处理过程较为繁琐,不利于推广。也有通过超高效液相色谱-串联质谱方法进行银杏叶提取物中银杏酸的检测【孙健, 等. 色谱, [b]2016[/b], 34 (2): 184-188.】,灵敏度和基体干扰问题都能较好的解决,但仪器昂贵,也难以推广。.[b] 本课题组在进行银杏活性成分提取研究的过程中也遇到了上述测试问题。为了改进现有方法,我们将简便有效的“分散液液微萃取”方法应用到样品的前处理过程中,有效解决了基体干扰问题,灵敏度也显著提高,同时该前处理方法十分简便,样品和试剂的用量也很少。相关研究前沿和创新内容已经撰文投稿,现将较为基础的实验方法介绍如下。[/b].[b]2 实验方法2.1 仪器与试剂[/b] 大连依利特230型高效液相色谱仪,安捷伦HC-C18(4.6*150 mm,5 μm)色谱柱。 色谱纯甲醇、乙腈为上海国药产,纯水为石英亚沸蒸馏。萃取剂为ACS级三氯乙烯,其余试剂为分析纯。 银杏叶提取物试样购于湖北某公司,相关制剂为市售药品(天保宁、金纳多)。 混合银杏酸标准品购于武汉某公司,总含量不低于99%,其中GA13:1占10.1%,GA15:1占50.5%,GA17:1占34.7%,GA17:2占1.7%,GA15:0占3.0%。用甲醇溶解配置成总银杏酸浓度为1.000 g/L的标准储备液,4℃保存。使用时用甲醇稀释成所需浓度的工作标液。.[b]2.2 实验方法 a)提取 准确称取0.5 g试样,加10 mL甲醇,常温超声提取10 min,冷却后定容、摇匀。 上述溶液用微孔滤膜过滤,收集滤液。 b)萃取 取上述滤液3.00 mL移入尖底离心管中,加入萃取剂三氯乙烯0.150 mL混匀,此时不分层。 加入水溶液(含10%无水硫酸钠 + 0.2%三氟乙酸)7.00 mL,加塞、摇匀,此时应得到浑浊液。 4000转离心3min,三氯乙烯萃取剂沉到底层。 c)取样 用注射器吸取三氯乙烯层0.100 mL移入样品瓶,氮气吹干,加0.100mL甲醇溶解。 d)色谱测定 条件见2.3。.2.3 色谱条件[/b] 采用Agilent HC-C18(4.6*150mm,5μm)色谱柱,甲醇-水-三氟乙酸体系(体积比92:8:0.1)为流动相,流速1.00mL/min,检测波长242nm,进样量50.0μL。.[b]2.4 定量分析[/b] 银杏酸工作标液直接进样测定,建立工作曲线,外标法定量。计算待测样时需乘以萃取的富集因子。富集因子为20。.[b]3 实验结果3.1 色谱图[/b] 银杏酸标样、银杏叶提取物试样、试样加标的色谱图见图2,分离效果较好,基线平直、基体干扰小。[img=,690,642]http://ng1.17img.cn/bbsfiles/images/2018/07/201807292222523305_3418_2204387_3.jpg!w690x642.jpg[/img].[b]3.2 方法验证[/b] 将银杏酸的甲醇标液按试样同样方法萃取和检测,考察了方法的重现性、线性范围、定量限(按S/N=10计算),测定了萃取过程的萃取率和富集因子,结果见表2。方法重现性2.9% ~4.8%。方法定量限0.007 ~ 0.020 mg/L,测定上限为5.00 mg/L。按取样0.5g定容至10mL计算,对试样的定量限为0.14 ~0.40 mg/Kg,对试样的测定上限为100 mg/Kg。 萃取率达到95.4% ~98.3%,富集因子达到19.1 ~19.7。[img=,690,231]http://ng1.17img.cn/bbsfiles/images/2018/07/201807292224269505_3788_2204387_3.png!w690x231.jpg[/img][b]3.3 样品测定[/b] 银杏叶提取物试样的测定结果见表3,进行了加标回收实验(总银杏酸加标量为5.00mg/Kg),加标回收率94.0% ~ 100.8%。以欧盟药典方法进行对照试验,结果与本方法一致。药品制剂试样的测定结果见表4,同样进行了加标回收实验和对照实验,结果也较好。[img=,690,306]http://ng1.17img.cn/bbsfiles/images/2018/07/201807292225141669_6540_2204387_3.png!w690x306.jpg[/img][img=,690,312]http://ng1.17img.cn/bbsfiles/images/2018/07/201807292225188364_2915_2204387_3.png!w690x312.jpg[/img].[b]4 相关讨论[/b] (1)试样体积与萃取剂体积之比影响萃取率和富集因子。此比值大时富集因子高但萃取率明显低于100%。反之则导致萃取率接近100%但富集因子很低。本方法选择3.00 mL试样加0.150 mL萃取剂,是兼顾两个方面考虑的结果。此时萃取率达到95.4% ~98.3%,接近100%。富集因子达到19.1 ~19.7,接近体积比计算结果,因此在定量计算时近似认为富集因子为20。 (2)萃取剂要选择低沸点、高密度、弱极性、难溶于水的有机溶剂,符合条件的主要是卤代烃。对比表明三氯乙烯效果最好。 (3)试样溶剂为甲醇,与萃取剂能够互溶,不能分成两相。但加入适量水之后可以实现分层。极性强的基质进入水相,从而使干扰减小。极性弱的银杏酸进入三氯乙烯层实现富集。水中加入10%硫酸钠起盐析作用,加0.2%三氟乙酸可以抑制银杏酸电离,都有利于提高萃取率。不加时萃取率显著降低。 (4)萃取过程形成浑浊的乳状液,两相接触面积大,因此很快达到平衡。加水溶液后震荡30秒到1min即可。萃取时间对结果几乎不影响。 (5)萃取在室温下进行,温度变化对结果影响不大。 (6)银杏酸的紫外吸收有3个特征峰,分别为210 nm、242 nm、310 nm。使用210 nm虽然灵敏度高,但干扰大。本方法使用242 nm检测,实际信噪比高于210 nm。使用310 nm检测的信噪比略有降低。 (7)由于萃取减少了基体干扰、实现了富集,本方法使用等度洗脱进行色谱分离也能获得很好的效果,并且没有基线漂移。本方法灵敏度也显著由于药典方法,定量限达到0.14 ~0.40 mg/Kg,而药典方法的检出限为0.5 mg/Kg。.[b]5 结论[/b] 采用“分散液液微萃取”方法对银杏叶提取物样品进行前处理,具有简单快捷的优点,同时减少基体干扰、实现富集的效果较好,能有效提高信噪比,降低检出限和定量限。方法准确可靠,易于推广。
阴性对照对比中,如果样品的包衣含有干扰,能算该方法行不通吗?
请问是否能检测银杏叶提取物中银杏酸的含量?
正在测牛奶中抗生素的含量,不知如何做阴性对照啊???从市场上买了不同品牌的奶粉和液态奶,但是空白对照怎么确定呢?需要版友们帮忙。谢谢!
[color=black][size=3][font=宋体]银杏酸[/font][/size][/color][color=black][size=3][font='Times New Roman']A[/font][/size][/color][color=black][size=3][font=宋体]中有[/font][/size][/color][color=black][size=3][font='Times New Roman']2[/font][/size][/color][color=black][size=3][font=宋体]个峰,银杏酸[/font][/size][/color][color=black][size=3][font='Times New Roman']B[/font][/size][/color][color=black][size=3][font=宋体]中有[/font][/size][/color][color=black][size=3][font='Times New Roman']3[/font][/size][/color][color=black][size=3][font=宋体]个峰,用于峰的定位。但银杏酸的含量很低(1ppm),所以还是很难判定各峰的位置,望各位大侠指点,能传上谱图的话更好,谢谢了![/font][/size][/color]
我们做的原料药的细菌内毒素的供试品阳性对照怎么老是阴性?该如何去除干扰呢?http://simg.instrument.com.cn/bbs/images/brow/em09512.gif
标准是HJ347.2-2018 多管发酵法阴性对照用的产气肠杆菌初发酵用乳糖蛋白胨15管复发酵是EC肉汤求问阴性对照实验中初发酵和复发酵分别是什么现象?我做出来初发酵产酸产气,复发酵不产酸不产气是否正常
在制定中药制剂的标准中,鉴别、含量测定都必须作阴性对照,各位战友谈谈阴性对照样品通常要求是什么?最终产品?或可以是压片装胶囊之前的颗粒粉末,抑或是所有提取步骤完成后的产品?通常是企业提供?或是也有为做标准自己制备的?
RT目前开展的阪崎肠杆菌pcr实验,看到出入境的标准是用大肠杆菌作为阴性对照,但我不太明白他们为什么要用大肠杆菌作为阴性对照?原则是什么?我们还有金黄色葡萄球菌、沙门氏菌这些需要做PCR,同样不知道选择哪一种菌作为阴性对照???谢谢各位~~~
流动相是乙腈水8比2,对照品的溶剂是甲醇( 标样不溶乙腈 ),检测波长208。用的是新的C18色谱柱,默克的乙腈请问:阴性对照是进一针什么?流动相?纯的乙腈?纯的甲醇?试过进一针流动相,出了2个峰,再进一针标准品,也出了2个峰,且与流动相出的2个峰重叠,并随进样体积增而增大。如果是溶剂峰,是不是不管进样体积如何变化,是不是都是 一样的?
接连两天,国家食品药品监督管理总局发布关于银杏叶药品违规生产情况。昨日,国家食药监总局表示,对于桂林兴达药业和万邦德(湖南)天然药物有限公司违规生产银杏叶产品一事,广西、湖南两省区要迅速查明产品销售流向。更值得关注的是,包括云南白药集团、河北省涿州东乐制药有限公司等24家药品生产企业,因从桂林兴达药业有限公司购买银杏叶提取物而受到波及,目前也在接受药监部门的核查。 根据国家食药监总局消息,桂林兴达药业有限公司擅自更改银杏叶提取生产工艺,同时从不具备资质的企业购进以盐酸工艺生产的银杏叶提取物,用于生产银杏叶片,并将外购的提取物销售给其他的药品生产企业,伪造原料购进台账和生产检验记录。而万邦德(湖南)天然药物有限公司用购进的银杏叶提取物生产银杏叶片和银杏叶胶囊等制剂,伪造原料购进台账和生产检验记录。食品药品监管部门已对其立案调查。 公开资料显示,银杏叶制剂临床多用于治疗心、脑血管疾病,如冠心病心绞痛、脑血管痉挛、脑供血不全、记忆力衰退等。“此次查处的桂林兴达药业,用盐酸工艺生产银杏叶提取物会分解药品有效成分,影响药品疗效,进而对使用者造成不利影响。”国家食药监总局相关负责人称。 同时,经查包括云南白药集团中药资源公司、黑龙江天宏药业股份有限公司以及河北省涿州东乐制药有限公司等24家药品生产企业,从桂林兴达药业有限公司购买非法银杏叶提取物。药监部门表示,上述公司凡使用盐酸工艺银杏叶提取物生产银杏叶制剂的,必须按通告要求立即采取停售、召回等措施,并向有关省(区、市)食品药品监管部门通报产品销售流向,抄报总局。 国家食药监总局还警示,根据市场监测,还有部分企业存在改变工艺违法生产银杏叶提取物的行为,故要求所有银杏叶提取物和银杏叶制剂生产企业立即开展自查。 土豆点评:那么,问题来了,现在监管部门对中药饮片、中药中间体(提取物)的监管越来越严格了,中药厂家如何应对?以后中药制剂会不会涨价?一堆小饮片企业会不会就此倒闭呢?
请问有没有权威部门检测银杏叶提取物中银杏酸的含量?在哪里检测?谢谢!
我公司生产一保健品含有银杏叶提取物、沙棘提取物等多种含黄酮类物质,请问如何测定此保健品的总黄酮含量?? 用液相以槲皮素做对照品还是用紫外以卢丁做对照品测定呢?? 或有更好的办法? [em40] [em43] [em46]

银杏酮酯中萜类内酯的含量测定方法学试验(新手上路) 根据相关文献资料,银杏酮酯中的萜类内酯含量测定方法主要有薄层扫描法、高效液相色谱法、差示检测法、ELSD法等。萜类内酯在紫外吸收较弱,极少量的黄酮杂质能严重干扰测定,紫外检测器检测较为困难,示差检测器灵敏度、稳定性和选择性相对较差。参照中国药典2005年版一部及目前大多数国家标准中多采用ELSD法测定萜类内酯的含量。方法学研究内容如下:1.主要仪器与试药SPD-10AP输液泵(日本岛津公司);ELSD2000蒸发光散射检测器(美国奥泰Alltech);SK3300H型超声清洗器(上海科导KUDOS);乙腈(色谱纯);四腈呋喃(色谱纯);水(重蒸水);其它试剂均为分析纯。银杏内酯A对照品、银杏内酯B、银杏内酯C及白果内酯(中国药品生物制品检定所提供)。2.对照品溶液的制备取在五氧化二磷干燥减压干燥器中放置过夜的白果内酯、银杏内酯A、银杏内酯B、银杏内酯C对照品分别约为5.0mg、5.0mg、3.0mg和2.0mg,精密称定,置同一10ml量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得(每1ml中含白果内酯、银杏内酯A、银杏内酯B、银杏内酯C分别为0.5mg/ml、0.5mg/ml、0.3mg/ml和0.2mg/ml)。3.试验条件的选择(1) 仪器条件流速:1.0ml.min-1,柱温:35℃,漂移管温度:115℃,氮气流速:3.0L/min。(2) 流动相的选择先后比较了正丙醇-四氢呋喃-水(1:15:84)、乙腈-四氢呋喃-水(1:1:6)、乙腈-四氢呋喃-水(11:11:78)。结果以乙腈-四氢呋喃-水([font=Times
各位老师: 请问,采用内标法进行色谱质谱分析时,空白(阴性)对照样品该不该加入内标?有的认为,空白样品不加内标,完全空白;也有人认为空白对照样应加入内标,请教各位,到底那个正确?
粪大肠菌群347.2 2018中阴性和阳性对照的意义是什么?验证的是培养基吗?为什么要做阴阳性对照实验?阴性对照的现象是什么呢?求解答
请教 :我们现在在做银杏内酯的含量测定方法学,做到进样精密度度时用的是供试品溶液,结果RSD很大有5%-9%,但是用对照品溶液做精密度RSD就小好多在2%以下,用的是蒸发光散射检测器,漂移管温度80度,流速2.2 流动相是正丙醇:四氢呋喃:水=1:15:84 安捷伦色谱柱C18 请教高手帮忙 补充我们的样品是复方制剂,样品处理是参照药典方法银杏提取物中的方法
《水和废水监测分析方法》四版中的“水中的细菌学测定”有提到要对培养基进行“阳性和阴性对照培养检查试验”,举个例子(摘自:表 5-2-4): 对照培养细菌类别 阳性 阴性粪大肠菌类 大肠埃希氏菌 产气肠杆菌是不是说要在培养基中分别加入大肠埃希氏菌和产气肠杆菌,看它们是否分别呈现阳性和阴性反应,如果阳性和阴性反应都符合要求的话培养基就合格?大家讨论一下,谢谢!
如题:怎样理解检测时必须设立阴性和阳性添加对照组? 具体应该怎样操作?请求各位大佬指教!!
又有一家知名医药企业中枪“银杏叶事件”,食药总局近日通报哈药集团制药总厂使用了违法银杏叶提取物生产保健食品。 此前,食药总局公告称,大连珍奥集团、汤臣倍健、无限极有限公司、如新(中国)有限公司等21家保健食品企业从桂林兴达药业、宁波立华制药购进银杏叶提取物。 “哈药集团制药总厂使用不合格银杏叶提取物生产了哈药牌银杏叶软胶囊,企业自检2批次产品,经检验均为质量存在问题产品。该企业共购进不合格原料2350公斤,封存1688.85公斤,其余661.15公斤已使用。企业已对质量存在问题产品采取控制措施,截至目前,已封存下架质量存在问题产品5203.01公斤,并启动召回。”食药总局通告中指出,不合格银杏叶提取物原料涉及8家保健食品企业中,其中哈药集团用量是最大的。 据悉,全国目前157家企业使用银杏叶提取物生产保健食品,不合格银杏叶提取物原料涉及8家保健食品企业:大连双迪科技股份有限公司、江苏省庆缘康生物科技有限公司、珠海联邦制药股份有限公司中山分公司、哈药集团制药总厂、杭州太和健康食品有限公司、浙江省磐安县外贸药业有限公司、山东圣海保健品有限公司、会心堂(北京)生物科技有限公司沈阳分公司。 记者致电哈药股份相关人士,但电话一直无人接听。哈药股份在公告中指出,子公司制药总厂生产的银杏叶软胶囊为保健食品,该产品生产所使用的原料银杏叶提取物供应商为徐州恒凯银杏制品有限公司,该公司具有相应生产资质。哈药总厂立即组织专项小组对银杏叶软胶囊产品的供应商资质的合法性、供应商审计流程、采购流程、物料进厂检测环节、生产使用环节及成品放行环节主动开展自检自查。经企业自查,哈药总厂银杏叶软胶囊生产组织过程符合工艺要求,原料购入、产品生产、质量控制环节无违法违规行为,公司产品各项指标符合国家标准。 “6月4日,国家食药监局总局公布银杏叶药品补充检验方法后,哈药总厂立即依照补充检验方法组织了银杏叶软胶囊的对照自检自查,发现企业自2014年1月1日以来生产的57批次产品不符合补充检验标准。目前,哈药总厂已对现有库存产品和原料进行了封存,并启动了银杏叶软胶囊产品的召回措施。”哈药股份说,2014年至今,哈药总厂银杏叶软胶囊产品销售收入为705.7万元。

[b][i]银杏叶提取物[/i][/b][align=center][b][img=,600,374]https://ng1.17img.cn/bbsfiles/images/2019/09/201909160940162933_9995_932_3.jpg!w600x374.jpg[/img][/b][/align]银杏叶提取物(Ginko Biloba Extract,GBE)是以银杏Ginkgo biloba L.的叶为原料,采用适当的溶剂,提取的有效成分富集的一类产品。以GBE为原料制成的各种制剂,广泛应用于药物、保健品、食品添加剂、功能性饮料、化妆品等领域。该产品是现代科学技术开发出的植物药(属中药)最成功的案例之一。我们今天来做的就是银杏叶提取物的测定,我们一起来看具体的实验步骤吧。[b]色谱条件[/b]色谱柱:月旭Ultimate LP-C18(4.6×250mm,5μm)。流动相: [table=511][tr][td=1,1,165]时间[/td][td=1,1,136]0.4%磷酸水[/td][td=1,1,210]乙腈[/td][/tr][tr][td=1,1,165]0[/td][td=1,1,136]85[/td][td=1,1,210]15[/td][/tr][tr][td=1,1,165]8[/td][td=1,1,136]85[/td][td=1,1,210]15[/td][/tr][tr][td=1,1,165]17[/td][td=1,1,136]83[/td][td=1,1,210]17[/td][/tr][tr][td=1,1,165]25[/td][td=1,1,136]83[/td][td=1,1,210]17[/td][/tr][tr][td=1,1,165]34[/td][td=1,1,136]80[/td][td=1,1,210]20[/td][/tr][tr][td=1,1,165]40[/td][td=1,1,136]80[/td][td=1,1,210]20[/td][/tr][tr][td=1,1,165]70[/td][td=1,1,136]65[/td][td=1,1,210]35[/td][/tr][/table]检测波长:360nm;柱温:45℃;流速:1.0ml/min;进样量:10μL。[b]谱图和数据[/b][align=center][b][img=,600,246]https://ng1.17img.cn/bbsfiles/images/2019/09/201909160940472243_5261_932_3.jpg!w690x284.jpg[/img][/b][/align][color=#333333][/color][color=#333333]1、芦丁对照[/color][color=#333333][/color][align=center][color=#333333][b][img=,600,273]https://ng1.17img.cn/bbsfiles/images/2019/09/201909160940234893_9532_932_3.jpg!w690x315.jpg[/img][/b][/color][/align][align=center][color=#333333][color=#333333][b][img=,600,43]https://ng1.17img.cn/bbsfiles/images/2019/09/201909160940281633_8466_932_3.png!w690x50.jpg[/img][/b][/color][/color][/align][color=#333333][color=#333333][/color][/color][color=#333333][color=#333333]2、银杏叶对照提取物[/color][/color][color=#333333][color=#333333][/color][/color][align=center][color=#333333][color=#333333][b][img=,600,271]https://ng1.17img.cn/bbsfiles/images/2019/09/201909160940325803_3603_932_3.jpg!w690x312.jpg[/img][/b][/color][/color][/align][align=center][color=#333333][color=#333333][color=#333333][b][img=,600,261]https://ng1.17img.cn/bbsfiles/images/2019/09/201909160940405873_9300_932_3.jpg!w690x301.jpg[/img][/b][/color][/color][/color][/align][color=#333333][color=#333333][color=#333333][/color][/color][/color][color=#333333][color=#333333][color=#333333]3、征求意见稿中参考图谱[/color][/color][/color][color=#333333][color=#333333][color=#333333][/color][/color][/color][align=center][color=#333333][color=#333333][color=#333333][b][img=,600,246]https://ng1.17img.cn/bbsfiles/images/2019/09/201909160940472243_5261_932_3.jpg!w690x284.jpg[/img][/b][/color][/color][/color][/align][color=#333333][color=#333333][color=#333333][b]结论[/b][/color][/color][/color][color=#333333][color=#333333][color=#333333][b]月旭UltimateLP-C18(4.6×250mm,5μm),在该色谱条件下进行测定,可以达到检测需求,可用于此产品的检测。[/b][/color][/color][/color]
据说银杏叶中含有银杏酸是有毒的,请问怎么去除呢?
中成药的薄层色谱鉴别一定要有阴性对照么?没有可不可以?
拜托各位帮忙,有银杏酮,银杏酚,槐果碱,槐定碱,川楝素的仪器分析方法吗?请大家帮帮忙啊!先谢谢了!