如果我们的宇宙不是从无而生,而是一个以前存在的宇宙的再生版本的话,会怎么样呢?请看 Anil Ananthaswamy的调查:ABHAY ASHTEKAR一直记得他第一次看到宇宙反弹时的反应。“我大吃一惊。”他如此描述道。当时他正注视着一个宇宙反向运行到大爆炸的模拟。基本上,模拟宇宙表现出预期的行为,随着星系的会聚宇宙变得越来越小,密度越来越大。但是,这个宇宙没有到达大爆炸的“奇点”,而是发生了反弹并重新开始扩展。这究竟是什么回事?Ashtekar希望确认他看到的东西,于是他邀请他的同事们共同讨论这个结果足有六个月,最后在2006年发表了这个结果。循环宇宙基于一个叫做圈量子宇宙学(LQC)的理论,那能够阐明宇宙诞生时的情形——那些东西甚至连爱因斯坦的广义相对论也无能为力。我们的宇宙有可能是在前一个宇宙崩塌之后出现的这一观念,自2003年以来一直令物理学家们非常着迷。现在这一理论已经能够提供我们可以加以实验验证的预言了。如果真的得到验证的话,大爆炸将被大反弹取代,而我们将终于能够理解时空的量子结构。宇宙源自一个有无穷密度的点的观念,将被反复循环的宇宙观所取代,宇宙有可能经历无穷无尽的扩展与收缩,无始无终。LQC实际上是另一个叫做圈量子引力的理论的第一个实际应用,圈量子引力理论巧妙地结合了爱因斯坦的引力理论和量子力学。我们需要这样的理论来解答当微小体积经历极端重力时会怎么样的问题,例如,接近大爆炸时的情形。在20世纪80年代中期Ashtekar在量子力学框架下重写了广义相对论方程式。和理论物理学家Lee Smolin与Carlo Rovelli一起,Ashtekar展示了由重力场线的回路编织成的空间-时间结构。在缩小足够多倍数以后空间看上去是平滑而连续的,而凑近观察的话会发现空间表现为一个个独立的块,或者说是量子,大概是10-35平方米大小。2000年,当时在宾夕法尼亚州立大学柏克校园跟Ashtekar做博士后的Martin Bojowald采用圈量子重力理论建立了宇宙的一个简化模型。LQC从此诞生了。Bojowald的重要成就在于:不同于广义相对论,LQC对物理过程的描述不会在大爆炸那一点失效。
[font=宋体][font=宋体]无细胞蛋白表达是一种体外重组蛋白质表达技术也称为无细胞蛋白质合成技术([/font][font=Calibri]CFPS[/font][font=宋体]:[/font][font=Calibri]Cell-free protein synthesis[/font][font=宋体]),是指用含有蛋白合成必需的组分(核糖体,转运[/font][font=Calibri]RNA[/font][font=宋体],氨酰合成酶,启动[/font][font=Calibri]/[/font][font=宋体]延伸[/font][font=Calibri]/[/font][font=宋体]终止因子,三磷酸鸟苷,[/font][font=Calibri]ATP[/font][font=宋体],[/font][font=Calibri]Mg2+[/font][font=宋体]和[/font][font=Calibri]K+[/font][font=宋体])的细胞裂解物在体外进行蛋白合成。无细胞蛋白表达技术适用于制备各种类型的蛋白质,包括难表达蛋白质、毒性蛋白质、复杂蛋白质等。在药物研究、生物制造和生命科学等领域中得到广泛关注和应用,无论是研究、开发还是商业化应用过程。目前无细胞蛋白表达主要应用于药物研发领域,例如抗体制备和生物药物生产等。随着人工智能技术的不断发展,无细胞蛋白表达技术可以与人工智能算法结合,构建计算机辅助的高通量生产系统,实现个性化、精准的生物医学治疗。除此之外,还能够应用于其他领域,例如基因工程、环境保护和农业生产等。随着无细胞蛋白表达技术的不断发展和人工智能技术的不断进步,我们可以看到更多的新领域和新应用出现,给生物科技行业带来更多的机遇和挑战。[/font][/font][font=宋体] [/font][font=宋体] [/font][b][font=宋体]相较于传统的活细胞蛋白表达技术,无细胞蛋白表达技术具有以下几个显著的优势:[/font][/b][font=宋体] [/font][font=宋体][font=Calibri]1. [/font][font=宋体]更高的蛋白质表达量:传统的活细胞蛋白表达技术受限于细胞本身的多方面因素,其表达的蛋白质数量往往受到限制。而无细胞蛋白表达技术通过在体外底物浓度高的环境中进行合成反应,不但避免了传统活细胞表达所面临的方方面面的限制,还能够很好地控制反应体系,从而获得表达量更高的蛋白质。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2. [/font][font=宋体]更快的表达速度:传统活细胞蛋白表达需要细胞生长并达到最佳密度才能进行蛋白质表达,这个过程往往需要数天时间。而无细胞蛋白表达技术通常只需要数小时就能够完成蛋白质的表达,这个速度明显快于传统活细胞表达技术。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]3. [/font][font=宋体]更精准的蛋白质合成:无细胞蛋白表达技术在体外进行蛋白质合成,能够精确控制底物浓度、反应温度、反应剂比例等参数,因此可以更加精准地合成定制的蛋白质,这对于研究和应用来讲具有重要意义。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]4. [/font][font=宋体]更灵活控制:在无细胞蛋白表达技术中,可以使用分离的组分体系进行蛋白质的合成,可以控制底物和反应剂的比例,也可以在适当的反应条件下进行自定义的修饰,如蛋白质标记、药效分析等。这些优点使得无细胞蛋白表达技术更加灵活、可控,适用于更广泛的应用领域。[/font][/font][font=宋体] [/font][b][font=宋体] [/font][font=宋体]无细胞蛋白表达应用[/font][/b][font=宋体] [/font][font=宋体]无细胞蛋白表达技术是一种飞速发展的新型生物技术,具有广阔的应用前景和潜力。该技术可以快速、高效、经济地合成蛋白质,可广泛应用于医疗、制药、农业、生物材料等多个领域。[/font][font=宋体] [/font][font=宋体][font=Calibri]1. [/font][font=宋体]医疗领域:无细胞蛋白表达技术在医疗领域应用广泛,可以用于生产多种蛋白质药品,如单克隆抗体等。其中,单克隆抗体是一种重要的治疗药物,具有高度特异性和亲和力,可用于肿瘤、心血管疾病、自身免疫性疾病等疾病的治疗。传统单克隆抗体生产方法需要花费大量时间和成本,而无细胞蛋白表达技术则可以在短时间内大规模合成单克隆抗体,从而大大缩短生产周期,并且可以降低成本。此外,无细胞蛋白表达技术也可以用于疫苗研发。比如疟疾疫苗研究开发昂贵又耗时,目前利用[/font][font=Calibri]WGE[/font][font=宋体]系统可加速疫苗研发,并建立高通量疟原虫抗体筛查系统。[/font][font=Calibri]Stark[/font][font=宋体]等利用大肠杆菌的便携式冻干裂解物再水化,[/font][font=Calibri]1h[/font][font=宋体]内合成高致病性病原体土拉弗朗西斯菌亚种的生物偶联疫苗,与工程菌生产的疫苗相比,其可引发更高水平的病原体特异性抗体。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2. [/font][font=宋体]制药领域:是无细胞蛋白表达技术的一个重要应用领域。药物开发的成功率取决于药物分子对目标蛋白的亲和力,而目标蛋白对于专一的细胞表达系统和分类的组织或器官非常敏感。通过无细胞蛋白表达技术,研究人员可以在不依赖于细胞的情况下直接生产大量需要的蛋白质,为药物研发提供了更快更便捷的方法。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]3. [/font][font=宋体]基础研究领域:利用无细胞蛋白质合成系统可以直接对表达产物进行核磁共振分析,目前已确定了数千个蛋白质的结构。可以通过合成蛋白质建立蛋白质阵列,解开基因产物的功能;应用核糖体展示和 [/font][font=Calibri]mRNA [/font][font=宋体]展示技术,更有利于实现高通量筛选,全面深入研究基因特征和功能。通过无细胞蛋白表达技术可以实现对大型蛋白质的生产和分析,同时也为基础研究打开了新的研究领域。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]目前义翘神州无细胞合成服务正在活动中,活动时间[/font][font=Calibri]2023[/font][font=宋体]年[/font][font=Calibri]10[/font][font=宋体]月[/font][font=Calibri]23[/font][font=宋体]日[/font][font=Calibri]-12[/font][font=宋体]月[/font][font=Calibri]31[/font][font=宋体]日。有需求的可以咨询或者进入义翘神州网进行查看。更多详情可以关注[/font][font=Calibri]https://cn.sinobiological.com/services/cell-free-protein-synthesis-service[/font][/font]
一 困惑与疑问 第二次世界大战已经结束将近60年了,那场战争给世界各国人民带来了深重的灾难,特别是反法西斯国家人民所付出的巨大代价。 但是,作为当时主要的法西斯国家的日本每当提到那场战争的时候,主要都是提到他们在那场战争中所受到的伤害和很少提到对他国造成的巨大灾难,最重要的原因是他们有一个很好的理由---日本是第一个受到核武器,也是目前为止唯一一个受到核武器攻击的国家。美国在日本的广岛和长崎各投下的原子弹给日本带来了严重的伤害,最后导致约30万人的死亡。 日本就是借助这两颗原子弹的“威力”来装饰自己“受害者”的面目,每年的8月6日和9日,分别在广岛和长崎都有纪念活动,所谓揭开伤口,教育下一代。 但是,从1995年以来,世界各地,包括美国、俄罗斯、中国、英国、德国日本等国的历史学家和科学家,以及原来的政治家和军人,经过单独或是联合研究,发现美国在日本投放原子弹的历史记载存在许多的疑问,无论是在文字还是图象资料上都有诸多的困惑。主要问题是: 一,由于B-29飞机的航程有限,原子弹的投放飞机的起飞地点选在距离日本较近的提尼安岛的美国空军基地上,从美国本土运送两颗原子弹到提尼安岛上的步骤是先运送到夏威夷,然后在运送到提尼安岛,由于当时飞机的航程和安全性的限制,这两步过程使用的只能是军舰,这两段路却有很大的危险性,因为虽然日本海军在美军的打击下几乎已经没有了战斗力,但是,日本海军却仍然相当数量的潜艇,即使在战争末期这些潜艇仍然偷袭美军的军舰,即运送原子弹的军舰随时有可能被日本潜艇偷袭,美国怎么会冒那么大的风险用军舰运送原子弹? 二,当时美国制造出的第一批原子弹只有三颗,其中一颗已经在1945年7月16日的新墨西哥州的原子弹实验厂实验,美国怎么敢用仅剩的两颗原子弹去攻击实际上已经没有任何还手之力的日本,而且还是以平民为主的城市呢?而且,美国在未来几个月内不要可能马上在造出原子弹,美国难道没有想到会有可能出现的有、突然事件吗? 三,当时,主要的原子物理的科学家包括爱因斯坦、费米甚至是奥本海默本人都极力反对使用这种威力过大的武器。美国政府难道一点也不尊重这些为他们研制核武器以后还得依赖的科学家的意见吗? 四,电影和照片资料的问题。有很多人看过广岛和长崎原子弹爆炸、后的电影和照片资料,但是,你只要有少许的常识和一些思考,你就回发现这些电影和照片资料中有着诸多的问题。原子弹爆炸过后谁有能力在强烈的核辐射区进行摄影或摄像,日本当时没有任何一种防辐射的装备。即使是少得可怜的电影资料还是有问题,你会发现一些“幸存者”在爆炸后从废墟中出来后排成行走路,似乎是经过训练的。另外,能在核武器的爆炸中幸存这本身就是不可思议的事。 五, “幸存者”的迷惑。从战争结束到今天,从未发现过一个可以直接证明在广岛和长崎有过原子弹爆炸的人。有些“幸存者”只看到有大火产生,另一些“幸存者”以自己所谓“受到辐射烧伤的”伤痕,实际上只是火烧伤的痕迹。没有一个日本人能自身经历的的证据证明在广岛和长崎曾爆炸过原子弹。 六,数字的困惑。当时由于日本的个大城市都受到美国飞机的整天狂轰滥炸,大多数市民都跑到乡下躲避,广岛和长崎也是如此,实际上,据一个在广岛的日本老人介绍,1945年3月以后,在广岛市的市民已经不足五万人了。当他在四月离开广岛到乡下时,广岛的人已经寥寥无几了。当然长崎也是如此,而日本政府最后却称两颗原子弹最后造成近30万人死亡,着实在令人费解。 七,科学证据。美国和德国科学家在广岛和长崎两地进行了土样品的秘密采集,拿回国后经化验发现这些土的土质与普通土几乎没有区别,辐射计量并非超常。根本无法与在核实验基地所采集的土样品的辐射剂量相比。实际上,在受到严重辐射的土地上在几百年内不可能可以生长植物,人在该地区生活也相当危险,这与今天广岛的事实相悖。这更使人们困惑。 八,最有力的证据。美国、中国和澳大利亚的科学家运用巨型计算机的有限元分析法,对在新墨西哥州、广岛和长崎的原子弹爆炸的电影图象资料进行分析后,其结果令他们大吃一惊--三份图象是同一颗原子弹的,也就是三份电影资料是在同一颗原子弹爆炸的不同角度拍摄的,当然应该是在新墨西哥州爆炸的那颗原子弹。种种令人不解的疑问和新的发现令许多科学家(特别是核物理学家)和历史学家十分困惑,但是,由于这种关于核武器的事件的极其特殊性以及对事实的谨慎态度,另外很多科学家和历史学家都是独立研究,使这种疑问没有通过新闻媒体公布于众。 二 事实与真相 但是,仍然有许多的学术人士要求知道事实真相,从1995年开始,他们通过些秘密的方式与美国政府交涉,要求美国政府解密一些文件,然而却没有得到任何答复。有些美国政府官员说这是些”疯子的行为”。但是,1999年末,一位参加过“曼哈顿计划”的科学家和一位当年美军的上级军官却联合披露了一个令人吃惊的历史--美国从来没有在日本本土投放过原子弹,在广岛和长崎投放原子弹的事件是一场骗局,那只是美军进行的一场非同寻常的信息站和心理站,一次非常成功的“软战争”。 由于这个消息是在十分保密的情况下披露的,而且受到了美国政府的压制和否定,最后甚至对这两位科学家和军官进行了软禁,没有人知道他们的真实姓名,因此只有极少数科学家和历史学家知道了历史的真相。 纸终究包不住火的,这些消息终究会公布于众,只是时间的问题。 以下就是历史的事实与真相。 这个信息与心理战被称为“曼哈顿2”计划。 1945年7月16日,世界上第一颗原子弹在美国的新墨西哥州实验爆炸成功。这颗原子弹的威力之大甚至超出了科学家、工程师和军方人士的预料。大多数的科学家也预料到了这种武器的存在将直接威胁到人类,这其中包括爱因斯坦和“原子弹之父”奥本海默本人。 但是,第二次世界大战还没有完全结束。虽然在欧洲战场上,战争的火焰已经熄灭,但是在亚洲和太平洋战场,日本帝国还在利用四处环海的地理优势进行垂死挣扎。美军的飞机虽然对日本本土进行了大规模的轰炸,使日本的许多工业城市(包括东京、大阪)几乎已经成为了一片废墟,而且人员伤亡十分惨重,但是,日本却没有任何要投降的迹象,而且种种迹象表明日本准备在本土与盟军决一死站。盟军在1945年6月份已经着手计划在日本本土进行大规模的登陆战,参加的盟军士兵大约为40万,其中以美军为主。美军却非常担心这次登陆行动,日本已全民皆兵,这次行动必将会造成盟军严重的伤亡。 但是原子弹研制成功后,美军便似乎发现了有新的希望。因为对日本使用原子弹会对日本造成巨大的伤亡,并且还有巨大的心理作用,可以达到逼迫日本投降的目的。那样就不再需要冒险进行大规模的强行登陆行动以及有可能在日本进行大规模的战争。这大概能避免约10万盟军的死亡。 因此,美国军方极力要求对日本本土进行原子弹轰炸,以达到逼迫日本投降的目的,这当中为首的美国军方人士是麦克阿瑟将军。 但是,许多科学家以及一些军方人士却反对使用原子弹。因为他们清楚原子弹的威力给平民带来巨大的伤害以及在爆炸后的辐射给土地的影响。 当然,他们也承认在日本进行登陆战将带来巨大的代价。因此,许多科学家和军方人士建议对日本政府施加巨大政治压力使其投降。不过这种想法可以说是很幼稚的,因为当时日本已经受到了世界的孤立和进攻,没有什么所谓“更大的压力”。因此军方人士甚至是美国总统杜鲁门本人也赞成对日本本土使用原子弹。即使这有巨大的风险。
[font=宋体][font=宋体]无细胞蛋白表达系统([/font][font=Calibri]Cell-Free Protein Expression System[/font][font=宋体])是一种基于原核和真核细胞提取物构建的体外蛋白表达系统。它具有许多优点,例如可以在短时间内生产大量的蛋白质,同时避免了细胞内的复杂调控机制和翻译后修饰等繁琐过程。因此,无细胞蛋白表达系统在生物制药、生物材料、生物燃料等领域具有广泛的应用前景。本文将详细介绍无细胞蛋白表达系统的优缺点。[/font][/font][font=宋体][b]一、无细胞蛋白表达系统的优点[/b][/font][font=宋体] [/font][font=宋体][font=Calibri]1.[/font][font=宋体]高效性:无细胞蛋白表达系统具有高表达效率的优点,这是由于体外体系中不存在靶蛋白累积所需的细胞分裂和细胞复杂代谢反应。此外,由于无细胞蛋白表达系统不受到细胞毒性和免疫反应的限制,可以实现大规模的蛋白质表达。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2.[/font][font=宋体]灵活性:无细胞蛋白表达系统可以使用一系列不同的原核和真核细胞提取物作为反应体系,例如[/font][font=Calibri]E.coli[/font][font=宋体]、小麦胚芽和人类细胞等。这意味着可以根据不同的实验目的和需求进行合理的选择,以适应多样化的研究需要。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]3.[/font][font=宋体]易操作性:无细胞蛋白表达系统非常容易操作。与传统的细胞表达系统相比,无细胞蛋白表达系统不需要细胞培养、生长和繁殖。此外,无细胞蛋白表达系统可以快速进行,通常只需要数小时至几天即可完成目标蛋白的表达。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]4.[/font][font=宋体]简单纯化:由于无细胞蛋白表达系统可以避免有机溶剂和离子交换剂等复杂的步骤,从而使目标蛋白的纯化工作更加简便和迅速。例如,可以使用亲和柱、凝胶过滤和电泳分析等方法来快速分离和纯化蛋白质。[/font][/font][font=宋体] [/font][font=宋体][b]二、无细胞蛋白表达系统的缺点[/b][/font][font=宋体] [/font][font=宋体][font=Calibri]1.[/font][font=宋体]成本较高:尽管无细胞蛋白表达系统可以大规模进行蛋白质表达,但是所需的原核和真核细胞提取物通常需要较高的成本。此外,涉及到的一些试剂和设备也比较昂贵,使得无细胞蛋白表达系统在应用过程中存在一定的经济压力。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2.[/font][font=宋体]表达限制:由于无细胞蛋白表达系统缺乏复杂的代谢反应和细胞分化机制,因此它不适用于某些特定类型的蛋白。例如,它无法表达复杂的膜蛋白和困难的药物蛋白等。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]3.[/font][font=宋体]不稳定性:无细胞蛋白表达系统通常具有一定的稳定性问题。由于缺乏细胞膜的保护,无细胞蛋白表达体系会更容易受到外部条件的影响,如温度、[/font][font=Calibri]pH[/font][font=宋体]、离子浓度等,从而导致蛋白质的不稳定性、聚集和降解等现象。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]4.[/font][font=宋体]不适合复杂蛋白结构:无细胞蛋白表达系统对于复杂蛋白结构的模拟效果不佳。例如,膜蛋白、多肽和糖蛋白等复杂蛋白质可能会被无细胞蛋白表达系统无法很好地复制,从而限制了其应用范围。[/font][/font][font=宋体] [/font][font=宋体]无细胞蛋白表达系统具有高效、灵活、易操作、简单纯化等优点,但同时也存在着成本较高、表达限制、不稳定性和不适合复杂蛋白结构等缺点。在实际应用中,需要根据具体的研究目的和需求进行选择,并结合其他技术手段来弥补其不足之处。[/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供[url=https://cn.sinobiological.com/services/cell-free-protein-synthesis-service][b]无细胞蛋白表达服务[/b][/url],服务优势:[/font][font=宋体]①快速、高效 ②高成功率 ③一致性 ④高难度抗体表达[/font][/font][font=宋体] [/font][font=宋体][font=宋体]详情可以咨询,具体[/font][font=Calibri]https://cn.sinobiological.com/services/cell-free-protein-synthesis-service[/font][/font]
今日 《扬子晚报》报道:连日来,刘明锁承包的镇江丹徒区延陵镇大吕村的40多亩西瓜大棚就像布下了“地雷阵”,从5月8日开始,已结满瓜藤的大小西瓜,还没有成熟就一个个“疯狂”地炸裂开来,有的炸得四分五裂,有的炸得像一朵花,瓜农刘明锁夫妇先是惊得目瞪口呆,后是伤心欲绝。就在记者采访时,却又听说,其他瓜农的数十亩西瓜同样开始满地“开花”。这事是否与“西瓜专家”提供的“西甜瓜膨大增甜剂”有关?有一种药叫“西瓜膨大素”,据查,主要成分为氯吡脲,属于植物生长调节剂。主要作用是加强细胞分裂,增加细胞数量,加速蛋白质的合成促进器官形成。提高花粉可孕性。其主要特点表现四个方面:一、促进细胞分裂,促进果实膨大。对细胞的分裂有明显的促进作用,对器官的横向生长和纵向生长都有促进作用,从而起到膨大果实的作用。二、延缓叶片衰老,保绿时间长,加强叶绿素合成,提高光合作用,促使叶色加深变绿。三、打破顶端优势,促进侧芽萌发,能够透导芽的分化,促进侧枝生成,增加枝数,增多花数,提高花粉受孕性,从而增加果实数量提高产量。四、改善作物品质,提高商品性。诱导单性结实,刺激子房膨大,防止落花落果,促进蛋白质合成,提高含糖量等。
一、细胞因子的概念细胞因子(cytokine)是由机体多种细胞分泌的小分子蛋白质,通过结合细胞表面的相应受体发挥以调节免疫应答为主的生物学作用。细胞因子具有 非常广泛的生物学活性,包括促进靶细胞的增殖和分化,增强抗感染和细胞杀伤效应,促进或抑制其它细胞因子和膜表面分子的表达,促进炎症过程,影响细胞代谢 等。二、细胞因子的命名细胞因子按其来源可分为:由单个核吞噬细胞产生的细胞因子称为单核因子(monokine);由淋巴细胞产生的细胞因子称为淋巴因子 (lymphokine)等。按其作用可分为干扰素、集落刺激因子、肿瘤坏死因子、生长因子和趋化因子等。部分由不同细胞分泌的细胞因子,其基因及编码蛋 白与结构清楚者,在免疫调节、造血和炎症中发挥重要作用,又称为白细胞介素(interleukin,IL)。也可以依据结构或者其受体结构分类,我们的 趋化因子目前没有受体产品。三、细胞因子的特征1、低分子量;一般为<60kD的多肽或糖蛋白。多以单体形式存在,少数为二聚体,三聚体。2、天然细胞因子由抗原、丝裂原或其他刺激物活化的细胞所分泌,通过旁分泌(paracrine)、自分泌(autocrine)或内分泌(endocrine)方式在局部发挥短暂作用。3、一种细胞因子可由多种细胞产生,同一种细胞可产生多种细胞因子。4、需通过与靶细胞表面相应受体结合后发挥其生物学效应。5、具有高效性、多效性、叠性、拮抗性、协同性和网络性。四、细胞因子的分类1、白细胞介素(interleukin,IL-s)最初是指由白细胞产生又在白细胞间发挥作用的细胞因子。2、干扰素(interferon,IFN)最早发现的细胞因子,有干扰病毒感染和复制的能力。分α、β和g三种类型。3、肿瘤坏死因子超家族(tumor necrosis factor,TNF)1975年发现的一种能使肿瘤发生出血坏死的物质。4、集落刺激因子(colony-stimulating factor,CSF)指能够刺激多能造血干细胞和不同造血祖细胞增殖分化,在半固体培养基中形成相应细胞集落的细胞因子。包括G-CSF(粒细胞)、M-CSF(巨噬细胞)、 GM-CSF(粒细胞、巨噬细胞)、Multi-CSF(多重)(IL-3)、红细胞生成素(EPO)、干细胞生长因子(SCF)、血小板生成素 (TPO)等。5、趋化因子(chemokine)主要功能是招募血液中的单核细胞、中性粒细胞、淋巴细胞等进入特定的淋巴器官和组织以及感染发生的部位。根据趋化因子近N端半胱氨酸(Cys)的位置、排列方式和数量,可分为CC、CXC、C、CX3C四个亚家族。6生长因子(growth factor,GF)生长因子(GF)是具有刺激细胞生长作用的细胞因子。五、细胞因子的生物学活性1.介导自然免疫、参与抗肿瘤和抗感染2.调节T、B细胞活化、生长和分化,介导细胞免疫和体液免疫3.刺激造血生成、刺激骨髓祖细胞生长和分化为各种成熟血细胞4.在炎症、感染和内毒素血症中的作用5.在超敏反应和自身免疫病中的作用6.细胞因子通过激活其相应受体(CKR),导致细胞的增殖与分化或分泌某种蛋白质。六、四种蛋白表达体系比较表达细胞优点缺点原核E. coli繁殖快、成本低、产量高遗传背景及基因表达调控机制清楚易于大规模培养,成本低廉蛋白常为包涵体,纯化困难无糖基化(分泌蛋白,细胞膜上蛋白不可用),生物活性不定无翻译后修饰,内毒素含量高酵母Pichia使用简单,表达量高,His-tag便于纯化,一定的翻译后加工可进行糖基化修饰,操作简单,适合大规模生产可诱导表达,也可分泌表达,产物便于纯化有时会出现蛋白切割问题糖基化不能满足要求昆虫High-5产量高 ,翻译后加工与哺乳动物相似对于部分有毒性或较难表达蛋白有优势无内毒素污染蛋白活性不如哺乳动物适合表达激酶等定位于细胞内的真核蛋白哺乳CHO HEK293完善的翻译后加工,活性接近天然蛋白周期长、技术要求高表达产量低
鸡蛋,在如今的社会里,更多时候是作为一种营养丰富的食品出现在我们的餐桌上。现代化大型养殖场如生产产品般输出鸡蛋的方式颠覆了人们对鸡蛋的认识,或许已经很少有人能够联想到从蛋黄蛋白到一个小生命的奇迹升华。但在人类漫长的历史中,农业是文明的核心。就在不太遥远的过去,大多数人还可以在家中目睹鸡生蛋、蛋生鸡的奇迹。这种神秘的现象让古时的人们感到好奇、困惑,甚至产生莫名的崇拜。我们华夏文明由雏鸡的诞生联想到世界的起源,“天地混沌如鸡子,盘古生其中”,看来在我们祖先的眼中,鸡蛋的孵化犹如天地诞生般神秘。这种“卵生崇拜”在史籍中屡见不鲜,如《史记·殷本纪》记述商朝人先祖契的来历时提到有娀氏的女儿简狄“见玄鸟坠其卵,简狄取吞之,因孕生契”,同样,在《史记·秦本纪》中,文章伊始就记载了颛顼的孙女女修织布时“玄鸟陨卵,女修吞之,生子大业”,而这位大业就是秦人的先祖。不得不佩服古人的想象,这玄鸟蛋孵化出了两个重要朝代。在漫长的历史中,这种对蛋朦胧而浪漫的崇拜逐渐融入了我们的文化中,直到如今,染红壳的鸡蛋依旧是新婚、生子、满月时,人们表达祝福的重要载体。随着科技的进步,人们对蛋的理解逐渐清晰,现在很多人都知道蛋和卵细胞有千丝万缕的关系。可是鸡蛋到底是否就是一个细胞?答案可谓五花八门,有人说整个鸡蛋就是一个放大的卵细胞,蛋壳内的那层膜是细胞膜,蛋清是细胞质,蛋黄是细胞核;也有人说蛋黄是卵细胞,卵黄膜就是细胞膜,蛋黄就是细胞质,而蛋黄上面的小白点是细胞核;还有人认为鸡蛋本就是由很多细胞构成的。
1. 利用诱导性多功能干细胞构建出小鼠精子祖细胞日本京都大学研究人员通过体外诱导胚胎干细胞(ESCs)和诱导性多功能干细胞(iPSCs),形成原始生殖细胞样细胞(primordial germ cell-like cells, PGCLCs),最后进一步分化,通过体内植入不能生育的小鼠睾丸中,产生了外观正常的精子。将这些精子注射到雌性小鼠的卵细胞中,不久雌性小鼠生出了健康的小鼠后代。2. 鉴定出阿尔茨海默病Alzheimer's disease的生物标记美国研究人员利用一种一般性和无偏差的方法---组合文库筛选(Combinatorial Library Screening)来鉴定出诊断上有用的抗体,而避免进行抗原鉴定。该方法涉及利用非自然的合成分子组合文库对病人血清样品和对照样品进行比较性筛选,这样就可鉴定出病人血清样品中要比和对照样品中保留极其多IgG抗体的分子,随后利用这些分子作为捕获试剂来捕获诊断上有用的抗体。研究人员利用多发性硬化症(multiple sclerosis)小鼠模式动物和证实这种方法的实用性,并利用该方法在阿尔茨海默病小鼠模式动物中鉴定出两种候选的IgG抗体生物标记。3. 发现干细胞多能性的选择性剪接开关加拿大多伦多大学研究人员发现了进化上保守的特异的FOXP1选择性剪接开关,可调控干细胞的多能性。研究人员发现这种剪接开关产生的FOXP1胚胎干细胞特异性异构体,与典型的FOXP1异构体相比,着不同的DNA结合性质。选择性剪接事件改变了FOXP1胚胎干细胞特异性异构体的DNA结合性质,促进维持多能性所需的转录因子基因的表达,包括OCT4、NANOG、NR5A2和GDF3,同时抑制胚胎干细胞分化所需的基因。同时,研究小组还发现FOXP1胚胎干细胞特异性异构体促进体细胞高效重编程为诱导性多功能干细胞(iPSC)。4. 追踪神经胶质瘤的起源美国研究人员利用双标记嵌合分析(Mosaic Analysis with Double Markers,MADM)---该技术的精髓在于用绿色荧光蛋白明确标示突变细胞,还有一个关键特色就是无论一个突变的绿色细胞何时产生,总是同时产生一个正常的红色细胞---来分析神经胶质瘤(glioma)的起源。他们将胶质瘤病人体内发现的两种流行突变p53与NF1导入神经干细胞(neural stem cells, NSCs)中,对源自神经干细胞的所有细胞系所作的进一步分析清楚地显示了少突胶质前体细胞(Oligodendrocyte precursor cells,OPCs)是该肿瘤的来源细胞,因为任何可见的肿瘤标志可被检出之前,变异的绿色少突胶质前体细胞的数量大大超过了其正常的红色对应物数量,足足超了130倍。为了进一步证实这点,研究人员也将p53与NF1突变直接导入小鼠少突胶质前体细胞,结果发现这些小鼠产生神经胶质瘤,从而再次证实少突胶质前体细胞是神经胶质瘤的来源。5. 发现新的组蛋白修饰方式美国芝加哥大学Ben Mary癌症研究所研究人员在细胞中筛查出了67个新组蛋白修饰标记,并从中发现了一种新型组蛋白翻译后修饰方式---赖氨酸巴豆酰化(lysine crotonylation)修饰。通过进一步的结构及基因组定位分析,研究人员证实氨酸巴豆酰化修饰是一种进化高度保守,且在生物学功能上完全不同于组蛋白赖氨酸乙酰化的蛋白质修饰方式。研究人员还发现在人类体细胞和小鼠精子细胞基因组中,组蛋白赖氨酸巴豆酰化分布于基因活性转录启动区域或增强子上。在减数分裂后的精子细胞中,赖氨酸巴豆酰化高丰度集中在性染色体上,被用来标记睾丸特异性基因。
赛百味突然之间成了新闻焦点,说是他们出售的食物中含有偶氮甲酰胺。这种物质也被用于生产瑜伽垫和鞋底原料,在澳大利亚和欧盟等国被禁止用于食品。新闻又称该物质可能导致呼吸、过敏与哮喘等方面的问题。在新闻媒体中,"赛百味承认食物中有鞋底成分"为导语,毫不奇怪会引起巨大关注。 然而这实在是一个没事找事的新闻。偶氮甲酰胺是一种食品添加剂,用于面粉的漂白和氧化。如果说漂白还不是那么重要的话,氧化对于改善面粉的性能至关重要。面粉形成面团,需要其中的面筋蛋白互相交联,充分形成网络结构。对面粉进行氧化处理,可以大大促进这种交联的发生,从而改善面包的口感。之前食品工业中大量采用溴酸钾,后来发现其安全风险较高,而偶氮甲酰胺的效果更好,而且没有发现安全风险。也就是说,偶氮甲酰胺是以"长江后浪"的姿态取代了前辈而进入食品中的。 国际食品添加剂联合专家委员会(JECFA)评估过偶氮甲酰胺的安全性,结论是添加量在每公斤不超过45毫克的范围内,带来的安全风险可以忽略。美国、加拿大和中国等国采用了这一结论。所以,美国的赛百味中含有这种物质,完全合法。而且,除了赛百味,其他公司的面包产品中也会有它的存在。这种物质对消费者没有什么危害,但在生产过程中可能会导致工人出现呼吸、过敏与哮喘等方面的问题。所以,澳大利亚和欧盟等国则没有采用JECFA的结论,而是禁止了它作为食品添加剂使用。 跟大多数的食品添加剂一样,偶氮甲酰胺也广泛用于生产工业产品。使用了偶氮甲酰胺的塑料可以用来生产鞋底,就被媒体阐释为"面包中含有鞋底原料",实在是缺乏基本逻辑。遵循同样的逻辑,任何一种食品都可以被阐释为含有工业产品原料甚至垃圾废料成分。比如淀粉可以用于生产可降解塑料,可以宣称"面包中含有塑料饭盒成分";许多食品乳化剂也用于油墨生产,可以宣称"冰激凌中含有油墨成分". 公众更关心为什么有的国家禁用,有的国家却又允许使用。这在食品行业中很平常。对于一种物质的安全评估,实验证据是全世界通用的,但对一种物质带来的好处和风险的权衡,则取决于主观的判断。比如JECFA认为实验证据已经足够充分说明限量范围内的偶氮甲酰胺很安全,而美国认为它带来的好处又很重要,所以就采用JECFA的结论。而欧盟并没有否认JECFA采用的数据和评估结果,但他们不认为这种添加剂带来的好处有多重要,而生产过程中导致工人出现症状的事情也值得关注,所以禁用也完全可以理解。许多别的食品添加剂,比如同是面粉改良剂的过氧化苯甲酰,还有食用色素等,也是同样的情况。 新闻报道称赛百味自己也承诺将从自己的食品中移除这种添加剂,有许多人认为这说明赛百味承认了它有害。实际上,企业主动选择停用一种原料,跟是否自认为它有害并没有什么关系--因为是否有害,该由监管部门来判断。但企业的经营核心是满足消费者需求--至于消费者的需求是否科学和理性,并不在考虑范围之中。 禁用偶氮甲酰胺当然不是什么大不了的事情。但我们需要知道,面包行业总是需要面粉改良剂的。停用了它,自然得有其他的替代品上位,就像它的上位是溴酸钾等前辈退出的结果一样。
提起美式食品,人们就会想起汉堡包。但美国食品分析公司Clear Labs 5月10日发布报告说,美国市面上的汉堡包超过10%存在问题。他们甚至在少数汉堡包中检测到人类与老鼠的DNA(脱氧核糖核酸)。不过,该公司以及美国食品安全专家都指出,食品里出现人类与老鼠DNA难以避免,不一定就会对人的健康造成损害。该公司研究人员最近对加利福尼亚州22个零售店销售的汉堡包进行了基因组分析,涉及77个品牌的258份样品。结果显示,13.6%的汉堡包存在问题,如所含成分与标签标示不相符、卫生问题与病菌污染等。研究人员还在一份汉堡包样品中发现了人类DNA,在3份汉堡包样品中发现老鼠DNA。报告分析认为,人类DNA可能来源于汉堡包加工过程中操作人员的头发、皮肤或指甲等。报告解释称:“尽管令人不快,但需要强调的是,人类或老鼠DNA不太可能对消费者健康造成损害。”报告指出,美国食品和药物管理局允许食品中存在一定量的人类与老鼠DNA,因为这在生产过程中无法完全避免。在他们研究中检测到的人类与老鼠DNA量很可能符合监管的要求范围。佐治亚大学食品微生物学教授迈克尔·多伊尔表达了类似看法。他说:“在食品中发现一些老鼠和人类DNA并不令人意外……听上去很恶劣,但需要客观看待。这与其说与人类健康相关,还不如说是审美关切。”此外,素食汉堡包问题颇多。在89份样品中,23.6%存在所含成分与标签不一致等问题。比如,两份素食汉堡包样品中出现牛肉DNA,一份黑豆汉堡包里根本不含黑豆。最引人关注的是,4.3%的样品里含有假结核耶尔森氏菌、嗜水气单胞菌等病菌的DNA。不过,多伊尔评价说,这一结果会有一点误导,因为基因组分析技术无法区分出死与活的细胞,发现死细胞的病菌DNA并没有多大意义。而且,所发现的病菌要么不是人们通常担心的病菌,要么数量较少不足以致病。
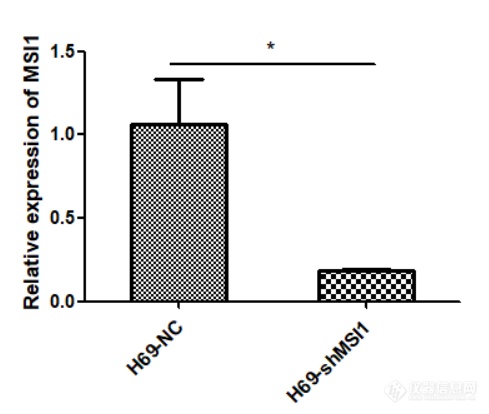
MSI1在人小细胞肺癌细胞系中的表达及MSI1低表达细胞模型的构建实验方法与步骤 细胞的复苏 1.复苏前的准备:打开水浴锅,设置温度37℃;紫外线将超净台消毒30 min;配置完全培养基。 2.将要复苏的H69、H446细胞从液氮取出,用一次性PE手套包裹冻存管,迅速放入水浴锅中震荡,使其快速融化。 3.在15 mL离心管中加入5 mL完全培养基及融化的细胞悬液,900 r/min离心8分钟,弃去上清,得到细胞沉淀。 4.在25 cm2的培养瓶中加入5 mL完全培养基,并用1 mL培养基将沉淀的细胞重悬并加入准备好的培养瓶中,放入CO2恒温培养箱中继续培养。 细胞的传代 1.选取在悬浮培养瓶中生长至90%的H69细胞,用移液枪将细胞悬液移入15 mL离心管中,选取在贴壁培养瓶中生长至90%的H446细胞,用PBS溶液将细胞吹至漂浮,并移入15 mL离心管中,两种细胞均900 r/min离心8分钟,弃掉上清。 2.分别在3个25 cm2培养瓶中加入5 mL完全培养基,在细胞沉淀中加入3 mL培养基并充分吹打混匀,将3 mL细胞悬液平均放入3个培养瓶中并混匀,放入培养箱中继续培养。 MSI1低表达细胞模型的构建1.从-80℃冰箱取出慢病毒载体冰上融化,将慢病毒用空白培养基稀释为滴度2×108,充分混匀,准备好病毒感染增强液。2.将25 cm2悬浮培养瓶中H69细胞移入15 mL离心管中并用移液枪充分吹打混匀,取其中500 μL放入细胞计数仪中计数,取出1.2×106个细胞置入新的离心管中,加入空白培养基至6 mL。3.在12孔板中以MOI=10的病毒滴度进行感染,培养16 h。4.16 h后将细胞悬液离心,换成不加双抗的完全培养基继续培养,72 h后观察荧光。5.待细胞生长至状态良好,加入1 μg/mL嘌呤霉素筛选至90%以上细胞均产生荧光。荧光实时定量PCR(Q-PCR)检测MSI1在mRNA水平的表达 总RNA的提取分别将细胞离心,PBS缓冲液清洗2次,900 r/min离心8 min,得到细胞沉淀。分别加入1 mL Trizol,用移液枪吸打至细胞完全破裂,加入200 μL氯仿,震荡30 s,室温静置10 min,以有效分离无机相和有机相,随后4℃,12,000 g/min离心15 min。将上清移至高压过的1.5 mL离心管中,加入与上清等体积的异丙醇,轻柔颠倒震荡数次,室温静置10 min,随后4℃,12,000 g/min离心10 min。弃去上清,加入75%无水乙醇,4℃,12,000 g/min离心5 min。弃去上清,沉淀置于冰上自然干燥,但不可完全干燥。用30 μL DEPC水溶解总RNA。用NanoDrop One超微量分光光度计进行定量和纯度检测,用1%琼脂糖凝胶电泳进行完整性检测。 cDNA的合成逆转录体系试剂名称使用量模板RNAMonScriptTM 5*RT111 All-in-One MixMonScriptTM dsDNaseNuclease-Free Water1 μg4 μL1 μLup to 20 μL将混合液轻柔吹打混匀,瞬时离心,37℃ 2 min,55℃ 15 min,85℃ 5 min,得到cDNA。 Q-PCR检测MSI1 mRNA的表达GAPDH引物序列:Forward primer:Reverse primer:5’-GGTCGGAGTCAACGGATTTG-3’5’-ATGAGCCCCAGCCTTCTCCAT-3’MSI1引物序列:Forward primer:Reverse primer:5’-GAACCATCCCGTCCTGTATCA-3’5’-GAAACCATGAAGCCCCAACC-3’Q- PCR反应体系:Q-PCR反应体系试剂名称使用量cDNAForward primerReverse primerMonAmpTM Chemhs qPCR MixLow ROXNuclease-Free Water50 ng0.2 μL0.2 μL5 μL0.1μLup to 10 μLQ-PCR反应程序: Q-PCR反应程序反应步骤反应温度反应时间循环次数预变性95℃10 min1变性95℃10 s40退火55-65℃10 s延伸72℃30 s溶解曲线溶解曲线按仪器默认溶解曲线 结果采用t检验,用Graphpad prism5计算MSI1在mRNA水平的表达量。 Western blot检测MSI1在蛋白水平的表达总蛋白的提取将对数生长期的H69-NC、H69-shMSI1细胞移入15 mL离心管中,900 r/min离心8 min,并用PBS溶液洗涤2次,以去除培养基中血清影响。分别加入含PMSF的蛋白裂解液100 μL,与细胞充分混匀。4℃裂解1小时后,4℃,12000 g/min离心15 min,将上清移至新的离心管中,得到细胞总蛋白。 BCA法测定蛋白浓度 将Solution A和Solution B以50:1的体积比配置BCA工作液,充分混匀。将2 mg/mL蛋白标准品等比稀释,最小浓度为125 μg/mL,并分别与配置好的200 μL BCA工作液混匀,铺入96孔板中。37℃孵育30 min,测定波长562 nm处OD(光密度值)值,并绘制蛋白标准曲线。取适量H69-NC、H69-shMSI1细胞总蛋白,20:1稀释后,与200 μL BCA工作液混合均匀。37℃孵育30 min,用酶标仪测定波长562 nm处OD值,根据标准曲线计算出样品中的蛋白浓度。Western blot检测MSI1蛋白的表达 分别收集对数生长期的H69-NC、H69-shMSI1细胞总蛋白,加入相应体积4×SDS Loading Buffer,沸水浴煮5 min,分别取40 μg细胞总蛋白,在提前配制的10% SDS-PAGE分离胶电泳。电泳结束后,将蛋白转至PVDF膜上。用含5%脱脂牛奶的封闭液 37℃封闭1.5 h。弃去封闭液,用TBST缓冲液洗3次,每次10 min,加入MSI1兔单克隆抗体(1:1000),并以GAPDH为内参,加入GAPDH鼠单克隆抗体(1:5000);4℃孵育过夜,次日用TBST缓冲液洗膜3次,每次10 min。在敷有MSI1抗体的膜上加入辣根酶标记山羊抗兔IgG(1:5000),在敷有GAPDH抗体的膜上加入辣根酶标记山羊抗鼠IgG(1:5000),37℃敷育1 h,TBST 缓冲液洗膜3次,每次10 min。用增敏化学发光底物试剂检测,暗室曝光显影。在GAPDH表达量相同的情况下比较MSI1的表达情况。多次重复,应用ImageJ计算出各个蛋白条带的灰度对比,结果采用t检验,并应用Graphpad prism5作出柱状图。 MSI1在人小细胞肺癌细胞系中高表达 提取人正常肺上皮细胞BEAS-2B、小细胞肺癌细胞H446、H69的RNA,利用Q-PCR检测MSI1在正常肺上皮及小细胞肺癌细胞系中的表达情况,结果如图2-1显示,MSI1在小细胞肺癌细胞系H446、H69中的表达远远高于正常肺上皮细胞。https://ng1.17img.cn/bbsfiles/images/2022/10/202210102201428158_6718_5389809_3.png1 MSI1 mRNA在小细胞肺癌细胞系中的表达(**代表与正常肺上皮细胞相比,小细胞肺癌细胞MSI1表达量增高具有统计学意义,P0.01)。 MSI1低表达细胞模型的构建本实验选取人小细胞肺癌细胞系H69细胞,使用慢病毒感染技术敲低MSI1的表达,同时设置对照组除外病毒本身对细胞产生的影响,待细胞状态良好使用嘌呤霉素筛选,然后在荧光显微镜下观察如图2-2,可见H69-NC、H69-shMSI1细胞均产生绿色荧光,表明人小细胞肺癌H69细胞慢病毒感染成功。https://ng1.17img.cn/bbsfiles/images/2022/10/202210102201428036_9359_5389809_3.png MSI1低表达细胞模型的构建。应用shMSI1慢病毒载体感染H69细胞,利用嘌呤霉素筛选,并在荧光显微镜下观察。 荧光实时定量PCR(Q-PCR)检测MSI1的mRNA表达水平提取对数生长期的H69-NC、H69-shMSI1细胞的RNA,并测量RNA浓度及完整性,用1%琼脂糖凝胶电泳检测完整性可见,RNA有三条带,从上到下依次为28S rRNA、18S rRNA和5S rRNA,且28S rRNA的亮度是18S rRNA的两倍。用NanoDrop One超微量分光光度计测定人总RNA的A260/A280的值为2.00左右,A260/A230的值为2.30左右,说明提取的RNA质量和完整性很好,可以用于后续试验。利用Q-PCR技术检测各细胞内MSI1 mRNA相对表达量,结果如图2-3所示,与对照组相比,H69-shMSI1组MSI1 mRNA表达量明显降低(P0.01),抑制率约为75%。https://ng1.17img.cn/bbsfiles/images/2022/10/202210102201434330_8277_5389809_3.png MSI1在RNA水平的表达(***代表与对照组相比,H69-shMSI1组MSI1 mRNA表达量下降具有统计学意义,P0.001)。 Western blot检测MSI1蛋白表达水平将BSA标准品(2 mg/mL)进行等比稀释,最低浓度为125 ug/mL,并应用BCA蛋白质浓度测定试剂盒测定在波长562 nm下的OD值,以OD值为纵坐标,对应蛋白质浓度(μg/mL)为横坐标,绘制标准蛋白曲线如图2-4所示。https://ng1.17img.cn/bbsfiles/images/2022/10/202210102201435248_4142_5389809_3.png图2-4 标准蛋白曲线分别提取H69-NC、H69-shMSI1细胞的总蛋白质,利用Western blot技术检测各细胞内MSI1蛋白的表达情况。结果如图2-5所示,与对照组相比,MSI1蛋白表达在H69-shMSI1细胞中明显降低。表明MSI1低表达细胞模型构建成功。ahttps://ng1.17img.cn/bbsfiles/images/2022/10/202210102201437240_855_5389809_3.pngbhttps://ng1.17img.cn/bbsfiles/images/2022/10/202210102201434999_3303_5389809_3.png图2-5 MSI1蛋白水平表达:(a)MSI1蛋白表达条带;(b)MSI1蛋白的相对表达量。(*表示与对照组相比,H69-shMSI1组MSI1蛋白表达下降具有统计学意义,P0.05)。首先验证MSI1在小细胞肺癌细胞系中的表达情况,利用Q-PCR技术检测在RNA水平,MSI1在肺正常上皮细胞及小细胞肺癌细胞系中的表达,结果显示,MSI1在小细胞肺癌细胞中的表达明显高于正常肺上皮细胞。随后以人经典型小细胞肺癌细胞系H69细胞为研究对象,构建MSI1低表达细胞模型,应用shMSI1慢病毒载体感染H69亲本细胞,同时设置对照组除外病毒本身对细胞产生的影响,利用Q-PCR及Western blot验证MSI1在RNA及蛋白水平的表达,结果显示,H69-shMSI1组MSI1的mRNA及蛋白的表达明显降低。表明MSI1低表达细胞模型构建成功,可以用于后续实验。
本文引用自发酵《在发酵工艺角度看蛋白表达》引用发酵 的 在发酵工艺角度看蛋白表达在分子生物学角度讲,找到或合成外源蛋白基因,构建质粒,并导入细胞以表达具有生物活性的折叠正确的蛋白,是一种成熟的常规技术。目前,包括酶,抗原,抗体,激素,其他小分子调节蛋白在内的很多蛋白,都已经用这种技术实现了工业化生产。在具体的工艺选择上,历史沿袭习惯和表达体系的选择,对工艺稳定性,成本,有巨大的影响。 目前,常用的蛋白表达系,有3个类别:1,大肠杆菌表达系。大肠杆菌的遗传背景十分清楚,代谢相对简单,发酵副产物少,在不是很严格的情况下,是表达蛋白的首选。通过按经验选择合适的菌株及合适的质粒,既可以以包涵体的形式得到大量的目标蛋白,又可以在细胞外得到可溶性蛋白,是常见的一种表达系。2,酵母菌表达系。用酵母做表达系,理由之一,也是遗传背景清楚,而且,当蛋白分子量过小,不能形成包涵体时,或蛋白的二硫键过多,不易体外复性时,酵母菌就成了合适的选择。另外,酵母对蛋白也会有一个简单的修饰,近似于高等动物的蛋白糖基化过程。这样,在合成在体液中发挥作用的蛋白,而且,又不能(技术水平限制)用动物细胞时,就可以退而求其次的选用酵母菌表达。一般是用信号肽把蛋白导出细胞,在发酵液中以可溶性蛋白的形式存在。这也是一个常见的表达系。3,动物(或说,人的)细胞表达系。这种情况,在纯度或毒性方面有较高要求的产品应用。一般国外产品应用较多,国内还没有用动物细胞表达蛋白实现商业化生产的报道。由于技术限制,国内工业化生产用这个方法目前还有较大难度。这3种表达系,各自有自己的优缺点。首先,在潜在的毒性影像方面讲,由于和真核生物亲缘关系太远,大肠杆菌就最不合适。其次是酵母菌。而在表达量和代谢控制成本上来讲,酵母菌和动物细胞又是差强人意的。现在,很多蛋白习惯性的选用酵母菌做表达系,就是因为早期提取蛋白技术低下,而动物细胞培养技术又不过关的原因所致。目前,虽然提取工艺提高了,但作为蛋白这种高附加值产品,运作成本集中在销售而不是生产,所以,降低生产成本的诉求很低。站在降低开发难度的角度讲,一方面,质粒构建和质粒与菌株的匹配方面依赖大量经验,另一方面,发酵工艺策略选择与发酵工艺优化又需要很大的投入,所以,技术开发部门沿用自己熟悉的,已经积累了大量经验的表达系,是合理的。不过,随着分子技术进一步的发展,分子技术进入低附加值的产品领域又是必然的,降低生产成本就变的越来越必要了。 大肠杆菌表达系有两种得到外源蛋白的方法:1,缓慢的表达,得到可溶性蛋白,这种方法产量和酵母菌表达类似,与酵母菌比,不具有明显的优势,一般是有做大肠杆菌传统的研究机构生产小分子蛋白的一种沿袭性做法。2,使用T7启动子表达蛋白,这样,高速的蛋白表达速率使蛋白来不及折叠,在细胞内形成非水溶性的包涵体。最后目标蛋白可以达到总细胞质量的15%-25%,这样,就为降低成本提供了一种可能。不过,在使用T7启动子表达时,也存在两个难点:1,蛋白的复性技术,如果形成可溶性蛋白,那利用(使用分子技术加载在目标蛋白上)信号肽,只要过一遍柱子就能分离得到纯度非常高的,具有生物活性的产品,而形成包涵体,对提取,复性就有较高的要求,特别是二硫键的存在,会对复性产生很大的影响。在目前国内和国际流行技术看,并不是所有的蛋白都能在预定成本下复性的。2,任何情况下,高产都是代谢网络互相依赖与作用的结果。在如此高的表达量下,甚至细胞的形态都已经发生很大变化,正常代谢受到严重干扰,以至于放大时,摇瓶工艺对发酵工艺几乎没有任何参考价值。发酵工艺策略的选择将直接依赖于工程人员在生化,生理水平对菌株的理解,而匮乏可资参考的数据资料。发酵工艺的优化要离开摇瓶经验在发酵罐上逐步进行,这样,整个发酵工艺的确立就需要比想象中要大得多的人员与时间的投入。另外,再说一下糖基化的问题。在动物细胞内合成的折叠正确的蛋白,在分泌入体液前会有一个糖基化的过程,加上一个糖链就不会很快被蛋白酶当做折叠错误的蛋白水解掉。但是以微生物为表达系表达的蛋白,不具有动物细胞的修饰过程,用大肠杆菌表达的目标蛋白,很快会在血液中被降解。解决或回避这个问题,有两种方法:1,用动物细胞表达,一般,是用癌化的人类细胞。由于动物细胞培养技术要求过高,在国外比较昂贵的医药中有应用,国内不常见。2,由于酵母菌也有一个对蛋白的粗略的修饰过程,可以用酵母菌表达目标蛋白。这个技术,国内国外都在用,可以是一个权宜之计。主要难点集中在对合适菌株的分子水平的改造,以达到尽可能接近满意的修饰效果。这样,就可以在不同目标蛋白上表达系和发酵工艺上做出选择。如果是小分子,无糖基化修饰或不在体液中发挥作用的蛋白,可以选择大肠杆菌和酵母菌表达系,得到可溶性蛋白,然后提取。如果分子量合适,并对生产成本有诉求,而且可以比较方便的复性,则选用大肠杆菌表达系,得到包涵体,然后复性。如果是需要在体液中发挥活性并有糖基化要求的 蛋白,则选用经过分子生物学改造的酵母菌表达系。当然,并不是任何一个实验室都同时拥有或擅长所有的方向的。而难点,往往集中在以下3个方面:1,大肠杆菌蛋白包涵体复性。2,糖基化修饰。3,发酵工艺(工程菌株的工业水平)的确定。做工程一般是理科实验室的弱项,而工科实验室做基础又很少,在把工科和理科结合方面,我们实验室还是有经验和成功先例的。下面,以溶菌酶为例,阐述一下蛋白表达系的选择和工艺的确定。溶菌酶是一类具有种属差异的非特异性免疫物质,在动物界中普遍存在,种类繁多,其实,在植物和微生物中也有发现。但研究最多的还是动物。开发兽用溶菌酶,主要是想作为抗生素的替代物,作为添加剂使用。因此是一个低附加值的产品。下面一切的工作,都会围绕“兽用”和“低附加值”展开。首先,比较几种常见和认为有效的溶菌酶,杀菌效果最好的是人的溶菌酶,但考虑到潜在的危险(具有对人溶菌酶产生抗性,并使抗性基因扩散),舍尔求其次,用了鸟类蛋清溶菌酶,作为表达对象。然后,在得到溶菌酶蛋白的一级结构后,对此进行了分析。此蛋白不会用于体液内,故没有糖链修饰的问题。分子量不是很大,但也不太小,130左右的氨基酸构成,足以形成包涵体,这就为用大肠杆菌表达系高效表达提供了可能。讨厌的是有4个二硫键,其中有两个在结构复杂区域,折叠正确有一定的困难。但是,如果用酵母菌做,可能没法解决成本问题,即便优化工艺现在过去了,也不会是最终版本----肯定会有人用大肠杆菌做。所以,结论就是必须知难而进,拿下复性工艺。另外,由于是低附加值产品,发酵吨位就不能太小。以往分子生物学流行的50升,100升小罐发酵,肯定是不行的。发酵罐的放大,除了溶氧,剪切力发生变化,更重要的是搅拌线速度改变了胞外酶以及包括细胞本身的代谢方式和速度。在胞内体现就是氧化还原电势的改变,这在工艺上会带来很多麻烦。虽然说,一般是放大后产量往往提高,但放大过程中,小罐的经验就不能照搬了。同时,也因为是低附加值产品,发酵过程中诸如质粒丢失等稳定性要求,就很高了,应为只有稳定,才能控制成本。这样,工艺就成了第二个难点。明白这些之后,按照大肠杆菌的喜好,合成了溶菌酶的基因。然后构建质粒,导入细胞。在摇瓶水平表达溶菌酶。在筛选复性条件的同时,就同时在发酵罐水平对工艺稳定性进行了优化。首先,为了进一步提高质粒稳定性,对初始培养基进行了重新设计。并改动发酵工艺策略,由于是胞内产物,我们应用高细胞密度发酵控制法延长限制性生长时间(不能用经典发酵的延长对数期生长时间的办法,对工程菌不适合,会造成质粒丢失,代谢紊乱等一系列问题),提高细胞量,并改变了诱导时机,得到了稳定的高产,具体数据比较枯燥,就不在此展开了。提取方面,经过不懈的努力,我们也掌握了比较成功的复性条件(具体由另外人员负责,也不做详细介绍了)。这样,工艺才基本拼凑好。进一步优化,在试生产多次重复时在进行。以上,是外源蛋白表达的粗略的技术和工艺的过程。
[font=宋体][font=Calibri]E. coli[/font][font=宋体]具有遗传背景清楚、细胞增殖快、表达量高、稳定性好和抗污染能力强等特点,适用于多种属蛋白的表达,尤其对小分子蛋白的生产具有极大的优势,但也存在一些问题,如易形成包涵体和含有内毒素等。义翘神州提供从密码子优化到重组蛋白表达[/font][font=Calibri]/[/font][font=宋体]纯化的一站式服务以及内毒素去除等附加服务,以满足不同的定制需求。我们拥有丰富的[/font][font=Calibri]E. coli [/font][font=宋体]可溶性蛋白表达[/font][font=Calibri]/[/font][font=宋体]纯化及蛋白复性经验,拥有多种[/font][font=Calibri]E. coli[/font][font=宋体]细胞株和表达载体,可为客户提供优质的[url=https://cn.sinobiological.com/services/e-coli-protein-expression-service][b]原核蛋白表达服务[/b][/url]。下面是在原核蛋白表达实验中常遇见的几大问题,为大家一一讲解:详情关注:[/font][font=Calibri]https://cn.sinobiological.com/services/e-coli-protein-expression-service[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]1[/font][font=宋体]、我不知道我的蛋白它有什么特性及其结构?[/font][/font][font=宋体] [/font][font=宋体]首先,你要确定一件事,那就是这几个蛋白质有人研究过没有?还是最新发现的蛋白质?如果没有人研究过,那就得用先测部分氨基酸,然后设计引物克隆了。如果有人研究过,那就好了可以根据软件来预测。[/font][font=宋体] [/font][font=宋体][font=宋体]如有[/font][font=Calibri]swiss[/font][font=宋体]—[/font][font=Calibri]pdb[/font][font=宋体]软件,但这个是要有氨基酸序列,知道基因序列,可以在[/font][font=Calibri]ncbi[/font][font=宋体]上进行[/font][font=Calibri]blastx[/font][font=宋体],得到蛋白。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2[/font][font=宋体]、如何选择蛋白表达宿主菌?[/font][/font][font=宋体] [/font][font=宋体]原核系统和真核细胞偏爱的密码子有不同,因此,在用原核系统表达真核基因的时候,真核基因中的一些密码子对于原核细胞来说可能是稀有密码子,从而导致表达效率和表达水平很低。[/font][font=宋体] [/font][font=宋体]原核表达现象:[/font][font=宋体]一、蛋白不表达[/font][font=宋体]①蛋白为毒蛋白[/font][font=宋体]②序列含有稀有密码子[/font][font=宋体] [/font][font=宋体]二、蛋白表达不理想[/font][font=宋体]①蛋白明显降解[/font][font=宋体]②蛋白表达为包涵体[/font][font=宋体]③二硫键错误折叠[/font][font=宋体]④过高的本底表达[/font][font=宋体] [/font][font=宋体][font=Calibri]3[/font][font=宋体]、质粒测序正确,蛋白无法表达怎么办?[/font][/font][font=宋体] [/font][font=宋体][font=宋体]①分析一下稀有密码子,如果比较多,可以尝试[/font][font=Calibri]rosetta[/font][font=宋体]([/font][font=Calibri]DE3[/font][font=宋体]);[/font][/font][font=宋体][font=宋体]②可能是基因本身的问题。[/font][font=Calibri]RNA3[/font][font=宋体]’的特殊结构可能导致转录出现问题,这种情况可以尝试融合表达,譬如[/font][font=Calibri]pET-32a[/font][font=宋体]。[/font][/font][font=宋体][font=宋体]③也许是表达量太低,也可以试一下[/font][font=Calibri]westernblot[/font][font=宋体],定性的检测一下。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]4[/font][font=宋体]、如果[/font][font=Calibri]IPTG[/font][font=宋体]诱导后细胞停止了生长,是不是表示细胞死了?[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]T7RNA[/font][font=宋体]聚合酶非常活跃,[/font][font=Calibri]T7[/font][font=宋体]转录和翻译信号极强,因此,一旦诱导,细胞的主要生理活动都向着目的蛋白表达的方面转化。在通常情况下,细胞将停止生长,形成克隆的能力大大降低,但并未死亡。菌落形成试验可以用来检测表达系统的性能。也有一些例外情况,例如特别的目的基因以及一些极为严紧的载体[/font][font=Calibri]/[/font][font=宋体]宿主菌组合(比如含有[/font][font=Calibri]pLysE[/font][font=宋体]的宿主菌)等,这时在诱导后菌落还是会继续生长。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]5[/font][font=宋体]、如何提高重组蛋白在原核细胞里的表达水平,特别是可溶性表达?[/font][/font][font=宋体] [/font][font=宋体]这个问题是最困扰做原核蛋白表达纯化的人的。比如大肠杆菌表达蛋白本身表达量就大,但是表达的大都是包涵体,想要获得可溶性蛋白,就需要做复性,或是再设计实验时就想办法让其在上清中表达。一般就要通过基因优化,载体宿主优化筛选,表达条件优化,诱导条件优化等等。[/font][font=宋体] [/font][font=宋体]①降低重组蛋白合成的速率[/font][font=宋体]可溶性蛋白的产率取决于蛋白的合成速率,蛋白的折叠速率,以及聚集的速率。高水平表达时,肽链聚集的速率一旦超过折叠速率,就会形成包涵体。因此,降低重组蛋白合成的速率有利于提高重组蛋白的可溶性表达。[/font][font=宋体] [/font][font=宋体]②密码子优化[/font][font=宋体][font=宋体]密码子优化就是根据表达系统对密码子的偏好性进行优化筛选。经过优化的基因序列往往能提高[/font][font=Calibri]mRNA[/font][font=宋体]二级结构的稳定性,有利于新生肽段的正确折叠,提高外源活性蛋白的表达。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]③表达温度的选择大肠杆菌的最适生长温度在[/font][font=Calibri]37[/font][font=宋体]~[/font][font=Calibri]39[/font][font=宋体]℃之间,但此温度下极易生成包涵体蛋白,降低可溶性蛋白的表达,而低温培养条件下表达外源蛋白能有效地增加可溶蛋白的比例。[/font][/font][font=宋体] [/font][font=宋体]④诱导条件优化[/font][font=宋体]摇瓶培养时,应选用低菌体浓度诱导,因为在低菌浓度下菌体处于对数生长期,生长活跃,有利于表达可溶性蛋白。然而,如果能保证合理的补料与充分的通气,在较高菌浓度下诱导也同样可能获得可溶蛋白的高效表达。在某些情况下,诱导剂的流加能显著提高可溶蛋白的表达水平。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体][font=Calibri]6[/font][font=宋体]、义翘神州提供标签去除服务吗?[/font][/font][font=宋体] [/font][font=宋体]是的。我们构建载体时可以在标签蛋白和目的蛋白之间加上蛋白酶的酶切位点,这样纯化后就可以利用蛋白酶去除标签,得到完整的目的蛋白。蛋白酶的切割效率受目的蛋白的影响,具体由实验结果而定。[/font][font=Calibri] [/font]
文章摘自:[URL=http://rohs-sh.dz-z.com/pddetailthree/news/detail-147730.html]http://rohs-sh.dz-z.com/pddetailthree/news/detail-147730.html[/URL]因應歐盟RoHS環保規範,旺旺友聯產物保險取得經濟部業界科專補助,將推出全球首創的RoHS保單,以鴻海等兩岸輸歐的資訊電子業廠商為主要爭取承保對象,建構RoHS風險評估系統,確保品牌廠商或大型供應商的供應鏈,生產的零組件等產品符合歐盟環保規範。 旺旺友聯這項獨步全球的RoHS新保單,雖然初期獲利不大,但前景可期,經濟部官員說,由於RoHS承保對象可能是大型製造商,一旦發生因觸犯歐盟RoHS規範而出現的經營風險,賠償金將相當可觀,因此旺旺友聯將爭取英國等海外再保公司支持。 歐盟95年7月1日實施RoHS環保規範,規定含有鉛等六類物質產品不得輸入歐盟國家,經濟部技術處長杜紫軍表示,國內輸歐電子產品,很多零組件都是下游廠商提供,若下游廠商生產的零組件含有禁止輸歐物質,即會遭到歐盟退貨。 旺旺友聯即將推出的RoHS新型保單,就是要控制廠商輸歐的這類風險,但承作這類保險的前提,必須要了解承保廠商的供應鏈,這是新型態的商業模式,因此經濟部以為期兩年,總計補助旺旺友聯集團1,620萬元,希望能夠協助廠商降低環保綠色規範所衍生的經營風險。 據了解,旺旺友聯曾經與宜特檢測公司等相關單位合作,並建置自動核保流程,所有輸歐的資訊電子業者都是旺旺友聯希望爭取的對象,尤其是兩岸輸歐的資訊電子廠商,初期估計兩年試辦期間的營收可達2,500萬元。
日前,国家食品药品监督管理局发出通知,曝光了“诺康舒眠宁”等十二种假药,并要求各省、自治区、直辖市食品药品监督管理部门加强对辖区内药品经营企业、医疗机构的监督检查,一旦发现,立即依法查处。 近日,国家食品药品监督管理局接到报告,反映在市场上有以伪造的医疗机构或研究机构的名义,违法宣传销售宣称具有治疗疾病功能的产品。经核实,报告反映的产品均为未经批准注册的假药,具体产品情况如下: 一、产品名称:“诺康舒眠宁”,标示研制单位名称:“中国中医药(国际)精神病医学研究总院”。 二、产品名称:“辉瑞健脑回春丹”,标示研制单位名称:“中国科学院脑病研究中心”。 三、产品名称:“宜康活力胶囊”,标示研制单位名称:“北京糖尿病研究所”、“中国生物科学制药有限公司”。 四、产品名称:“舒络疝立消”,标示研制单位名称:“中华国际疝病治疗中心”、“中华国际疝病(京)治疗中心”。 五、产品名称:“安神解郁养心胶囊”,标示研制单位名称:“北京中医药研究总院”、“北京巨仁堂药业股份有限公司”。 六、产品名称:“清脑清血清肝降压胶囊”,标示研制单位名称:“中国中医学会高血压专研中心”。 七、产品名称:“拜耳·愈压宁”,标示研制单位名称:“中国(国际)中医药高血压研究总院”。 八、产品名称:“拜耳·胰康王”、“红星一号胶囊”、“奥邦·生胰肽”、“奥邦·生胰素”、“诺尔·骨肽”,标示研制单位名称: “中国人民解放军军事医学科学糖尿病专研院”、“中国(国际)中医药糖尿病研究总院”、“中国(国际)中医药糖尿病联合会”、“北京东城区东单同芝堂大药房”、“首都协和医学院骨病专科”、“中国国际红十字会总会糖尿病救助中心”、“中科院糖尿病研究中心”。 国家食品药品监督管理局要求各省(区、市)食品药品监督管理局依法加强辖区药品市场监督检查,发现上述产品,依法严肃查处;涉嫌刑事犯罪的,按照“最高人民法院、最高人民检察院关于办理生产、销售假药、劣药刑事案件具体应用法律若干问题的解释”移送公安机关追究刑事责任。 国家食品药品监督管理局提醒患者不要购买上述产品,避免贻误诊治,危害身体健康。同时提醒患者去正规有资质的药店或医疗机构购买药品;查询药品是否经过批准注册应登陆国家食品药品监督管理局官方网站查询。
现代人由于快节奏的生活以及强大的工作压力,大部分人的胃都处于亚健康状态。不少人对此不屑一顾,认为胃病不是什么大病,挺一挺就过去了,往往疏于预防,延误治疗,造成严重问题。伤胃的“十大恶习”为什么白领阶级、职业记者、专业司机、空中小姐、影星歌星以及新兴的SOHO族们,容易患胃病,这与职业带来的不良生活习惯密切相关。归纳起来,伤胃的恶习有十种:一曰精神紧张长期精神紧张会通过大脑皮层影响植物神经系统,使胃粘膜血管收缩,胃功能紊乱,胃酸和胃蛋白酶分泌过多,导致胃炎和溃疡发生。二曰过度劳累无论从事体力劳动还是脑力劳动,都不能过度劳累,否则就会引起消化器官供血不足,胃粘膜分泌失调,从而导致种种胃病发生。三曰饥饱不均饥饱不均对胃有很大的伤害,饥饿时胃中空空,胃粘膜分泌的胃酸和胃蛋白酶很容易伤害胃壁,导致急、慢性胃炎或溃疡发生。暴饮暴食甚至会导致急性胃扩张、胃穿孔。四曰酗酒无度酒精会使胃粘膜发生充血水肿、甚至糜烂出血而形成溃疡。长期饮酒还损害肝脏,会引起酒精性肝硬化,胰腺炎的发生也与酗酒有关,这些损害反过来又会加重对胃的伤害。五曰嗜烟成癖吸烟会引起胃粘膜血管收缩,使胃粘膜中的前列腺素合成减少,使胃粘膜受到伤害。吸烟又会刺激胃酸和胃蛋白酶的分泌,所以嗜烟成癖是引起各种胃病的重要诱因。六曰浓茶咖啡浓茶和咖啡都是中枢兴奋剂,能通过神经反射以及直接的影响,使胃粘膜发生充血、分泌功能失调、粘膜屏障破坏,促成发生溃疡病。七曰狼吞虎咽进食时狼吞虎咽,食物未经充分咀嚼,势必增加胃的负担。细嚼慢咽时唾液分泌增多,在保护胃粘膜的作用,可避免不良刺激物对胃粘膜的损害。八曰睡前进食睡前进食不仅影响睡眠,而且会刺激胃酸分泌,容易诱发溃疡。九曰不讲卫生幽门螺杆菌感染是导致胃炎、溃疡和胃癌发病的元凶,它可以通过餐具、牙具、接吻等相互传染。因此,讲究卫生,可以预防幽门螺杆菌感染,从而可以预防各种胃病。十曰监用药物常用的能损伤胃粘膜的药物有三类:一类是解热镇痛药如阿司匹林、保泰松、消炎痛等;一类是激素类药如强的松、地塞米松;还有一类是抗菌药如红霉素等。注意应用这类药物时,要严格遵医嘱慎而用之,以避免对胃造成损伤。保胃的“十字诀窍”胃病三分治七分养,合理的膳食结构是健康的基础、“保胃”的前提,如何才是合理的膳食结构呢,《健康快车》有个很好的归纳,就是十个字:“红黄绿白黑”+“一二三四五”:所谓“红黄绿白黑”,就是五种对健康大有裨益的食物:“红”是一天一个西红柿,熟吃西红柿,效果更好。“黄”是指老玉米、胡萝卜、老南瓜、红辣椒等,这些食物维生素A多。“绿”是指绿茶,绿茶含有多种抗氧自由基物质。 “白”是指燕麦片,它不但可降低胆固醇,还对糖尿病、减肥有特别好的功效。“黑”是指黑木耳,科学实践证明黑木耳能降低血黏度,每天吃5-15克就行了。 所谓“一二三四五”,是关于每个人每天健康膳食的五个要点:“一”是每天一袋牛奶。我们中国的膳食有很多优点,但是缺钙,几乎90%的人都缺钙。大多数中国人的伙食里只有500毫克钙,还有300毫克的缺口———正好一袋牛奶就有300毫克的钙,所以每天补充一袋牛奶,就齐了。“二”是250克主食。每天250克碳水化合物,即半斤大米或麦面粉,体力劳动多的可以多一些,一些稍胖体力劳动又较少的女性可以适量减少一点。但吃饭要按四条规矩进行:饭前喝汤,进食速度慢,多咀嚼,晚饭吃得少,这样体重就很容易维持正常。 “三”是三份高蛋白。可从“一两瘦肉、一个鸡蛋,2两豆腐、2两鱼虾、2两鸡鸭、半两黄豆”中任意选择,每天要有三份———比如早上吃了一个荷包蛋,中午吃一个肉片苦瓜,晚上吃2两豆腐或2两鱼。“四”是四句话:有粗有细、不甜不咸、三四五顿、七八分饱。有粗有细,就是要粗细粮搭配,营养有互补作用。不甜不咸,是说不要净吃甜的,或不要吃太多甜的;也不要吃得太咸,一天吃6克左右的盐就适中。三四五顿,是指变每天三餐为四五顿,少吃多餐。早餐与午餐中间加一顿点心餐,下午四五时吃一顿,晚饭吃得晚一些,这样总量不变而不是越吃越多。七八分饱,是指要低热量膳食,七八分饱即可,这点非常重要。“五”是500克蔬菜和水果。 这是预防癌症的最好办法,对食道癌、胃癌能减少一半以上。
本次采购国家水环境质量监测网300个水质自动监测站2017年-2019年连续3年的运行维护服务。(2017年度服务期:2017年5月1日-2018年4月30日 2018年度服务期:2018年5月1日-2019年4月30日 2019年度服务期:2019年5月1日-2020年4月30日) 根据水站建设及上收进度,计划2017年5月1日起开展126个水站大运维,33个国界水站小运维,2018年5月1日起开展254个水站大运维,46个水站小运维(具体要求详见第四章服务需求书)。委托合同根据运维服务考核情况及招标人预算批复情况,逐年签订。 此次采购按照地理连片分区,划分了6个包。同一投标人及与其存在直接控股或直接参股关系的其他投标人可以参加本项目不同包的投标,但按包号顺序最多只能中两包。(本文中所述“直接控股关系”是指:直接持有其他投标人50%以上股权或被其他投标人直接持有50%以上股权。“直接参股关系”是指:虽直接持有其他投标人股权或被其他投标人直接持有股权,但该持股或被持股关系未形成控股或被控股,管理与被管理的关系。) 二、投标人的资格要求: (1) 满足《中华人民共和国政府采购法》第二十二条要求,包括:a.具有独立承担民事责任的能力 b.具有良好的商业信誉和健全的财务会计制度 c.具有履行合同所必须的设备和专业技术能力 d.有依法缴纳税收和社会保障资金的良好记录 e.参加此采购活动前三年内,在经营活动中没有重大违法记录 f.符合法律、法规规定的其他条件。(2) 投标人在本项目开标前五年内,在环境监测服务活动中未发生过数据弄虚作假行为(以市级及以上环保部门出具的行政处罚决定或整改通知等处理文件为准),投标人须提供加盖公章的承诺函。(3) 鉴于国家环境信息安全和相关政策考虑,不接受外商全资企业或外资控股单位的投标。(4) 投标人应在中华人民共和国境内注册,不能是被列入“信用中国”网站(www.creditchina.gov.cn)失信被执行人、重大税收违法案件当事人名单、政府采购严重违法失信行为记录名单的供应商。(5) 投标人必须从中化国际招标有限责任公司购买招标文件并登记备案。(6) 本次招标不接受联合体投标,不允许分包和转包。 三、招标文件的发售时间及地点等: 预算金额:14625.0 万元(人民币) 时间:2017年03月03日 08:30 至 2017年03月10日 16:30(双休日及法定节假日除外) 地点:北京市复兴门外大街A2号中化大厦大堂西侧售标书处 招标文件售价:¥500.0 元,本公告包含的招标文件售价总和 招标文件获取方式:网络标书销售:登陆中化国际招标有限责任公司网站 http://www.sinochemitc.com/zb,进入网络标书销售系统购买。购标人需先进行网上注册(免费),具体步骤请参考登陆页面的《使用手册》。 现场文件领取地点:北京市复兴门外大街A2号中化大厦大堂西侧售标书处 标书发售联系人:马翠玲、王晓斌 联系方式:电话:010-59368256、010-59368971 传真:010-59368911 联系邮箱:wang_xb@sinochem.com 文件售价:每包人民币伍佰元整(500元)。如需邮寄加收100元邮寄费,招标文件售后不退。 四、投标截止时间:2017年03月27日 09:00 五、开标时间:2017年03月27日 09:00 六、开标地点: 北京复兴门外大街A2号中化大厦19层第七会议室 七、其它补充事宜 分包预算: 1.包1华南片区:总预算3164万元/3年。 (1)2017年度:大运维29个水站,小运维3个水站,2017年度预算540万元/年。 (2)2018年度/2019年度:大运维65个水站,小运维5个水站,2018年度/2019年度预算:1312万元/年。 2.包2华北片区:总预算2990万元/3年。 (1)2017年度:大运维24个水站,小运维4个水站,2017年度预算515万元/年。 (2)2018年度/2019年度:大运维53个水站,小运维6个水站,2018年度/2019年度预算:1237.5万元/年。 3. 包3华东片区:总预算2796万元/3年。 (1)2017年度:大运维32个水站,小运维0个水站,2017年度预算542万元/年。 (2)2018年度/2019年度:大运维65个水站,小运维0个水站,2018年度/2019年度预算:1127万元/年。 4.包4西南片区:总预算1936万元/3年。 (1)2017年度:大运维13个水站,小运维5个水站,2017年度预算405万元/年。 (2)2018年度/2019年度:大运维25个水站,小运维7个水站,2018年度/2019年度预算:765.5万元/年。 5.包5东北片区:总预算2033万元/3年。 (1)2017年度:大运维17个水站,小运维17个水站,2017年度预算556万元/年。 (2)2018年度/2019年度:大运维22个水站,小运维22个水站,2018年度/2019年度预算:738.5万元/年。 6.包6西北片区:总预算1706万元/3年。 (1)2017年度:大运维11个水站,小运维4个水站,2017年度预算317万元/年。 (2)2018年度/2019年度:大运维24个水站,小运维6个水站,2018年度/2019年度预算:694.5万元/年。 具体分包情况详见招标文件。 八、采购项目需要落实的政府采购政策: 财库〔2011〕181号《政府采购促进中小企业发展暂行办法》[b] 那些公司将来瓜分亿元水站运维大单呢?[/b]

背景: 据扬子晚报报道,江苏镇江一农户承包的几十亩西瓜,近几天,不管个头大小、成熟与否接连炸裂。有人怀疑可能与使用西瓜"膨大增甜剂"有关,记者咨询相关专家后,解释说可能与天气因素有关。但具体原因还不能下定论。http://ng1.17img.cn/bbsfiles/images/2011/05/201105230847_295583_1641058_3.jpg 1、膨大剂主要包含哪些成分? 膨大剂这个名称比较混乱,现在看最靠谱的就是氯吡脲了。这是一种可以促进植物细胞分裂,提高坐果率的化学物质。 2、对蔬果营养、口味、安全性有什么影响? 口味上可能会有影响,比如过量使用,可能会让甜瓜变苦。营养成分应该没有明显变化,可能会影响有机酸酸和糖的合成。 安全性还可以,只要不过量使用,不会引起中毒,动物实验的数据,小白鼠口服急性中毒剂量为每千克体重4918毫克。如果长期接触可能会引起体内蛋白质紊乱。不过,在通常条件下,膨大素降解较快,在喷施到植物上24小时后就有60%发生降解。即使进入动物体内后,膨大素也不会赖着不走,实验老鼠吃下去的膨大素在7天后只有2%存在于老鼠体内。 毒性:属低毒植物生长调节剂。原药大鼠急性经口LD50为4918毫克/千克,大鼠急性经皮LD50〉20000毫克/千克,对兔眼睛和皮肤有轻微刺激作用。鱼毒LC50(96小时),虹鳟鱼9.2毫克/千克。 3、长期食用,对人体有没有危害? 长期接触对肝肾的影响还在研究中,还没有直接的实验证据。目前也没有致癌的证据。
我们单位的液氮罐每隔一阵就会自动放气,声音巨大,大的都有些吓人,让你觉得它快爆炸了,你们的液氮罐放气时声音大吗?大家都用什么型号的液氮罐。
我们知道,PeproTech的所有细胞因子和蛋白均为冻干粉,这使得运输非常便捷,只要常温即可。而且,细胞因子和蛋白冻干粉非常稳定,在-20℃或-80℃条件下可保存数年。冻干粉在使用前需进行溶解,然后以液体形式加到培养体系或注射入动物体内。溶解步骤非常关键,因溶解不好会导致细胞因子或蛋白的失活,这也是很多用户在实际使用中经常遇到的问题。 那么,应该如何进行正确的溶解呢? 下面我们以Recombinant Human IL-4 (重组人IL-4,产品编号:200-04)的说明书为例,对细胞因子或蛋白的溶解方法进行详细的阐述。 拿到重组人IL-4的说明书后,您会发现有一段关于Reconstitution(重悬)的叙述,这段内容含有溶解相关的所有信息。 1. Centrifuge the vial prior to opening.第1步:开盖前离心试剂管 PeproTech的细胞因子或蛋白冻干粉装盛在塑料管中,为无菌包装。冻干粉在运输过程中可能会因颠簸而漂散并粘贴于管壁或管盖上,所以在打开塑料瓶盖前,需将冻干粉通过离心收集到管底,以便用很小体积的液体即可将冻干粉完全溶解。 有很多用户会问一个问题,即应该用多少转速、多长时间离心试剂管,才能达到良好的收集效果?答:有些小型高速离心机(多为进口品牌)的面板上有一个Spin键,按了此键后,离心机会自动快速上升到其最大速度(10000rpm或12000rpm),上升到最高点后速度即刻下降,直至停止旋转,整个过程大约30s。这个Spin键足以很好的将细胞因子或蛋白收集到管底。 但有些实验室没有这样的高速离心机,只有最高转速为4000-4500rpm的离心机。这种情况下,需3000-3500rpm离心5min,也能达到类似的效果。 2. Reconstitute in water to a concentration of 0.1-1.0 mg/ml. Do not vortex.第2步:用无菌水重悬至0.1-1.0 mg/ml,不可振荡。 这个步骤即为溶解步骤,非常重要。 1) 一定要用推荐的溶液重悬(或溶解)冻干粉 用于溶解细胞因子或蛋白的溶液千差万别。此例中的重组人IL-4需用水溶解,而重组人IL-2 (产品编号:200-02)则需用100mM Acetic Acid (醋酸)溶解,重组人TGF-beta1 (产品编号:100-21)需用10mMCitric Acid (柠檬酸),pH3.0溶解,重组人FGF-basic(产品编号:100-18B)需用5mMTris,pH7.6溶解,重组人FGF-10(产品编号:100-26)需用5mMSodium Phosphate(磷酸钠),pH7.4溶解,重组IL-13(产品编号:200-13)需用20mMMHCl溶解。(注:即使同一重组细胞因子或蛋白,不同批次的溶解方法也可能有所不同,因此上面的叙述仅供参考。具体应该如何溶解应以相应批次的官方说明书为准)。后续的文章中将对各种溶解液的配制方法进行详细的阐述,望继续关注。 经常有用户会问,为什么会有这么多种溶解方法?答:我们知道,蛋白的溶解性与很多因素有关,其中比较重要的是pH值和离子强度。PeproTech的细胞因子或重组蛋白在出厂前均经严格测试,说明上所标明的溶解液是能够将该细胞因子或重组蛋白完全溶解的液体。如果您所用的溶解液的pH值和离子强度与说明书中所标明的不符,很多时候会造成细胞因子或重组蛋白不能完全溶解或者根本无法溶解,这样所配得的细胞因子或重组蛋白必然活性不够或丧失。 有不少用户没注意说明书上的描述,而是根据习惯,直接用PBS或培养液(1640或DMEM等)等溶解细胞因子或蛋白的冻干粉。这样做可以吗?答:有时可以,要看具体情况。PeproTech的大多数细胞因子或蛋白冻干粉的溶解液不是PBS,此时千万不能用PBS或培养液直接来溶解,具体原因在上面已经叙述过。而有部分细胞因子,如重组人KGF(产品编号:100-19)和重组人FGF-23(产品编号:100-52)等,说明书上的溶解液即为1x PBS,此时用PBS溶解完全没问题,那么用培养液溶解也是可以的,不过最好还是用先用PBS溶解,然后再用培养液稀释。
[font=宋体]在现代生命科学研究中,[url=https://cn.sinobiological.com/resource/protein-review/protein-production][b]重组蛋白表达技术[/b][/url]扮演着至关重要的角色。通过将外源基因导入宿主细胞,并使其表达特定蛋白,我们能够获取大量高纯度的重组蛋白,为疾病治疗、药物研发和生物工程等领域提供了强有力的支持。本文将介绍重组蛋白表达的原理、表达系统、生产步骤以及应用前景。[/font][font=宋体][b]一、重组蛋白表达的原理[/b][/font][font=宋体][font=宋体]重组蛋白表达是利用[/font][font=Calibri]DNA[/font][font=宋体]重组技术,将目标基因(外源基因)导入宿主细胞中,并通过宿主细胞的生物机制使其表达出特定蛋白。其主要步骤包括:[/font][/font][font=宋体][font=宋体]基因克隆:将目标基因经过[/font][font=Calibri][url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url][/font][font=宋体]扩增后,与表达载体连接,形成重组质粒。[/font][/font][font=宋体]转染或转化:将重组质粒导入宿主细胞中,可以使用化学方法、电穿孔或者嗜热菌等方式进行转染或转化。[/font][font=宋体]表达蛋白:重组质粒进入宿主细胞后,融合到宿主细胞的染色体中,随后遵循细胞的转录和翻译机制,表达出目标蛋白。[/font][font=宋体] [/font][b][font=宋体]二、常见的重组蛋白表达系统[/font][/b][font=宋体]大肠杆菌表达系统:大肠杆菌是常用的重组蛋白表达宿主细胞之一。其优点在于生长快速、易于培养,并且能够产生大量的蛋白。此外,大肠杆菌的遗传工具和代谢途径也被广泛研究,提供了便利。[/font][font=宋体]酵母表达系统:酵母表达系统包括酿酒酵母和毕赤酵母。这些酵母细胞具有真核细胞的特点,能够进行正确的蛋白折叠和修饰。同时,酵母细胞也可以进行大规模培养和高表达,适用于一些复杂蛋白的表达。[/font][font=宋体]昆虫细胞表达系统:昆虫细胞表达系统常用于大规模蛋白表达。昆虫细胞具有真核细胞的优势,能够对蛋白进行正确的折叠和修饰,适合于表达大量需求复杂结构的重组蛋白。[/font][font=宋体]哺乳动物细胞表达系统:哺乳动物细胞的表达系统可用于高效表达复杂蛋白和进行蛋白质研究。哺乳动物细胞具有真核细胞特点,能够进行正确的蛋白质修饰和折叠,并且在一些特殊情况下需要考虑到人类蛋白的免疫原性。[/font][font=宋体] [/font][font=宋体][b]三、重组蛋白生产步骤[/b][/font][font=宋体] [/font][font=宋体]细胞中有两个蛋白生产阶段:转录和翻译,被称为分子生物学的中心法则。换言之,转录和翻译步骤属于重组蛋白表达步骤。[/font][font=宋体] [/font][font=宋体]为了生产重组蛋白,基因被分离并克隆到表达载体中。重组蛋白的生产需要蛋白表达系统、蛋白纯化系统和蛋白识别系统。[/font][font=宋体] [/font][font=宋体][b]获取重组蛋白的基本步骤:[/b][/font][font=宋体] [/font][font=宋体][font=Calibri]1.[/font][font=宋体]目标基因的扩增。[/font][/font][font=宋体][font=Calibri]2.[/font][font=宋体]插入克隆载体。[/font][/font][font=宋体][font=Calibri]3.[/font][font=宋体]亚克隆到表达载体中。[/font][/font][font=宋体][font=Calibri]4.[/font][font=宋体]转化到蛋白表达宿主中[/font][font=Calibri]([/font][font=宋体]细菌[/font][font=Calibri]([/font][font=宋体]大肠杆菌[/font][font=Calibri])[/font][font=宋体]、酵母细胞、哺乳动物细胞或杆状病毒[/font][font=Calibri]-[/font][font=宋体]昆虫细胞系统[/font][font=Calibri])[/font][font=宋体]。[/font][/font][font=宋体][font=Calibri]5.[/font][font=宋体]重组蛋白鉴定试验[/font][font=Calibri](Western blot[/font][font=宋体]或荧光[/font][font=Calibri])[/font][/font][font=宋体][font=Calibri]6.[/font][font=宋体]大规模生产。[/font][font=Calibri]([/font][font=宋体]大规模发酵[/font][font=Calibri])[/font][/font][font=宋体][font=Calibri]7.[/font][font=宋体]分离和纯化。[/font][/font][font=宋体] [/font][font=宋体]需要考虑多种因素:[/font][font=宋体][font=Calibri]1.[/font][font=宋体]选择哪个宿主系统?[/font][/font][font=宋体][font=Calibri]2.[/font][font=宋体]如何分离和纯化重组蛋白?[/font][/font][font=宋体] [/font][font=宋体]选择适当的表达宿主或使用正确的纯化方法并不容易,应考虑目标重组蛋白的性质。下面列出了一些重要因素:[/font][font=宋体] [/font][font=宋体]? 膜结合[/font][font=宋体]? 溶解度[/font][font=宋体]? 单或多结构域[/font][font=宋体][font=宋体]? 大小[/font][font=Calibri]([/font][font=宋体]分子量[/font][font=Calibri])[/font][/font][font=宋体]? 表达位置[/font][font=宋体] [/font][font=宋体][font=宋体]对于大多数没有足够经验来表达和分离重组蛋白的人来说,重组蛋白的生产是非常耗时的。许多生物公司为各种不同规模的重组蛋白表达提供良好的服务:[/font][font=Calibri]https://cn.sinobiological.com/services/recombinant-protein-expression-service[/font][font=宋体],例如义翘神州[/font][/font][font=宋体] [/font][font=宋体][b]四、重组蛋白表达技术的应用前景[/b][/font][font=宋体]药物研发:重组蛋白表达技术被广泛应用于药物研发领域,用于生产重组蛋白药物。这些药物包括多肽类、蛋白类和抗体类药物,如生长因子、抗体药物和血液制剂等。通过重组蛋白表达技术,我们可以获得高效纯度的药物,满足临床上的需求。[/font][font=宋体]生物工程:重组蛋白表达技术被广泛应用于生物工程领域,用于生产特定的蛋白产品。这些产品可以应用于食品、化妆品、工业发酵等领域,如酶制剂、生物染料和生物材料等。[/font][font=宋体]疾病治疗:通过重组蛋白表达技术,我们能够合成特定的蛋白,用于疾病的治疗和诊断。例如,利用重组抗体技术,可以开发出用于癌症治疗和免疫治疗的抗体药物。[/font][font=宋体] [/font][font=宋体][font=宋体]详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/protein-production[/font][/font]
现在的生物仿制药市场规模并不算大,2012年,全球市场规模只达到约16亿美元,但是业界普遍公认,未来的10~15年是生物仿制药的黄金发展期。生物医药领域世界著名咨询公司IMS预测,到2015年全球生物仿制药市场会达到19~37亿美元的规模,更有其他权威机构大胆预测,2017年的这一数字会达到179亿美元。这也促使国内外不少著名药企纷纷投资进军生物仿制药市场。为何生物仿制药在全球范围内变得异常火爆,背后的原因、驱动因素究竟是什么?http://www.ibioo.com/data/attachment/portal/201309/22/095336emfm77zi8mflmlos.jpg高昂的医药成本压力持续已久且席卷全球尤其是欧美的经济危机,使本来就很昂贵、逐年上升的医药成本问题更加突出,尤其在只有3亿人口的美国,尽管人口不到全球的5%,但是其医药开销却高达全球的一半,占美国GDP总量的17.6%,位于全球发达国家之首。因此,本已债台高筑的美欧政府不得不想方设法通过降低药价来降低医疗开支。而价格昂贵的生物药(尤其是抗体药)随着一些原研药专利已经或者即将到期,在2015年后,生物仿制药有望为政府缩减医疗成本增加不少机会。而对于新兴市场国家如巴西、印度和中国而言,生物仿制药同样有很大的发展空间。这些国家都有众多的人口,随着经济的发展和不断提高的医疗保险覆盖人口范围的扩大,对医药需求必然要高于发达国家的增幅。然而,作为发展中国家,其有限的财政预算也迫使政府必须要对上述需要和对创新原研药的需求做一个平衡,在此情况下,生物仿制药胜出几乎是没有悬念的。对于韩国、印度、巴西等国而言,生物仿制药也被视为重要的宏观经济的增长引擎,这些国家通过建立先进制造和研发中心吸引不少外商投资。对于我国而言,这一趋势也日益明显。其中一个例子和信号就是,去年,世界最大的独立生物公司安进高调进入中国,并在上海设立中国分公司,决定要和中国的合作企业一同开发生物仿制药。到期的生物药专利生物仿制药火爆的另外一个重要因素是:不少全球销量最大的生物原研药的专利已经或者不久将到期。这从图一可以清楚看出,全球销售额最高的10种生物药(最高每年82亿美元,最低每年24亿美元),其专利到期时间均集中在2012年到2019年间。仅仅这10种生物药,其销售总额在2011年就高达575亿美元,因此,生物仿制药有巨大的市场潜力并不是空穴来风。值得一提的是,基因泰克(Genentech,现属罗氏)和安进(Amgen)两家公司就分别拥有Top10生物药中的4种和2种,这也充分显示了作为全球最大、最著名的两家生物公司的实力。如果按照生物药的治疗领域来划分,主要集中于以下几个领域:糖尿病(胰岛素)、类风湿性关节炎(主要是靶向肿瘤坏死因子TNF类抗体)以及肿瘤。上述三大治疗领域现在仍然是生物药的最主要的适应症范围,且在全球均有至少上百亿美元的市场。由于此类药物需要长期使用,因此市场前景较好,这也是生物仿制药以后的主要竞争领域。而据最新报道,我国的糖尿病患者已经高达上亿人,占全球的三分之一,所以,可以预见的是,我国将成为治疗糖尿病的胰岛素全球第一大市场。但是胰岛素仿制药属于所谓的第一波(或第一轮)生物仿制药,而上世纪末兴起的第一波生物仿制药中还包括图二中的分子量相对较小的G-CSF(粒细胞集落刺激因子)和EPO(促红细胞生成素),我国本土制药公司均有生产供应国内市场并出口境外。目前,第二波生物仿制药主要是仿制抗体类药物,尤其是图一中的10大抗体药物更是仿制热点目标。对生物药的巨大需求生物仿制药既反映了市场急于寻找昂贵药物的廉价替代品,更反映了市场对生物药这些特殊药的不断增长的巨大需求。自从1982年全球第一个生物药在美国诞生以来,生物药的市场规模以超过化学药的增速迅速扩大,2012年全球生物药已经超过1600亿美元的规模,大约相当于药物市场总规模的16%~17%。由于原研生物药的制造商还会不断发现生物药新的适应症和推出全新的生物药,上述比例预计还将不断增长。据预测,到2017年,全球生物药的规模将达到2520亿美元。在生物药30余年的历史中,标志性生物药包括全球第一个、1982年在美国获批的Humulin(即用于治疗糖尿病的重组胰岛素),阿替普酶(纤维蛋白溶酶原激活药,t-PA)以及EPO、G-CSF和单克隆抗体。值得一提的是,2012年在全球销售额最大的10种药品中,生物药已经超过一半,其中销量冠军是雅培(即现在拆分后的艾伯伟AbbVie)的阿达木单抗(Humira,治疗类风湿性关节炎),2012年的销售额为92.6亿美元,今年有望突破百亿美元大关。自从小分子化学药、著名的降脂药、辉瑞的立普妥(Lipitor)专利到期后,全球药品销售冠军甚至包括亚军就是生物药的天下了。当然,生物仿制药之所以火爆还有其他多种原因,比如近年来,新药研发成本不断攀升(尤其是对于大型药企而言),投资收益比不断下降,不少跨国大型制药公司也在缩减研发开支,在此形势下,开发风险更低的生物仿制药对于一些创新药企而言是无奈又必然的选择。
[b][color=#cc0000][font=微软雅黑]问:招标文件可以限定投标人的投标包数和中标包数吗?[/font][/color][/b][font=微软雅黑][color=#cc0000][b]答:采购人应当综合专业要求、管理要求、政策要求等综合因素,对采购项目合理分包。投标人参与项目投标,选择投标包数,是其自主权力,采购人不得限定。是否可以限定投标人的中标包数,目前现行法规无禁止性规定,采购人可以结合项目实际情况、产业发展状况和合同履约需要,在招标文件中合理设置投标人的中标包数。[/b][/color][/font]
95%。目前细胞分选主要用于研究,临床应用较少。血液学应用最多的是造血干细胞的研究,最近随着造血理论的深入研究关于造血干细胞究竟是否都是CD34+细胞出现一些争论,实验研究证明, CD34-造血干细胞较CD34+造血干细胞更具造血潜能,这些实验研究所用的CD34- 和CD34+细胞就是通过细胞分选获得的。小鼠造血干细胞分选一般按lin-c-Kit+CD34+/ lin-c-Kit+CD34-分选,人造血干细胞分选一般按lin-CD34+/ lin-CD34-分选。 为避免某些遗传性血液病如海洋性贫血、异常血红蛋白病的纯合子出生,产前诊断非常重要,这些疾病的主要靶细胞是红细胞,而孕妇血循环中存在着胎儿有核红细胞,只是数量非常少,利用流式细胞仪可从孕妇血液中分选出胎儿有核红细胞(分选条件:CD45-GPA+)进行基因分析,作出产前诊断。利用流式细胞仪分选免疫担当细胞进行细胞免疫学研究也是目前的热门课题。总之,流式细胞仪能够分选出你想得到的任何一亚群细胞,只要你想得到的某一亚群细胞有合适的单克隆抗体标记,流式细胞仪的分选功能将得到越来越多的科学研究和临床应用。二十二. 流式细胞术在血液学中的应用 其他流式细胞仪可能在两方面对骨髓增生异常综合症(MDS)有用,一是测定CD34阳性细胞数,以监测病情,二是测定核蛋白增殖因子(PCNA),有报告PCNA再在生障碍性贫血、骨髓增生异常综合症、白血病三种疾病中表达有明显差异,可辅助鉴别诊断。 此外流式细胞仪也可检耐药蛋白,如肺耐药相关蛋白(LRP)、多药耐药蛋白(MRP)、 P170等。 流式细胞仪也可检测细胞因子,细胞内细胞因子如白介素系列(IL-1—IL-14),肿瘤坏死因子(TNF),干扰素(IFN)等,[/color
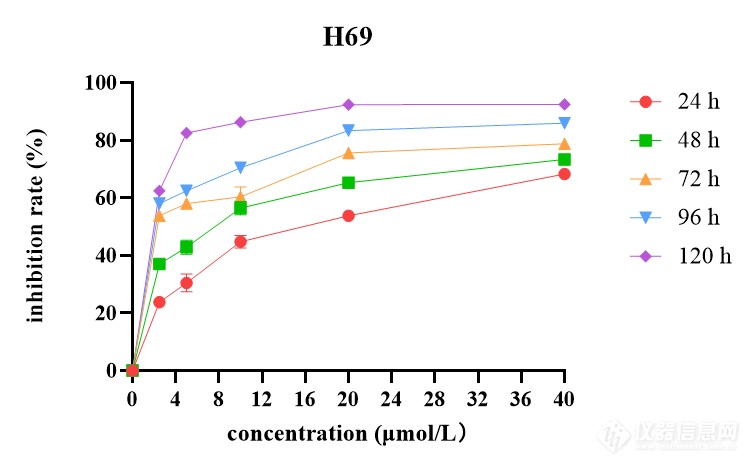
[align=left][size=18px]西达本胺促进[/size][size=18px]S[/size][size=18px]CLC[/size][size=18px]细胞系组蛋白乙酰化[/size][/align][align=left][size=18px] [/size][size=18px] [/size][size=16px]为验证西达本胺是否上调[/size][size=16px]SCLC[/size][size=16px]细胞系的乙酰化水平,我们使用[/size][size=16px]Western blot[/size][size=16px]检测了不同浓度([/size][size=16px]I[/size][size=16px]C10[/size][size=16px]、[/size][size=16px]IC20[/size][size=16px]、[/size][size=16px]IC50[/size][size=16px])西达本胺处理[/size][size=16px]4[/size][size=16px]8[/size][size=16px] [/size][size=16px]h[/size][size=16px]后,[/size][size=16px]S[/size][size=16px]CLC[/size][size=16px]细胞系中乙酰化组蛋白[/size][size=16px]H[/size][size=16px]3[/size][size=16px]、[/size][size=16px]H[/size][size=16px]4[/size][size=16px]表达水平,并以组蛋白[/size][size=16px]H[/size][size=16px]3[/size][size=16px]、[/size][size=16px]H[/size][size=16px]4[/size][size=16px]表达水平为对照。结果如图所示。在四种亚型细胞系中,总组蛋白[/size][size=16px]H[/size][size=16px]3[/size][size=16px]、[/size][size=16px]H[/size][size=16px]4[/size][size=16px]表达水平无变化,乙酰化组蛋白[/size][size=16px]H[/size][size=16px]3[/size][size=16px]、[/size][size=16px]H[/size][size=16px]4[/size][size=16px]表达量随加药浓度增大而增多,这证明了西达本胺对[/size][size=16px]S[/size][size=16px]CLC[/size][size=16px]细胞系组蛋白乙酰化的促进作用,这种作用呈剂量依赖性。[/size][/align][align=left][size=18px]A[/size][/align][align=left][img]https://ng1.17img.cn/bbsfiles/images/2022/11/202211302350400898_8640_5887180_3.png[/img][/align][align=left][/align][align=left][/align][align=left][/align][align=center][/align][align=left][size=18px] [/size][size=18px]西达本胺通过线粒体凋亡途径诱导[/size][size=18px]S[/size][size=18px]CLC[/size][size=18px]细胞系凋亡[/size][/align][align=left][size=16px]我们的功能实验表明,西达本胺[/size][size=16px]可剂量依赖的[/size][size=16px]促进[/size][size=16px]SCLC[/size][size=16px]细胞[/size][size=16px]系[/size][size=16px]凋亡[/size][size=16px],但其机制尚未明确。[/size][size=16px]依据国内外报道,西达本胺主要通过线粒体凋亡途径诱导细胞凋亡[/size][size=16px]。除此之外,[/size][size=16px]西达本胺[/size][size=16px]能[/size][size=16px]使[/size][size=16px]线粒体[/size][size=16px]DNA[/size][size=16px]双链断裂,发生损伤。[/size][size=16px]为探究其是否通过此途径在[/size][size=16px]S[/size][size=16px]CLC[/size][size=16px]细胞系中发挥作用,我们检测了加药[/size][size=16px]4[/size][size=16px]8[/size][size=16px] [/size][size=16px]h[/size][size=16px]后,[/size][size=16px]H69[/size][size=16px]、[/size][size=16px]H[/size][size=16px]446[/size][size=16px]、[/size][size=16px]H[/size][size=16px]526[/size][size=16px]、[/size][size=16px]DMS114[/size][size=16px]细胞中由线粒体介导的[/size][size=16px]C[/size][size=16px]aspase[/size][size=16px]信号通路相关蛋白[/size][size=16px]Bcl-2[/size][size=16px],[/size][size=16px]Bax[/size][size=16px],细胞色素[/size][size=16px]C[/size][size=16px],[/size][size=16px]Ca[/size][size=16px]spase 9[/size][size=16px],[/size][size=16px]c[/size][size=16px]leaved Caspase 9[/size][size=16px],[/size][size=16px]P[/size][size=16px]ARP[/size][size=16px],[/size][size=16px]c[/size][size=16px]leaved [/size][size=16px]PARP[/size][size=16px],[/size][size=16px]Ca[/size][size=16px]spase 3[/size][size=16px],[/size][size=16px]c[/size][size=16px]leaved Caspase 3[/size][size=16px]以及[/size][size=16px]D[/size][size=16px]NA[/size][size=16px]双链断裂标志物[/size][size=16px] [/size][size=16px]γH2AX[/size][size=16px]表达水平。[/size][size=16px]Western blot[/size][size=16px]结果显示,[/size][size=16px]Ca[/size][size=16px]spase 9[/size][size=16px],[/size][size=16px]P[/size][size=16px]ARP[/size][size=16px] [/size][size=16px],[/size][size=16px]Ca[/size][size=16px]spase 3[/size][size=16px]表达水平无明显变化,[/size][size=16px]Bcl-2[/size][size=16px]表达下调,其余蛋白表达均上调。这些结果表明,在[/size][size=16px]S[/size][size=16px]CLC[/size][size=16px]细胞中,西达本胺可以通过线粒体凋亡途径诱导细胞凋亡。[/size][/align][align=left][/align][align=left][/align][align=left][/align][align=left][/align][align=left][/align][align=left][/align][align=left][/align][align=left][/align][align=left][size=16px]A[/size][/align][align=left][img]https://ng1.17img.cn/bbsfiles/images/2022/11/202211302350402755_79_5887180_3.png[/img][/align][align=left][size=18px] [/size][size=18px]西达本胺通过抑制[/size][size=18px]C[/size][size=18px]yclin-CDK[/size][size=18px]复合物活性阻滞[/size][size=18px]S[/size][size=18px]CLC[/size][size=18px]细胞系周期[/size][/align][align=left][font='宋体'][size=16px]据文献报道,[/size][/font][size=16px]不同[/size][size=16px]HDACI[/size][size=16px]对不同细胞阻滞时相不一致。为验证西达本胺对[/size][size=16px]SCLC[/size][size=16px]细胞周期的作用,我们检测了[/size][size=16px]经[/size][size=16px]西达本胺[/size][size=16px]处理[/size][size=16px]48[/size][size=16px] [/size][size=16px]h[/size][size=16px]后,[/size][size=16px]H69[/size][size=16px]、[/size][size=16px]H446[/size][size=16px]、[/size][size=16px]H526[/size][size=16px]、[/size][size=16px]DMS114[/size][size=16px]细胞中细胞周期相关蛋白的表达水平,如图所示。[/size][size=16px]在[/size][size=16px]H69[/size][size=16px]、[/size][size=16px]H526[/size][size=16px]、[/size][size=16px]D[/size][size=16px]MS114[/size][size=16px]细胞系中[/size][size=16px]P21[/size][size=16px]、[/size][size=16px]P27[/size][size=16px]表达上调,[/size][size=16px]C[/size][size=16px]yclin A2[/size][size=16px]与[/size][size=16px]C[/size][size=16px]DK[/size][size=16px]2[/size][size=16px]表达下调[/size][size=16px],[/size][size=16px]说明西达本胺阻滞[/size][size=16px]H69[/size][size=16px]、[/size][size=16px]H526[/size][size=16px]、[/size][size=16px]D[/size][size=16px]MS114[/size][size=16px]于[/size][size=16px]S[/size][size=16px]期。在[/size][size=16px]H446[/size][size=16px]细胞系中[/size][size=16px]C[/size][size=16px]yclin E1[/size][size=16px]与[/size][size=16px]C[/size][size=16px]DK2[/size][size=16px]表达下调[/size][size=16px],说明西达本胺阻滞其于[/size][size=16px]G[/size][size=16px]1[/size][size=16px]/S[/size][size=16px]期。[/size][/align][align=left][img]https://ng1.17img.cn/bbsfiles/images/2022/11/202211302350422585_1956_5887180_3.png[/img][size=16px] [/size][img]https://ng1.17img.cn/bbsfiles/images/2022/11/202211302350405804_8826_5887180_3.png[/img][/align][align=left][size=18px]小结[/size][/align][size=16px]1[/size][size=16px].[/size][size=16px]西达本胺可以增强[/size][size=16px]S[/size][size=16px]CLC[/size][size=16px]细胞系组蛋白乙酰化水平。[/size][size=16px]2.[/size][size=16px]西达本胺诱导[/size][size=16px]S[/size][size=16px]CLC[/size][size=16px]细胞凋亡的机制可能与其激活线粒体介导的[/size][size=16px]caspase[/size][size=16px]凋亡途径有关。[/size][size=16px]3[/size][size=16px].[/size][size=16px]西达本胺可阻滞[/size][size=16px]S[/size][size=16px]CLC[/size][size=16px]细胞周期,可能与其上调细胞周期蛋白激酶抑制剂表达、从而抑制[/size][size=16px]C[/size][size=16px]yclin-CDK[/size][size=16px]复合物活性有关。[/size]
水果树莓可明显抑制肝癌细胞系增殖,使肝癌细胞血管内皮生长因子(VEGF)的表达减弱,并使抑癌基因野生p53的表达增强。由哈医大附属第四医院刘明博士完成的一项国家自然基金课题,首次成功锁定树莓预防肝癌生长的两个特异性蛋白质作用靶点,为果蔬预防原发性肝癌提供了重要的理论依据。这一成果近日获得2008年度黑龙江省医药卫生科技进步一等奖。 2000年,刘明博士赴美国康奈尔大学研修深造期间,尝试将树莓中的鞣化酸与肝癌细胞混合培养,发现前者能显著抑制后者的生长。近年来,他从医学、营养学等角度开展了“树莓预防及抑制肝癌机制的研究”。 研究结果表明,随着树莓中植物化学物质浓度的增加,总抗氧化自由基清除能力也随之增强。0.25毫克/毫升至10毫克/毫升的树莓提取物对肝癌细胞系HepG-2的抑制率呈逐渐增加趋势,最高抑制率可达90%%左右。 在利用化学毒物黄曲霉毒素和二乙基亚硝胺建立的稳定大鼠原发肝癌模型上,随着树莓提取物浓度的增高,实验组大鼠肝脏上的瘤径变小,肿瘤的数量减少,成瘤率减低,结节程度减轻;肝癌细胞VEGF、增殖细胞核抗原表达的程度亦明显降低。同时,实验组大鼠血清在两种特异蛋白(M2597、M4513)质峰上与树莓干预组及正常大鼠血清差异明显,说明蛋白质峰M2597、M4513极有可能为树莓预防肝癌的蛋白质作用靶点。 专家评价,今后,利用树莓中提取的植物化学成分,进行合理搭配及组成预防剂,十分有助于防范肝癌的发生,并能抑制肝癌的发展,提高患者生存率。
11月9日,河南省水利厅2015年第二批农水安全工程(河南省农村饮水安全区域水质检测中心仪器设备采购)中标结果公布,本次采购仪器设备高达1168套,中标总额为5446万元。 日前,河南豫信招标有限责任公司受河南省水利厅的委托,按规定程序对包4和包6进行了复审会议,其中包4为92套紫外可见光分光光度计,限定国产品牌,原本由河南茂生仪科技有限公司以2687688元中标,复审结果改由北京普析通用仪器有限责任公司以3477600元中标。包6为71套原子吸收分光光度计,进口产品可投标,原本由郑州崇源科贸有限公司以9585000元中标,复审中标结果不变。http://www.instrument.com.cn/news/20151127/178625.shtml===============================================缘何很多仪器都由经销商投标?为什么厂家不直接投标?为什么厂商的价格高于经销商?
备受关注的四川食品药品局21台微波消解仪大单终于尘埃落定,CEM公司以单价13.285万的超低价格夺冠。具不完全分析,这是国内分析仪器采购历史上最大金额的进口微波消解仪单品招标项目,就是在资金雄厚且发达的上海、江浙、广州都不曾出现,而是出现在欠发达的西部城市成都,真是令人深思??第二包:微波消解仪(进口产品) 21台第一中标候选供应商四川骏骥商贸有限公司,报价金额:278.985万元(CEMMARS-XP55 ) 。 第二中标候选供应商成都瑞恒精密仪器有限责任公司,报价金额:327.6万元(MilestoneETHOS A)。第三中标候选供应商成都市海云物质有限责任公司,报价金额:405.72万元(安东帕Multiwave3000 )。
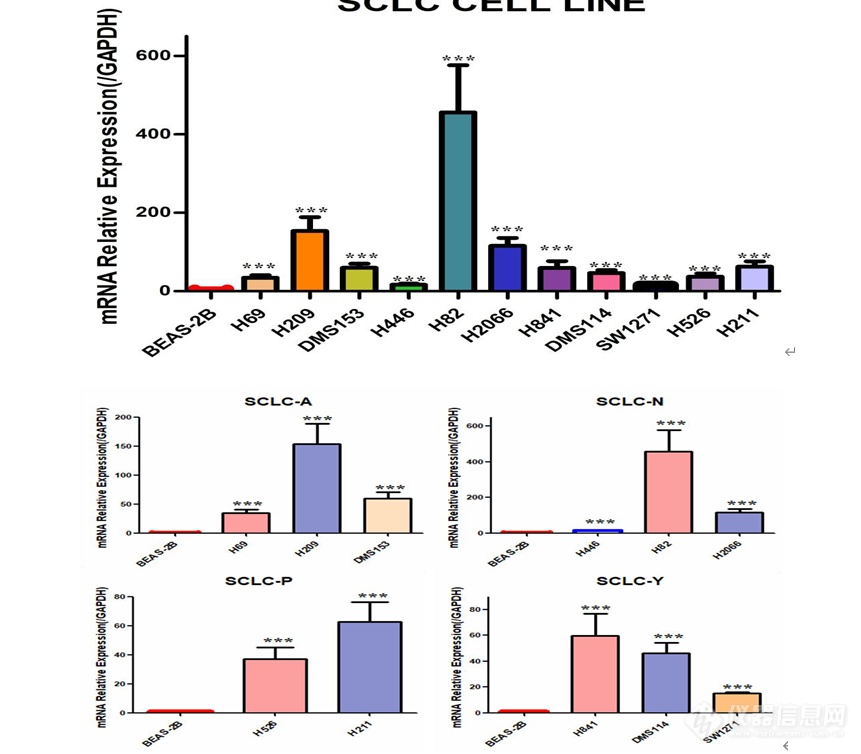
[font='times new roman'][color=#000007]MSI1[/color][/font][font='times new roman'][color=#000007] [/color][/font][color=#000007]在人小细胞肺癌细胞系中的表达及[/color][color=#000007] [/color][font='times new roman'][color=#000007]MSI1[/color][/font][font='times new roman'][color=#000007] [/color][/font][color=#000007]低表达[/color][color=#000000]细胞模型的构建[/color]MSI1 在人小细胞肺癌细胞系中高表达提取人正常肺上皮细胞 BEAS-2B,SCLC-A 型 H69、H209、DMS153 细胞,SCLC-N 型 H446、H82、H2066 细胞,SCLC-P 型 H526、H211 细胞,SCLC-Y 型 H841、DMS114、SW1271 细胞的 RNA,利用 q-[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url] 检测 MSI1 在正常肺上皮及小细胞肺癌细胞系中的表达情况,结果如图 2-1 显示,MSI1 在小细胞肺癌细胞系中的表达远远高于正常肺上皮细胞,综合分析,选取了 H69、H82、H526 及 SW1271 细胞用于后续实验。 [img]https://ng1.17img.cn/bbsfiles/images/2022/11/202211232326443512_4838_5389809_3.png[/img]图 小细胞肺癌细胞系中 MSI1 mRNA 的表达(***P0.001)MSI1 低表达细胞模型的构建本实验选取人小细胞肺癌细胞系 H69、H82、H526、SW1271 细胞,使用慢病毒感染技术敲低 MSI1 的表达,同时设置对照组除外病毒本身对细胞产生的影响,待细胞状态良好使用嘌呤霉素筛选, 然后在荧光显微镜下观察如图 , 可见 H69-NC 、H69-shMSI1-1、H69-shMSI1-2、H82-NC、H82-shMSI1-1、H82-shMSI1-2、H526-NC、H526-shMSI1-1、H526-shMSI1-2、SW1271-NC、SW1271-shMSI1-1、SW1271-shMSI1-2细胞均产生绿色荧光,表明人小细胞肺癌细胞慢病毒感染成功。 [img]https://ng1.17img.cn/bbsfiles/images/2022/11/202211232326451025_2121_5389809_3.png[/img]图 慢病毒感染后 4X 荧光显微镜下图片(H69、H82、H526、SW1271 明场及荧光照片) 敲低 MSI1 后转录和蛋白水平验证分别提取对数生长期的 H69-NC 、H69-shMSI1-1 、H69-shMSI1-2 、H82-NC 、H82-shMSI1-1、H82-shMSI1-2、H526-NC、H526-shMSI1-1、H526-shMSI1-2、SW1271-NC、SW1271-shMSI1-1、SW1271-shMSI1-2 细胞的 RNA 和蛋白,利用 q-[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url] 技术分别检测各细胞 MSI1 mRNA 相对表达量,结果如图 所示,与对照组相比,H69-shMSI1-1、 H69-shMSI1-2 、 H82-shMSI1-1 、 H82-shMSI1-2 、 H526-shMSI1-1 、 H526-shMSI1-2 、SW1271-shMSI1-1、SW1271-shMSI1-2 组 MSI1 mRNA 表达量明显降低(P0.01), 抑制率约为 75%。利用 Western blot 技术检测各细胞内 MSI1 蛋白的表达情况。结果如图 2-3 所示,与对照组相比,MSI1 蛋白表达在 H69-shMSI1-1、H69-shMSI1-2、H82-shMSI1-1、H82-shMSI1-2、H526-shMSI1-1、H526-shMSI1-2、SW1271-shMSI1-1、SW1271-shMSI1-2 细胞中明显降低。表明 MSI1 低表达细胞模型构建成功。[img]https://ng1.17img.cn/bbsfiles/images/2022/11/202211232326454704_2148_5389809_3.png[/img]图 敲低 MSI1 在转录水平和蛋白水平的验证(***P0.001)
[align=center][font=Verdana][b]浙大重点实验室被曝评估造假 高校有教授“一女嫁两夫”[/b][/font][/align] “前不久评估获得‘优秀’,没想到会发生这样的事情。”浙江大学环境与资源学院办公室工作人员说。 这位工作人员所说的“事情”,是指2009年10月31日,网上举报浙江大学污染环境修复与生态健康教育部重点实验室评估造假。一个月后,浙江大学给中国青年报记者发了一份关于“举报评估造假的情况说明”(以下简称“情况说明”)。 近日,记者在浙江杭州调查采访此事时发现,确有一些教授同时在两所高校担任专职,他们忙碌的“两栖”生活引起了争议。[b] 网友举报与浙大回应[/b] “浙江大学是一所以‘求是’学风著称的高等学府。但近年来,从论文、成果到学科评估、重点实验室评估等,常常靠虚假、欺骗为手段赢得‘好名声’。这次在教育部重点实验室评估中,浙大利用造假、欺骗的做法,玷污学术纯洁,令业界震惊。”笔名扬刚的作者在网上举报说。 举报者所指的实验室是浙江大学污染环境修复与生态健康实验室。据浙大介绍,该实验室于2003年经教育部批准立项建设,2005年通过验收。根据《高等学校重点实验室建设与管理暂行办法》和《教育部重点实验室评估规则》的要求,每5年参加一次评估。2009年,教育部组织对数理科学和地球科学领域教育部重点实验室进行评估。 举报者称,在评估中,浙大存在人员虚假。杨肖娥(实验室主任)的丈夫何振立在美国已全职工作10多年,早已不是浙江大学的人员,近十年也没有在浙大实验室待过。刘维屏在2005年就到浙江工业大学工作,是浙工大“最耀眼的旗帜”。若他们作为“污染环境修复与生态健康教育部重点实验室”的学术带头人和重要成员,显然是造假。 对此,浙江大学在给中国青年报记者的“情况说明”中称,何振立教授1999年以浙江大学访问学者身份到美国佛罗里达大学进行合作研究。2004年,何教授被聘为佛罗里达大学助理教授,2008年转为副教授。根据何教授的具体情况,校人事处决定保留其公职到2011年3月。其间,何教授一直参与浙江大学的相关研究工作,并联合发表论文。 浙江大学称,评估材料中收录的有关何教授的研究工作,均在本次评估统计数据要求范围内。其中,纵向课题为2000年度国家杰出青年科学基金项目“红壤质量演变的微生物学和生物化学机理及其调控”,资助年度为2001年1月至2004年12月 国家自然科学基金面上项目“土壤重金属污染微生物学及生物化学过程及诊断技术”,资助年度是2001年1月至2004年12月。 校方同时称,按《实验室评估申请书》有关“客座人员研究成果在署名本实验室名称前提下,视为固定人员情况填报”的要求,何教授的研究(包括合作研究)成果发表时,作者单位标注为“浙江大学污染环境修复与生态健康教育部重点实验室”的9篇论文统计时列入“标注论文”,标注为“浙江大学”的10篇论文统计时列入“未标注论文”。 记者查阅了相关文件,统计评估期限确为2004年1月至2008年12月 《实验室评估申请书》也确有上述要求。 关于刘维屏教授的情况,浙江大学回应称:他从1982年起为浙江大学教师,1995年被评聘为教授,1999年担任环资学院副院长 2005年10月经学校同意调往浙江工业大学工作 2009年5月被浙江大学聘为环资学院院长。本次评估材料中所收录的为刘教授2004年至2005年在浙江大学的研究工作。其中,纵向课题为2002年度国家杰出青年科学基金项目“环境化学:手性农药土壤污染化学修复基础研究”,资助年限为2003年1月至2006年12月 国家自然科学基金面上项目“土壤与植物中手性农药的对映体行为差异性”,资助年限是2003年1月至2006年12月。刘教授的研究成果发表时,作者单位标注为“浙江大学”或“浙江大学环资学院”的8篇论文统计时列入“未标注论文”。 另外,浙江大学称,2003年实验室建设申请报告、2004年实验室建设计划任务书和2005年实验室验收报告中,何振立、刘维屏教授均是该实验室人员。 记者调查发现,在实验室评估申请书中,何振立教授19篇在国外出版的学术刊物发表的论文,都是冠以美国佛罗里达大学、浙江大学多个名分。一篇论文署名常是六七个人。 据荷兰埃尔塞维尔公司出版的2006年5月第三期生态毒物学环境安全期刊证实,刘维屏发表论文同时署名“浙江大学”与“浙江工业大学”,另外6篇论文每篇的署名人数都在四五人左右。 举报人还称,申请评估过程还存在课题、经费、成果虚假。“在浙江大学环境与资源学院,分别设有‘农业部面源污染控制重点实验室’、‘浙江省亚热带土壤与植物营养重点实验室’、‘浙江省农业遥感重点实验室’和‘污染环境修复与生态健康教育部重点实验室’。他们将以上四个省、部重点实验室分别争取到的科研项目和经费都挪到一个‘教育部重点实验室’。”“他们将设在浙江大学环境与资源学院的四个省、部重点实验室的成果归于一个‘教育部重点实验室’。” 另外,浙大环境与资源学院还回应,根据教育部教技司[2003]59号文件精神,学院以“浙江省亚热带土壤与植物营养重点实验室”和“浙江省农业遥感与信息技术重点实验室”为基础,整合了相关学科的优势力量,申报“污染环境修复与生态健康教育部重点实验室”,并获得教育部批准立项建设。举报所指的“农业部面源污染控制重点实验室”为2008年农业部批准立项建设,评估材料(包括课题、经费、成果等)是该实验室51名成员在2004年到2008年科研工作的统计结果,均有证明材料。