维生素E醋酸酯在甲醇中的溶解性好吗?
积分奖励对错题: 高度的回缩弹性是羊毛纤维的重要特征,也是促进羊毛缩绒的因素 ()
可溶性元素是直接加硝酸酸化到ph<2;总元素是9ml样品 加0.8ml硝酸和0.2ml盐酸消解后测的,实验结果铜元素总含量低于可溶性元素,百思不得其解。
用铜水,纯碱和冰乙酸做醋酸铜水溶性老不好怎么解决?还有怎么才能得产品晶体好点,求大家帮帮忙!爱心捐助
水溶性肥料中微量元素的检测目前是用AAS和ICP但是ICP和AAS测试出来的结果是样品的中微量元素的总量比如:EDTA-Cu和硫酸铜就不能区分出来时多少这样的测试有意义么还是我理解的有问题
麦饭石溶出性如何做:Fe、Ca、Mg、Ba、Cd、Co、Cu、Cr、Mn、Ni、Pb、Zn、Na、K、Sr、Hg、Cd等元素如何测定。麦饭石吸附性如何做:Pb、Cd、Hg等元素如何测定。
如何让脂溶性维生素与水溶性维生素互溶?
请教,水溶液 呈兰色,(PH7.6) 会是?CUSO4?其他的可能性?
大家在做新版EN71-3时,有没有遇到可溶铜测试的困扰?
‘有奖问答’对错题:醋酯纤维是热塑性纤维。( )
如题,那种溶剂对香兰素的溶解性好?日化香精,香草味的香精。
有测壁纸中的可溶性元素的吗?用icp-oes测壁纸中的8种可溶性元素,在测加标回率时发现As,Sb,Cd的回收率偏低,不知问题出在那了? 是不是壁纸样品基体影响太大呢?各位指点一下.
塑化剂检测特刊及LCMS溶剂促销特刊第二版图谱资料,供参考
[align=center][/align][font=宋体]一、原理[/font][font=宋体]1.[/font][font=宋体]多糖的分级与纯化[/font][font=宋体]多糖纯化的实质是将粗多糖中的杂质(包括蛋白质、色素、低聚糖、无机盐等非糖物质)除去而获得分子量和极性均一的多糖组分。比较常用的方法有:醇沉法、超滤法和柱层析法等。其中柱层析法应用比较普遍,多用于样品的精细分级,具有操作简单,重现性好的优点,但样品上样量小。用于多糖分离的柱层析主要有两类:一类是通过分子量大小进行分级的凝胶柱层析,如Sephadex G-100(200、50、25、10)、SepharoseCL-6B等系列;另一类是离子交换层析,是根据多糖所带电荷的性质不同选择相应的离子交换柱对多糖进行分级。如待分离的多糖带有负电荷,可选择阴离子型的DEAE-纤维素柱或DEAE-Sepharose柱进行分级,以获得均一的多糖组分。[/font][font=宋体]通过热水煮提方法提取的多糖,通常是混合物,且分子量不均一,其单糖组成、分子结构和聚合度往往不同,可通过柱层析的方法,对其进行分级以达纯化的目的。本实验中,采用[/font]DEAE-[font=宋体]纤维素柱层析的方法对中草药中水溶性粗多糖进行分级纯化,分离纯化出各级分多糖,[/font][font=宋体]为后续研究多糖的结构特征和生物活性奠定基础。[/font][font=宋体]2.[/font][font=宋体]苯酚—硫酸法[/font][font=宋体]游离的寡糖、多糖中的己糖或糖醛酸在浓硫酸的作用下,脱水生成糠醛,再与苯酚作用起显色反应,在一定范围内其颜色深浅与糖的含量成正比,吸收值与糖含量呈线性关系。且己糖在[/font]490 nm[font=宋体]处(戊糖及糖醛酸在[/font]480 nm[font=宋体])有最大吸收,故用比色法测定多糖含量。该法简单,快速,灵敏,且颜色持久,同一台设备同一光源仅需制作一条标准曲线。[/font][font=宋体] [/font][font=宋体]二、步骤[/font]1.[font=宋体]中草药水溶粗多糖的提取流程[/font][font=宋体]中草药粉末[/font][font=Symbol][/font][font=宋体]蒸馏水浸泡过夜[/font][font=Symbol][/font][font=宋体]超声[/font]/[font=宋体]微波[/font][font=Symbol][/font][font=宋体]水浴浸提[/font][font=Symbol][/font][font=宋体]过滤去除药渣[/font][font=Symbol][/font][font=宋体]定容[/font][font=Symbol][/font][font=宋体]多糖含量测定[/font][font=宋体]加等体积[/font]95%[font=宋体]乙醇[/font][font=Symbol][/font]4[font=宋体]℃冰箱过夜,醇沉多糖[/font][font=Symbol][/font]5000r/min[font=宋体]离心去上清液[/font][font=Symbol][/font][font=宋体]粗多糖[/font][font=Symbol][/font][font=宋体]脱蛋白[/font][font=Symbol][/font][font=宋体]脱色素[/font][font=Symbol][/font][font=宋体]透析[/font][font=Symbol][/font][font=宋体]浓缩[/font][font=Symbol][/font][font=宋体]冷冻干燥得水溶多糖[/font][font=Symbol][/font]DEAE-[font=宋体]纤维素色谱柱[/font][font=Symbol][/font][font=宋体]收集多糖组分[/font][font=Symbol][/font][font=宋体]测定每[/font]50s[font=宋体]洗脱液的[/font]OD[font=宋体]值[/font][font=Symbol][/font][font=宋体]绘制横坐标为管数与纵坐标为[/font]OD[font=宋体]值的洗脱曲线[/font][font=宋体]根据洗脱曲线收集多糖溶液[/font][font=Symbol][/font]4[font=宋体]℃无水乙醇醇沉过夜[/font][font=Symbol][/font][font=宋体]离心[/font][font=Symbol][/font][font=宋体]多糖沉淀[/font][font=Symbol][/font][font=宋体]常规干燥[/font][font=Symbol][/font][font=宋体]纯度鉴定[/font][font=Symbol][/font][font=宋体]纯多糖[/font]2.[font=宋体]脱蛋白[/font][font=宋体]由于粗多糖中含有一定量游离的和结合的蛋白,为保证多糖的纯度,必须将蛋白质脱去。常用的脱蛋白方法有[/font]Sevag[font=宋体]法、三氯乙酸法和蛋白酶法(如链蛋白酶、胰蛋白酶、木瓜蛋白酶)等。[/font][font=宋体]([/font]1[font=宋体])[/font]Sevag[font=宋体]法[/font][font=宋体]根据蛋白质在有机溶剂(如氯仿)中易发生变性析出的特点[/font][font=宋体],把多糖配制成[/font]5%[font=宋体]的糖液,然后按照[/font]1:3[font=宋体]的体积比加入[/font]Sevag[font=宋体]试剂(氯仿∶正丁醇[/font]=4[font=宋体]∶[/font]1[font=宋体]),混匀后剧烈振荡,静置分层后吸去水层与溶剂层交界处的变性蛋白质,重复操作多次,直到除尽蛋白质为止。[/font][font=宋体]([/font]2[font=宋体])三氯乙酸法[/font][font=宋体]将粗多糖配成[/font]5%[font=宋体]的糖液,加入[/font]30%[font=宋体]三氯乙酸溶液,使三氯乙酸终浓度为[/font]15%[font=宋体],在[/font]4℃[font=宋体]冰箱中放置过夜,离心弃去沉淀,得无蛋白的多糖溶液,再用[/font]1 mol/L NaOH[font=宋体]溶液中和至[/font]PH[font=宋体]为[/font]7[font=宋体]。[/font][font=宋体]([/font]3[font=宋体])蛋白酶法[/font][font=宋体]将粗多糖配成[/font]5%[font=宋体]的糖液,用酸碱调[/font]pH[font=宋体]至中性,加链蛋白酶[/font]0.5 L[font=宋体],放恒温箱中[/font]37℃[font=宋体]保温[/font]24 h[font=宋体]后,加热升温至[/font]80℃[font=宋体]使酶失活,离心,得无蛋白的多糖溶液。[/font]3.[font=宋体]脱色[/font][font=宋体]([/font]1[font=宋体])[/font] [font=宋体]活性炭法[/font][font=宋体]将脱蛋白后的多糖配成[/font]5%[font=宋体]的糖液,用[/font]NaOH[font=宋体]溶液调[/font]pH[font=宋体]为[/font]4.5[font=宋体],加入活性炭粉末,于[/font]80℃[font=宋体]保温[/font]2 h[font=宋体]后过滤。反复进行[/font]3[font=宋体]次,直到溶液颜色不再降低为止。[/font][font=宋体]([/font]2[font=宋体])过氧化氢法[/font][font=宋体]将脱蛋白后的多糖溶液,用浓氨水调至[/font]pH[font=宋体]为[/font]8.0[font=宋体],逐滴滴加[/font]20%H[sub]2[/sub]O[sub]2[/sub][font=宋体]至溶液为浅黄色,[/font]50℃[font=宋体]水浴,保温[/font]2 h[font=宋体]后过滤。[/font]4.[font=宋体]透析脱盐[/font][font=宋体]将脱蛋白、脱色后多糖配成[/font]5%[font=宋体]溶液,置于透析袋中,先用自来水逆向流水透析[/font]72 h[font=宋体]后,再用蒸馏水透析[/font]24 h[font=宋体],每[/font]4 h[font=宋体]换水一次。[/font]5.[font=宋体]干燥[/font][font=宋体]将脱蛋白、脱色、脱盐后的中草药多糖溶液,水浴[/font]80℃[font=宋体]浓缩至[/font]10 mL[font=宋体],加三倍体积的无水乙醇过夜,离心取沉淀,经无水乙醇、乙醚洗涤后,常规干燥得中草药去蛋白去色素的多糖。[/font]6.[font=宋体]多糖含量测定[/font][font=宋体]采用苯酚[/font]-[font=宋体]硫酸法测定样品中的多糖含量。绘制标准曲线,根据葡萄糖标准曲线和样品吸光值计算其糖含量。[/font][font=宋体]标准曲线的制作:准确称取[/font]105℃[font=宋体]干燥恒重的标准葡萄糖[/font]50 mg[font=宋体]定容于[/font]500 mL[font=宋体]容量瓶中,加水至刻度,用移液管分别吸取[/font]0[font=宋体]、[/font]0.1[font=宋体]、[/font]0.2[font=宋体]、[/font]0.3[font=宋体]、[/font]0.4[font=宋体]、[/font]0.5[font=宋体]、[/font]0.6[font=宋体]、[/font]0.7[font=宋体]、[/font]0.8[font=宋体]、[/font]0.9[font=宋体]、[/font]1.0 mL[font=宋体]转入试管中,各以蒸馏水补至[/font]1.0 mL[font=宋体],每个浓度重复四个平行。然后分别向每支试管中加入[/font]4%[font=宋体]苯酚试剂[/font]1mL[font=宋体]及浓硫酸[/font]2 mL[font=宋体],摇匀,沸水浴中煮沸[/font]10 min[font=宋体],冷却至室温,放置[/font]10 min[font=宋体]后在[/font]λ= 480 nm[font=宋体]处测定吸光值[/font]A[font=宋体]。以吸光值[/font]A[font=宋体]为纵坐标,糖含量[/font]C[font=宋体]为横坐标,得糖的标准曲线。[/font][font=宋体]样品溶液制备:精密称取水溶性粗多糖[/font]5 mg[font=宋体],先加[/font]10 mL[font=宋体]蒸馏水溶解,然后定容至[/font]50 mL[font=宋体]。[/font][font=宋体]样品含量测定:用移液管吸取样品液[/font]1.0 mL[font=宋体],加入[/font]4%[font=宋体]苯酚溶液[/font]1 mL[font=宋体]及浓硫酸[/font]2 mL[font=宋体],按上述方法进行操作,测其吸光值,以标准曲线计算样品糖含量[/font][font=宋体]按下式计算中草药多糖的质量浓度与得率。[/font] [img=,300,41]https://ng1.17img.cn/bbsfiles/images/2021/11/202111021041176368_5305_3528941_3.gif!w300x41.jpg[/img]7.[font=宋体]分级[/font][font=宋体]([/font]1[font=宋体])[/font] DEAE-[font=宋体]纤维素的预处理和装柱[/font][font=宋体]将[/font]DEAE-[font=宋体]纤维素用蒸馏水充分浸泡溶胀后,倾倒除去水分,再用[/font]0.5 M NaOH[font=宋体]溶液浸泡[/font]1 h[font=宋体],用蒸馏水反复洗涤至[/font]PH[font=宋体]等于[/font]7[font=宋体]。再用[/font]0.5 M[font=宋体]的[/font]HCl[font=宋体]溶液浸泡[/font]1 h[font=宋体],用蒸馏水洗至中性,真空清除气泡,备用。[/font][font=宋体]装柱时,先将[/font]DEAE-[font=宋体]纤维素沿着玻璃棒缓慢倒入,以防产生气泡。柱子装好后,依次用[/font]5[font=宋体]倍柱体积的蒸馏水、[/font]3[font=宋体]倍柱体积的[/font]1.0 M NaCl[font=宋体]和[/font]5[font=宋体]倍柱体积的蒸馏水进行平衡,流速设定为[/font]20 cm/ h[font=宋体]。[/font][font=宋体]([/font]2[font=宋体])水溶性粗多糖的离子交换柱层析的线性梯度洗脱[/font][font=宋体]称取[/font]50 mg[font=宋体]水溶性粗多糖,溶于[/font]5 mL[font=宋体]蒸馏水中,在已平衡好的[/font]DEAE-[font=宋体]纤维素离子交换柱([/font]1.5 × 14 cm[font=宋体],[/font]Cl[sup]-[/sup][font=宋体]型)上进行上样,先用[/font]100 mL[font=宋体]蒸馏水做流动相进行洗脱,再用[/font]0~1.0 M NaCl[font=宋体]溶液[/font]300 mL[font=宋体]进行线形梯度洗脱,流速[/font]1.0 mL/min[font=宋体],每个试管收集[/font]3 mL[font=宋体]洗脱液,苯酚—硫酸法测定洗脱液中相对的糖含量分布。[/font]8.[font=宋体]纯度鉴定[/font][font=宋体]([/font]1[font=宋体])高效液相色谱法[/font][font=宋体]采用高效液相色谱仪系统,[/font] 10A[font=宋体]检测器,[/font]CLASS-Vp[font=宋体]工作站,[/font]TSK-gel G-3000PWXL[font=宋体]不锈钢色谱柱([/font]7.8 × 300 mm)[font=宋体],柱温为[/font]40℃[font=宋体]。[/font][font=宋体]取各级多糖样品溶于[/font]0.7 M Na2SO4[font=宋体]溶液中,其多糖终浓度为[/font]2 mg/mL[font=宋体],上样[/font]20 μL[font=宋体],流动相为[/font]0.7 M Na2SO4[font=宋体]溶液,流速为[/font]0.5 mL/min[font=宋体]。[/font][font=宋体]([/font]2[font=宋体])紫外光谱分析[/font][font=宋体]将水溶性粗多糖各级分多糖样品配成[/font]0.1 mg/mL[font=宋体]的溶液,用[/font]752PC[font=宋体]型紫外可见分光光度计于[/font]200-400 nm[font=宋体]处扫描检测。[/font][font=宋体]([/font]3[font=宋体])旋光仪分析[/font][font=宋体]不同的多糖具有不同的比旋度,它们在不同浓度的乙醇中具有不同溶解度,所以,如同一多糖水溶液经不同浓度的乙醇沉淀所得的沉淀物,具有相同比旋度,则证明该多糖为均一组分。[/font][font=宋体]将评估多糖样品溶于水,成为近似半饱和溶液,置于磁力搅拌器上,在搅拌下加乙醇,使溶液中乙醇浓度达到[/font]20%[font=宋体],搅拌片刻,使沉淀完全,离心得沉淀。上清液中再继续滴加乙醇,使溶液中乙醇浓度达[/font]40%[font=宋体],所产生的沉淀再经离心。前后两次沉淀,分别干燥后在相同条件下测定其水溶液的比旋度。[/font][font=宋体]将[/font]10 mL5%[font=宋体]饱和糖液用国产[/font]WXG[font=Symbol]-[/font]6[font=宋体]型自动旋光仪,钠灯光源,以蒸馏水调零点,[/font]1dm[font=宋体]管室温下测定。[/font]
时下补充维生素成了日常保健的常见环节,但其实补充维生素不当容易中毒。维生素是人体必需的微量营养元素,但过多补充也是浪费,其中一些维生素补充过量易中毒。水溶性维生素如维生素B、C等,服用过量后可随尿液排出体外,毒性较小。而过量补充脂溶性的维生素,易引起中毒。脂溶性维生素包括维生素A、E、K、D等。其中滥用维生素E可引起高血压、乳腺肿瘤。大量服用维生素C可致泌尿系结石。服大量维C会破坏血清中及体内贮存的维生素B12。因此脂溶性维生素必须按照国家规定的量来补。
分子排阻高效液相色谱法检测促胰岛素分泌肽融合蛋白纯度_王婉如
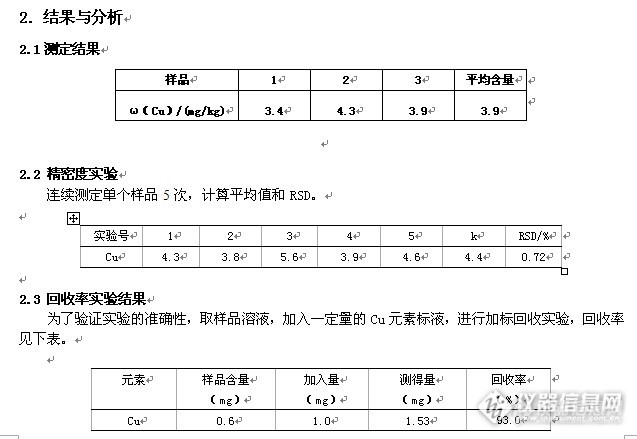
汉中绿茶中微量元素(Cu)的测定1、引言古巴蜀地区是中国茶的摇篮,汉中茶区属古老的巴蜀茶区的最北缘,是茶叶原生地和优生区,也是茶文化的重要发祥地之一。汉中茶叶始于商周,兴于秦汉,盛于唐宋,繁荣于明清,系跨越千年“茶马互市”的主要基地。汉中绿茶以其“纬度高、海拔高、云雾几率高、富含锌硒、远离污染”的自然地理优势和生长环境而著称于世,尤其汉中绿茶以“香高、味浓、耐泡、形美、保健”的品质特点被推崇为名茶中之佼佼者。2、实验部分2.1实验材料(汉中绿茶)http://ng1.17img.cn/bbsfiles/images/2013/06/201306011438_442591_2352694_3.jpg2.2仪器及试剂仪器:SPS8000-电感耦合等离子体原子发射光谱仪(北京科创海光仪器有限公司)、DGB20003—电热干燥箱(中国重庆实验设备厂)、WX-4000微波快速消解系统、DKQ-3B型智能控温电加热器、EL104型电子分析天平(梅特勒-托利多仪器(上海)有限公司)、量筒、移液管、容量瓶等试剂:标准储备液:Cu标准储备液为1mg/ mL(国家标准物质研究中心) 2.3计算方法ω(Cu)/(mg.Kg-1)=ρ*50/m2.4仪器条件http://ng1.17img.cn/bbsfiles/images/2013/06/201306011440_442592_2352694_3.jpg2.5样品预处理将茶叶样品置于电热恒温干燥箱中,烘至恒重。随机取干燥茶叶适量,用研钵研磨样品过60目筛,备用。准确称取制备好的样品0.2060g、0.2031g、0.2024g三份,放入消解罐中。加入5mLHNO3(优级纯),2 ml过氧化氢,按规定程序消解。放冷,将消化液转移至烧杯中,反复淋洗。驱酸后全部转入50ml容量瓶定容,混匀备用。http://ng1.17img.cn/bbsfiles/images/2013/06/201306011440_442593_2352694_3.jpgWX-4000微波快速消解系统的最佳工作条件见下表。http://ng1.17img.cn/bbsfiles/images/2013/06/201306011440_442594_2352694_3.jpg3实验结果3.1测定按照仪器最佳工作条件,测定标液和样品。3.2标准曲线绘制用1mg/mL 的Cu元素的标准溶液,用蒸馏水稀释配制一系列标准溶液。http://ng1.17img.cn/bbsfiles/images/2013/06/201306011440_442595_2352694_3.jpg3.3、测定结果经测定,汉中绿茶中Cu元素的含量见下表。http://ng1.17img.cn/bbsfiles/images/2013/06/201306011442_442596_2352694_3.jpg3.4精密度实验测定样品中Cu元素浓度,每份样品连续测定5次,计算平均值。http://ng1.17img.cn/bbsfiles/images/2013/06/201306011442_442597_2352694_3.jpg3.5回收率实验结果为了验证实验的准确性,取样品溶液,加入一定量的Cu标液,进行加标回收实验,回收率见下表。http://ng1.17img.cn/bbsfiles/images/2013/06/201306011443_442598_2352694_3.jpg
如题:丝裂霉素的水溶性怎么样?非常感谢!!
醋酸纤维素薄膜是由醋酸纤维素加工制成的。醋酸纤维素薄膜作为是电泳支持体 有以下优点:①电泳后区带界限清晰;②通电时间较短(二十分钟至一小时);③它 对各种蛋白质(包括血清白蛋白,溶菌酶及核糖核酸酶)都几乎完全不吸附,因此无 拖尾现象;④对染料也没有吸附,因此不结合的染料能完全洗掉,无样品处几乎完全 无色。它的电渗作用虽高但很均一,不影响样品的分离效果,由于醋酸纤维素薄膜吸 水量较低,因此必需在密闭的容器中进行电泳,并使用较低有电流避免蒸发。 醋酸纤维素薄膜电泳已经广泛用于血清蛋白,血红蛋白,球蛋白,脂蛋白,糖蛋 白,甲胎蛋白,类固醇及同工酶等的分离分析中,尽管它的分辨力比聚丙酰胺凝胶电 泳低,但它具有简单,快速等优点。根据样品理化性质,从提高电泳速度和分辨力出 发选择缓冲液的种类,pH和离子强度。选择好的缓冲液最好是挥发性强,对显色或紫 外光等观察区带没有影响,若样品含盐量较高时,宜采用含盐缓冲液。例如血清蛋白 电泳可选用pH8.6的巴比妥缓冲液或硼酸缓冲液;氨基酸的分离则可选用pH7.2的磷酸 盐缓冲液等。电泳时先将滤膜剪成一定长度和宽度的纸条。在欲点样的位置用铅笔做 上记号,点上样品,在一定的电压,电流下电泳一定时间,取下滤膜,进行染色。不 同物质需采用不同的显色方法,如核苷酸等物质可在紫外分析灯下观察定位,但许多 物质必须经染色剂显色。 醋酸纤维素薄膜电泳染色后区带可剪下,溶于一定的溶剂中进行光密度测定。也 可以浸于折射率为1.474的油中或其他透明液中使之透明,然后直接用光密度计测 定。它的缺点是厚度小,样品用量很小,不适于制备。
有做广东出入境的灰色油漆粉末的可溶性8元素的没有,讨论下
那位大侠有黄曲霉毒素的溶解性的相关资料,可否发我一下,非常感谢!
[font=宋体][/font][align=left][color=#fe2419][size=2]维权声明:本文为[color=#f10b00]chuanxinlian[/color]原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。[/size][/color][color=#f10b00][size=5]混有色素的脂溶性成分的分离[/size][/color][/align][size=3][b][color=#f10b00]背景介绍[/color][/b][font=宋体] 对于做天然药物分离的同仁们都知道,很多时候我们用溶剂提取完之后的浸膏经常是有颜色的,就是说我们的目标化合物或者说对我们有用的东西与杂质色素混在一起,色素有脂溶性的,也有水溶性的,有时候色素与其他的化合物很难分离,下面就我个人求学期间的一点小小的经验来跟大家分享一下,仅供参考,说的不对的地方还请大家多指正。[/font][font=宋体] 硕士期间做的课题为某植物环己烷萃取部分的分离。因为之前就有师姐做过该植物,提取工作我就省了,当时直接拿到手的就是该植物乙醇提取物的环己烷萃取后的浸膏,看到黑糊糊的浸膏(其实是绿的都发黑了),心里也没有太多感受,因为那时候才刚上完研一,对化合物分离也不是很了解,没什么概念,不知道眼前的东西是好做还是难做,只是听其他人说:这怎么分啊,这么多色素。由于本实验室课题有限,课题的质量也有待于改善,我也只有做这个题的命了,怎么着都不可能换题了,于是接下来就开始了我与色素斗争的实验生涯。[/font][color=#f10b00][font=宋体][b]把我分离化合物的过程与方法与大家分享一下:[/b][/font][/color][font=宋体] [b][color=#f10b00]1[/color][/b][/font][font=宋体][b][color=#f10b00].[/color][/b]首先把所有的浸膏过一遍大的硅胶柱色谱,按极性大小把化合物大致的粗略地分一下段,最后分成7-10个流分,其实每一个流分中都是混有色素的,只是色素在里面占得比例不同罢了,因为色素也有极性大的和极性小的,而且色素在硅胶柱上还很容易拖尾,从平时展的硅胶薄层板上就能看出来,一展有时候就成一条绿绿的长带。但是即使这样,过一遍硅胶柱还是有用的。[/font][font=宋体] [b][color=#f10b00]2. [/color][/b][/font][font=宋体]上面的硅胶柱下来的流分如果量比较大(比如几十克)的话,我就会选择换一个溶剂系统,再过一遍小点的硅胶柱,因为脂溶性的流分可以选择的填料毕竟太少了,只能在硅胶上下功夫了,然后再分成几个量小的流分,同样,色素依然留在各个流分中。[/font][font=宋体] [b][color=#f10b00]3. [/color][/b][/font][font=宋体]第一次过硅胶柱洗脱下来的量小的流分可以用过Sephdex LH-20柱(就是平时所说的[/font][font=宋体]羟丙基葡聚糖凝胶,其分离原理是根据分子量的大小,将分子量不同的化合物分离开来[/font][font=宋体]),这种填料对色素和其他化合物的分离效果很好,因为一般的色素(比如叶绿素),分子量都很大,与一般的化合物的分子量差别都较大,利用这种方法很容易将他们分开,还有就是过Sephdex LH-20柱上样量一定不要太大,否则效果很不好,甚至有时候会没有效果;柱子的流速也要控制,不能太快,否则也会达不到预期的效果。[/font][font=宋体] [b][color=#f10b00]4. [/color][/b][/font][font=宋体]过完凝胶的流分基本上就没有色素了,然后就可以按正常的分离方法分离了。在硅胶薄层板上分离效果好,且成分比较简单的流分可以采用制备薄层的方法分离,不仅效果好,而且速度很快,我们[/font][font=宋体]对分离的化合物的量要求不是很多,mg级就行了,够测NMR,然后能剩点测活性的就差不多了,所以制备薄层是一种很好的分离方法,快速,有效,还经济。[/font][color=#f10b00][font=宋体][b] 5. [/b][/font][/color][font=宋体]极性稍大的,且在硅胶薄层板上的分离效果不佳的,还可以用制备液相,其实脂溶性的成分有的还是可以用反相HPLC的,只不过有机溶剂的比例稍大而已。[/font][color=#f10b00][font=宋体][b] 6. [/b][/font][/color][font=宋体]还有的样品如果成分比较复杂的话,还可以再试试过一遍Sephdex LH-20,不过这时候就应该选稍长一点的柱子,这样效果可能更好。[/font][color=#f10b00][font=宋体][b] 7. [/b][/font][/color][font=宋体]化合物就一个个地出来了,然后去测NMR,解谱,。。。。。。最后就等着毕业了。[/font][font=宋体][b][color=#013add]附:还有一个可能有效的除色素的方法,跟大家分享一下:[/color][/b][/font][font=宋体] 将药材的乙醇提取液(大于50%乙醇提取液均可)直接通过一个装有D152树脂柱(此树脂也以同浓度的乙醇湿法装柱,并以同浓度乙醇洗至流液无浑浊现象,树脂量与药材比例一般为1:3左右),收取流液即可。此方法快速,此树脂对叶绿素有超强的吸附能力容量极大,而在大于50%乙醇的溶剂环境中,对其它成分吸附较少。[/font][b][color=#0162f4][font=宋体]我的愿望: MP3一部,音乐无处不在,谢谢。[/font][font=宋体]最后祝大家上学的学业有成,上班的工作顺利![/font][/color][/b][/size]
水溶性肥料中中量元素钙镁硫的检测各位是用哪个标准?是用EDTA滴定么说下注意点
我们在实验中酶解的效果不好,明显有颗粒存在,维生素B6的测定值小于检出限了,但是百度到有说大米中富含维生素B6。有没有前辈做过大米中的水溶性维生素,特别是维生素B1、B2和B6这几个需要酶解的项目。请教大侠:1.需要将样品粉碎到一个什么样的粒度;2.按照标准操作酶解的效果怎样;3.大米中维生素B6在一个什么水平。
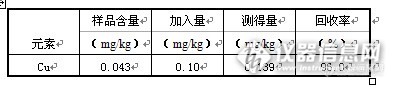
【生活中的仪器分析】活动原创作品:食品安全——“镉”大米中重金属检测大米中微量元素Cu的测定 由于金属元素对人体的生理功能具有特殊作用, 因此其含量关系到人们的身心健康。 微量元素其特点是数量少、功能作用大, 对许多生物活性分子往往起着关键的调控作用。 但长期以来, 对食品营养的研究通常都偏重于有机成分的研究。从某些微量元素在体内的重要作用来看, 尤其是有机营养成分中的羟基、酚基、氨基、杂环氮以及硫巯基等和微量元素的相互作用以及它们生成的化合物所产生的生物活性来看, 对大米中的微量元素的研究的确是不容忽视的。1.实验部分1.1 主要仪器和试剂仪器: SPS8000-电感耦合等离子体原子发射光谱仪(北京科创海光仪器有限公司)、DGB20003—电热干燥箱(中国重庆实验设备厂)、EL104型电子分析天平(上海梅特勒-托利多仪器有限公司)、XT-9900型智能微波消解仪(上海新拓微波溶氧测试技术有限公司)试剂:1000μg/ mL Cu标准储备液、硝酸、蒸馏水1.2样品处理1.2.1样品的预处理先将样品阴干,置于电热恒温干燥箱中,于80℃烘至恒重。随机取干燥大米适量,用研钵研磨样品过60目筛,备用。http://ng1.17img.cn/bbsfiles/images/2013/07/201307110820_450574_2352694_3.jpg1.2.2样品的消解准确称取样品0.2025g、0.2016g、0.2022g三份置于清洁的聚四氟乙烯关中,将消解罐盖好置于微波消解仪中消解,按设定的消解条件进行分步消解(消解条件见下表)。消解结束后,在通风橱内开罐冷却,等溶液澄清后,转移至50mL容量瓶中,用蒸馏水定容、备测。同时做试剂空白实验。 http://ng1.17img.cn/bbsfiles/images/2013/07/201307110821_450575_2352694_3.jpg1.3.3样品的测定测定在仪器最佳工作条件下,制作各元素的校准曲线,根据校准曲线对各个样品进行测定。1.4 实验方法1.4.1标准溶液的配制用1000μg/mL 的Cu元素的标准溶液,逐级稀释配制一系列标准溶液。http://ng1.17img.cn/bbsfiles/images/2013/07/201307110823_450576_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2013/07/201307110823_450577_2352694_3.jpg3.结论3.1、采用ICP-AES法测定大米中的微量元素Cu,其含量是3.94mg/kg,精密度为0.72,加标回收率为93%,结果基本满意。3.2、铜是人体健康不可缺少的微量营养素,对于血液、中枢神经和免疫系统,头发、皮肤和骨骼组织以及脑子和肝、心等内脏的发育和功能有重要影响。铜主要从日常饮食中摄入。世界卫生组织建议,为了维持健康,成人每公斤体重每天应摄入0.03毫克铜。孕妇和婴幼儿应加倍。大米中的Cu可以满足人们日常需求。3.3、建立了一种微波消解电感耦合等离子体-原子发射光谱法测定大米中微量元素的方法,可用于大米中微量元素的测定,可为探讨微量元素与大米的质量关系提供一定的理论依据,同时为人们使用大米时提供科学的数据参考。
求助:谁有最新的用高效液相测定水溶性维生素的检测方法?求分享http://simg.instrument.com.cn/bbs/images/default/em09511.gif
最近,我在学习脂溶性维生素的测定,感觉不好测定,主要问题是2个。第一,前处理,比方说奶粉样品和肉样品,如何处理才好,2 如何用质谱测定,感觉基本没用文献资料,估计是不好测定,有做过的同志们,给点提示,谢谢
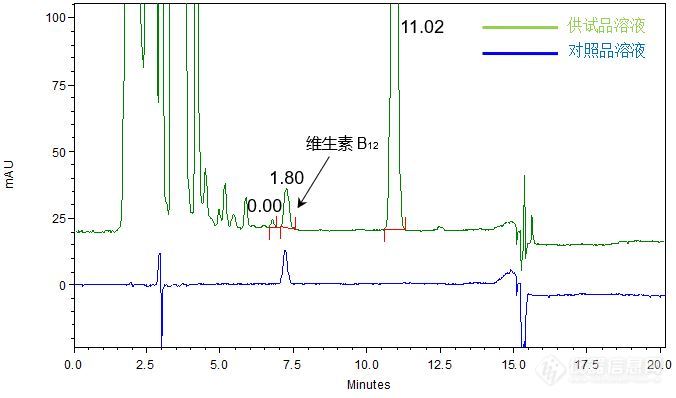
[align=center][b]注射用水溶性维生素的分析(3)[/b][/align][align=center][b]——维生素B12[/b][/align]客户提供了注射用水溶性维生素粉针剂及维生素B12对照品,要求本实验室依据客户所提供方法选择合适色谱柱,实现粉针剂供试品溶液中维生素B12主峰同其相邻杂质峰的良好分离,进而达到准确定量的目的。结合客户所提供的分析方法,由于[b]流动相为高水系条件[/b],我们直接尝试能够在100%的水系流动相下使用的[color=#ff0000][b]高极性AQ[/b][/color]色谱柱,分析对照品溶液及粉针剂供试品溶液。分析对照品溶液,维生素B12主峰保留时间为7.25 min,能够得到良好保留和峰形;分析供试品溶液,维生素B12主峰同其前后相邻杂质均能够得到良好分离,分离度分别为1. 80和11.02,满足方法中1.0的分离度要求(如图1)。[align=center][img=,676,398]http://ng1.17img.cn/bbsfiles/images/2018/01/201801161142145797_2257_2222981_3.jpg!w676x398.jpg[/img][/align][align=center]图1 CAPCELL PAK C18 AQ分析对照品及供试品溶液结果[/align][align=left]注:峰上所标数字为分离度,下同。[/align][align=left][img=,690,269]http://ng1.17img.cn/bbsfiles/images/2018/01/201801161142155690_3262_2222981_3.jpg!w690x269.jpg[/img][/align][align=left][/align][align=left]为使客户有更多的色谱柱选择,尝试使用中等极性的CAPCELL PAK C18 MGII色谱柱进行分析,也可实现供试品溶液中维生素B12及其前后杂质间的良好分离,分离度均在1.0以上,仍满足方法中1.0以上的分离度要求(见图2)。[/align][align=left][/align][align=center][img=,665,432]http://ng1.17img.cn/bbsfiles/images/2018/01/201801161143182281_3783_2222981_3.jpg!w665x432.jpg[/img][/align][align=center]图2 CAPCELL PAK C18 MGII分析对照品及供试品溶液结果[/align][align=left][/align][align=left][img=,690,266]http://ng1.17img.cn/bbsfiles/images/2018/01/201801161143186343_4699_2222981_3.jpg!w690x266.jpg[/img][/align][align=left][/align][align=left]综上实验结果,在客户提供的色谱条件下,使用[b]高极性色谱柱[color=#ff0000]CAPCELL PAK C[sub]18 [/sub]AQ S5[/color][/b] 4.6 mm i.d. × 250 mm(A6AD 04261)色谱柱及[b]中等极性色谱柱[color=#ff0000]CAPCELL PAK C[sub]18[/sub] MGII S5[/color][/b] 4.6 mm i.d. × 250 mm(A4AD 11407)均能满足注射用水溶性维生素中维生素B[sub]12[/sub]及其相邻杂质峰之间的分离要求。[/align]
[color=#444444]想咨询一下各位大神:有测血清样品中脂溶性维生素(维生素A,D,E,K)浓度的嘛?从质谱扫分子量开始,就步步是坎坷,100ng/ml的对照品溶液扫不出来母离子,是样品不稳定还是什么原因呢,急求各位大神的指导。。。拜托拜托[/color]
复合维生素片中既有水溶性的也有脂溶性的怎么完全提起出来[color=#000000][url=http://www.so.com/s?q=%E7%BB%B4%E7%94%9F%E7%B4%A0A&ie=utf-8&src=internal_wenda_recommend_textn]维生素A[/url]、[url=http://www.so.com/s?q=%E7%BB%B4%E7%94%9F%E7%B4%A0D&ie=utf-8&src=internal_wenda_recommend_textn]维生素D[/url]、[url=http://www.so.com/s?q=%E7%BB%B4%E7%94%9F%E7%B4%A0E&ie=utf-8&src=internal_wenda_recommend_textn]维生素E[/url][/color]、维生素B1,[url=http://www.so.com/s?q=%E7%BB%B4%E7%94%9F%E7%B4%A0B2&ie=utf-8&src=internal_wenda_recommend_textn]维生素B2[/url]和维生素C