一、原理 超氧物歧化酶(superoxidedismutase,SOD)普遍存在于动、植物体内,是一种清除超氧阴离子自由基的酶。本实验依据超氧物歧化酶抑制氮蓝四唑(NBT)在光下的还原作用来确定酶活性大小。在有氧化物质存在下,核黄素可被光还原,被还原的核黄素在有氧条件下极易再氧化而产生O2,可将氮蓝四唑还原为蓝色的甲腙,后者在560nm处有最大吸收。而SOD可清除O2,从而抑制了甲腙的形成。于是光还原反应后,反应液蓝色愈深,说明酶活性愈低,反之酶活性愈高。据此可以计算出酶活性大小。 二、材料、仪器设备及试剂 (一)材料;水稻或小麦叶片 (二)仪器设备:1.高速台式离心机;2.分光光度计;3.微量进样器;4.荧光灯(反应试管处照度为4000Lx);5.试管或指形管数支。 (三)试剂 1. 0.05mol/L 磷酸缓冲液(pH7.8);2. 130mmol/L 甲硫氨酸(Met)溶液:称1.9399gMet用磷酸缓冲液定容至100ml;3.750μmol/L 氮蓝四唑溶液:称取0.06133gNBT用磷酸缓冲液定容至100ml,避光保存;4. 100μmol/L EDTA-Na2溶液:称取0.03721gEDTA-Na2用磷酸缓冲液定容至1000ml;5. 20μmol/L 核黄素溶液:称取0.0753g核黄素用蒸馏水定容至1000ml避光保存。三、实验步骤 1. 酶液提取 取一定部位的植物叶片(视需要定,去叶脉)0.5g于预冷的研钵中,1ml预冷的磷酸缓冲液在冰浴上研磨成浆,加缓冲液使终体积为5ml。取1.5~2ml于1000rpm下离心20min,上清液即为SOD粗提液。2. 显色反应 取5ml指形管(要求透明度好)4支,2支为测定管,另2支为对照管,按下列加入各溶液:试剂(酶)用量(ml)终浓度(比色时)0.05mol/L 磷酸缓冲液1.5130mmol/L Met溶液0.313mmol/L 750μmol/L NBT溶液0.375μmol/L 100μmol/L EDTA-Na2液0.310μmol/L 20μmol/L 核黄素0.320μmol/L 酶液0.052支对照管以缓冲液代替酶液蒸馏水0.25总体积3.0混匀后将1支对照管置暗处,其它各管于4000Lx日光下反应20min(要求各管受光情况一致,温度高时间缩短,低时延长)。 3. SOD活性测定与计算 至反应结束后,以不照光的对照管做空白,分别测定其它各管的吸光度。四、结果计算 已知SOD活性单位以抑制NBT光化还原的50%为一个酶活性单位表示,按下式计算SOD活性。SOD总活性=(Ack-AE)×V/(Ack×0.5×W×Vt) 上式中,SOD比活力=SOD总活性蛋白质含量式中SOD总活性以每克鲜重酶单位表示;比活力单位以酶单位/mg蛋白表示Ack照光对照管的吸光度AE样品管的吸光度V样品液总体积(ml)Vt测定时样品用量(ml)W样鲜重(g)蛋白质含量单位为:mg蛋白/g鲜重。
用第四版亚甲蓝法做硫化物,买的标液,空白为0.025.,加热煮沸的水冷却,50ml的比色管,看别人的空白都很低啊。求教~http://ng1.17img.cn/bbsfiles/images/2014/05/201405271351_500506_2085045_3.jpg
1、实验室使用的是SDL的CI3000+的日晒机,灯管及衬管都是配套的。 2、4级蓝羊毛(欧标,SDL蓝羊毛布)晒至4级需要的时间:与别的实验室交流过,有的16个小时左右,有的20个小时左右等。这个与灯管使用时间相关。3、ISO105-B02或者国标上面说的是4级蓝羊毛晒至灰卡4级,这就涉及到评级问题,是目光评级或仪器评级。 我们实验室采用的是目光+仪器结合,用仪器测出来晒至16小时的 ΔE值是1.7±0.3左右,仪器给出评级4级; 平行实验员目光评级也接近灰卡4级,所以定为16小时,若灯管超出使用寿命或其他原因不在考虑之内。 问题:A、你们实验室 欧标或国标 4级蓝羊毛晒至对应灰卡四级时间?评定方法? B、3级蓝羊毛晒至4级时间长短?做光汗复合色牢度的时间长短如何确定,依据?
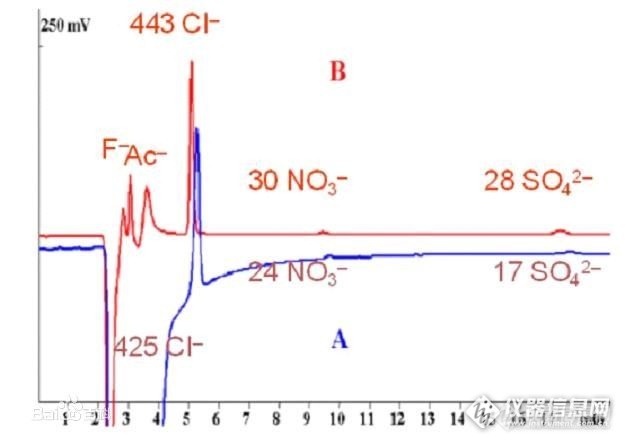
英蓝技术之四:英蓝基体消除在日常分析离子的实验中,常见的基体(或溶剂)是水,这对于一般的离子色谱来说都很容易处理。但是对于某些特殊的情况,需要检测有机相中的无机离子含量,例如汽油中的无机离子。此时必须对样品做相应的处理,将基体去除,否则基体将对色谱柱、管路等部件造成损坏;基体的干扰也往往使得需要的离子无法正常出峰。常见的手工基体消除技术为手工萃取后过C18柱处理,通过C18柱对基体的吸附作用,去除部分有机物。但是这种方法很难实现自动化,处理容量小;另一方面,C18柱的再生非常困难,一般的基体在C18柱上吸附力较强,很难完全洗脱。有的时候为了再生C18柱,在洗脱剂中加入氯仿,虽然能一时洗净,但是C18柱也会因此很快损坏。对于经常测量有机基体中的离子的使用者,传统的方法无疑是费时且费钱的选择。英蓝基体消除技术将基体消除的功能集成到软件控制的自动化设备上,使得整个基体消除的过程完全自动化。另一方面,基体消除柱可反复冲洗使用,大大降低了实验消耗的成本。1、英蓝基体消除的步骤:1)样品从机器人样品处理器上被转移到基体消除柱上,所有的待测离子被保留在柱上,而基体部分则不被保留,直接进入废液池2)转移液将基体消除柱上的待测离子冲洗下来,转移至进定量环进样分析3)机器人样品处理器开始处理下一个样品2、基体消除柱基体消除柱根据保留离子的不同分为阴离子专用和阳离子专用,还针对不同的进样体积设计,常用的基体消除柱包括:1)Metrosep A PCC 1 (阴离子)/ Metrosep C PCC 1(阳离子)死体积较小,确保了极佳的峰形2)Metrosep A PCC 1 HC(阴离子)/ Metrosep C PCC 1 HC (阳离子)高容量版本,主要用于进样体积大,离子含量低的实验3)此外还有VHC (Very High Capacity)超大容量版本基体消除实例用于预浓缩样品基体离子浓度较高的情况,如自来水中的阴离子分析,拜耳液体中的阴离子分析等。3、英蓝基体消除实例有机溶剂(轻油)中的阴离子检测如图所示,蓝色图为不经过基体消除进样的谱图,由于基体的干扰,F-,Cl-,Ac-都被掩蔽,其他的离子检测误差也很大红色图为经过基体消除后的谱图,基线平稳,各离子都能准确出峰,并可全自动连续进样分析。http://ng1.17img.cn/bbsfiles/images/2014/12/201412111119_526684_312_3.jpg
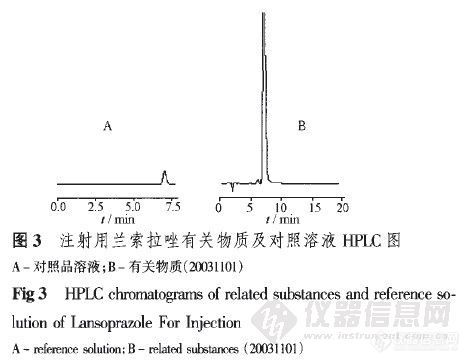
HPLC测定注射用兰索拉唑中兰索拉唑的含量和有关物质 杨艳,谢俊霞,李冰,孙英华,方金玲,刘艳,何仲贵”(沈阳药科大学药学院,沈阳110016)摘要:目的采用高效液相色谱法建立注射用兰索拉唑有关物质检查及其含量测定方法。方法Diamonsil—c18柱(4.6 l_mm×200 mm,5um),以甲醇.水一三乙胺.磷酸(640:360:5:1.5,pH为7.3)为流动相,检测波长为284Ⅲn。结果制剂中辅料对主药测定无干扰,兰索拉唑与有关物质完全分离。在10.0~400.0 mg·L一内峰面积与浓度呈良好的线性关系。精密度(RsD=0.13%)良好。平均回收率为99.6%。结论 本方法简便,迅速,准确,专属性强。关键词:高效液相色谱法;注射用兰索拉唑;含量测定;有关物质http://ng1.17img.cn/bbsfiles/images/2012/07/201207241917_379474_2355529_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/07/201207241917_379475_2355529_3.jpg
四甲级联苯胺测余氯加2滴开始上层变黄绿色 摇匀了变红 再加4,5滴变蓝 联苯胺是按国标用0.1mol盐酸配的 求解答
有没有版友用waters atlantis hilic silica色谱柱做三聚氰胺的?之前用的是安捷伦RX-sil做三聚氰胺,重现性比较差,重复5针响应程下降趋势,近期入手一款waters hilic 色谱柱今天做了一下,仍然有之前的问题。。这款柱子做三聚氰胺应该是没问题的呀,请教做过的版友有没有什么经验介绍,不胜感激

http://ng1.17img.cn/bbsfiles/images/2013/06/201306082039_443658_1699201_3.png 虽然使用ICP-MS一段时间了,但有很多东西还是不清楚。请问大家:蓝色、红色、绿色是对应离子通过四级杆的运动轨迹吗?
做SPME时发现一直有个大的峰,鉴定出来是Silanol, trimethyl-,不知道来至哪里?
最近jem2100plus光很暗,做电子枪对中时忘记六硼化镧灯丝像长什么样子了…
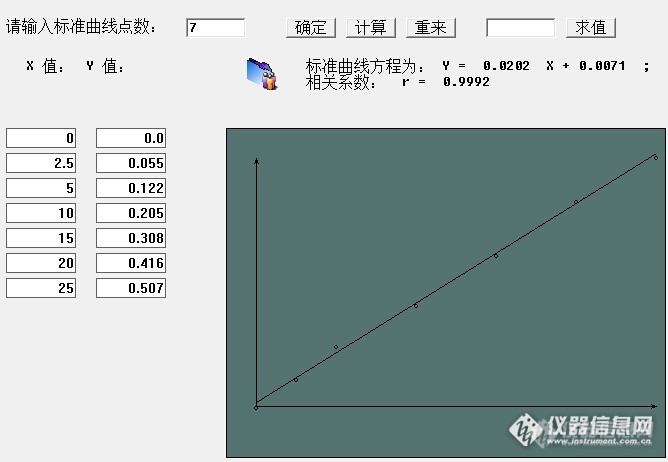
一、标准曲线一般用分光光度法测物质的含量,先要制作标准曲线,然后根据标准曲线查出所测物质的含量。因此,制作标准曲线是生物检测分析的一项基本技术。二、蛋白质含量测定方法 1. 凯氏定氮法2. 双缩脲法3. Folin-酚试剂法4. 紫外吸收法5. 考马斯亮蓝法三、考马斯亮蓝法测定蛋白质含量—标准曲线制作 (一)试剂: 1. 考马斯亮蓝试剂:考马斯亮蓝G—250 100 mg溶于50 ml 95%乙醇,加入100 ml 85% H3 PO4 ,雍蒸馏水稀释至1000 ml,滤纸过滤。最终试剂中含0.01%(W/V)考马斯亮蓝G—250,4.7%(W/V)乙醇,8.5%(W/V)H3 PO4 。2. 标准蛋白质溶液:纯的牛血清血蛋白,预先经微量凯氏定氮法测定蛋白氮含量,根据其纯度同0.15 mol/LNaCl配制成100 ug/ml蛋白溶液。(二)器材: 1. 722S型分光光度计使用及原理。2. 移液管使用。(三)标准曲线制作: 1. 试管编号0123456100ug/ml标准蛋白(ml)0.00.10.20.30.40.50.60.15mol/L NaCl (ml)10.90.80.70.60.50.4考马斯亮蓝试剂 (ml)5555555摇匀,1h内以1号管为空白对照,在595nm处比色A595nm2. 以A595nm 为纵坐标,标准蛋白含量为横坐标(六个点为10ug、20 ug、30 ug、40 ug、50 ug、60 ug),在坐标轴上绘制标准曲线。(1)利用标准曲线查出回归方程。(2)用公式计算回归方程。(3)或用origin作图 ,测出回归线性方程。即A595nm =a×X( )+6;一般相关系数应过0.999以上,至少2个9以上。(4)绘图时近两使点在一条直线上,在直线上的点应该在直线两侧。(四)蛋白质含量的测定: 样品即所测蛋白质含量样品(含量应处理在所测范围内),依照操作步骤1操作,测出样品的A595nm ,然后利用标准曲线或回归方程求出样品蛋白质含量。一般被测样品的A595nm 值在0.1—0.05之间,所以上述样品如果A595nm 值太大,可以稀释后再测A595nm值,然后再计算。(五)注意事项: 1. 玻璃仪器要洗涤干净。2. 取量要准确。3. 玻璃仪器要干燥,避免温度变化。4. 对照:用被测物质以外的物质作空白对照。蛋白质含量测定实验难度系数 0共 0 人点评打分实验材料结晶牛血清清蛋白 g—球蛋白试剂(盒)Na2CO3酒石酸钾钠蒸馏水硫酸铜钨酸钠钼酸钠磷酸硫酸锂液体溴NaOH酚酞仪器耗材可见光分光光度计旋涡混合器秒表[url=http://www.biomart.cn/equipm
蓝人的处女作终于问世,为了刺激蓝人继续加大原创创作力度,飞燕决定,每创作一篇,根据创作质量给予积分悬赏奖励,因为第一篇是处女座,先悬赏100,以资鼓励!http://simg.instrument.com.cn/bbs/images/brow/em09502.gif
锅炉炉水和过热蒸汽中SiO2测定采用硅钼蓝分光光度法,首先加入酸性钼酸铵。这个试剂容易变蓝失效。大家如何配制,保存,使用呢?
[size=4]请问各位高手为什么做镁的时候加氧化澜配的溶液?请问各位高手为什么做钠的时候加硝酸铯?[/size]我做[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原吸[/color][/url]盲样镁考核时,加了澜溶液,控样马上对了,不加澜溶液,结果偏低,这是为什么呢?我做[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原吸[/color][/url]盲样钠考核时,加了硝酸铯,控样马上对了,不加硝酸铯,结果偏差很大,这是为什么呢?
用酸性铬蓝K做指示剂测量水中钙镁含量时,钙离子浓度从1~5mg/L,加入酸性铬蓝K后感觉颜色没有明显变化,全都是偏蓝紫色,可能是什么原因?
蓝宝石上溅射铝膜样品断面制作,普通金刚笔制作断面,铝膜脱落?

[b][color=#cc0000]北欧芬兰雪景(四)![/color][color=#cc0000][img=,690,918]https://ng1.17img.cn/bbsfiles/images/2021/05/202105141555025213_1293_1841897_3.jpg!w690x918.jpg[/img][/color][/b]
普鲁士蓝,又名柏林蓝、贡蓝、铁蓝、亚铁氰化铁、中国蓝、滕氏蓝、密罗里蓝、华蓝。英文名称Prussian blue ,是一种古老的蓝色染料,可以用来上釉和做油画染料。中文名称: 普鲁士蓝 中文别名: (OC-6-11)-六氰合铁酸(4-)铁(3+)(3:4),柏林蓝,贡蓝,铁蓝,亚铁氰化铁,中国蓝,滕氏蓝,密罗里蓝,华蓝。 英文名称: Prussian blue ,Turnbull blue 英文别名: Steel blue,Ferric ferrocyanide,Milori blue,Chinese blue,Berlin blue 分子式: C6FeN6·4/3Fe、Fe43 分子量: 859.25 普鲁士蓝是一种古老的蓝色染料 可以用来上釉和做油画染料
哪里可以做不锈钢的蓝点检测
求助铝硅合金20%用钼蓝光度法做的标准曲线
Kazumasa Yoshida, Keiji Matsumoto,Tatsuo Oguchi,Kenichi Tonokura,*§ and Mitsuo KoshiDepartment of Chemical System Engineering, School ofEngineering, The University of Tokyo, 7-3-1 Hongo,Bunkyo-ku, Tokyo 113-8656, Japan, and Department ofEcological Engineering, Toyohashi University ofTechnology, Toyohashi 441-8580, JapanJ. Phys. Chem. A, 2006, 110 (14), pp 4726–4731DOI: 10.1021/jp055280pPublication Date (Web): March 18, 2006Copyright © 2006 American Chemical SocietyAbstractThermal decomposition of disilane was investigated using time-of-flight (TOF) massspectrometry coupled with vacuum ultraviolet single-photon ionization (VUV-SPI) at atemperature range of 675−740 K and total pressure of 20−40 Torr. SinHm species werephotoionized by VUV radiation at 10.5 eV (118 nm). Concentrations of disilane and trisilaneduring thermal decomposition of disilane were quantitatively measured using the VUV-SPImethod. Formation of Si2H4 species was also examined. On the basis of pressure-dependentrate constants of disilane dissociation reported by Matsumoto et al. , kinetic simulation including gas-phase and surface reactions was performed toanalyze thermal decomposition mechanisms of disilane. The branching ratio for (R1) Si2H6 →SiH4 + SiH2/(R2) Si2H6 → H2 + H3SiSiH was derived by the pressure-dependent rate constants.Temperature and reaction time dependences of disilane loss and formation of trisilane werewell represented by the kinetic simulation. Comparison between the experimental results andthe kinetic simulation results suggested that about 70% of consumed disilane was converted totrisilane, which was observed as one of the main reaction products under the presentexperimental conditions.
[color=red][b]亚甲基蓝分光光度法《空气和废气监测分析方法》(第四版) 还有 环境空气 硫化氢的测定 亚甲蓝分光光度法 GB-T 11742-89[/b][color=#000000]这两个标准是怎么回事啊 ? 书籍我有,第一方法找得到,第二个国标怎么回事,官网都找不到,只有一些非官方的网页上面能看到,是废止了吗? 还有GB-T和GB/T到底什么区别??请大家知道的麻烦告知一下,很疑惑,感谢![/color][/color][align=center][color=#000000][b][/b][/color][/align][color=#000000][/color]
做溶出时,蓝法和浆法的本质区别是?

一直做靛酚蓝氨曲线,老是斜率太大,不知道什么原因。。。。次氯酸钠是新买的滴定的,滴定的浓度是0.572mol/L,配试剂的水都是用的无氨水~配的时候都是按标准配的。。。愁人~问下大家~有遇到相同情况的么?谢谢啦~实在是找不到什么原因啊~http://simg.instrument.com.cn/bbs/images/brow/em09509.gif用的VIS-723N分光光度计~北京瑞利的~ http://ng1.17img.cn/bbsfiles/images/2011/08/201108091457_309349_2255963_3.jpg
实验室在做右兰索拉唑的合成,主要是对成品进行含量和手性分析。跪求分析条件。
我们一般用的螺丝是镀镍的,有些外购部件中也会有螺丝,是蓝锌,彩锌,大家接触的经验来看,哪种镀锌 六价铬容易超标呢?
用靛酚蓝分光光度计法做氨的标准曲线时,吸光度偏高,最后一个吸光度达到0.9。,请问是怎么回事?
用磷钼蓝法做磷酸盐曲线好做吗?为什么我做了两次,最后几个点都在降呢?是不是氯化亚锡的原因?跪求解答!!!!

哪里能买到四芯公转6芯母的电缆线?[img]https://ng1.17img.cn/bbsfiles/images/2020/09/202009161350508316_2151_1615838_3.jpg[/img]
[align=center]板栗叶水浸液对商洛丹参幼苗酶活性的影响[/align][align=center]西安国联质量检测技术股份有限公司[/align][align=center]食品事业部:魏娜[/align][b]摘要:[/b]本实验以商洛丹参种子为材料,以板栗叶为供体,研究不用浓度板栗叶水浸液对商洛丹参幼苗酶活性的影响。采用生物测定法测定丹参幼苗酶活性的状况。关键词:丹参,板栗叶水浸液,酶活性植物化感作用(Allelopathy)是指植物(含微生物)向环境释放特殊的化学物质而对其他植物或微生物产生直接或间接的有害或有益的作用,这些特殊的化学物质叫做化感物质。化感物质一方面通过植物体释放产生,另一方面通过植物地上和地下部分的残体分解产生。化感作用广泛存在于自然界中,它涵盖了各种植物之间、包括微生物间的相生相克关系,对解释植物个体及种间的相互作用机制和构建可持续的植物群落都起着重要的作用,并对农、林业生产有重要的影响,如农作物的连作障碍、森林更新失败以及生物入侵等现象都与化感作用密切相关。 化感物质进入土壤后,植物根际微生态系统将发生复杂的变化。化感物质对土壤微生物区系及酶活性的研究,包括根系分泌物数量和成分的变化与土壤微生物类群的关系、土壤酶活性与土壤微生物种类及数量的关系等,这为研究化感作用对土壤根际微生态系统的影响,特别是为根际微生物区系的变化提供了有益的参考。目前,有关植物某一部位水浸液以及纯化感物质对土壤酶活性、土壤养分和微生物数量影响的相关研究相对较少,已有研究主要包括:黄益宗等研究发现化感物质阿魏酸对土壤硝化反应的抑制作用最强,其次是对叔丁基苯甲酸 吕可等通过用花椒叶水浸液浇灌盆栽花椒幼苗研究水浸液对土壤酶和微生物的影响,结果表明:花椒叶水浸液使根际土中的细菌、真菌和放线菌数量以及微生物总数均有不同程度的减少,使根际土蛋白酶、蔗糖酶和酸性磷酸酶活性明显低于非根际土相应的酶活性,而过氧化氢酶和多酚氧化酶活性则显著升高 印楝种子壳的酒精水浸液显著抑制了土壤中放线菌的数量,显著增加了土壤中自由固氮细菌的数量,显著抑制了土壤中反硝化细菌的数量,土壤脱氢酶活性未受到影响,而磷酸酶活性受到了严重的抑制 2,4二叔丁基苯甲酸(PEDT)和香草酸两种化感物质均在低浓度下提高而在高浓度下抑制了微生物生物量及其活力。板栗(Castanea mollissima Blume),有较高的药用价值,有健脾胃、益气、补肾、强心的功用。其中所含的丰富的不饱和脂肪酸和维生素,能防治高血压病、冠心病和动脉硬化等疾病。板栗在商洛地区大面积种植,是商洛主要经济林品种之一、五大商药之一、也是商洛的主要经济作物之一。丹参(Salvia miltiorrhiza Bge. )为唇形科鼠尾草属多年生草本植物,具有祛瘀止痛、活血通经、清心除烦等功能。 其根及根茎是常用的重要中药[sup][color=#3366cc][/color][/sup],有活血化瘀、消肿止痛、养血安神的功能[sup][color=#3366cc][/color][/sup]。丹参根中含有丹参素、丹参酮等生物活性物质[sup][color=#3366cc][/color][/sup],对治疗冠心病、心绞痛和脑血管疾病有很好的疗效,同时还具有抗菌消炎、保肝和改善肾功能的作用[sup][color=#3366cc][/color][/sup]。研究不同浓度板栗叶水浸液对商洛丹参幼苗酶活性的影响,对科学构建林药复合系统,合理选择林下中药材品种,提高土地利用率,增加农民收入,促进地方经济发展,不仅具有理论指导作用,还具有非常重要的现实意义。化感作用的研究对农林(林药)复合系统中物种的配置、耕作制度和栽培措施的优化,农田病虫害的控制、复合系统的经营管理,以及保持生物多样性和农业可持续发展有重要意义。在农林(林药)复合系统中,林木会通过淋溶、挥发、残体分解和根系分泌向林下植物释放有益或有害的化学物质,促进或抑制植物的生长和生产,那么合理选择林下作物品种直接影响整个复合系统的总产量和农民的经济收入。研究板栗和丹参之间的化感作用,对林药复合生态系统的构建、管理、经营有着十分重要的意义。[b]1.材料与方法1.1 实验材料[/b]1.1.1实验材料[b] [/b] 供体材料为板栗叶,采自商州区。受体种子为商洛地道中药材丹参。1.1.2实验仪器 人工气候培养箱、分光光度计、水浴锅、冷冻离心机、制冰机、天枰、真空干燥器1.1.3实验试剂[b] 1.2 实验方法1.2.1 板栗叶水浸液的制备[/b]。取风干的板栗叶样品,剪成1cm长的小段,按30g/600mL的比例用蒸馏水浸泡,在振荡器上震荡48h(25℃),过滤后即得浓度为0.05g/mL的水浸液(母液),用蒸馏水将水浸液分别稀释至0.01、0.02、0.03、0.04、0.05mol/L,置于4℃冰箱备用。 表 1 制作不同浓度的板栗叶水浸液[table][tr][td] 板栗叶水的浓度(mol/L)[/td][td] 母液(mL)[/td][td=1,6]分别用蒸馏水定容至500mL。[/td][/tr][tr][td] 0.01[/td][td] 10[/td][/tr][tr][td] 0.02[/td][td] 20[/td][/tr][tr][td] 0.03[/td][td] 30[/td][/tr][tr][td] 0.04[/td][td] 40[/td][/tr][tr][td] 0.05[/td][td] 50[/td][/tr][/table][b]1.2.2 丹参种子萌发及幼苗培养。 [/b]取丹参种子先用0.1%HgCL[sub]2 [/sub]消毒10min,浸泡24h。蒸馏水冲洗数次,滤干后均匀排列放至培养皿中,于人工气候培养箱(温度25℃,湿度62°)中培养。从培养的第二天起及时补充等量水浸液和蒸馏水,使滤纸始终保持湿润。[b]1.2.3 [/b]超氧化物歧化酶活性的测定 取丹参种子0.20g,加5ml的mmol/L的磷酸缓冲液,研磨成匀浆,匀浆液以5000r/min离心15min,按谁谁的比色法(愈创木酚法),测定各组丹参幼苗SOD酶活性,最后以OD470/ming表示超氧化物歧化酶的活性[align=center][b]实验一 氮蓝四唑(NBT)法测定超氧化物歧化酶(SOD)活力[][/b][/align]一、原理 超氧化物歧化酶(superoxide dismutase,SOD)普遍存在于动、植物体内,是一种清除超氧阴离子自由基的酶。本实验依据超氧化物歧化酶抑制氮蓝四唑(NBT)在光下的还原作用来确定酶活性大小。在有氧化物质存在下,核黄素可被光还原,被还原的核黄素在有氧条件下极易再氧化而产生超氧阴离子自由基,超氧阴离子自由基可将氮蓝四唑还原为蓝色的甲腙,后者在560nm处有最大吸收。而SOD可清除超氧阴离子自由基,从而抑制了甲腙的形成。于是光还原反应后,反应液蓝色愈深,说明酶活性愈低,反之酶活性愈高。据此可以计算出酶活性大小。二、材料、仪器设备及试剂(一)材料:植物叶片。(二)仪器设备:高速台式离心机,分光光度计,微量进样器,荧光灯(反应试管处照度为4000lx),试管或指形管数支,黑色硬纸套。(三)试剂(1)0.05mol/L磷酸缓冲液(pH7.8)。A母液:0.2mol/L 磷酸氢二钠溶液:取Na[sub]2[/sub]HPO[sub]4[/sub]12H[sub]2[/sub]O (分子量358.14) 71.7gB母液: 0.2mol/L 磷酸二氢钠溶液:取NaH[sub]2 [/sub]PO[sub]4[/sub]2H[sub]2[/sub]O ( 分子量156.01) 31.2g分别用蒸馏水定容至1000mL;0.05mol/L磷酸缓冲液(pH7.8)的配制:分别取A母液(Na[sub]2[/sub]HPO[sub]4[/sub])228.75mL,B母液(NaH[sub]2 [/sub]PO[sub]4[/sub])21.25mL,用蒸馏水定容至1000mL。(2)130mmol/L甲硫氨酸(Met)溶液:称1.9399gMet用磷酸缓冲液定容至100ml。(3)750μmol/L氮蓝四唑溶液(NBT):称取0.06133gNBT用磷酸缓冲液定容至100ml,避光保存。(4)100μmol/L EDTA-Na[sub]2[/sub]溶液:称取0.03721g EDTA-Na[sub]2[/sub],用磷酸缓冲液定容至1000ml。(5)20 μmol/L核黄素溶液:称取0.0753g核黄素用蒸馏水定容至1000ml,避光保存。三、实验步骤1.酶液提取 取丹参幼苗0.5g于研钵中研磨成粉末,加2ml预冷的提取介质在冰浴上研磨成浆,加入提取介质冲洗研钵,提取介质终体积为5ml。取1.5-2ml于4℃下10000r/min下离心20min,上清液即为SOD粗提液。2.显色反应 取5ml指形管或试管(要求透明度好)4支,2支为测定管,另2支为对照管,按下表加入各种溶液: 表2 制作[table][tr][td][align=center]试剂名称[/align][/td][td][align=center]用量(mL)[/align][/td][td][align=center]终浓度(比色时)[/align][/td][/tr][tr][td][align=center]0.05mol/L磷酸缓冲液[/align][/td][td][align=center]1.5[/align][/td][td][align=center] [/align][/td][/tr][tr][td][align=center]130mmol/L Met溶液[/align][/td][td][align=center]0.3[/align][/td][td][align=center]13mmol/L[/align][/td][/tr][tr][td][align=center]750μmol/L NBT溶液[/align][/td][td][align=center]0.3[/align][/td][td][align=center]75μmol/L[/align][/td][/tr][tr][td][align=center]100μmol/L EDTA-Na[sub]2[/sub]溶液[/align][/td][td][align=center]0.3[/align][/td][td][align=center]10μmol/L[/align][/td][/tr][tr][td][align=center]20 μmol/L核黄素溶液[/align][/td][td][align=center]0.3[/align][/td][td][align=center]2.0μmol/L[/align][/td][/tr][tr][td][align=center]酶液[/align][/td][td][align=center]0.05[/align][/td][td][align=center]2支对照管以缓冲液代替酶液[/align][/td][/tr][tr][td][align=center]蒸馏水[/align][/td][td][align=center]0.25[/align][/td][td][align=center] [/align][/td][/tr][tr][td][align=center]总体积[/align][/td][td][align=center]3.0[/align][/td][td][align=center] [/align][/td][/tr][/table]混匀后将1支对照管罩上比试管稍长的双层黑色硬纸套遮光或置暗处,其他各管于4000lx日光下反应20min 至反应结束后,用黑布罩盖上试管,以不照光的对照管作空白,分别测定其他各管在560nm下的吸光度。