
万古霉素是由链霉菌产生的、结构复杂的糖肽类抗生素,易溶于水,甲醇中极微溶解,乙醇或丙酮中几乎不溶.万古霉素主要抑制细菌细胞壁合成,由于万古霉素有较强的抗菌作用,在人医临床上也较少使用,而且同氨基糖苷类药物一样,具有严重耳毒性及肾毒性,故只宜在其他抗生素对病菌无效时才会被短期使用于抢救,也就是所谓的最后一线药物. 近年来,一些养殖者和饲料生产企业在动物饲喂过程或加工生产中,为追求利润,将万古霉素添加到饲料中应用,长期使用的后果是使需要万古霉素来治疗的一种能够致死的细菌产生抗药性,变异成万古霉素抗药性肠球菌(VRE),对人类生命安全造成了极大的威胁.因此,建立饲料中万古霉素的测定方法是非常必要的.1、适用范围适用于饲料中万古霉素的检测。2、提取称取1 g 均质样品于15 mL 离心管中,加入8 mL 乙酸提取液* 和4 mL 三氯甲烷;振荡4 min, 4,000 rpm下离心4 min,收集上清液;下层残留物用5 mL、5 mL 乙酸提取液重复提取两次,合并三次提取液;作为上样液,待净化。* 乙酸提取液:10% 乙酸溶液(用50% 甲醇水溶解)3、净化ProElut PXC 500 mg/12 mL (Cat.#68207)a 活化: 依次加入6 mL 甲醇,6 mL 水,流出液弃去;b 上样: 将上样液加入柱中,流出液弃去;c 淋洗: 依次用10 mL 水,3 mL 甲醇淋洗,流出液弃去;d 洗脱: 10 mL 10% 氨水(甲醇/ 水= 3/7)溶液洗脱,收集洗脱液;e 重新溶解:50 oC 下用减压蒸馏将洗脱液浓缩近干,然后用1% 乙酸重新定容至1 mL,上机供HPLC 分析。4、色谱条件色谱柱:Spursil C18 250 x 4.6 mm ID, 5 μm (Cat. #82001)流动相:50 mmol/L 磷酸二氢钾(1 L 磷酸二氢钾溶液需加入300 μL 磷酸)/ 乙腈= 92/8流速:1.0 mL/min 进样量:20 μL 柱温:30 oC 检测器: UV 210 nm5、添加回收结果5.1 添加水平为1.0 mg/kg 饲料中万古霉素检测的液相色谱图http://ng1.17img.cn/bbsfiles/images/2015/08/201508041358_559009_2452211_3.pnghttp://ng1.17img.cn/bbsfiles/images/2015/08/201508041358_559010_2452211_3.png回收率:71.6%(注:被仪器的logo遮住了)5.2 添加水平为10.0 mg/kg 饲料中万古霉素检测的液相色谱图http://ng1.17img.cn/bbsfiles/images/2015/08/201508041421_559012_2452211_3.png回收率:69.4%(注:被仪器的logo遮住了)5.3 饲料中万古霉素检测(空白样品)的液相色谱图http://ng1.17img.cn/bbsfiles/images/2015/08/201508041422_559013_2452211_3.png5.4 万古霉素标准品10.0 mg/L 的液相色谱图http://ng1.17img.cn/bbsfiles/images/2015/08/201508041423_559014_2452211_3.png5.5 万古霉素标准品1.0 mg/L 的液相色谱图http://ng1.17img.cn/bbsfiles/images/2015/08/201508041424_559015_2452211_3.png
用waters的液质不知如何建立万古霉素的质谱方法?Scanwave模式下能自动优化锥孔电压和碰撞能量吗?Scanwave模式的具体操作过程是怎样的?
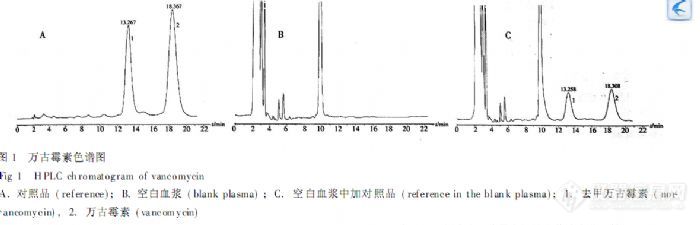
【作者中文名】徐兵; 李昕; 张莉;【作者英文名】XU Bin; LI Xin; ZHANG Li(Third Hospital of Changsha; Changsha Hunan 410015);【作者单位】长沙市第三医院;【摘要】目的建立快速测定人血浆中万古霉素的RP-HPLC法。方法采用液-液萃取法对血样进行预处理,以去甲万古霉素为内标。色谱条件:Diamonsil C18柱(250 mm×4.6 mm,5μm),流动相为乙腈-0.05 mol.L-1磷酸二氢钾缓冲液(9.5∶90.5,pH=3.0),流速为1.0 mL.min-1,检测波长为紫外230 nm。结果万古霉素的最低定量浓度为2.07 mg.L-1,线性范围为2.07~132.64 mg.L-1,相对回收率95%,绝对回收率65%,日内、日间RSD均10%。结论该方法方便、经济、无杂质干扰,适用于万古霉素血药浓度监测及药动学研究。http://ng1.17img.cn/bbsfiles/images/2012/08/201208061206_381806_2379123_3.jpg
大家有没有做过万古霉素的检测,用液相或是液质都行
做动物性食品中的万古霉素,回收也就40-50%

10,抽取5个版友);中奖名单:玲儿响叮当(注册ID:jshbhh)夏天的雪(注册ID:bingwang228)牛一牛(注册ID:v2700892)千层峰(注册ID:jxyan)dahua1981(注册ID:dahua1981)http://ng1.17img.cn/bbsfiles/images/2016/11/201611251519_01_1610895_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/11/201611251519_02_1610895_3.jpg【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================饲料中万古霉素测定方法:SPE基质:饲料应用编号:101707化合物:万古霉素固定相:ProElut PXC色谱柱/前处理小柱:Spursil C18 5u 150 x 4.6mm样品前处理:1.样品准备/提取(1)称取1 g均质样品于15 mL离心管中,加入8 mL乙酸提取液 *和4 mL三氯甲烷。(2)振荡4 min, 4000 rpm下离心4 min,收集上清液;(3)下层残留物用5 mL、5 mL 乙酸提取液重复提取两次,合并三次提取液;作为上样液,待净化。*乙酸提取液:10%乙酸溶液(用50%甲醇水溶解)2.SPE柱净化——ProElut PXC 500 mg/12 mL(Cat.# 68207)(1)活 化:依次加入6 mL甲醇,6 mL水,流出液弃去;(2)上 样:将上样液加入柱中*,流出液弃去;(3)淋 洗:依次用10 mL水,3 mL甲醇淋洗,流出液弃去;(4)洗 脱:10 mL10%氨水(甲醇:水=3:7)溶液洗脱,收集洗脱液;(5)重新溶解:在50 ℃下用减压蒸馏将洗脱液浓缩近干,然后用1%乙酸重新定容至1mL,上机供HPLC分析。色谱条件:分析条件 色谱柱:Spursil C18 250×4.6mm ID,5μm(Cat.#82001) 流 速:1.0 mL/min 检测器:UV 210nm 柱 温:30 ℃ 进样量:20 μL 流动相:50mmol/L磷酸二氢钾(1L磷酸二氢钾溶液需加入300uL磷酸):乙腈(92:8)文章出处:天津迪马实验室关键字:饲料,万古霉素,ProElut PXC,68207,Spursil ,82001摘要:饲料中万古霉素测定谱图:http://www.dikma.com.cn/Public/Uploads/images/wangumeisu%201.PNGhttp://www.dikma.com.cn/Public/Uploads/images/wangumeisu%202(1).PNGhttp://www.dikma.com.cn/Public/Uploads/images/wangumeisu%203.PNG图例:万古霉素
[em09511]有哪位大侠有万古霉素红外图谱,麻烦请上传。QQ1043071882 谢谢!
万古霉素的液相检测条件,很难做的一个东西,这个条件也可以用于液质ColumnCogent Diamond Hydride™, 4µm, 100ACatalog No.70000-7.5PDimensions4.6 x 75 mmSolventsA:DI H2O/ 0.1% formic acidB:Acetonitrile/ 0.1% formic acidGradienttime (min.)%B070610770Post Time2 minInjection Vol.5 microLFlow rate1.0 mL/min.DetectionUV 210 nmSampleStock Solution: 1 mg/mL vancomycin HCl in 50/50 solvent A/solvent B diluent. The solution was filtered through a 0.45 µm nylon syringe filter (MicroSolv Tech Corp).Working Solution: Stock solution was diluted 1:100 with 50/50 solvent A/solvent B mixture.PeakVancomycint00.9 minhttp://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_646162_2254157_3.gif
万古霉素的液相检测条件,很难做的一个东西,这个条件也可以用于液质ColumnCogent Diamond Hydride™, 4µm, 100ACatalog No.70000-7.5PDimensions4.6 x 75 mmSolventsA:DI H2O/ 0.1% formic acidB:Acetonitrile/ 0.1% formic acidGradienttime (min.)%B070610770Post Time2 minInjection Vol.5 microLFlow rate1.0 mL/min.DetectionUV 210 nmSampleStock Solution: 1 mg/mL vancomycin HCl in 50/50 solvent A/solvent B diluent. The solution was filtered through a 0.45 µm nylon syringe filter (MicroSolv Tech Corp).Working Solution: Stock solution was diluted 1:100 with 50/50 solvent A/solvent B mixture.PeakVancomycint00.9 minhttp://ng1.17img.cn/bbsfiles/images/2012/02/201202241724_350939_2254157_3.gif
各位老师本公司生产的万古霉素过程中只用到了乙醇一种有机溶剂,我在测本公司盐酸万古霉素残留乙醇的时候在乙醇前面和后面各出现了一个杂质峰,而且这两个杂质峰会越来越大,我做了EP万古霉素标准,也有同样的情况,请问你们有谁遇到过这种情况吗?如果有,怎么解决?谢谢!我的色谱条件:顶空进样:50度平衡30min,进样针温度105,环线温度105,进样口120,柱子是HP-5,0.25um*30m,柱温50度,检测器200,流速2.0ml/min
各位老师本公司生产的万古霉素过程中只用到了乙醇一种有机溶剂,我在测本公司盐酸万古霉素残留乙醇的时候在乙醇前面和后面各出现了一个杂质峰,而且这两个杂质峰会越来越大,我做了EP万古霉素标准,也有同样的情况,请问你们有谁遇到过这种情况吗?如果有,怎么解决?谢谢!我的色谱条件:顶空进样:50度平衡30min,进样针温度105,环线温度105,进样口120,柱子是HP-5,0.25um*30m,柱温50度,检测器200,流速2.0ml/min
老师们好哈,最近公司做链霉素项目,我们公司是做农药5批次的,我做的就是杂质纯化,要原药里50mg杂质纯品,链霉素各位老师应该都知道,不保留,现在方法开发好了,用的是庚烷磺酸钠,这应该是通用的方法。氨基柱也试过205nm基线噪音有点大,效果也不好。总之用庚烷磺酸钠跑出来5个杂质,液相归一含量低于1%,如果是别的项目也好做,但是链霉素不容有机溶剂,过普通硅胶柱都没法过,而且链霉素也没办法走质谱,确定杂质分子量,就算确定分子量结构猜出来也无法合成,正相柱也试过效果也不好,过柱子基本放弃。中高压制备的话流动相也用的庚烷磺酸钠,但是制备上样量太大,链霉素还没来得及和庚烷磺酸钠结合就直接被冲不来,大部分不保留,而且制备上也基本看不到杂质峰,如果制备出来,后面怎么除去庚烷磺酸钠也是问题。能有老师傅懂的么,要不要换个液相条件跑跑,让杂质少一点,或者给我出出主意怎么才能拿到杂质纯品,现在是没办法了。感觉所有的都试过了。如果能提点建议,真就帮了大忙了,各位老师傅们,我在这里跪谢了。
参考了几篇文献的方法,该物质回收率怎么也做不好,有没有做过的大侠指点一二?
万古霉素、去甲万古霉素和替考拉宁均属于糖肽类抗生素,对革兰氏阳性菌具有很强的抗菌作用,可用于治疗由严重耐甲氧西林金黄色葡萄球菌和耐甲氧西林表皮葡萄球菌引起的感染。目前,糖肽类抗生素作为添加剂普遍用于家禽、猪、牛饲料和兽药中,对人类安全造成威胁。[align=center][img=,600,451]http://www.gdkjfw.com/images/image/32891528255363.jpg[/img][/align]来自河北省食品检验研究院和河北省食品安全重点实验室的范素芳,王丽明,李强等建立了基于快速前处理的牛乳中万古霉素、去甲万古霉素和替考拉宁的高效液相色谱-串联质谱测定方法。结果与分析1 实验条件优化及方法验证取适量牛乳样品,加入0.1%甲酸水溶液-乙腈溶液(85∶15,V/V),经涡旋混匀、超声提取、离心后,万古霉素和去甲万古霉素经阳离子交换柱净化、替考拉宁经C18固相萃取柱净化,采用HP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS仪测定。采用外标法定量,通过绘制标准曲线进行定量分析,万古霉素和去甲万古霉素的线性范围为10~100 μg/L,替考拉宁为20~100 μg/L。以目标化合物仪器响应信号与仪器噪声比(RS/N)约为3时的目标化合物添加量为方法的检出限(limit of detection,LOD),以RS/N约为10时的目标化合物添加量为方法的定量限(limit of quantitation,LOQ)。结果表明,本方法中万古霉素、去甲万古霉素和替考拉宁的LOD分别为2、1、2 μg/kg,LOQ分别为4、2、4 μg/kg。分别作LOQ、5 倍LOQ和10 倍LOQ 3 个水平的添加回收率实验,结果表明,3 种分析物的方法回收率为77.3%~84.5%,相对标准偏差为4.7%~7.2%。2 基质效应评价万古霉素、去甲万古霉素和替考拉宁的基质效应分别为80.2%、81.3%和91.5%,表明3种分析物均存在离子化抑制效应,且万古霉素和去甲万古霉素的ME相对比较严重。3 实际样品测定从当地市场购买的15 份牛乳样品中均未检测到万古霉素、去甲万古霉素和替考拉宁。上述结果表明,该方法可用于市售牛乳样品中糖肽类抗生素万古霉素、去甲万古霉素和替考拉宁的检测。本文来源于《乳业科学与技术》2018年41卷第2期文章《高效液相色谱-串联质谱法测定牛乳中3 种糖肽类抗生素残留》,作者:范素芳,王丽明,李强,张冬生,孙文毅,张岩(河北省食品检验研究院,河北省食品安全重点实验室)。
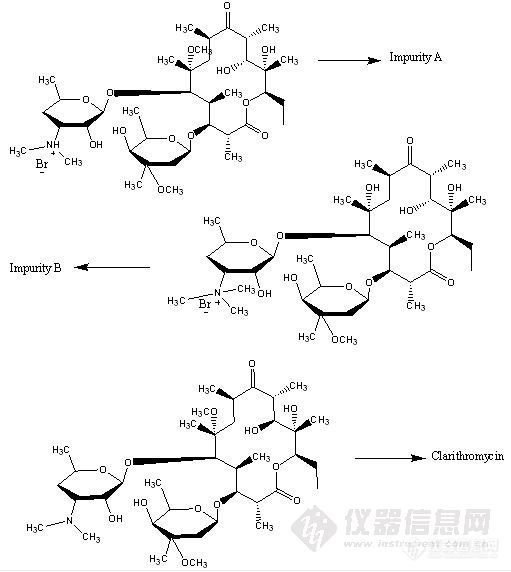
单位工艺生产出来的克拉霉素在主峰的相对保留时间0.84处出现了一个超过0.1%的杂质,现在需要对其进行结构确证。对这个未知杂质,我们了解的情况是,(一)这个杂质对EP/USP液相条件很是敏感的,主要体现在流动相的PH值上,EP/USP液相条件的缓冲液PH值是4.4,当我们把PH值调到4.0时,其他峰的保留时间基本没有变化,提前约0.2~0.3min,但是该杂质的保留时间提前约2min;当把PH调到5.0时,其他峰的保留时间也是基本不变,但是该杂质在主峰之后出峰了,大约延后了约4min。(二)将该杂质接出来做[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url],最明显的离子峰是748.4,但是这个峰是不是分子离子峰不是很确定,继续对这个离子做多级[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url],其主要碎片情况与克拉霉素一样。EP/USP液相条件:溶液A— 4.76 g磷酸二氢钾至1000ml水中,用磷酸) (l - 10) 或氢氧化钾(45% w/v) 调PH至4.4溶液B— 乙腈. Time (minutes) Solution A (%) Solution B (%) 0 75 2532 40 6034 40 6036 75 2542 75 25 流速是1.1ml/min然后我们根据748.4的离子峰,以及工艺,推测了几个可能的杂质,希望大家帮我看看,哪个可能,或者是不是还有其他的可能呢? [img]http://ng1.17img.cn/bbsfiles/images/2010/01/201001280805_199202_1638724_3.jpg[/img]
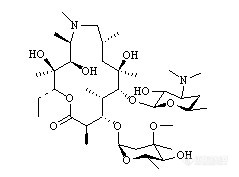
(一)分析背景及色谱条件 红霉素是一种十四元大环内酯类抗生素,一直是临床上治疗革兰氏阳性菌感染的重要药物,半个世纪以来为人类提供了一条安全高效的用药途径。经过不断研究人们相继开发出了耐酸性好的第二代红霉素和不易引起细菌耐药性的第三代红霉素。阿奇霉素可以说是目前第二代红霉素中最具有活力的大环内酯类抗生素,其生产步骤简单,在国内外都具有很大的生产量,尤其在国内,在许多药厂都有生产。但与其它第二代大环内酯类抗生素相比阿奇霉素的HPLC分析一直是个难点,这也与其独特的十五元环结构有关系。而且我们经过试验发现不同色谱柱对其检测的结果差别很大,普通的C18柱无法保证效果,C18 BDS的色谱柱的检测结果也不是很好,我们尝试了几种不同的在C18柱基础上经过各种填料处理的色谱柱,其中包括了“极限”系列的色谱柱。 阿奇霉素分子式http://ng1.17img.cn/bbsfiles/images/2009/11/200911211508_185763_1916092_3.jpg 色谱条件:磷酸氢二钾盐水溶液与乙腈以45:55混合。检测波长210纳米,柱温30°C,流速1.0ml/min,进样量50微克。阿奇霉素样品取自上海某药厂提供的产品,其纯度在95%以上。色谱柱我们共尝试了五根:(1)普通C18柱,编号为1;(2)某品牌BDS C18柱,编号为2;(3)大连某国产色谱柱,编号3;(4)日本某色谱柱(药检所推荐)。编号4;(5)Ultimate XB-C18色谱柱,编号5.(二)试验结果 (1)http://ng1.17img.cn/bbsfiles/images/2009/11/200911211502_185756_1916092_3.jpg(2)http://ng1.17img.cn/bbsfiles/images/2009/11/200911211503_185757_1916092_3.jpg(3)http://ng1.17img.cn/bbsfiles/images/2009/11/200911211503_185758_1916092_3.jpg(4)http://ng1.17img.cn/bbsfiles/images/2009/11/200911211503_185759_1916092_3.jpg(5)http://ng1.17img.cn/bbsfiles/images/2009/11/200911211503_185760_1916092_3.jpg 主峰时间 拖尾因子不对称度半峰宽 理论塔板数 杂质分离度118.4324.8567.2580.6534409——216.7801.4551.7040.42088440.452318.6201.0381.0390.41711067——428.9951.2311.4490.583136981.860527.3920.7440.4750.582123061.172(三)分析与讨论(1)对于两种主要杂质的显示情况,1和3只能显示出一种。4对它们的分离度最好,5次之。(2)从主峰阿奇霉素的峰型来看3最好,4,5次之。(3)关于主峰也就是阿奇霉素的出峰时间,4,5明显晚于前三个色谱柱。关于不同厂家不同批次的阿奇霉素我们已做过很多实验,绝大多数杂质出峰都在阿奇霉素之前,而且种类很多,也就是除了本实验所测样品显示的这两种主要杂质之外还存在有很多杂质,理论上讲主峰出峰时间晚有利于前面杂质峰的分离。 总结起来,从初步的对比检测中发现Ultimate XB-C18色谱柱对阿奇霉素杂质检测的情况还是很令人满意的,甚至不亚于药检所推荐使用的色谱柱。我们准备继续进行一系列的分析实验,对几种较难分离的杂质进行对比分析。
链霉素:798.3 单位/mg卡那霉素:831.6单位/mg磺苄西林:904.0单位/mg四环素:1000单位/mg土霉素:927单位/mg多西环素:866.45单位/mg美他环素:923.86单位/mg西索米星:646.3单位/mg磷霉素:711.5单位/mg克拉霉素:1000单位/mg大观霉素:670.9单位/mg小诺霉素:654.3单位/mg金霉素:1000单位/mg红霉素:1000单位/mg氯霉素:1000单位/mg去甲万古霉素:975.2单位/mg两性霉素B:1000单位/mg奈替米星:660.1单位/mg阿奇霉素:1000单位/mg妥布霉素:1000单位/mg罗红霉素:1000单位/mg阿米卡星:1000单位/mg头孢噻肟钠:951.85单位/mg
抗生素(Antibiotics)及分类指由细菌、霉菌或其它微生物在生活过程中所产生的具有抗病原体或其它活性的一类物质。自1940年以来,青霉素应用于临床,现抗生素的种类已达几千种。在临床上常用的亦有几百种。其主要是从微生物的培养液中提取的或者用合成、半合成方法制造。其分类有以下几种: (一)β-内酰胺类青霉素类和头孢菌素类的分子结构中含有β-内酰胺环。近年来又有较大发展,如硫酶素类(thienamycins)、单内酰环类(monobactams),β-内酰酶抑制剂(β-lactamadeinhibitors)、甲氧青霉素类(methoxypeniciuins)等。 (二)氨基糖甙类 包括链霉素、庆大霉素、卡那霉素、妥布霉素、丁胺卡那霉素、新霉素、核糖霉素、小诺霉素、阿斯霉素等。 (三)四环素类 包括四环素、土霉素、金霉素及强力霉素等。 (四)氯霉素类 包括氯霉素、甲砜霉素等。 (五)大环内脂类 临床常用的有红霉素、白霉素、无味红霉素、乙酰螺旋霉素、麦迪霉素、交沙霉素等。 (六)作用于G+细菌的其它抗生素,如林可霉素、氯林可霉素、万古霉素、杆菌肽等。 (七)作用于G菌的其它抗生素,如多粘菌素、磷霉素、卷霉素、环丝氨酸、利福平等。 (八)抗真菌抗生素 如灰黄霉素。 (九)抗肿瘤抗生素 如丝裂霉素、放线菌素D、博莱霉素、阿霉素等。 (十)具有免疫抑制作用的抗生素如环孢霉素。
金黄色葡萄球菌的耐药性分析【摘要】目的了解我院共分离出152株金黄色葡萄球茵在临床住院者标本中的分布构成情况及其耐药趋势,为-临床感染的预防和治疗提供参考资料。方法回顾分析2005--2009年间我院患者标本中金黄色葡萄球菌在标本和病区的分布构成情况以及对16种抗茵药物的耐药率。结果金黄色葡萄球菌在呼吸道标本(痰液+咽拭子)的分离率最高(109/152),其次是分泌物(27/152),血液(16/152);金黄色葡萄球茵株中,耐甲氧西林金黄色葡萄球茵(MRSA)占68.4%;诺氟沙星92.3%耐药、复方新诺明91%耐药、四环素和利福平88.5%耐药、红霉素86.5%耐药、左旋氧氟沙星84.6%耐药、庆大霉素81.7%耐药;万古霉素、替考拉宁均对金黄色葡萄球茵100%敏感。结论在治疗金黄色葡萄球菌引起的感染时,临床医生应根据本地分离金黄色葡萄球菌的耐药情况,合理应用抗生素,减少细茵耐药,使金黄色葡萄球菌得到有效控制;MRSA药物敏感性较好的有万古霉素、替考拉宁、夫西地酸、呋喃妥因;甲氧西林敏感金黄色葡萄球茵除青霉素、庆大霉素、红霉素外,其它药物均具有较好的敏感性,可作为临床用药的参考。MRSA在对16种抗生素的平均耐药率中最高的前三位分别是青霉素100%、苯唑西林100%、诺氟沙星92.3%,最后三位是喹奴普汀·达福普汀23.1%、夫西地酸15.4%、呋喃妥因7.7%。而甲氧西林敏感金黄色葡萄球菌(Methieillin—sensitive staphylococcusaureus,MSSA)耐药率最高的前三位分别是青霉素89.6%、红霉素62.5%、庆大霉素54.1%,最后三位是左旋氧氟沙星10.4%、米诺霉素6.3%、四环素4.1%。
手性色谱柱是由具有光学活性的单体,固定在硅胶或其它聚合物上制成手性固定相。通过引入手性环境使对映异构体间呈现物理特征的差异,从而达到光学异构体拆分的目的。要实现手性识别,手性化合物分子与手性固定相之间至少存在三种相互作用。这种相互作用包括氢键、偶级-偶级作用、π-π作用、静电作用、疏水作用或空间作用。手性分离效果是多种相互作用共同作用的结果。这些相互作用通过影响包埋复合物的形成,特殊位点与分析物的键合等而改变手性分离结果。由于这种作用力较微弱,因此需要仔细调节、优化流动相和温度以达到最佳分离效果。常见的手性色谱柱有以下两种类型: A、配位交换型: 手性配位交换色谱(ChiralLigandExchangeChromatography,CLEC)由Davankov发明,是通过形成光学活性的金属络合物而达到手性分离,属于IrvingWainer分类中的第4类手性固定相,主要用于分离氨基酸类。 由于此类固定相是由手性氨基酸—铜离子络合物键合到硅胶或聚合物上形成,因此流动相中必须含有铜离子以保证手性固定相上的铜离子不至流失。其它的过渡金属元素也已用于手性配位交换色谱,但铜离子应用最广。形成络合物的过程十分缓慢,因此有时需提高柱温,最佳温度约50℃。 手性配位交换色谱仅对α-氨基酸和其类似物有效。β-氨基酸很难用手性配位交换色谱得以分离。手性配位交换色谱可用于制备,由于流动相中存在铜离子,虽然铜离子能用离子交换柱除去,但增加了样品处理的困难。 B、大环抗生素型: 大环抗生素型手性色谱柱是最近发展起来的,通过将大环抗生素键合到硅胶上制成的新型手性色谱柱。大环抗生素型手性色谱柱的出现归功于DanArmstrong的贡献。此类色谱柱常用的大环抗生素主要由三种:利福霉素(Rifamycin),万古霉素(Vancomycin),替考拉宁(Ticoplanin)。利福霉素作为手性添加剂在毛细管电泳分离手性化合物方面得到了成功运用。万古霉素和替考拉宁分子结构中存在“杯”状结构区和糖“平面”结构区。此类色谱柱性质稳定,可用于多种分离模式。手性分离基于氢键、π-π作用、形成包合物、离子作用和肽键等。 替考拉宁分子量为1885,结构中存在20个手性中心,3个糖基和4个环。酸性基团在多肽杯”/“裂层”的一端,碱性基团在它的另一端。酸性基团和碱性基团提供了离子作用点。糖基在三个平面上,可折叠起来将化合物分子包埋在多肽“杯”中。 万古霉素分子量为1449,结构中存在18个手性中心,3个环。万古霉素具有“篮状”结构,它的附近还有一个可弯曲的糖平面,可将分析物分子包埋在“篮子”中。羧基和仲氨基分布在“篮子”的边缘,参与和分析物分子产生离子作用。万古霉素手性色谱柱可用于反相模式、正相模式和极性模式。万古霉素手性色谱柱可以分离胺类、中性酰胺、脂类。但对于酸性化合物选择性较低。在反相模式中,有机相常用四氢呋喃、乙腈和甲醇。水相常用三乙胺-乙酸缓冲液。色谱柱适用的pH范围为4-7。通常优化碱性化合物手性分离条件时,选择pH=7为起点比较好。另外四氢呋喃、乙腈有最好的选择性。有时采用纯的甲醇和乙醇作流动相也可达到好的分离效果。万古霉素手性色谱柱也可用正相模式,采用正己烷/乙醇为流动相。
各位大虾!小弟在做CEC—MS。整体柱毛细管(reversed phase)是我自己做的。仪器为Agilent CE 和 Agilent MSD (single quadruple).样品为Atenolol (阿替洛尔)and Vancomycin (万古霉素)。流动相为ACN/water/50mM tris buffer pH=7.8 6:2:2.mobile phase driving force:30kV+6bar 在UV(220nm)两物质都有信号。但检测器改为MS后阿替洛尔有明显信号峰但万古霉素的信号(724.7 m/z,double charged)极弱.sheath liquid:0.1%v/v formic acid/methanol=3:7 and flow rate=0.4ul/min.是万古霉素电离不完全?请各位高手指教!
实验室有个老顽固,别人说什么基本上听不进去,自己想一出是一出,咋办?说了N多次,依旧我行我素的。
21世纪的今天,由于抗生素的滥用,中国每年有8万人丧生,年损失800亿,全球每年15万人因为滥用抗生素而死亡;而对于很多耐药性细菌目前世界上无药可治,看到这些,你不觉得细菌耐药性给人类生存带来了很大的威胁吗?自从1929年弗莱明发现青霉素,1941年Florey Chain Heatley等用青霉素粗制品治疗感染性疾病,从此人类便开始了与细菌感染性疾病斗争的新时代,而恰恰在20世纪40年代许多因为细菌感染导致的严重疾病得到了有效的治疗。随着青霉素的广泛使用,慢慢地,金黄色葡萄球菌的耐药性迅速增加,为了解决这一问题,在1961年,半合成甲氧西林诞生了,这种新型抗生素的问世,一时间让金黄色葡萄球菌感染的疾病得到了有效的治疗,可是不久之后,耐甲氧西林金黄色葡萄球菌(MRSA)出现了,让这种菌感染引起的疾病又再次爆发起来,后来万古霉素的出现再次将金黄色葡萄球菌扼杀在深渊之中。但是20世纪90年代,又相继有报道发现耐万古霉素的金黄色葡萄球菌的菌株,可见人类一直在同不同种类的耐药细菌战斗着,人类开发新型抗生素,抑制或者杀灭致病细菌,可是细菌在最短的时间内予以反应,随即便会有耐药菌株的出现,于是人类继续开发,细菌继续对抗着,如此下去,一直循环着……如今,细菌耐药性在全世界范围内都非常严重,面对这样的问题,我们该何去何从?哪里才是我们的出路? 我们都知道,抗生素是战胜细菌感染疾病的良药。自从青霉素开创了抗生素药物的市场后,大量针对不同致病细菌的抗生素类药物问世。然而,我们在这场持久战中似乎越来越不利,35年来,只有一类新型抗菌药物问世,那就是辉瑞公司的Zyyox,现在的医学界比任何时候更需要新型抗生素来抵御无法无天的耐药细菌,由于非常多的细菌对目前市场上有抗生素都有了耐药性,在美国每年有成千上万的人死于肺结核和葡萄球菌感染,当病人感染了导致肺炎、脑膜炎和中耳炎的链球菌后,大约1/3对青霉素产生了耐药性,而一种新抗生素的出现,往往能使人类免于一场世界性的灾难。如今,抗生素耐药性被广泛认为是一个重要的健康危机,因此我们更需要制药行业格外关注并采取相应的行动开发出新型的抗生素;然而,近几十年来,抗生素一直被众多制药公司所忽视,大多数制药公司更关注利润更大的慢性疾病药物市场。不过近日,有些制药公司对抗生素开发恢复了兴趣,也增加了投入,有望为开发新的抗生素奠定基础。现代社会的人们已经意识到了细菌耐药这一问题的严重性和危害,世界卫生组织也发出警告,如果人类不迅速采取一些措施,耐药性危机即将到来。世界卫生组织总干事陈冯富珍做出了这样的预测,人类即将进入“后抗生素时代,到时候甚至对许多普通的感染性疾病都将无药可用,细菌将再一次不能被杀灭。”
各位达人,求助十一烷酰氯含量及杂质的检测方法,找了好久一直没找到,请各位达人帮忙~~~不胜感激~~~~
医院里做万古霉素的血药浓度监测,自己查了点资料,一是直接沉淀血清蛋白后进样,另一个是用萃取方法,因为前者简单就想用沉淀法,但遇到一个问题是:万古是一糖肽类抗生素,一般的蛋白沉淀剂都可以让它也沉淀下来,所以想问一下高手的解决方法?[em07]
本人正在使用岛津HPLC做一条肽的药代动力学,用的C18硅胶柱,流动相是水和乙腈梯度洗脱(都含有千分之一三氟乙酸),求做过多肽血浆样品的高手给一些血浆处理方法的建议,目前使用乙腈沉淀法发现峰几乎检测不到,加了点甲酸好一点。参考文献中做万古霉素的方法,血浆样品加入25%三氯乙酸酸与乙腈(2:1),药品的峰还是特别小。使用乙酸乙酯萃取法也做了,提取下层水层,也是没有峰,而且血浆中杂蛋白特别多。多肽药做血浆样品是不是不能用乙腈沉淀法呢?调整乙腈的比例会出现理想的效果吗?最近几天测纯样品(当天解冻的)不加到血浆里发现目标峰面积表小很多,内标就比较正常,不清楚是柱效问题还是紫外检测器问题。以上问题求高手给一些建议,感激涕零!
辐射灭菌是诸多灭菌方法中的一种,但那些药物适合用辐射法灭菌?那些药物不适合用辐射法灭菌呢?现简要总结,供同一个战壕的战友参考。一、可用辐射法灭菌的药物包括:1、抗菌素类:青霉素钾、普卡因青霉素水混悬液、普鲁卡因青霉素油剂、苯基青霉素钠、苯甲氧基青霉素、氨苄青霉素、链霉素、氯霉素、红霉素、卡那霉素、金霉素、土霉素、万古霉素、硫酸新霉素、制菌霉素、利福平、两性霉素B等 2、激素类:丙酸睾丸素粉液及其油溶液、雌二醇、己烯雌酚、醋酸孕烯炔醇酮、孕甾醇、醋酸皮质素、可的松、强的松龙 3、巴比妥类:苯巴比、苯巴比妥、戊巴比妥、戊巴比妥4、菌苗抗毒素类 :斑疹伤寒疫苗、白喉抗毒素 5其他类:生理盐水、注射用水、盐酸普鲁卡因及其溶液、10%葡萄糖酸钙 二、不适宜用辐射法灭菌的药物包括:1、生物碱类:硫酸阿托品注射液、盐酸吗啡注射液、盐酸麻黄碱注射液等、苹果酸麦角新碱注射液、0.5%盐酸利多卡因等。2、生物制品类:脑垂体后叶激、胰岛素注射液、果青蛋白锌胰岛素注射液、肝素及其注射液、果青制破伤风抗毒素、三磷酸腺苷注射液、冻干人血浆 等。3、强心苷类:毛花强心苷注射液、洋地黄毒甙注射液等 4、维生素类:维生素B6液、维生素B12注射液等 5、酶类:玻璃酸酶、粘脘酸 等
《菜根谭》中说:“天地有万古,此身不再得。”?人生无法重来,生命仅有一次,应当且行且珍惜。?我们不只是要养好身体,延长生命的长度,远离疾病苦痛。?更要富养内心,活出生命的宽度,让身心丰盈,福泽绵绵,才不枉来人间一趟。[img]https://ng1.17img.cn/bbsfiles/images/2023/08/202308060317108348_9326_1642069_3.png[/img]
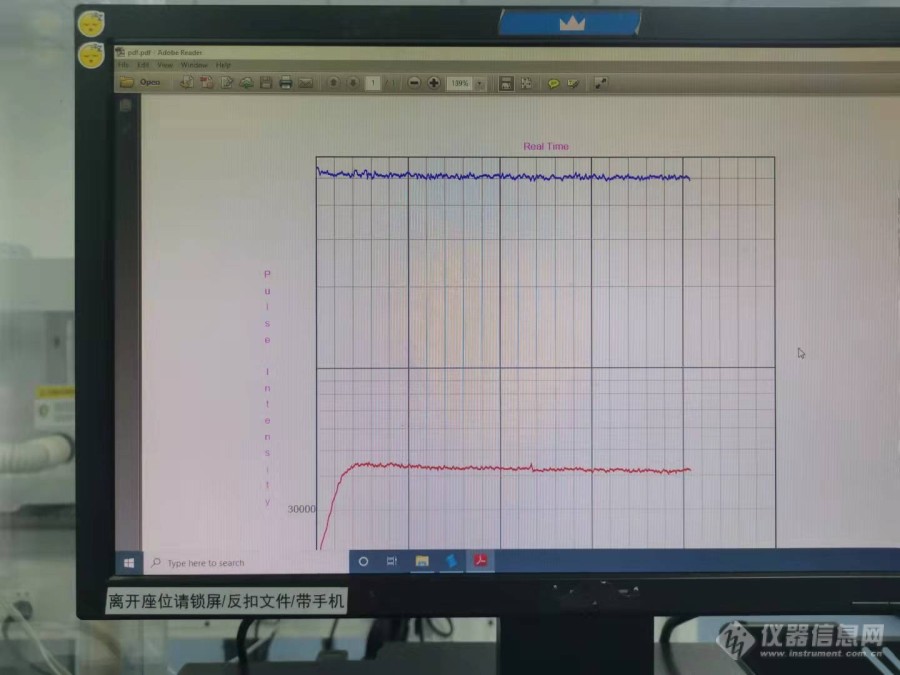
[color=#333333]ICHQ3D元素杂质指导原则下的药物中24种元素杂质方法开发与验证[/color][color=#333333]第一部分:一套[url=https://insevent.instrument.com.cn/t/yp][color=#3333ff]ICP-MS[/color][/url]方法精确稳定测试ICHQ3D元素杂质指导原则下的药物中24种元素杂质可行性[/color][color=#333333]对于[url=https://insevent.instrument.com.cn/t/yp][color=#3333ff]ICP-MS[/color][/url]来说,几十种元素同时测定对于仪器来说理论上是可行的,但是存在很多挑战。以ICH Q3D元素杂质指导原则下的药物中24种元素杂质同时测定为例,从实践经验出发,做简要说明。[/color][color=#333333]首要问题是要考虑这些元素包括各自溶液里面含有的基体离子是否可以稳定共存。由于Ru,Pd,Au,Os,Pt等元素基体为盐酸,银离子这个氯离子会产生AgCl沉淀。很多有经验的人都说Ag可以用2%盐酸络和,可是AgCl2与AgCl肯定是存在沉淀溶解平衡的,简单说,我不认为可溶性银可以在含有氯离子的溶液里长时间稳定存在。但是,可以有个折中的办法,就是把Ag和其他含有盐酸基体的元素分开配成母液,等制备线性和加标样品溶液时再让他们混合在一起。《医药分析杂质》2020年的顾宵等人曾考察了葡萄糖酸钙注射液24种元素的溶液稳定性,无论是标准线性溶液还加标样品溶液的波动均在8%以内。[/color][color=#333333]第二个问题是,Hg,Au,Os等元素需要加2%左右的盐酸才能较好得稳定在待测溶液里,否则,会有严重的残留可能连元素线性都走不出来。问题就来了:仪器必须要有较强的消除干扰的能力。(如果仪器无法耐受ClO的质谱干扰,那至少要两套方法,V和Cr需要另外做了)。[/color][color=#333333]第三个问题:由于元素过多,可能会存在同量异位素,比如说Pd与Sn。通过软件推荐与个人判断选择没有重叠的质量数。可在参考前篇文献的基础上,再做微调即可。[/color][color=#333333]最后,随着进样系统的改进,稀释气成了主流[url=https://insevent.instrument.com.cn/t/yp][color=#3333ff]ICP-MS[/color][/url]仪器的标配,但是因为含有Os,Au,Hg等元素,如果你没有加盐酸去增加溶液对这些元素的溶解性,稀释气不要开太大,不推荐超过0.2L/min。避免更严重的元素残留。[/color][color=#333333]其实,从分析可以看出来,即使做到一个方法里,对仪器与人员都要求较为严苛,付出的劳动肯定是加倍的。这种情况,不论是最终两套还是一套方法,理所当然得要更多的报价才符合实际。[/color][color=#333333]第二部分:谁是ICHQ3D元素杂质里最难测定的元素?[/color][color=#333333]前文说,在不考虑样品基体的情况下,存在24种ICH要求元素的一次测定的可能性。本篇文章以最近实验为例,做简要说明:实际项目里复杂基体做24种元素的复杂性。[/color][color=#333333]在不能抗ClO干扰的仪器上,Au就是YYDS。为了Hg的稳定性不得不加入了200μ/l的金元素,搞得Au深度残留。所谓深度残留就是说:在碰撞反应池前可能都有大量的残留,也就是说你把仪器的能换的东西都换一遍,也不能解决金元素的残留。在更换炬和锥的前提下,也需要冲洗很久,需要数个小时,才能将空白冲洗到亚ppb级别。显然,在第三方实验室是不可能给你这么用仪器的。现实往往就是需要我们在较高金元素背景的基础上去做实验。[/color][color=#333333]大家都知道可以Au的基体是盐酸,理论上来说,用盐酸会更好,也可以把金元素和含盐酸基体的元素一起做。但如果真的用盐酸体系去做实验会遇到很多坑。原因是:不同Cl的含量和Cl的化学形态会影响在仪器上Au脱附的程度(结论来自于实践经验,不作赘述)。所以,前文那个在葡萄糖酸钙注射液里同时测定24元素的文献是比较鸡贼的,挑了一个最简单的情况去做应用。[/color][color=#333333]曾遇到的比较反直觉的用盐酸基体做Au的案例:开发实验的样品金元素测得值基本平行,加标回收率虽然波动比较大,但也符合要求。但是过程空白RB偏高,按说强度应该和同等酸度的线性空白一致,你总不能说加热一下,就凭空出来很多金元素吧?所以,这时候我为了避免偶然性,读了一百次数据,如下图[/color][img]https://ng1.17img.cn/bbsfiles/images/2021/09/202109200126549456_7799_3426767_3.[/img][align=center][img=,690,517]https://ng1.17img.cn/bbsfiles/images/2021/09/202109231031398718_2301_3237657_3.jpg!w690x517.jpg[/img][/align][color=#333333]此时信号,经过四十多秒的上升期,以后信号相当稳定,但是有一点点下降趋势。分析如下:前面那40多秒的上升期:属于基体切换过程中的进样系统脱附的过程,后面的信号其实就是Au不断洗脱而检测下来的信号。重新走线性空白(含有和过程空白与样品溶液同等含量的盐酸)就信号变得很低,所以不可能是试剂里面的。真相就是:不同Cl的化学形态影响了仪器进样系统的金元素的洗脱效率,并且,这个过程较为稳定(洗脱Au的过程比较漫长),所以信号也比较稳定,只是略有下降趋势。图中绿色线为内标Bi,红色为Au元素信号。[/color][color=#333333]前文说的折中方案其实就是最终方案。实际的项目复杂性,不仅仅在于理论上的,更多时候是要考虑此时此地的资源。最后结论是:很多时候ICH的24个元素三套验证是可以保证的,两套要看实际情况,一套除非是特例,比如可以直接溶解,样品浓度比较小等情况时。关键性元素Ag,V,Cr一起,贵金属,Os等盐酸基体元素一组,Au理论上可以归到第二组,实际上,很多需要消解的例子,只能是单独拿出来用硝酸体系做,以避免Au的洗脱效率不同而造成数据异常。如果您的仪器用Au去做Hg的稳定剂,那么Au就是最难做的元素,没有之一,此时最后解决之道也变成了:索性让Au稳定在仪器上,往往避免加盐酸,而把金做到硝酸体系里去,但是硝酸溶解金的能力弱,所以溶液残留也比较严重。做实验的时候需要注意冲洗,算是一个折中的办法。如果想要扯彻底的解决Au难测定的问题,只有用额外加稀盐酸的方式去稳定Hg,此时实验室的解决方案才更有可能一套方法去测定24元素。[/color][color=#333333]第三部分:在深度残留Au的仪器上,且仪器可使用时间有限的情况下,做Au元素开发验证的要点。[/color][color=#333333]降低仪器本底还是必须要做的:用样品溶液冲洗仪器的Au残留20min,同时起到了老化锥口的作用。[/color][color=#333333]关闭稀释气体,稀释气会让气溶胶更干,从而让难溶解的Au更容易的残留,增大冲洗的难度。[/color][color=#333333]每针溶液之间用稀释剂(稀硝酸)冲洗,千万不要用盐酸冲洗,这会把残留的Au大量得冲洗下来,而完全冲洗下来又需要的时间太长,反而把事情搞得更复杂了。[/color][color=#333333]当进第一个样品基体时,要注意放置一段时间(比如:3分钟)再开始测试,避免切换样品溶液过程中冲洗下来比稀硝酸多几倍的金。当然,如果样品就是盐酸,我们可以尽可能得减小样品浓度,并且考虑基体匹配。[/color]
小妹我要试验固相萃取HPLC测定万古霉素血药浓度的方法。线性在2.5ug~80ug/ml。固相萃取预处理血浆样品的话,一般使用什么小柱的?怎么定下规格?http://simg.instrument.com.cn/bbs/images/brow/emyc1010.gif我看有文献提到用Cleanert PEP萃取柱,30mg/ml,对于这个填料量和空柱管体积,是怎样选择的?也有的文献用phenom enexstrata 200mg/3ml,怎么差别那么大呀?菜鸟痛苦中http://simg.instrument.com.cn/bbs/images/brow/em09509.gif