新人有难,还请各位大仙帮助。我需头孢妥仑匹酯片的进口标准,有货源的给新人说声,感谢!我的邮箱ahwuyan@live.cn。
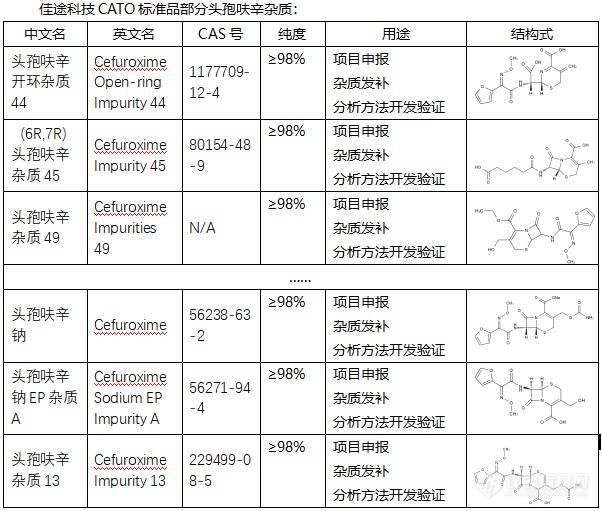
头孢呋辛是一种广泛使用的抗生素,主要用于治疗由敏感细菌引起的各种感染。在生产、储存和使用头孢呋辛的过程中,可能会产生一些杂质。这些杂质的存在可能会影响头孢呋辛的纯度和疗效,因此了解和控制这些杂质对于确保药物的安全性和有效性至关重要。头孢呋辛的杂质有多种,其中一些具有特定的CAS号、化学式和分子量。例如,头孢呋辛杂质33(Cefuroxime Impurity 33)的CAS号为929531-94-2,分子式为C16H16N4O9S,分子量为440.38。此外,还有其他一些头孢呋辛杂质,如头孢呋辛杂质A、B、C、D、E、F、G、H等。 CATO标准品提供的头孢呋辛全套的杂质,这些杂质对于药物的纯度和稳定性研究至关重要,也是药物研发过程中不可或缺的一部分。[img=,602,511]https://ng1.17img.cn/bbsfiles/images/2024/02/202402192104451830_7644_6381607_3.png!w602x511.jpg[/img] 广州佳途科技股份有限公司深知药物研发与质量控制的重要性,CATO标准品厂家,提供头孢呋辛全套的杂质,为客户提供更加精准、可靠的分析标准品,助力药物研发事业的快速发展,以满足客户在药物研发和质量控制方面的需求。[list][*]原创检测区[/list]◇头孢呋辛杂质头孢呋辛是一种广泛使用的抗生素,主要用于治疗由敏感细菌引起的各种感染。在生产、储存和使用头孢呋辛的过程中,可能会产生一些杂质。这些杂质的存在可能会影响头孢呋辛的纯度和疗效,因此了解和控制这些杂质对于确保药物的安全性和有效性至关重要。头孢呋辛的杂质有多种,其中一些具有特定的CAS号、化学式和分子量。例如,头孢呋辛杂质33(Cefuroxime Impurity 33)的CAS号为929531-94-2,分子式为C16H16N4O9S,分子量为440.38。此外,还有其他一些头孢呋辛杂质,如头孢呋辛杂质A、B、C、D、E、F、G、H等。CATO标准品提供的头孢呋辛全套的杂质,这些杂质对于药物的纯度和稳定性研究至关重要,也是药物研发过程中不可或缺的一部分。广州佳途科技股份有限公司深知药物研发与质量控制的重要性,CATO标准品厂家,提供头孢呋辛全套的杂质,为客户提供更加精准、可靠的分析标准品,助力药物研发事业的快速发展,以满足客户在药物研发和质量控制方面的需求。
请教各位有没有做过头孢呋辛酯(USP)的???能否讨论一下,具体操作!谢谢!!
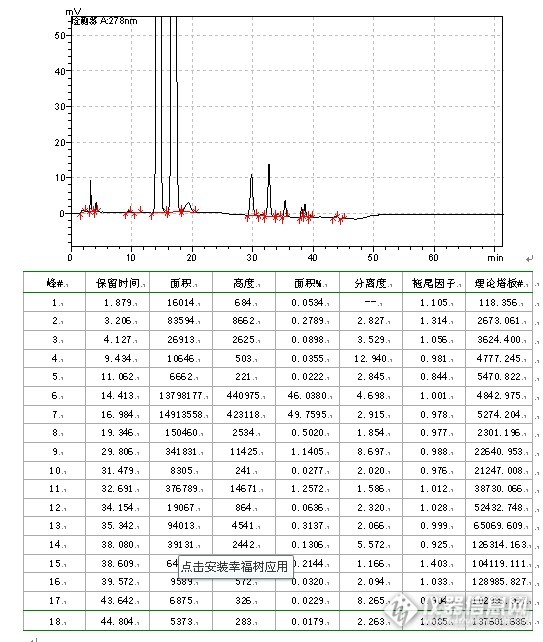
“色”路蹒跚,不拘一格,头孢呋辛酯干混悬剂有关物质流动相摸索部分。我主要工作是仿6,在遇到国家标准,我一般持研究态度,因为仿制药提倡的是仿制其质量而不是标准,一般会进行些比较。例如该品种在中国药典2010年班二部有收载,用的是等度洗脱方式,在进行研究的时候,发现梯度洗脱更具优势,所以就改变了系统方式。其具体研究方式如下:6.4 有关物质6.4.1方法的选择参照中国药典2005年版二部收载的头孢呋辛酯原料药质量标准、美国药典USP32-NF27收载的头孢呋辛酯混悬剂质量标准和新药转正标准第60册收载的头孢呋辛酯干混悬剂质量标准WS1-(X-391)-2004Z有关物质检查项,本品选择高效液相色谱法作为有关物质检测方法。6.4.2方法学验证6.4.2.1 试验材料仪器:LC-10AT、20AT VP泵(SHIMADZU CORPORATION)SPD-10A、20A、M20A VP紫外检测器(SHIMADZUCORPORATION)工作站:LC solution(SHIMADZU CORPORATION) 色谱柱:C18色谱柱,粒度5um,规格250mm×4.6mm,wel518425,LN:W1801.19,SN:1021096.主要试剂:甲醇(色谱纯)、磷酸二氢铵(分析纯)、6.4.2.2 波长选择根据专属性试验结果并参照中国药典2010年版(二部)收载的头孢呋辛酯原料药质量标准、美国药典USP32-NF27收载的头孢呋辛酯混悬剂质量标准和新药转正标准第60册收载的头孢呋辛酯干混悬剂质量标准WS1-(X-391)-2004Z有关物质检查项,本品选择高效液相色谱法作为有关物质检测方法。波长选择为278nm。6.4.2.3 流动相选择参照中国药典2010年版(二部)收载的头孢呋辛酯原料药质量标准、美国药典USP32-NF27收载的头孢呋辛酯混悬剂质量标准和新药转正标准第60册收载的头孢呋辛酯干混悬剂质量标准WS1-(X-391)-2004Z有关物质检查项色谱条件:用十八烷基硅烷键合硅胶为填充剂;流速为每分钟1.0ml,检测波长278nm,进样量20μl。6.4.2.3.1 等度洗脱流动相配制:①0.2mol/L磷酸二氢铵溶液-甲醇(60:40);②0.2mol/L磷酸二氢铵溶液-甲醇(50:50);③0.2mol/L磷酸二氢铵溶液-甲醇(55:45)。供试样品配制:称取头孢呋辛酯对照品适量(约相当于头孢呋辛11mg),置20ml量瓶中,加2ml甲醇超声溶解,分别用相应的流动相稀释至刻度,摇匀,滤过,精密量取20μl注入液相色谱仪并记录色谱图。试验结果见表10-6,色谱图见图37~39。表10-6等度洗脱试验结果 流动相异构体保留时间 (min.)拖尾因子与相邻峰 分离度理论板数出峰个数①异构体B15.7570.9922.189487111异构体A18.6880.9673.030[f
[align=right][b]SGLC-LC-338[/b][/align][b]摘要:[/b]本文建立了头孢呋辛钠有关物质分析的HPLC方法。参照2020版《中国药典》中色谱条件,采用色谱柱ShimNex HE C8分析头孢呋辛钠有关物质,结果显示,去氨甲酰头孢呋辛与头孢呋辛分离度大于3.0,且主峰与后相邻杂质峰基线分离,满足《中国药典》要求。此方法可为头孢呋辛钠有关物质分析提供参考。。[b]关键词:[/b]头孢呋辛钠 有关物质 ShimNex HE C8 HPLC[b]1. 实验部分1.1 实验仪器及耗材[/b]Shimadzu LC-40D高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url];色谱柱:ShimNex HE C8 (5 μm,4.6×250 mm;P/N:380-01241-09);纯水机:PR-FP-0120α-MT1(+ 60L水箱 + 取水器)SHIMSEN Arc Disc HPTFE针式过滤器(P/N:380-00341-05);[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]认证样品瓶LabTotal Vial(P/N:227-34001-01);SHIMSEN Pipet[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url]:SHIMSEN Pipet PMII-10(P/N:380-00751-02);SHIMSEN Pipet PMII-100(P/N:380-00751-04);SHIMSEN Pipet PMII-1000(P/N:380-00751-06)。[b]1.2 系统适用性溶液的制备[/b]取头孢呋辛对照品适量,加水溶解并稀释制成每1 mL含0.5 mg的溶液,置60℃水浴放置30分钟,放冷,使头孢呋辛部分转化为去氨甲酰头孢呋辛。[b]1.3 分析条件[/b]色谱柱:ShimNex HE C8 (5 μm,4.6×250 mm;P/N:380-01241-09)柱温:30℃检测波长:273 nm流速:1.0 mL/min进样量:20 μL流动相:A: 醋酸盐缓冲液(取醋酸钠0.68 g,冰醋酸5.8 g,加水稀释成 1000 mL,用冰醋酸调节pH值至3.4) B:乙腈梯度程序如下:[img]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGLC-LC-338-01.png[/img][b]2. 实验结果[/b]按照上述色谱条件(1.3)进行采集,系统适用性溶液色谱图如下:[b]系统适用性溶液[/b][img]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGLC-LC-338-02.png[/img][b]系统适用性放大图[/b][img]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGLC-LC-338-03.png[/img][img]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGLC-LC-338-04.png[/img][img]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGLC-LC-338-05.png[/img][b]重现性[/b]系统适用性溶液重现性[img]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGLC-LC-338-06.png[/img][b]3. 结论[/b] 本文建立了头孢呋辛钠有关物质分析的HPLC方法。参照2020版《中国药典》中色谱条件,采用色谱柱ShimNex HE C8分析头孢呋辛钠有关物质,结果显示,去氨甲酰头孢呋辛与头孢呋辛分离度大于3.0,且主峰与后相邻杂质峰基线分离,满足《中国药典》要求。此方法可为头孢呋辛钠有关物质分析提供参考。
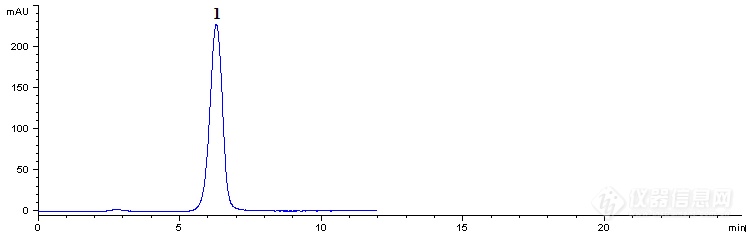
β-内酰胺类抗生素中存在的各类高分子聚合杂质是引发速发过敏反应的过敏原,因此,有必要对头孢呋辛赖氨酸原料药中的聚合物进行控制。根据《中国药典》2020年版(四部)分子排阻色谱法测定。色谱条件色谱柱:葡聚糖凝胶色谱柱 (10 mm×300 mm,40~120 μm);流动相A:pH 7.0 的0.025 molL-1磷酸盐缓冲液[0.025 molL-1磷酸氢二钠-0.025 molL-1磷酸二氢钠溶液(61:39)];流动相B:水;流速:1.2 mLmin-1 ;检测波长:254 nm ;柱温:35[font=宋体]℃[/font] 。系统适用性试验以流动相B为流动相测定,取0.5 mgmL-1蓝色葡聚糖2000溶液100 μL注入液相色谱仪,记录色谱图。再精密量取对照溶液100 μL,连续进样6次,记录色谱图,计算峰面积值的相对标准偏差。以流动相A为流动相测定,取0.5 mgmL-1蓝色葡聚糖2000溶液100 μL注入液相色谱仪,记录色谱图。称取头孢呋辛赖氨酸约0.2 g,置10 mL量瓶,0.5 mgmL-1蓝色葡聚糖2000溶液溶解并稀释至刻度,摇匀,得头孢呋辛赖氨酸的蓝色葡聚糖2000溶液。取100 μL上述溶液注入液相色谱仪,记录色谱图。再取供试品溶液100 μL注入液相色谱仪,记录色谱图。蓝色葡聚糖2000溶液在A、B两种流动相条件下,理论塔板数按蓝色葡聚糖2000峰计算均不低于700,拖尾因子均小于2.0。在两种流动相系统中蓝色葡聚糖2000峰保留时间的比值为1.03,对照溶液主峰和供试品溶液中聚合物峰与相应色谱系统中蓝色葡聚糖2000峰的保留时间的比值分别为1.02,1.02。头孢呋辛赖氨酸蓝色葡聚糖2000溶液的色谱图中高聚体峰高和单体与高聚体之间的谷高的比值为8.5。对照溶液连续进样6次的峰面积值的RSD值为1.2%。试验结果见Fig.1[font=宋体]~[/font]Fig.5。[align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/10/202110101406333568_7396_3528941_3.png[/img][/align]Fig.1 The HPLC chromatogram of blue dextran 2000 with mobile phase B(1. blue dextran 2000)[align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/10/202110101406335695_9383_3528941_3.png[/img][/align][align=center]Fig.2 The HPLC chromatogram of blue dextran 2000 with mobile phase A (1. blue dextran 2000)[/align][align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/10/202110101406337638_107_3528941_3.png[/img][/align][align=center]Fig.3 The HPLC chromatogram of cefuroxime lysine dissolved in blue dextran 2000[/align][align=center]with mobile phase A(1.cefuroxime polymer and blue dextran 2000)[/align][align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/10/202110101406338373_9932_3528941_3.png[/img][/align][align=center]Fig.4 The HPLC chromatogram of cefuroxime lysine sample with mobile phase A[/align][align=center] (1.cefuroxime polymer)[/align][align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/10/202110101406339357_599_3528941_3.png[/img][/align][align=center]Fig.5 The HPLC chromatogram of contrast solution with mobile phase B (1.cefuroxime)[/align]
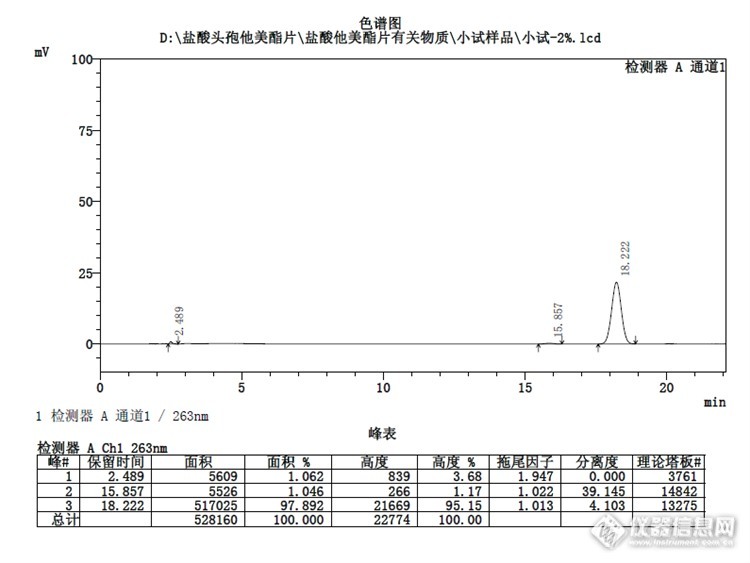
盐酸头孢他美酯是种广谱抗生素,可用于对它敏感细菌感染所引起的炎症。该产品为口服用。化学名:(6R,7R)-3-甲基-7-结构式:http://ng1.17img.cn/bbsfiles/images/2014/03/201403302127_494735_1621890_3.gif 英文名:Cefetamet Pivoxil Hydrochloride Tablets 药物别名:威锐片 成份:本品主要成分为盐酸头孢他美酯 性状:本品为薄膜衣片,除去包衣后呈白色、类白色,有引湿性。 药代动力学:本品单一剂量和多剂量的药代动力学参数基本一致。本品口服后,经过肠黏膜或首次经过肝脏时盐酸头孢他美酯被迅速代谢,在体内转变为头孢他美而发挥作用。本品随食物口服后,平均约55%的剂量转变为头孢他美。口服本品500mg后3~4小时,血药浓度达峰值4.1±0.7mg/L,分布容积为0.29L/kg,与细胞外水平一致。约22%头孢他美与清蛋白结合。年龄、肾脏及肝脏疾病对盐酸头孢他美酯的生物利用度无影响。抗酸剂(镁、铝、氢氧化物等)或雷尼替丁不改变本品生物利用度。本品90%以头孢他美形式随尿液排出,清除半衰期为2~3小时。肾衰竭患者,头孢他美的清除情况同肾功能成正比。 适应症:本品适用于敏感菌引起的下列感染:1.耳、鼻、喉部感染,如中耳炎、鼻窦炎、咽炎、扁桃体炎等。2.下呼吸道感染,如慢性支气管炎急性发作、急性气管炎、急性支气管炎等。3.泌尿系统感染,如非复杂性尿路感染、复杂性尿路感染(包括肾盂肾炎)、男性急性淋球菌性尿道炎等。注意事项 1.对青霉素类药物过敏者慎用。 2.若发生严重过敏反应,应立即停药,并紧急治疗。 3.在使用本品期间,由于肠道微生物的改变,可能导致伪膜性肠炎。若发生假膜性肠炎,应积极治疗(推荐使用万古毒素)。 4.本品应放到儿童触及不到的地方。 孕妇及哺乳期妇女用药:1.由于缺乏有关人类胎儿的临床数据,妇女妊娠期间,不推荐使用本品。若有对该药敏感的微生物严重感染时,必须充分权衡利弊。2.在乳汁中尚未发现本品的代谢物。 儿童用药:本品对新生儿的有效性和安全性尚无可靠的临床数据。 药物相互作用: 抗酸剂,H2受体拮抗剂对本品的药代动力学无影响。目前尚未见到本品对实验室检测值和/或方法有影响的报道,也未观察到伴随利尿药治疗的患者在使用本品时对肾功能的损伤。 药物过量: 若过量服用,发生严重反应,应洗胃,并采取对应治疗。 贮藏:遮光、密封、在干燥处保存。详见:http://baike.so.com/doc/6048874.html该品种国内批准文号有40个,见国家药监局网。截图如下:http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_646694_1621890_3.png试验条件:主要参照中国药典2010年版二部。用十八烷基硅烷键合硅胶为填充剂;以乙腈-甲醇-水-磷酸盐缓冲液(取无水磷酸氢二钠5.8g与磷酸二氢钾3.5g,加水溶解并稀释成1000ml)(360:95:500:45)为流动相;检测波长为263nm。取头孢他美酸和头孢他美酯对照品适量,用乙腈溶液(9→20)溶解并稀释制成每1ml中约含头孢他美酸0.05mg和含头孢他美酯1.4mg的混合溶液,取10μl注入液相色谱仪,头孢他美酯峰与头孢他美酸峰的分离度应不小于28.0,头孢他美酯峰与其相对保留时间约为0.9和1.1处杂质峰的分离度均应大于于2.0,理论板数按头孢他美酯峰计算不低于3000。取本品的细粉适量,加乙腈溶液(9→20)溶解并定量稀释制成每1ml中约含头孢他美1.0mg的溶液,滤过,取续滤液作为供试品溶液;精密量取供试品溶液适量,用乙腈溶液(9→20)定量稀释制成每1ml中约含头孢他美20μg的溶液,作为对照溶液。照含量项下的色谱条件,取对照溶液10μl注入液相色谱仪,调节检测灵敏度,使主成分色谱峰的峰高约为满量程的25%;再精密量取供试品溶液与对照溶液各10μl,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的4.5倍。供试品溶液色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液主峰面积(2.0%),各杂质峰面积的和不得大于对照溶液主峰面积的2.5倍(5.0%)。色谱柱信息:月旭Welchrom C18, 5μm, 4.6×250mm(货号:00310-02043;序列号:w13211564)试验图谱:1.系统适用性溶液:http://ng1.17img.cn/bbsfiles/images/2014/03/201403302057_494730_1621890_3.png2.供试品溶液:http://ng1.17img.cn/bbsfiles/images/2014/03/201403302112_494732_1621890_3.png3.对照溶液:http://ng1.17img.cn/bbsfiles/images/2014/03/201403302121_494734_1621890_3.png
服用头孢类药物后喝酒等于服用毒药。截至今年上半年,我市人民医院共接到30余起此类事件,严重者酒后休克。"广大市民一定要注意,服用或者注射头孢类药物后一周内不要饮酒,否则极易发生危险。"市人民医院急诊科主任刘建强说。 一名40岁女性在服用头孢类药物后,酒场上盛情难却,喝了一口白酒,10分钟后,昏倒在地,浑身出现潮红症状,被紧急送往医院抢救。一位老年人睡眠有障碍,喜欢吃完安定后,再喝上一些酒来促进睡眠,自认为喝点酒更有利于睡眠,不曾想差点要了性命。幸好家人及时拨打了120急救电话,避免了悲剧的发生。"这都是典型的药物和酒精混和发生的反应,市民一定要注意吃药避免饮酒。""服用头孢类药物一周内不要饮酒。"刘建强说,尽管一些市民了解吃药后不能喝酒的情况,但是服药后一周内不要饮酒却鲜为人知。酒精混药,药物抑制了解酒酶,容易形成中毒反应,通常表现为面色潮红、憋气、头痛、头晕、恶心、呕吐、心慌、胸闷、血压下降等状况。 药物在人体通过新陈代谢排出体外一般需要一周左右。"当然也与多种因素有关。药物本身,比如,头孢哌酮和酒反应最强烈的头孢类药物,同时与个人体质也有关系。不单独是头孢类药物,其他药物也会对人体产生影响,因此服药后一周内不要饮酒。"市人民医院急诊科医生谭秀岭介绍。 不知道各位有没有见过头孢类药物的说明书,是否有说明服用时不能饮酒?
用Sephadex G-10做头孢他啶,个别能分离,大多数不能分离,之所以这样,头孢他啶里有头孢他腚聚合物,但是我一直不没搞清楚这聚合物含量是多少呢,它分子结构是什么样呢?还有,我用的是G-10,10mmX300mm的柱子?望各位大虾多指教和发表言论![em09]
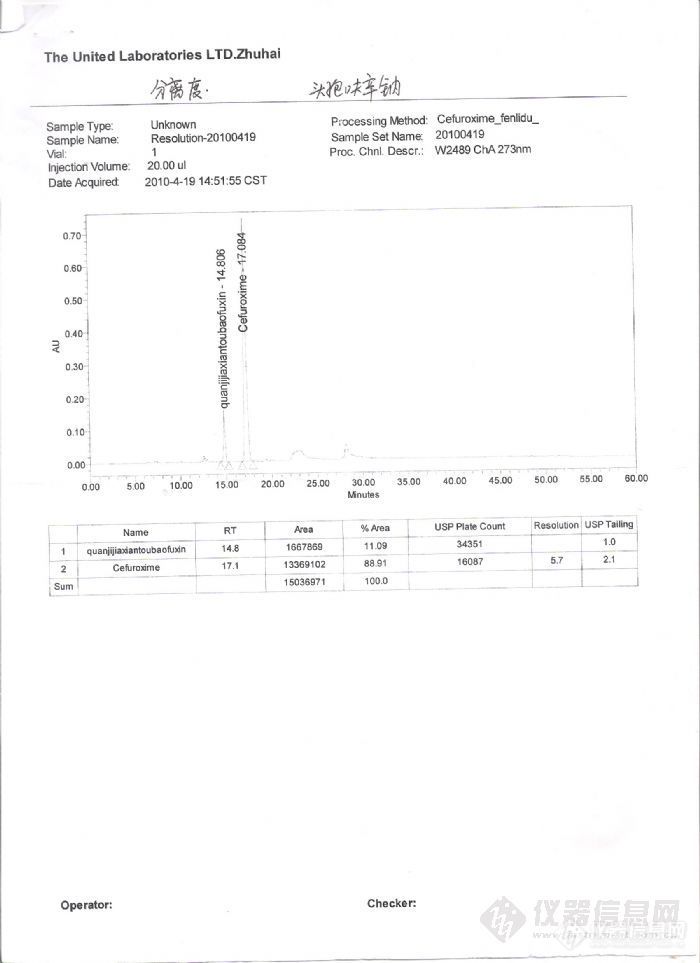
样品名称:头孢呋辛钠谱图提供者:珠海丽珠制药方法来源:2010年药典所用色谱柱:Ultimate XB-C8,5um,4.6*250mm标准品谱图及数据:http://ng1.17img.cn/bbsfiles/images/2010/06/201006021635_221858_1628076_3.jpg样品谱图及数据:http://ng1.17img.cn/bbsfiles/images/2010/06/201006021635_221857_1628076_3.jpg
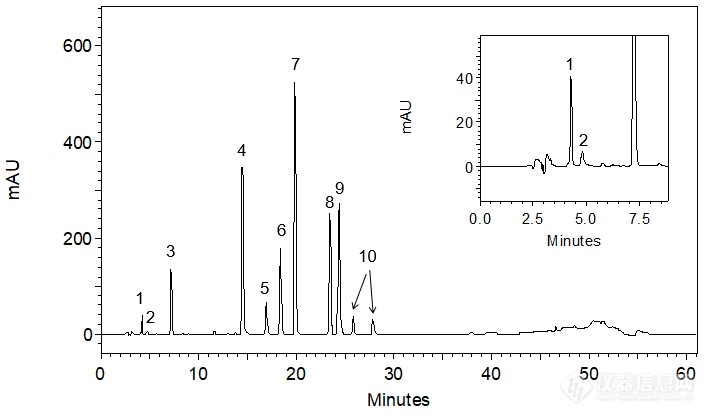
[align=center][b]头孢克洛有关物质——与9种杂质的共同分析[/b][/align]头孢克洛(cefaclor)为白色至微黄色粉末或结晶性粉末的化学品,微臭,本品在水中微溶,在甲醇、乙醇、三氯甲烷或二氯甲烷中几乎不溶,分子式:C15H14ClN3O4S。头孢克洛是β-内酰胺类抗生素,头孢菌素类药,是第二代头孢菌素,主要适用于敏感菌所致的急性咽炎、急性扁桃体炎、中耳炎、支气管炎、肺炎等呼吸道感染、皮肤软组织感染和尿路感染等。[align=center][img=,144,171]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140859582934_5220_2222981_3.gif!w144x171.jpg[/img][/align][align=center]头孢克洛[/align][align=center]M.W.: 367.81[/align]本实验对客户提供的头孢克洛原料药以及9种杂质(杂质A、B、C、D、E,7-ACCA,头孢克洛δ-3异构体,α-苯甘氨酸,苯甘氨酸甲酯盐酸盐)进行分析,希望得到杂质混合对照溶液及供试品溶液中各杂质的良好分离。客户反馈,将流动相磷酸盐体系的pH值由4.0提高到4.5可得到杂质混合对照溶液中7-ACCA和α-苯甘氨酸之间的良好分离,但头孢克洛与其相邻杂质E峰之间分离较难。客户前期使用了CAPCELL PAK C[sub]18 [/sub]MGII S3 4.6 mm i.d. × 250 mm色谱柱进行分析,在此基础上,我们尝试了其他填料的几款色谱柱进行分离尝试,分别为CAPCELL PAK C[sub]18[/sub] AQ(S3& S5)、CAPCELL PAK ADME(金刚烷基)、SUPERIOREX ODS、CAPCELL PAK PFP(五氟苯基)、CAPCELL PAK CN(氰基)。首先,参考客户提供的液相条件,使用高极性色谱柱[b]CAPCELL PAK C[sub]18 [/sub]AQ[/b]对杂质混合对照溶液进行分析尝试;为了得到杂质间的更好分离,粒径选择3 μm,如图1,[color=#2F5496]各杂质间均能得到良好的分离结果,头孢克洛与杂质[/color][color=#2F5496]E[/color][color=#2F5496]的分离度为[/color][color=#2F5496]2.70[/color][color=#2F5496],达到基线分离。[/color][color=#2F5496][/color][align=center][img=,690,405]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140902184290_9307_2222981_3.png!w690x405.jpg[/img][/align][align=center]图1 AQ S3 分析杂质混合对照溶液结果[/align][align=center] [/align][align=center]1.α-苯甘氨酸 2. 7-ACCA 3. 杂质A 4. 杂质B 5. 苯甘氨酸甲酯盐酸盐 6.杂质C[/align][align=center]7. 头孢克洛δ-3异构体 [color=#ff0000]8. 头孢克洛 9. 杂质E [/color]10.杂质D[/align][color=#2F5496][img=,555,311]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140902187828_2715_2222981_3.png!w555x311.jpg[/img][/color]进一步分析供试品溶液,如图2,由于样品浓度较高,导致头孢克洛主峰向后展宽,进而将杂质E包于其中。[color=#2F5496][/color][align=center][color=#2F5496][img=,659,441]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140915544228_5404_2222981_3.png!w659x441.jpg[/img][/color][/align][align=center]图2 AQ S3 分析供试品溶液结果[/align][align=center][/align][align=left]为使头孢克洛和杂质E之间得到更好的分离,我们尝试对色谱条件进行调整。[/align][align=left][/align][align=left][b]1.调整柱温[/b][/align][align=left][b][/b]首先对温度进行调整:实验过程中发现柱温对头孢克洛与杂质E的出峰行为有较大影响——当柱温设置为20 ℃时,头孢克洛和杂质E之间能够得到良好分离;将温度提高到30℃时,杂质E向前移动趋势较大。为使杂质E峰出在头孢克洛峰前,避免由于供试品中头孢克洛峰的展宽而使杂质E被包于其内,进一步将柱温提高到40℃,发现头孢克洛与杂质E峰重合;最终,将柱温提高到45℃,此时杂质E峰移至头孢克洛峰前,但未能得到理想的分离结果。[/align][align=left][/align][align=center][img=,659,430]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140916597550_373_2222981_3.png!w659x430.jpg[/img][/align][align=center]图3 不同柱温条件下AQ S3分析杂质混合对照溶液结果[/align][align=center][/align][align=left][b]2.调整流动相[/b][/align][align=left][b][/b][/align][align=left]考虑到提高柱温对色谱柱寿命的影响,仍选择初始使用的20℃,对流动相梯度条件进行调整。在增强整体保留时间的同时,发现[color=#538135]头孢克洛和杂质[/color][color=#538135]E[/color][color=#538135]的出峰顺序发生了颠倒[/color],且[color=#538135]分离良好[/color],进而有效避免了杂质E被包于头孢克洛主峰中的问题;而在主峰后出峰的杂质D与头孢克洛之间分离度亦较高,即使供试品溶液中的头孢克洛峰展宽,也不会出现将杂质D包于其中的问题。[/align][align=left]因此我们在此梯度条件下进一步对供试品溶液进行分析,如图4,头孢克洛与各杂质峰之间均能得到良好的分离结果。[/align][align=left][/align][align=center][img=,679,417]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140917450308_6331_2222981_3.png!w679x417.jpg[/img][/align][align=center]图4 AQ S3分析杂质混合对照溶液及供试品溶液结果(调整梯度)[/align][align=center] [/align][align=center]1.α-苯甘氨酸 2. 7-ACCA 3. 杂质A 4. 杂质B 5. 苯甘氨酸甲酯盐酸盐 6.杂质C[/align][align=center]7. 头孢克洛δ-3异构体 [color=#ff0000]8. 杂质E 9. 头孢克洛[/color] 10.杂质D[/align][align=left][img=,587,335]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140918136074_9375_2222981_3.png!w587x335.jpg[/img][/align][align=left][/align][align=left]为使客户有更多的色谱柱选择,本实验室也尝试使用键合金刚烷基的高极性色谱柱CAPCELL PAK ADME分析杂质混合对照溶液和供试品溶液,如图5,在分析杂质混合对照溶液时,能够得到各组分的良好分离,同时发现杂质E和头孢克洛出峰顺序发生颠倒,但同时也发现头孢克洛峰与其后相邻杂质D峰之间分离度较低(Rs=1.71);因此,如图6,在分析供试品溶液时,由于色谱峰向后展宽,使得杂质D被包于头孢克洛主峰中,未能得到理想分离结果。[/align][align=left][/align][align=center][img=,690,426]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140918484278_6616_2222981_3.png!w690x426.jpg[/img][/align][align=center]图5 ADME 分析杂质混合对照溶液结果[/align][align=center] [/align][align=center]1.α-苯甘氨酸 2. 7-ACCA 3. 杂质A 4. 杂质B 5. 苯甘氨酸甲酯盐酸盐 6.杂质C[/align][align=center]7. 头孢克洛δ-3异构体 [color=#ff0000]8. 杂质E 9. 头孢克洛[/color] 10.杂质D[/align][align=left][/align][align=center][img=,689,417]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140918485898_9906_2222981_3.png!w689x417.jpg[/img][/align][align=center]图6 ADME 分析杂质混合对照溶液结果[/align][align=left][img=,585,336]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140919331328_5070_2222981_3.png!w585x336.jpg[/img][/align][align=left][/align][align=left][/align][align=left]之后,我们也尝试使用了CN(氰基柱)和PFP(五氟苯基)以及高碳载量的SUPERIOREX ODS色谱柱,在客户提供的色谱条件下对杂质混合对照溶液进行分析,均未能得到更理想的分离结果。[/align]
以头孢曲松钠聚合物举例:按外标法以峰面积计算,含头孢曲松聚合物以头孢曲松计,不得过0.5%。 A供*M对*对照纯度聚合物%=----------------------------- A对*供试量*?举例来说,供试量为0.2g,百分含量为76.0%,?这个地方应不应该乘以76.0%,有何依据,不乘又有何依据?期盼得到各位老师的指导。个人意见:应该乘以头孢曲松的纯度76.0%,“含头孢曲松聚合物以头孢曲松计”,这里的头孢曲松我理解为供试品中的纯头孢曲松,因为是它产生的聚合物。如果那位老师有兴趣可以用QQ305115490和邮箱zongrui0911@163.com和我联系。寇宗睿
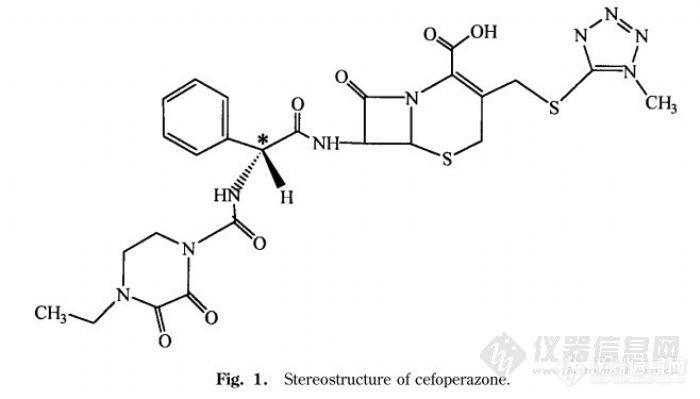
哪位老师知道头孢哌酮的s异构体是哪个C原子的手型导致的啊?就是药典中所述头孢哌酮s异构体是指哪个C原子? 另外有文献指出如下:“头孢哌酮钠在C3位可形成同分异构体,即日抗基所称副产物II,质量标准中控制限度1.5%。需要注意的是,头孢哌酮常有一未知杂质容易被误为认为是S-异构体,但是其UV吸收与S-异构体不同,可采用二极管阵列检测器进行鉴别或者控制。”这里所说的一未知杂质具体是哪个有老师知道吗?另外一篇文献显示头孢哌酮手性碳如图,该碳引起的异构体是否是药典中的S异构体呢?file:///C:/Users/ADMINI~1/AppData/Local/Temp/PQL651~GYQV‚3)CJ$JHK2.jpghttp://ng1.17img.cn/bbsfiles/images/2011/01/201101102123_273270_1352078_3.jpg这EP中有关物质F的手性碳不同。有没有可能该图即为上一文献中的未知杂质呢???谢谢指导。。
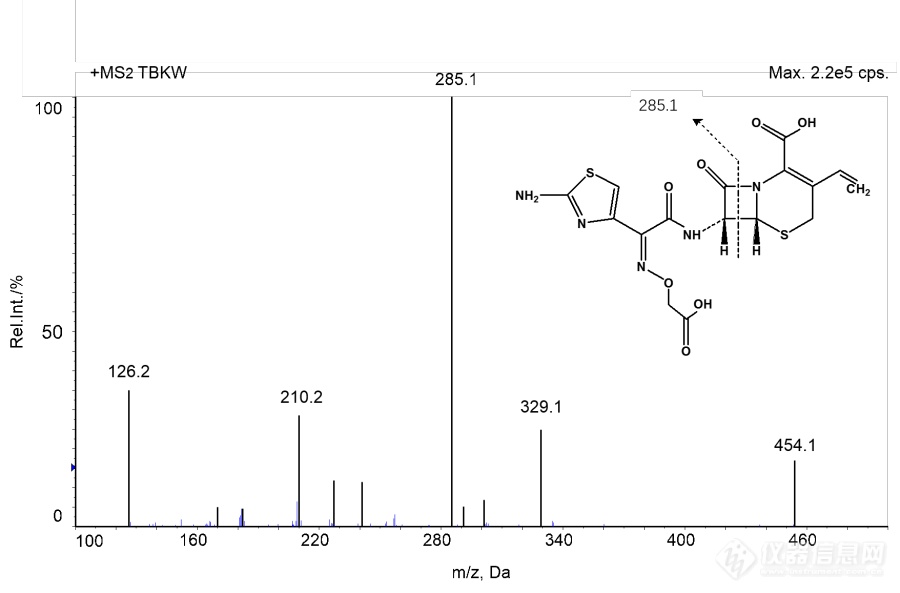
[align=left][b][size=32px][color=#ff0000]本篇文章暂不授权任何公众号发布[/color][/size][/b][/align][align=center][b]高脂肪饮食对头孢克肟片的药动学影响 [/b][/align][align=left][b]摘要:[/b]目的:研究比较空腹和高脂餐后单剂量口服用头孢克肟的药代动力学和生物利用度。方法:采用双交叉给药实验设计,12名健康男性受试者空腹及餐后单剂量口服1mg头孢克肟片,以头孢他美为内标,HP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS法测定血药浓度,DAS 2.0软件处理药动学参数。结果:头孢克肟空腹和餐后单剂量给药的主要药动学参数为:Cmax分别为([color=black]3.805 ±0.710[/color])μg/ml和([color=black]1.604 ±0.483[/color]) μg/ml,Tmax 分别为([color=black]4.792±0.582[/color]) h和([color=black]4.000±1.225[/color]) h,AUC[sub]0-t [/sub]分别为([color=black]32.923±7.804[/color]) μghmL[sup]-1[/sup]和([color=black]12.785±4.688[/color]) μghmL[sup]-1[/sup],AUC[sub]0-[/sub][sub][color=#231f20]∞[/color][/sub]([color=black]33.955±8.484[/color]) μghmL[sup]-1[/sup]和([color=black]13.082±4.932[/color]) μghmL[sup]-1[/sup]。两种给药方案的Cmax和AUC取自然对数后经方差分析,Tmax经非参数检验,发现Cmax,AUC和Tmax的差异有统计学意义(P<0. 05)。结论;与空腹组给药相比,餐后组吸收速率减慢,消除半衰期延长,生物利用度降低。[/align][align=left][b]关键词:[/b]头孢克肟;药动学;空腹餐后;生物利用度;[/align][align=left]头孢克肟(Cefixime)是一种重要的头孢菌素类抗生素,属于可口服的第三代头孢菌素类抗生素,临床上应用于敏感菌引起的肺炎、支气管炎、泌尿道感染、淋病、胆囊炎、胆管炎、猩红热、中耳炎、副鼻窦炎等。本研究参考有关人血浆中头孢克肟的定量方法,志愿者在空腹和餐后两种情况下服用进口头孢克肟片后取血,采用灵敏的[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS分析技术评价饮食对头孢克肟在人体内的药动学影响,为临床用药提供指导。[/align][align=left][b]材料与方法[/b][/align][align=left][b]1 仪器与试药[/b][/align][align=left]API4000型三重四级杆串联离子肼质谱仪,美国Applied Biosystem Sciex公司;Aglient 1260型液相色谱系统,包括G1312B二元泵,G1322A在线脱气机,G1316A柱温箱,Aglient Technology公司; NASCA F5100型自动进样器,日本SHISEIDO公司;资生堂CAPCELL PAC ADME柱(2.1*100mm,3mm,日本SHISEIDO公司);保护柱:Phenomenex C18(4*3.0mm,5mm,Torrance,CA,USA);梅特勒-托利多AG135电子天平,梅特勒-托利多仪器上海有限公司;Heraeus Multifuge XIR型离心机,美国Thermo Fisher公司;IKA VIBRAX VXR型振荡器;KQ5200DE型数控超声清洗机,昆山市超声仪器有限公司;Eppendorf可调式及自动[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]电动[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液器[/color][/url][/color][/url],德国Eppendorf公司。[/align][align=left]头孢克肟标准品(批号:130503-201716,纯度:89.2%,中国食品药品检定研究院);头孢他美(批号:130564-201601,纯度>99.8%,中国食品药品检定研究院);甲醇:美国Fisher公司,[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url] 级,批号:LOT180821;甲酸:美国MREDA公司,色谱纯,批号:LOT095224;乙腈:美国Fisher公司,[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url] 级,批号:LOT180821;超纯水:屈臣氏重蒸水,批号:20180815.[/align][align=left][b]2 试验方法[/b][/align][align=left][b]2.1 试验方案[/b][/align][align=left][b]2.1.1 受试对象[/b][/align][align=left]12名健康男性受试者,年龄在18-45岁,体重指数在19-24范围内,健康,无心血管、肝脏、肾脏、消化道、精神神经等疾病史,无药物过敏史。试验前详细询问既往病史,作全面的体格检查及实验室检查,心电图、血压、肝肾功能及血尿常规检查均正常,试验前两周未用任何药物。所有受试者均签署知情同意书,试验方案经本院伦理委员会审批同意。[/align][align=left][b]2.1.2 给药方案与样品采集[/b][/align][align=left] 试验采用双交叉设计。12名受试者随机分成两组,每组6人。1组为空腹组,另1组为餐后组。受试者在试验前1 d的17:00进人I期临床试验病房,晚上统一清淡饮食,并禁食10h,但不禁水。次日晨1组空腹口服药物,用250mL水送服。另1组则统一进食高脂标准餐,进餐时程为30 min,后即用250 ml温开水送服试验药物。0, 0.5,1,1. 5,2,2.5,3,3.5,4,4.5,5,6.5,7,8,10,12,15和24小时,抽取静脉血4 ml,置肝素化抗凝试管中,分离血浆于-80℃贮存,待测。[/align][align=left][b]2.2 色谱及质谱条件[/b][/align][align=left]色谱条件:流动相:乙腈(0.5%甲酸):水(0.5%甲酸)=40:60等度洗脱;柱温:40℃;流速:0.2 mL/min;进样量:5 mL;运行时间:4min。洗针程序:50%甲醇洗针5s,超声洗针5s(纯水),再次用50%甲醇洗针5s。[/align][align=left]质谱条件:离子源:电喷雾(ESI);扫描方式:多反应监测(MRM);离子化方式:正离子;检测离子对:TBKW m/z454.2/285.1;内标:389.2/241.1.离子源电压:4800V;离子源温度:400℃;气帘气:15psi;碰撞气:4psi 雾化气:60psi;辅助气:55psi;解簇电压:70V;碰撞诱导解离电压:TBKW:28V,TBTM :21V。[/align][align=left][b]2.3 溶液配制及样品处理[/b][/align][align=left][b]2.3.1溶液配制[/b][/align][align=left]对照品溶液:精密量取头孢克肟对照品11.21 mg,置于15 mL EP管中,用自动[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url][/color][/url]精密加入10 mL甲醇溶解,得到1 mg/mL的对照品储备液,置于-20℃备用。用50%甲醇-水配制成系列头孢克肟标准工作液,浓度分别0.5,1,5,10,20,50,100,160 mg/mL。4℃冰箱避光保存。[/align][align=left]质控工作液:精密量取头孢克肟对照品11.15 mg,置于15 mL EP管中,用自动[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url][/color][/url]精密加入10 mL甲醇溶解,得到1 mg/mL的对照品储备液,置于-20℃备用。用50%甲醇-水配制成系列头孢克肟标准工作液,浓度分别1,5, 20,130mg/mL。4℃冰箱避光保存。[/align][align=left]内标工作液:精密量取头孢他美对照品10.02 mg,置于15 mL EP管中,用自动[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url][/color][/url]精密加入10 mL甲醇溶解,得到1 mg/mL的内标储备液,置于-20℃备用。用纯甲醇稀释至500 ng/mL,4℃冰箱避光保存。[/align][align=left][b]2.3.2生物样本处理方法[/b][/align][align=left]a.血浆标准品及质控样品处理方法:取药前血浆190 uL,加10 uL适当浓度的标准溶液,混匀,加400 uL甲醇(含内标500 ng/mL),涡旋2min,离心(4℃,14000r/min)15min, 取100 uL上清液,加流动相A相200uL混匀,取5μL进样。[/align][align=left]血浆标准曲线范围: 0.025,0.05,0.25,0.5,1,2.5,5,8 u g/ml。[/align][align=left]质控样品浓度为: 0.075,1,6.5μg/ml 最低定量限: 0.075 ng/mL。[/align][align=left]b.血浆样品处理方法:取给药血浆200 uL,加400 uL甲醇(含内标500ng/mL),涡旋2min,离心(4℃, 14000 r/min) 15min, 取100 μL上清液,加流动相A相200μL混匀,取5μL进样。[/align][align=left][b]2.3.3数据统计处理方法[/b][/align][align=left]使用AB Secix公司Analyst 1.5.2软件采集处理数据。[/align][align=left][b]3方法学确证[/b][/align][align=left]对建立的方法进行方法验证, 参照中国药典2015版《生物样品定量分析方法指导原则》(草案),从方法的选择性、标准曲线和定量下限、精密度和准确度、稳定性、回收率、基质效应、残留效应和同位素效应等各方面进行方法验证。[/align][align=left][b]3.1选择性 [/b]分别取6份不同来源的人空白血浆样品以及相应人空白血浆配制的LLOQ 样品进行[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS分析测定,考察空白血浆中的内源性物质是否干扰待测物及其内标的测定。接受标准为:空白血浆中待测物保留时间处色谱峰面积不高于LLOQ色谱峰面积的20%;空白血浆中内标保留时间处色谱峰面积不高于内标色谱峰面积的5%。[/align][align=left][b]3.2 标准曲线[/b] 标准曲线设计8个浓度点, 头孢克肟血浆浓度分别为0.025, 0.05,0.25,0.5,1,2.5,5,8 u gmL-1, 按“血浆标准品及质控样品处理方法”项下操作, 以每个待测物浓度为横坐标, 待测物与内标物的峰面积比值为纵坐标, 用加权 ([i]W [/i]= 1/[i]x[/i]2) 最小二乘法进行回归运算, 求得的直线回归方程即为标准曲线。接受标准为:校正标样回算的浓度一般应该在标示值的±15%以内,定量下限处应该在±20%内;至少75%校正标样,含最少6个有效浓度,应满足上述标准标准;曲线的相关系数的值r≥0.990。[/align][align=left][b]3.3 残留考察 [/b]在标准曲线最高浓度点后连续进样2个空白样品, 考察样品与内标的残留效应。接受标准为:空白血浆中待测物保留时间处色谱峰面积不高于LLOQ色谱峰面积的20%;空白血浆中内标保留时间处色谱峰面积不高于内标色谱峰面积的5%。[/align][align=left][b]3.4 定量下限 [/b]根据血浆标准品处理方法,配制头孢克肟定量下限浓度的血浆样品6份(2.50ng/mL) ,考察其准确度和精密度。[/align][align=left][b]3.5 精密度与准确度[/b] 按“血浆标准品及质控样品处理方法”项下操作,配制最低定量限、低、中、高4个浓度的血浆样品,每浓度进行6个样本分析,分别在3日内测试,根据当日标准曲线计算质控样品的测得浓度,根据结果计算本法的日内、日间精密度与准确度。接受标准:批内精密度:低、中、高浓度批内变异系数≤15%,定量下限的变异系数≤20%。批间精密度:低、中、高浓度批间变异系数≤15%,定量下限的变异系数≤20%。准确度:所有质控样品准确度均值一般应在标示值的±15%之内,定量下限准确度应在标示值的±20%之内。[/align][align=left][b]3.6 回收率和基质效应 [/b]取6份不同来源的空白人血浆,加入人脂肪,制备不同来源的含20%的高脂肪血浆,另取同样6份不同来源的空白人血浆,加入人全血,制备不同来源的含4%的溶血血浆,按比例加入内标溶液和沉淀蛋白溶剂,混匀,离心,取上清,将基质提取出来,分别加入低,中,高浓度质控溶液,经流动相稀释进样分析,测定血浆,高脂血浆,溶血血浆三种处理后的基质下的低、中、高浓度质控样品TBKW及其内标的峰面积。 [/align][align=left]取6份不同来源的空白人血浆及6份水,按“血浆标准品及质控样品处理方法”项下操作,测定空白血浆,标准溶液状态下的低、中、高浓度质控样品TBKW及其内标的峰面积。 [/align][align=left]基质因子(效应)=处理后的空白血浆归一化后的峰面积/标准溶液归一化的峰面积*100% [/align][align=left]提取回收率=未处理空白血浆归一化后的峰面积/处理后的空白血浆归一化后的峰面积*100%。[/align][align=left]接受标准:提取回收率不一定需要满足接近100%,但是必需是稳定而可重现的。基质因子不一定需要接近100%,但是在不同个体的基质中应是稳定而可重现的。不同来源的内标归一化基质因子精密度应≤15%。[/align][align=left][b]3.7 溶液稳定性 [/b]按“血浆标准品及质控样品处理方法”项下操作,新鲜配制头孢克肟储备液并用50%甲醇稀释到低,高质控溶度,每个浓度各3个;取-20℃存放7天,30天的储备液稀释到高质控浓度3个以及4℃对应存放7天,30天储存的低,高浓度质控工作液各3个,进样分析,分别评价储备液和工作液溶液7天,30天的稳定性。接受标准:各储备条件下和对照(新鲜配制)的溶液的归一化峰面积的比值偏差在±15%之间。[/align][align=left][b]3.8 血浆样品稳定性 [/b]室温放置:取多份空白血浆适量,分别加入相应浓度的TBKW标准溶液,配制低、中、高三个浓度血浆样品室温放置5h、处理后的样本室温放置6h、冰箱4°C放置20h,按“血浆标准品及质控样品处理方法”项下操作,进样分析,考察血浆质控样品室温放置稳定性。另取精密度试验第二批三个浓度血浆样品,测定后于自动进样器(10°C)中放置16h后再进样分析,考察血浆质控样品于自动进样器(10℃)中放置16h后稳定性。[/align][align=left]冻融:取多份空白血浆适量,分别加入定量的TBKW标准溶液,配制低、中、高三个浓度血浆样品放置-30°C至少12h,分别经1次冻融、2次冻融、3次冻融冷冻解冻循环,每次溶解时流动自来水溶解不超过15min,放置室温15 min后冷冻,按“血浆标准品及质控样品处理方法”项下操作,处理后进样分析,观察各次循环后稳定性。[/align][align=left] 长期冷冻:取多份空白血浆适量,分别加入定量的TBKW标准溶液,配制低、中、高三个浓度血浆样品,于-30°C放置3天、8天和27天,按“血浆标准品及质控样品处理方法”项下操作,处理后进样分析,观察-30°C条件下冷冻保存稳定性。接受标准:各储备条件下每一浓度水平测定值的精密度≤15%,准确度应在±15%之内。[/align][align=left][b]3.9 批分析 [/b]将精密度实验组样本中最低定量限、低、中和高四个浓度的样品进行了8轮进样,在实验样品开始前证实生物分析方法的效能。[/align][align=left][b]4实验结果[/b][/align][align=left][b]4.1 质谱结果 [/b]由于 TBKW 的结构中既含有碱性氮原子, 也含有羧基, 所以本实验比较了正、负两种离子检测。结果发现, TBKW 的甲醇-水 (50∶50) 溶液 (在正离子模式下响应约为负离子的10倍, 故优先选择ESI 源下正离子检测方式。在正离子检测模式下,TBKW 及内标 TBTM 分别主要生成 m/z454.2 和m/z389.2 的 [sup]+[/sup]峰, 选择性对 [sup]+[/sup]峰进行产物离子扫描分析, TBKW 生成的主要碎片离子分别为[i]m/z [/i]285.1 ,[i]m/z[/i]126.1和[i]m/z[/i]210.1,TBTM生成的主要碎片离子有[i]m/z [/i]241.1。但实验过程中发现,[i] m/z[/i]126.1和[i]m/z[/i]210.1 的碎片离子响应弱, 且噪音高, 故最终选择[i]m/z [/i]285.1 和[i]m/z [/i]241.1 分别作为TBKW 及内标 TBTM 定量分析时的产物离子。待测物及内标的[sup]+[/sup]产物离子全扫描质谱图及相应出峰时间见图1-4。[/align][align=center] [img=,562,319]https://ng1.17img.cn/bbsfiles/images/2019/10/201910241116590213_28_3255306_3.png!w562x319.jpg[/img] [/align][align=center]图1 TBKW二级特征碎片质谱图[/align][align=center][img=,555,315]https://ng1.17img.cn/bbsfiles/images/2019/10/201910241117114646_9141_3255306_3.png!w555x315.jpg[/img] [/align][align=center]图2 TBTM二级特征碎片质谱图[/align][align=center][img=,559,296]https://ng1.17img.cn/bbsfiles/images/2019/10/201910241117239993_3223_3255306_3.png!w559x296.jpg[/img] [/align][align=center]图3 TBKW色谱质谱图[/align][align=center][img=,567,326]https://ng1.17img.cn/bbsfiles/images/2019/10/201910241117339148_8729_3255306_3.png!w567x326.jpg[/img] [/align][align=center]图4 TBTM色谱质谱图[/align][align=left][b]4.2 方法学验证结果[/b][/align][align=left][b]4.2.1 选择性 [/b]结果表明, 空白人血浆中的内源性物质不干扰头孢克肟和内标头孢他美的测定, 且同位素内标头孢他美不干扰头孢克肟的测定。[/align][align=left][b]4.2.2 标准曲线[/b] 用加权 ([i]W [/i]= 1/[i]x[/i][sup]2[/sup])最小二乘法进行回归运算, 求得的标准曲线的相关系数 ([i]r[/i][sup]2[/sup]) 均大于0.99。根据标准曲线,头孢克肟的线性范围为0.025~8 ug/ml。典型标准曲线如下所示: [i]y [/i]= 0.828 [i]x [/i]+4.35e[sup]-3[/sup]([i]r[/i][sup]2[/sup]= 0.9994)。[/align][align=left][b]4.2.3 残留考察 [/b]结果显示,样品与内标保留时间处均未出现干扰杂质峰, 在本实验选择的色谱和质谱条件下, 待测物及内标无残留。[/align][align=left][b]4.2.4 定量下限[/b] 其准确度和精密度见“精密度与准确度”项下。[/align][align=left][b]4.2.5 精密度与准确度[/b] 头孢克肟每一浓度水平的QC样品的日内、日间平均准确度均在15%之内,相对标准偏差均<15%,日内、日间精密度与准确度结果符合生物样本测定要求。相关数据见表1。[/align][align=center]Table 1 Precision and accuracy of TBKW (n=18).[/align][align=center] [img=,610,133]https://ng1.17img.cn/bbsfiles/images/2019/10/201910241121176922_9541_3255306_3.png!w610x133.jpg[/img][/align][align=left][b]4.2.6 回收率和基质效应 [/b]待测物TBKW基质效应的平均值为27.7-42.9% 内标TBTM基质效应的平均值为2.1-52.1%,经内标归一化计算后得出TBKW内标归一化基质效应平均为59.1-62.8%,RSD符合要求。待测物TBKW高脂血浆基质效应的平均值为25.3-28.4% 内标TBTM的高脂血浆基质效应平均为41.9-47.6%,经内标归一化计算后得出TBKW内标归-化高血脂基质效应平均值为59.0-60.4%,RSD均符合要求。待测物TBKW溶血血浆基质效应的平均值为22.0-25.5%,内标TBTM的高血脂基质效应平均为38.6-43.9%,经内标归一化计算后得出TBKW内标归一化高血脂基质效应平均值为55.9-62.6%,RSD均符合要求。表明在试验选择的样品处理、色谱与质谱条件下,待测物和内标均表现出较强的基质效应,均表现出较强的离子抑制作用,特别是TBKW,但该机制效应对待测物和内标作用方向致、稳定,经内标校正后,虽然还存在基质效应,但对分析结果不会产生明显影响。TBKW及其内标TBTM的提取回收率结果,分别见表7-3。待测物TBKW在低、中、高三个QC浓度水平上提取回收率的平均值在138.2%-148.2%之间,内标的提取回收率的平均值在124.0%-130.4%之间,内标校正后提取回收率的平均值在110.4-114.1%之间,RSD符合要求。待测物和内标物在不同浓度水平的提取回收率结果是精密和可重现的,相关数据见表2。[/align][align=center]Table 2 Extraction recoveryand matrix effect of TBKW (n = 6).[img=,631,234]https://ng1.17img.cn/bbsfiles/images/2019/10/201910241121399474_1836_3255306_3.png!w631x234.jpg[/img][/align][align=left][b]4.2.7 溶液稳定性[/b] 用甲醇配制的TBKW储备液1mg/mL-20℃冻存7、22天后的含量均值为新鲜配制的TBKW的106.5%和106.0%,未见降解;TBKW工作液储备液75、6500ng/mL 4℃冷藏7、30天后的含量均值分别为新鲜配制的TBKW的94.5%,113.4% 和89.8%,109.2%,不存在明显降解。[/align][align=left][b]4.2.8 血浆样品稳定性 [/b]TBKW血浆样品在室温放置5h、处理好的血浆样本室温放置6h、自动进样器放置16h,冻融3次、长期冷冻(27天,高于待测样本保存时间)试验条件下,各浓度质控样本的准确度均值在85-115%之间,RSD%均小于15%,表明TBKW血浆样品在上述所考察的情况下稳定。血浆样品稳定性测试结果满足人体血浆样本检测需求。[/align][align=left][b]4.2.9 批分析 [/b]对8轮试验数据进行了比较。结果表明在同一进样批中,每浓度含 48个样本,共计192个样本,其中LLOQ中有6个点准确度20%,少于总样品数的20% (12.5%),且LLOQ准确度和精密度平均值均15%,QC-L、 QC-M 和QC-H的准确度和精密度平均值均15%,总进样时间约18小时。即除血浆标准曲线外和质控点,同批次测定 180个样本能够满足生物样本分析要求.[/align][align=left][b]4.3 药时曲线[/b] 12名志愿者单剂量空腹及餐后口服300 mg头孢克肟胶囊后,平均药-时曲线见图5[/align][align=center][img=,507,279]https://ng1.17img.cn/bbsfiles/images/2019/10/201910241122298854_2799_3255306_3.png!w507x279.jpg[/img] [/align][align=center]图5 12名健康受试者在空腹和餐后口服单剂量头孢克肟后平均药-时曲线 [/align][align=left][b]4.4药代动力学参数及统计结果 [/b]见表3。[/align][align=center]Table 3 Mainpharmacokinetic parameters of cefixime capsules taken on an empty stomach andafter meals[/align][align=center] [img=,546,175]https://ng1.17img.cn/bbsfiles/images/2019/10/201910241122478527_4468_3255306_3.png!w546x175.jpg[/img][/align][align=left][b]5 讨论[/b][/align][align=left]比较空腹和高脂餐后口服头孢克肟的血药浓度的达峰时间[color=black]Tmax,[/color]达峰浓度[color=black]Cmax[/color][color=black]及曲线下面积[/color]AUC的数值,发现餐后口服头孢克肟的达峰时间推迟约0.792 h,达峰浓度约为空腹时的42.2%,餐后相对于空腹给药的相对生物利用度为39%,证明食物对头孢克肟的吸收速率、消除半衰期及吸收总量等药动学参数有显著的影响,故推荐头孢克肟片剂饭前空腹服用。[/align][align=left]饮食因素对口服药物的影响常为病人所忽视,为了避免药物对胃肠道的刺激常喜饭后服药,但餐后服药易受食物等因素的影响。本文结果提示:头孢克肟片不宜餐后服药,较合理的给药方案应是在空腹或饭前2h服用。[/align][align=left]食物降低头孢克肟的吸收速率及吸收程度的原因可能有以下几点: ①食物的存在降低了胃排空速率,使药物在胃中停留时间延长,使胃中的药物浓度降低,药物的吸收减慢,从而导致达峰时间延长 ②头孢克肟为弱酸性药物,主要在小肠吸收,食物会使肠液的 pH 减小,降低了头孢克肟的溶解性和溶出度,从而导致头孢克肟的吸收量降低。这些研究结果为头孢克肟片在临床安全合理用药提供重要的参考依据。[/align][align=left][b]参考文献[/b][/align][align=left]张羽长,李明铭,隋欣蕙,赵春杰.头孢克肟胶囊人体药动学研究及生物等效性评价.药学服务与研究,2008,8(06):429-431.[/align][align=left] Meng, Fang, et al."Sensitive liquid chromatography-tandem mass spectrometry method for thedetermination of cefixime in human plasma: Application to a pharmacokineticstudy." Journal of Chromatography B 819.2 (2005): 277-282.[/align][align=left]KREMER JM,WESTHOVENSR ,LEON M ,et al .Treatment of rheumatoid arthritis by selective inhibition ofT-cell activation with fusion protein CTLA4lg. N Engl J Med ,2003,349(20):1907 - 1915.生物样品定量分析方法指导原则(草案),中国药典,2015。[/align]
我按照药典规定的方法测定头孢他啶聚合物含量,可做了好多次也检测不出头孢他啶聚合物峰,这是怎么回事?望各位大虾指教!
【第十一届原创】HPLC法测定注射用头孢他啶聚合物含量1样品简介注射用头孢他啶,主要成份为头孢他啶,加适量碳酸钠做助溶剂。2.仪器设备、试剂与对照品2.1仪器设备:waters e2695高效液相色谱仪赛托利斯 CPA225D分析天平色谱柱:天津开发区色谱分析仪器有限公司葡聚糖G-10 凝胶色谱柱 400mm×14mm2.2试剂:硫酸铵(AR) 广州化学试剂厂磷酸二氢钠(AR) 广州化学试剂厂磷酸氢二钠(AR) 广州化学试剂厂碳酸钠(AR) 广州化学试剂厂2.3 对照品:头孢他啶(来源是齐鲁安替制药有限公司,批号为WST-C-8034EJ82JC,含量85.81%)蓝色葡聚糖2000(来源是Bei Jing Biodee Biotechnology Co.Ltd,批号为9004-54-01,含量100%)3.色谱条件流动相:以含3.5%硫酸铵的pH7.0的0.1mol/L磷酸盐缓冲液为流动相A,以水为流动相B,波长:254nm 流速:0.8ml/min 温度:室温洗脱方式:等度 进样体积:100ul4.样品制备4.1系统适用性溶液制备4.1.1 1.5mg/ml蓝色葡聚糖2000溶液制备:称取37.5mg蓝色葡聚糖2000至25ml容量瓶中,加水溶解并稀释至刻度,摇匀。4.1.2 系统适用性溶液制备:称取头孢他啶约0.2g 与碳酸钠20mg,置10ml量瓶中,用1.5mg/ml的蓝色葡聚糖2000溶液溶解并稀释至刻度,摇匀。4.2 对照溶液制备取头孢他啶对照品约12mg,精密称定,加水溶解并定量制成每1ml中约含0.1mg的溶液。4.3供试品溶液制备取本品,按标示量加水溶解并定量稀释制成每1ml中含20mg的溶液,照头孢他啶项下的方法测定,含头孢他啶聚合物的量不得过标示量的1.0%。4.4测定法4.4.1 量取100μl系统适用性溶液注入液相色谱仪,用流动相A进行测定,记录色谱图。高聚体的峰高与单体和高聚体之间的谷高比应大于1.5。4.4.2 量取1.5mg/ml蓝色葡聚糖2000溶液100μl注入液相色谱仪,分别以流动相A,B进行测定,记录色谱图。按蓝色葡聚糖2000峰计算理论板数均不低于500,拖尾因子均应小于2.0。在两种流动相系统中蓝色葡聚糖2000峰的保留时间比值应在0.93~1.07之间,对照溶液主峰与供试品溶液中聚合物峰与相应色谱系统中蓝色葡聚糖2000峰的保留时间的比值均应在0.93~1.07之间。4.4.3 另以流动相B为流动相,精密量取对照溶液100μl,连续进样5次,峰面积的相对标准偏差应不大于5.0%。5. 结果讨论系统适用性结果报告:流动相A中蓝色葡聚糖2000理论塔板数为1875,拖尾因子为0.93。流动相B中蓝色葡聚糖2000理论塔板数为1356,拖尾因子为0.79。在两种流动相中蓝色葡聚糖2000峰保留时间比值0.98,对照溶液主峰中聚合物峰与相应色谱系统中蓝色葡聚糖峰的保留时间比值为1.00,供试品溶液主峰中聚合物峰与相应色谱系统中蓝色葡聚糖峰的保留时间比值为1.00。系统适用性溶液以流动相A测定,记录图谱,高聚体的峰高与单体和高聚体之间的谷高比值为3.9。结果表明:葡聚糖G-10凝胶色谱柱能满足分析要求。[img]https://ng1.17img.cn/bbsfiles/images/2018/08/201808221931500102_136_3170710_3.jpeg[/img][img]https://ng1.17img.cn/bbsfiles/images/2018/08/201808221931501152_5601_3170710_3.jpeg[/img][img]https://ng1.17img.cn/bbsfiles/images/2018/08/201808221931503923_2007_3170710_3.jpeg[/img][img]https://ng1.17img.cn/bbsfiles/images/2018/08/201808221931506933_7008_3170710_3.jpeg[/img]
头孢类药物结构
如题:有没有同行检测过2010版药典头孢呋辛钠的溶剂残留啊?实验室一直没有做出来,标准品出峰正常,但是样品加标准品混合后,就只有五个峰,分离度肯定没有问题,怀疑是基质效应导致的;不知道有没有同行做出来?方便提供一张图谱,谢谢还有就是药典提供的方法就是标准加入法,好像有点问题,标准品和供试品配置的不对啊
头孢西丁钠有关杂质 头孢西丁钠有关杂质
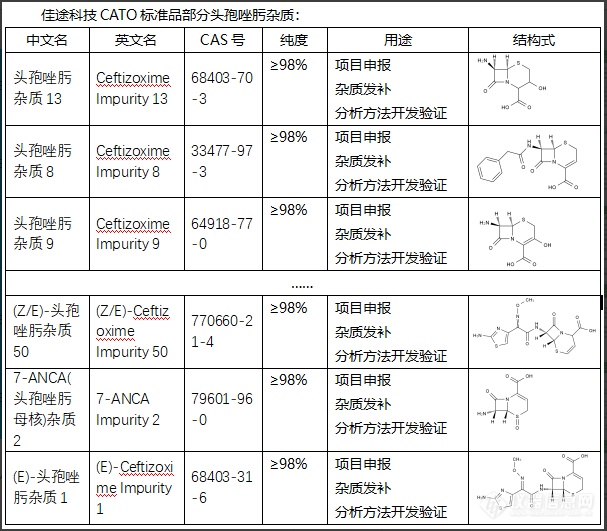
有关头孢唑肟杂质的作用,以下是要注意的一些可能性:1.负面作用:过多的杂质可能导致药物效力下降,并可能引发不良反应或副作用。例如,有些杂质可能导致过敏反应。2.毒性:某些杂质可能具有毒性。例如,某些杂质可能具有致癌性。3.影响药效:杂质可能会影响药物的生物利用度,即药物进入体内后能达到预期药效的能力。CATO标准品药品生产中的质量控制步骤非常重要,目的就是要尽可能减少杂质的存在。任何药品都必须经过严格的质量检测,确保其安全有效。[img=,607,531]https://ng1.17img.cn/bbsfiles/images/2024/02/202402041449269442_4660_6381668_3.png!w607x531.jpg[/img]
在GMP法规中,对一些药物的生产厂房设施做出了特殊的规定,跟小伙伴儿们分享一下,青霉素类和头孢类两者之间有没有本质的区别。抗生素是由微生物(包括细菌、真菌、放线菌属)产生、能抑制或杀灭其他微生物的物质。抗生素分为天然品和人工合成品,前者由微生物产生,后者是对天然抗生素进行结构改造获得的部分合成产品,头孢是属于抗生素类。这两者都属于β-内酰胺类抗生素。头孢菌素类(Cephalosporins)是由冠头孢菌培养液中分离的头孢菌素C,经改造侧链而得到的一系列半合成抗生素。其抗菌谱广,对厌氧菌有高效;引起的过敏反应较青霉素类低;对酸及对各种细菌产生的β-内酰胺酶较稳定;作用机理同青霉素,也是抑制细菌细胞壁的生成而达到杀菌的目的.属繁殖期杀菌药。(头孢菌素是青霉素近源的头孢菌属的真菌发酵液离而来。)青霉素一般是静脉滴注的,药效强,但抗菌谱窄,且半衰期短。1.笫一代头孢菌素第一代头孢菌素是60年代初开始上市的。从抗菌性能来说,对第一代头孢菌素敏感的菌主要有β-溶血性链球菌和其他链球菌、包括肺炎链球菌(但肠球菌耐药),葡萄球菌(包括产酶菌株)、流感嗜血杆菌、大肠杆菌、克雷伯杆菌、奇异变形杆菌、沙门菌、志贺菌等。不同品种的头孢菌素可以有各自的抗菌特点,如头孢噻吩对革兰阳性菌的抗菌作用较优,而头孢唑林则对某些革兰阴性菌有一定作用。但是,第一代头孢菌素对革兰阴性菌的β-内酰胺酶的抵抗力较弱,因此,革兰阴性菌对本代抗生素较易耐药。第一代头孢菌素对吲哚阳性变形杆菌、枸橼酸杆菌、产气杆菌、假单胞菌、沙雷杆菌、拟杆菌、粪链球菌(头孢硫脒除外)等微生物无效。本代抗生素中常用品种有头孢唑林、头孢氨苄、头孢拉定、头孢羟氨苄、头孢克罗等。其中除头孢唑林只能供注射外,其他的均可用于口服,也称口服头孢。头孢噻吩、头孢噻啶、头孢来星、头孢乙腈、头孢匹林等均已少用或不用。 2.笫二代头孢菌素第二代头孢菌素对革兰阳性菌的抗菌效能与第一代相近或较低,而对革兰阴性菌的作用较为优异,表现在:(l)抗酶性能强一些革兰阴性菌(如大肠杆菌、奇异变形杆菌等)易对第一代头孢菌素耐药。第二代头孢菌素对这些耐药菌株常可有效。(2)抗菌谱广第二代头孢菌素的抗菌谱较第一代有所扩大,对奈瑟菌、部分吲哚阳性变形杆菌、部分枸橼酸杆菌、部分肠秆菌属均有抗菌作用。第二代头孢菌素对假单胞属(铜绿假单胞菌)、不动杆菌、沙雷杆菌、粪链球菌等无效。临床应用的第二代头孢菌素主要品种有头孢孟多、头孢西汀(美福仙),头孢呋新(西力欣),头孢克罗等。3.笫三代头孢菌素第三代头孢菌素对革兰阳性菌的抗菌效能普遍低于第一代(个别品种相近),对革兰阴性菌的作用较第二代头孢菌素更为优越。(1)抗菌谱扩大第三代头孢菌素的抗菌谱比第二代又有所扩大,对铜绿假单胞菌、沙雷杆菌、不动杆菌、消化球菌、以及部分脆弱拟杆菌有效(不同品种药物的抗菌效能不尽相同)。对于粪链球菌、难辨梭状芽胞杆菌等无效。(2)耐酶性能强对第一代或第二代头孢菌素耐药的一些革兰阴性菌株,第三代头孢菌素常可有效。常用有:头孢哌酮(先锋必素)、头孢三嗪(罗塞秦、菌必治)、头孢噻肟钠、头孢他啶、头孢唑肟等。 4.笫四代头孢菌素第三代头孢菌素对革兰阳性菌的作用弱,不能用于控制金黄色葡萄球菌感染。近年来发现一些新品种如头孢匹罗(Cefpirome)等,不仅具有第三代头孢菌素的抗菌性能,还对葡萄球菌有抗菌作用,称为第四代头孢菌素。关于第一至第四代的划分不仅适用于头孢菌素,其他的一些β-内酰胺抗生素也可按此分代。常用有拉他头孢、头孢匹罗、氨曲南等。1.青霉素和头孢菌素都属于β-内酰胺类抗生素。2.青霉素是青霉菌培养液中提取精致获得的,是一种窄普抗生素,其基本结构是母核6--氨基青霉烷酸(6-APA),其中β--内酰胺环对抗菌活性起重要作用。3.头孢菌素是一类来自头孢菌的广谱抗生素。4.头孢菌素和青霉素类都具有相同的β-内酰胺环,所不同的是头孢菌素系7--氨基头孢烷酸(7--ACA)的衍生物,青霉素由6--氨基青霉烷酸(6-APA),两者的区别只是青霉素母核中五元噻唑环换成头孢菌素的六元双氢噻嗪环。
[font=宋体]化合物对紫外-可见光的选择性吸收及其在最大吸收波长处的吸收系数,是化合物的物理常数之一,也是药物重要的质量控制指标。[/font][b][font=宋体]紫外吸收光谱[/font][/b][font=宋体]取头孢呋辛赖氨酸约[/font]25 mg[font=宋体],精密称定,置[/font]50 mL[font=宋体]量瓶,加水溶解并稀释至刻度,摇匀,作为储备液。再准确量取储备液[/font]1.0 mL[font=宋体],置于[/font]25 mL[font=宋体]量瓶中,加水稀释至刻度,摇匀,得供试品溶液。照《中国药典》[/font]2020 [font=宋体]年版(四部)[/font][font=宋体]紫外[/font]-[font=宋体]可见分光光度法测定,在[/font]200 nm[font=宋体]~[/font]400 nm[font=宋体]的波长范围内绘制吸收谱图。结果见[/font]Fig.1[font=宋体]。[/font][align=center][/align][align=center][img=,395,337]https://ng1.17img.cn/bbsfiles/images/2021/10/202110092150319513_5582_3528941_3.gif!w395x337.jpg[/img][/align][align=center][b]Fig1 The UV absorption spectrum of cefuroximelysine[/b][/align][b] [font=宋体]百分吸收系数([/font][/b][img=,29,25]https://ng1.17img.cn/bbsfiles/images/2021/10/202110092151368269_6611_3528941_3.gif!w29x25.jpg[/img][b][font=宋体])[/font][/b][font=宋体]使用五台不同型号的紫外[/font]-[font=宋体]分光光度计,参照《中国药典》[/font]2020 [font=宋体]年版(四部)附录[/font]IV[font=宋体]紫外[/font]-[font=宋体]可见分光光度法进行测定。[/font][font=宋体]仪器校正和检定[/font][font=宋体]取在[/font]120[font=宋体]℃[/font][font=宋体]干燥至恒重的基准重铬酸钾约[/font]60 mg[font=宋体],精密称定,用[/font]0.005 molL[sup]-1[/sup][font=宋体]硫酸溶液溶解并稀释至[/font]1000 mL[font=宋体],在规定的波长处测定并计算其百分吸收系数,并与规定的百分吸收系数比较,结果均符合要求。[/font][font=宋体]溶剂的选择[/font][font=宋体]由溶解度试验可知,头孢呋辛赖氨酸在水中的溶解性能较好,因此,预选用水作为溶剂,测定其百分吸收系数。[/font][font=宋体]将水置石英吸收池中,以空气为空白(即空白光路中不置任何物质)测定吸光度。药典规定,溶剂和吸收池的吸光度,在[/font]220 nm[font=宋体]~[/font]240 nm[font=宋体]范围内应不超过[/font]0.40[font=宋体],在[/font]240 nm[font=宋体]~[/font]250 nm[font=宋体]范围内应不超过[/font]0.20[font=宋体],在[/font]251 nm[font=宋体]~[/font]300 nm[font=宋体]范围内应不超过[/font]0.10[font=宋体],在[/font]300 nm[font=宋体]以上时应不超过[/font]0.05[font=宋体]。测定结果均符合要求,确定以水为测定头孢呋辛赖氨酸百分吸收系数的溶剂。[/font][font=宋体]最大吸收波长的确定[/font][font=宋体]如头孢呋辛赖氨酸紫外吸收光谱([/font]Fig.2-1[font=宋体])所示,本品在[/font]273 nm[font=宋体]附近处有最大吸收。因此,确定[/font]273 nm[font=宋体]作为头孢呋辛赖氨酸的最大吸收波长。[/font][font=宋体]百分吸收系数[/font][font=宋体]的测定[/font][font=宋体]溶液的配制[/font] [font=宋体]取头孢呋辛赖氨酸对照品约[/font]25 mg[font=宋体],精密称定,置[/font]50 mL[font=宋体]量瓶中,加水溶解并稀释至刻度,摇匀,得贮备液。精密量取贮备液[/font]1.0 mL[font=宋体],置[/font]25 mL[font=宋体]量瓶中,用水稀释至刻度,摇匀,作为溶液[/font]1([font=宋体]浓度约为[/font]20 μgmL[sup]-1[/sup])[font=宋体]。精密量取贮备液[/font]1.0 mL[font=宋体],置[/font]50 mL[font=宋体]量瓶中,用水稀释至刻度,摇匀,作为溶液[/font]2([font=宋体]浓度约为[/font]10 μgmL[sup]-1[/sup])[font=宋体]。[/font][font=宋体]溶液稳定性[/font] [font=宋体]取溶液[/font]1[font=宋体],避光放置,分别于[/font]0[font=宋体],[/font]0.5[font=宋体],[/font]1.0[font=宋体],[/font]2.0[font=宋体],[/font]3.0[font=宋体],[/font]4.0 h [font=宋体]时测定,结果与[/font]0 h[font=宋体]比较,吸光度的[/font]RE[font=宋体]值均在±[/font]1%[font=宋体]以内,表明溶液在[/font]4 h[font=宋体]内稳定。[/font][font=宋体]测定结果[/font] [font=宋体]按《中国药典》[/font][font='Times New Roman']2020 [/font][font=宋体]年版(四部)[/font][font=宋体]方法校正与检定仪器并在[/font]273 nm[font=宋体]波长处测定。各溶液测得百分吸收系数[/font][font=宋体]结果见[/font]Tab.2[font=宋体],头孢呋辛赖氨酸对照品溶液在[/font]273 nm [font=宋体]波长处的百分吸收系数[/font][font=宋体]为[/font]298.3[font=宋体],按±[/font]1.5%[font=宋体]计算,样品百分吸收系数应在[/font]293.8[font=宋体]~[/font]302.8[font=宋体]之间。测得[/font]3[font=宋体]批头孢呋辛赖氨酸原料药在[/font]273 nm[font=宋体]波长处的百分吸收系[/font][font=宋体]分别为[/font]301.0[font=宋体],[/font]295.8[font=宋体],[/font]296.5[font=宋体]。[/font][b] [/b][align=center][b] [/b][/align][align=center][b]Tab.The specific absorbance([/b][img=,29,25]https://ng1.17img.cn/bbsfiles/images/2021/10/202110092153204355_8883_3528941_3.gif!w29x25.jpg[/img][b])of reference substance of cefuroxime lysine ([i]n[/i]=5)[/b][/align] [table=100%][tr][td] [align=center]Concentration[/align] [align=center](μgmL[sup]-1[/sup])[/align] [/td][td] [align=center]4802H[/align] [/td][td] [align=center]UV-1801[/align] [/td][td] [align=center]TU-1800[/align] [/td][td] [align=center]UV-2000[/align] [/td][td] [align=center]Spectrum 725[/align] [/td][td] [align=center]Average of [img=,29,25]https://ng1.17img.cn/bbsfiles/images/2021/10/202110092154296408_4276_3528941_3.gif!w29x25.jpg[/img][/align] [/td][td] [align=center]RSD/%[/align] [/td][td] [align=center]Average[/align] [align=center]of [b][img=,29,25]https://ng1.17img.cn/bbsfiles/images/2021/10/202110092155129453_2127_3528941_3.gif!w29x25.jpg[/img][/b][/align] [/td][/tr][tr][td] [align=center]20[/align] [/td][td] [align=center]294.2[/align] [/td][td] [align=center]302.1[/align] [/td][td] [align=center]297.1[/align] [/td][td] [align=center]295.8[/align] [/td][td] [align=center]301.4[/align] [/td][td] [align=center]298.1[/align] [/td][td] [align=center]1.2[/align] [/td][td=1,2] [align=center]298.3[/align] [/td][/tr][tr][td] [align=center]10[/align] [/td][td] [align=center]292.2[/align] [/td][td] [align=center]298.8[/align] [/td][td] [align=center]300.6[/align] [/td][td] [align=center]298.0[/align] [/td][td] [align=center]302.5[/align] [/td][td] [align=center]298.4[/align] [/td][td] [align=center]1.3[/align] [/td][/tr][/table][font=宋体]结论:头孢呋辛赖氨酸在[/font]273 nm[font=宋体]附近处有最大吸收,其百分吸收系数([/font][img=,29,25]https://ng1.17img.cn/bbsfiles/images/2021/10/202110092155306771_680_3528941_3.gif!w29x25.jpg[/img][font=宋体])在[/font]293.8[font=宋体]~[/font]302.8[font=宋体]之间。[/font]
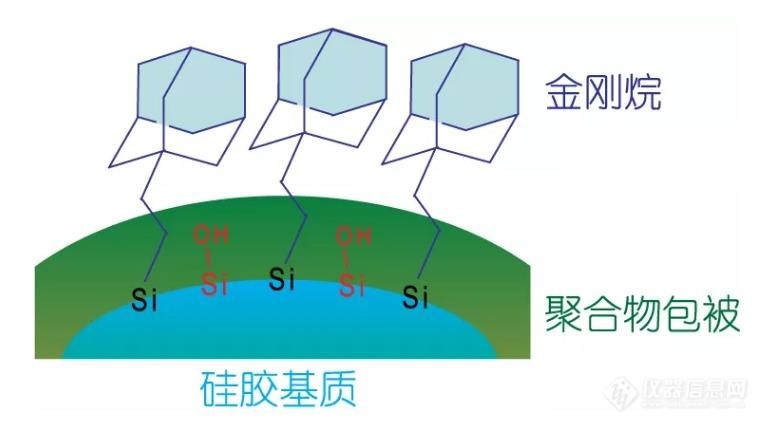
利用ADME柱快速分析头孢类药物[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS方法摸索前言:由于ADME色谱柱具有其他类型色谱柱所不具备的特殊表面极性和疏水性,因此最适用于常规C18色谱柱(ODS)无法实现的强极性化合物与疏水性化合物同时保留的情况。当使用C18色谱柱分析保留弱、无法取得分离的时候,使用ADME色谱柱,在原色谱条件下也能改善分离效果。因此,ADME是分析时的第二选择色谱柱。头孢克肟(Cefixime)是一种重要的头孢菌素类抗生素,属于可口服的第三代头孢菌素类抗生素,临床上应用于敏感菌引起的肺炎、支气管炎、泌尿道感染、淋病、胆囊炎、胆管炎、猩红热、中耳炎、副鼻窦炎等。由于头孢克肟极性极强,我们选择资生堂生产的一款键合金刚烷基团的高表面极性色谱柱CAPCELL PAK ADME进行分析。图1为金刚烷基ADME填料表面示意图。C[sub]18[/sub]色谱柱在反相色谱中应用最广泛,适用于分析很多化合物,但是在反相模式下很难对强极性化合物进行分析。而且随着药物代谢产物分析技术的发展,在以药代动力学为代表的多个相关领域中,对于含有多种成分的强极性代谢产物与强疏水性代谢前体进行共同分析的需求也越来越多。对此,资生堂开发了导入与迄今为止的常规C[sub]18[/sub]基团结构完全不同的金刚烷基填料。这种填料的官能团结构虽然与常规C[sub]18[/sub]色谱柱的烷基不同,但仍然是烷基,因此完全可以作为反相色谱柱来使用。(引自大曹色谱微信公众号)[img=,690,384]https://ng1.17img.cn/bbsfiles/images/2019/07/201907010000401455_8549_3255306_3.jpg!w690x384.jpg[/img][align=center]图1 金刚烷基ADME填料表面示意图(引自大曹色谱微信公众号)[/align]在常规液相色谱分析中,反相C[sub]18[/sub](ODS)色谱柱可满足绝大多数化合物的分析。但是大家应该也遇到过强极性物质保留弱/不保留的情况。这种情况下,一般的思路是:★调整流动相★尝试其他种类反相柱(C[sub]8[/sub]、C[sub]4[/sub]、CN、C[sub]1[/sub]等)★在100%水相流动相条件下,使用高极性色谱柱进行分析★改变分离模式——从反相模式到HILIC模式上面的方法对于极性化合物的分析也许有效,但如果是强极性化合物和疏水性化合物共同分析,怎么办?可以考虑选择ADME色谱柱。因为金刚烷基填料具有以下特长:1.CAPCELL PAK ADME色谱柱键合立体笼状结构官能团——金刚烷基团,因此具有与常规C18色谱柱完全不同的表面特性,在极性较强化合物的分析中有独特的优势,兼具疏水选择性和笼状结构的立体选择性,能够对一些具有微小差异的化合物进行有效分离,在药物代谢分析中也表现出明显的优势。2. 键合立体笼状结构官能团——金刚烷基团,同时采用聚合物包被技术进行表面处理。3. 兼具高表面极性和一定疏水性,适用于高极性物质和疏水性物质的共同分析。(引自大曹色谱微信公众号)选择好色谱柱后,我们挑选了性质想近的几个内标化合物,分别为头孢他美、阿莫西林、氟氯西林钠等,其pka见图2-5。使用CAPCELL PAK ADME色谱柱在0.1%甲酸水/乙腈体系下对混合对照品和血浆样品进行分析,如图6和图7所示。头孢克肟峰形良好,保留时间为1.66 min。在混合对照品中,阿莫西林在该检测离子下显示为两个峰,头孢他美保留时间1.71,峰形正常,可考虑选做内标物。血浆样品能够正常检测目标物质峰。[align=center][img=,690,315]https://ng1.17img.cn/bbsfiles/images/2019/07/201907010000576845_7274_3255306_3.jpg!w690x315.jpg[/img][/align][align=center]图2 头孢克肟pka及其在不同PH值下存在的形态(由化学结构信息网Chemicalize查询得到)[/align][align=center][img=,690,315]https://ng1.17img.cn/bbsfiles/images/2019/07/201907010001104105_2821_3255306_3.jpg!w690x315.jpg[/img][/align][align=center]图3 头孢他美pka及其在不同PH值下存在的形态(由化学结构信息网Chemicalize查询得到)[/align][align=center][img=,690,311]https://ng1.17img.cn/bbsfiles/images/2019/07/201907010001351254_8475_3255306_3.jpg!w690x311.jpg[/img][/align][align=center]图4 阿莫西林pka及其在不同PH值下存在的形态(由化学结构信息网Chemicalize查询得到)[/align][align=center][img=,690,258]https://ng1.17img.cn/bbsfiles/images/2019/07/201907010001499164_2317_3255306_3.jpg!w690x258.jpg[/img][/align][align=center]图5 氟氯西林钠pka及其在不同PH值下存在的形态(由化学结构信息网Chemicalize查询得到)[/align][align=center][img=,690,426]https://ng1.17img.cn/bbsfiles/images/2019/07/201907010002022105_4314_3255306_3.jpg!w690x426.jpg[/img][/align][align=center]图6 混合对照品[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]分析图(由化学结构信息网Chemicalize查询得到)[/align][align=center][img=,690,428]https://ng1.17img.cn/bbsfiles/images/2019/07/201907010002155095_4831_3255306_3.jpg!w690x428.jpg[/img][/align][align=center]图7 血浆样品[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]分析图(由化学结构信息网Chemicalize查询得到)[/align][align=center] [/align]质谱结果:由于 TBKW 的结构中既含有碱性氮原子, 也含有羧基, 所以本实验比较了正、负两种离子检测。结果发现, TBKW 的甲醇-水 (50∶50) 溶液 (在正离子模式下响应约为负离子的10倍, 故优先选择ESI 源下正离子检测方式。在正离子检测模式下,TBKW 及内标 TBTM 分别主要生成 m/z 454.2 和m/z 389.2 的 +峰, 选择性对 +峰进行产物离子扫描分析, TBKW 生成的主要碎片离子分别为m/z 285.1 ,m/z126.1和m/z210.1, TBTM 生成的主要碎片离子有m/z 241.1。但实验过程中发现, m/z126.1和m/z210.1 的碎片离子响应弱, 且噪音高, 故最终选择m/z 285.1 和m/z 241.1 分别作为TBKW 及内标 TBTM 定量分析时的产物离子。待测物及内标的+产物离子全扫描质谱图及相应出峰时间见图8-11。[img=,690,454]https://ng1.17img.cn/bbsfiles/images/2019/07/201907010002323798_8974_3255306_3.jpg!w690x454.jpg[/img][align=center]图8 头孢克肟Q1 质谱图[/align][align=center][img=,690,473]https://ng1.17img.cn/bbsfiles/images/2019/07/201907010002565715_3868_3255306_3.jpg!w690x473.jpg[/img]图9 头孢他美Q1质谱图[/align][align=center][img=,690,445]https://ng1.17img.cn/bbsfiles/images/2019/07/201907010003130350_5750_3255306_3.jpg!w690x445.jpg[/img]图10 头孢克肟质谱色谱峰[img=,690,469]https://ng1.17img.cn/bbsfiles/images/2019/07/201907010003275629_4582_3255306_3.jpg!w690x469.jpg[/img][/align][align=center]图11 头孢他美质谱色谱峰[/align]我们对导入金刚烷基团的CAPCELL PAK ADME色谱柱对于极性化合物的保留行为进行了考察,可以看出CAPCELL PAK ADME色谱柱对强极性化合物的保留作用良好。CAPCELL PAK ADME色谱柱可以对常规C18色谱柱所无法保留的强极性化合物进行良好保留,并且因其能在反相模式下使用,故可作为改善C18色谱柱分离效果的“第二选择”色谱柱。今天的分享就到这里了,有什么疑问都可以在文章下方留言讨论交流哦。最后感谢第12届科学仪器网络原创作品大赛的负责人,感谢你们为我们提供了这么好的交流平台,感谢第12届科学仪器网络原创作品大赛评委会,感谢你们为我们的作品一一指正。
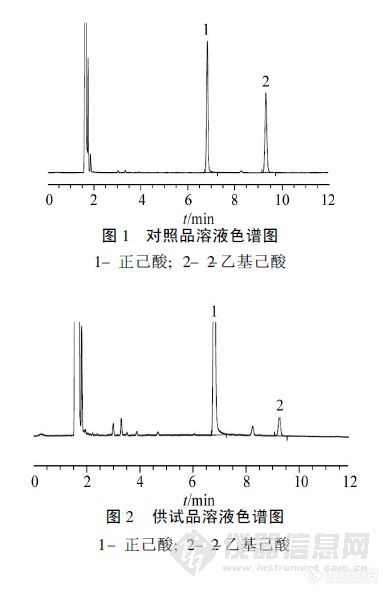
【作者】 崔锋; 窦爱兰;【机构】 山西省药品检验所; 山西省药品检验所 太原030001; 太原030001;【摘要】 建立气相色谱法测定头孢孟多酯钠中2-乙基己酸的含量。色谱柱为DM-FFAP石英毛细管柱(30 m×0.32 mm×0.5μm);选用正己酸作内标物。采用FID检测,检测器温度为250℃;进样口温度为200℃;柱温170℃。2-乙基己酸的线性范围为0.15~0.73 mg/mL(r=0.9990);平均回收率为98.99%;RSD小于2%(n=6)。本法可用于头孢孟多酯钠的质量控制。 http://ng1.17img.cn/bbsfiles/images/2012/07/201207181215_378453_1761902_3.jpg
药典规定头孢曲松钠的流动相是0.05%正辛胺溶液,但我们在做样的过程中发现柱损伤太快。一根新柱子可能做一个月就拖尾严重,柱压升高很快。但用拖尾的柱子做其他品种又没问题。这是什么原因?请问做过这个品种的老师们,用哪个厂家的柱子比较好。一根柱子就竟能用多长时间。现在最让我头痛的就是这个问题。柱子又比较贵,经常买会挨批的。最近还遇到了一个新问题,在做样的过程中,峰面积会不断增加。仪器是岛津2010。做其他品种对照品的RSD都很好,就是做这个品种的时候峰面积不断增加,RSD甚至超过了2%。这是什么原因造成的?请各位老师指点迷津!先此谢过!
测头孢类药物用那种柱子效果较好?
头孢类聚合物怎么检测
牛用兽药抗生素头孢类药物用哪些
跪求头孢地尼活性酯的监测方法[em0702]
1.概述REAGEN™头孢噻呋酶联免疫反应测试盒是利用竞争性的酶联反应原理,用于牛奶、尿液、组织(肝、肾、肉)、蛋、血清和血浆中头孢噻呋残留的定量检测。该试剂盒具有以下特点:Ø 快速,高回收率(75-105%),多种样品的低成本提取方法。Ø 高灵敏度(2ng/g或ppb)。Ø 高重复性。Ø 检测过程只需要不到2小时。 2.试剂盒原理REAGEN™头孢噻呋酶联免疫反应测试盒基于竞争性酶联反应原理,头孢噻呋已经包被于微孔板上。药物分析时,样品同头孢噻呋捕获蛋白共同被添加到板孔中。如果样品中含有药物,会竞争捕获蛋白,抑制捕获蛋白与板上包被的药物结合。加入酶标记的二抗,形成包被药物-捕获蛋白-酶标二抗复合物。加入底物后,产物的颜色强弱与样品中药物的浓度成反比。