硫氰酸盐是硫氰酸根离子SCN‐所成的盐,常见的包括无色的硫氰酸钾、硫氰酸钠、硫氰酸铵和硫氰酸汞。 硫氰酸钠(化学式:NaSCN) 是白色斜方晶系结晶或粉末,毒害品。易溶于水、乙醇和丙酮。主要用作丙烯睛纤维抽丝溶剂、化学分析试剂、彩色电影胶片冲洗剂、某些植物脱叶剂以及机场道路除莠剂,还用于制药、印染、橡胶处理,黑色镀镍及制造人造芥子油等。 硫氰酸钠的毒性主要由其在体内释放的氰根离子而引起。氰根离子在体内能很快与细胞色素氧化酶中的三价铁离子结合, 抑制该酶的活性,使组织不能利用氧。氰根离子所致的急性中毒分为轻、中、重三级。轻度中毒表现为眼及上呼吸道刺激症状,有苦杏仁味,口唇及咽部麻木,继而可出现恶心、呕吐、震颤等;中度中毒表现为叹息样呼吸,皮肤、黏膜常呈鲜红色,其他症状加重; 重度中毒表现为意识丧失,出现强直性和阵发性抽搐,直至角弓反张,血压下降,尿、便失禁,常伴发脑水肿和呼吸衰竭。 原料乳或奶粉中掺入硫氰酸钠后可有效的抑菌、保鲜,但硫氰酸钠是毒害品,少量的食入就会对人体造成极大伤害。2008年12月,卫生部发布的《食品中可能违法添加的非食用物质和易滥用的食品添加剂品种名单(第一批)》中明确规定乳及乳制品中硫氰酸钠属于违法添加物质。
碘化物、硫氰酸盐、硫代硫酸盐的...
我实验室测钼一直用原子吸收光谱法,最近因钼灯损坏而准备用硫氰酸盐法测定,但加硫氰酸盐后,再加氯化亚锡却不退色?是何原因?请各位给分析分析。步骤如下:分别称取含钼样品0.1克和纯铁粉0.1克于250ml锥形瓶中;分别各加入6ml浓盐酸和3ml浓硝酸,小火加热溶解;溶解后分别加入3ml高氯酸,小火加热至冒白烟,维持约一分钟后取下冷却;加入5ml(1+3)硫酸,加水至约60ml,加热,沸腾后小火加热约5分钟后取下;分别各加入10ml10%硫氰酸按溶液;再分别加入10ml10%氯化亚锡溶液,但均不退色,再各加30ml氯化亚锡,还是没有脱色。是何原因?我怀疑有两点:1、 是否氯化亚锡已失去还原性?2、 我用的是硫氰酸铵,而书上说的是硫氰酸钠,会有区别吗?3、 我的操作上有问题?请各位大侠解疑。谢谢。
碘化物、硫氰酸盐、硫代硫酸盐的测定
过去一年中,测定很多奶粉中均含有硫氰酸盐(3-50PPM)。用的是食品卫生部颁布的方法,但是没有用梯度,因为等度测得的峰型和线性都很好。但是从多奶粉中都含有好像不大可能。会不会有什么物质与硫氰酸盐共淋洗?大家有没有遇到过类似情况?
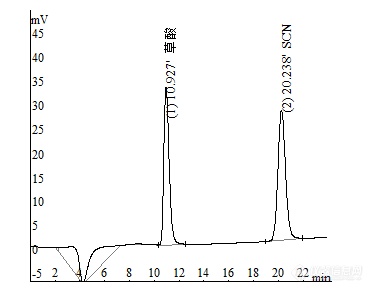
[font=宋体][size=13px]中[/size][/font][font=宋体][size=13px][color=#444444][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法同时测定尿液中草酸和硫氰酸盐[/color][/size][/font][align=center]黄选忠[/align][align=center](湖北兴山县疾病预防控制中心,湖北兴山,443711)[/align]摘要:【目的】建立以SH-AC-3型阴离子交换柱为分离柱,[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url][font=times new roman][size=18px]-[/size][/font]抑制电导检测法同时测定尿样中草酸和硫氰酸盐的新方法。【方法】研究用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法同时测定尿液中草酸和硫氰酸盐的可能性,通过试验优化确定了各项色谱条件。【结果】以SH-AC-3型阴离子交换柱为分离柱,以10.0mmol/LNa2CO3为淋洗液,流量为1.0mL/min,等度洗脱可将草酸和硫氰酸盐与尿液中大量共存的氯化物、磷酸盐和硫酸盐等常见阴离子完全分离,通过抑制电导检测,草酸和硫氰酸盐的峰面积、峰高均与其浓度在0.20~30.0mg/L范围内呈良好的线性关系,相关系数[size=13px][i]r[/i][/size]在0.9991~0.9999,方法应用于尿液中草酸和硫氰酸盐的同时测定,加标回收率在93.2%~105.2%[size=13px]和95.3%~99.8%,[/size], 5次平行测定的相对标准偏差(RSD)小于5%(n=5)。【结论】本方法可用于尿液中草酸和硫氰酸盐的同时测定。关键词:[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法;[font=times new roman][color=#444444]尿液[/color][/font];硫氰酸盐;草酸;中图分类号:O652.63 文献标识码: 文章编号:尿中硫氰酸盐(SCN-)含量是人体接触氰化物的一项生物接触指标[1],而SCN-又是致甲状腺肿物质,可阻滞甲状腺激素合成,尤其对胎儿和婴儿的智力和神经系统发育存在较大的风险[2],因此监测人血、尿等生物标本中的SCN-含量具有重要意义。目前,测定尿中微量SCN-的方法主要有分光光度法[3-5]、衍生-顶空[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法[6-7]等,其中分光光度法和[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法都存在氰化物的干扰问题。尿结石约70%为草酸钙结石,草酸代谢异常所引起的高含量草酸尿是泌尿系结石形成的主要原因[8]。因此准确测定尿中草酸含量对研究结石形成机理、结石的鉴别等均具有重要意义。目前测定尿中草酸的方法主要有光度法包括络合物褪色比色法[9]和催化光度法[10-11]、催化荧光法[12-13]、高效液相色谱法[14-15]和毛细管电泳法[16]等,而比色法、光度法、荧光法等光谱分析方法因特异性差样品要进行前处理,操作繁杂,高效液相色谱法和毛细管电泳法均需要专用仪器使其应用受限。[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法以其操作简便、试剂消耗少、可自动化和多组分同时测定的优势现已成为阴离子分析的首选方法[17],并成功应用于尿液中草酸[17-18]和SCN- [19-20]的分别测定,用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法同时测定尿液中草酸和SCN-似未见报道。本工作拟定的以SH-AC-3型阴离子交换柱为分离柱,10.0mmol/LNa2CO3溶液为淋洗液, 1.0mL/min的流量等度洗脱,[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]-抑制电导检测法同时测定尿液中草酸和硫氰酸盐的新方法,草酸和SCN-的含量均在0.20~30.0mg/L范围内与其峰高和峰面积呈良好的线性关系(相关系数r在0.9991~0.9999),方法应用于尿液中草酸和SCN-的同时测定,加标回收率分别为:95.0%~101.1%和95.5~100.5%,5次平行测定的相对标准偏差(RSD)小于3%,以3倍信噪比(3N/b)计算草酸和SCN-最低检出限分别为0.04mg/L和0.03mg/L。1、试验部分1.1主要仪器CIC-100型[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url](青岛盛瀚色谱公司,编号15601),抑制器:自再生抑制器,检测器:电导检测器,定量环体积为25μL;SHA—15自动进样器(青岛盛瀚色谱公司,编号AS1518050);SH-AC-3型阴离子交换柱(250×4.0mm i.d,青岛盛瀚色谱公司,批号:1602037);SH-AC-3型保护柱(50×4.0mm i.d,青岛盛瀚色谱公司,批号:1602037)。1.2 仪器工作条件及参数设置色谱仪:柱箱温度35℃,电流:75mA,量程:1档。自动进样器:全定量环取样,取样后清洗(每针之间),置换量70μL,取样量25μL,扎针深度4mm。1.3主要试剂草酸标准溶液:1000 mg/L,称取优级纯草酸(H2C2O42H2O)0.1401g用超纯水溶解定容至100mL;SCN-标准溶液:1000 mg/L,称取烘干的优级纯硫氰酸钾0.1673g用超纯水溶解定容至100mL。Cl-标准溶液:GBW(E)080268,1000 mg/L;SO4-2标准溶液:GBW(E)080266,1000 mg/L;H2PO4-标准溶液:1000 mg/L,称取分析纯磷酸二氢钾0.1402g用超纯水溶解定容至100mL。用前将各种标准溶液用纯水分别稀释成含草酸和SCN-10.0mg/L(A液)、100.0mg/L(B液)混合标准应用液备用。无水碳酸钠(分析纯,国药集团化学试剂有限公司),草酸(优级纯,国药集团化学试剂有限公司),硫氰酸钾(优级纯,国药集团化学试剂有限公司)。试验所用其他试剂均为AR级,试验用水为超纯水(18.2ΜΩcm)。1.4 试验方法1.4.1 标准曲线的绘制 取混合标准应用液(A液)0.20、0.50和1.00mL及B液0.50、1.0、1.50、2.00和3.00 mL于10mL容量瓶中加纯水至刻度,混匀,配制成含草酸和SCN-均为0.20~30.0 mg/L的标准系列,各管取1.5mL于样品瓶中,启动自动进样器进样分别测定各组分的峰面积(S)和峰高(H),以S及H对各组分浓度(C)绘制工作曲线。1.4.2尿样的采集 用清洗干净并干燥的聚乙烯瓶采集尿样50mL储存于4℃冰箱待测定。1.4.3 尿样测定 取新鲜尿样经8000转/min离心10min,取上清液用高纯水稀释10倍后分别用C18柱净化、用0.22μm滤膜过滤后取1.5mL于样品瓶中,启动自动进样器进样测定各组分的S和H,以标准曲线法定量,同时进行加标回收试验。2、结果与讨论2.1 色谱条件的选择2.1.1 淋洗液的选择 试验结果表明,当以SH-AC-3型阴离子交换柱为分离柱,以Na2CO3+NaHCO3溶液为淋洗液,其浓度配比在6 mmol/L+1 mmol/L~6 mmol/L+3 mmol/L时,均可将草酸和硫氰酸盐与尿液中的氯化物、磷酸盐和硫酸盐等常见阴离子完全分离,各组分的分离度R(相对于后续组分,如磷酸盐的R是相对于硫酸盐的,下同)可达1.5及以上,但硫氰酸盐的保留时间(T)长达24min以上,分析效率低下。为缩短硫氰酸盐的T提高分析工作效率,以洗脱能力较强的Na2CO3溶液进行了淋洗试验,结果显示当Na2CO3溶液浓度分别为8.0、10.0和12.0 mmol/L时,硫氰酸盐的T分别缩短至21、20和19分多钟,且草酸和硫氰酸盐与尿液中的磷酸盐和硫酸盐等阴离子完全分离,试验结果见表1。考虑到Na2CO3溶液浓度大,相应的抑制电流也高,不利于抑制器的使用[17],在保证适宜的R和较短的T的情况下,试验选择10.0mmol/LNa2CO3溶液为淋洗液。[align=center]表1 Na2CO3溶液浓度选择试验结果(流量1.0 ml/min)[/align][table][tr][td=1,2][align=center]组分[/align][/td][td=2,1][align=center]8.0mmol/L[/align][/td][td=2,1][align=center]10.mmol/L[/align][/td][td=2,1][align=center]12.0mmol/L[/align][/td][/tr][tr][td][align=center]T/min[/align][/td][td][align=center]R[/align][/td][td][align=center]T/min[/align][/td][td][align=center]R[/align][/td][td][align=center]T/min[/align][/td][td][align=center]R[/align][/td][/tr][tr][td][align=center]SO4-2[/align][/td][td][align=center]10.245[/align][/td][td][align=center]3.07[/align][/td][td][align=center]8.606[/align][/td][td][align=center]2.60 [/align][/td][td][align=center]7.868 [/align][/td][td][align=center]2.34[/align][/td][/tr][tr][td][align=center]草酸[/align][/td][td][align=center]13.121[/align][/td][td][align=center]8.15[/align][/td][td][align=center]10.891[/align][/td][td][align=center]9.45[/align][/td][td][align=center]9.828[/align][/td][td][align=center]10.18 [/align][/td][/tr][tr][td][align=center]SCN- [/align][/td][td][align=center]21.665[/align][/td][td][align=center]/[/align][/td][td][align=center]20.151[/align][/td][td][align=center]/[/align][/td][td][align=center]19.177 [/align][/td][td][align=center]/[/align][/td][/tr][/table]2.1.2 色谱柱的选择 以10.0mmol/LNa2CO3溶液为淋洗液、流量1.0mL/min等度洗脱,考察了青岛盛翰色谱公司生产的SH-AC-1型和SH-AC-3型阴离子交换柱对草酸和硫氰酸盐与氯化物、磷酸盐和硫酸盐等常见阴离子的分离情况,结果表明,在此条件下SH-AC-1型柱虽能将草酸与常见阴离子完全分离,但硫氰酸盐至少在90min内未出峰,而SH-AC-3型柱不但可将草酸和硫氰酸盐与氯化物、磷酸盐和硫酸盐等常见阴离子完全分离,且硫氰酸盐的T在21min以内,故本试验选择SH-AC-3型阴离子交换柱为分离柱。2.1.3淋洗液流量的选择 对于相同浓度的淋洗液,不同的流量组分的T和R的将发生改变。试验结果表明,当淋洗液流量从0.8mL/min增加至1.2mL/min时,硫酸盐、草酸和硫氰酸盐的T逐渐变短,R逐渐变小,但硫酸盐和草酸的R远大于1.5达到完全分离的标准,见表2。在保证待测组分与干扰离子完全分离的前提下尽量使用较低的流量,以使系统有较低的压力,淋洗液流量选定为1.0mL/min。[align=center]表2 不同淋洗液流量试验结果(10.0mmol/LNa2CO3)[/align][table][tr][td=1,2][align=center]组分[/align][/td][td=2,1][align=center]0.8ml/min[/align][/td][td=2,1][align=center]1.0ml/min[/align][/td][td=2,1][align=center]1.2ml/min[/align][/td][/tr][tr][td][align=center]T/min[/align][/td][td][align=center]R[/align][/td][td][align=center]T/min[/align][/td][td][align=center]R[/align][/td][td][align=center]T/min[/align][/td][td][align=center]R[/align][/td][/tr][tr][td][align=center]SO4-2[/align][/td][td][align=center]10.471[/align][/td][td][align=center]2.65[/align][/td][td][align=center]8.726[/align][/td][td][align=center]2.54 [/align][/td][td][align=center]7.331 [/align][/td][td][align=center]2.46 [/align][/td][/tr][tr][td][align=center]草酸[/align][/td][td][align=center]13.856[/align][/td][td][align=center]9.34[/align][/td][td][align=center]11.097[/align][/td][td][align=center]9.24 [/align][/td][td][align=center]9.540 [/align][/td][td][align=center]8.95 [/align][/td][/tr][tr][td][align=center]SCN- [/align][/td][td][align=center]24.793[/align][/td][td][align=center]/[/align][/td][td][align=center]20.383[/align][/td][td][align=center]/[/align][/td][td][align=center]17.350 [/align][/td][td][align=center]/[/align][/td][/tr][/table]2.1.4 柱箱温度的确定 考察了柱温在30℃、35℃和40℃时各组分的分离效果,结果显示,在30℃~40℃范围内,草酸和硫氰酸盐均能与氯化物、磷酸盐和硫酸盐等常见阴离子完全的分离,且随着柱温的升高组分的T稍微缩短,R逐渐下降,草酸的S和H均随着柱温的升高而增长,从30℃上升35℃,增长10%左右,35℃上升40℃,增长6%左右;硫氰酸盐的S随着柱温的升高基本保持不变,而其H随着柱温的升高而增长,从30℃上升35℃,增长7%左右,35℃上升40℃,增长9%左右;在保证适宜的T和较高的R的情况下,尽量采用较低的柱温,本试验确定柱箱温度为35℃,这也是产品说明书推荐的柱箱温度。2.2标准曲线按照1.4.1配制标准系列,测定各管的峰面积(S)和峰高(H),以S、H对浓度(C)绘制标准曲线,其标准曲线的线性范围、回归方程、相关系数r(回归曲线的截距、斜率和r由仪器软件给出)列于表3。从表3可见,以峰面积计算的草酸标准曲线的线性优于峰高,硫氰酸盐则反之,同时分段计算的标准曲线的线性较好,故在计算结果时草酸和硫氰酸盐可分别用峰面积和峰高计,并根据样品浓度范围采用分段计算的回归方程来计算,以减少测量误差,尤其对低含量的样品。其中,含10.0mg/L的草酸和硫氰酸盐标准溶液色谱图见图1。[align=center]表3 标准曲线试验结果[/align][table][tr][td=1,2][align=center]组分[/align][/td][td=3,1][align=center]以峰面积计[/align][/td][td=2,1][align=center]以峰高计[/align][/td][/tr][tr][td][align=center]线性范围/mg/L[/align][/td][td][align=center]回归方程[/align][/td][td][align=center]相关系数/r[/align][/td][td][align=center]回归方程[/align][/td][td][align=center]相关系数/r[/align][/td][/tr][tr][td=1,3][align=center]草酸[/align][/td][td][align=center]0.20~10.0[/align][/td][td][align=center]S=96700C-17000[/align][/td][td][align=center]0.99957[/align][/td][td][align=center]H=3320C-770[/align][/td][td][align=center]0.99930 [/align][/td][/tr][tr][td][align=center]10.0~30.0[/align][/td][td][align=center]S=112800C-177600[/align][/td][td][align=center]0.99996[/align][/td][td][align=center]H=3862C-6116[/align][/td][td][align=center]0.99993[/align][/td][/tr][tr][td][align=center]0.20~30.0[/align][/td][td][align=center]S=107100C-53210[/align][/td][td][align=center]0.99929[/align][/td][td][align=center]H=3671C-1995[/align][/td][td][align=center]0.99928[/align][/td][/tr][tr][td=1,3][align=center]SCN- [/align][/td][td][align=center]0.20~10.0[/align][/td][td][align=center]S=114600C+621.7[/align][/td][td][align=center]0.99913[/align][/td][td][align=center]H=2718C-108.6[/align][/td][td][align=center]0.99999[/align][/td][/tr][tr][td][align=center]10.0~30.0[/align][/td][td][align=center]S=124700C-141500[/align][/td][td][align=center]0.99971[/align][/td][td][align=center]H=2934C-2787[/align][/td][td][align=center]0.99984[/align][/td][/tr][tr][td][align=center]0.20~30.0[/align][/td][td][align=center]S=119200C-22340[/align][/td][td][align=center]0.99949[/align][/td][td][align=center]H=2835C-609.3[/align][/td][td][align=center]0.99972[/align][/td][/tr][/table]2.3 方法的精密度和检出限对2种浓度的标准溶液各平行测定5次,计算各成分峰面积的RSD,同时测定仪器30min的基线噪声,以3倍基线噪声除以标准曲线(峰面积计)的斜率(3N/b)计算草酸和硫氰酸[align=center][img=,374,293]https://ng1.17img.cn/bbsfiles/images/2020/09/202009021441333779_9714_3389662_3.png!w374x293.jpg[/img][/align][align=center]图1 标准溶液色谱法图[/align]盐的检出限,5次平行测定的RSD在0.86%~2.26%,方法的重复性良好,方法的检出限分别为0.04 mg/L和0.03 mg/L,见表4。[align=center]表4 方法的精密度和检出限[/align][table][tr][td=1,2][align=center]组分[/align][/td][td=3,1][align=center]标液1[/align][/td][td=3,1][align=center]标液2[/align][/td][td][align=center]检出限/mg/L[/align][/td][/tr][tr][td]浓度/mg/L[/td][td]平均峰面积[/td][td][align=center]RSD/%[/align][/td][td][align=center]浓度/mg/L[/align][/td][td]平均峰面积[/td][td][align=center]RSD/%[/align][/td][/tr][tr][td][align=center]草酸[/align][/td][td][align=center]1.00 [/align][/td][td][align=center]78077.3[/align][/td][td][align=center]2.10[/align][/td][td][align=center]10.00 [/align][/td][td][align=center]955086.6[/align][/td][td][align=center]0.86 [/align][/td][td][align=center]0.04[/align][/td][/tr][tr][td][align=center]SCN- [/align][/td][td][align=center]1.00 [/align][/td][td][align=center]116110.4[/align][/td][td][align=center]2.26[/align][/td][td][align=center]10.00 [/align][/td][td][align=center]1146968.6[/align][/td][td][align=center]1.16 [/align][/td][td][align=center]0.03 [/align][/td][/tr][/table]2.4 [size=12px] [/size]共存阴离子及抗坏血酸的影响由于尿液中含有大量的有机物和氯化物、磷酸盐和硫酸盐等阴离子,尿样通过C18柱的净化可以消除有机物的影响,尿液经10倍稀释以降低氯化物、磷酸盐和硫酸盐的影响。考察了氯化物等3种阴离子对草酸和硫氰酸盐测定结果的影响,结果表明,氯化物、磷酸盐和硫酸盐的保留时间远小于草酸和硫氰酸盐,且500mg/L Cl-、300mg/L H2PO4-、SO4-2(H2PO4-、SO4-2完全分不开合并为一个峰)不影响50mg/L的草酸、3mg/L的测定,分离色谱图见图2。[align=center][img=,379,281]https://ng1.17img.cn/bbsfiles/images/2020/09/202009021441474631_778_3389662_3.png!w379x281.jpg[/img][/align][align=center]图2 常见阴离子与草酸和硫氰酸盐分离色谱图[/align]尿液中可能含有抗坏血酸,在碱性条件下,抗坏血酸易发生降解反应,而草酸是抗坏血酸的降解产物之一,影响草酸的准确测定,有研究显示在15.0mmol/LNaHCO3溶液(pH=8.3)中40mg/L的抗坏血酸在80min内未降解为草酸[17],本试验使用10.0mmol/LNa2CO3溶液(pH≈11.1)为淋洗液,pH值远大于8.3,样品从进样到草酸出峰需要11min多钟,这段时间尿液中的抗坏血酸可能降解生成草酸而影响其测定。试验用纯水配制30mg/L的抗坏血酸观察其降解情况,结果表明,本试验条件下30mg/L的抗坏血酸降解产生约0.3mg/L的草酸,试验采用亚硫酸盐(SO3-2)抑制抗坏血酸的降解,这与在易氧化药物制剂中加入亚硫酸盐以提高药物稳定性的方法有相似原理。[align=center][img=,517,262]https://ng1.17img.cn/bbsfiles/images/2020/09/202009021442032319_2305_3389662_3.png!w517x262.jpg[/img][/align][align=center]图3 抗坏血酸降解抑制试验结果[/align][align=center]曲线1、30mg/L抗坏血酸(黑色)2、1+50 mg/L的SO3-2(粉红色)[/align][align=center] 3、[size=12px]30mg/L抗坏血酸+10mg/L草酸(蓝色)4、3+50 mg/L的SO[/size][size=12px]3[/size][size=12px]-2[/size][size=12px](桔红色)[/size][/align]试验结果显示,50mg/L的SO3-2可抑制30mg/L抗坏血酸的降解,见图3,且至少在120min内30mg/L抗坏血酸对10.0mg/L的草酸的峰面积与峰高无明显影响(增加值5%)。同时50mg/L的SO3-2对草酸和硫氰酸盐的测定结果无明显影响(误差5%),见图4。[align=center][img=,565,254]https://ng1.17img.cn/bbsfiles/images/2020/09/202009021442164802_4125_3389662_3.png!w565x254.jpg[/img][/align][align=center]图4 50mg/L的SO3-2对草酸和硫氰酸盐测定结果的影响[/align][align=center]曲线1、10mg/L草酸和硫氰酸盐(蓝色)[/align][align=center] 2、1+50 mg/L的SO3-2(粉红色)[/align]2.5尿液测定及回收率试验结果按试验方法1.4.3的步骤操作取1.5mL样液于样品瓶中,启动自动进样器进样测定各组分的峰面积(S)和峰高(H),以标准曲线法定量,同时进行加标回收试验。3份尿液草酸和[align=center]表5 尿液测定及回收率试验结果(以峰面积计)[/align][table][tr][td=1,2][align=center]组分[/align][/td][td=3,1][align=center]尿液1[/align][/td][td=3,1][align=center]尿液2[/align][/td][td=3,1][align=center]尿液3[/align][/td][/tr][tr][td][align=center]本底/mg/L[/align][/td][td][align=center]加入量[/align][align=center]/mg/L[/align][/td][td][align=center]回收率/%[/align][/td][td][align=center]本底/mg/L[/align][/td][td][align=center]加入量/mg/L[/align][/td][td][align=center]回收率[/align][align=center]/%[/align][/td][td][align=center]本底[/align][align=center]/mg/L[/align][/td][td]加入量/mg/L[/td][td]回收率/%[/td][/tr][tr][td][align=center]草酸[/align][/td][td][align=center]4.71[/align][/td][td][align=center]10.0[/align][/td][td][align=center]101.1[/align][/td][td][align=center]6.21[/align][/td][td][align=center]5.0[/align][/td][td][align=center]97.0[/align][/td][td][align=center]14.83[/align][/td][td][align=center]2.0[/align][/td][td][align=center]95.0[/align][/td][/tr][tr][td][align=center]SCN-[/align][/td][td][align=center]0.21[/align][/td][td][align=center]10.0[/align][/td][td][align=center]100.5[/align][/td][td][align=center]0.45[/align][/td][td][align=center]5.0[/align][/td][td][align=center]97.2[/align][/td][td][align=center]0.72[/align][/td][td][align=center]2.0[/align][/td][td][align=center]95.5[/align][/td][/tr][/table]硫氰酸盐的测定结果分别在4.71mg/L~14.83mg/L和0.21mg/L~0.72mg/L,加标回收率分别为:95.0%~101.1%和95.5~100.5%,结果见表5。其中尿液2的加标色谱图见图5.[align=center][img=,574,253]https://ng1.17img.cn/bbsfiles/images/2020/09/202009021442298329_66_3389662_3.png!w574x253.jpg[/img][/align][align=center]图5 尿液2及其加标色谱图[/align]曲线1、尿液[align=center] 2、尿液加5mg/L草酸和硫氰酸盐[/align]3 小结本工作采用国产[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]设备,建立了以青岛盛翰色谱公司生产的SH-AC-3型阴离子交换柱为分离柱,10.0mmol/LNa2CO3为淋洗液、流量1.0mL/min等度洗脱,抑制电导检测-[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法同时测定尿液中草酸和硫氰酸盐的分析方法。方法具有良好的重现性和准确性,操作简便快速,尿样通过C18柱的净化可以消除有机物的影响,尿液稀释10倍后可降低氯化物、磷酸盐和硫酸盐的影响。方法以自动进样器进样,降低检验人员的工作强度,提高了工作效率,适用尿液中草酸和硫氰酸盐的同时测定。参考文献1)中华人民共和国卫生部.GBZ209-2008职业性急性氰化物中毒诊断标准.北京:人民卫生出版社,20082)顾 欣,黄士新,李丹妮,等.乳中硫氰酸盐对人类健康的风险评估[J],中国兽药杂志,2010,44(9):45-523)WS/T39-1996.尿中硫氰酸盐的吡啶-巴比妥酸分光光度测定方法.北京:中国标准出版社,19974)冯翠霞,林丽玲,黄辉涛.分光光度法测定尿中硫氰酸盐的异烟酸-吡唑酮[J],中国职业医学,2009,36(6):501,5045)黄选忠,汪 波,舒开继等.异烟酸-巴比妥酸分光光度法测定尿硫氰酸盐[J],山东化工,2019,48(20):106-107,1126)钟良康,方波. 超短柱顶空[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定尿中硫氰酸盐[J],中国卫生检验杂志,2005,15(5):568,6287)武和平,武景福.尿中硫氰酸盐的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]测定法[J],职业与健康,2005,21(1):40-418)马腾骧,孙 光. 现代泌尿外科学[M].天津:天津科学技术出版社,2000:587-5889)李桂兰.锆-偶氮胂Ⅲ络合物比色法测定尿草酸[J].临床检验杂志,1997,15(2):86-8710)张爱梅,贾丽萍,牛学丽.表面活性剂增敏阻抑动力学光度法测定痕量草酸[J].分析化学,2003,31(9):1115-111811)麻全生,杨文初.铬酸钾氧化甲基红催化光度法测定微量草酸[J].理化检验化学分册,1998,37(7):309-31012)冯素玲,陈小兰,樊 静,等.抑制动力学荧光法测定草酸[J].分析化学,2000,28(5):621-62313)陈兰化,赵丹华.催化荧光法测定痕量草酸[J].光谱学与光谱分析,2003,23(1):203-20414)廖贤平,宋光庆.HPLC法同时测定尿液中草酸和枸橼酸含量的方法学评价及临床应用[J].武警医学院学报,2010,19(1):47-5015)彭 婕,郭卫红,谈恒山,等.高效液相色谱法测定人尿液中草酸的含量[J].中国医院药学杂志,2006,26(3):299-30116)谈绮文,郭 玮,顾梅秀,等.高效毛细管电泳法测定尿液中微量草酸和柠檬酸[J].中华检验医学杂志,2014,37(4):281-28417)杭义萍,卢祝靓子,杨春英.抗坏血酸存在下[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法直接测定尿液中草酸含量的研究[J].分析科学学报,2014,33(11):1307-131118)颜金良,高 杰,颜勇卿,等.[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法快速测定人尿液中草酸含量研究[J],中国卫生检验杂志,2009,19(3):554-55519)郭爱华,袁 佗,王 玮.[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法快速测定人尿中的硫氰酸盐[J],环境与职业医学,2015,32(6):593-59620)何 漪,王 钟,刘月月,等.抑制电导检测-[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法测定人尿中硫氰酸盐[J].现代预防医学,2017,44(22):4165-4167
求教:硫氰酸盐分光光度法测三氧化钼的方法我没查到硫氰酸盐分光光度法国标,有谁知道在哪能查到国标本文,请告诉我,或者有这个国标的发给我,谢谢!cyiping051@hotmail.com
硫氰酸盐光度法测定三氧化钨能否加硫脲
GB/T 223.26-2008 钢铁及合金 钼含量的测定 硫氰酸盐分光光度法[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=190510]GBT 223.26-2008 钢铁及合金 钼含量的测定 硫氰酸盐分光光度法.pdf[/url]
[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法同时测定环境水样中硫氰酸盐等8种阴离子,预压2000积分,7月
【序号】:1【作者】:张宝; 刘晓玲; 李东刚; 孙长华;【题名】:离子色谱法测定液体乳制品中硫氰酸盐【期刊】:理化检验(化学分册),【年、卷、期、起止页码】:2011年 02期 【全文链接】:http://202.119.208.220:8002/kns50/detail.aspx?dbname=CJFD2011&filename=LHJH201102030
[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法同时测定环境水样中硫氰酸盐等8种阴离子,预压2000积分,7月
目前,使用的EDTA-Na2盐蒸馏预处理,异烟酸吡唑啉酮光度比色,能测定全部简单氰化物和绝大部分络合氰化物,但是否包括了硫代氰酸盐叠氮化物能够测定吗?
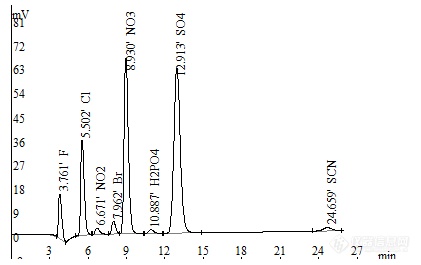
[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法同时测定环境水样中硫氰酸盐等8种阴离子[align=center]黄选忠[/align][align=center](湖北兴山县疾病预防控制中心,湖北兴山,443711)[/align]摘要:【目的】建立以SH-AC-3型阴离子交换柱为分离柱,[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url][font=times new roman][size=14px]-[/size][/font]抑制电导检测法同时测定环境水样硫氰酸盐、硫酸盐等8种阴离子的新方法。【方法】试验研究同时测定8种阴离子特别是硫氰酸盐的色谱条件和可行性,优化确定色谱条件。【结果】以SH-AC-3型阴离子交换柱为分离柱,以6.0mmol[font='Calibri',sans-serif][size=14px]/LNa[sub][size=14px]2[/size][/sub]CO[sub][size=14px]3[/size][/sub][/size][/font]-2.0mmol/L NaHCO[size=14px]3[/size]为淋洗液,流量为1.0mL/min,采用等度洗脱的方式可将硫氰酸盐、硫酸盐、磷酸盐、硝酸盐、溴化物、亚硝酸盐、氯化物和氟化物等8种阴离子完全分离,通过抑制电导检测,各组分的峰面积与其浓度分别0.05~5.0、2.5~125.0、0.2~10.0、0.25~25.0、0.20~10.0、0.10~5.0、0.25~25.0、0.2~10.0mg/L范围内呈良好的线性关系,相关系数在0.9994~0.9999,方法应用于环境水样中硫氰酸盐等8种阴离子的同时测定,加标回收率在93.2%~105.2%, 5次平行测定的相对标准偏差(RSD)小于5%(n=5)。【结论】本方法可用于环境水样中硫氰酸盐等8种阴离子的同时测定。关键词:[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法;水;硫氰酸盐;阴离子;中图分类号:O652.63 文献标识码: 文章编号:[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法以其操作简便、试剂消耗少、可自动化和多组分同时测定的优势在环保、卫生等行业中得到广泛的应用。《水和废水监测分析方法》(第四版)推荐用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法[size=14px][1][/size]同时测定水中氟化物、氯化物、亚硝酸盐、硝酸盐、磷酸盐和硫酸盐等六种阴离子,文献[2-4]报道用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法同时测定水中前述六种阴离子加上溴化物等七种阴离子,硫氰酸盐是有毒有害物质,过量摄入可引起急性中毒,少量摄取也会妨碍机体对碘的利用,引起甲状腺疾病,尤其对胎儿和婴儿的智力和神经系统发育存在较大的风险[size=14px][5][/size],水是人们日常生活必不可少的物质,水中的硫氰酸盐也可被人体摄取危害健康,因此,检测水中硫氰酸盐是一项有意义的工作。目前测定水中硫氰酸盐国家标准推荐的是异烟酸-吡唑啉酮分光光度法[size=14px][6][/size],该法为消除氰化物及其金属配合物的影响,测定前样品要进行前处理,操作繁杂。由于水中硫氰酸盐含量较低,一维[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法测定较为困难,林立等人[size=14px][7][/size]曾利用二维色谱的富集功能和毛细管[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]的高灵敏度,以二维[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法测定环境了水样中微量的[font=times new roman]硫氰酸根等阴离子,但大多基层实验室因缺乏仪器而难以应用。[/font][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法[font=times new roman]目前[/font]主要应用于乳及乳制品中硫氰酸盐(非法添加,含量较高)的测定,也是农业、出入境检验检疫等的行业推荐的标准方法[size=14px][8-9][/size],用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法同时测定环境水样中硫氰酸盐、硫酸盐、磷酸盐、硝酸盐、溴化物、亚硝酸盐、氯化物和氟化物等八种阴离子特别是硫氰酸盐似未见报道。本试验研究用SH-AC-3型阴离子交换柱为分离柱,以抑制电导检测[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法同时测定环境水样中硫氰酸盐等8种阴离子的分析方法。[font=times new roman]通过试验优化确立了相关色谱条件[/font],建立了以SH-AC-3型阴离子交换柱为分离柱,以6.0mmol/LNa[size=14px]2[/size]CO[size=14px]3[/size]-2.0mmol/L NaHCO[size=14px]3[/size]为淋洗液,流量为1.0mL/min等度洗脱抑制电导检测-[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法同时测定环境水样中硫氰酸盐等8种阴离子的新方法。加标回收率分别为:95.6%~105.4%、98.5~106.8%、91.3%~96.7%、98.4~109.3%、96.5~107.3%、96.8%~109.2%、103.0%~105.2%和95.3%~99.8%,各组分5次平行测定的相对标准偏差(RSD)小于4%,方法的检出限在0.02mg/L~0.10 mg/L 。1、试验部分1.1主要仪器CIC-100型[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url](青岛盛瀚色谱公司,编号15601),抑制器:自再生抑制器,检测器:电导检测器,定量环体积为25μL;SHA—15自动进样器(青岛盛瀚色谱公司,编号AS1518050);SH-AC-3型阴离子交换柱(250×4.0mm i.d,青岛盛瀚色谱公司,批号:1602037);SH-AC-3型保护柱(50×4.0mm i.d,青岛盛瀚色谱公司,批号:1602037)。1.2 仪器工作条件及参数设置色谱仪:柱箱温度35℃,电流:75mA,量程:1档。自动进样器:全定量环取样,取样后清洗(每针之间),置换量70μL,取样量25μL,扎针深度4mm。1.3主要试剂F[size=14px]-[/size]标准溶液:GBW(E)080549,1000 mg/L; Cl[size=14px]-[/size]标准溶液:GBW(E)080268,1000 mg/L;SO[size=14px]4[/size][size=14px]-2[/size]标准溶液:GBW(E)080266,1000 mg/L;NO[size=14px]2[/size][size=14px]-[/size]标准溶液:GBW(E)080264,1000mg/L;NO[size=14px]3[/size][size=14px]-[/size]标准溶液(以N计):GBW(E)080223,1000 mg/L;SCN[size=14px]-[/size]标准溶液:1000 mg/L,按照文献[9]配制;H[size=14px]2[/size]PO[size=14px]4[/size][size=14px]-[/size]和Br[size=14px]-[/size]标准溶液:1000 mg/L,按照文献[2]配制。用前将各种标准溶液用纯水稀释成含F[size=14px]-[/size]、H[size=14px]2[/size]PO[size=14px]4[/size][size=14px]-[/size]和Br[size=14px]- [/size]10.0mg/L,Cl[size=14px]-[/size]和NO[size=14px]3[/size][size=14px]-[/size](以N计) 25.0 mg/L,NO[size=14px]2[/size][size=14px]-[/size]和SCN[size=14px]-[/size] 5.0 mg/L, SO[size=14px]4[/size][size=14px]-2[/size] 125.0 mg/L混合标准应用液(A液)及含F[size=14px]-[/size]、H[size=14px]2[/size]PO[size=14px]4[/size][size=14px]-[/size]和Br[size=14px]- [/size]20.0mg/L,Cl[size=14px]-[/size]和NO[size=14px]3[/size][size=14px]-[/size](以N计) 50.0 mg/L,NO[size=14px]2[/size][size=14px]-[/size]和SCN[size=14px]-[/size] 10.0 mg/L, SO[size=14px]4[/size][size=14px]-2[/size] 250.0 mg/L混合标准应用液(B液)备用。无水碳酸钠(分析纯,国药集团化学试剂有限公司),碳酸氢钠(分析纯,国药集团化学试剂有限公司)。试验所用试剂均为AR及以上级,试验用水为超纯水(18.2ΜΩcm)。1.4 试验方法1.4.1 标准曲线的绘制 取混合标准应用液(A液)0.10、0.20mL及B液0.20、0.50、1.0、2.0、3.0、4.0和5.0 mL于10mL容量瓶中加纯水至刻度,混匀,配制成含F[size=14px]-[/size]、H[size=14px]2[/size]PO[size=14px]4[/size][size=14px]-[/size]、Br[size=14px]- [/size] 0.10~10.0mg/L,Cl[size=14px]-[/size]、NO3[size=14px]-[/size](以N计)0.25~ 25.0 mg/L,NO[size=14px]2[/size][size=14px]-[/size]和SCN[size=14px]-[/size] 0.05~5.0 mg/L, SO[size=14px]4[/size][size=14px]-2[/size] 1.25~125.0 mg/L的标准系列,各管取1.5mL于样品瓶中,启动自动进样器进样分别测定各组份的峰面积(S),以S对各组份浓度绘制工作曲线。1.4.2 样品测定 取水样经0.45μm滤膜过滤后取1.5mL于样品瓶中,启动自动进样器进样测定各组份的峰面积(S),以标准曲线法定量,同时进行加标回收试验。2、结果与讨论2.1 色谱条件的选择2.1.1 淋洗液的选择 当以4.5mmol/L Na[size=14px]2[/size]CO[size=14px]3[/size]-4.0 mmol/L NaHCO[size=14px]3[/size]溶液为淋洗液、流量1.0mL/min等度洗脱,SH-AC-3型柱能将氟化物、氯化物、亚硝酸盐、溴化物、硝酸盐、磷酸盐、硫酸盐和硫氰酸盐等8种阴离子完全分离,但硫氰酸盐的保留时间T(下同)长达33min以上,无分析应用价值。为缩短硫氰酸盐的T,选用洗脱能力较强的Na[size=14px]2[/size]CO[size=14px]3[/size]溶液为淋洗液进行试验,结果显示当Na[size=14px]2[/size]CO[size=14px]3[/size]溶液浓度分别为6.0、8.0、10.0和12.0 mmol/L时,硫氰酸盐的T分别缩短至24、21、20和19分多钟,但硝酸盐、磷酸盐和硫酸盐分离度欠佳甚至是完全分不开,试验结果见表1。从表1可见,要将前述8种阴离子完全分离,不宜以单纯的Na[size=14px]2[/size]CO[size=14px]3[/size]溶液为淋洗液,宜以Na[size=14px]2[/size]CO[size=14px]3[/size]-NaHCO[size=14px]3[/size]溶液为淋洗液。Na[size=14px]2[/size]CO[size=14px]3[/size]+NaHCO[size=14px]3[/size]浓度配比试验结果表明,[align=center]表1 Na[size=14px]2[/size]CO[size=14px]3[/size]溶液浓度对分离情况的影响(流量1.0 ml/min)[/align][table][tr][td=1,2][align=center]组分分离情况[/align][/td][td=4,1][align=center]Na[size=14px]2[/size]CO[size=14px]3[/size]溶液浓度/mmol/L[/align][/td][/tr][tr][td][align=center]6.0 [/align][/td][td][align=center]8.0 [/align][/td][td][align=center]10.0 [/align][/td][td][align=center]12.0 [/align][/td][/tr][tr][td][align=center]SCN[size=14px]-[/size] 保留时间T/min[/align][/td][td][align=center]24.704[/align][/td][td][align=center]21.695[/align][/td][td][align=center]20.643[/align][/td][td][align=center]19.119[/align][/td][/tr][tr][td]NO[size=14px]3[/size][size=14px]-[/size]、H[size=14px]2[/size]PO[size=14px]4[/size][size=14px]-[/size]和SO[size=14px]4[/size][size=14px]-2[/size]的分离情况[/td][td]NO[size=14px]3[/size][size=14px]-[/size]与H2PO[size=14px]4[/size][size=14px]-[/size]完全分开,H[size=14px]2[/size]PO[size=14px]4[/size][size=14px]-[/size]和SO[size=14px]4[/size][size=14px]-2[/size]不能完全分开[/td][td]NO[size=14px]3[/size][size=14px]-[/size]与H[size=14px]2[/size]PO[size=14px]4[/size][size=14px]-[/size]完全分开,H[size=14px]2[/size]PO[size=14px]4[/size][size=14px]-[/size]和SO[size=14px]4[/size][size=14px]-2[/size]合并为一个峰[/td][td]NO[size=14px]3[/size][size=14px]-[/size]与H[size=14px]2[/size]PO[size=14px]4[/size][size=14px]-[/size]、SO[size=14px]4[/size][size=14px]-2[/size]不能完全分离,H[size=14px]2[/size]PO[size=14px]4[/size][size=14px]-[/size]和SO[size=14px]4[/size][size=14px]-2[/size]合并为一个峰[/td][td]NO[size=14px]3[/size][size=14px]-[/size]、H[size=14px]2[/size]PO[size=14px]4[/size][size=14px]-[/size]和SO[size=14px]4[/size][size=14px]-2[/size]三者合并为一个峰[/td][/tr][/table]当Na[size=14px]2[/size]CO[size=14px]3[/size]+NaHCO[size=14px]3[/size]浓度为6 mmol/L+1 mmol/L~6 mmol/L+3 mmol/L时,前述8种阴离子能完全分离,各组分的分离度R(相对于后续组分,如氟化物的R是相对于氯化物的,下同)可达1.5及以上,硫氰酸盐的T在26min以内,试验结果见表2。综合考虑硝酸盐、磷酸盐的R,试验选择6.0mmol/LNa[size=14px]2[/size]CO[size=14px]3[/size]-2.0mmol/L NaHCO[size=14px]3[/size]溶液为淋洗液。[align=center]表2 Na[size=14px]2[/size]CO[size=14px]3[/size]+NaHCO[size=14px]3[/size]溶液浓度(mmol/L)配比试验结果(流量1.0 ml/min)[/align][table][tr][td=1,2][align=center]组分[/align][/td][td=2,1][align=center]6.0mmol/L+1.0mmol/L[/align][/td][td=2,1][align=center]6.0mmol/L+2.0mmol/L[/align][/td][td=2,1][align=center]6.0mmol/L+3.0mmol/L[/align][/td][/tr][tr][td][align=center]T/min[/align][/td][td][align=center]R[/align][/td][td][align=center]T/min[/align][/td][td][align=center]R[/align][/td][td][align=center]T/min[/align][/td][td][align=center]R[/align][/td][/tr][tr][td][align=center]F[size=14px]-[/size][/align][/td][td][align=center]4.319[/align][/td][td][align=center]3.09[/align][/td][td][align=center]4.148[/align][/td][td][align=center]3.20 [/align][/td][td][align=center]4.176 [/align][/td][td][align=center]3.26 [/align][/td][/tr][tr][td][align=center]Cl[size=14px]-[/size][/align][/td][td][align=center]6.014[/align][/td][td][align=center]1.89[/align][/td][td][align=center]5.852[/align][/td][td][align=center]1.96 [/align][/td][td][align=center]5.893 [/align][/td][td][align=center]1.98 [/align][/td][/tr][tr][td][align=center]NO[size=14px]2[/size][size=14px]-[/size][/align][/td][td][align=center]7.135[/align][/td][td][align=center]2.09[/align][/td][td][align=center]6.992[/align][/td][td][align=center]2.13 [/align][/td][td][align=center]7.035 [/align][/td][td][align=center]2.12 [/align][/td][/tr][tr][td][align=center]Br[size=14px]- [/size][/align][/td][td][align=center]8.412[/align][/td][td][align=center]1.56[/align][/td][td][align=center]8.287[/align][/td][td][align=center]1.58 [/align][/td][td][align=center]8.307 [/align][/td][td][align=center]1.59 [/align][/td][/tr][tr][td][align=center]NO[size=14px]3[/size][size=14px]-[/size][/align][/td][td][align=center]9.348[/align][/td][td][align=center]3.12[/align][/td][td][align=center]9.231[/align][/td][td][align=center]2.44 [/align][/td][td][align=center]9.247 [/align][/td][td][align=center]2.00 [/align][/td][/tr][tr][td][align=center]H[size=14px]2[/size]PO[size=14px]4[/size][size=14px]-[/size][/align][/td][td][align=center]11.556[/align][/td][td][align=center]1.49[/align][/td][td][align=center]10.993[/align][/td][td][align=center]1.88 [/align][/td][td][align=center]10.688 [/align][/td][td][align=center]2.83 [/align][/td][/tr][tr][td][align=center]SO[size=14px]4[/size][size=14px]-2[/size][/align][/td][td][align=center]12.778[/align][/td][td][align=center]10.27[/align][/td][td][align=center]12.641[/align][/td][td][align=center]10.52 [/align][/td][td][align=center]13.054 [/align][/td][td][align=center]10.74 [/align][/td][/tr][tr][td][align=center]SCN[size=14px]-[/size] [/align][/td][td][align=center]24.891[/align][/td][td][align=center]/[/align][/td][td][align=center]24.938[/align][/td][td][align=center]/[/align][/td][td][align=center]25.337 [/align][/td][td][align=center]/[/align][/td][/tr][/table]2.1.2 色谱柱的选择 以6.0mmol/LNa[size=14px]2[/size]CO[size=14px]3[/size]-2.0mmol/L NaHCO[size=14px]3[/size]为淋洗液、流量1.0mL/min等度洗脱,考察了青岛盛翰色谱公司生产的SH-AC-1型和SH-AC-3型阴离子交换柱对硫氰酸盐、硫酸盐、磷酸盐、硝酸盐、溴化物、亚硝酸盐、氯化物和氟化物等8种阴离子的分离效果,结果表明,在此条件下SH-AC-1型柱虽能将上述前7种阴离子完全分离,但硫氰酸盐至少在50min内未出峰,分离效率低下,而SH-AC-3型柱可将硫氰酸盐、硫酸盐、磷酸盐、硝酸盐、溴化物、亚硝酸盐、氯化物和氟化物等8种阴离子完全分离,且硫氰酸盐的T在26min以内,故本试验选择SH-AC-3型阴离子交换柱为分离柱。2.1.3淋洗液流量的选择 当淋洗液组成和浓度一定时,淋洗液流量是影响组分的T和R的主要因素,本试验淋洗液流量在0.8mL/min~1.2mL/min时硫氰酸盐、硫酸盐、磷酸盐、硝酸盐、溴化物、亚硝酸盐、氯化物和氟化物等8种阴离子的R在1.51以上,表明各组分已完全分离[size=14px][10][/size],见表3。综合考虑各组分的T和R及系统压力,淋洗液流量选定为1.0mL/min。[align=center]表3 淋洗液流量对分离度和保留时间的影响(6.0mmol/LNa[size=14px]2[/size]CO[size=14px]3[/size]-2.0mmol/L NaHCO[size=14px]3[/size])[/align][table][tr][td=1,2][align=center]组分[/align][/td][td=2,1][align=center]0.8ml/min[/align][/td][td=2,1][align=center]1.0ml/min[/align][/td][td=2,1][align=center]1.2ml/min[/align][/td][/tr][tr][td][align=center]T/min[/align][/td][td][align=center]R[/align][/td][td][align=center]T/min[/align][/td][td][align=center]R[/align][/td][td][align=center]T/min[/align][/td][td][align=center]R[/align][/td][/tr][tr][td][align=center]F-[/align][/td][td][align=center]5.152[/align][/td][td][align=center]3.41[/align][/td][td][align=center]4.181[/align][/td][td][align=center]3.31 [/align][/td][td][align=center]3.470 [/align][/td][td][align=center]3.34 [/align][/td][/tr][tr][td][align=center]Cl[size=14px]-[/size][/align][/td][td][align=center]7.252[/align][/td][td][align=center]2.13[/align][/td][td][align=center]5.906[/align][/td][td][align=center]2.02 [/align][/td][td][align=center]4.921 [/align][/td][td][align=center]2.03 [/align][/td][/tr][tr][td][align=center]NO[size=14px]2[/size][size=14px]-[/size][/align][/td][td][align=center]8.674[/align][/td][td][align=center]2.25[/align][/td][td][align=center]7.065[/align][/td][td][align=center]2.16 [/align][/td][td][align=center]5.900 [/align][/td][td][align=center]2.19 [/align][/td][/tr][tr][td][align=center]Br[size=14px]- [/size][/align][/td][td][align=center]10.238[/align][/td][td][align=center]1.72[/align][/td][td][align=center]8.354[/align][/td][td][align=center]1.62 [/align][/td][td][align=center]6.998 [/align][/td][td][align=center]1.61 [/align][/td][/tr][tr][td][align=center]NO[size=14px]3[/size][size=14px]-[/size][/align][/td][td][align=center]11.425[/align][/td][td][align=center]2.53[/align][/td][td][align=center]9.315[/align][/td][td][align=center]2.32 [/align][/td][td][align=center]7.806 [/align][/td][td][align=center]2.21 [/align][/td][/tr][tr][td][align=center]H[size=14px]2[/size]PO[size=14px]4[/size][size=14px]-[/size][/align][/td][td][align=center]13.543[/align][/td][td][align=center]2.75[/align][/td][td][align=center]10.969[/align][/td][td][align=center]2.59 [/align][/td][td][align=center]9.151 [/align][/td][td][align=center]2.57 [/align][/td][/tr][tr][td][align=center]SO[size=14px]4[/size][size=14px]-2[/size][/align][/td][td][align=center]16.283[/align][/td][td][align=center]11.14[/align][/td][td][align=center]13.178[/align][/td][td][align=center]10.84 [/align][/td][td][align=center]10.995 [/align][/td][td][align=center]10.72 [/align][/td][/tr][tr][td][align=center]SCN[size=14px]-[/size] [/align][/td][td][align=center]30.636[/align][/td][td][align=center]/[/align][/td][td][align=center]24.997[/align][/td][td][align=center]/[/align][/td][td][align=center]21.175 [/align][/td][td][align=center]/[/align][/td][/tr][/table]2.1.4 柱箱温度的确定 考察了30℃、35℃和40℃时各组分的分离效果,结果显示,在30℃~40℃范围内,8种组分均能较好的分离,其R值均在1.5以上,且随着柱温的升高组分的T稍微缩短,在保证各组分有适宜的R和T的前提下尽量使用较低的柱温,故本试验确定柱箱温度为35℃。2.2标准曲线按照1.4.1配制标准系列,测定各管的峰面积(S),以S对浓度(C)绘制标准曲线,其标准曲线的线性范围、回归方程、相关系数r(回归曲线的截距、斜率和r由系统生成)列于表4。其中,含12.5mg/L的硫酸盐、2.5mg/L的氯化物和硝酸盐、1.0mg/L的氟化物、溴化物、磷酸盐,0.50mg/L的亚硝酸盐和硫氰酸盐的标准溶液色谱图见图1。[align=center]表4 标准曲线试验结果[/align][table][tr][td][align=center]组分[/align][/td][td][align=center]线性范围/mg/L[/align][/td][td][align=center]回归方程[/align][/td][td][align=center]相关系数/r[/align][/td][/tr][tr][td=1,2][align=center]F-[/align][/td][td][align=center]0.20~4.0[/align][/td][td][align=center]S=329500C-54510[/align][/td][td][align=center]0.9998[/align][/td][/tr][tr][td][align=center]4.0~10.0[/align][/td][td][align=center]S=385500C-280500[/align][/td][td][align=center]0.9994[/align][/td][/tr][tr][td][align=center]Cl[size=14px]-[/size][/align][/td][td][align=center]0.25~25.0[/align][/td][td][align=center]S=3823+242700C[/align][/td][td][align=center]0.9998[/align][/td][/tr][tr][td][align=center]NO[size=14px]2[/size][size=14px]-[/size][/align][/td][td][align=center]0.10~5.0[/align][/td][td][align=center]S=123200C-6043[/align][/td][td][align=center]0.9998[/align][/td][/tr][tr][td][align=center]Br[size=14px]- [/size][/align][/td][td][align=center]0.20~10.0[/align][/td][td][align=center]S=95570C-3100[/align][/td][td][align=center]0.9998[/align][/td][/tr][tr][td=1,2][align=center]NO[size=14px]3[/size][size=14px]-[/size][/align][/td][td][align=center]0.25~15.0[/align][/td][td][align=center]S=615800C-40830[/align][/td][td][align=center]0.9997[/align][/td][/tr][tr][td][align=center]15.0~25.0[/align][/td][td][align=center]S=2726000+423200C[/align][/td][td][align=center]0.9996[/align][/td][/tr][tr][td=1,2][align=center]H[size=14px]2[/size]PO[size=14px]4[/size][size=14px]-[/size][/align][/td][td][align=center]0.20~4.0[/align][/td][td][align=center]S=55450C-10500[/align][/td][td][align=center]0.9997[/align][/td][/tr][tr][td][align=center]4.0~10.0[/align][/td][td][align=center]S=63760C-43130[/align][/td][td][align=center]0.9998[/align][/td][/tr][tr][td=1,2][align=center]SO[size=14px]4[/size][size=14px]-2[/size][/align][/td][td][align=center]2.5~75.0[/align][/td][td][align=center]S=183100C-163700[/align][/td][td][align=center]0.9999[/align][/td][/tr][tr][td][align=center]75.0~125.0[/align][/td][td][align=center]S=2224000+151600C[/align][/td][td][align=center]0.9999[/align][/td][/tr][tr][td][align=center]SCN[size=14px]-[/size] [/align][/td][td][align=center]0.05~5.0[/align][/td][td][align=center]S=128200C-4033[/align][/td][td][align=center]0.9997[/align][/td][/tr][/table]2.3 方法的精密度和检出限对2种浓度的标准溶液各平行测定5次,计算各成分峰面积的RSD,同时测定仪器30min的基线噪声,以3倍基线噪声除以标准曲线的斜率计算各组分的检出限,5次平行测定的RSD[align=center][img]file:///C:/Users/maqy/Documents/WXWork/1688853676850491/Cache/Image/2020-07/海报3(1).png[/img][img=,421,265]https://ng1.17img.cn/bbsfiles/images/2020/07/202007221800484311_9016_3389662_3.png!w421x265.jpg[/img][/align][align=center]图1 标准溶液色谱法图[/align]小于4%,方法的重复性良好,方法的检出限在0.02mg/L~0.10 mg/L,见表5。[align=center]表5 方法的精密度和检出限[/align][table][tr][td=1,2][align=center]组分[/align][/td][td=3,1][align=center]标液1[/align][/td][td=3,1][align=center]标液2[/align][/td][td][align=center]检出限/mg/L[/align][/td][/tr][tr][td]浓度/mg/L[/td][td]平均峰面积[/td][td][align=center]RSD/%[/align][/td][td][align=center]浓度/mg/L[/align][/td][td]平均峰面积[/td][td][align=center]RSD/%[/align][/td][/tr][tr][td][align=center]F-[/align][/td][td][align=center]0.40 [/align][/td][td][align=center]78874.3[/align][/td][td][align=center]1.42[/align][/td][td][align=center]4.00 [/align][/td][td][align=center]1309698[/align][/td][td][align=center]0.17 [/align][/td][td][align=center]0.10 [/align][/td][/tr][tr][td][align=center]Cl[size=14px]-[/size][/align][/td][td][align=center]1.00 [/align][/td][td][align=center]264703.2[/align][/td][td][align=center]1.83[/align][/td][td][align=center]10.00 [/align][/td][td][align=center]2405065.8[/align][/td][td][align=center]0.39 [/align][/td][td][align=center]0.02 [/align][/td][/tr][tr][td][align=center]NO[size=14px]2[/size][size=14px]-[/size][/align][/td][td][align=center]0.20 [/align][/td][td][align=center]19378.8[/align][/td][td][align=center]1.63[/align][/td][td][align=center]2.00 [/align][/td][td][align=center]238313.5[/align][/td][td][align=center]1.09 [/align][/td][td][align=center]0.04 [/align][/td][/tr][tr][td][align=center]Br[size=14px]- [/size][/align][/td][td][align=center]0.40 [/align][/td][td][align=center]35641.4[/align][/td][td][align=center]1.72[/align][/td][td][align=center]4.00 [/align][/td][td][align=center]381821.2[/align][/td][td][align=center]0.32 [/align][/td][td][align=center]0.05 [/align][/td][/tr][tr][td][align=center]NO[size=14px]3[/size][size=14px]-[/size][/align][/td][td][align=center]1.00 [/align][/td][td][align=center]582741[/align][/td][td][align=center]0.74[/align][/td][td][align=center]10.00 [/align][/td][td][align=center]6095210.2[/align][/td][td][align=center]0.40 [/align][/td][td][align=center]0.04 [/align][/td][/tr][tr][td][align=center]H[size=14px]2[/size]PO[size=14px]4[/size][size=14px]-[/size][/align][/td][td][align=center]0.40 [/align][/td][td][align=center]11739.7[/align][/td][td][align=center]3.53[/align][/td][td][align=center]4.00 [/align][/td][td][align=center]225523.6[/align][/td][td][align=center]0.64 [/align][/td][td][align=center]0.09 [/align][/td][/tr][tr][td][align=center]SO[size=14px]4[/size][size=14px]-2[/size][/align][/td][td][align=center]5.00 [/align][/td][td][align=center]773850.8[/align][/td][td][align=center]0.71[/align][/td][td][align=center]50.00 [/align][/td][td][align=center]9109257.8[/align][/td][td][align=center]0.47 [/align][/td][td][align=center]0.03 [/align][/td][/tr][tr][td][align=center]SCN[size=14px]-[/size] [/align][/td][td][align=center]0.20 [/align][/td][td][align=center]21936.8.3[/align][/td][td][align=center]2.51[/align][/td][td][align=center]2.00 [/align][/td][td][align=center]252786.2[/align][/td][td][align=center]1.25 [/align][/td][td][align=center]0.04 [/align][/td][/tr][/table]2.4 样品测定及回收率试验结果取水样经0.45μm滤膜过滤后取1.5mL于样品瓶中,启动自动进样器进样测定各组份的峰面积(S),以标准曲线法定量,同时进行加标回收试验。硫氰酸盐、硫酸盐、磷酸盐、硝酸盐、溴化物、亚硝酸盐、氯化物和氟化物等8种阴离子加标回收率分别为:95.6%~105.4%、[align=center]表6 样品测定及回收率试验结果[/align][table][tr][td=1,2][align=center]组分[/align][/td][td=3,1][align=center]水样1[/align][/td][td=3,1][align=center]水样2[/align][/td][td=3,1][align=center]水样3[/align][/td][/tr][tr][td][align=center]本底/mg/L[/align][/td][td][align=center]加入量[/align][align=center]/mg/L[/align][/td][td][align=center]回收率/%[/align][/td][td][align=center]本底/mg/L[/align][/td][td][align=center]加入量/mg/L[/align][/td][td][align=center]回收率[/align][align=center]/%[/align][/td][td][align=center]本底[/align][align=center]/mg/L[/align][/td][td]加入量/mg/L[/td][td]回收率/%[/td][/tr][tr][td][align=center]F-[/align][/td][td][align=center]0.37[/align][/td][td][align=center]1.00[/align][/td][td][align=center]95.3[/align][/td][td][align=center]0.21[/align][/td][td][align=center]2.00[/align][/td][td][align=center]96.8[/align][/td][td][align=center]0.17[/align][/td][td][align=center]4.00[/align][/td][td][align=center]99.8[/align][/td][/tr][tr][td][align=center]Cl[size=14px]-[/size][/align][/td][td][align=center]11.27[/align][/td][td][align=center]2.50[/align][/td][td][align=center]103.6[/align][/td][td][align=center]2.79[/align][/td][td][align=center]5.00[/align][/td][td][align=center]103.0[/align][/td][td][align=center]9.58[/align][/td][td][align=center]10.00[/align][/td][td][align=center]105.2[/align][/td][/tr][tr][td][align=center]NO[size=14px]2[/size][size=14px]-[/size][/align][/td][td][align=center]0.22[/align][/td][td][align=center]0.50[/align][/td][td][align=center]96.8[/align][/td][td][align=center]0.04[/align][/td][td][align=center]1.00[/align][/td][td][align=center]104.2[/align][/td][td][align=center]0.04[/align][/td][td][align=center]2.00[/align][/td][td][align=center]109.2[/align][/td][/tr][tr][td][align=center]Br[size=14px]-[/size][/align][/td][td][align=center]0.15[/align][/td][td][align=center]1.00[/align][/td][td][align=center]96.5[/align][/td][td][align=center]0.05[/align][/td][td][align=center]2.00[/align][/td][td][align=center]107.3[/align][/td][td][align=center]0.05[/align][/td][td][align=center]4.00[/align][/td][td][align=center]100.5[/align][/td][/tr][tr][td][align=center]NO[size=14px]3[/size][size=14px]-[/size][/align][/td][td][align=center]26.01[/align][/td][td][align=center]2.50[/align][/td][td][align=center]98.4[/align][/td][td][align=center]1.08[/align][/td][td][align=center]5.00[/align][/td][td][align=center]109.3[/align][/td][td][align=center]12.63[/align][/td][td][align=center]10.00[/align][/td][td][align=center]103.6[/align][/td][/tr][tr][td][align=center]H[size=14px]2[/size]PO[size=14px]4[/size][size=14px]-[/size][/align][/td][td][align=center]0.56[/align][/td][td][align=center]1.00[/align][/td][td][align=center]91.3[/align][/td][td][align=center]0.09[/align][/td][td][align=center]2.00[/align][/td][td][align=center]92.5[/align][/td][td][align=center]0.43[/align][/td][td][align=center]4.00[/align][/td][td][align=center]96.7[/align][/td][/tr][tr][td][align=center]SO[size=14px]4[/size][size=14px]-2[/size][/align][/td][td][align=center]60.68[/align][/td][td][align=center]12.50[/align][/td][td][align=center]104.1[/align][/td][td][align=center]21.06[/align][/td][td][align=center]25.00[/align][/td][td][align=center]106.8[/align][/td][td][align=center]55.86[/align][/td][td][align=center]50.00[/align][/td][td][align=center]98.5[/align][/td][/tr][tr][td][align=center]SCN[size=14px]-[/size][/align][/td][td][align=center]0.05[/align][/td][td][align=center]0.50[/align][/td][td][align=center]95.6[/align][/td][td][align=center]0.04[/align][/td][td][align=center]1.00[/align][/td][td][align=center]96.8[/align][/td][td][align=center]0.06[/align][/td][td][align=center]2.00[/align][/td][td][align=center]105.4[/align][/td][/tr][/table]98.5~106.8%、91.3%~96.7%、98.4~109.3%、96.5~107.3%、96.8%~109.2%、103.0%~105.2%和95.3%~99.8%,结果见表6。3 小结本工作建立了以SH-AC-3型阴离子交换柱为分离柱,6.0mmol/LNa[size=14px]2[/size]CO[size=14px]3[/size]-2.0mmol/L NaHCO[size=14px]3[/size]为淋洗液、流量1.0mL/min等度洗脱,抑制电导检测-[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法同时测定环境水样中硫氰酸盐等8种阴离子的分析方法。方法重现性良好,操作简便快速,测定结果准确可靠,适用环境水样中硫氰酸盐等8种阴离子的同时测定。参考文献1)国家环境保护总局《水和废水监测分析方法》编委会.水和废水监测分析方法(第四版)[M]. 北京:中国环境科学出版社,2002:156-1612)《水质分析大全》编写组. 水质分析大全[M]. 重庆:科学技术文献出版社重庆分社,1989:115-1183)廖德丰,孙振中,戚隽渊.[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法同时测定水中7中阴离子的含量[J].水产科技情报,2013,40(3):156-1594)黄选忠,杜宏山,向培文,等.碱化底液消除水负峰[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法测定水中F[size=14px]-[/size]、Cl[size=14px]-[/size]等7种阴离子[J],化学分析计量,2014,23(1):48-525)顾 欣,黄士新,李丹妮,等.乳中硫氰酸盐对人类健康的风险评估[J],中国兽药杂志,2010,44(9):45-526)[color=#333333]GB/T 13897-1992 水质 硫氰酸盐的测定 异烟酸-吡唑啉酮分光光度法[/color][s].北京.中国标准出版社,19937)林 立,王海波,史亚利.[url=http://www.docin.com/p-832791022.html?docfrom=rrela%22 \o %22%E4%BA%8C%E7%BB%B4%E7%A6%BB%E5%AD%90%E8%89%B2%E8%B0%B1%E6%B3%95%E5%90%8C%E6%97%B6%E6%B5%8B%E5%AE%9A%E7%8E%AF%E5%A2%83%E6%B0%B4%E6%A0%B7%E4%B8%AD%E7%9A%84%E7%A2%98%E7%A6%BB%E5%AD%90 %E3%80%81 %E7%A1%AB%E6%B0%B0%E9%85%B8%E6%A0%B9%E5%92%8C%22 \t %22_blank][color=#3c3c3c]二维[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法同时测定环境水样中的碘[/color][/url]离子、硫氰酸根和高氯酸根[J],色谱,2013,31(3):281-2858)NY/T3513-2019 生乳中硫氰酸根的测定 [url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法[s].20199)SN/T3927-2014 出口乳制品中硫氰酸钠的测定 第一法 [url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法[s]. 北京.中国标准出版社,201410)许春向,邹学贤.现代卫生化学[M].北京:人民卫生出版社,2000:492-590[/s][/s][/s]
建立高效阴离子交换色谱电导法分析生鲜乳中硫氰酸盐的方法。采用乙酸溶液沉淀生鲜乳中蛋白,过滤后用RP 柱去除样品中的脂类物质。净化后,直接将试样注入[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url]分离,淋洗液OH-浓度为60mmol/L,外标法定量。稳定性实验中5 次进样1mg/L 硫氰酸根溶液的保留时间平均值为15.445min(RSD 为0.12%),峰面积平均值为0.1839μSmin(RSD 为0.26%)。方法回收率为96.0%~98.0%,RSD < 1.06%,检测限为0.2mg/kg,线性范围为0.5~6mg/L。
谁有:GB/T 223.26-1989或2008 钢铁及合金化学分析方法 硫氰酸盐直接光度法测定钼量请回复上传下,谢谢
[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法同时测定尿液中草酸和硫氰酸盐,预压4000积分,色谱赛区,8月

[align=center][b]异烟酸-巴比妥酸分光光度法测定尿硫氰酸盐[/b][/align][align=center][b]黄选忠[sup]*[/sup] [/b][/align][align=center][b](湖北兴山县疾病预防控制中心,443711)[/b][/align][b]摘要 [/b] 在弱酸性介质中及氯胺T存在条件下,SCN[sup]-[/sup]可与异烟酸-巴比妥酸形成一紫蓝色染料,该染料最大吸收波长位于598nm,且其吸光度A与SCN[sup]-[/sup]含量在一定的范围内呈良好的线性关系,据此我们建立了测定人尿中微量SCN[sup]-[/sup]的异烟酸-巴比妥酸分光光度法,本法SCN[sup]-[/sup]含量均在0~2.50μg/5.0mL范围内符合比耳定律,方法用于人尿中微量SCN[sup]-[/sup]的测定,结果令人满意。[b]关键词[/b] 硫氰酸盐 分光光度法 异烟酸 巴比妥酸[b]中图分类号[/b]:O657.3硫氰酸盐(SCN[sup]-[/sup])是致甲状腺肿物质,可阻滞甲状腺激素合成,引起甲状腺肿,因此监测人血、尿等标本中的SCN[sup]-[/sup]含量具有重要意义。同时尿中SCN[sup]-[/sup]含量也是接触氰化物的一项生物接触指标[sup][/sup],目前,测定尿中微量SCN[sup]-[/sup]的方法主要有分光光度法、[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法[sup][/sup]、[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法[sup][/sup]等,其中[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法和[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法均需要专门仪器,且耗时较长。分光光度法以其简便灵敏、设备简单而被广泛采用。已报道的分光光度法主要有异烟酸-吡唑啉酮光度法[sup][/sup]、吡啶-巴比妥酸光度法[sup][/sup](为国家卫生行业标准方法)、三氯化铁显色光度法等[sup][/sup],其中吡啶-巴比妥酸法和三氯化铁法的灵敏度较低,且所用吡啶有恶臭,有损于分析人员的健康,使其应用受到影响。异烟酸-巴比妥酸光度法已应用于生活饮用水微量氰化物的测定[sup][/sup],但应用于人尿中微量SCN[sup]-[/sup]的测定似未见报道。我们对异烟酸-巴比妥酸光度法比妥酸光度法测定人尿中微量SCN[sup]-[/sup]进行了研究,结果表明,在弱酸性介[u] [/u]*黄选忠,男,1962-10,主任技师,主要研究方向:卫生化学检验技术。工作单位:兴山县疾病预防控制中心,联系电话:13872688318,E-mail:xscdchxz@sina.com)质中,氯胺T可将SCN[sup]-[/sup]转化成氯化氰(CNCl),CNCl再与异烟酸-巴比妥酸形成一紫蓝色染料,该染料的最大吸收波长(λ[sub]max[/sub])位于598nm,其表观摩尔吸光系数ε达1.19×10[sup]5[/sup]Lmol[sup]-1[/sup]cm[sup]-1[/sup],且其吸光度与SCN[sup]-[/sup]含量在一定的范围内呈良好的线性关系(r0.9996),据此建立了测定人尿中微量SCN[sup]-[/sup]的异烟酸-巴比妥酸分光光度法,该法SCN[sup]-[/sup]含量在0~2.50μg/5.0mL范围内符合比耳定律,方法用于人尿中微量SCN[sup]-[/sup]的测定,其结果与国家行业标准方法相吻合,加标回收率在90%~104%,方法的选择性、稳定性和灵敏度均令人满意。[b]1 实验部分 1.1主要仪器及试剂[/b]TU-1810SPC紫外可见分光光度计(北京普析通用仪器有限公司);SCN[sup]-[/sup]标准溶液:1.0mg/mL的标准储备液,按文献的方法配制。临用时稀释成1.0μg/mL(A液)和5.0μg/mL(B液)的标准应用液;1.0mol/L的KH[sub]2[/sub]PO[sub]4[/sub]缓冲溶液:pH≈4.67[sup][/sup];异烟酸-巴比妥酸(含二个水分子)溶液:称取0.615g异烟酸和1.025g巴比妥酸(含二个水分子)加入1.0mol/L的NaOH溶液12~13mL,搅拌使其溶解后补充纯水至100 mL(此溶液pH为近中性,其浓度分别为0.05mol/L和0.063mol/L);0.044 mol/L的氯胺T溶液(临用时配制);以上试剂为AR级,实验用水为超纯水(18.25ΜΩcm)。[b]1.2实验方法[/b]1.2.1标准曲线的绘制:取SCN[sup]-[/sup]标准应用A液(1.0μg/mL )0、0.20、0.50mL和B液0.20、0.30、0.40和0.50mL于10 mL比色管中,补充纯水至0.80mL,加入1.0mol/L的KH[sub]2[/sub]PO[sub]4[/sub]缓冲溶液2.0 mL、氯胺T溶液0.25 mL混匀,放置3min,加入异烟酸-巴比妥酸溶液2.0mL混匀,放置20-25min,以试剂空白为参比用1cm比色皿于598nm处测定各管吸光度A,以SCN[sup]-[/sup]含量对A绘制标准曲线。1.2.2尿样分析:取新鲜尿液0.10mL(SCN[sup]-[/sup]≤2.5μg)按实验方法1.2.1操作测定吸光度,以标准曲线法进行SCN[sup]-[/sup]定量,同时进行标准方法[sup][/sup]对照分析及加标回收实验。[b]2 结果与讨论2.1吸收光谱[/b]在本试验条件下,SCN[sup]-[/sup]与异烟酸-巴比妥酸形成一紫蓝色染料, 该染料的λ[sub]max[/sub]位于598 nm,而相应试剂空白在500-700nm基本无吸收,见图1。[b]2.2pH值的影响、缓冲溶液的选择及用量[/b][align=center][img=,384,268]https://ng1.17img.cn/bbsfiles/images/2019/09/201909161110577563_8288_3237657_3.png!w384x268.jpg[/img][/align][align=center]图1 吸收光谱[/align][align=center] 曲线1、2:分别为0.4和0.8μgSCN[sup]-[/sup]显色液(对试剂空白)[/align]试验结果表明,pH值对该显色体系的影响主要在SCN[sup]-[/sup]转化成CNCl的这一阶段,对后续显色阶段的影响相对较小,且溶液pH值在4.5~5.7的KH[sub]2[/sub]PO[sub]4[/sub]/Na[sub]2[/sub]HPO[sub]4[/sub](1/15mol/L)[sup][/sup]缓冲介质中体系有最大稳定的吸光度,同时对柠檬酸钠/盐酸(pH=5.25)、醋酸钠/盐酸(pH=4.58)、1.0mol/L的KH[sub]2[/sub]PO[sub]4[/sub]溶液(pH≈4.67)和KH[sub]2[/sub]PO[sub]4[/sub]/Na[sub]2[/sub]HPO[sub]4[/sub](1/15mol/L ,pH=5.29)等缓冲体系的进行了试验,结果表明,用柠檬酸钠/盐酸、醋酸钠/盐酸两种缓冲体系不仅吸光度偏低,且尿样加标回收率也偏低,用KH[sub]2[/sub]PO[sub]4[/sub]/Na[sub]2[/sub]HPO[sub]4[/sub]缓冲体系虽然体系可达最大吸光度,但尿样加标回收率偏低,而用1.0mol/L的KH[sub]2[/sub]PO[sub]4[/sub]溶液时,体系可达最大吸光度且尿样加标回收率较高这可能与尿样的基体干扰有关,当1.0mol/L的KH[sub]2[/sub]PO[sub]4[/sub]溶液的加入抵消了尿样的基体干扰,试验选用1.0mol/L的KH[sub]2[/sub]PO[sub]4[/sub]溶液控制显色体系酸度及离子强度,其用量在1.5-2.5 mL时体系有最大稳定的吸光度,试验选用2.0 mL[b]2.3氯化氰转化时间及氯胺T溶液用量的影响[/b]本试验条件下,SCN[sup]-[/sup]转化成CNCl的时间在2~5min ,0.044mol/L的氯胺T溶液用量在0.20~0.30 mL体系有最大稳定的吸光度,试验分别选用3min 和0.25mL。[b]2.4异烟酸和硫代巴比妥酸溶液用量的影响[/b]试验表明,0.10 mol/L的异烟酸和巴比妥酸溶液用量分别在0.50~1.50mL和 1.0~1.50 mL体系有最大稳定的吸光度,试验分别选用1.0 mL和1.25mL。[b]2.5异烟酸和巴比妥酸溶液混合加入实验[/b]试验表明,将异烟酸和巴比妥酸分别以0.05mol/L和0.063mol/L的浓度配成混合溶液一次加入2.0mL,可使体系吸光度提高20%以上,且提高了工作效率。[b]2.6共存物质的影响[/b]在本试验条件下,CN[sup]-[/sup]与SCN[sup]-[/sup]可发生相同显色反应而产生正干扰,但正常尿液中CN[sup]-[/sup]的含量较低,其影响可忽略。但考虑到尿液的成分较复杂,其中含量较大的物质(主要有尿素、氯化物、硫酸盐、磷酸氢盐、肌酐和铵离子等)可能因基体效应(较大的离子强度)对体系的显色反应产生影响,这在结果与讨论部分2.2结果中得到印证。为考察基体效应对体系显色反应的影响,按照尿液正常成分[sup][/sup]配制成含尿素(20g/L)、Cl[sup]-[/sup](13g/L)、Na[sup]+[/sup](9g/L),HPO[sub]4[/sub][sup]2-[/sup]、SO[sub]4[/sub][sup]2-[/sup](2.0g/L)、肌酐(1.4g/L)、NH[sub]4[/sub][sup]+[/sup](0.93 g/L)的尿液对照液,取0.10-0.30 mL尿液对照液加入1.0μg SCN[sup]-[/sup]测定吸光度,结果表明,至少三倍于尿样中的上述成分对1.0μg SCN[sup]-[/sup]的测定结果基本无影响(吸光度误差在±5%范围内),可见方法的选择性良好。[b]2.7标准曲线[/b]本法SCN[sup]-[/sup]含量在0~2.50μg/5.0mL范围内符合比耳定律(标准色阶见图2),标准曲线的回归方程及由曲线斜率法求得的表观摩尔吸光系数为:A=0.4118C[sub](SCN-,[/sub][sub]μ[/sub][sub]g[/sub][sub])[/sub]-0.0086,r=0.9996,ε=1.19×10[sup]5[/sup]Lmol[sup]-1[/sup]cm[sup]-1[/sup]若以吸光度为0.01、取样量为0.10mL计,方法最低检出浓度为0.5mg/L。[b][/b][align=center][img=,690,517]https://ng1.17img.cn/bbsfiles/images/2019/09/201909161111153203_545_3237657_3.jpg!w690x517.jpg[/img][/align][align=center]图2 0~2.50μg SCN[sup]-[/sup]/5.0mL的标准色阶[/align][b]2.8呈色稳定性[/b]在本试验条件下,SCN[sup]-[/sup]与异烟酸-巴比妥酸形成蓝色染料,其吸光度在20-25min达稳定最大值且至少再1h内基本稳定(吸光度变化值小于5%)。[b]2.9 重复性实验[/b]分别对0.20、0.50和2.00 μg SCN[sup]-[/sup]标准液平行测定5次,测定结果见表1,从表1可见,三水平测定结果的相对标准偏差(RSD)分别为2.98%、1.97%和1.06%,表明方法的重复性良好。[align=center][b]表1 重复性试验结果[/b][/align] [table=469][tr][td] [align=center]SCN[sup]-[/sup][/align] [/td][td] [align=center]测定值/[/align] [/td][td] [align=center]平均值/[/align] [/td][td] [align=center]RSD/[/align] [/td][/tr][tr][td] [align=center](μg )[/align] [/td][td] [align=center](A)[/align] [/td][td] [align=center](A)[/align] [/td][td] [align=center]%[/align] [/td][/tr][tr][td] [align=center]0.20[/align] [/td][td] [align=center]0.072,0.074,0.075,0.076,0.078[/align] [/td][td] [align=center]0.075[/align] [/td][td] [align=center]2.98[/align] [/td][/tr][tr][td] [align=center]0.50[/align] [/td][td] [align=center]0.178,0.182,0.183,0.184,0.188[/align] [/td][td] [align=center]0.183[/align] [/td][td] [align=center]1.97[/align] [/td][/tr][tr][td] [align=center]2.00[/align] [/td][td] [align=center]0.807,0.815,0.819,0.824,0.830[/align] [/td][td] [align=center]0.819[/align] [/td][td] [align=center]1.06[/align] [/td][/tr][/table][b]2.10尿样分析及回收试验结果[/b]取8份尿样按实验方法1.2.2操作测定SCN[sup]-[/sup]含量,同时用国家行业标准方法(吡啶-巴比妥酸光度法[sup][/sup])作对照分析,并进行加标回收实验,本法结果与标准方法结果相吻合,加标回收率在90%~104%,见表2。[align=center][b]表2 尿样分析结果[/b][/align] [table=592][tr][td=1,3] [align=left]样品编号[/align] [/td][td=5,1] [align=center]本法结果[/align] [/td][td] [align=center]标准方法结果/[/align] [/td][/tr][tr][td] [align=left]测定结果/[/align] [/td][td] [align=left]本底值/[/align] [/td][td] [align=left]加入量/[/align] [/td][td] [align=left]测定量/[/align] [/td][td] [align=left]回收率/[/align] [/td][td=1,2] [align=center]μg/mL[/align] [/td][/tr][tr][td] [align=center]μg/mL[/align] [/td][td] [align=center]μg[/align] [/td][td] [align=center]μg[/align] [/td][td] [align=center]μg[/align] [/td][td] [align=center]%[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]4.41 [/align] [/td][td] [align=center]0.44[/align] [/td][td] [align=center]1.00[/align] [/td][td] [align=center]1.45[/align] [/td][td] [align=center]101[/align] [/td][td] [align=center]4.19[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]3.56 [/align] [/td][td] [align=center]0.36[/align] [/td][td] [align=center]1.50[/align] [/td][td] [align=center]1.92[/align] [/td][td] [align=center]104[/align] [/td][td] [align=center]3.35[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]8.20 [/align] [/td][td] [align=center]0.82[/align] [/td][td] [align=center]0.50[/align] [/td][td] [align=center]1.30[/align] [/td][td] [align=center]96[/align] [/td][td] [align=center]8.53[/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]10.72 [/align] [/td][td] [align=center]1.07[/align] [/td][td] [align=center]0.20[/align] [/td][td] [align=center]1.25[/align] [/td][td] [align=center]90[/align] [/td][td] [align=center]10.56[/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]6.72 [/align] [/td][td] [align=center]0.67[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]6.74[/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]7.57 [/align] [/td][td] [align=center]0.76[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]7.72[/align] [/td][/tr][tr][td] [align=center]7[/align] [/td][td] [align=center]6.55 [/align] [/td][td] [align=center]0.66[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]6.55[/align] [/td][/tr][tr][td] [align=center]8[/align] [/td][td] [align=center]9.66 [/align] [/td][td] [align=center]0.97[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]9.53[/align] [/td][/tr][/table][b]3结语[/b] 以异烟酸-巴比妥酸为显色剂分光光度法测定微量SCN[sup]-[/sup],方法灵敏度高,选择性及重复性良好,方法操作简便,测定结果准确,所用试剂无毒无害,可用于人尿中微量SCN[sup]-[/sup]的定量分析。[b]参考文献[/b]1 中华人民共和国卫生部.GBZ209-2008职业性急性氰化物中毒诊断标准[s].北京:人民卫生出版社,2008[/s][align=left]2[color=#333333]邵国建,郭和光,余娟.[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法测定尿中硫氰酸盐含量研究[/color][color=#333333],浙江预防医学,2011,23(4):95-96[/color][/align][align=left][url=http://www.istic.ac.cn/suoguan/searchList.htm?indexname=101&text=%E9%92%9F%E8%89%AF%E5%BA%B7&option=101][color=windowtext]3[/color][color=windowtext]钟良康[/color][/url],方波.超短柱顶空[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定尿中硫氰酸盐,[url=http://www.istic.ac.cn/suoguan/searchList.htm?indexname=101&text=%E4%B8%AD%E5%9B%BD%E5%8D%AB%E7%94%9F%E6%A3%80%E9%AA%8C%E6%9D%82%E5%BF%97&option=110][color=windowtext]中国卫生检验杂志[/color][/url],2005,15(5):568,628[/align][align=left]4刘晓宇,云自厚.衍生[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定人尿和唾液中微量硫氰酸根,环境与健康杂志,1994,11(3):130-131[/align]5 冯翠霞,[url=http://www.istic.ac.cn/suoguan/searchList.htm?indexname=101&text=%E6%9E%97%E4%B8%BD%E7%8E%B2&option=101][color=windowtext]林丽玲[/color][/url],[url=http://www.istic.ac.cn/suoguan/searchList.htm?indexname=101&text=%E9%BB%84%E8%BE%89%E6%B6%9B&option=101][color=windowtext]黄辉涛[/color][/url].分光光度法测定尿中硫氰酸盐的异烟酸-吡唑酮,中国职业医学,2009,36(6):501,5046 WS/T39-1996.尿中硫氰酸盐的吡啶-巴比妥酸分光光度测定方法[s].北京:中国标准出版社,19977 蔡秀丽,施逸岚,陈建忠.人尿中硫氰酸盐的快速测定方法,中国卫生检验杂志,2015,25(11):1703-1704,17078 GB/T5750.5-2006.生活饮用水标准检验方法 无机非金属指标[s].北京:中国标准出版社,2007:18-199 全国高等医学院校检验专业专科教材.无机化学.北京:中国医药科技出版社,1990:31-3310 张孙玮,汤福隆,张 泰.现代化学试剂手册第二分册化学分析试剂.北京:化学工业出版社,1987:391-39211 全国中等卫生学校试用教材.临床检验.成都:四川人民出版社,1980:162[/s][/s][align=center][b][color=#333333]Determination of UrineThiocyanate by[/color][/b][/align][align=center][b][color=#333333]Isonicotinic acid [/color][color=#333333]-[/color] barbituric acid[color=#333333]Spectrophotometry[/color][/b][/align][b] [/b][align=center][b]HUANGXuan-zhong WANG Bo SHU Kai-ji ZOU Shao-xian[/b][/align][b] [/b]([b][i]Prevention andHealth Protection Centre of Xingshan County,Hubei,[/i]443711[/b],[b]china)Abstract: [/b]In a weakly acidic solution,and in the presence of chloramine T,[color=#333333]thiocyanate[/color] reacts with iso nicotinicacid -barbituric acid to form purple blue dye.The absorption peck of dye lies 598nm,andits apparent absorptivity is 1.19×10[sup]5[/sup]L· mol[sup]-1[/sup]· cm[sup]-1[/sup],a newspectrophotometry for determination of [color=#333333]thiocyanate[/color]was established.Beer's law is obeyed for[color=#333333]thiocyanate[/color] in the range of 0~2.50μg /5.0mL.The method shows satisfactory selectivity and precisionand has been applied to determine [color=#333333]thiocyanate[/color]in human urine with satisfactory results.[b]Keywords:[/b] [color=#333333]Thiocyanate[/color];Spectrophotometry[b];[/b]Iso Nicotinic Acid;Barbituric Acid

MA监督评审盲样考核之硫氰酸盐分光光度法测定钨精矿中钼的含量一、方法摘要样品经过氧化钠-氢氧化钠熔融,用水浸取,加柠檬酸掩蔽钨,以铜盐为催化剂,在稀硫酸溶液中,用硫脲将钼还原成五价,然后与硫氰酸盐生成桔红色络合物,在波长460nm处用分光光度计测定吸光度,从而计算出样品中钼的含量。二、试剂2.1 过氧化钠(分析纯)2.2 氢氧化钠(分析纯)2.3 5%氢氧化钠溶液2.4 硫酸(分析纯)2.5 硫酸-柠檬酸-硫酸铜混合溶液:称取100g柠檬酸,放入500ml烧杯中,加入200ml去离子水,80ml硫酸,0.1g硫酸铜,用水定容至500ml2.6 硫脲-硫氰酸铵混合溶液:称取40g硫脲,250g硫氰酸铵,用水溶解并定容至500ml2.7 1000 μg/ml钼标准储备溶液2.8 10 μg/ml钼标准溶液:移取10ml标准储备溶液,用5%氢氧化钠溶液定容至1000ml,摇匀2.9 3%硫酸高铁铵:称取3g硫酸高铁铵溶于100ml水中,滴加几滴硫酸三、仪器与设备3.1 电子天平http://ng1.17img.cn/bbsfiles/images/2014/12/201412312148_530719_1657564_3.jpg3.2 UV-2000紫外可见分光光度计(带比色皿)http://ng1.17img.cn/bbsfiles/images/2014/12/201412312157_530726_1657564_3.jpg3.3 高铝坩埚3.4 高温马弗炉http://ng1.17img.cn/bbsfiles/images/2014/12/201412312157_530727_1657564_3.jpg3.5 烧杯3.6 干燥器四、样品消解与分析4.1 样品预先在110°C烘样2小时,于干燥器中冷却至室温4.2 取样量,按下表http://ng1.17img.cn/bbsfiles/images/2014/12/201412312205_530744_1657564_3.png 4.3 样品处理4.3.1 将样品置于30ml高铝坩埚中,加入4g过氧化钠,1g氢氧化钠,充分搅匀后,放入预先升温700°C的马弗炉中熔融20分钟,取出冷却;4.3.2 将坩埚置于预先装有50ml热水的250ml烧杯中,浸取10分钟,用热水洗净坩埚,趁热加入10ml硫酸高铁铵溶液,冷却后移入100ml容量瓶中用水定容至刻度,摇匀。4.3.3 移取(4.3.2)10ml溶液于25ml比色管中,用硫酸-柠檬酸-硫酸铜混合溶液稀释至刻度,混匀;加入1ml硫脲-硫氰酸铵混合溶液,混匀,放置30分钟;4.3.4 随样品做空白、标准物质质控样;4.3.5 将4.3.3所得部分溶液移入2cm比色皿中,以样品空白为参比,在波长460nm处用紫外可见分光光度计测定其吸光度,从工作曲线上查出相应的钼含量。4.4 工作曲线的绘制移取0.00,1.00,2.00,3.00,4.00ml钼标准溶液(2.8),置于一组25ml比色皿中,各补加5%氢氧化钠溶液至10ml,用硫酸-柠檬酸-硫酸铜混合溶液稀释至刻度,混匀;加入1ml硫脲-硫氰酸铵混合溶液,混匀,放置30分钟;将部分溶液移入2cm比色皿中,以试剂空白为参比,于460nm处测定其吸光度。以钼量为横坐标,吸光度为纵坐标,绘制工作曲线。http://ng1.17img.cn/bbsfiles/images/2014/12/201412312139_530716_1657564_3.png4.5 分析结果的计算按下式计算钼的含量http://ng1.17img.cn/bbsfiles/images/2014/12/201412312130_530715_1657564_3.png其中:m1--------从工作曲线查的钼量,μg; V0---------试液总体积,ml; m0--------称取的样品量,g; V1--------分取试液体积,ml。五、结果与讨论http://ng1.17img.cn/bbsfiles/images/2014/12/201412312140_530717_1657564_3.png5.1 我们报出的结果是1.14%,专家组给出的参考值是1.16%,在范围内(允许偏差0.04);5.2 样品烘样2h,否则结果会偏低很多;5.3 显色反应时间不宜太久,最好在1h内测完,否则需重新显色;5.4 比色皿表面要用镜头纸搽干净,否则可能影响其吸光度。
对照品芥子碱硫氰酸盐,喷完显色剂后,烘箱加热,对照品没有点,只有样品跟对照药材。
现有一种样品,理论上硫氰酸根含量应为7.4%左右,考虑纯度的因素,实际值预计为6.0%左右但是目前测试的最大结果仅有4.5%因为样品的可能含有较大量的三乙胺,最初认为是三乙胺干扰检测导致。40摄氏度减压干燥(共计24小时),每3个小时取样测试硫氰酸根含量。结果很不幸的逐步减小(而不是增大)。于是推测不是三乙胺的干扰,那是什么原因?求高手指点~~~~最好能具体的列出可能影响硫氰酸根含量紫外分光光度法检测的影响因素。测试的机理是硫氰酸根与FeCl3络合的反应;或求其它测试硫氰酸根含量的方法。http://simg.instrument.com.cn/bbs/images/brow/em09509.gif
基本实验方法如下:
测氯时用到硫氰酸铵,见它的包装瓶上写着:加酸或加热可产生剧毒物质!我查了一下它的资料:硫氰化物 化 工 词 典 内 容 名称 硫氰酸盐 硫氰化物 thiocyanate thiocyanide rhodanate rhodanide 资料 分子式: CAS号: 性质:又称硫氰化物。含硫氰根离子(SCN)-的化合物。无毒。易与金属离子形成配位化合物。硫氰离子与铁(Ⅲ)离子能形成血红色的配位化合物,常被用于检测硫氰离子和铁(Ⅲ)离子。具有还原性,能与二氧化锰反应生成硫氰(SCN)2。重金属硫氰酸盐均难溶于水。碱金属硫氰酸盐均易溶于水,为常用的试剂,如硫氰酸钾、硫氰酸铵。主要用于印染。这个资料显示硫氰化化物没毒!难道把硫氰酸铵加热或加酸能产生氰化物?[em09509]
做了一个硫氰酸盐,但是碳谱没有看到可能属于SCN-的峰。请问SCN-出现在碳谱中么?峰位大约多少?溶剂CDCl3。谢谢!
98% 储存温度:0℃~8℃ 同时,玛咖科研团队经过长期科研积累,根据玛咖产业发展面向全国开展各项技术服务: http://i05.c.aliimg.com/img/ibank/2014/404/045/1641540404_1639412196.jpg?__r__=1409631792515 玛咖研发技术服务: 玛咖研究中心引领我国玛咖产业发展——玛咖核心技术研究——玛咖良种培育——玛咖标准化种植——采收及深加工——玛咖新型健康产品开发和推广。 核心技术:玛咖良种培育——玛咖标准化种植——玛咖中生物活性成分含量检测分析——玛咖中活性成分浓缩提取制备技术——玛咖生理活性物质作用机理研究——玛咖深加工过程中生物活性成分稳定性研究等。 http://i03.c.aliimg.com/img/ibank/2014/683/551/1659155386_1639412196.jpg?__r__=1409632084109 开展多项技术服务: 玛咖研究中心实现了玛咖中生物活性成分物质,如:玛咖酰胺、玛咖烯、玛咖咪唑生物碱、玛咖苄基芥子油苷、异硫氰酸苄酯类物质等玛咖特征活性物质的结构解析、含量测定、制备技术。 样品品质检测分析: 玛咖生物活性成分:1 玛咖酰胺;2 玛咖烯;3 总芥子油苷;4 挥发油(主要检测异硫氰酸苄酯类物质等);5 玛咖咪唑生物碱;6 甾醇 7 皂苷等 玛咖基础营养成分:1 蛋白质;2 氨基酸(氨基酸总量及水解17种氨基酸比例);3 膳食纤维
各位大神好,我在做莱菔子的含量测定时,用药典的方法采用苯基柱,乙腈-3%醋酸(15:85),与对照品芥子碱硫氰酸盐相近的位置有一个稍微低一点的峰a,分离度不好,然后我调大水相后,峰a没有了,而且水相调的越大,峰面积都逐渐变小,我想问一下,苯基柱会改变峰的多少么,或是对峰面积也会改变么?后来我用C18的柱子按照药典的方法做了一下,也没有那个峰a,调到10:90的时候,分离度达到1.5了 但是峰数特很少,面积也比之前的低,我想问一下能用C18的柱子代替苯基柱么,药典要求用的是苯基柱
食用蔬菜如芥菜、水芹、水芥子及甘兰等含有各种各样的有机异硫氰酸盐(-N=C=S,ITC)类,经证明它们都有抑制化学致癌作用。此外也证明许多ITC能在体内抑制致癌物在肺、胃、结肠、肝、食管、膀胱及乳腺诱导肿瘤的生成。ITC的化学预防性能是因它能在致癌过程中打断多个步骤,如抑制致癌物激活酶、诱导致癌物去毒素酶及诱导癌细胞的细胞凋亡与细胞周期停止。芬兰的研究人员报告说,发酵的卷心菜,又名为德国泡菜,它要比生的或者是烹制过的卷心菜更加符合健康要求。研究人员发现,卷心菜在发酵后能够产生多种不同的化合物,被称为异硫氰酸盐。在试验室和动物实验中已经证实能够预防肿瘤的生长,尤其是对乳腺癌、结肠癌、肺癌和肝癌。许多食物中都含有异硫氰酸盐,其中也包括十字花科蔬菜,比如说花茎甘蓝、芽甘蓝等。ITC除了阻断化学致癌作用外,还有潜力在培养的人癌细胞系列中诱导细胞凋亡和细胞周期停止而成为治疗癌症的药物。烯丙基ITC(AITC)腹腔内注射后能抑制小鼠的人前列腺癌异种移植物的生长。有趣的是,苯乙基ITC(PEITC)或其半胱氨酸轭合物三小时即可最大程度地抑制人白血病细胞的生长,提示与细胞靶位的快速相互作用。故在体内PEITC的抗癌活性大部分不会受到这类化合物快速处理动力学的影响。研究人员报告了AITC、PEITC或苯甲基ITC以不受时间影响的方式抑制一系列癌细胞,如血液(HL60/S及8226/S)、乳腺(MCF-7)、肝脏(HepG2)、结肠(HT-29)及皮肤(HaCaT)的增殖。这一发现是有意义的,因ITC进入人体后很快从尿中排出。在白血病HL60/5细胞中,发现AITC及BITC能调节增殖的多个细胞靶位,包括破坏线粒体膜电位,激活多种caspase,停止细胞周期进展及诱导细胞分化。这些发现提示选出的ITC能很快同时调节多个细胞靶位而启动抑制癌细胞的生长,它们抑制生长的活性可能不会因体内代谢及处理因素而受到很大的影响。口服异硫氰酸盐(ITCs)对于肿瘤的预防有一定的作用,十字花科的蔬菜富含ITCs,结合食疗亦值得关注。许多致癌化合物在体内经细胞色素酶P450激活后发挥作用,而ITCs则可抑制此种激活作用。例如苯乙异硫氰酸盐(PEITC)便可抑制细胞色素酶IAZ。ITCs的毒性在毒性研究中,虽然曾发现ITCs也具有较弱的致突变作用,且在某些动物实验中可促进肿瘤的出现,但所需剂量较大。人类膳食中摄入的ITCs量较小,所以是安全的。
品名氢氰酸 Hydrocyanic acid Prussic acid CAS:74-90-8 理化性质为无色伴有轻微的苦杏仁气味的液体, 分子式C-H-N。分子量27.03。相对 密度0.69。熔点 -14℃。沸点 26℃。闪点 -17.8℃。 蒸气密度 0.94。蒸气压101.31kPa(760mmHg, 25.8℃)。 蒸气与空气混合物爆炸限6~41% 。易溶于水、乙醇 微溶于乙醚。水溶液呈弱酸性。 侵入途径主要经口或吸入致中毒。液体可经皮肤及眼结膜吸收致中毒。毒理学简介可经各种途径吸收入人体。如吸收非致死量,部分以原形呼出; 大部分氰 离子可逐渐从体内细胞色素氧化酶或从高铁血红蛋白的结合中释出, 在体内硫氰酸的作用下与体内的硫代硫酸离子结合而转化为相 对无毒的硫氰酸盐从尿中排泄。 毒性数据人口服LDLo: 570μg/kg 人吸入TCL0: 500mg/m^33min 人吸入LCLo: 120mg/m^3h, 200mg/m^310min, 400mg/m^32min, 300mg/m^3, 立即死亡 人皮下LDLo:1mg/kg 人静注TDLo: 55μg/kg。皮肤吸收蒸气6760mg/m^3, 50分钟,无症状 1230mg/m^3 浓度下发生吸收。嗅觉阈为0.22~5.71mg/m^3。20~40mg/m^3下,几小时后出现轻度症状,如头痛、恶心、呕吐、心悸等。IDLH:+50 ppm [R30] 发病机理: 主要为氰离子与氧化型细胞色素氧化酶中的三价铁结合, 阻断了氧化过程中三价铁的电子传递,使组织细胞不能利用氧,形成内窒息。 临床表现主要引起机体组织内窒息。 急性中毒病情进展迅速,无明显潜伏期。一般病情危重。吸入高浓度氰化氢或口服多量氢氰酸后立即昏迷、呼吸停止,于数分钟内死亡(猝死)。重症而非猝死病例: 早期症状,吸入者有眼和上呼吸道刺激症状, 呼出气带杏仁气味 口服者有口腔、咽喉灼热感、流延、呕吐,呕出物有杏仁气味。并有头痛、头晕、胸闷、呼吸加深加快、 血压升高、 心悸、脉率加快、皮肤及粘膜呈鲜红色。后有胸部压迫感、 呼吸困难、意识朦胧。 继而抽搐、 昏迷、 呼吸减慢、 血压下降、 紫绀、 全身肌肉松弛、 呼吸停止、脉搏弱而不规则、 心跳停止、 死亡。静脉血呈鲜红色。尿硫氰酸盐量可增高。轻症者可有头痛、 头晕、 乏力、胸闷、呼吸困难、心悸、恶心、呕吐等表现。皮肤或眼接触氢氰酸可引起灼伤。亦可吸收致中毒。诊断原则与鉴别诊断:主要根据接触史及临床表现, 中毒早期呼出气或呕吐物中有杏仁气味,皮肤、粘膜及静脉血呈鲜红色为特征, 有助诊断, 但呼吸障碍时可出现紫绀。血及尿中硫氰酸盐量可作为接触指标, 其受吸烟及饮食影响, 应参考当地正常值。中毒时起病急, 不能等化验结果才作诊断。应与其他原因引起的中毒、脑血管疾病、心肌梗塞等所致的猝死或昏迷相鉴别。 处理一般治疗原则:立即脱离现场至空气新鲜处。 猝死者应同时立即进行心肺脑复苏。急性中毒病情进展迅速,应立即就地应用解毒剂。吸入者给吸氧。皮肤接触液体者立即脱去污染的衣着,用流动清水或5%硫代硫酸钠冲洗皮肤至少20分钟。 眼接触者用生理盐水、 冷开水或清水冲洗5~10分钟。口服者用 0.2%高锰酸钾或 5%硫代硫酸钠洗胃。皮肤或眼灼伤按酸灼伤处理。 标准车间空气卫生标准: 中国 MAC 0.3mg/m^3 (皮) 美国 OSHA PEL-TWA 氢氰酸 11mg/m^3(皮), 危规: 氢氰酸:GB 6,1类 61004。原铁规: 无机剧毒品, 81005。UN NO.1613。IMDG CODE 6092页, 6.1 类。
建立气相色谱-质谱选择离子检测土壤中痕量芥子气的方法。该方法采用二氯甲烷萃取土壤中的芥子气,萃取液经净化、浓缩,加入内标丁基硫醚后进行分析,可实现对土壤中0.02mg/kg芥子气的定量检出,且加标回收率大于70%,相对标准偏差小于10%。
氢氰酸 品名氢氰酸 Hydrocyanic acid Prussic acid CAS:74-90-8 理化性质为无色伴有轻微的苦杏仁气味的液体, 分子式C-H-N。分子量27.03。相对 密度0.69。熔点 -14℃。沸点 26℃。闪点 -17.8℃。 蒸气密度 0.94。蒸气压101.31kPa(760mmHg, 25.8℃)。 蒸气与空气混合物爆炸限6~41% 。易溶于水、乙醇 微溶于乙醚。水溶液呈弱酸性。 侵入途径主要经口或吸入致中毒。液体可经皮肤及眼结膜吸收致中毒。毒理学简介可经各种途径吸收入人体。如吸收非致死量,部分以原形呼出; 大部分氰 离子可逐渐从体内细胞色素氧化酶或从高铁血红蛋白的结合中释出, 在体内硫氰酸的作用下与体内的硫代硫酸离子结合而转化为相 对无毒的硫氰酸盐从尿中排泄。 毒性数据人口服LDLo: 570μg/kg 人吸入TCL0: 500mg/m^33min 人吸入LCLo: 120mg/m^3h, 200mg/m^310min, 400mg/m^32min, 300mg/m^3, 立即死亡 人皮下LDLo:1mg/kg 人静注TDLo: 55μg/kg。皮肤吸收蒸气6760mg/m^3, 50分钟,无症状 1230mg/m^3 浓度下发生吸收。嗅觉阈为0.22~5.71mg/m^3。20~40mg/m^3下,几小时后出现轻度症状,如头痛、恶心、呕吐、心悸等。IDLH:+50 ppm [R30] 发病机理: 主要为氰离子与氧化型细胞色素氧化酶中的三价铁结合, 阻断了氧化过程中三价铁的电子传递,使组织细胞不能利用氧,形成内窒息。 临床表现主要引起机体组织内窒息。 急性中毒病情进展迅速,无明显潜伏期。一般病情危重。吸入高浓度氰化氢或口服多量氢氰酸后立即昏迷、呼吸停止,于数分钟内死亡(猝死)。重症而非猝死病例: 早期症状,吸入者有眼和上呼吸道刺激症状, 呼出气带杏仁气味 口服者有口腔、咽喉灼热感、流延、呕吐,呕出物有杏仁气味。并有头痛、头晕、胸闷、呼吸加深加快、 血压升高、 心悸、脉率加快、皮肤及粘膜呈鲜红色。后有胸部压迫感、 呼吸困难、意识朦胧。 继而抽搐、 昏迷、 呼吸减慢、 血压下降、 紫绀、 全身肌肉松弛、 呼吸停止、脉搏弱而不规则、 心跳停止、 死亡。静脉血呈鲜红色。尿硫氰酸盐量可增高。轻症者可有头痛、 头晕、 乏力、胸闷、呼吸困难、心悸、恶心、呕吐等表现。皮肤或眼接触氢氰酸可引起灼伤。亦可吸收致中毒。诊断原则与鉴别诊断:主要根据接触史及临床表现, 中毒早期呼出气或呕吐物中有杏仁气味,皮肤、粘膜及静脉血呈鲜红色为特征, 有助诊断, 但呼吸障碍时可出现紫绀。血及尿中硫氰酸盐量可作为接触指标, 其受吸烟及饮食影响, 应参考当地正常值。中毒时起病急, 不能等化验结果才作诊断。应与其他原因引起的中毒、脑血管疾病、心肌梗塞等所致的猝死或昏迷相鉴别。 处理一般治疗原则:立即脱离现场至空气新鲜处。 猝死者应同时立即进行心肺脑复苏。急性中毒病情进展迅速,应立即就地应用解毒剂。吸入者给吸氧。皮肤接触液体者立即脱去污染的衣着,用流动清水或5%硫代硫酸钠冲洗皮肤至少20分钟。 眼接触者用生理盐水、 冷开水或清水冲洗5~10分钟。口服者用 0.2%高锰酸钾或 5%硫代硫酸钠洗胃。皮肤或眼灼伤按酸灼伤处理。 标准车间空气卫生标准: 中国 MAC 0.3mg/m^3 (皮) 美国 OSHA PEL-TWA 氢氰酸 11mg/m^3(皮), 危规: 氢氰酸:GB 6,1类 61004。原铁规: 无机剧毒品, 81005。UN NO.1613。IMDG CODE 6092页, 6.1 类。