
问题:用waters测有机酸时,柠檬酸和琥珀酸的出峰时间接近,峰型分不开。描述:流动相为95% 5mM H2SO4 + 5% 甲醇,流速0.4ml/min。测定五种有机酸(草酸,苹果酸,柠檬酸,琥珀酸和富马酸)。样品和标品均用超纯水溶解。之前一直用这个体系,混标能出现5个分离的峰,可是现在变成四个了,发现是柠檬酸和琥珀酸混一起了。这个问题该怎么解决?所有药品和流动相均重新配制也还是不能分离开柠檬酸和琥珀酸。柱子是伊力特Hypersil BDS C18, 4.0×150mm下图是第一次做,分离得很好的[img=这是五个峰都分离好的,690,297]https://ng1.17img.cn/bbsfiles/images/2018/10/201810111449075618_7115_3220400_3.jpg!w690x297.jpg[/img]之后即使把流速换成0.2ml/min,也没分离开[img=没分离开,690,231]https://ng1.17img.cn/bbsfiles/images/2018/10/201810111451090611_9280_3220400_3.jpg!w690x231.jpg[/img]
[color=#444444]本人最近按2015版药典做了一个药用辅料-醋酸羟丙甲纤维素琥珀酸酯的的游离乙酸的含量测定实验。实验过程如下:[/color][color=#444444] 游离乙酸、琥珀酸 取本品0.102g,精密称定,置锥形瓶中,精密加入磷酸盐溶液(取0.02mol/L磷酸二氢钾溶液,用1mol/L氢氧化钠溶液调pH值至7.5)4.0ml,搅拌2小时,加磷酸溶液(取1.25mol/L磷酸1ml,置50ml量瓶中,加水稀释至刻度,摇匀)4.0ml,强力振摇,离心,上清液作为供试品溶液;精密称取琥珀酸0.13g,置100ml量瓶中,加水适量,振摇使完全溶解,加水至刻度,摇匀,作为琥珀酸贮备液;取加有水20ml的100ml量瓶,称重,精密加入冰乙酸2ml,再称重,用水稀释至刻度,摇匀,精密量取6ml,置100ml量瓶中,用水稀释至刻度,摇匀,作为乙酸贮备溶液;精密量取乙酸贮备液和琥珀酸贮备液各4.0ml,置同一25ml量瓶中,用流动相稀释至刻度,摇匀,作为对照溶液。照高效液相色谱法(中国药典2015年版四部通则0512)试验。以十八烷基硅烷键合硅胶为填充剂,以0.02moI/L磷酸二氢钾溶液(用6mol/L磷酸溶液调pH值至2.8)为流动相,流速每分钟1ml,检测波长为215nm。取对照溶液10μl, 注入液相色谱仪,按琥珀酸峰计算,理论板数不得少于8000。取供试品溶液与对照溶液各10μl,注入液相色谱仪,按干燥品计算,游离乙酸和琥珀酸总量不得过1.0%。[/color][color=#444444]计算公式: 游离乙酸含量=0.0768(WA/(W(1-干燥失重)))(γUA/γSA)[/color][color=#444444] 式中 WA为乙酸贮备溶液中冰乙酸量,mg;[/color][color=#444444] W为供试品的取样量,mg;[/color][color=#444444] γUA、γSA为供试品溶液、对照溶液中乙酸的峰面积。[/color][color=#444444] 游离琥珀酸含量=1.28(WS/(WUS(1-干燥失重)))(γUS/γSS)[/color][color=#444444] 式中 WS为琥珀酸贮备液中琥珀酸量,mg;[/color][color=#444444] WUS为供试品取样量,mg;[/color][color=#444444] γUS、γSS为供试品溶液、对照溶液琥珀酸的峰面积。[/color][color=#444444]我的问题是,根据“干燥品计算,游离乙酸和琥珀酸总量不得过1.0%”这句话,游离乙酸含量的最后计算的结果要不要乘以100%,比如我最后计算结果是0.0139,如果这个结果再乘以100%,就变为1.39%,从而超过限度,那么就需要重新做实验复核一遍。[/color]

作为中华民族的伟大创造之一,中药既可以治病,也可以养生。皮肤敏感的你,是否钟情于副作用小的中药护肤品呢?注重健康的你,也曾留恋于养生馆的中药保养吗?作为爱吃的你,肯定钟意于中药美食的扑鼻清香吧?日常生活中几乎每个人都会与中草药发生联系,做菜、泡茶、泡酒、足浴、美容等方面总会有中草药的影子。那么中药中的有效成分如何检测呢?就以半夏中琥珀酸含量测定为例。 半夏(学名:Pinellia ternata),又名地文、守田等,属天南星目。广泛分布于中国长江流域以及东北、华北等地区。药用植物,具有燥湿化痰,降逆止呕,生用消疖肿作用,兽医用以治锁喉癀。且研究表明,半夏中的琥珀酸有止咳平喘的作用,这与半夏的作用基本一致。我们根据中国药典的规定,采用电位滴定法对半夏中琥珀酸的含量进行了检测,结果如下:http://ng1.17img.cn/bbsfiles/images/2017/01/201701191701_669817_3134100_3.png1.参考文献《中华人民共和国药典》2015年版第一部。 http://ng1.17img.cn/bbsfiles/images/2017/10/2016083016063176_01_3134100_3.png 2.实验仪器与试剂 T860电位滴定仪,PH复合电极,无水乙醇,氢氧化钠溶液:c(NaOH)=0.1mol/L,滴定剂:c(HCl)=0.1mol/L,待测半夏样品3.实验步骤 电位滴定仪清洗完毕,精密称取样品粉末5g左右,至锥形瓶中,加乙醇50ml,加热回流1小时,同上操作,再重复提取2次,放冷,滤过,合并滤液,蒸干,残渣精密加入氢氧化钠滴定液(0.1mol/l)10ml,超声处理(功率500W频率40khz)30分钟,转移至100ml容量瓶中,加纯化水溶解至刻度,摇匀,精密量取40ml至滴定杯中,加水40ml,用盐酸滴定液(0.1mol/l)进行电位滴定至终点,并将滴定结果用空白实验校正。4.测试结果1)T860电位滴定仪参数设置:常量滴定 终点数:1结束体积:15.000ml终点突跃量:300.0添加最小体积:0.020ml 初次添加体积:0.050ml http://ng1.17img.cn/bbsfiles/images/2017/10/2016083016071206_01_3134100_3.png2)实验结果空白体积:3.575ml滴定剂浓度:c(NaOH)=0.100mol/L编号 m(g)V(ml)E’E(mv)琥珀酸含量(%)平均含量(%)样品15.021192.611600-61.90.28340.28402.592515-76.90.2890样品25.044172.586500-87.00.28942.620515-64.70.2794样品35.025622.624610-79.40.27932.609605-80.90.28373)曲线图谱 http://ng1.17img.cn/bbsfiles/images/2017/10/2016083016102712_01_3134100_3.png图一http://ng1.17img.cn/bbsfiles/images/2017/10/2016083016111018_01_3134100_3.png图二5.讨论 半夏中琥珀酸平均含量为0.28%,合格(中国药典规定不得少于0.25%)。采用电位滴定法测定半夏药材中琥珀酸含量简便、快捷,可以省时省力,
发愁,求问,有木有人知道琥珀酸生育酚的沸点到底是多少啊?到处都查不到呢。
[color=#333333]求助各位高手帮帮忙,最近在做醋酸纤维素琥珀酸酯乙酸的检测,按照[/color][color=#333333]2015[/color][color=#333333]版药典方法检测,出峰的时候发现琥珀酸有两个峰出现,不知道是什么原因,琥珀酸的对照买的是麦克林公司的试剂,纯度也都在[/color][color=#333333]99.5%[/color]

【中文名称】琥珀酸柠檬酸铁钠;丁二酸亚铁合枸橼酸钠【英文名称】ferrous succinate sodium citrate;sodium ferricsuccinate citrate【结构或分子式】 http://ng1.17img.cn/bbsfiles/images/2012/04/201204192020_362339_1855403_3.jpg【毒性LD50(mg/kg)】 大鼠经口2200【性状】 青白至微带绿色的白色粉末,无臭,有微弱的铁味。有绿色的荧光。【溶解情况】 易溶于热水,溶液呈中性并显黄绿色,不溶于乙醇及其他有机溶剂。【用途】 用作食品的铁强化剂或饲料添加剂,用于调制奶粉、离乳食品以及缺铁病人、孕妇和产妇等食品的强化。【制备或来源】 用柠檬酸、琥珀酸、硫酸亚铁、碳酸钠溶液为原料制得。【其他】 略
[color=#333333]求助各位高手帮帮忙,最近在做醋酸纤维素琥珀酸酯乙酸的检测,按照2015版药典方法检测,出峰的时候发现琥珀酸有两个峰出现,不知道是什么原因,琥珀酸的对照买的是麦克林公司的试剂,纯度也都在99.5%。[/color][color=#333333][/color]
最近测的环氧琥珀酸和酒石酸总是一个出峰时间这是怎么回事?我用的是0.02M磷酸氢二钾PH2.6的流动相,波长210nm
查了很多资料,好像没有使用液相单独测定琥珀酸的含量,一般都是测定有机酸的(同时测定几种有机酸,其中包括琥珀酸)。今天我按照参考文献做了琥珀酸的测定。条件如下色谱柱:Shimadzu C18柱(5um粒径 250×4.6mm)流动相:5% CH3OH – 0.10 mol/ L KH2PO4(pH 3.0)缓冲溶液(V/ V)流速:1 mL/ min 柱箱温度:室温(22 ±2 ℃) 检测波长:215 nm进样量:20μL资料说此条件下琥珀酸的保留时间为7-8min,线性范围0-600ug/mL.今天分别进了1mg/L,10mg/L的标样,可是20min内一直不出峰,怀疑是标样的浓度太低,后来又进了1mg/mL 的标样,结果20mi内仍然不出峰。(我是新手,当时没有继续延长时间.....)我以为此方法测不出来,后来用甲醇冲洗柱子时在60min左右出现了几个很大的峰。 我不知道是我的标样琥珀酸的峰,还是其他的物质?? 比如柱子里的其他残留物? 不过我觉得进样前柱子已经冲洗干净了哪位大侠测过琥珀酸的,能不能给些指导? 液相是不是不适合低或是微含量琥珀的测定。先跪谢 @ 哭谢!!
请问乙二胺二琥珀酸(EDDS)怎么溶解,有没有人知道,感觉在水中不溶
各位朋友好,我想用毛细管电泳测定苹果酸、柠檬酸、草酸、琥珀酸等有机酸,所用电源为正电压(0-30KV),总是不出峰。查文献,测定以上各酸都是负电源,缓冲溶液中一般加了阳离子表面活性剂。另有一些文献如测定水杨酸、丁香酸、苯甲酸、咖啡酸、儿茶酸、绿原酸等有机酸的电源为正电源,缓冲溶液中一般加了阴离子表面活性剂。我们实验室只有正电源,能不能测定苹果酸、柠檬酸、草酸、琥珀酸等酸呢?不都是酸吗,用正电源,阴离子表面活性剂能否分离苹果酸、柠檬酸、草酸、琥珀酸等酸呢?
我需要药品[S,S]-EDDS,中文名是乙二胺二琥珀酸,请与我联系bluebell22@tom.com
[color=#333333]请问喹乙醇半琥珀酸酯做质谱的条件要怎样设置?[/color]
酒石酸、琥珀酸、乳酸色谱级的哪个厂家的好?[img]http://simg.instrument.com.cn/bbs/images/brow/em09511.gif[/img]谢谢啊

[color=#444444]各位大神帮帮忙,高效液相色谱测琥珀酸出现两个峰是怎么回事啊?测定条件是:0.01mol/ L KH2PO4(pH2.9)∶乙腈(98∶2)缓冲溶液为流动相, 控制流速为 1mL/min, 柱温 25 ℃, 检测波长 213 nm, 进样量 20 μL[/color][color=#444444][img=,690,181]https://ng1.17img.cn/bbsfiles/images/2019/08/201908051544510458_9969_1827556_3.png!w690x181.jpg[/img][/color]
食品安全国家标准 食品营养强化剂 维生素E琥珀酸钙
【序号】:1【作者】: 张雅伦【题名】:聚乙二醇的N-羟基琥珀酰亚胺琥珀酸酯的合成工艺、苏氨酸负载及催化应用【期刊】:兰州大学【年、卷、期、起止页码】:2017【全文链接】:https://kns.cnki.net/kcms2/article/abstract?v=3uoqIhG8C475KOm_zrgu4lQARvep2SAkOTSE1G1uB0_um8HHdEYmZhkBIZJEK02VaOdneXeYijuWwpOfpIhlJTd0mjIpAyz7&uniplatform=NZKPT
为规范琥珀酸舒马普坦口服制剂说明书,确保患者用药安全,日前,国家食品药品监督管理局对琥珀酸舒马普坦片剂和胶囊剂说明书进行修订,并要求各省(区、市)食品药品监督管理部门通知辖区内药品生产企业按照说明书样稿尽快修订说明书和标签,同时将修订的内容及时通知相关医疗机构、药品经营企业等单位。

条件:thermo液相;[font=宋体]色谱柱为[/font][font='Times New Roman','serif']Phenomenex Luna 5 μm C[sub]18[/sub][/font][font=宋体]([/font][font='Times New Roman','serif']2[/font][font=宋体])([/font][font='Times New Roman','serif']250 mm×4.6 mm[/font][font=宋体]);[/font][font=宋体]波长[/font]210nm[font=宋体]。流动相为A[font=宋体]磷酸二氢钾[/font]-[font=宋体]磷酸缓冲液([/font]pH2.3[font=宋体])-B[font=宋体]甲醇。[/font][/font][/font][font=宋体]结果如下,前边不是有小峰就是有包;而且我配的浓度都在2mg/ml左右,但是色谱峰高度很小。[/font][font=宋体]我在想是不是琥珀酸和流动相的盐反应了,求助大家[/font][font=宋体][img=,654,308]https://ng1.17img.cn/bbsfiles/images/2021/04/202104291002509746_2833_5257820_3.png!w654x308.jpg[/img][img=,654,308]https://ng1.17img.cn/bbsfiles/images/2021/04/202104291002555122_5886_5257820_3.png!w654x308.jpg[/img][/font]
请问专家:我急需要做黑索今(三次甲基三硝胺,一种六元环形化合物的高能炸药,环上带3个硝基)的粒度分布,用的分散剂是二辛基琥珀酸磺酸钠,分散介质用的是水,平行结果不好,请问有没有什么合适的分散剂和分散介质?-我用的是美国库尔特公司的LS-230激光粒度仪。——盼回复,不胜感激!
pH4.5的琥珀酸钠缓冲液怎么样配制?
[color=#3333ff]请问:[/color][color=#3333ff]日本药典标准里面的 醋酸羟丙甲纤维素琥珀酸酯 的质量标准中,(如下为标准的译文)[/color](2)游离醋酸以及游离琥珀酸 精密称量本品约0.1g,准确加入pH7.5的0.02mol/L磷酸盐缓冲液4mL,盖紧瓶盖,搅拌2小时。准确添加稀释后的磷酸(1→500)4mL,数次倒置振摇混合。对该溶液进行离心分离,取上清液作为供试溶液。另将20mL水放入100mL的量瓶中,精密称量其质量,加入2.0mL醋酸(100),精密称量其质量,计算出醋酸(100)的质量,再加入水,使其达到100mL。准确称量6mL该溶液,加水使其达到100mL,制成醋酸原液。接下来,精密称量大约0.13g的琥珀酸,溶解于水中,使之达到100mL,作为琥珀酸原液。准确称量4mL醋酸原液以及4mL琥珀酸原液,添加流动相,使之达到25mL,作为标准溶液。准确量取供试溶液以及标准溶液各10μL,在下述条件下根据液相色谱法进行试验,测定各个液体的醋酸以及琥珀酸的峰面积A[sub]TA[/sub]、A[sub]TS[/sub]以及A[sub]SA[/sub]、A[sub]SS[/sub],根据以下公式求出游离醋酸和游离琥珀酸的量,其总量不得超过1.0%。游离醋酸(C[sub]2[/sub]H[sub]4[/sub]O[sub]2[/sub])的量(%) =M[sub]SA[/sub]/M[sub]T [/sub]× A[sub]TA[/sub]/A[sub]SA [/sub]× 48/625游离琥珀酸(C[sub]4[/sub]H[sub]6[/sub]O[sub]4[/sub])的量(%) =M[sub]SS[/sub]/M[sub]T[/sub] × A[sub]TS[/sub]/A[sub]SS[/sub] ×32/25M[sub]SA[/sub]:醋酸(100)的称取量(mg)M[sub]SS[/sub]:琥珀酸的称取量(mg)M[sub]T[/sub]:换算成干燥品之后的本品的称取量(mg)[color=#3333ff]计算公式中的48/625和32/25是怎么得来的啊?[/color][color=#3333ff]请各位帮忙讨论一下,不甚感激。[/color]
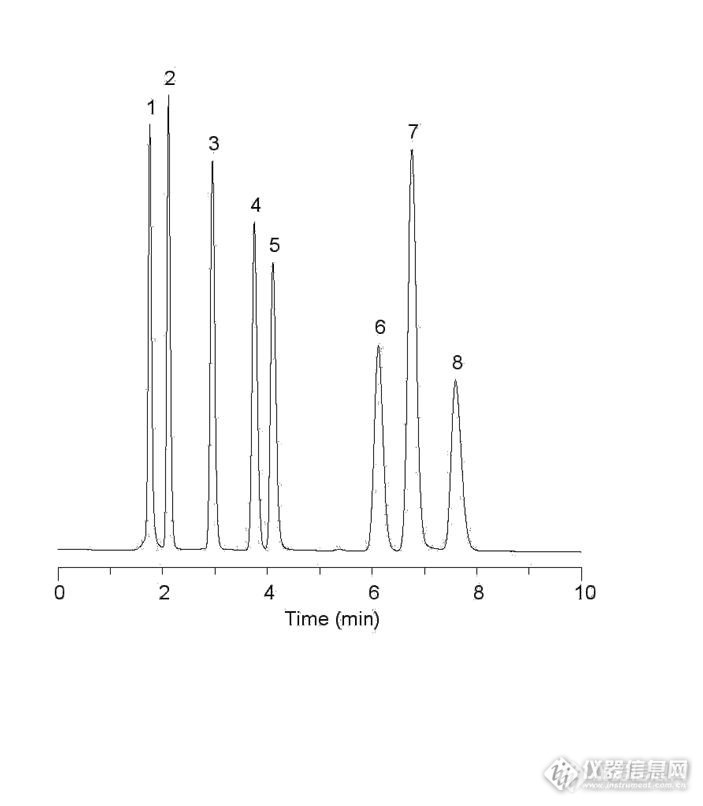
有机酸分析有机酸是一类典型的可解离型有机化合物,通常具有较高的水溶性,它们的相对分子量处于几十~几百之间,因而色谱柱可以锁定在离子抑制色谱、离子对色谱或离子交换色谱,其中前两种用的均是反相色谱柱。分析这类物质时,离子抑制色谱法是最常用的方法。由于羧基的存在,有机酸的极性较强,为了使这类物质能被反相柱保留,流动相中会有较大比例的水,有时甚至用到100%水溶液;然而在水介质中有机酸会部分解离,每一种纯净物都会以两种甚至两种以上的形式存在,这是造成有机酸峰形变差的根本原因。解决办法就是将流动相的pH值设定为酸性,以抑制羧基的解离,这样化合物以单一的未解离形式存在,疏水性增强,在反相柱上的保留也增大。pH值可参考解离性最强的有机酸的pKa,通常流动相pH值比该化合物的pKa小一个数量级,就能使每种化合物得到比较完美的峰形。下面为迪马应用实验室做到一个具体应用:迪马实验室 2012-06-06基质:标准溶液应用编号:101837化合物:1. 草酸(Oxalic acid) 2. 酒石酸(Tartaric acid) 3. 苹果酸(Malic acid) 4. 乳酸(Lactic acid) 5. 乙酸(Acetic acid) 6. 柠檬酸(Citric acid) 7. 富马酸(Fumaric acid) 8. 琥珀酸(Succinic acid)色谱柱:Inspire C18,150×4.6 mm, 5 μm (Cat#:81001)流动相:25 mM KH2PO4, pH 2.5 流 速:1.0 mL/min柱 温:室温检测器:UV 210 nm 进样量:10 μL文章出处:迪马实验室http://ng1.17img.cn/bbsfiles/images/2015/05/201505181732_546585_2452211_3.jpg图例:1. 草酸(Oxalic acid) 2. 酒石酸(Tartaric acid) 3. 苹果酸(Malic acid) 4. 乳酸(Lactic acid) 5. 乙酸(Acetic acid) 6. 柠檬酸(Citric acid) 7. 富马酸(Fumaric acid) 8. 琥珀酸(Succinic acid)
我用waters专门测酸的柱子,检测苹果酸和琥珀酸,单标还有峰,但是混标峰都分不开,只有一个大峰,流动相用的是0.01,0.02,0.03mol硫酸都试过了,结果都一样,测样品也是峰分不开,是什么原因啊
各位老师好,本人现有IC-600一台,阴离子分离柱为AS23,现欲分离测试以下种类的离子与有机酸,请问现在设备可以最大限度的测试多少种?若欲测试所有的种类还需要哪些设备?或是其他设备,只要能完成分离检测出以下的离子种类,请各位不吝赐教? [table=218][tr][td]锂离子[/td][td]lithium[/td][/tr][tr][td]钠离子[/td][td]sodium[/td][/tr][tr][td]铵离子[/td][td]ammonium[/td][/tr][tr][td]钾离子[/td][td]potassium [/td][/tr][tr][td]镁离子[/td][td]magnesium[/td][/tr][tr][td]钙离子[/td][td]calcium [/td][/tr][tr][td]氟离子[/td][td]fluoride [/td][/tr][tr][td]氯离子[/td][td]chloride[/td][/tr][tr][td]亚硝酸根[/td][td]nitrite[/td][/tr][tr][td]溴离子[/td][td]bromide[/td][/tr][tr][td]硝酸根[/td][td]nitrate[/td][/tr][tr][td]硫酸根[/td][td]sulfate[/td][/tr][tr][td]磷酸根[/td][td]phosphate[/td][/tr][tr][td]甲酸[/td][td]formate [/td][/tr][tr][td]乙酸[/td][td]acetate [/td][/tr][tr][td]柠檬酸盐[/td][td]Citrate[/td][/tr][tr][td] 邻苯二甲酸盐[/td][td]Phthalate [/td][/tr][tr][td]谷氨酸盐[/td][td]Glutamate[/td][/tr][tr][td]苯六甲酸盐[/td][td]Mellate[/td][/tr][tr][td]甲磺酸盐[/td][td]Methane Sulfate[/td][/tr][tr][td]琥珀酸盐[/td][td]Succinate[/td][/tr][/table]
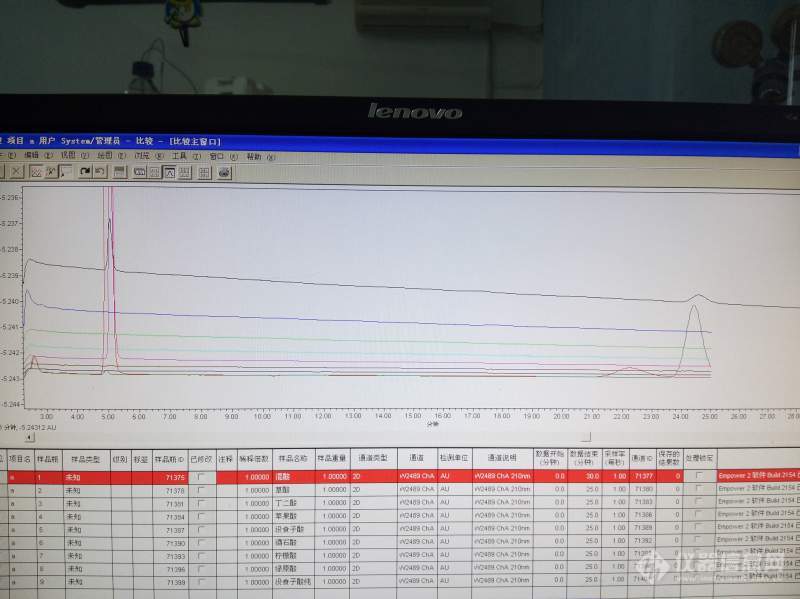
[color=#444444]现在用高效液相色谱紫外测定几种有机酸(草酸、柠檬酸、没食子酸、琥珀酸、苹果酸、绿原酸等),参照文献方法测定,结果都没出峰。用的机子是water2695带紫外,色谱条件是色谱柱安捷伦sb-C18,250cm,流动相是乙腈:0.02moL/L磷酸二氢钾=5:95,ph为2.6,然后调过缓冲液的ph值2.8、3.0,都不出峰。不知道有哪位同仁有做过有机酸的测定。目前是只有安捷伦sb-C18,250cm这么一根柱子,没有其他的柱子了[/color][color=#444444][img=,690,516]https://ng1.17img.cn/bbsfiles/images/2019/08/201908051108362215_8982_1827556_3.jpg!w690x516.jpg[/img][/color]
我可以把发酵液的样品萃取,干燥之后寄样,然后你们按照你们那的有机酸测定条件溶解样品测,这样可以吗?我的发酵液是大肠杆菌发酵之后的上清液,未萃取时,主要成分是葡萄糖、乙酸、甲酸、琥珀酸、苹果酸等有机酸等。不萃取可以直接测吗?我主要要测的参数是乙酸含量,琥珀酸含量,但是如果其他的有机酸能测出来更好。测样的价格合理就行,价钱不是啥问题。
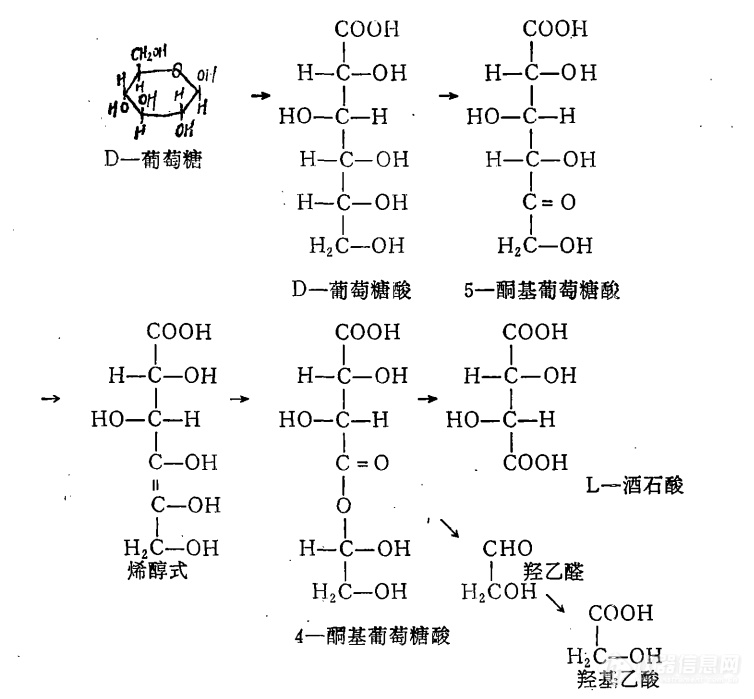
闫丽洁[align=center]关于食品添加剂L(+)-酒石酸的研究[/align]摘要:[size=13px]L(+)-酒石酸是一种天然有机酸,它的酸味值约是柠檬酸的1.25倍,可用于清凉饮料,它和柠檬酸、氧化亚铁产生鲜绿色作为食用色素用于糕点。本文主要介绍了L(+)-酒石酸的检测方法及生产方法。[/size]关键词:[size=13px]L(+)-酒石酸,检测,生产[/size]1 引言L(+)-酒石酸广泛存在与自然界的多种植物果实中,其中成熟葡萄中L-酒石酸含量较多。L-酒石酸时一种用途非常广泛的天然有机酸,主要作为食品添加剂和医药拆分剂应用于食品、医药和化学工业等领域,据报道,L-酒石酸还可以用于纳米材料的制备及作为染料经济性改性剂和抗磨剂。2 L(+)-酒石酸简介2.1 L(+)-酒石酸基本结构L(+)-酒石酸又称为L(+)-2,3-二羟基丁二酸,分子式是C4H6O6,结构简式HOOCCH(OH)CH(OH)COOH。有两个不对称的碳原子,有3个立体异构体,即:右旋型(D型,L型)、左旋型(L型,D型)、内消旋型。通常,外消旋型酒石酸又称为葡萄酸。右旋型酒石酸以游离的或K盐、 Ca盐、Mg盐的形态广泛分布于高等植物中,特别是多存在与果实和叶中。2.2 L(+)-酒石酸的发现酒石酸氢钾存在与葡萄汁中,此盐难溶于水和乙醇,在普通纸酿酒过程中沉淀析出,成为酒石,酒石酸的名称由此得来。在制造葡萄酒时,会沉积大量酒石(氢钾盐)。另外,在霉菌和地衣类中也常见到它的存在。分离到的酒石酸发酵细菌,在体内是通过葡萄糖氧化分解,经由5-酮葡萄糖酸,在形成羟基乙酸的同时形成酒石酸。酒石酸铵受微生物作用,可编程琥珀酸。因此,工业中用酒石酸作为生产琥珀酸的原料。酒石酸主要以钾盐的形式存在于多种植物和果实中,也有少量是以游离态存在的。L(+)-酒石酸在某些植物果实如葡萄、罗望子果等中有较高的含量。1769年舍勒首次从葡萄汁的发酵液内得到游离的无色酒石酸结晶。它的各种立体异构体和外消旋体具有不同的物性。自然界存在的多为右旋体,葡萄汁和其他浆果汁中尤多,故又叫果酸。如用丁烯二酸控制氧化得到的是外消旋体。将上述反应过程中产生的酒石以石灰乳处理生成酒石酸钙,再酸化则得内消旋体。酒石酸盐在历史上对建立有机立体化学起了作用。1848年法国化学家巴斯德从事酒石酸钠铵结晶学研究工作时,看到一种前人未曾注意的有趣现象:无旋光性的酒石酸钠铵是由二种不同结晶组成的混合物,它们的外形互为Chemicalbook镜像关系,实际上是外消旋体。他用放大镜和镊子将混合物细心分成小堆。一堆是右旋体晶体,一堆是左旋体晶体,它们犹如一堆是右手套,一堆是左手套。两堆晶体溶于水都有旋光性。他首次发现了分子的立体异构和旋光的关系,提出了对映异构概念,为有机立体化学的发展奠定了基础。酒石酸常用于制药物、媒染剂和鞣剂等,也常用作拆分外消旋碱性化合物的试剂。它也是食品添加剂中的酸味剂,酸感优于苹果酸、乳酸等。它的几种盐都有重要应用,例如实验室中用酒石酸钾钠配制斐林试剂,用于鉴定有机分子结构中醛基官能团。它的钾钠盐又叫罗谢尔盐,其晶体在压力作用下发生极化而使两端表面产生电势差(压电效应),借此可以制成压电元件,用于无线电和有线电广播的受话器和拾音器。医疗上将酒石酸锑钾(俗称吐酒石)用于治疗血吸虫病。2.2 L(+)-酒石酸的理化性质外观为无色半透明晶体或白色细至粗结晶粉末,有酸味,熔点为170-172°C,比旋光度12°(c=20,H2O),沸点191.56°C,密度1.76,蒸汽密度5.18,蒸气压 5Pa(20°C),折射率12.5°(c=5,H2O),在室温下进行储存,溶解度1M(20℃)无色溶液。毒性:小鼠经口LD50为4.36 g/kg ;ADI 0~30 mg/kg(酒石酸及其盐类)。3 L(+)-酒石酸的检测3.1 国标检测3.1.1 范围本标准适用于以顺丁烯二酸酐和过氧化氢为原料经氧化、酶法水解而制得的食品添加剂L(+)-酒石酸。3.1.2 检测方法以酚酞为指示剂,用氢氧化钠标准滴定溶液滴定干燥试样的水溶液,根据氢氧化钠标准滴定溶液的用量,计算以C4H6O6计的总酸含量为L(+)-酒石酸含量。3.1.3 试剂和材料氢氧化钠标准滴定溶液:c (NaOH) = 1.0 mol / L酚酞指示剂:10 g / L3.1.4 分析步骤称取2.0 g 干燥样,精确至0.0002 g,加40 mL 无二氧化碳的水溶液,加2滴酚酞指示剂,用氢氧化钠标准滴定溶液滴定至微红色,保持30 s 不褪色为终点。在测定的同时,按与测定相同的步骤,对不加试样而使用相同数量的试剂溶液做空白试验。3.1.5 数据计算L(+)-酒石酸(以C4H6O6计,以干量计)的质量分数ω1,数值以 % 表示,按式1计算: ——————————式1式中:V——试料消耗氢氧化钠标准滴定溶液体积的数值,单位为毫升(mL);V0——空白试验消耗氢氧化钠标准滴定溶液体积的数值,单位为毫升(mL);c——氢氧化钠标准滴定溶液浓度的准确数值,单位为摩尔每升(mol/L);m——试料质量的数值,单位为克(g);M——酒石酸(1/2 C4H6O6)的摩尔质量的数值,单位为克每摩尔(g/mol)(M=75.04).取两次清醒测定结果的算术平均值为报告结果。两次平均测定结果的绝对差值不大于0.2 % 。3.2 高效液相色谱3.2.1 检测原理采用高效液相色谱分析测定酒石酸的含量以及与标准酒石酸的分析对比,高效液相色谱分析法是主要具有高压、高速、高效、高灵敏度等特点,对试样进行分析测定。流动相与固定相都是液体,流动相与固定相之间应互不相溶(极性不同,避免固定相流失),有一个明显的分界面。当试样进入色谱柱,[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]在两相间进行分配。达到平衡时,服从于高效液相色谱计算公式:式中,Cs——[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]在固定相中的浓度; Cm——[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]在流动相中的浓度; Vs——固定相的体积; Vm——流动相的体积。3.2.2 试剂和仪器试剂:80%乙醇,酒石酸,磷酸二氢铵均为分析纯,实验用水均为二次蒸馏水。仪器:高效液相色谱仪C18色谱柱(250*4.60nm)3.2.3 色谱条件固定相为Phencmenex luna 5μm C18 色谱柱(250*4.60nm),流动相为 0.01 mol/L(NH4)2HPO4溶液,流速1mLmin-1,检测波长为210 nm,柱温为30℃。3.2.4 分析步骤精确称取酒石酸标准品0.25 g,置于烧杯中用二次蒸馏水完全溶解,转移至100 mL容量瓶中加二次蒸馏水稀释并定容,然后用移液管移取分别稀释成2.5 μgmL-1、2.0 μgmL-1、1.5 μgmL-1、1.0 μgmL-1、0.8 μgmL-1 等不同质量浓度的标准品,并用0.45 μm的滤膜过滤,然后超声处理。采用电子天平准确称取1.3206 g (NH4)2HPO4 晶体,于小烧杯中加入二次蒸馏水完全溶解,然后转移到1000 mL容量瓶中稀释并定容至刻度线,最后用0.45 μm的滤膜过滤,超声15 min处理作为流动相。3.2.5 数据处理依次对不同浓度的标准品进行色谱分析,并拟合标准曲线,对样品进行色谱分析,并进行定量计算。3.2.6 方法优点色谱分析法检测线性范围宽,具有操作简便,快捷,选择性好等优点。4 L(+)-酒石酸的生产4.1 L(+)-酒石酸的生产方法一个方法是,以制造葡萄酒时生成的酒石为原料,将其转化为钙盐,再用稍过量的稀酸使其分解而得。或以顺丁烯二酸和过氧化氢为原料,在一定温度下转化为环氧丁二酸,再水解得D L-酒石酸。也可由化学合成法制得的环氧琥珀酸,经琥珀酸诺卡氏菌所含的开环酶的作用而得L(+)酒石酸。另一个方法是,将蒸馏水加到工业品酒石酸中,通蒸气加热并搅拌使之溶解。加入适量活性炭,充分搅拌后静置,过滤,滤液加热浓缩至表面结膜时,趁热抽滤,滤液冷却结晶,待完全后,结晶用少量蒸馏水洗淋后于30~40℃下平铺干燥至不沾勺即可。若控制活性炭脱色温度为80℃,过滤后于80℃减压浓缩,冷却结晶,将得到的结晶在非铁质容器中重结晶精制低温下烘干,可得右旋酒石酸 [ L(+)-酒石酸 ] 成品。4.2 酒石酸的生物合成途径酒石酸的生物合成途径如图1所示:[align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107251428084146_7015_1608728_3.png[/img][/align][align=center]图1 酒石酸的生物合成途径[/align]直接发酵法生产酒石酸异性物质多,提取困难,收率低,经济上目前还没有吸引力。4.3 酶法生产L-酒石酸1974年佐藤英次等人首先报道了采用Achromobater lartarogenes 和Alcaligenes epoxylyticus 水解顺式环氧琥珀酸生产L-酒石酸的前体发酵,过程如图二所示:[align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107251428086957_2391_1608728_3.png[/img][/align][align=center]图2 酒石酸生产[/align]以无水马来酸(顺丁烯二酸酐)为原料经水解得到马来酸,再以钨酸钠(Sodium tungstate)作为催化剂将马来酸与过氧化氢反应制得顺式环氧琥珀酸。培养具有L-酒石酸外氧化酶的微生物作酶源将顺式环氧琥珀酸转化为酒石酸。具有L-酒石酸外氧化酶的微生物主要是细菌,目前报道的有无色杆菌、产碱杆菌、醋酸杆菌、不动杆菌、土壤杆菌、诺卡氏菌、根瘤菌、假单胞菌和棒杆菌。酒石酸外氧化酶是一种诱导酶,在培养这类微生物生产酒石酸时通常在培养基中需加入少量顺式环氧琥珀酸进行诱导培养。这种酶的分子量在25000~45000之间,在pH5~9范围内稳定,最适pH 为7.5~8.5,作用温度范围为25~55℃。酶法生产L-酒石酸的工艺流程大致如图3 :[align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107251428088052_2948_1608728_3.png[/img][/align][align=center]图3 酶法工艺流程图[/align]4.4 棒状杆菌固定化细胞生产L-酒石酸采用卡拉胶将含环氧琥珀酸水解酶的诺卡氏菌细胞包埋固定,利用固定化细胞转化底物环氧琥珀酸生成L-(+)-酒石酸,以将环氧琥珀酸水解酶反复多次使用。采用卡拉胶作为载体制得固定化微生物细胞生产L-酒石酸,这种方法具有较高的酶活性回收率和良好的化学和机械稳定性。固定化细胞经过底物活化处理后顺式环氧琥珀酸水解酶酶活性回收率在100%以上。另外此固定化细胞的贮藏稳定性较好,经0.2 molL-1底物溶液浸泡,在4℃冰箱中贮藏90d酶活性基本不变。底物和表面活性剂能大幅度提高固定化细胞的酶活性回收率,这主要是增加了细胞膜对底物的渗透性或造成菌体的自溶,当菌体自溶时,酶被截留在凝胶腔内,不会由凝胶溢出,而底物和产物则易由凝胶网溢出,维持了固定化细胞较高的稳定性。4.5 糖质发酵法[color=#333333]制造L-(+)-酒石酸[/color]在L-酒石酸的生物代谢途径中,认为葡萄糖经过Gluconobater suboxydans 发酵形成葡萄糖酸,继而氧化为2-酮基-D-葡萄糖酸(2-KGA)和5酮基-D-葡萄糖酸(5-KGA),5-KGA在金属催化剂的作用下,可以形成羟基乙酸和L-酒石酸。1972年,Kotera等在研究5-KGA转化为L-酒石酸的过程中,发现了一种能与AbdelAkhel和Smith试剂形成紫红色的物质,并对这种物质进行了分离纯化,通过红外光谱及质谱分析,证实该物质为1,2-二羟乙基氢酒石酸,并命名为“前酒石酸”,同时提出了相关机理如图4,5-KGA通过烯醇化,转化为4-KGA,再形成“前酒石酸”。通过该物质的过渡,5-KGA被催化分解为L-酒石酸和羟基乙酸。[align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107251428090793_95_1608728_3.png[/img][/align][align=center]图4 L-酒石酸形成机理[/align]1995年,Klasen等认为5-KGA主要在氧化葡萄糖酸杆菌的细胞质中合成,并在G.oxydans DSM3503中过表达了依赖NADP的GNO,该酶在细胞质中催化葡萄糖酸形成5-KGA,最终酶活提高了85倍;1999年,Shinagawa等通过对G.suboxydans IFO12528静息细胞培养和膜结合部分催化实验发现,5-KGA的形成主要是膜结合蛋白PQQ-依赖的葡萄糖酸脱氢酶,并考察了该酶翠花形成5-KGA的最适pH 为4.0和温度15℃,在此条件下,膜结合蛋白部分催化转化形成5-KGA为110 mmol/L ;因此,在氧化葡萄糖酸杆菌中,酮基葡萄糖酸催化合成途径如图5所示,PQQ-依赖的葡萄糖酸脱氢酶是主要的5-KGA合成酶,而FAD-依赖的葡萄糖酸脱氢酶是合成2-KGA的主要酶,从代谢流上分析为5-KGA的主要分流节点。[align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107251428091768_3741_1608728_3.png[/img][/align][align=center]图5 氧化葡萄糖酸杆菌中酮基葡萄糖酸的催化反应[/align]糖质发酵法生物制造L-酒石酸因利用可再生生物质资源而日益备受关注。但是,要提高其相对于酶法合成L-酒石酸的竞争力,就必须使用现代生物技术,包括分子生物学、代谢工程以及合成生物学等手段,提高L-酒石酸的前体——5-KGA的发酵水平以及5-KGA到L-酒石酸的转化水平。5 用途及应用5.1 食品添加剂方面首先,L(+)-酒石酸广泛用作饮料和其他食品的酸味剂,用于葡萄酒、软饮料、糖果、面包、某些胶状甜食。其次,可以作为食品中添加的抗氧化剂﹐可以使食物具有酸味。酒石酸最大的用途是饮料添加剂。5.2 药物方面利用其光学活性,作为化学拆分剂,用于制造抗结核病药物中间体DL-氨基丁醇的拆分;还可以作为手性原料用于酒石酸衍生物的合成;利用其络合性,用作电镀、脱硫、酸洗以及化学分析、医药检验中的络合剂、掩蔽剂、螯合剂、印染的防染剂;也是药物工业原料。5.3 工业方面利用其酸性,作为涤纶织物树Chemicalbook脂整理的催化剂,谷维素生产的PH调节剂;利用其还原性,用作化学制镜的还原剂。照相的显影剂。还能与多种金属离子络合,可作金属表面的清洗剂和抛光剂;在制镜工业中,酒石酸是一个重要的助剂和还原剂,可以控制银镜的形成速度,获得非常均一的镀层;金属离子掩蔽剂;防染剂;用于天然产物的手性砌块,也与化合物 TiCl2(O-i-Pr)2形成Diels-Alder 催化剂。最后,可用作生化试剂、掩蔽剂及啤酒发泡剂,也用于鞣革工业。6 结语L(+)-酒石酸是天然的有机酸,应用十分广泛,在食品、医药、纳米材料等各个方面具有显著的应用,L(+)-酒石酸的检测方法主要有滴定法、液相色谱法等。以前L(+)-酒石酸主要从葡萄酒酿造的副产物酒石中提取,但由于酒石供应量有限,来源不稳定,近年来采用化学合成和生物转化相结合的方法来生产L(+)-酒石酸。7 参考文献袁建锋,吴绵斌,林建平,岑沛霖.基于5-酮基-D-葡萄糖酸生物制造L-(+)-酒石酸的研究进展[J].现代化工,2013,33(09):13-16.张建国,黄滕华.微生物转化法生产L-(+)-酒石酸的研究[J].工业微生物,1990,2(2):7-12.刘斌,须辑.半生物合成法合成酒石酸[J].化学世界,1996,8(10):527-531.[color=black]郑璞,孙志浩.用诺卡氏菌酶法转化顺式环氧琥珀酸生产L(+)-酒石酸的研究[/color][J].化工业微生物,1994,3(24):12-17.张建国,钱亚娟.棒状杆菌固定化细胞生产L(+)-酒石酸[J].生物工程学报,2000(02):72-76.万屹东, 蒋志清, 顾松林,等. 一种L(+)酒石酸的生产方法:, CN102093208B[P]. 2015.楼锦芳, 张建国. 酶法合成L(+)-酒石酸的研究进展[J]. 食品科技, 2006, 31(011):162-164.杨阳, 李文鹏, 陆鲁生,等. L(+)-酒石酸发酵法生产工艺改进的研究[J]. 生物工程学报, 2001, 17(3):345-348.柯昌武, 蔡水洪, 叶勤. 卡拉胶固定化Nocardia sp.生产L(+)酒石酸[J]. 华东理工大学学报(自然科学版), 2006.Yamada K. Kodama T. Obata T, et al.Microbial formation tartaric acid from glucose 1 Isolation and identification tartaric acid producing microorganisms[J].Journal of Fermentation Technology, 1971. 49 (2) :85-89.Kotera U, Kodama T, Yamada к, et al.Microbial formation of tartaric acid from glucose 5 lsolation and chemical structure of new oxidation product of 5-ketogluconic acid, and a hypothetical pathway from glucose !o tararic acid through this new compound[J]Agricultural and Biological Chemistry. 1972. 36 (8) 1315-1325.Klasen R. Bringerneyer s, Sahm H.Biochemical characterization and sequence analysis of the gluconate-NADP 5-oxidoreductase gene from Gluconobacter oxydans[J].Journal of Bacteriology, 1995, 177 (10) :2637-2543.Shinagawa E, Matsushita K, Toyama H, et al.Production of 5-ketod-gluconate by acetic acid bacteria iscatalyzed by pyrroloquinoline quinone (PQQ) -dependent membrane-bound d-gluconate dehydrogenase[J].Journal of Molecular Catalysis B:Enzymatic, 1999, 6 (3) :341-350.
想在北京做苹果酸、柠檬酸、酒石酸、琥珀酸、乳酸、乙酸、甲酸等有机酸的定量分析,不知哪里又快又准啊?望知情人推荐,谢谢!
RT。我要做土壤中的乙酸、丙酸、丁酸、柠檬酸,琥珀酸,苹果酸、乳酸、苯甲酸、马来酸的检测,前三种挥发性的应该怎么做呢?后几种用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]检测。后几种的回收率不太理想,重现性也不好,有没有人做过啊?帮帮忙啊!