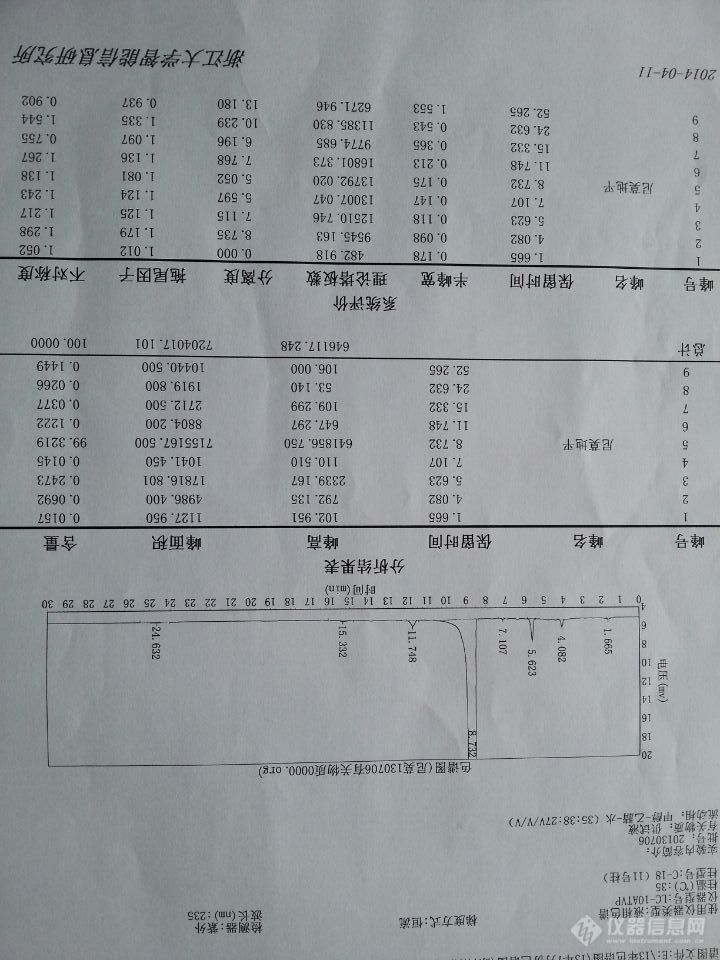
哪位能帮忙指出下面的尼莫地平图谱中欧标中所指的杂质A、B、C?[img=,690,521]https://ng1.17img.cn/bbsfiles/images/2019/08/201908301335345959_8586_1815404_3.jpg!w690x521.jpg[/img]
[size=3]尼莫地平滴定的方法是:取本品约0.18g,精密称定,加无水乙醇25ml,微温使溶解,加高氯酸溶液(取70%高氯酸溶液8.5ml,加水至100ml)25ml,加邻二氮菲指示液4滴,用硫酸铈滴定液(0.1mol/L)滴定至溶液由橙红色变为浅黄绿色,并将滴定结果用空白试验校正。每1ml硫酸铈滴定液(0.1mol/L)相当于20.92mg C21H24N2O7。该滴定是氧化还原吗?那么高氯酸是和尼莫地平的NH反应的吗?那么硫酸铈和什么反应呢?[/size]
以V氯仿∶V甲醇∶V二氯甲烷∶V正己烷=2.6∶1.2∶1∶5为展开剂, 建立了薄层色谱扫描法测定痕量药物尼莫地平的新方法。 其Rf值为0.48。 扫描波长为365 nm, 该法的最低检出限为0.005 μg,相对标准偏差为2.94%, 工作曲线的线性范围为0.005~1 μg。 用该法测定了加有尼莫地平的血清和尿样, 尼莫地平的平均回收率为96.7%~103%。关键词 尼莫地平, 紫外薄层色谱法 尼莫地平(nimodipine)为一钙离子拮抗剂, 能有效地调节细胞内钙的水平, 具有抗缺血和抗血管收缩作用[1], 是近年来治疗高血压和脑血管疾病的一种新药, 其结构式如右所示。 有关该药的测定方法, 曾报道过的有高效液相色谱法[2]、 分光光度法[3], 但用紫外薄层色谱扫描法测定尼莫地平至今未见文献报道。 本文首次采用紫外薄层色谱法, 以氯仿-甲醇-二氯甲烷-正己烷为展开剂, 对尼莫地平的测定进行了研究。 该法具有简单、 快速、 灵敏、 准确的特点, 我们成功地做了血清和尿样中不同浓度的加标回收实验, 结果令人满意。 该法可用于临床作为测定尼莫地平血药及尿药浓度的一种简单、 有效的新方法。1 实验部分1.1 仪器与材料 CS-9000双波长薄层色谱扫描仪(日本岛津); 毛细管定量点样器(美国Drummond); UV-1型紫外分析仪(上海顾村电光分析仪器厂); 硅胶GF254 板(青岛海洋化工厂); 尼莫地平(山东新华制药厂提供)。 其它试剂均为分析纯以上规格。1.2 实验方法 用1 μL定量毛细管点样, 标样与试样点于同一板上 待溶剂挥发后, 放入盛有展开剂的层析缸中, 用蒸汽预吸附3~5 min, 然后用展开剂展开, 展开剂为V氯仿∶V甲醇∶V二氯甲烷∶V正己烷=2.6∶1.2∶1∶5, 展开到距板上端1 cm处, 展距9 cm 取出板, 待溶剂挥发干净, 置于紫外分析仪, 在254 nm波长下可观察到样品暗红色斑点, 尼莫地平的Rf值为0.48 然后用薄层色谱扫描仪扫描, 以外标两点法定量。 紫外薄层扫描条件: 以尼莫地平光谱λmax=365 nm为测定波长,锯齿扫描, 数据累加4, 数据平滑11,高灵敏度。2 结果与讨论2.1 展开剂的选择 我们根据Glajch三角形最优化法[4]及参照Snyder溶剂参数法[4]对展开剂的组成及配比进行了选择,确定了以氯仿-甲醇-二氯甲烷-正己烷作为四元混和展开剂,其配比为V氯仿∶V甲醇∶V二氯甲烷∶V正己烷=2.6∶1.2∶1∶5 。

尼莫地平注射液含量方法学研究尼莫地平为1,4-二氢吡啶类钙通道拮抗剂。其药理特性是阻断中枢神经系统内细胞膜的钙通道,有效地调节细胞内钙的水平,使之保持正常的生理功能。下面是含量方法学研究。 含量测定照高效液相色谱法(中国药典2010年版二部附录Ⅴ D)测定,避光操作。1.色谱条件:色谱柱:以十八烷基硅烷键合硅胶为填充剂;流动相:甲醇:乙腈:水=35:38:27;检测波长:235nm;进样量:20ul;柱温:35°C流速:1.0ml/min。2.精密度试验精密称取尼莫地平对照品约20mg,置100ml量瓶中,加流动相溶解并稀释至刻度,摇匀,精密量取5.0ml,分别置50ml量瓶中,加流动相稀释至刻度,摇匀,精密量取20μl注入液相色谱仪,记录色谱图,重复进样6次,计算精密度。结果见表1。http://ng1.17img.cn/bbsfiles/images/2012/12/201212261100_415567_2583865_3.jpg由试验结果可知,RSD小于1%,表明该方法精密度良好。3.线性关系精密称取尼莫地平对照品约20mg,置100ml量瓶中,加流动相溶解并稀释至刻度,摇匀,精密量取2.0、3.0、5.0、6.0、7.0、8.0ml,分别置50ml量瓶中,加流动相稀释至刻度,摇匀,分别精密量取20μl注入液相色谱仪,记录色谱图,结果见表2。http://ng1.17img.cn/bbsfiles/images/2012/12/201212261053_415553_2583865_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/12/201212261053_415554_2583865_3.jpg 线性方程为A=67935.82C-1996.73;r=0.9999。结论:本品在8.06~32.24μg/ml范围内,浓度与峰面积呈线性关系。4.溶液的稳定性试验取本品适量,加流动相稀释制成1ml中约含20μg的溶液,在避光条件下放置,分别于0,1,2,4,8小时,精密量取20μl注入液相色谱仪,记录色谱图,结果见表3。 http://ng1.17img.cn/bbsfiles/images/2012/12/201212261053_415555_2583865_3.jpg试验结果表明:本品溶液在8小时内测定稳定。5.回收率试验精密称取尼莫地平约8、10、12mg各三份,分别置50ml量瓶中,分别加入处方量的辅料空白溶液,超声助溶后,加水稀释至刻度,摇匀,滤过,量取续滤液1.0ml,置10ml量瓶中,用流动相稀释至刻度,摇匀,精密量取20μl注入液相色谱仪,记录色谱图;另取尼莫地平约20mg,用流动相稀释制成每1ml中约含20μg的溶液,同法测定,按外标法以峰面积计算,即得。测定结果见表4。http://ng1.17img.cn/bbsfiles/images/2012/12/201212261054_415556_2583865_3.jpg平均回收率为99.65%;RSD为0.33%结论:由以上结果知,本品
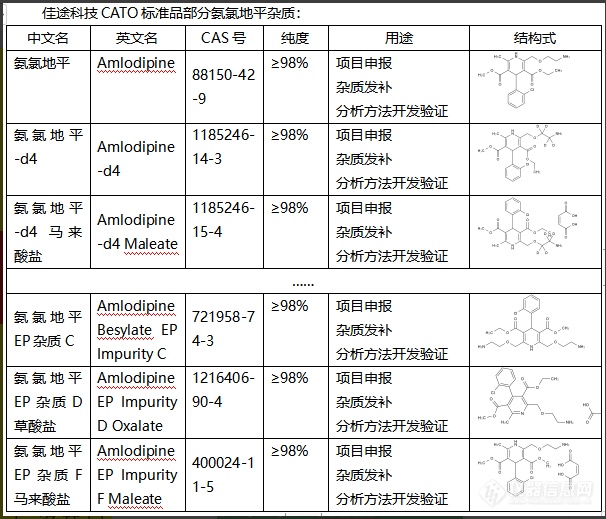
氨氯地平是一种常用的抗高血压药物,对于其中的杂质,氨氯地平杂质其作用主要体现在以下几个方面:1. 质量影响:杂质会影响氨氯地平的纯度和稳定性,可能会导致药品质量下降。2. 安全性影响:杂质可能会产生一些未知的副作用和毒性反应,影响药品的安全性。3. 药效影响:杂质可能会干扰氨氯地平的药效,使得药物的治疗效果降低。4. 法规因素:食品药品监管部门对药品中的杂质有严格的限制标准,过多的杂质可能会导致药品不能上市。CATO标准品对于氨氯地平这类药物的生产,控制和降低杂质的含量是非常注重的。[img=,606,519]https://ng1.17img.cn/bbsfiles/images/2024/02/202402041354066781_2922_6381668_3.png!w606x519.jpg[/img]
比如2015版药典说了测定杂质含量说另有规定外进样不少于三针通常含量低于0.5%的杂质RSD小于10% 等等还说供试品溶液稀释成与杂质限度相当的溶液作为对照溶液进样几路色谱图。 重点是原来我们都是杂质进一针 再加上对照品进一针 系统适用性等等. 大家都是怎么做的。例如2015版药典算的尼莫地平的检测.不是有杂质I吗。真的需要进3针吗.
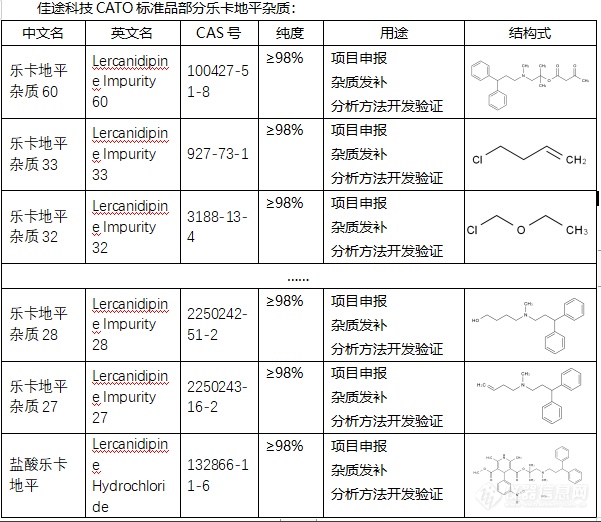
乐卡地平杂质的作用是多方面的,并且主要取决于它们的类型和含量。1. 降低药效:如果杂质的含量过高,可能会降低乐卡地平的药效。例如,杂质可能会与乐卡地平的活性成分竞争,降低其与体内靶点的结合能力,从而降低其药效。2. 引发副作用:某些类型的杂质可能会引发副作用,例如过敏反应、肝脏损伤等。这通常取决于杂质的类型和含量,以及患者的个体差异。3. 质量控制:在药品制造过程中,杂质也被用作一种质量控制的手段。通过测量杂质的含量,可以评估药品的纯度和质量,以确保药品的安全性和有效性。CATO标准品药品中杂质的含量都会严格控制在一定范围内,以确保药品的安全性和有效性。药品在上市之前,必须经过严格的质量检测,以确保其杂质含量符合法定标准。[img=,601,522]https://ng1.17img.cn/bbsfiles/images/2024/02/202402041448095358_8809_6381668_3.png!w601x522.jpg[/img]

HPLC法测定西尼地平的有关物质西尼地平(Cilnidipine)为一新型抗高血压药,其通过L-型钙通道长时间地抑制钙内流,具有长时间持续扩张血管作用,还可预防卒中和降低死亡率并减少肾、心、血管并发症,具有良好的发展前景。有关西尼地平药理作用的文献较多,但其质量分析方法的研究报道较少,本文采用反相高效液相色谱面积归一化法,对西尼地平合成工艺中各步中间体及可能产生的有关物质予以分离检测。 具体方法如下:(一)色谱条件:色谱柱:十八烷基硅烷键合硅胶柱(Xtimate C18),250×4.6mm,5um流动相:0.03mol/L磷酸氢二钠溶液(用磷酸调节pH为4.0)-甲醇-乙腈(40:35:25)检测波长:240nm流速:1.0ml/min进样量:20ul系统适用性试验要求:理论塔板数按西尼地平峰计算应不低于3000;在供试品图谱中西尼地平与相邻杂质峰的分离度应符合规定。(二)供试品溶液:称取本品约10mg,加甲醇溶解并稀释至50.0ml,制成每1ml含0.2mg的溶液,作为供试品溶液。(临用新制) (三)测定:按照高效液相色谱仪操作规程准备仪器,平衡后取空白溶液20ul注入液相色谱仪,再取供试品溶液20ul注入液相色谱仪,记录色谱图至主成分峰保留时间的4倍。色谱图如下:http://ng1.17img.cn/bbsfiles/images/2012/12/201212231401_414537_2583865_3.jpg结果计算:供试品溶液的色谱图如有杂质峰,按面积归一化法计算:单个杂质峰面积不得大于所有峰面积总和的0.2%;各杂质峰面积的和不得大于所有峰面积总和的0.5%。注意:供试品溶液配制应避光操作。
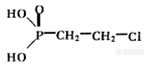
尼莫地平滴定的方法是:取本品约0.18g,精密称定,加无水乙醇25ml,微温使溶解,加高氯酸溶液(取70%高氯酸溶液8.5ml,加水至100ml)25ml,加邻二氮菲指示液4滴,用硫酸铈滴定液(0.1mol/L)滴定至溶液由橙红色变为浅黄绿色,并将滴定结果用空白试验校正。每1ml硫酸铈滴定液(0.1mol/L)相当于20.92mg C21H24N2O7。该滴定是氧化还原吗?那么高氯酸是和尼莫地平的NH反应的吗?那么硫酸铈和什么反应呢因为我们现在要测定尼莫地平杂质对照品的含量,想依法算出其滴定度,但是不了解其反应式?请大家帮个忙[img]http://ng1.17img.cn/bbsfiles/images/2010/04/201004270910_214908_1695299_3.gif[/img]
尼莫地平滴定的方法是:取本品约0.18g,精密称定,加无水乙醇25ml,微温使溶解,加高氯酸溶液(取70%高氯酸溶液8.5ml,加水至100ml)25ml,加邻二氮菲指示液4滴,用硫酸铈滴定液(0.1mol/L)滴定至溶液由橙红色变为浅黄绿色,并将滴定结果用空白试验校正。每1ml硫酸铈滴定液(0.1mol/L)相当于20.92mg C21H24N2O7。该滴定是氧化还原吗?那么高氯酸是和尼莫地平的NH反应的吗?那么硫酸铈和什么反应呢因为我们现在要测定尼莫地平杂质对照品的含量,想依法算出其滴定度,但是不了解其反应式?请大家帮个忙[img]http://ng1.17img.cn/bbsfiles/images/2010/04/201004270910_214909_1695299_3.gif[/img]
各位老师,我现在在做硝苯地平的有关物质,有一个硝苯地平杂质1的含量忽大忽小,后来我们发现不同的色谱柱,检测出来的含量不同,用了安捷伦、迪马家的C18柱,杂质1含量约0.3%,但是用Waters家的色谱柱,杂质1就是未检出。所以,我想问一下,C18色谱柱中,会不会存在微量物质,促使硝苯地平降解为杂质1。硝苯地平在紫外光破坏、酸破坏、热破坏条件下产生杂质1。另外,单独进杂质1对照品溶液峰面积无变化,每个色谱柱都很稳定。
尼达尼布杂质可能会对药物的药理活性产生不利影响,导致药效降低。比如,有可能降低尼达尼布对肿瘤细胞的抑制作用,从而影响治疗效果。另一方面,尼达尼布杂质可能对人体产生毒性反应,对患者的身体健康产生不良影响。例如,有可能引起过敏反应,导致患者出现皮疹、呼吸困难等症状。但是,值得注意的是,这些展示都是可能性,并不一定在所有情况下都会发生。具体情况需要根据尼达尼布药品中杂质的类型和含量来判断。为了避免杂质对药物效果的影响,CATO标准品在药品生产中会进行严格的质量控制,对杂质进行有效的控制和清除。同时,掌握和理解杂质的产生机制,也有助于进一步完善和优化药品的生产工艺。[img=,604,514]https://ng1.17img.cn/bbsfiles/images/2024/02/202402041439114552_8061_6381668_3.png!w604x514.jpg[/img]

[font=宋体]莫西沙星是一种广谱的抗生素,被广泛用于治疗很多种的细菌感染。莫西沙星杂质会影响到药物的安全性和有效性。[/font][font=宋体][/font][font=宋体][/font][font=宋体]1. 影响药物的安全性:如果莫西沙星中的杂质过多或是有毒性较高的杂质,可能会导致药品的毒副作用增加,影响到药品的安全应用。[/font][font=宋体][/font][font=宋体][/font][font=宋体]2. 影响药物的有效性:有一些杂质可能会与莫西沙星发生化学反应,改变其化学结构,从而降低其抗菌活性,影响治疗效果。[/font][font=宋体][/font][font=宋体][/font][font=宋体]3. 影响药物的稳定性:某些杂质可能会影响莫西沙星的稳定性,导致药物质量的降低。[/font][font=宋体][/font][font=宋体][/font][font=宋体]因此,对莫西沙星的杂质进行控制是非常重要的,相关监管部门也对其中的含量有着严格的标准。[/font][font=宋体][font=Calibri]CATO[/font][font=宋体]标准品[/font][/font][font=宋体]在药品的生产过程中,对杂质进行定期的检测和控制,以确保药品的质量。[img=,600,610]https://ng1.17img.cn/bbsfiles/images/2024/02/202402021649392583_1508_6381668_3.png!w600x610.jpg[/img][/font]

在甲基培尼皮质醇的制造过程中,可能会生成一些杂质。这些杂质可能会出现在原料中,也可能在制药过程中的化学反应中产生。不论其来源,杂质的存在都可能影响到药物的质量、安全性和疗效。例如,甲基培尼皮质杂质可能增加药物的毒性,或导致不良反应。同样,杂质也可能对甲基培尼皮质醇的药效产生影响。因此,制药公司必须在生产过程中严格检测和控制这些杂质。检测和控制药品中的杂质是药品质量控制的重要组成部分。CATO标准品对杂质的研究不仅有助于保证药品的质量和安全性,也可以为优化制药过程提供参考。比如,通过对杂质的研究,可以找到产生这些杂质的原因,从而改进制药过程,减少杂质的生成。[img=,600,588]https://ng1.17img.cn/bbsfiles/images/2024/02/202402052058222428_1748_6381668_3.png!w600x588.jpg[/img]
[color=#444444]各位前辈好,我描述一下具体问题,希望前辈能指点迷津:[/color][color=#444444] 最近用waters走液相,总能在同一个保留时间,出现一个差不多高度的不明杂质峰,这是怎摸回事?怎样解决? water是2695与2487检测器,碳18短柱子,流动相中有磷酸二氢钾缓冲盐、乙腈、四氢呋喃。[/color][color=#444444] 我换过色谱柱,杂质峰仍存在;重新配过样品,杂质峰仍存在。现在感觉是系统或流动相的问题,想问一下,各位前辈这个问题是哪出了问题,怎摸解决呢?[/color]
布美他尼杂质是药物布美他尼制剂中可能存在的杂质,这些杂质可能来源于原料药的生产过程、制剂的准备过程或者储存过程。1. 影响药效:药物中含有过多的杂质可能会影响药物的药效,产生药效不稳定、药效降低等问题。2. 影响安全性:部分杂质可能具有潜在的毒性,长期或高剂量使用可能对人体造成伤害。严重情况下可能出现药品不良反应甚至中毒。3. 影响药物的稳定性:不同类型的杂质结构,可能影响药物的稳定性,例如酸性或碱性杂质可能引起药物分解,导致药效降低或失效。4. 影响药物的外观质量:杂质可能会影响药物的外观性状,如颜色、透明度和溶解性等。因此,确定和控制药物中的杂质是药品质量控制的重要环节。CATO标准品对于药物杂质的研究,主要包括杂质的来源、形成机理、控制策略和杂质的鉴定、定量测定等内容。[img=,607,514]https://ng1.17img.cn/bbsfiles/images/2024/02/202402041444015575_2473_6381668_3.png!w607x514.jpg[/img]
厄洛替尼杂质是药物制备过程中的副产品或污染物,可能会影响药物的安全性和有效性。常见的杂质有重金属、溶剂残留、有毒化合物等。对于厄洛替尼来说,杂质可能会影响其药效和安全性。一方面,杂质可能降低药物的纯度,从而降低其抑制肿瘤生长的效果。另一方面,某些杂质可能具有毒性或致敏性,可能导致患者出现不良反应。因此,对厄洛替尼的杂质进行检测和控制是药品质量控制的重要环节。这需要使用一种或多种分析方法,如高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法、[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]法、质谱法等,以检测并定量药物中的杂质。CATO标准品针对可能的杂质源(如起始材料、反应条件、催化剂、溶剂等)进行控制,可以有效地减少杂质的生成。[img=,603,517]https://ng1.17img.cn/bbsfiles/images/2024/02/202402021655361773_9862_6381668_3.png!w603x517.jpg[/img]
阿莫西林有关杂质
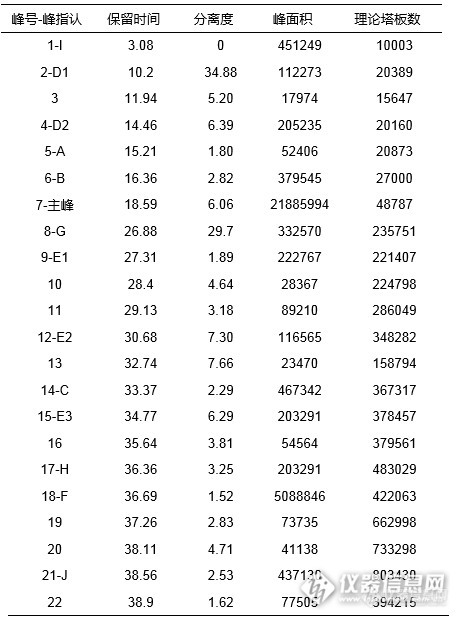
[align=center][b][color=black]阿莫西林及其杂质的液相分析[/color][/b][/align][b][/b][align=left]首先参考客户提供液相条件,对客户提供的阿莫西林样品进行分析尝试。由于梯度条件水相较高,故使用可在100%水相条件下稳定使用的资生堂高极性C[sub]18[/sub]色谱柱CAPCELL PAK AQ;同时,为提高杂质间分离度,我们选择柱效更高的3μm粒径色谱柱进行实验条件的优化。实验中发现,柱温对阿莫西林杂质B与杂质D2,杂质G与杂质E1,以及杂质H与杂质F间的分离有较大影响,结果如图1所示。[/align][align=center][img=,690,305]http://ng1.17img.cn/bbsfiles/images/2017/06/201706150846_02_2222981_3.png[/img][/align][align=center][/align][align=center]图1 不同温度下分离情况比较[/align][align=left][b]HPLC Conditions[/b]色谱柱:CAPCELL PAK C[sub]18[/sub] AQ S3 4.6mm i.d.×250mm流动相:A : 磷酸缓冲盐* B : 磷酸缓冲盐*/ 乙腈= 80/ 20 25°C B% 0%(0min)→0%(10min)→100%(40min)→100%(45min)→0%(45.1min)→0%(55min) 30°C B% 0%(0min)→0%(10min)→80%(40min)→80%(45min)→0%(45.1min)→0%(55min) 35°C B% 0%(0min)→0%(10min)→70%(40min)→70%(45min)→0%(45.1min)→0%(55min)流 速:1.0 mL/ min温 度:25°C、30°C、35°C检 测:PDA 254nm浓 度:客户提供进样量:20µ L*注:磷酸缓冲盐:0.05mol/L 磷酸二氢钾,用2mol/L 氢氧化钾调节pH为5.0[/align][align=left]由图1,温度越高,杂质D2保留时间越短,在35℃时杂质D2与杂质A、杂质B得到了完全分离;杂质G和杂质E1在35℃时亦得到良好分离;而杂质H与杂质F在35℃条件下反而重合在一起,无法分离。经过多番考量,最终选择在柱温31℃条件下对梯度条件进行优化,得到图2结果,同时通过图3单标定位和客户参考谱图共同参考,标定杂质峰序(因有杂质出多个峰,指定仅供参考)。[/align][align=center][img=,690,390]http://ng1.17img.cn/bbsfiles/images/2017/06/201706150846_03_2222981_3.png[/img][/align][align=center]图2 阿莫西林对照品及放大谱图[/align][align=center](图中显示数字为分离度)[/align][align=center][img=,690,358]http://ng1.17img.cn/bbsfiles/images/2017/06/201706150846_04_2222981_3.png[/img][/align][align=center]图3 阿莫西林对照品及单标谱图[/align][align=center][img=,460,620]http://ng1.17img.cn/bbsfiles/images/2017/06/201706150846_01_2222981_3.png[/img][/align][align=center]表1 阿莫西林对照品峰表[/align][align=center][b][/b][/align][align=left][b]HPLC Conditions[/b]色谱柱:CAPCELL PAK C18 AQ S3 4.6mm i.d.×250mm流动相:A : 磷酸缓冲盐* B : 磷酸缓冲盐*:乙腈 = 8 : 2 B% 0%(0min)→0%(10min)→50%(30min)→100%(40min)→0%(40.1min)→0%(50min)流 速:1.0 mL / min温 度:31°C检 测:PDA 254nm浓 度:客户提供进样量:20µ L*注:磷酸缓冲盐:0.05mol/L 磷酸二氢钾,用2mol/L氢氧化钾调节pH为5.0[/align][align=center][/align]
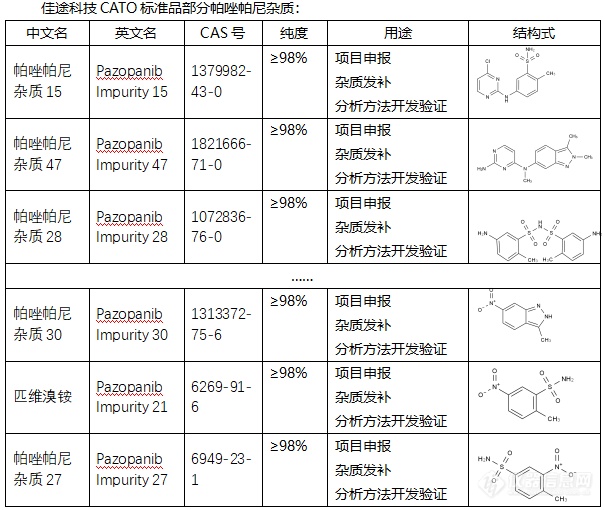
◇帕唑帕尼杂质 帕唑帕尼杂质是在帕唑帕尼药物制备或存储过程中可能产生的物质。帕唑帕尼杂质有多种,其中一些具有特定的CAS号、化学式和分子量。例如,帕唑帕尼杂质(Pazopanib Impurities)的CAS号为59816-94-3,化学式为C22H22N8,分子量为398.46。此外,帕唑帕尼杂质还包括一些异构体和其他结构类似物,如Pazopanib Isomer等。 CATO标准品提供的帕唑帕尼全套的杂质,这些杂质对于药物的纯度和稳定性研究至关重要,也是药物研发过程中不可或缺的一部分。[img=,605,510]https://ng1.17img.cn/bbsfiles/images/2024/02/202402192050040241_6306_6381607_3.png!w605x510.jpg[/img] 广州佳途科技股份有限公司深知药物研发与质量控制的重要性,CATO标准品厂家,提供帕唑帕尼全套的杂质,为客户提供更加精准、可靠的分析标准品,助力药物研发事业的快速发展,以满足客户在药物研发和质量控制方面的需求。
1MOL/L的锂离子测杂质金属干扰问题,我的锂离子浓度过高,但要测钾离子,钠离子,铁离子,铜离子,镍离子,钙离子,铅离子,镁离子,杂质离子含量在2PPM左右。不知道锂离子对这些离子的影响大不大。密度可能比标样液大点。谢谢
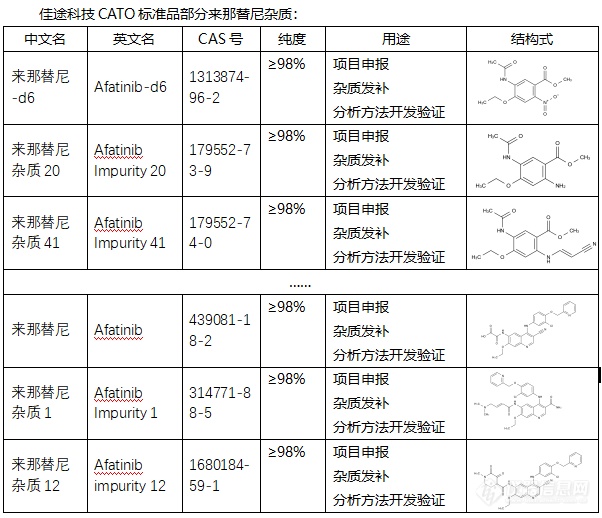
[font=宋体]◇来那替尼杂质[/font][font=宋体] 来那替尼杂质是在来那替尼药物制备或存储过程中可能产生的物质[/font][font=宋体],[/font][font=宋体][font=宋体]这些杂质可能会影响药物的纯度和效果,因此对其进行研究和控制对于确保药物的安全性和有效性至关重要。来那替尼杂质有多种,它们具有不同的[/font][font=Calibri]CAS[/font][font=宋体]号、化学式和分子量。例如,来那替尼杂质[/font][font=Calibri]NOQ[/font][font=宋体]的[/font][font=Calibri]CAS[/font][font=宋体]号为[/font][font=Calibri]1348481-03-7[/font][font=宋体],纯度通常为[/font][font=Calibri]95% HPLC[/font][font=宋体]。此外,还有其他来那替尼杂质,如来那替尼杂质[/font][font=Calibri]1144516-15-3[/font][font=宋体]等。[/font][/font][font=宋体][font=Calibri] CATO[/font][font=宋体]标准品提供的来那替尼全套的杂质[/font][/font][font=宋体],[/font][font=宋体]这些杂质对于药物的纯度和稳定性研究至关重要,也是药物研发过程中不可或缺的一部分[/font][font=宋体]。[img=,602,518]https://ng1.17img.cn/bbsfiles/images/2024/02/202402192110007699_8786_6381607_3.png!w602x518.jpg[/img][/font][font=宋体][color=#05073b][back=#fdfdfe] 广州[/back][/color][/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]佳途科技[/back][/color][/font][font=宋体][color=#05073b][back=#fdfdfe]股份有限公司[/back][/color][/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]深知药物研发与质量控制的重要性[/back][/color][/font][font=宋体][font=宋体],[/font][font=Calibri]CATO[/font][font=宋体]标准品厂家,提供来那替尼全套[/font][/font][font=宋体]的[/font][font=宋体]杂质,为客户提供更加精准、可靠的分析标准品,助力药物研发事业的快速发展[/font][font=宋体],[/font][font=宋体]以满足客户在药物研发和质量控制方面的需求。[/font]
前些日子,接到一石墨块状样品,要求使用ICP-OES测量其中的杂质含量,初步考虑是放到马弗炉内灰化样品,然后用稀盐酸复溶。测量结果出来后,担心灰化过程使得大部分元素损失,请问各位,有什么其他方法样品消解呢
莫西沙星有关物质分析方法采用USP43制剂方法测定,色谱柱:Inertsil Phenyl 4.0*250mm,5μm,其中杂质A的校正因子0.70,药典方法1.89.相差很大,大家有没有遇到这个问题?
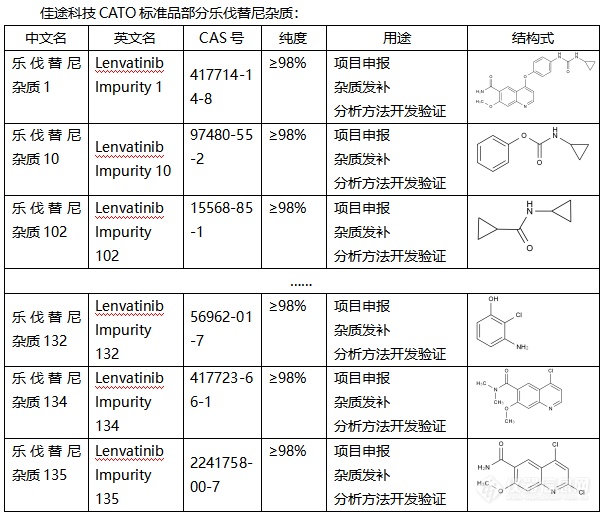
乐伐替尼,作为现代医学的瑰宝,广泛应用于肿瘤治疗领域。然而,就像其他药物一样,乐伐替尼在生产过程中也可能会产生杂质。这些微小的杂质,虽然量少,却可能对药物的疗效和安全性产生不可忽视的影响。为了确保乐伐替尼的纯净与安全,科学家们引入了CATO标准品进行杂质分析。CATO标准品,就像一把精准的尺子,能够帮助研究人员准确地检测和衡量乐伐替尼中的杂质。通过对比和分析,我们可以清楚地了解杂质的种类、数量以及可能对药物产生的影响。这项应用研究不仅提升了乐伐替尼的生产质量,更为患者的安全用药提供了有力保障。借助CATO标准品,我们能够及时发现并控制杂质,确保每一颗乐伐替尼都是纯净、有效的。未来,随着科学技术的不断进步,我们期待看到更多关于乐伐替尼杂质分析的研究成果,为患者带来更加安全、可靠的治疗方案。同时,也期待CATO标准品在更多药物杂质分析中发挥重要作用,守护人类的健康与安全。[img=,603,515]https://ng1.17img.cn/bbsfiles/images/2024/02/202402021836237186_8744_6381568_3.png!w603x515.jpg[/img]广州佳途科技股份有限公司是一家专业的CATO标准品生产厂家,我们目前库存有全套乐伐替尼杂质,能够提供相应的系列图谱和产品COA证书,并支持溯源。我们公司已经通过了国内外双ISO 17034质量体系认证,欢迎广大客户选购。
[center]三家制药企业被检出不合格药品[/center] 国家食品药品监督管理局12月8日发布2008年第三期药品质量公告。锦州九天药业有限责任公司、四川锡成药业有限公司生产的茶碱制剂以及重庆科瑞制药有限责任公司生产的尼莫地平制剂等相关批次药品经检验为不合格产品。 根据2008年国家药品评价抽验计划安排,国家食品药品监督管理局组织对乙型脑炎减毒活疫苗、麻疹减毒活疫苗两个生物制品,清开灵制剂、茶碱制剂、尼莫地平制剂及硝酸甘油片4个药品品种进行了全国评价抽验。 乙型脑炎减毒活疫苗和麻疹减毒活疫苗的评价抽验,共抽取样品103批,经中国药品生物制品检定所检验全部符合标准规定。 对清开灵制剂、茶碱制剂、尼莫地平制剂及硝酸甘油片4个品种的评价性抽验,共抽取样品1751批,分别经广东省、四川省、湖南省和天津市药品(食品)检验所检验,清开灵制剂、硝酸甘油片全部符合标准规定,尼莫地平制剂、茶碱制剂共有13个批次(涉及两个品种)不符合标准规定。 其中,此次尼莫地平制剂(片、胶囊、缓释片、缓释胶囊、注射液)抽样覆盖率为85.7%,经湖南省药品检验所检验,有4批次不符合标准规定,均为重庆科瑞制药有限责任公司生产(批号:070501),不合格项目为溶出度检查;茶碱制剂(缓释片、缓释胶囊、控释胶囊)抽样覆盖率为40.4%,经四川省食品药品检验所检验,有9批次不符合标准规定,锦州九天药业有限责任公司生产的批号为20071001的4批次,不合格项目为释放度检查;四川锡成药业有限公司生产的批号为080101的5批次,有4批次不合格项目为释放度检查,1批不合格项目为释放度和重量差异检查。 据悉,国家食品药品监督管理局已发出通知,要求地方食品药品监督管理部门对本期质量公告中不合格药品的被抽样单位进行查处,并继续组织对不合格品种进行跟踪抽样检验。 信息来源:健康报网
有第三方可以测试五氧化铌金属杂质的单位吗?急需!!QQ 346805152
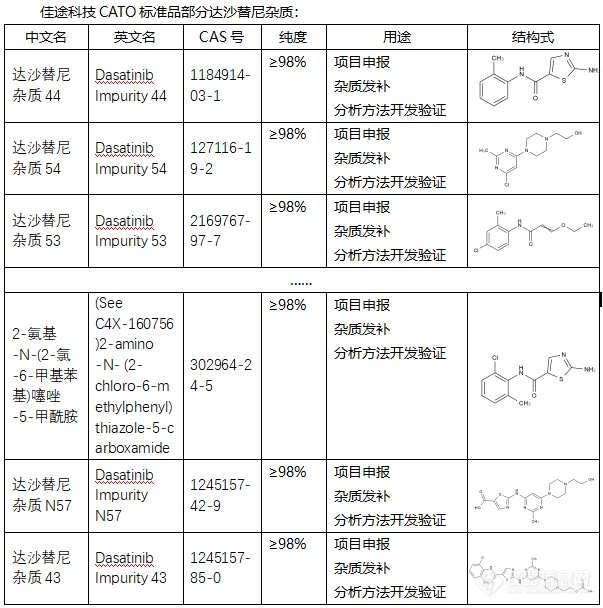
[font=宋体]◇达沙替尼[/font][font=宋体]杂质[/font][font=宋体] 达沙替尼[/font][font=宋体],[/font][font=宋体]其英文名为[/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]Dasatinib[/back][/color][/font][font=宋体][color=#05073b][back=#fdfdfe],)是一种创新的第二代双重酪氨酸激酶抑制剂(TKI),也被称作DASA锡IB或商品名SPRYCEL(施达赛)。[/back][/color][/font][font=宋体]达沙替尼[/font][font=宋体][font=宋体]杂质过抑制[/font][font=Calibri]BCR-ABL[/font][font=宋体]蛋白的活性来发挥治疗作用。达沙替尼能够与[/font][font=Calibri]BCR-ABL[/font][font=宋体]蛋白结合并抑制其激酶活性,从而阻断白细胞的异常增殖,并促进正常白细胞的生成。[/font][/font][font=宋体][font=Calibri] CATO[/font][font=宋体]标准品提供的达沙替尼杂质用途主要是用于分析化学物质和质量控制的化学物质。[img=,603,608]https://ng1.17img.cn/bbsfiles/images/2024/02/202402062123365450_9441_6381607_3.png!w603x608.jpg[/img][/font][/font][font=宋体][font=宋体] 广州佳途科技股份有限公司,[/font][font=Calibri]CATO[/font][font=宋体]标准品厂家,提供达沙替尼全套[/font][/font][font=宋体]的[/font][font=宋体]杂质,通过全面的检测、高效的沟通、专业的服务和完善的售后,确保所有产品均能现货供应[/font][font=宋体],[/font][font=宋体]致力于为客户提供高质量的产品和优质的服务,以满足客户在药物研发和质量控制方面的需求。[/font]
铅酸废水处理后用石墨炉法测铅含量,可是杂质太高,消解完还是杂质高。可能是什么情况?要怎么办?消解是用40ml水样加5ml浓硝酸,150℃加盖2h,然后加热到近干,用水配到40ml。
[color=#333333]机械杂质指石油或油品中所有不溶于油和规定溶剂的沉淀或 悬浮物质,如泥砂、尘土、铁屑、纤维和某些不熔性盐类,这些 杂质是在开采、精制、储存或使用过程中带进来的。机械杂质含 量是许多油品的一项质量指标。对于轻质油来说,机械杂质会堵 塞油路,促使生胶或腐蚀,锅炉燃料中的机械杂质,将会堵塞喷 嘴,降低燃烧效率,增加燃料消耗;润滑油中的机械杂质则会破 坏油膜,增加磨损,堵塞油滤器,促进生成积炭等。[/color]