苯乙酸是医药、农药、香料等有机合成的中间体。在医药工业中用于青霉素、地巴唑等药物的生产。苯乙酸经氯化、酯化得到α-氯代苯乙酸乙酯,用于稻丰散和乙基稻丰散的生产,这两种农药是广谱性有机磷杀虫剂。苯乙酸本身也是农药植物生长激素。苯乙酸广泛存在于葡萄、草莓、可可、绿茶、蜂蜜等中。苯乙酸在低浓度时具有甜蜂蜜味,在1ppm以下仍具有甜味,是一种重要的香料成分。苯乙酸还具有很强的杀菌作用。
如题,在合成中有一步反应是用邻羟基苯乙酸制备其二钠盐,其中产物中可能含有的成分有邻羟基苯乙酸、邻羟基苯乙酸的一钠盐、二钠盐,请问如何建立检测方法将其分离呢?谢谢! 试过液相的方法,但是分不开,也试过双相滴定,但是里面还有过量的NaOH,影响结果,也试过用酚羟基的显色反应,但这个又太灵敏了,无法定量。请大家指导一下吧。
求助各位同行:苯乙酸的国标或行标(HGB3444-62)全文.多谢了.我的邮箱:zjp9933@163.com
[color=#444444]甲酰基苯乙酸甲酯的色谱含量测试中。由于甲酰基苯乙酸甲酯会有醇酮互变性质,在液相色谱(乙腈:水=50:50)下出现三个峰。但是在LC——MS下从第一个峰开始到第三个峰这之间所有的时间都出现了M+1峰(包括峰之间的)。谁能告诉我这是怎么回事。[/color][color=#444444]有哪个大侠做过甲酰基苯乙酸甲酯的含量测试的,求指导。[/color]
目前所做项目需要液相检测联苯乙腈(原料)和联苯乙酸(产物),但两者出峰时间一致,已尝试多种方法进行混合样分离,但始终只有一个尖峰显示,没有任何分离趋势,目前试过的方法有:甲醇:0.05%磷酸水=70:30(C-18长柱);乙腈:水=70:30;乙腈:0.1%氨水水溶液=70:30(NX-C18);甲醇:0.1%醋酸水=55:45(C18短柱)。求助是否有可行的方法能够较好的分离两种物质。谢谢。
请问从哪儿能查到海水中下面的杂质含量测定的方法:甲醇氯化石蜡-52乙二醇二乙二醇二甲基甲酰胺苯乙烯丙酮冰醋酸氯仿甲苯二甲苯1,4-丁二醇苯酚环氧乙烷
[color=#444444]求助一下啊!!!![/color][color=#444444]我做的羟基苯乙酸去送样,结果GC分析人员做出了两个峰,做了两次都是这样。[/color][color=#444444]我的样品应该是纯的,是分析方法不对,还是其它什么原因啊?有没有哪个遇到这个的情况呢?求助哈[/color]
异氰基乙酸乙酯和N,N-二甲基苯胺是否可以用[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]检测?有没有方法条件呢?
[font=Helvetica Neue,Helvetica,PingFang SC,Tahoma,Arial,sans-serif][size=14px][color=#333333]4-羟基苯乙酸酯[/color][/size][/font],[font=Helvetica Neue,Helvetica,PingFang SC,Tahoma,Arial,sans-serif][size=14px][color=#999999]CAS No.:[b]58556-55-1[/b][/color][/size][/font][font=Helvetica Neue,Helvetica,PingFang SC,Tahoma,Arial,sans-serif][size=14px][color=#999999]分子式:C[sub]1[/sub][sub]0[/sub]H[sub]1[/sub][sub]2[/sub]O[sub]3[/sub][/color][/size][/font]
测定乙酸乙酯残留,溶剂为二甲基亚砜,测定精密度,发现有一些溶剂峰没有出现,而有的溶剂峰却出现了。请教大家是怎么回事,应该主溶剂的峰都是应该出现的啊,而且很大。溶剂峰和乙酸乙酯峰分离度很好。乙酸乙酯出峰在10分钟,二甲基亚砜出峰在17分钟。
氧化器主要含异丙苯,测定其中所含杂质含量,主要杂质有二甲基苯甲醇,苯乙酮和过氧化氢异丙苯等,选用何种色谱柱?如何选择操作条件,我们要使用安捷伦1200液相色谱仪,
请问DMBC Acetate乙酸二甲基苄基原醇酯的质谱图是怎样的?CAS000151-05-3
完全按GB29708-2013的方法处理,衍生化后质谱检不出五氯苯乙酸酯,不知道哪里有问题!请做过这个项目的指点。
[color=#d40a00][size=2]维权声明:本文为[font=Times New Roman]11093661[/font]原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。[/size][/color] 青霉素发酵过程中利用液相分析对发酵液中的苯乙酸,效价检测存在着很是矛盾的主体,那就是发酵过程中的效价检测是批量检测,在检测过程中青霉素效价有高有低,这样就不利于药典中规定的标准品与待测品的含量大致相同的规定,这就不可能每做一个样品就做一个标准,这样不实际也不利于节约成本的。那么就需要我们做一个线性范围来使在实际检测的过程中的效价范围在线性范围类,这样就有利于测样的准确性。本人通过长期反复工作实践发现在青霉素发酵过程中发酵液的稀释倍数在100倍以上时,出现了这样一个情况:在检测效价的过程中对苯乙酸检测的结果很不稳定,特别是长期工作的液相更是如此,本人在工作中试验发现原因主要是基线的漂移造成了这个现象。而检测苯乙酸对生产发酵中的地位相当重要,苯乙酸是青霉素发酵过程中的主要原材料之一,而苯乙酸的多少又决定了发酵水平高低。所以说苯乙酸的检测也同样重要。 而效价,苯乙酸是同时检测出来的,如果稀释倍数大于100后解决了效价检测的准确性得到了提高,但是苯乙酸的检测准确性也就低了。所以这个矛盾主体也就出现了。本人在长期的检测中实践发现如果分开来检测,也就是两次检测,而对于两次检测过程中的效价与苯乙酸两种物质稀释倍数采取不同的稀释倍数这样有利于检测结果的准确性。或者对苯乙酸检测采取[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]检测同时稀释倍数根据苯乙酸残量的多少采取不同的稀释倍数这样有利于检测结果的准确性,重现性。而根据本人了解某特大型青霉素发酵公司也就是只是对效价采取的稀释倍数的不同,这样提高了效价的准确性而导致了苯乙酸残量的检测的准确性也就降低了,导致发酵水平无法与成都某特大型青霉素发酵公司的水平相比较。这就说明了苯乙酸检测尤为重于效价检测。而分两次检测或气,液相同时检测这样不利于成本降低,本人通过长期的摸索,比较发现利用苯乙酸的多少来决定稀释倍数后,再根据效价的高低采取不同的标准品的含量,这样就利于检测的准确性与成本的降低——相当于分段检测。 本人事先声明这个纯属个人自己摸索试验得出的结论,在实际生产,检测中虽然得到了应用,但由于自己的试验结果,水平有限所以具体过程没有完全介绍,十分抱歉。
如题,在2.9min时乙酸乙酯出峰,在17min左右N,N-二甲基乙酰胺出峰,出峰时间为10min,峰形特别不好,四分之一圆形,我用的是岛津-2010,进样口和检测器温度均为200度,柱温为70度,分流比为10,急求!!!谢谢各位前辈!!
谁告诉我下 巯基乙酸异辛酯 二甲基二氯锡 用GC什么检测器?什么柱子分析啊?
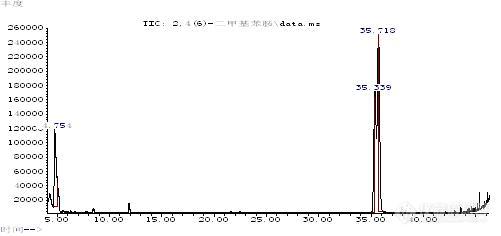
2,4-二甲基苯胺和2,6-二甲基苯胺的鉴别2,4-二甲基苯胺和2,6-二甲基苯胺同属于国家强制标准GB18401-2003附录C中所列的还原条件下染料中不允许分解出的23种芳香胺之一,二者又属于同分异构体,沸点和极性都很接近,故在检测过程中很难鉴别。目前,对于两者的分离鉴别主要靠液相色谱来实现,而使用气-质联用仪来鉴别两者还没有很好的方法。而针对有害芳香胺的气相色谱-质谱检测方法,大多采用非极性或极性较弱的色谱柱,如HP-5MS,DB-5MS,DB-35MS,这些色谱柱普遍存在的缺点是对常见的芳香胺异构体不能很好的分离。由于2,4-二甲基苯胺和2,6-二甲基苯胺沸点太接近,单纯依靠两者的沸点差异来实现其分离鉴别是有一定难度的。于是,作者考虑采用中等极性色谱柱DB-17MS(固定相等同于50%苯甲基聚硅氧烷),除了利用2,4-二甲基苯胺和2,6-二甲基苯胺的沸点差异外,再利用中等极性柱对于二者的保留作用差异来研究二者的分离鉴别。通过改善优化色谱条件,作者使用中等极性色谱柱DB-17MS,同时使用三阶程序升温,实现了2,4-二甲基苯胺和2,6-二甲基苯胺的较好分离。1 试验1.1 仪器与试剂气相色谱-质谱联用仪(GC-MS):Agilent 7890A/5975C,美国Agilent公司毛细管柱:DB-17MS柱(30m×0.25mm×0.25μm)叔丁基甲醚 分析纯 国药集团化学试剂有限公司甲醇 色谱纯 美国Fisher公司旋转蒸发仪 上海亚荣生化仪器厂2,4-二甲基苯胺和2,6-二甲基苯胺均为德国Dr.Ehrenstorfer公司。1.2 试样的制备分别称取适量的2,4-二甲基苯胺和2,6-二甲基苯胺,以甲醇为溶剂分别配制适宜浓度的2,4-二甲基苯胺溶液、2,6-二甲基苯胺溶液和2,4-二甲基苯胺和2,6-二甲基苯胺混合溶液。1.3 仪器操作条件色谱柱:DB-17MS 30m×0.25mm×0.25μm;温度:进样口220℃ ;辅助器280℃;离子源230℃ ;四极杆温度:150℃;柱温:40℃保持2分钟,以15℃/分钟升温至[/font
[font=&][size=18px]N,N-二甲基乙酰胺又称乙酰基二甲胺、乙酰二甲胺,简称DMAC,是一种非质子高极性溶剂,有微氨气味,溶解力很强,可溶解的物质范围很广,能与水、芳香族化合物、酯、酮、醇、醚、苯和三氯甲烷等任意混溶,且能使化合物分子活化,因此广泛用作溶剂及催化剂。在溶剂方面作为高沸点、高闪点、热稳定性高、化学性稳定的溶剂,可用于聚丙烯腈的抽丝溶剂、合成树脂及天然树脂、甲酸乙烯酯、乙烯基吡啶等共聚物及芳烃羧酸的溶剂;在催化剂方面可用于尿素加热制氰尿酸、卤代烷与金属氰化物反应制腈、乙炔钠与卤代烷反应制烷基炔、有机卤化物与氰酸盐反应制异氰酸酯等过程。N,N-二甲基乙酰胺还可用作电解溶剂及摄影用成色剂的溶剂、脱油漆剂、有机合成原料、农药及医药原料。从C8馏分中分离苯乙烯的萃取蒸馏溶剂等。[/size][/font]
我在使用凝胶色谱仪时,采用DMAC(二甲基乙酰胺)为溶剂时,在25度下的聚苯乙烯的K和a是多少呀?
我们实验室现在刚开始做偶氮,我想问下各位大虾你们做偶氮的时候2,4-二甲基苯胺和2,6-二甲基苯胺能分开吗?我们用的是Rtx-5ms的柱子。哪位大侠告知我下,我会不胜感激的!谢谢!我们现在做标准曲线的时间两种物质分不开。http://simg.instrument.com.cn/bbs/images/brow/em09509.gif
用二甲基亚砜做溶剂溶样,一般用什么类型的柱子不会出现干扰峰啊(测定乙酸乙酯和酒精),各位都说说啊,
我做中控转化率,需要把二甲基亚砜与间羧基苯甲酸分离开,现正在寻找最佳的流动相比例.原先的比例是70+30+0.1+0.2(甲醇+水+醋酸+磷酸),但是分不开,出现包峰.望各位指导.
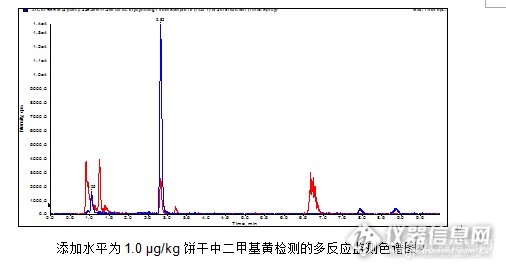
食品中二甲基黄的测定解决方案二甲基黄属于亲脂性偶氮染料,用作显色剂可测定硒、钌、碘、砷、铜和溴酸根等。工业上常用于油漆、鞋油和纺织品等的染色。因具神经及生殖毒性,长期摄取二甲基黄会增加罹患肝癌、肺癌、膀胱癌风险,国际癌症研究署(IARC)已将其列为2B等级的致癌物,禁止作为食品添加剂使用。但是,我国台湾地区不断报道出在豆干中检出了二甲基黄。目前二甲基黄的测定方法主要有气相色谱串联质谱法,固相萃取-超高效液相串联质谱。我们采用的是固相萃取-超高效液相串联质谱。方法优势:迪马科技开发的《食品中二甲基黄的测定》采用固相萃取-超高效液相串联质谱测定食品中的二甲基黄,以乙酸乙酯和水为提取液,采用ProElutDMY固相萃取柱净化样品,通过UPLC检测;本方案前处理步骤简便、操作简单、净化效果好,重现性好,回收率高。以下为详细解决方案,敬请参考!食品中二甲基黄的测定1、适用范围 适用于豆干、糕点和饼干中二甲基黄的检测,方法检出限是0.03μg/kg,定量限是0.1 μg/kg。2、提取取1.0 g样品(易乳化的样品需加1.0 g氯化钠),加入2 mL水,涡旋混匀,加入5 mL乙酸乙酯,振荡5 min,6000 rpm下离心2 min,精密量取2.5 mL上清液待净化。3、净化——ProElut DMY 3 mL(Cat.#65914) a活 化:3 mL乙酸乙酯活化;b上 样:c 淋 洗:加入待净化液,弃去流出液;加入3 mL乙酸乙酯,弃去流出液(推干小柱);d洗 脱:加入4 mL10%氨水甲醇,收集流出液;e重新溶解:将流出液在50 ℃下氮吹至干,用流动相定容至1 mL,过0.22 μm微孔滤膜,供LC-MS分析。4、色谱条件4.1UPLC 条件:色谱柱:Endeavosil C18,100× 2.1 mm,1.8 μm (Cat#:87003)流 速:0.2 mL/min进样量:5 μL柱 温:35 ℃流动相: A:0.1%甲酸水 B:乙腈 A:B=20:804.2质谱条件:电离模式:ESI 扫描方式:正离子扫描检测方式:多反应监测 电喷雾电压:5500 V雾化气压力:50 psi 辅助气压力:50 psi气帘气压力:20 psi 离子源温度:500 ℃定性离子对、定量离子对、碰撞气能量及去簇电压见下表 目标物 定性离子对 定量离子对 碰撞气能量/eV 去簇电压/ V (m/z) (m/z) (母离子/子离子) (母离子/子离子) 二甲基黄 226.3/77.2 226.2/77.2 30 74 226.3/134.1 30 5、添加回收结果食品中二甲基黄的LC-MS检测添加回收结果 基质 添加水平(μg/kg) 回收率(%) 豆干 1.0 100.08 糕点 1.0 90.75 饼干 1.0 108.63 http://ng1.17img.cn/bbsfiles/images/2016/02/201602021751_584170_708_3.pnghttp://ng1.17img.cn/bbsfiles/images/2016/02/201602021752_584171_708_3.pnghttp://ng1.17img.cn/bbsfiles/images/2016/02/201602021752_584172_708_3.pnghttp://ng1.17img.cn/bbsfiles/images/2016/02/201602021752_584173_708_3.png食品中二甲基黄的测定相关产品信息: 货号 名称 规格 样品前处理 65914 ProElut DMY 3 mL, 50/pk 244358 12管防交叉污染真空SPE萃取装置 12位 4803 1,3,6mL柱管通用连接器 15/pk 4806 考克(控制流量) [/
如题,发现这两个物质在DB-5的柱子上是分不开的,也看到有文献说液相可以分开的,试着做了一下,用甲醇和0.1%磷酸作为流动相也分不开,柱子是eclipse C18的,15mm长的。另:为什么标准中只限制了这两种二甲基苯胺,如果将其他异构体的二甲基苯胺误判为2,4-或2,6-怎么办?如何区分?
用YC/T207-2014方法,测混合标液,苯乙烯 2-乙氧基乙基乙酸酯 邻-二甲苯分离不好还,出现了重合峰情况,用谱库搜出来是间二甲苯,邻二甲苯甲苯去哪里了呢?[img]https://ng1.17img.cn/bbsfiles/images/2022/12/202212221658210017_6074_5898744_3.png[/img][img]https://ng1.17img.cn/bbsfiles/images/2022/12/202212221658214942_5520_5898744_3.png[/img]
用YC/T207-2014方法,测混合标液,苯乙烯 2-乙氧基乙基乙酸酯 邻-二甲苯分离不好还,出现了重合峰情况,用谱库搜出来是间二甲苯,邻二甲苯甲苯去哪里了呢?![img]https://ng1.17img.cn/bbsfiles/images/2022/12/202212221603511087_6024_5898744_3.png[/img][img]https://ng1.17img.cn/bbsfiles/images/2022/12/202212221603511511_1108_5898744_3.png[/img]
配制完N,N二甲基对苯二胺,溶液应该呈紫色,为什么这次溶液呈透明淡黄色?
请问上海地区有[B]一甲基胂酸和二甲基胂酸,Fluck [/B]试剂卖吗?急需,请联系!谢谢!
我需要几十克的3,5-二甲基-2-氨基苯甲酸,请问哪里有卖的
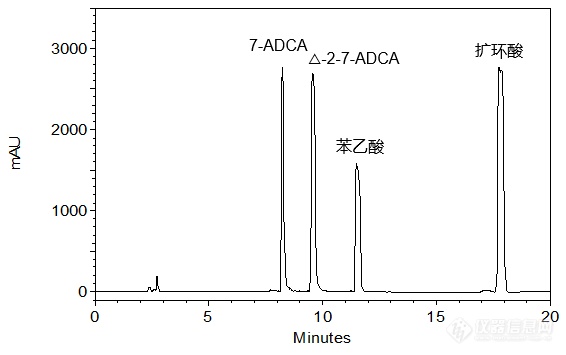
[align=center][b]4种头孢中间体的共同分析[/b][/align][align=right][b]——7-ADCA、△-2-7-ADCA、苯乙酸及扩环酸的分析[/b][/align][align=right][b][/b][/align]客户提供了7-ADCA(7-氨基去乙酰氧基头孢烷酸),△-2-7-ADCA、苯乙酸及扩环酸原料,希望本实验室依据客户所提供的色谱条件筛选合适的C[sub]18[/sub]色谱柱,实现以上4种化合物的稳定良好分析。本实验室参考客户提供的色谱条件,首先尝试使用经过聚合物包被处理的中等极性色谱柱——CAPCELL PAK C[sub]18[/sub] MGII对客户所提供样品进行分析,使用PDA检测器进行检测。如图1,在高浓度大体积进样的情况下,各色谱峰发生严重过载现象,出现平头峰;如图2,降低进样体积至5 μL可得到相对良好峰形,且各组分间能够得到良好分离,分离度均在10.0以上(结果详见表1)。[align=center][img=,566,355]http://ng1.17img.cn/bbsfiles/images/2018/05/201805101537444868_8925_2222981_3.png!w566x355.jpg[/img][/align][align=center]图1 CAPCELL PAK C[sub]18 [/sub]MGII色谱柱分析结果(进样量:50 μL)[/align][align=center][img=,575,365]http://ng1.17img.cn/bbsfiles/images/2018/05/201805101545063985_5910_2222981_3.png!w575x365.jpg[/img][/align][align=center]图2 CAPCELL PAK C[sub]18 [/sub]MGII色谱柱分析结果(进样量:5 μL)[/align][align=center] [/align][align=center]表1 CAPCELL PAK C[sub]18[/sub] MGII分析结果详表(进样量:5 μL)[/align][align=center][img=,553,136]http://ng1.17img.cn/bbsfiles/images/2018/05/201805101537465105_7074_2222981_3.png!w553x136.jpg[/img][/align][align=center][/align][align=left][img=,579,319]http://ng1.17img.cn/bbsfiles/images/2018/05/201805101545307700_4011_2222981_3.png!w579x319.jpg[/img][/align][align=left][/align][align=left]为使客户有更多色谱柱选择,本实验室也尝试了能够在纯水系流动相下稳定使用的高极性色谱柱——CAPCELL PAK C[sub]18[/sub] AQ进行分析。如图3,几种头孢中间体的整体保留有所增强,而高浓度上样仍会出现与MGII色谱柱相似的过载现象;如图4,降低进样体积进行分析,可得到良好结果,同时发现扩环酸有一定程度的拖尾(见表2)。[/align][align=center][/align][align=center][img=,527,377]http://ng1.17img.cn/bbsfiles/images/2018/05/201805101546103944_1716_2222981_3.png!w527x377.jpg[/img][/align][align=center]图3 CAPCELL PAK C[sub]18 [/sub]AQ色谱柱分析结果(进样量:50 μL)[/align][align=center][img=,525,374]http://ng1.17img.cn/bbsfiles/images/2018/05/201805101546123571_3070_2222981_3.png!w525x374.jpg[/img][/align][align=center]图4 CAPCELL PAK C[sub]18 [/sub]AQ色谱柱分析结果(进样量:5 μL)[/align][align=center] [/align][align=center]表2 CAPCELL PAK C[sub]18 [/sub]AQ分析结果详表(进样量:5 μL)[/align][align=center][img=,558,135]http://ng1.17img.cn/bbsfiles/images/2018/05/201805101546125551_7090_2222981_3.png!w558x135.jpg[/img][/align][align=center][/align][align=left][img=,577,319]http://ng1.17img.cn/bbsfiles/images/2018/05/201805101547424196_8227_2222981_3.png!w577x319.jpg[/img][/align][align=left][/align][align=left]综上实验结果,使用中等极性色谱柱CAPCELL PAK C[sub]18 [/sub]MGII S5 4.6 mm i.d. × 250 mm和高极性色谱柱CAPCELL PAK C[sub]18[/sub] AQ S5 4.6 mm i.d. × 250 mm,以磷酸盐缓冲液(pH 6.0)-乙腈为流动相体系,在30°C柱温条件下进行梯度分析,均能够实现7-ADCA、△-2-7-ADCA、苯乙酸和扩环酸的良好分离,其中,CAPCELL PAK C[sub]18[/sub] MGII色谱柱所得峰形更佳。[/align]