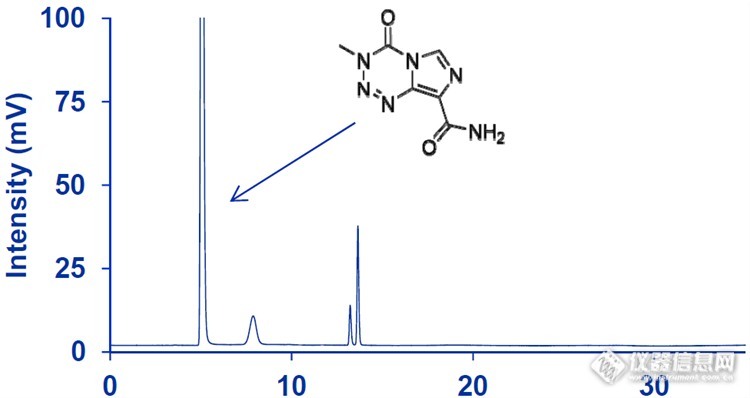
1、前言抗癌药物中,有一类影响DNA和RNA合成而抑制细胞生长的药物,如阿扎胞苷、替莫唑胺等,此类化合物极性大,在反相色谱柱难有保留,给准确的HPLC分析带来麻烦,ZIC-HILIC提供了理想的解决方案。2、应用(1). 阿扎胞苷和有关物质分析色谱柱:ZIC®-HILIC 5um 150*4.6mm (1.50455.0001)流动相:10% (10mM乙酸铵) : 90%乙腈流速:2.0 mL/min检测:UV242nm进样量: 10μL柱温: 25 °Chttp://ng1.17img.cn/bbsfiles/images/2014/03/201403201259_493761_1837380_3.png化合物出峰时间拖尾因子分离度1阿扎胞苷14.21.1—2杂质16.71.02.5(2). 替莫唑胺和有关物质分析色谱柱:ZIC®-HILIC 5um 250*4.6mm (1.50458.0001)流动相:时间(min) A 40mM乙酸铵 B 乙腈0.0min 3% 97%2.0min 3% 97%25.0min 50% 50%30.0min 3% 97%35.0min 3% 97%流速:0.8 mL/min检测:UV254nm进样量: 10μL柱温: 25 °Chttp://ng1.17img.cn/bbsfiles/images/2014/03/201403201301_493762_1837380_3.png化合物出峰时间拖尾因子分离度1替莫唑胺5.11.3[/al
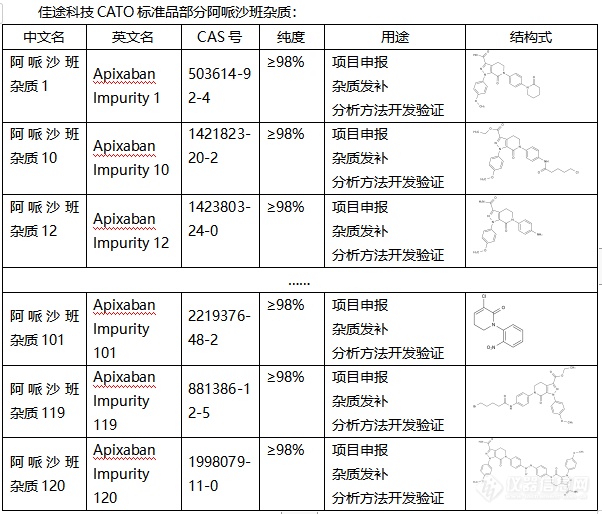
◇关于阿哌沙班杂质 阿哌沙班杂质是用于髋关节或膝关节择期置换术的成年患者,预防静脉血栓栓塞的杂质,阿哌沙班是一种结构新颖的中性双环吡唑,分子量为459.5 g/mol,水溶性为 40–50 μg/mL,Caco-2细胞渗透率为0.9?×?10?6 cm/s。阿哌沙班是通过抑制凝血因子Xa来发挥抗凝作用,阿哌沙班杂质的吸收主要发生在小肠。与其它的杂质相比,阿哌沙班杂质疗效更好,安全性更高。[font=UICTFontTextStyleBody]CATO[/font]标准品提供的[font=宋体]阿哌沙班杂质[/font][font=宋体],是抗凝[/font][font=宋体][font=宋体]剂领域的[/font]“领头羊”[/font][font=宋体]。[img=,602,514]https://ng1.17img.cn/bbsfiles/images/2024/02/202402040843332660_3775_6381607_3.png!w602x514.jpg[/img][/font]
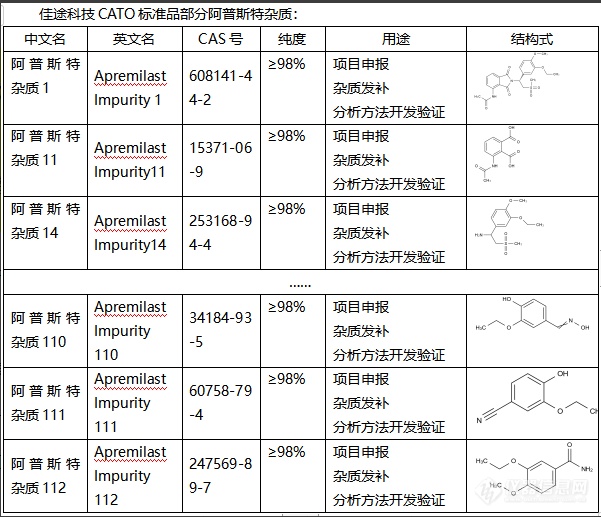
阿普斯特杂质(Acceptor impurities)在半导体中起到了非常关键的作用。1. 提供洞:阿普斯特杂质是电子受主,它会吸收自由电子,形成空穴(或称为“洞”)。这些空穴可以移动,起到电流传导的作用。因此,添加阿普斯特杂质后,半导体的导电性能会增强。2. 形成P型半导体:当阿普斯特杂质的浓度足够高时,半导体中的空穴数量将超过电子数量,形成了主导电流传导的是空穴的P型半导体。3. 局域能级:阿普斯特杂质也能产生在能带间的局域态,充当了能量级的“桥梁”,使电子更容易通过能阶间跃迁,也有助于电流的传导。CATO标准品改变半导体性质:通过改变阿普斯特杂质的种类和浓度,可以改变半导体的性质,如导电性、光学性质、磁性等,使之满足特定的使用需求。[img=,601,517]https://ng1.17img.cn/bbsfiles/images/2024/02/202402021700369834_2567_6381668_3.png!w601x517.jpg[/img]
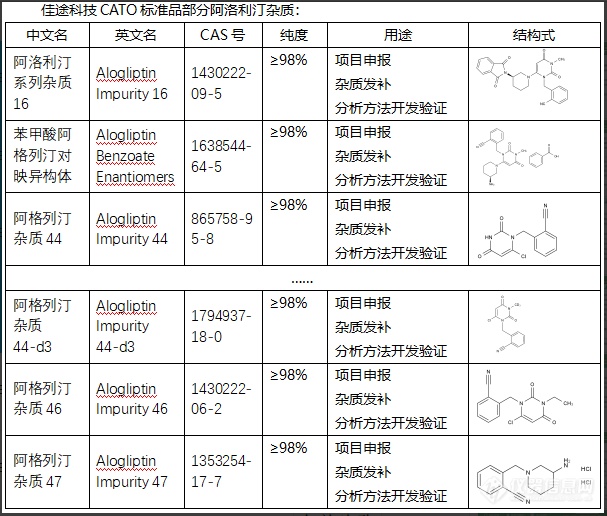
阿洛利汀杂质可以作为标准物质,用于评价阿洛利汀的质量和纯度。通过测量此类杂质的含量,可以对阿洛利汀的生产过程进行控制和优化,以制造出更优质的药物。此外,某些类型的杂质还可能被用作药物的标记物,以跟踪药物在体内的分布和代谢。CATO标准品目前的药品生产技术已经可以有效地降低杂质的含量,保证药品的质量和安全性。任何药物在上市之前,都需要经过严格的质量控制检测,以确保其杂质含量符合规定的标准。此外,药品在上市后也会进行定期的质量监控,以确保其安全性和效力。[img=,607,516]https://ng1.17img.cn/bbsfiles/images/2024/02/202402041447097355_1644_6381668_3.png!w607x516.jpg[/img]
各位高手:我现在遇到很棘手的问题,希望大家帮帮忙,着急啊。草甘膦含量95%以上,杂质含量0.5%以上的都要能够检测出。杂质包括:甘氨酸,亚氨基二乙酸,双甘膦,增甘膦。整个检测时间不超过15分钟,并且检测方法不能太复杂。检测器可为紫外或者DAD或ELSD或其他都可以。希望各位高手指点指点阿。我都快急疯了。谢谢阿。
阿伐那非杂质是阿伐那非的同分异构体或相关化合物,其纯度、含量和杂质情况对阿伐那非的药效和安全性有重要影响。在药物研发和生产过程中,需要使用标准品来检测和鉴定阿伐那非及其杂质的性质和含量。COTO标准品是一种高纯度的标准物质,用于测定阿伐那非及其杂质的纯度、含量和化学性质。通过与COTO标准品进行对比和分析,可以确定阿伐那非及其杂质的结构、组成和含量,从而保证阿伐那非的质量和安全性。在药物研发和生产过程中,COTO标准品的使用非常重要。它可以提供可靠的参照物,用于质量控制、药物分析和化学计量学研究。通过使用COTO标准品,可以确保阿伐那非及其杂质的准确性和可靠性,为药物的安全性和有效性提供保障。总的来说,COTO标准品在阿伐那非杂质的研究和控制中具有重要作用。通过使用COTO标准品,可以更好地了解阿伐那非及其杂质的性质和含量,从而确保药物的安全和有效性。同时,也需要加强生产过程中的管理和监督,加强质量标准和监管措施的执行力度,确保药物质量和安全。
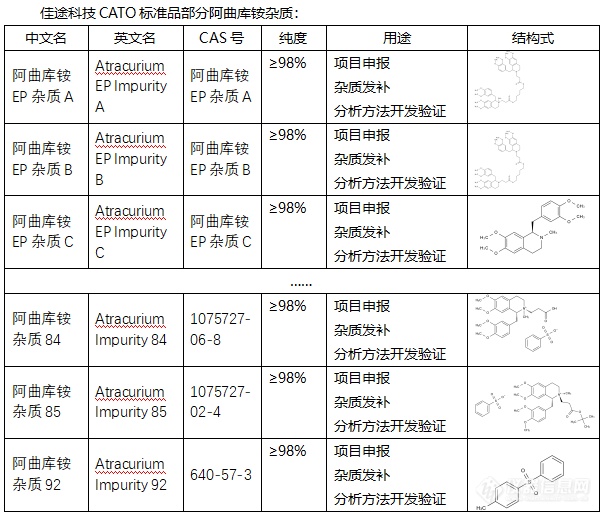
◇关于阿曲库铵杂质 阿曲库铵杂质是一种神经肌肉接头阻断剂的杂质,阿曲库铵杂质主要通过竞争胆碱能受体,来阻断乙酰胆碱的传递而起作用,并且可以被新斯的明等抗胆碱酯酶药所逆转。阿曲库铵杂质可以作为麻醉辅助药,不仅可以起镇静作用、松弛骨骼肌,还适用于气管插管时所需的肌肉松弛。阿曲库铵杂质静注后,95%主要分布在胆汁、尿液、[font=.pingfang sc]粪便及呼出气体,剩余的约[/font]5%集中于肝脏。[font=UICTFontTextStyleBody]CATO[/font]标准品提供的[font=宋体]阿曲库铵杂质[/font][font=宋体],可以用于手术的全麻的辅助作用。[img=,603,516]https://ng1.17img.cn/bbsfiles/images/2024/02/202402041034214652_487_6381607_3.png!w603x516.jpg[/img][/font]
最近我们在做阿伐他汀中3位上的羟基变成甲氧基那个杂质,我们判断它相对阿伐他汀峰的相对保留时间是0.89,但是阿伐他汀前面一直没有峰出现,我想请我问下是不是我们的判断是错误的,还是我们这个杂质一直没有做出来。

[font=宋体] 阿戈美拉汀杂质是在阿戈美拉汀的生产或保存过程中产生的非目标化合物。这些杂质可能会影响阿戈美拉汀的纯度和药效。阿戈美拉汀[/font][font=宋体]在临床上[/font][font=宋体][font=宋体]是一种治疗抑郁症的药物,属于褪黑素受体激动剂和[/font][font=Calibri]5-[/font][font=宋体]羟色胺受体拮抗剂。[/font][/font][font=宋体][font=宋体] 阿戈美拉汀杂质有多种类型,每一种都具有不同的化学特性,如[/font][font=Calibri]CAS[/font][font=宋体]号、分子式、分子量等。例如,阿戈美拉汀杂质[/font][font=Calibri]7-Desmethyl-3-hydroxyagomelatine[/font][font=宋体]([/font][font=Calibri]3-Hydroxy-7-desmethyl agomelatine[/font][font=宋体])是[/font][font=Calibri]Agomelatine[/font][font=宋体]的代谢产物,其[/font][font=Calibri]CAS[/font][font=宋体]号为[/font][font=Calibri]166526-99-4[/font][font=宋体],纯度为[/font][font=Calibri]98%[/font][font=宋体],具有特定的化学结构和性质。另一种阿戈美拉汀杂质是[/font][font=Calibri]AgoMelatine DiMer Urea[/font][font=宋体],其[/font][font=Calibri]CAS[/font][font=宋体]号为[/font][font=Calibri]185421-27-6[/font][font=宋体]。[/font][font=Calibri]CATO[/font][font=宋体]标准品提供的阿戈美拉汀全套的杂质[/font][/font][font=宋体],[/font][font=宋体]这些杂质对于药物的纯度和稳定性研究至关重要,也是药物研发过程中不可或缺的一部分[/font][font=宋体]。[img=,606,514]https://ng1.17img.cn/bbsfiles/images/2024/02/202402182106267012_9724_6381607_3.png!w606x514.jpg[/img][/font][font=宋体][color=#05073b][back=#fdfdfe] 广州[/back][/color][/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]佳途科技[/back][/color][/font][font=宋体][color=#05073b][back=#fdfdfe]股份有限公司[/back][/color][/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]深知药物研发与质量控制的重要性[/back][/color][/font][font=宋体][font=宋体],[/font][font=Calibri]CATO[/font][font=宋体]标准品厂家,提供阿戈美拉汀全套[/font][/font][font=宋体]的[/font][font=宋体]杂质,为客户提供更加精准、可靠的分析标准品,助力药物研发事业的快速发展[/font][font=宋体],[/font][font=宋体]以满足客户在药物研发和质量控制方面的需求。[/font]
药典描述:分别精密量取供试品溶液、对照品溶液和系统适用性溶液各1μl注入气相色谱仪,记录色谱图,按内标法以峰面积计算,供试品含二甘醇与乙二醇均不得过0.025%;如有其他杂质,扣除内标峰按归一化法计算,单个未知杂质不得过0.1%;杂质总量(包含二甘醇、乙二醇)不得过1.0%。其中杂质总量应该是按面积归一法计算,还是由其他杂质+二甘醇、乙二醇(内标结果)?请问生产厂家和使用单位都是如何计算的?杂质总量前为分号!!!
甘油杂质中甘油的峰总是怪怪的,特丑,还分叉,不知大家做的怎么样,能否发张图看看
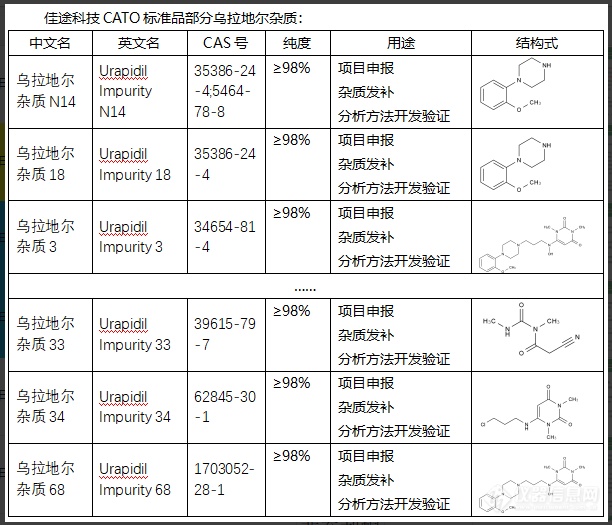
乌拉地尔(Uradil)是RNA分子中的一种核苷酸,通常聚合在RNA链上对编码蛋白质起重要作用。然而,乌拉地尔杂质通常被认为是DNA序列中的错误或错误的插入。乌拉地尔杂质的存在可能会导致DNA复制和转录的错误,从而导致基因表达的改变或突变,进而可能导致细胞功能异常,诱发一些健康问题,比如癌症等。由于这个原因,CATO标准品生物体内有专门的机制,例如尿苷DNA糖苷酶,可以检测并修复DNA中的乌拉地尔杂质,以维持DNA的稳定性和遗传信息的准确性。[img=,612,525]https://ng1.17img.cn/bbsfiles/images/2024/02/202402041442469549_3655_6381668_3.png!w612x525.jpg[/img]
(一)分析背景及色谱条件 红霉素是一种十四元大环内酯类抗生素,一直是临床上治疗革兰氏阳性菌感染的重要药物,半个世纪以来为人类提供了一条安全高效的用药途径。经过不断研究人们相继开发出了耐酸性好的第二代红霉素和不易引起细菌耐药性的第三代红霉素。阿奇霉素可以说是目前第二代红霉素中最具有活力的大环内酯类抗生素,其生产步骤简单,在国内外都具有很大的生产量,尤其在国内,在许多药厂都有生产。但与其它第二代大环内酯类抗生素相比阿奇霉素的HPLC分析一直是个难点,这也与其独特的十五元环结构有关系。而且我们经过试验发现不同色谱柱对其检测的结果差别很大,普通的C18柱无法保证效果,C18 BDS的色谱柱的检测结果也不是很好,我们尝试了几种不同的在C18柱基础上经过各种填料处理的色谱柱,其中包括了“极限”系列的色谱柱。 阿奇霉素分子式http://ng1.17img.cn/bbsfiles/images/2009/11/200911211508_185763_1916092_3.jpg 色谱条件:磷酸氢二钾盐水溶液与乙腈以45:55混合。检测波长210纳米,柱温30°C,流速1.0ml/min,进样量50微克。阿奇霉素样品取自上海某药厂提供的产品,其纯度在95%以上。色谱柱我们共尝试了五根:(1)普通C18柱,编号为1;(2)某品牌BDS C18柱,编号为2;(3)大连某国产色谱柱,编号3;(4)日本某色谱柱(药检所推荐)。编号4;(5)Ultimate XB-C18色谱柱,编号5.(二)试验结果 (1)http://ng1.17img.cn/bbsfiles/images/2009/11/200911211502_185756_1916092_3.jpg(2)http://ng1.17img.cn/bbsfiles/images/2009/11/200911211503_185757_1916092_3.jpg(3)http://ng1.17img.cn/bbsfiles/images/2009/11/200911211503_185758_1916092_3.jpg(4)http://ng1.17img.cn/bbsfiles/images/2009/11/200911211503_185759_1916092_3.jpg(5)http://ng1.17img.cn/bbsfiles/images/2009/11/200911211503_185760_1916092_3.jpg 主峰时间 拖尾因子不对称度半峰宽 理论塔板数 杂质分离度118.4324.8567.2580.6534409——216.7801.4551.7040.42088440.452318.6201.0381.0390.41711067——428.9951.2311.4490.583136981.860527.3920.7440.4750.582123061.172(三)分析与讨论(1)对于两种主要杂质的显示情况,1和3只能显示出一种。4对它们的分离度最好,5次之。(2)从主峰阿奇霉素的峰型来看3最好,4,5次之。(3)关于主峰也就是阿奇霉素的出峰时间,4,5明显晚于前三个色谱柱。关于不同厂家不同批次的阿奇霉素我们已做过很多实验,绝大多数杂质出峰都在阿奇霉素之前,而且种类很多,也就是除了本实验所测样品显示的这两种主要杂质之外还存在有很多杂质,理论上讲主峰出峰时间晚有利于前面杂质峰的分离。 总结起来,从初步的对比检测中发现Ultimate XB-C18色谱柱对阿奇霉素杂质检测的情况还是很令人满意的,甚至不亚于药检所推荐使用的色谱柱。我们准备继续进行一系列的分析实验,对几种较难分离的杂质进行对比分析。
化药质量控制CTD申报资料中杂质研究的几个问题张哲峰成海平宁黎丽田洁化药药学二部 摘要:杂质研究与控制是把控药品质量风险的重要内容之一,基于杂质谱分析的杂质控制是“质量源于设计”基本理念在杂质研究与控制中的具体实践,需要与CMC各项研究乃至药理毒理及临床安全性研究等环节关联思考、综合考虑,而不仅仅拘泥于提供准确的分析数据。本文针对当前CTD申报资料中杂质研究方面存在的问题与不足,结合CTD过程控制和终点控制相结合、研究和验证相结合、全面系统的药品质量控制理念,探讨仿制药杂质研究与控制的基本逻辑思路,提出CTD申报资料中杂质研究与控制方面几个需要关注的问题。 关键词:杂质研究与控制 杂质谱 CTD格式 杂质研究与控制是一项系统工程,需要以杂质谱分析为主线,安全性为核心,按照风险控制的策略,将杂质研究与CMC各项研究,乃至药理毒理及临床安全性研究等环节关联思考、综合考虑,而不仅仅拘泥于提供准确分析数据的传统思维,不是一项孤立的分析工作。CTD(Common Technical Document)申报格式体现了过程控制和终点控制相结合、研究和验证相结合、全面系统的药品质量控制理念,更加符合杂质研究与控制的基本规律和逻辑思路。自2011年4月起,药审中心陆续发布了多项有关CTD格式及技术审评的相关要求及电子刊物,对于国内研发单位正确理解CTD格式内含的基本精神起到了一定的促进作用,但就目前阶段的申报情况看,有些申报资料在杂质研究方面仍存在一些不足,仅仅是形式上的CTD格式,尚未实质性贯彻CTD的基本逻辑思路。以下是针对目前CTD申报资料中杂质研究相关问题的一些考虑。 1、CTD格式中杂质控制的考虑要体现在CMC的各个环节,而不是仅仅局限在“质量控制”模块。如制剂的原辅料控制中,原辅料的选择与控制要考虑以符合制剂质量要求(杂质等)为核心,必要时进行精制处理并制定内控标准;关键工艺步骤及参数的确立、工艺开发过程等要考虑以杂质是否得到有效控制为重点关注之一;制剂相关特性中要体现与原研产品杂质谱等的对比情况;包材、贮藏条件以及有效期的确立等也要以杂质是否处于安全合理的可控范围内为核心等等。实际上这正是源头控制、过程控制与终点控制相结合的杂质控制理念的体现,在研发工作及申报资料的整理中都需要针对性的贯彻实施。 问题与案例:有些申报资料在某种程度上未能充分体现杂质研究的整体性,对杂质控制措施仅强调了终点控制措施,尚未充分体现源头控制与过程控制的基本思路,具体表现在如下方面: (1)制剂杂质控制受制于原料药质控水平的约束,以目前国内批准的原料药杂质水平现状为由,未能根据该品当前杂质控制的水平与趋势,对原料药提出较为严格的针对性的杂质控制要求,并进行质量内控,因而难以确保制剂杂质控制水平与目前国际水平相适应; (2)在论述说明制剂相关特性时,未提供与原研产品杂质谱的对比分析情况; (3)关键工艺步骤及参数的确立、工艺开发过程相关内容中未详细说明杂质谱的变化情况,缺失关键质量数据的支持。 2、CTD格式的特点之一是研究内容模块化呈现,但需关注杂质分析与控制的系统性与整体性,不能割裂各项内容的必然联系和有机统一。比如对原料药而言,杂质分析与控制的相关内容会分布在分析方法(3.2.S.4.2)、方法学验证(3.2.S.4.3)、杂质对比研究与杂质谱分析(3.2.S.4.5)、杂质情况分析总结(3.2.S.3.2)、样品检测与数据积累(3.2.S.4.4)、控制限度(2.3.S.4.1)等各模块中,但杂质研究又是一项系统工程,具有统一的整体性,因此,不要因为申报资料格式的模块化而人为割裂各项研究内容的相互联系,甚至遗漏相关研究内容,要高度关注杂质分析与控制的系统性与整体性,将杂质研究与控制的全部内容和信息体现在相应模块中。如详细的杂质研究报告可以体现在3.2.S.4.5中;3.2.S.3.2要报告杂质研究的结果;杂质分析方法的筛选、研究与验证内容要在3.2.S.4.3中体现;对仿制药而言,杂质限度确定的论证与依据需要在与原研产品进行全面的杂质谱对比研究基础上进行论证说明,因此,与原研产品的对比研究及结论要在3.2.S.4.5中体现。 问题与案例:有些申报资料忽视了各项研究间的关联性,未能充分突出仿制药研发的特点,具体体现如下: (1)对分析方法的来源没有足够明确的说明,在分析方法的筛选、优化等方面做了哪些研究等信息缺失,只有方法学验证内容,缺失方法学筛选研究的相关信息; (2)没有比较说明采用的杂质分析方法与USP、BP/EP、JP等药典同品种分析方法相比有哪些区别和优势,未能从分析方法、杂质控制种类及限度要求等方面的比较情况评估拟定质量标准的杂质控制水平; (3)缺失放行标准质控限度确定的依据进行论述,3.2.S.4.5中只对货架期标准限度的确定进行了相关说明,未从杂质来源与特点、数据积累、稳定性考察等角度论述放行标准中相关限度确定的依据。 3、从杂质谱分析入手确立科学的杂质研究基本思路。杂质谱包括药物中所有杂质的种类、来源及特性等信息,通过杂质谱分析较为全面地掌握产品中杂质概貌(种类、含量、来源和结构等);有针对性地选择合适的杂质分析方法,以确保杂质的有效检出和确认;通过与原研产品杂质谱的对比研究,根据各相应杂质的一致性求证,或跟踪杂质谱对安全性试验或临床试验结果产生的影响,评估各杂质的安全性风险和可接受水平;结合规模化生产时杂质谱的变化情况,确立安全合理的杂质控制水平。 基于杂质谱分析的杂质研究是一种“以源为始”的主动思维模式,以“质量源于设计”的观点,从杂质来源入手,从制备工艺、化学结构、处方组成的分析出发,评估、预测产品中可能存在的及潜在的副产物、中间体、降解物以及试剂、催化剂残留等大体的杂质概况,辅以适当的强制降解、对照物质的加入等验证的手段,考证建立的分析方法是否能够将它们逐一检出,并进行相应的方法学验证工作;相比之下,传统的杂质研究是一种“以终为始”的被动行为和逆向思维模式,从杂质分析的结果出发,仅从建立的某种检测方法所检出的有关物质中归属其来源情况,而未充分分析与验证可能存在的潜在杂质情况,建立的分析方法能否全面检出这些杂质,故容易出现杂质漏检的情况,难以全面掌握产品的杂质谱。 问题与案例:杂质谱分析表明某原料药所采用的合成路线会产生具有遗传毒性的双叠氮杂质ROX,但最初建立的分析方法未检出该杂质,但不能确定是产品中的确不存在该杂质,还是建立的分析方法不能有效检出该杂质,经定向制备该杂质,采用标准加入法有针对性的分析考查,采用改进后分析方法在正常产品中检测到该物质,尽管其含量极低,考虑到其较强的毒性情况,质量标准中仍作为特定杂质予以严格控制,保证了其临床应用的安全性。因此,基于杂质谱分析的杂质研究是一种相对科学的思维模式,对于有效掌控杂质安全性风险具有重要意义。 4、分析方法的验证应具备针对性和全面性。杂质的微量性和复杂性,使得检测方法的专属性、灵敏度和准确度十分关键。杂质分析方法的对象是各个潜在的杂质,因此,其分析方法的验证需要根据不同杂质的特点综合设计验证方案,进行有针对性的规范验证。 问题与案例:一些申报资料中对杂质分析方法的灵敏度、准确度等仅仅针对主药化合物进行验证,仍无法说明是否适用于相关杂质的检出和定量。如下是某药物有关物质测定方法学验证总结,基本体现了方法学验证的针对性与全面性,建议参考。 项目验证结果专属性①统适用性良好,峰形、峰纯度、柱效参数等符合要求。②在酸、碱、高温、氧化各破坏条件下的主峰峰纯度角均小于纯度阈值,主峰峰纯度良好,破坏后的主峰与各杂质峰均能有效分离,分离度均大于1.5。③供试液加入起始原料、反应试剂、副产物及中间体等,均可有效检出,并良好分离。线性和范围①质A浓度在0.036μg/ml~1.204μg/ml范围内,线性关系良好(n=8);y=13703x-174.83;R2=0.9991。②杂质B浓度在0.089μg/ml~1.192μg/ml范围内,线性关系良好(n=7);y=10941x-517;R2=0.9995。③杂质C浓度在0.299μg/ml~4.784μg/ml范围内,线性关系良好(n=7);y=13257x-492.44;R2=0.9999。④主药浓度在0.3μg/ml~4.8μg/ml范围内,线性关系良好(n=6);y=15008x+565.48;R2=0.9999。灵敏度杂质A、B、C及主药最低检出限分别为0.012ng、0.0
我现在做甘油中乙二醇、二甘醇及其他杂质,没有DB-624的柱子,可以用DB-1701吗?
某产品结构是这样的:3,3',4,4'-联苯四甲酸二酐,属于二酐,进水极易分解,现在要分离二酐中的二酸和四酸杂质。对此有什么好的方法?
求助各位大佬,目前检测母液中的甘氨酸含量用的丹磺酰氯柱前衍生法,出峰图在下面。里面杂质有海因、海因酸、甘氨酸二肽、三肽,求指导这些杂质用什么方法检测,感谢。[img=,690,270]https://ng1.17img.cn/bbsfiles/images/2024/02/202402171748266762_3661_5796173_3.jpg!w690x270.jpg[/img]
本人新手小白,刚进实验室半年,勉强算学会[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]基础操作吧。安排了要定性分析药用甘油杂质的任务,给了几种甘油,用[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]软件分析里面的杂质成分,只要确定有哪几种杂质即可。有朋友知道这个要怎么操作吗?
Help!Help!Help!有木有大神做过甘油的杂质?用什么气相柱子?升温程序是怎么设定的?我们用过HP-5,DB-1,DB-WAX,对照各个峰都分得很好,可样品里还是分不开,就是二甘醇分不开,而且甘油峰真心难看。试过的升温程序:100℃,保持6分钟,5℃/min升至105℃,保持10min,50℃/min升至220℃,保持6min
低分子量肝素钙中杂质的测定用什么色谱柱好[img]http://simg.instrument.com.cn/bbs/images/brow/em09511.gif[/img]

回忆贴:远去了的GC-MS和不用再伺候的科技精英,这个是几年前的事了,当时没机会发表,现在没机会用GC-MS了,把以前的经历作写出来,虽然数据和图谱基本找不到了,但记忆还是非常深刻的,乘着今天加班无聊,完成这月的原创任务。以前单位的重点项目羰基合成醋酐,其中的杂质在研发阶段是别人做的(后来跳槽了,我也不知道她以前怎么做的,反正科研精英们也不会告诉我),生产了也就不关心里面的杂质了,质检的主任工程师闲得无聊,拿来一点产品让我分析,总离子流图出来了,但靠检索得到的数据都有点问题。http://ng1.17img.cn/bbsfiles/images/2012/12/201212301032_417223_1640192_3.jpg以上是GC-MS的总离子流图,醋酐保留时间为4.28min,杂质醋酸为3.60min、EDA为4.99min,而在醋酐和EDA中有多个小杂质,其中4.76min的杂质(以下称为A)质谱图三个明显的碎片为29,43,57,检索结果是2,3-戊二酮(原图没有了,只能用标准图代替了)http://ng1.17img.cn/bbsfiles/images/2012/12/201212301042_417224_1640192_3.jpg记得匹配率还是很好的,但我总觉得有点问题,因为醋酐沸点在139℃,EDA沸点为168℃,而2,3-戊二酮在我查到的资料中只有115℃,不该这么后面,更重要的是我写不出得到这个物质的机理(毕竟搞分析的不是科研精英),然后就跟送样的人商量,给我找各种中间馏分,终于拿到了一个A含量很高的物料,当时我想醋酐在水中会水解成醋酸并且和水混溶,而里面含量较高的杂质EDA微溶于水,通过萃取来看看A是水溶还是酯溶性的,可以推测大致结构,同时分开醋酐和EDA,相当于浓缩提纯。做法是:将物料加入一定量的水,搅拌至油相不再减少,加入乙酸乙酯进行振荡静置分离,用GC-MS分析两相的成分。另人意外的是两相中均不含有A,而出现了一定量的丙酸。虽然分离并不成功,但试验过程中的现象给了我重要的线索,A遇水很容易完全水解,显然要比一般的丙酸酯快的多,而且从质谱碎片来看它的结构应该是比较简单的,而从谱库中无法检索到匹配的物质则说明这个物质可能不在谱库中。因此我怀疑是丙醋酸酐,虽然没有该物质的物性资料,但它沸点应该在醋酸酐和丙酸酐之间,而丙酸酐的沸点是168℃,因此丙醋酸酐出峰位置应该在醋酐和EDA之间,而且乙酰基分子量为43,丙酰基分子量为57,乙基分子量29,和质谱图相符合。既然谱库没有,标样肯定是买不到了,只好自己合成了。虽然合成酸酐的方法很多,但用于验证的合成方法有其特殊性。虽然无需考虑成本,对产率也无要求。但采用的方法应当尽可能使用少量试剂,以免混合物中物质过多造成判断失误。而用于GC-MS分析,还要考虑不能有对仪器不利的物质进入仪器。显然用常规的浓酸催化或者酰氯钠盐反应生成的酸酐如果不进行分离是不能用于GC-MS分析的。由于丙醋酸酐是丙酸和醋酸脱水而成,而醋酐本身也有脱水功能,因此我就把丙酸和醋酸酐反应进GC-MS分析,没有使用其它催化剂。试验方法:将丙酸和醋酐等比例混合,在120度加热4小时,冷却,进GC-MS分析。反应液一共出现了非常明显的[/fo
有个甘油样品,需要用到气质联用分析甘油中杂质,我们属于县级市,本地质检所没有,上一市级药检所也没有GCMS,各位好心的朋友能否帮个忙分析一下,柱子可用DB-624,检测方法参考“甘油(供注射用)中国药典2010版”,方法详见附件!谢谢!
[B][center]药物中杂质的来源及杂质限量检查[/center] [/B]药物只有合格品与不合格品;一般化学试剂分为4个等级(基准试剂、优级纯、分析纯、化学纯) [B]药物中一般杂质检查 [/B][B]氯化物为一指示性杂质。[/B] 通过对氯化物的控制,可同时控制与氯化物结合的一些阳离子以及某些同时生成的副产物。可从氯化物检查结果显示药物的纯度,间接考核生产、贮藏过程是否正常。 1. 原理 药物中微量的氯化物在硝酸酸性条件下与硝酸银反应,生成氯化银的胶体微粒而显白色浑浊,与一定量的标准氯化钠溶液在相同条件下产生的氯化银浑浊程度比较,判定供试品中氯化物是否符合限量规定。 Ag+ + Cl- → AgCl ↓ [B]硫酸盐检查法 [/B] 1. 原理 药物中微量的硫酸盐在稀盐酸酸性条件下与氯化钡反应,生成硫酸钡的微粒而显白色浑浊,与一定量的标准硫酸钾溶液在相同条件下产生的硫酸钡浑浊程度比较,判定供试品中硫酸盐是否符合限量规定。 [B]铁盐检查法 [/B]硫氰酸盐法 巯基醋酸法 砷盐检查法 1. 古蔡氏法 1. 原理 金属锌与酸作用产生新生态的氢,与药物中微量砷盐反应生成具挥发性的砷化氢,遇溴化汞试纸产生黄色至棕色的砷斑,与同条件下一定量标准砷溶液所生成的砷比较斑,判断砷盐的含量。 [B]硒、氟及硫化物检查法 [/B]1. 氧瓶燃烧法 适用于以共价键结合的卤素、硫、硒的有机药物。 本法系将有机药物防入充满氧气的密闭燃烧瓶中进行燃烧,将燃烧所产生的欲测组分吸收于适当的吸收液中,然后根据欲测组分的性质,选用合适的分析方法进行鉴别、检查或含量测定。 [B]注意事项及讨论 [/B]1. 根据被燃烧分解的样品量选用适宜大小的燃烧瓶。 2. 测定氟化物时应改用石英燃烧瓶。 1. 硒检查法 (1). 操作方法 样品与对照品液,调节Ph2.0±0.2,加盐酸羟胺,二氨基萘,比色。 [B]硫化物检查法 [/B] 方法同砷盐检查第一法,不装醋酸铅棉花,以醋酸铅试纸代替溴化汞试纸。 标准液取1ml 5/ml [B]澄清度检查法 [/B]将一定浓度的供试品溶液与浊度标准液分别置于配对的比浊用玻璃管,同置黑色背景上,在漫射光下观察。浊度标准液 硫酸肼与乌洛托品溶液混合分五个等级,未超过0.5等级即为澄清。BP98规定未超过1等级即为澄清。 [B]溶液颜色检查法 [/B]CHP2000 [B]1. 比色法[/B] 色调标准贮备液 黄色液 重铬酸钾液(BP98用氯化铁) 红色液 氯化钴液 蓝色液 硫酸铜液 配成各种色调色号标准比色液共50种。 [B]2. 分光光度法 [/B] [B]易碳化物检查法 [/B]检查药物中含有的遇硫酸易碳化或易氧化而呈色的有机杂质。 对照品液 样品液 加硫酸5后,加供试品。 [B]炽灼残渣检查法[/B] 取供试品1.0~2.0g或个药品项下规定的重量,置已炽灼至恒重的坩埚中,精密称定,缓缓炽灼至完全碳化,放冷至室温;除另有规定外,加硫酸使湿润,低温加热至硫酸蒸气除尽后,在700~800炽灼使完全灰化,移至干燥器内,放冷至室温,精密称定,再在700~800炽灼至恒重,即得。残渣限量一般为0.1~0.2% 一般应使炽灼残渣量为1~2mg 若需将炽灼残渣留作重金属检查时,炽灼温度必须控制在500~600。 [B]干燥失重测定 [/B]1. 常压恒温干燥法 2. 干燥剂干燥法 3. 减压干燥法 [B]水分测定法 [/B][B]费休氏法 [/B] 本法是根据碘和二氧化硫在吡啶和甲醇溶液中能与水起定量反应的原理以测定水分。 [B]甲苯法[/B] 在加热状态下,甲苯夹带着水分蒸出,收集蒸出的水分测定。 [B]药物中特殊杂质检查 [/B] [B]一、物理法 [/B] [B]二、化学反应法 [/B](一)容量分析法 (二)重量分析法 (三)比色法和比浊法 [B]三、色谱法 [/B]1.纸色谱法 薄层色谱法 TLC是药典中最常用的特殊杂质限量检查方法。 1.在一定供试品及检查条件下,不允许有杂质斑点存在 2.以待测杂质对照品检测 3.将供试品稀释到适当浓度作为杂质对照品溶液 4.选用质量符合规定的与供试品相同的药物作为杂质对照品 [B]高效液相色谱法 [/B] [B][url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法 [/B] 1.面积归一化法 2.主成分自身对照法 3.内标法测定 4.内标法加校正因子法 5.外标法 有机溶剂残留量测定法 [B]分光光度法 紫外分光光度法 比色法 [url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]分光光度法[/B]
常用辅料及相关杂质在系统一时保留时间参考值极性色谱柱 辅料或杂质名称 相对保留时间 异丙醇 0.098 正丙醇 0.168 二甲基甲酰胺 0.500 乳酸乙酯 0.512 二甲基乙酰胺 0.591 二甲基亚砜 0.785 1,2-丙二醇 0.803 1,3-丁二醇 0.956 1,3-丙二醇 1.000 苯甲醇 1.083 二甘醇 1.178 肉豆寇酸异丙酯 1.206 三乙酸甘油酯 1.263 丙三醇 1.469 油酸乙酯 1.564 苯甲酸苄酯 1.683 中等极性色谱柱辅料或杂质名称 相对保留时间乙醇 0.281 异丙醇 0.333 丙三醇 1.000 三甘醇 1.227 以上是从别的地方看到的,有的样品出峰时间非常接近。在新药申报时遇到的问题是:当同一个样品在做检出限时,很可能出峰时间出现较小的变化,会不会影响到样品种类判断及资料申报呢?
继续讨论:饱和食盐水中杂质测定之容器篇 上贴讨论了测定饱和食盐水时有关混标配置的问题,现在继续讨论要测定饱和食盐水中的杂质元素,要测定的元素有Al、Ba、Ca、Mg、Si、Sr等元素,含量小于20ppb,大家认为用玻璃瓶测定的准确还是用聚乙烯类的准确。说出各自的理由。 [em0814][em0814][em0814]
日前,Cell杂志公布新一届编委名单,编委中第一次出现中国科学家的名字:中国医学科学院曹雪涛院士、北京大学生命科学院邓宏魁教授。据悉,Cell杂志编委们是生命科学领域的一流科学家和学科带头人,曹雪涛、邓宏魁成为Cell杂志新编委,从一定程度上表明中国科学家的工作正在逐步得到国际学术界的认可。Cell杂志是学术界公认的生命科学领域的顶级杂志,自1974年创刊迄今近40年间,其一向以学术严谨、评审严格、以发表具有重要意义的原创性科研论文为主而且发表的论文系统性非常强而著称.2009年Cell杂志编委换届时有4位华裔编委,分别是加州大学伯克利分校教授钱泽南(Robert Tijan),加州大学旧金山分校/伯克利分校联合納米医学中心主任林温德(Wendell Lim)、哈佛大学物理系教授庄小威、耶鲁大学遗传系分子遗传学系副主任许田。这四位华裔科学家均是HHMI研究员,其中,钱泽南教授自2009年起任美国休斯医学研究所HHMI所长,庄小威教授是最年轻的美国科学院院士。目前Cell杂志编委中华人科学家增至6位,曹雪涛教授是著名免疫学家,1964年出生,是国内自主培养出来的学者,1986年本科毕业于上海第二军医大学并于1990年在该校获得博士学位,2005年当选中国工程院院士,今年当选德国科学院院士,目前是医学免疫学国家重点实验室主任、中国医学科学院院长、中国免疫学会理事长、亚洲大洋洲免疫学联盟主席、全球慢性疾病防控联盟候任主席。 在天然免疫、免疫调控与免疫治疗方面取得了系列成绩, 以通讯作者在Cell、Cancer Cell、Nature Immunology等SCI杂志发表论文210余篇。培养的10名博士生获得全国优博论文。邓宏魁教授是著名细胞生物学家,1963年出生,1984年本科毕业于武汉大学,1995年获得美国加州大学洛杉矶分校博士,后于纽约大学DAN LITTERMAN院士实验室从事博士后研究;2001年4月回国后在北京大学生命科学学院建立了细胞分化与细胞工程实验室,主要从事细胞分化、干细胞工程及其再生医学研究。曾经在Cell、Nature、Science等杂志发表过多篇论文。今年7月18日, Science刊登了其研究团队用小分子化合物诱导体细胞重编程为多潜能干细胞,该成果开辟了一条全新的实现体细胞重编程的途径,给未来应用再生医学治疗重大疾病带来了希望。
2010版《药典》规定,“如有其他杂质峰,扣除内标峰按面积归一化法计算。”可是,我们在做的时候发现主峰甘油峰出峰很丑,这样的峰形貌似不能用面积归一化法,不知各位高手有没有做过这个品种,有没有遇到过这个问题,是怎样处理的呢?(样品溶液的配制方法为甘油加内标溶液,溶剂为甲醇,很简单)。谢谢各位了!http://simg.instrument.com.cn/bbs/images/brow/em09511.gif
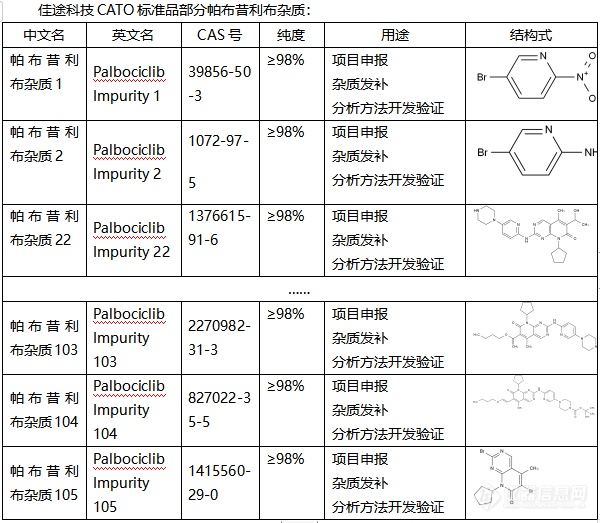
◇关于帕布昔利布杂质 帕布昔利布杂质是一种治疗乳腺癌的杂质,它也是一种新型的CDK4/6抑制剂,它是FDA首个获得批准的药物。帕布昔利布杂质是通过调节细胞周期,抑制CDK4和CDK6的活性,从而阻止细胞从G1期进入到S期,进一步抑制DNA的合成。 帕布昔利布首次于 2015 年 2 月在美国获得批准,CATO标准品提供的帕布昔利布杂质,在妇女绝经后的人群中还显示它还可以与来曲唑合并用于 HR+、HER2-晚期或转移性乳腺癌治疗。[img=,600,523]https://ng1.17img.cn/bbsfiles/images/2024/02/202402040904326373_1427_6381607_3.png!w600x523.jpg[/img]

一些溶剂因为种种原因总是含有杂质,这些杂质如果对溶剂的使用目的没有什么影响的话,可直接使用。可是在进行化学实验和进行一些特殊的化学反应时,必须将杂质除去。虽然除去全部杂质是有困难的,但至少应该将杂质减少到对使用目的没有防碍的限度。除去杂质的操作称为溶剂的精制,故溶剂的精制几乎都要进行脱水,其次再除去其他的杂质。1.溶剂的脱水干燥溶剂中水的混入往往是由于在溶剂制造,处理或者由于副反应时作为副产物带入的,其次在保存的过程中吸潮也会混入水分。水的存在不仅对许多化学反应,就是对重结晶,萃取,洗涤等一系列的化学实验操作都会带来不良的影响。因此溶剂的脱水和干燥在化学实验中是很重要的,又是经常进行的操作步骤。尽管在除去溶剂中的其他杂质时有时往往加入水分,但在最好还是要进行脱水,干燥。精制后充分干燥的溶剂在保存过程中往往还必须加入适当的干燥剂,以防止溶剂吸潮。溶剂脱水的方法有下列几种:(1)干燥剂脱水这是液体溶剂在常温下脱水干燥最常用使用的方法。干燥剂有固体,液体和气体,分为酸性物质,碱性物质,中性物质以及金属和金属氢化物。干燥剂的性质各有不同,在使用时要充分考虑干燥剂的特性和干燥剂的性质,才能有效达到干燥的目的。在选择干燥剂时首先要确保进行干燥的物质与干燥剂不发生任何反应;干燥剂兼做催化剂时,应不使溶剂发生分解,聚合,并且干燥剂与溶剂之间不形成加合物。此外,还要考虑倒干燥速度,干燥效果和干燥剂的吸水量。在具体使用时,酸性物质的干燥最好选用酸性物质干燥剂,碱性物质的干燥用碱性干燥剂,中性物质的干燥用中性干燥剂。溶剂中有大量水存在的,应避免选用与水接触着火(如金属钠等)或者发热猛烈的干燥剂,可以先选用氯化钙一类缓和的干燥剂进行干燥脱水,使水分减少后再使用金属钠干燥。加入干燥剂后应搅拌,放置一夜。温度可以根据干燥剂的性质,对干燥速度的影响加以考虑。干燥剂的用量应稍有过剩。在水分多的情况下,干燥剂因吸水吸收水分发生部分或全部溶解生成液状或泥状分为两层,此时应进行分离并加入新的干燥剂。溶剂与干燥剂的分离一般采用倾析法,将残留物进行过滤,但过滤时间太长或周围的湿度过大会再次吸湿而使水分混入,因此,有时可采用与大气隔绝的特殊的过滤装置。有的干燥剂操作危险时,可在安全箱内进行。安全箱在置有干燥剂,使箱内充分干燥(我知道是无水五氧化二磷),或吹入干燥空气或氮气。使用分子筛或活性氧化铝等干燥剂时应添在玻璃管内,溶剂自上向下流动进行脱水,不与外界接触效果较好。大多数溶剂都可以用这种脱水方法,而且干燥剂还可以回收使用。常用的干燥剂有:① 金属,金属氢化物Al,Ca,Mg:常用于醇类溶剂的干燥Na,K:适用于烃,醚,环己胺,液氨等溶剂的干燥。注意用于卤代烃时有爆炸危险,绝对不能使用。也不能用于干燥甲醇,酯,酸,酮,醛与某些胺等。醇中含有微量的水分可加入少量金属钠直接蒸馏。CaH:一克氢化钙定量与0.85克水反应,因此比碱金属,五氧化二磷干燥效果好。适用于烃,卤代烃,醇,胺,醚等,特别是四氢呋喃等环醚,二甲亚碸,六甲基磷酰胺等溶剂的干燥。有机反应常用的极性非质子溶剂也是用此法进行干燥的。LiAlH4:常用醚类等溶剂的干燥。②中性干燥剂CaSO4,NaSO4,MgSO4:适用于烃,卤代烃,醚,酯,硝基甲烷,酰胺,腈等溶剂的干燥。CuSO4:无水硫酸铜为白色,含有5个分子的结晶水时变成蓝色,常用检测溶剂中微量水分。CuSO4适用于醇,醚,酯,低级脂肪酸的脱水,甲醇与CuSO4能形成加成物,故不宜使用。CaC2:适用于醇干燥。注意使用纯度差的碳化钙时,会发生硫化氢和磷化氢等恶臭气体CaCl2: 适用于干燥烃,卤代烃,醚硝基化合物,环己胺,腈,二硫化碳等。CaCl2能于伯醇,甘油,酚,某些类型的胺,酯等形成加成物,故不适用。活性氧化铝:适用于烃,胺,酯,甲酰胺的干燥。分子筛:分子筛在水蒸气分压低和味素高时吸湿容量都很显著,于其他干燥剂相比,吸湿能力非常大的。表3-1为各种干燥剂的吸湿能力比较(指常温下经足够量的干燥剂干燥的1升空气中残存水分的毫克数)。分子筛在各种干燥剂中,其吸湿能力仅次于五氧化二磷。由于各种溶剂的几乎都可以用分子筛脱水,故在实验室和工业上获得广泛的应用。表1各种干燥剂的吸湿能力http://ng1.17img.cn/bbsfiles/images/2015/12/201512161151_578308_2961690_3.jpg③ 碱性干燥剂KOH,NaOH:适用于干燥胺等碱性物质和四氢呋喃一类环醚。酸,酚,醛,酮,醇,酯,酰胺等不适用。K2CO3:适用于碱性物质,卤代烃,醇,酮,酯,腈,溶纤剂等溶剂的干燥。不适用于酸性物质。BaO,CaO:适用于干燥醇,碱性物质,腈,酰胺。不适用于酮,酸性物质和酯类。④酸性干燥剂H2SO4:适用于干燥饱和烃,卤代烃,硝酸,溴等。醇,酚,酮,不饱和烃等不适用。P2O5:适用于烃,卤代烃,酯,乙酸,腈,二硫化碳,液态二氧化硫的干燥。醚,酮,醇,胺等不适用。(2)分馏脱水沸点与水的沸点相差较大的溶剂可以用分馏效率高的蒸馏塔(精馏塔)进行脱水,这是一般常用的脱水方法。(3)共沸蒸馏脱水与水生成共沸物的溶剂不能采用分馏脱水的方法。如果含有极微量水分的溶剂,通过共沸蒸馏,虽然溶剂有少量的损失,但却能脱去大部分水。一般多数溶剂都能与水组成共沸混合物。(4)蒸发,蒸馏干燥进行干燥的溶剂很难挥发而不能与水组成共沸混合物的,可以通过加热或减压蒸馏使水分优先除去。例如,乙二醇,乙二醇-丁醚,二甘醇-乙醚,聚乙二醇,聚丙二醇,甘油等溶剂都适用。(5)用干燥的气体进行干燥将难挥发的溶剂进行干燥时,一般慢慢回流,一面吹入充分干燥的空气或氮气,气体带走溶剂中的水分,从冷凝器末端的干燥管中放出。此法适用与乙二醇,甘油等溶剂的干燥。(6)其他在特殊情况下,乙酸脱水可采用在乙酸中加入与所含水等摩尔的乙酐,或者直接加入乙酐干燥。甲酸的脱水可用硼酸经高温加热熔融,冷却粉碎后得到的无水硼酸进行脱水干燥。此外还有冷却干燥的方法。如烃类用冷冻剂冷却,其中水分结成冰而达到脱水目的。2.溶剂的精制方法一般通过蒸馏或精馏进行分馏的方法得到几乎接近纯品的溶剂。然而对于一些用精馏塔难以将杂质分离的溶剂,必须将这些杂质预先除去,方法之一是分子筛法。分子筛的种类按照分子筛的有效直径进行分类,例如有效直径为3埃的分子筛称3A分子筛,4埃的称4A分子筛,5埃的称5A分子筛,9埃的称10X分子筛,10埃的称13X分子筛。表3-2为各种分子所选用的分子筛类型。例如用5A分子筛可以从丁醇异构体混合物中吸附分离丁醇,用4A分子筛分离甲胺和二甲胺。适用方法与干燥剂脱水方法相同,用填充层装置较好。溶
http://www.biomart.cn//upload/userfiles/image/2012/02/1329478430.jpg光遗传学技术Optogenetics(optical stimulation plus genetic engineering 光刺激基因工程/光遗传学)是2010年Nature杂志评出的年度技术,近年来在这一领域获得了不少重要的成果,近期来自日本东京大学,美国斯坦福大学等处的研究人员发表了题为“Crystal structure of the channelrhodopsin light-gated cation channel”的文章,报道了两个光敏感通道构成的一个嵌合体的X-射线晶体结构,这将有助于光遗传学的发展,这一成果公布在2月16日Nature杂志上,并被作为封面文章推荐。领导这一研究的是东京大学Osamu Nureki,与斯坦福大学的Karl Deisseroth副教授,其中Deisseroth副教授曾开发出多种光遗传学技术新方法,比如其研究组曾经利用光遗传学技术开展多项试验对工程动物的中枢神经系统进行研究。光敏感通道(channelrhodopsins)是一种受光脉冲控制的具有7次跨膜结构的非选择性阳离子通道蛋白,自1991年从莱茵衣藻中发现后被许多实验室所关注,由于这一通道可以快速形成光电流,使细胞发生去极化反应的电生理特性,因此已被广泛应用于神经系统的研究。与传统的神经系统研究方法如电生理技术、神经药理学方法相比,这一方法具有更高的空间选择性和特异性,作为光遗传学技术的核心组成部分,这一领域的研究吸引了不少科学家的关注。在这篇文章中,研究人员报道了两个光敏感通道构成的一个嵌合体的X-射线晶体结构(2.3 Å ),光敏感通道在神经科学研究中扮演了重要角色,但是有关它的分子作用机制至今了解的并不多,这项研究就通过其晶体结构,揭示了光敏感通道的结构,及电生理作用机制,结果表明这一离子通道的分子架构包括与视网膜相结合的区域和阳离子通道。这将有助于揭示光敏感通道的功能,并且为光遗传学更好的利用光敏感通道提供了更加精确的信息。生命现象离不开细胞发挥着各种功能。实时了解细胞间的活动状况是揭开复杂生命谜团和疾病治疗方法获取的重要途径。在保护头盖骨的同时,对处理大脑庞大信息的大量神经细胞活动进行实时性成像是非常困难的。因此研究人员开发了各种方法,包括光遗传学技术进行探索。去年来自斯坦福大学的华裔研究组则接连设计了几种新颖的光遗传学工具,可以更好的分析活体哺乳动物大脑神经环路生理现象,比如他们将光遗传学技术结合细菌人工染色体(BAC)转基因策略成功构建了四种神经元可被蓝光激活的转基因小鼠动物模型。除此之外,Bamberg研究组的一项最新成果:看似简单的融合方法解决了光遗传学研究的一大问题。之前的研究表明channelrhodopsin-2受到蓝光的刺激时,会导致阳离子通过细胞膜,细胞去极化,神经元激活,而盐菌紫质(halorhodopsin)在受到橙色光的刺激时,则会引发氯离子通过细胞膜,细胞极化,阻止细胞激活。这些成果都有利用更好的通过光遗传学分析生物现象,当然要实现这些方法并不容易,比如Bamberg研究组这项成果,因为当细胞表达两种光遗传学蛋白的时候,它们表达两种蛋白的表达水平不均衡,一种可能很多,而另一种可能很少。而且不同细胞的表达比率也不一致。