实验室刚扩的己烯雌酚用的是 sn/t3235-2012的标准,方法上不是己二烯雌酚才用内标么?己烯雌酚 也要用是么?如果用内标,用什么内标?,新手望大神指点
一、案例己烯雌酚(DES)是一种人工合成的激素类药物,医学上主要用于治疗雌激素缺乏症。但是其具有促进动物生长,促进动物蛋白质的合成代谢,提高动物日增重和提高饲料转化率的作用。曾被作为动物生长促进剂用于畜禽以及水产品的养殖中。但是含有己烯雌酚的肉制品能扰乱人体内的激素平衡,导致妇女更年期紊乱,女童性早熟,男性女性化,生育能力降低;国际癌症研究机构(IARC)研究发现DES是一种致癌物质,诱发女性乳腺癌、卵巢癌等。从1981年,世界卫生组织禁止使用己烯雌酚、己烷雌酚作为动物的生长促进剂。世界各国规定食品动物养殖中不得以任何途径和方式使用DES,养殖动物及动物性食品中不得检出DES。我国农业部早已明令禁止在畜牧养殖业中使用己烯雌酚及其盐、酯等。但受利益驱动,仍有部分养殖者非法使用。为保障畜产品质量安全,我国已将其作为兽药残留监控的重点对象。二、选用的国家标准GB/T 5009.108—2003畜禽肉中己烯雌酚的测定。三、测定方法1.提取及净化精确称取5.0g绞碎肉试样,放入50mL具塞离心管中,加10.00ml。甲醇,充分搅拌,振荡20min,于3000r/min离心10min,将上清液移出,残渣中加lO.00mL甲醇,混匀后振荡20min,于3000r/min离心10min,合并上清液,此时如出现混浊,需再离心10min,取上清液过0.5μmFH滤膜,备用。2.色谱条件①紫外线检测器:检测波长230nm。②灵敏度:0.04AUFS。③流动相:甲醇+O.043mol/L磷酸二氢钠(70+30),用磷酸调pH值至5。④流速:1mL/min。⑤进样量:20μL。⑥色谱柱:CLC—ODS—C18(5μm)6.2mm×150mm不锈钢柱。⑦柱温:室温。3.标准曲线绘制精确称取5份(每份5.0g)绞碎的肉试样,放入50mL具塞离心管中,分别加入不同浓度的标准液0、6.0μg/mL、12.0μg/mL、18.0μg/mL、24.0μg/mL,其中甲醇总量为20.00mL,使其测定浓度为0、0.30μg/mL、0.60μg/mL、0.90μg/mL、1.20μg/mL,按步骤一方法提取备用。4.测定分别取样20μL,注入HPLC柱中,可测得不同浓度DES标准溶液峰高,以DES浓度对峰高绘制工作曲线,同时取样液20μl,注入HPLC中,测得的峰高从工作曲线图中查相应含量,Rt一8.2355.结果计算式中 X一一试样中己烯雌酚的含量,mg/kg;A一进样体积中己烯雌酚的含量,ng;m——试样质量,g;V1——试样甲醇提取液总体积,mL;V2——进样体积,mL。6.试剂①甲醇。②0.043mol/L磷酸二氢钠溶液:取1g磷酸二氢钠(NaH2PO4·2H2O)溶于水,定容至500mL。③己烯雌酚(DES)标准溶液:精确称取100mg己烯雌酚(DES)溶于甲醇,移入100mL容量瓶中加甲醇定容,混匀,每毫升含DESl.0mg,储存于冰箱中。④己烯雌酚(DES)标准使用液:吸取10.00mL DES储备液,移入100mL容量瓶,加甲醇定容,每毫升含DESl00μg。⑤磷酸。7.仪器①高效液相色谱仪:具紫外检测器。②小型绞肉机。③小型粉碎机。④电动振荡器。
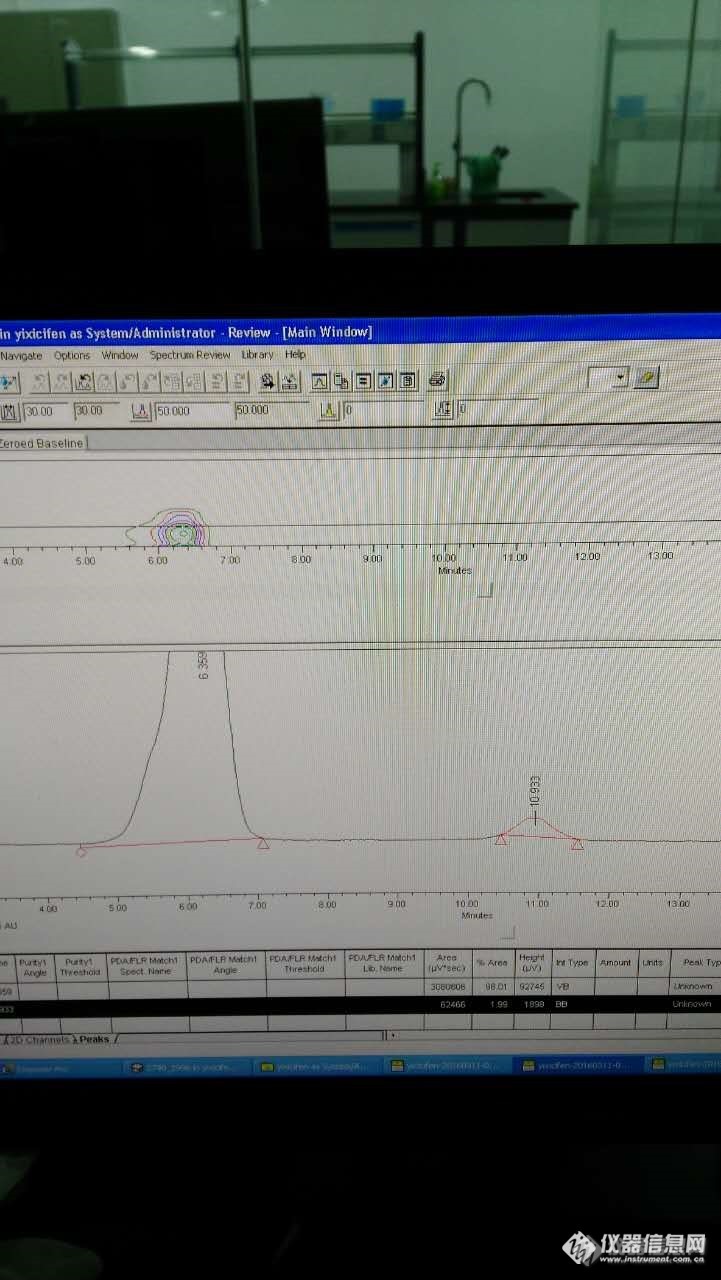
【液相色谱之家】己烯雌酚的检测为何要在三氯甲烷中侵泡5小时 来自微友:质量检测-曾http://ng1.17img.cn/bbsfiles/images/2016/03/201603141931_586966_2960432_3.jpg维A:为什么要溶解在三氯甲烷中5小时挥发干,再检测?使用的检测器为:PDA检测器微B:己烯雌酚具有较大的共轭结构,用三氯甲烷溶解也许是使这种具有两种几何体的结构更容易分开,己烯雌酚反式体比己烯雌酚顺式体极性较大,这两种几何体在三氯甲烷的长时间作用下,由于其结构的特殊性与溶剂产生一定的作用力,使其断键满足分析。微A:我现在遇到的问题是:没有泡过直接用甲醇溶解,只有一个峰,然后样品再经过制备液相后纯化的样品重新HPLC检测,居然多了一个峰,会不会是它的顺反异构的峰讲过流动相的长时间浸泡导致它的出现?微A:我走制备,没有经过三氯甲烷的浸泡,直接走样,只有一个峰,讲收集的溶液进行分析,就多了一个峰。多了后面的峰,就是用甲醇和水的流动相,经过制备收集的。http://ng1.17img.cn/bbsfiles/images/2016/03/201603141954_586967_2960432_3.jpg微iA:甲醇泡了一晚上的没有经过制备的乙烯雌酚进行分析没有那个小峰。对此您有什么看法呢?
动物源性食品己烯雌酚检验方法—高效液相色谱法1 范围本方法规定了动物源性食品中己烯雌酚残留量的快速测定方法。原理试样中的残留的己烯雌酚经快速检测前处理试剂盒提供的试剂提取、浓缩、净化后用液相色谱进行检测,外标法定量。3 试剂和材料除另有规定外,所有试剂均为分析纯,水为重蒸馏水。3.1乙腈:色谱纯。3.2冰乙酸:色谱纯。3.3甲醇:色谱纯。3.4无水乙酸钠。3.5对-甲苯磺酸。3.6乙酸盐缓冲液:称取4.950g无水乙酸钠及0.950g对-甲苯磺酸,溶解于950mL水中,用冰乙酸调节溶液pH到4.5,最后用水定溶到1000mL。3.7标准品: 己烯雌酚3.8标准贮备溶液:分别称取标准品各10.0mg,用甲醇溶解后转移至10mL棕色容量瓶中,用甲醇定容,于—20℃条件下保存。使用时,用甲醇稀释上述标准储备溶液,配制成不同浓度的标准工作液。3.9己烯雌酚快速检测前处理试剂盒*。4 仪器和设备4.1高效液相色谱仪:配紫外-可见检测器。4.2匀浆机。4.3旋转蒸发仪。4.4离心机:4 000 r/min4.5聚四氟乙烯离心管:100 mL,具塞。4.6微孔滤膜:0.45 µ m。5测定步骤5.1提取、浓缩、净化准确称取已捣碎的样品10.00 g于50 mL离心管中,先加己烯雌酚快速检测前处理试剂盒中的提取剂(液体20.0 mL)、8000r/min均质1min,于4000 r/min离心5 min,取出上清液10mL用水稀释至30mL。残留物用2.0 mL蒸馏水溶解。取稀释液于层析柱中(使用前依次用5mL甲醇、5mL蒸馏水激活)挤干,加5mL洗涤剂洗涤挤干,加5mL洗脱剂洗脱,接收洗脱液,50℃水浴旋转蒸干,用1mL甲醇溶解残渣于0.45 µ m微孔滤膜过滤,供仪器测定。5.2绘制标准工作曲线移取己烯雌酚混和标准溶液, 50µ g/kg、100µ g/kg、200µ g/kg、500µ g/kg、1000µ g/kg标准工作溶液,样液用高效液相色谱仪测定,得出标准工作曲线。5.3测定5.3.1液相色谱条件a) 色谱柱: C18柱,150 mm×4.6 mm(i.d.),粒度5m b) 流动相:乙腈+乙酸盐缓冲液 (70+20,体积分数) c) 流速:1.0 mL/min d) 柱温:室温 e) 检测波长:250nmf) 进样量:20 L。5.3.2色谱测定根据样液中己烯雌酚的含量情况,选定峰面积相近的标准工作溶液。标准工作溶液和样液中的己烯雌酚响应值均应在仪器的检测线性范围内。5.3.3空白实验除不加试样外,按上述测定步骤进行。5.3.4结果计算用色谱数据处理机或按式(1)分别计算供试样品中的己烯雌酚残留量。 2 ci×Vω= …… (1)mω-样品中己烯雌酚残留量,μg/kg;ci -标准曲线上查出试样溶液中己烯雌酚标准工作溶液的浓度,μg/L;2-换算常数;V-最终定容体积数,mL;m-供试试料样品重量,g。6测定低限、回收率6.1检测限本方法的检测限己烯雌酚为10μg/kg。6.2回收率本方法回收率己烯雌酚为:85%~105%。
做GB/T5009.108-2003畜禽肉中己烯雌酚的测定,其中磷酸二氢钠要配制0.043mol/L标准要求取1g磷酸二氢钠溶于水500mL。这个配制方法想不通啊,总觉得不对,算出来需要3.354g磷酸二氢钠才对吧。需要高人给预指点,谢谢
[align=center][b][b][font=黑体]分馏柱在环己烯制备实验中的使用及其作用[/font][/b][/b][/align][align=center][font='Times New Roman']Application and function of fractionation column in cyclohexene preparation experiment[/font][/align][align=center][font=宋体][font=宋体]北京化工大学[/font] 材料科学与工程学院 高元[/font][/align][font=宋体] [/font][font=黑体]摘要[/font][font=宋体]:[/font][font=宋体]目前大学化学实验教学中,大多采用环己醇制备[/font][font=宋体]环己烯[/font][font=宋体]。环己醇[/font][font=宋体]在加热以及[/font][font=宋体]酸[/font][font=宋体]催化的条件下发生[/font][font=宋体]消去反应,生成环己烯。本文简单介绍了分馏法用环己醇制备环己烯的实验原理和实验方法[/font][font=宋体],[/font][font=宋体]阐述了分馏柱在实验中的作用原理和优点;介绍了采用[/font][font=宋体]带分水器回流替代分馏的[/font][font=宋体]改进[/font][font=宋体]方法[/font][font=宋体],希望对现有的实验室环己烯制备实验方案提出一些建议和看法[/font][font=宋体][font=宋体]。[/font] [/font][font=黑体]关键词[/font][font=宋体]:环己烯;制备;[/font][font=宋体]分馏柱[/font][align=left][font=宋体][/font][font=黑体]前言[/font][font=宋体]环己烯又名四氢化苯,由环己醇脱水而制得[/font][font=宋体],[/font][font=宋体]是一种很重要的有机合成原料[/font][font=宋体],可以用于聚合物合成、催化剂溶剂、合成医药的中间体以及作[/font][font=宋体]为反应溶剂[/font][sup][font=宋体][font=宋体][[/font][/font][/sup][sup][font=宋体]1][/font][/sup][font=宋体]。[/font][font=宋体]实验室[/font][font=宋体]制备[/font][font=宋体]环己烯[/font][font=宋体]的方法,[/font][font=宋体]是[/font][font=宋体]在[/font][font=宋体][font=宋体]环己醇在催化剂磷酸或硫酸的存在下[/font], 加热分馏[/font][font=宋体],[/font][font=宋体]得到粗产品[/font][font=宋体],[/font][font=宋体]再用氯化钠饱和溶液洗涤[/font][font=宋体]、[/font][font=宋体][font=宋体]用[/font]5%的碳酸钠溶液中和微量的酸[/font][font=宋体],[/font][font=宋体]经过洗涤、分液、干燥、蒸馏而得到精制[/font][font=宋体]环己烯[/font][sup][font=宋体][font=宋体][[/font][/font][/sup][sup][font=等线]2[/font][/sup][sup][font=宋体]][/font][/sup][font=宋体]。[/font][font=宋体]本文主要探讨分馏柱在环己烯制备实验中的作用,简要介绍采用[/font][font=宋体]带分水器回流替代分馏[/font][font=宋体]的方法,以此作为对现有教学实验的改进建议。[/font][img=,313,93]https://ng1.17img.cn/bbsfiles/images/2021/12/202112011029317337_7606_3237657_3.jpg!w313x93.jpg[/img][font=黑体]1[/font][font=黑体] [/font][font=黑体]实验原理[/font][font=宋体]主反应为可逆反应,本实验采用的措施是:[/font][font=宋体]一[/font][font=宋体]边反应[/font][font=宋体],一[/font][font=宋体][font=宋体]边蒸出反应生成的环己烯和水形成的二元共沸物(沸点[/font]70.8℃,含水10%)。但是[/font][font=宋体],[/font][font=宋体]原料环己醇[/font][font=宋体](分析纯)[/font][font=宋体]也[/font][font=宋体]可以跟[/font][font=宋体][font=宋体]水形成二元共沸物(沸点[/font]97.8℃,含水80%)。为了使产物以共沸物的形式蒸出反应体系,而又不[/font][font=宋体]附[/font][font=宋体]带原料环己醇,本实验采用分馏装置[/font][font=宋体],[/font][font=宋体][font=宋体]并控制柱顶温度不超过[/font]90℃[/font][sup][font=宋体][2][/font][/sup][font=宋体][font=宋体]。[/font] [/font][font=宋体][font=宋体]实验装置如图[/font]1所示。[/font][font=宋体][font=宋体]在该实验中,若使用硫酸作为催化剂,一般产率不高,且硫酸腐蚀性强,容易产生碳渣及[/font]SO[/font][sub][font=宋体][font=宋体]2 [/font][/font][/sub][font=宋体]等副产物,后处理麻烦,污染环境[/font][sup][font=宋体][3][/font][/sup][font=宋体][font=宋体]。因此,本实验选用了[/font]8[/font][font=宋体]5%[/font][font=宋体][font=宋体]的磷酸[/font](分析纯[/font][font=宋体])[/font][font=宋体]作为脱水剂。[/font][font=宋体] [/font][font=黑体]2[/font][font=黑体].[/font][font=黑体]分馏[/font][font=黑体]2[/font][font=黑体].1 [/font][font=黑体]分馏柱[/font][/align][align=center][img=,274,223]https://ng1.17img.cn/bbsfiles/images/2021/12/202112011030007833_8836_3237657_3.png!w274x223.jpg[/img][/align][align=left][font=宋体][color=#333333][font=宋体][/font][/color][/font][/align][align=center][font='等线 Light'][font=黑体]图[/font][/font][font='等线 Light']1[/font][font='等线 Light'] [font=黑体]环己烯[/font][/font][font=黑体]分馏装置[/font][sup][font=宋体][4][/font][/sup][/align][align=center][font='Times New Roman']Figure 1. Cyclohexene fractionation unit[/font][/align][align=left][font=宋体][color=#333333][font=宋体][/font][/color][/font][/align][align=left][font=宋体][color=#333333][font=宋体][/font][/color][/font][/align][align=left][font=宋体][color=#333333][font=宋体]本实验使用的是刺形分溜柱,分馏柱的刺形内壁用来[/font][/color][/font][font=宋体][color=#333333][font=宋体]填充[/font][/color][/font][font=宋体][color=#333333][font=宋体]分馏柱,[/font][/color][/font][font=宋体][color=#333333][font=宋体]增大[/font][/color][/font][font=宋体][color=#333333][font=宋体]了[/font][/color][/font][font=宋体][color=#333333][font=宋体]液相和[url=https://insevent.instrument.com.cn/t/Mp]气相[/url][/font][/color][/font][font=宋体][color=#333333][font=宋体]的接触面积,[/font][/color][/font][font=宋体][color=#333333][font=宋体]使其充分进行热交换,提高不同沸点的物质[/font][/color][/font][font=宋体][color=#333333][font=宋体]的[/font][/color][/font][font=宋体][color=#333333][font=宋体]分离效率。[/font][/color][/font][font=宋体][color=#333333] [/color][/font][font=黑体]2[/font][font=黑体].2 [/font][font=黑体]分馏[/font][img=,274,63,left]file:///C:\Users\yangcf\AppData\Local\Temp\ksohtml\wps3F10.tmp.png[/img][font=宋体][color=#333333]在沸腾温度下,两种挥发性液体混合物在反应容器中达到气[/color][/font][font=宋体][color=#333333]-液平衡状态,得到的蒸气中含有较多易挥发的气体组分,将此部分蒸气体经液化转化为液体;液相中含有较多难挥发的高沸点组分。这样就完成了一次蒸馏。[/color][/font][font=宋体][color=#333333][font=宋体]将上述由蒸气冷凝而成的液体重新蒸馏,再次产生的蒸气中,易挥发物质组分的比例会增大,进而液化得到易挥发物质更多的液体。利用这样一连串的系统的重复蒸馏,最后可以得到接近纯组分的两种液体。[/font][/color][/font][font=宋体]分馏就是[/font][font=宋体]将这一连串的重复蒸馏控制在分馏柱中,让[/font][font=宋体]上升的蒸汽和下降的冷凝液在分馏柱中进行多次热交换,从而使低沸点的物质不断上升、被蒸出[/font][font=宋体],[/font][font=宋体]高沸点的物质不断地被冷凝、下降[/font][font=宋体],[/font][font=宋体]流回[/font][font=宋体]到[/font][font=宋体]加热容器中[/font][font=宋体],最终[/font][font=宋体]将沸点不同的物质分离[/font][font=宋体]。简单地讲,就是[/font][font=宋体]在分馏柱中进行多次蒸馏。[/font][font=宋体] [/font][font=黑体]2.3[font=黑体]分馏柱[/font][/font][font=黑体]的[/font][font=黑体]优点[/font][font=宋体]反复多次的简单蒸馏,既浪费时间,在重复多次蒸馏操作中的损失[/font][font=宋体]又[/font][font=宋体]大[/font][font=宋体],且[/font][font=宋体]设备复杂,所以,通常是利用分馏柱进行多次气化和冷凝[/font][font=宋体],[/font][font=宋体]得到接近纯组分的两种液体[/font][font=宋体],[/font][font=宋体]这就是分馏。工业上的[/font][font=宋体]精馏塔[/font][font=宋体]就相当于分馏柱。[/font][font=宋体] [/font][font=黑体]3[/font][font=黑体]. 环己烯制备实验的改进[/font][font=宋体]目前各有机化学实验教材中,环己烯的制备方法都采用分馏的方法,该方法存在分离提纯困难、产物纯度不高和收率较低的缺陷。[/font][font=宋体][img=,85,271]https://ng1.17img.cn/bbsfiles/images/2021/12/202112011031386093_8635_3237657_3.jpg!w85x271.jpg[/img]在杜钦芝[/font][font=宋体]的[/font][font=宋体]改进方法中[/font][sup][font=宋体][5][/font][/sup][font=宋体],采用[/font][font=宋体]了[/font][font=宋体]带分水器回流的方法替代分馏的方法[/font][font=宋体],在[/font][font=宋体]烧瓶上安装分水器,分水器上接球形冷凝管[/font][font=宋体][font=宋体](见图[/font]2)[/font][font=宋体]。将烧瓶在石棉网上加热回[/font][img=,85,271,left]file:///C:\Users\yangcf\AppData\Local\Temp\ksohtml\wps3F11.tmp.jpg[/img][font=宋体]流。[/font][font=宋体]在[/font][font=宋体]分水器中预先加入适量饱和食盐水,以[/font][font=宋体]增大[/font][font=宋体]分水器中有机层的高度,使其能[/font][font=宋体]够[/font][font=宋体]及时流回[/font][font=宋体]到[/font][font=宋体]烧瓶[/font][font=宋体]中[/font][font=宋体],并降低环己醇在水中的溶解度[/font][font=宋体]。当[/font][font=宋体]水面达到分水器支管时,及时放出少量水。[/font][font=宋体]改进后的实验方法,不但实验操作更为简单,[/font][font=宋体]而且由于[/font][font=宋体]使用了分水器,[/font][font=宋体]反应[/font][font=宋体]平衡向产物方向移动,反应几乎可以进行完全,避免了因环己醇与环己烯[/font][font=宋体]、[/font][font=宋体]环[/font][font=宋体]己[/font][font=宋体]醇与水形成的共沸物馏出,所以分离提纯简单,产物的纯度高,[/font][font=宋体]回收[/font][font=宋体][font=宋体]率可提高到[/font]60%~70%,完全可以替代传统的分馏制备方法运用于实验教学中。[/font][font=宋体] [/font][font=黑体]总结与展望[/font][img=,212,67,left]file:///C:\Users\yangcf\AppData\Local\Temp\ksohtml\wps3F22.tmp.png[/img][font=宋体][font=宋体]本实验涉及多个基础有机化学实验基本操作[/font],[/font][font=宋体]是一个[/font][font=宋体]能够有效提高学生的综合实验技能的基础有机化学实验。[/font][font=宋体]分馏操作在整个实验中的作用十分重要,分馏的效果直接影响到最终产品的回收率和纯度,因此,有必要认识分馏柱的使用方法和作用,探究更加简单高效的分馏制备方法。[/font][font=宋体] [/font][font=黑体]参考文献[/font][font=宋体][[/font][font=宋体]1][/font][font=等线] [/font][font=宋体][font=宋体]李芬芳[/font],安道利,刘秀萍,王艳[/font][font=宋体].[/font][font=等线] [/font][font=宋体]环己烯制备实验的改进[/font][font=宋体][[/font][font=宋体]J].山西大同大学学报(自然科学版)[/font][font=宋体].[/font][font=宋体]2015,31(01):31-32[/font][font=宋体][[/font][font=宋体]2][/font][font=宋体] [font=宋体]张丽丹[/font],李顺来,张春婷[/font][font=宋体].新编[/font][font=宋体]大学化学实验[/font][font=宋体][M].[/font][font=宋体][font=宋体]北京[/font]:化学工业出版社[/font][font=宋体],2020(9):118-124[/font][font=宋体][3][/font][font=等线] [/font][font=等线][font=等线]张颖[/font],姜文清,卞国庆.[/font][b][font=微软雅黑][color=#333333] [/color][/font][/b][font=等线][font=等线]环己烯合成实验的绿色化改进[/font][[/font][font=等线]J].化学教育[/font][font=等线].[/font][font=等线]2012,33(03):65-68[/font][font=宋体][4][/font][font=等线] [/font][font=宋体]李福枝[/font][font=宋体],[/font][font=宋体]肖细梅[/font][font=宋体],[/font][font=宋体]龚慧芳[/font][font=宋体],[/font][font=宋体]傅欣[/font][font=宋体],[/font][font=宋体]周晓媛[/font][font=宋体].[/font][font=宋体]浅谈环己烯制备实验中的有关注意事项[/font][font=宋体][[/font][font=宋体]J].化学工程与装备[/font][font=宋体].[/font][font=宋体]2010(08):21-23[/font][font=宋体][5][/font][b][font=宋体][color=#333333] [/color][/font][/b][font=宋体]杜钦芝[/font][font=宋体].[/font][font=宋体][font=宋体]环己烯制备方法的改进[/font][[/font][font=宋体]J][/font][font=宋体].[/font][font=宋体]教育教学论坛[/font][font=宋体].[/font][font=宋体]2020(31):[/font][font=宋体]391-392[/font][/align]
酶联免疫法 1 范围本标准规定了水产品中己烯雌酚残留量的酶联免疫测定方法。本标准适用于水产品肌肉中己烯雌酚的测定。2 规范性引用文件下列文件中的条款通过本标准的引用而成为本标准的条款。凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。凡是不注日期的引用文件,其最新版本适用于本标准。GB/T 6682 分析实验室用水规格和试验方法。3 原理测定的基础是竞争性酶联免疫抗原抗体反应,所有的免疫反应都在微孔中进行,加入己烯雌酚标准或样品溶液、己烯雌酚酶标记物、己烯雌酚抗体后,己烯雌酚与己烯雌酚酶标记物相互竞争己烯雌酚抗体的结合位点。结合的己烯雌酚酶标记物可以将无色的发色剂转化为蓝色的产物,在450nm处检测,吸收光强度与样品中的己烯雌酚浓度成反比,按校正曲线定量。4 试剂和材料本标准所用试剂除标明外,其它均为分析纯及其更高纯度,试验用水符合GB/T 6682一级水标准。4.1 叔丁基甲基醚,色谱纯。4.2 石油醚。4.3 二氯甲烷。4.4 甲醇,色谱纯。4.5 氢氧化钠,1 mol/L。4.6 磷酸,6 mol/L。4.7 百分之20甲醇的20mmol/L三羟基甲基氨基甲烷(Tris)缓冲液(pH 8.5), 百分之40、百分之70、 百分之80的甲醇溶液,此溶液现用现配。4.8 67 mmol/L 磷酸盐缓冲液(pH 7.2) : 9.61g磷酸氢二钠,1.79g 磷酸二氢钠溶解于蒸溜水,定容至1000mL,此溶液现用现配。4.9 己烯雌酚酶联免疫定量测定试剂盒, 参见附录A。5 仪器与设备5.1 酶标仪,波长450nm。5.2 离心机,转速4000r/min。5.3 氮吹仪。5.4 电热恒温水浴锅。5.5 高速匀浆机。5.6 C18 固相提取柱,长6.5cm,内径0.7cm。5.7 固相萃取器。5.8 微型漩涡混合仪。5.9 振荡器。5.10 微量加样器:20uL, 50uL, 100uL, 250uL,1000uL。 5.11 微量多通道加样器:50uL, 100uL。
最近在做苹果香精的检测,其中常见的有反-2-己烯醛,但是老板问探索一种己烯醛(就只是己烯醛,我自己都不知道有没有这种物质http://simg.instrument.com.cn/bbs/images/brow/em09508.gif)的检测方法,所以想问各位前辈们有没有做过己烯醛检测的,能否分享下,谢谢!
[color=#444444]环己烯水合制备环己醇的实验,反应结束后用乙酸乙酯萃取,最终得到含有环己烯、环己醇、乙酸乙酯的有机相(应该有一些副产物)。[/color][color=#444444] [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分析产物中环己烯和环己醇的质量,来确定环己烯的转化率和反应选择性。准备用内标法,没确定好用什么内标物,最好是毒性比较小的,望大神相助!谢谢![/color]
最近在做苹果香精的检测,其中常见的有反-2-己烯醛,但是老板问探索一种己烯醛(就只是己烯醛,我自己都不知道有没有这种物质http://simg.instrument.com.cn/bbs/images/brow/em09508.gif)的检测方法,所以想问各位前辈们有没有做过己烯醛检测的,能否分享下,谢谢!
有用[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]连用作组织或饲料中己烯雌酚残留的吗,大家都用什么衍生试剂,哪种比较好用,希望大家交流一下
准备开始做,但是条件都不知道,还要摸,有大虾知道环己烯的氧化反应用毛细柱分析的一些条件参数么?准备用Alltech的EC-5毛细柱。
水产品中己烯雌酚残留量的测定 气相色谱-质谱法 1、安全要求操作时穿工作服、戴口罩和手套,提取、净化和浓缩时在通风橱中进行,避免溶液、气体吸入和皮肤接触,废液和废渣分别倒入专用容器中,按要求处理。2、急救措施皮肤接触到有机溶剂或酸、碱溶液后用清水清洗,有机溶剂或酸、碱溅入眼中用清水冲洗。3、适用范围该标准操作规程适用于鱼、虾可食部分中己烯雌酚残留量的测定。4、检测原理以乙酸乙酯提取样品中的己烯雌酚,固相萃取柱净化,硅烷化试剂衍生化后,用气相色谱-质谱仪测定,外标法定量。5、仪器设备5.1 气相色谱质谱联用仪:配备电子电离(EI)离子源。5.2 分析天平:感量0.000 01 g。5.3 旋涡混合器。5.4 高速冷冻离心机。5.5 氮吹仪。5.6 旋转蒸发仪。5.7 固相萃取装置。5.8 具塞玻璃离心管:10 mL。5.9 SLH固相萃取柱:500 mg,6 mL。5.10 样品反应瓶:2 mL,去活,螺纹口。6、试剂和溶液6.1 试验用水应符合GB/T 6682中一级水的规定。6.2 己烯雌酚标准品:纯度≥ 99%。 6.3 乙酸乙酯:色谱纯。6.4 甲醇:色谱纯。6.5 正己烷:色谱纯。6.6 无水碳酸钠:分析纯。6.7 碳酸钠溶液:10%(W/V),称取10 g无水碳酸钠,溶于100 mL水中。6.8 己烯雌酚标准贮备液:准确称取己烯雌酚标准品0.010 g,用甲醇溶解,定容于100 mL容量瓶中,即浓度为100 μg/mL的标准贮备液,置于-18℃冰箱中保存,有效期为6个月。6.9 己烯雌酚标准工作液:临用前,准确吸取己烯雌酚标准贮备液,用甲醇稀释成浓度为0.0
最近在做苹果香精的检测,其中常见的有反-2-己烯醛,但是老板问探索一种己烯醛(就只是己烯醛,我自己都不知道有没有这种物质http://simg.instrument.com.cn/bbs/images/brow/em09508.gif)的检测方法,所以想问各位前辈们有没有做过己烯醛检测的,能否分享下,谢谢!
求教,最近在用气质做水产品中己烯雌酚的检测,但是衍生化后只有一个衍生物,可是标准上有两个,分别是cis和trans-des,谁知道是什么原因啊。还有大家前处理都是怎么做的,回收率一直在50%左右。
大家好,请问氯霉素、甲硝唑、己烯雌酚、呋喃唑酮的酸碱性是怎样的?谢谢!
我们目前采用LC-MS-MS检测肌肉中的己烯雌酚。在提取过程中发现采用乙腈、乙醚、二氯甲烷等试剂提取,经常会出现没有回收的现象。大家也遇到过这种现象吗? 把PH调到8左右也不管用。真郁闷。
按GB/T5009.108-2003的前处理方法,用单点校正法做了鸡肉中的己烯雌酚的检测,在其保留时间的地方出的峰相当的小,或都说是没有吧(因为刚做,不知道多大的峰可以算为出峰呢),我将其定为未检出,也不知道对不对.有没有决对没有己烯雌酚的样品呢.
有谁做过环己烯的纯化呀,请指导一下,非常感谢!
大家好,我最近刚开始接触试剂盒用的是德国拜发公司的试剂盒,方法是其提供的,来检验己烯雌酚我做了样品和加标的样品,可是最后加标的样品也呈现阴性,是怎么回事呢?拜托大家了
用气质检测己烯雌酚,cis-DES线性时好时坏,怎么回事啊?整个过程处理都很细心 也还是做不好
昨儿用GC-MS做一样,SCAN时候发现最大的4个碎片:267,159,296,121,疑似己烯雌酚二甲醚(cas号7773-34-4,不知道对不对?),想问问这个己烯雌酚二甲醚作何种用途?望指教指教。
[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相[/color][/url]质谱联用仪分析为何不同溶剂的反-2-己烯醇香气不同在一次调香中,发现用丙二醇和三醋酸甘油酯这两种不同溶剂稀释的反-2-己烯醇香气不一样,这两瓶不同溶剂稀释的反-2-己烯醇都是去年配制的,有点怀疑是否拿错原料(怀疑可能反-2-己烯醛)稀释了,利用[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相[/color][/url]质谱联用仪验证。样品:PG稀释的1%反-2-己烯醇(丙二醇)、GT稀释的1%反-2-己烯醇 (三醋酸甘油酯)。[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]条件:色谱柱为HP-5MS(30m*0.25mm*0.25μm);载气为高纯氦气(99.999%),恒定流速1mL/min;进样口温度为250℃;进样方式是分流模式,分流比40:1;进样量为1.0μL;柱温为二阶程序升温:初始温度为50℃,保持1min;以2℃/min的升温速率升至160℃,保持5min;以10℃/min的升温速率升至250℃,保持20min。质谱条件:色谱/质谱接口温度(MSD传输线温度)为300℃;四极杆温度:150℃;离子源温度:230℃;电离方式是EI电离,电子能量70ev;数据采集扫描类型是全扫描(SCAN),扫描范围:33~550m/z。通过数据分析化学工作站(MSD ChemStation)结合NIST20标准谱库图数据库进行检索,并对质谱图进行综合分析。图1为丙二醇稀释反-2-己烯醇的总离子流图,图2为三醋酸甘油酯稀释的反-2-己烯醇总离子流图[table][tr][td=1,2][align=center]化合物名称[/align][/td][td=1,2][align=center]分子式[/align][/td][td=1,2][align=center]保留时间/min[/align][/td][td=2,1][align=center]含量/%[/align][/td][/tr][tr][td][align=center]PG溶剂[/align][/td][td][align=center]GT溶剂[/align][/td][/tr][tr][td][align=center]丙二醇[/align][/td][td][align=center]C3H8O[/align][/td][td][align=center]6.132[/align][/td][td][align=center]98.214[/align][/td][td][align=center]0[/align][/td][/tr][tr][td][align=center]三醋酸甘油酯[/align][/td][td][align=center]C9H14O6[/align][/td][td][align=center]36.642[/align][/td][td][align=center]0[/align][/td][td][align=center]96.458[/align][/td][/tr][tr][td][align=center]甲酸[/align][/td][td][align=center]CH2O2[/align][/td][td][align=center]1.712[/align][/td][td][align=center]0[/align][/td][td][align=center]0.029[/align][/td][/tr][tr][td][align=center]乙酸[/align][/td][td][align=center]C2H4O2[/align][/td][td][align=center]2.075[/align][/td][td][align=center]0[/align][/td][td][align=center]0.276[/align][/td][/tr][tr][td][align=center]反-2-己烯醛[/align][/td][td][align=center]C6H10O[/align][/td][td][align=center]5.387 [/align][/td][td][align=center]0.103[/align][/td][td][align=center]0.337[/align][/td][/tr][tr][td][align=center]反-2-己烯醇[/align][/td][td][align=center]C6H12O[/align][/td][td][align=center] 6.070 [/align][/td][td][align=center]1.471[/align][/td][td][align=center]0.854[/align][/td][/tr][tr][td][align=center]甲酸反-2-己烯酯[/align][/td][td][align=center]C7H12O2[/align][/td][td][align=center]7.782[/align][/td][td][align=center]0[/align][/td][td][align=center]0.027[/align][/td][/tr][tr][td][align=center]乙酸反-2-己烯酯[/align][/td][td][align=center]C8H14O2[/align][/td][td][align=center]12.125[/align][/td][td][align=center]0[/align][/td][td][align=center]0.413[/align][/td][/tr][tr][td][align=center]反-2-己烯醛丙二醇缩醛[/align][/td][td][align=center]C9H16O2[/align][/td][td][align=center]17.570 +17.951 [/align][/td][td][align=center]0.036[/align][/td][td][align=center]0[/align][/td][/tr][tr][td][align=center]反-2-己烯酸-反-2-己烯-1-酯[/align][/td][td][align=center]C12H20O2[/align][/td][td][align=center]38.698[/align][/td][td][align=center]0.006[/align][/td][td][align=center]0[/align][/td][/tr][/table]分析出的化合物及含量整理成上表,由表可知,这两种用不同溶剂稀释过的反-2-己烯醇没有配制错误,只是放置时间过久了,稀释过的反-2-己烯醇发生了一系列的化学反应。反-2-己烯醇在这两种溶剂中都有一些转化为反-2-己烯醛。在丙二醇溶液中,反-2-己烯醛会和丙二醇发生缩醛反应,而在三醋酸甘油酯溶液中,有出现少量酸,甲酸和乙酸跟反-2-己烯醇发生酯化反应。所以也能解释为什么两种溶剂稀释的反-2-己烯醇放置一段时间后,分别呈现出不一样的味道啦。有不对或者想得不周到之处还望各位老师多多指点。
有没有做过4-苯基环己烯的朋友,我们找不到对应的方法,有没有大神指教一下
我们有进厂原料己烯-1,需要分析其中的羰基化合物,燕山石化有分光光度测定法,但我们建项做曲线时发现空白的吸光度都非常大,颜色很深,无法调零,想请教有经验的老师,这是怎么回事?具体步骤因为家里没有,没记住,有做过的应该知道吧。
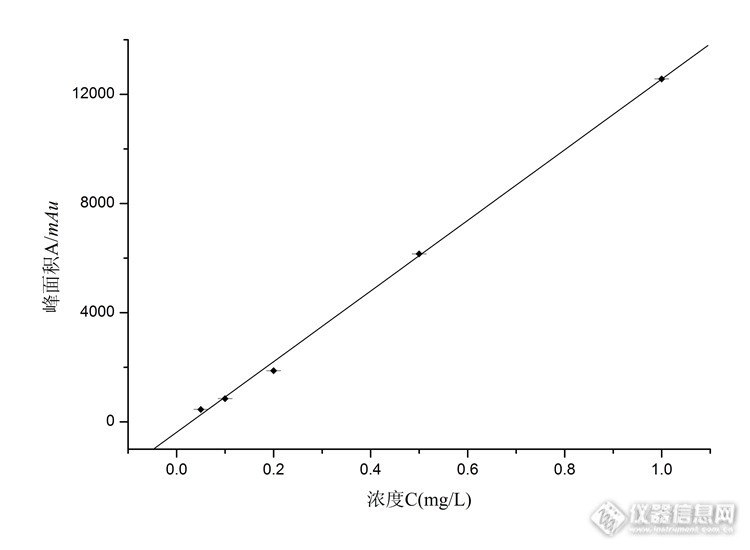
气相色谱-串联质谱技术检测水中己烯雌酚残留量摘要:本实验建立水中己烯雌酚残留量的气相色谱-串联质谱联用(GC-MS/MS)分析方法。样品采用乙酸乙酯提取,浓缩后甲醇溶解,经氮气吹干后加入BSTFA/TMCS衍生化试剂70℃衍生30mins,氮气吹干后甲醇定容待测,采用GC-MS/MS分析时,己烯雌酚衍生物在15 mins内流出。对采集的水样进行两种浓度的加标质控,回收率均在90%以上,相对标准偏差(RSD)在3.0%以内。在0.05~1.00 mg/L的浓度范围内呈线性关系,相关系数大于0.999。检出限为1.20 μg/L。该方法可准确用于环境水样中己烯雌酚残留的定量分析,灵敏度、精密度和准确度均满足残留检测的分析要求。关键词: 己烯雌酚;气相色谱-串联质谱;残留量;水中图分类号: 文献标识码: 文章编号: Determination of Diethylstilbestrol residues in water sample by gas chromatography-tandem mass spectrometry ABSTRACT: To establish a method determination of diethylstilbestrol (DES) in water sample by gas chromatography-tandem mass spectrometry (GC-MS/MS). The samples were extracted by ethyl acetate, derived with silanization reagent at 70℃ for 30 mins, then the extracts were determined with MS/MS detector based on SCAN and MRM mode, DES was well separated within 15 min. When the spiked average recoveries above 85%. The RSD ranged within 3.0%, The calibration of those pesticides were linear (correlation coefficients not less than 0.999) within the range of 0.05~1.00 μg/mL. The method was accurate and sensitive, was suitable for analysis of DES residues in water samples.KEY WORDS: diethylstilbestrol; gas chromatography-tandem mass spectrometry; residues; water sample1 引言 己烯雌酚(Diethylstilbestrol, DES)属激素类化合物,作为生长促进剂被广泛添加在饲料中应用于水产养殖行业促进鱼类生长,为水产业产品数量的增长发挥了一定作用。但己烯雌酚作为一种人工合成的具有雌激素样作用的化学物质,许多科学实验证实对人类和动物具有危害,导致机体代谢紊乱、发育异常或肿瘤等,是一种致癌物质,被欧盟等国在食用性动物饲养中列为禁用品,2002 年我国农业部发布176号公告禁止在畜禽水产养殖过程中使用己烯雌酚。己烯雌酚是脂溶性物质,难降解,易在动物体内残留,在水源和土壤中容易大量富积,造成环境激素污染恶性循环,由于会对环境水造成严重影响, 可通过饮用水威害人体健康 。因此,建立水样中己烯雌酚残留量的分析方法具有重要意义。目前,测定雌酚类激素的方法有酶联免疫(ELISA)法、比色法、电化学法、放射免疫(RIA) 法、色谱-质谱法、高效液相色谱(HPLC)法及毛细管电色谱法等。比色法、电化学法由于不能用于分离且干扰大等缺点,很少用于残留检测。本实验采用灵敏度和准确度较高的串联质谱检测器,可提高己烯雌酚定性与定量的准确性,二级质谱相对于一级质谱,其抗干扰能力更强,可有效消除单级质谱离子信息少的问题,对样品前处理的要求较低,可准确反映样品中己烯雌酚的残留量,其灵敏度、稳定性、准确度均较高。2 材料与方法2.1 材料2.1.1 试验原材料无公害水产养殖基地:淡水养殖用水。2.1.2 主要试剂与材料乙酸乙酯、二氯甲烷、正己烷、甲醇(色谱纯,美国Fisher Scientific公司);乙醚、叔丁基甲醚(优级纯,天津化学试剂厂);己烯雌酚标准品(德国Dr. Ehrenstorfor公司);衍生化试剂:N-甲基-N-三甲基硅基三氟乙酰胺(MSTFA)、二硫赤藓糖醇(DTE)、三甲基碘硅烷(TMIS)、N,O-双(三甲基硅烷基)三氟乙酰胺/三甲基氯硅烷(BSTFA/TMCS体积比99:1)(美国Supelco公司)。2.1.3 主要仪器气相色谱-串联质谱仪(7890B-7000B,美国Agilent公司);离心机(CT18RT,上海天美公司);氮吹仪(MG-2000,日本EYELA公司);旋转蒸发仪(SB-1100,日本EYELA公司)。2.2 标准溶液和衍生化试剂配制己烯雌酚标准溶液:配制10.0 mg/L的标准储备液,保存于1~4 ℃冰箱中冷藏,使用时用甲醇稀释至相应浓度做标准工作曲线。MSTFA-DTE-TMIS衍生化溶液:准确称取0.0040g DET溶解到2.00mL MSTFA,加入5.00μL TMIS,低温于1~4 ℃冰箱中冷藏避光保存。2.3 样品前处理2.3.1 分离提取准确量取40.0 mL水样品于具塞离心管中,加入20 mL提取试剂乙酸乙酯,振荡后放入高速离心机10000 r/min离心3 min,将上层有机相倒入浓缩瓶中,40℃减压浓缩近干,用甲醇溶液5 mL定容,转移至10 mL试管中氮气吹干。2.3.2 衍生化在吹干的试管中加入0.20 mL的衍生化试剂,在70℃烘箱中衍生化30 min,取出后氮气吹干1.00 mL甲醇定容上机。2.3.3 标准曲线及质控样分别配置0.05、0.10、0.20、0.50、1.00 mg/L浓度的标准工作液,按2.3.2衍生化后进样制作标准曲线,同时将样品添加不同浓度的标准品按2.3.1和2.3.1试验过程进行回收率质控试验。2.4 仪器条件色谱柱:HP-5MS(30 m×0.25 mm, 0.50 μm);载气:氦气(99.999%);恒流模式流速:1.00 mL/min;进样:1.00 μL,不分流;进样口温度:250 ℃;程序升温:80 ℃保持1 min,以20 ℃/min升温至280 ℃,保持10 min;离子化方式:电子轰击(EI);离子化能量:70 eV;离子源温度:230 ℃;传输线温度270 ℃;溶剂延迟:3 min;扫描方式:多反应监测(MRM)。扫描范围:50~450 amu;定量方式:外标法。3 结果与讨论3.1 提取溶剂选择本实验选择了乙醚、叔丁基甲基醚、乙酸乙酯、正己烷、二氯甲烷等溶剂作为提取剂,通过对添加浓度为1.00 mg/L的样品分别进行萃取回收率测定,由图1可见乙酸乙酯的萃取效率最高,萃取回收率稳定并达到90%以上, 所以本方法选择乙酸乙酯作为提取溶剂。http://ng1.17img.cn/bbsfiles/images/2016/07/201607081537_599845_1634341_3.jpg图1不同溶剂提取效率Fig. 1 Effect of Different Solvents on Extraction Efficiency 3.2 衍生化试剂及衍生化温度的选择本次试验选择MSTFA-DTE-TMIS和BSTFA/TMCS(99:1)两种衍生化试剂,均能与己烯雌酚的羟基进行硅烷化衍生反应,确定衍生化时间为30min,考察不同温度对于衍生化效率的影响,结果见图2。由图2可见,在70℃条件下衍生化效率最好,不同温度条件下衍生化试剂BSTFA/TMCS (99:1)的效率均优于MSTFA-DTE-TMIS,同时BSTFA/TMCS(99:1)有配制好的商品可供购买,使用便捷,且毒性也较小,因此本次试验选用BSTFA/TMCS为最佳衍生化试剂。[img=,
己烯雌酚哪种检测方法的效果较好?[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]还是[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]?望老师不吝赐教

领导让用气质做己烯雌酚,我们的仪器是热电的DSQII,刚开始做这个项目的时候出峰挺好的,最近不出峰了,让人很困惑,机器调谐没有问题 所以请教一下论坛网友 看能否解答 用的是硅烷基衍生剂 衬管加不加玻璃棉都出不了峰图1: 上面是我今天做的 0.5ppm衍生后上机的图谱 下图是我刚开始做这个项目上的0.1ppm衍生后上机的图谱 都是同一个方法做的http://ng1.17img.cn/bbsfiles/images/2014/07/201407101438_506150_2886868_3.jpg图2 10-100 的峰 柱评价和 机器面板上的 leak check都能passhttp://ng1.17img.cn/bbsfiles/images/2014/07/201407101440_506151_2886868_3.jpg图3 调谐液的峰良好 我觉得质谱部分良好http://ng1.17img.cn/bbsfiles/images/2014/07/201407101441_506152_2886868_3.jpg图5 调谐报告部分 响应不错 真不知道 为什么 做不出己烯雌酚http://ng1.17img.cn/bbsfiles/images/2014/07/201407101442_506153_2886868_3.jpg
畜禽肉中己烯雌酚的测定测量不确定度分析依据JJF1059-1999《测量不确定度评定与表示》、CNAL/AG06《测量不确定度政策实施指南》和CNAL/AR11《测量不确定度政策》分析1目的对畜禽肉中己烯雌酚的测定的不确定度进行分析,找出影响不确定度的因素,对不确定度进行评估,如实反应测量的置信度和准确性。2适用范围畜禽肉中己烯雌酚的测定。3 职责3.1检测人员负责按操作规程操作仪器,确保测量过程中仪器正常运转,消除各种可能影响实验结果的意外因素,了解影响不确定度的因素。3.2校核人员负责检查原始记录及不确定度的计算方法。3.3技术人员负责审核检测结果和不确定度分析结果。4不确定度分析4.1. 测定方法按照国家标准GB/T5009.108-2003《畜禽肉中己烯雌酚的测定》中规定进行测定。 检测过程为:1) 称取样品:用精度为0.1mg的精密电子天平称取50.0000g样品,称准至0.1mg。2) 样品前处理:把样品置于300mL烧杯中,加入50mL水和100mL丙酮,用组织捣碎机提取1~2分钟。匀浆液过滤后,取滤液100ml于500mL分液漏斗中。向滤液中加入10-15g无水硫酸钠,充分摇动,静置分层;取上层有机相。下层水相用50mL二氯甲烷再提取一次。合并提取液,经装有20g-30g无水硫酸钠的玻璃漏斗脱水后滤入250ml茄型瓶中,再以40mL二氯甲烷分数次洗涤容器和无水硫酸钠,洗涤液也并入茄型瓶中,用旋转蒸发器浓缩后用二氯甲烷定容到10mL。装样上机,进样1.0uL。3) 己烯雌酚标准原液:使用国家标准物质中心提供的100mg/L的标准溶液。4) 己烯雌酚标准曲线溶液:将己烯雌酚标准原液用1ml移液管和100ml容量瓶稀释成1mg/L ;再用1ml移液管和100ml容量瓶把1mg/L的标准稀释成0.01mg/L;用5ml移液管和10ml容量瓶把1mg/L的标准稀释成0.5mg/L;用1ml移液管和10ml容量瓶把1mg/L的标准稀释成0.1mg/L;用1ml移液管和50ml容量瓶把1mg/L的标准稀释成0.05mg/L。共得到1mg/L、 0.5mg/L、0.1mg/L、0.05mg/mL、0.01mg/L的标准系列溶液。5) 样品的上机分析后,在[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]上用5点校准曲线法进行定量。4.2. 测量流程方框示意图 4.3. 己烯雌酚含量的计算 式中:X——试样中己烯雌酚的含量,单位为毫克每千克(mg/kg);Aop——己烯雌酚的峰强度(峰面积);Aref——己烯雌酚标准的的峰强度(峰面积);Vop——最终定容体积,单位为毫升(mL);Vext——提取液总体积,单位为毫升(mL);Vclean——取用的提取液总体积,单位为毫升(mL);Msample——试样质量,单位为克(g);Rec——回收率。计算结果保留两位有效数字。 4.4 不确定度的来源本测试方法的不确定度来源主要来自如下几部分:4.4.1 测量重复性带来的不确定度分量 (含人员、环境、测量方法和仪器重复性等其他分量的贡献)。样品反复进行10次分析,见表1。表1 10.2050.00636×10-620.2110030.2040.00749×10-640.2300.019361×10-650.2240.013169×10-660.2130.0024×10-670.1990.011121×10-680.2130.0024×10-690.2010.010100×10-6100.2090.0024×10-6 0.211 (A类不确定度)4.4.2 样品测试全过程中引入的不确定度分量 。(B类不确定度)4.4.2.1 样品称取和前处理过程中天平准确度和容量瓶准确度引起的不确定度分量 。a 天平准确度引起的不确定度分量 天平的准确度为σ=0.1mg,采用矩型分布计算标准不确定度。 b 100ml容量瓶准确度引起的标准不确定度分量 。允差值为±0.1ml,按矩形分布。 C. 10ml容量瓶准确度引起的标准不确定度分量 允差值为±0.02ml,按矩形分布。 , 4.4.2.2标准溶液配制过程和GC/FPD制定校准曲线时引入的不确定度分量 。a). 己烯雌酚标准溶液引入的不确定度分量 。己烯雌酚标准溶液的浓度值为100mg/L±0.11mg/L,采用矩形分布。 b). 稀释过程中的移液管引起的不确定度分量 。1ml移液管的允差值为±0.008ml,5ml移液管的允差值为±0.025ml,都是矩形分布。1ml的移液管: , 5ml的移液管: , C). 容量瓶的准确度引起的不确定度分量 。10ml的容量瓶的允差值为±0.02ml,50ml的容量瓶的允差值为±0.05ml,100ml的容量瓶的允差值为±0.1ml,都是矩形分布。10ml的容量瓶: , 50ml的容量瓶: , 100ml的容量瓶: , d). 10μl进样针准确度引起的不确定度分量 。允差值为±0.02μl,矩形分布。 5. 合成标准不确定度计算标准不确定度一览表标准不确定度分量u(xi)不确定度来源标准相对不确定度 样品测量重复性0.0460 样品测试全过程( )0.0111 样品称取和前处理( )1.28×10-3 标准溶液配制过程和GC/FPD制定校准曲线( )0.0110 天平的准确度1.15×10-3 100ml容量瓶准确度5.77×10-4 10 ml容量瓶准确度1.15×10-3 己烯雌酚标准原液浓度5.77×10-4 标准稀释过程中移液管的准确度0.0107 标准稀释过程中容量瓶的准确度1.91×10-3 10μl进样针1.15×10-3合成相对不确定度: 6. 扩展不确定度的评定扩展不确定度通过使用包含因子k=2计算得出: 7.不确定度报告按照国家标准GB/T5009.108-2003规定的检测程序进行,最后测量出本次蔬菜水果中己烯雌酚含量为:0.21(2)mg/kg。[img]http://bbs.instrument.com.cn//images/affix.gif[/img][url=http://bbs.instrument.com.cn/download.asp?ID=194104]畜禽肉中己烯雌酚的测定测量不确定度分析.doc[/url] [color=#DC143C][size=4][font=黑体]应疯子哥的要求,把公式及图片贴上来,在9楼-13楼有版主ROGERSW的完整佳作。[/font][/size][/color]
BP 028-2002 饲料中己烯雌酚的测定