Countstar® FL在抗体亲和力实验中的应用
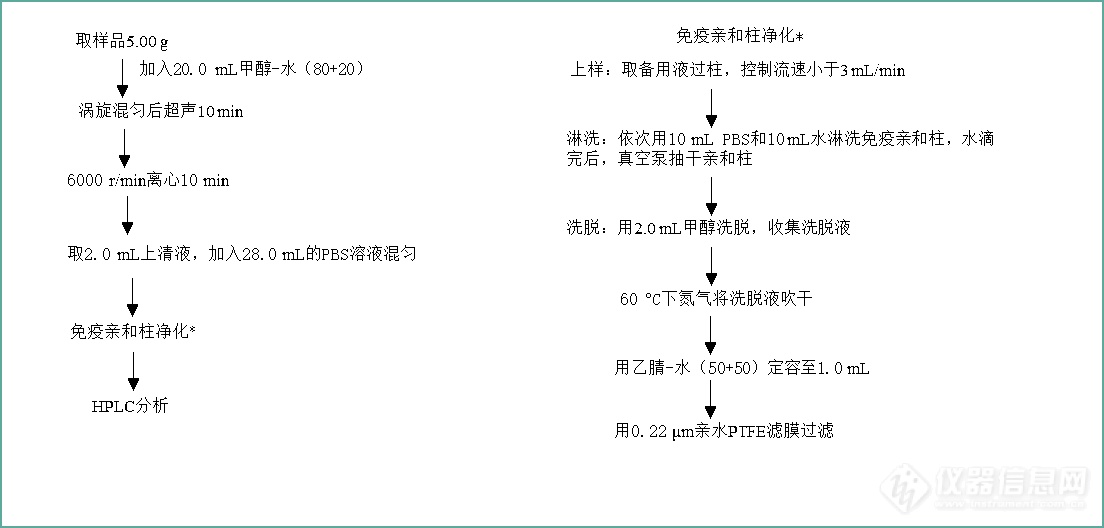
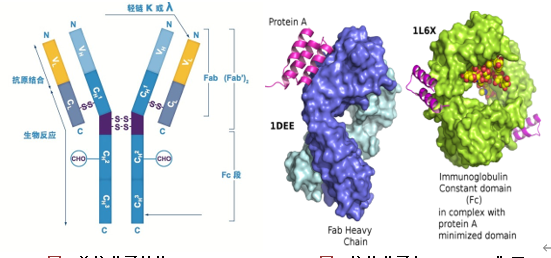
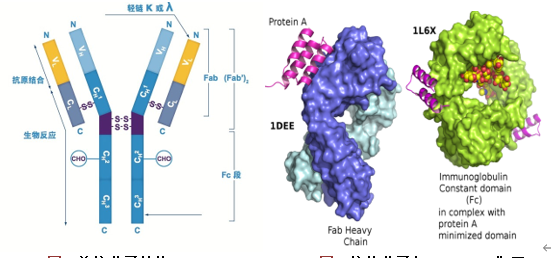
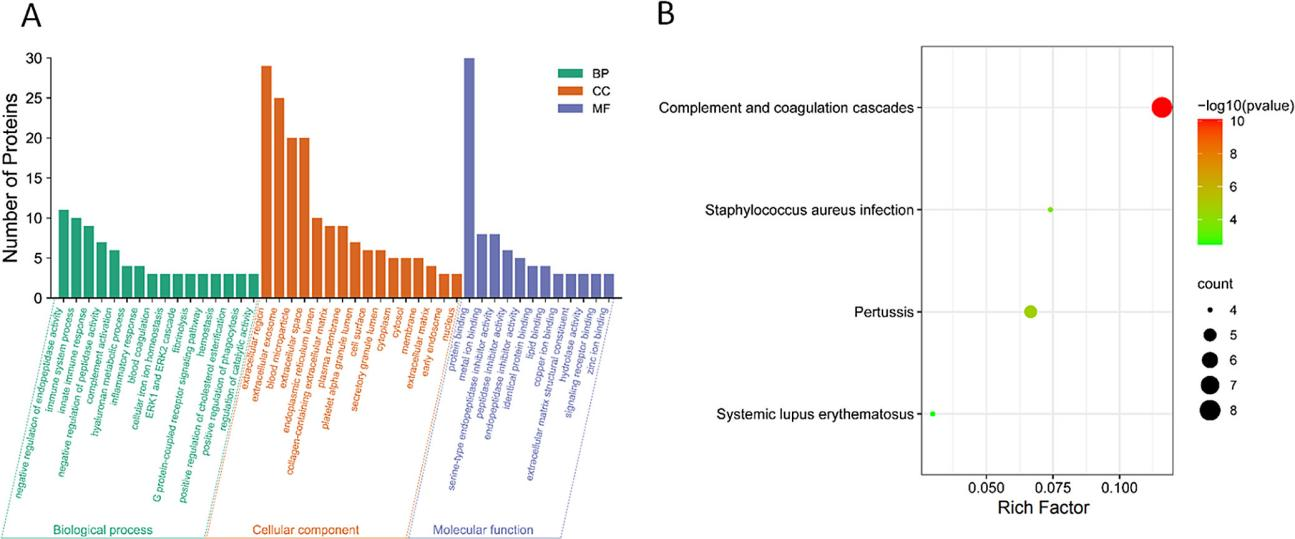
抗体是自然产生用于帮助免疫系统抵御细胞内外侵害的免疫球蛋白。免疫荧光法测定细胞水平的抗体亲和力大小是评价抗体效果非常重要的指标,当前主要的测定方法是利用流式细胞仪以实现相对定量。而countstar fl可通过间接免疫荧光法检测不同抗原抗体反应呈现的平均荧光强度直接定量评价抗体亲和力大小,同时也可检测细胞浓度、活率。此外,可获得细胞图片,实验过程中实时拍摄明场和荧光图像。countstar fl为客户在抗体药物筛选中提供了快速、准确、可靠的抗体亲和力检测方法。countstar fl(图1)是一个智能的、直观的细胞分析仪器用于多种细胞实验,包括细胞转染,细胞凋亡,细胞表面标志物,细胞活力,抗体亲和力和细胞周期的评估。该系统提供了强大的荧光定量结果。易于使用的自动化程序指导你完成从细胞图像采集到数据分析的过程。 材料:countstar 产品:countstar fl细胞分析仪/countstar样品板/0.2% 台盼蓝染色液 (cs0101001-50)其他材料cho细胞系/dmem细胞培养基(hyclone-sh30243.01)/胎牛血清(hyclone-sh30084.03)/胰蛋白酶(hyclone-sh30042.01),其中,cho细胞系稳定表达x蛋白,用于评价原研药和仿制药的亲和力一抗:不同浓度梯度的002-bmk1,002-bmk2, ab1, ab2, ab3, ab4, ab5, ab6, ab7, ab8, ab9, pcsk-9。其中,002-bmk1,002-bmk2能特异性的与x蛋白结合(阳性抗体),pcsk-9是阴性对照抗体。二抗:alexa fluor 488 goat anti-mouse igg (biolegend),5μg/ml软件graphpad prism5方法:细胞培养条件1. cho细胞培养在完全培养基中,组成为:500mldmem培养基,2 mm l-谷氨酰胺, 1.5 g/l 碳酸氢钠和10% 胎牛血清。于37°c, 5% co2培养箱中培养48小时;2. 消化收集细胞。染色步骤1. 使用台盼蓝计数测定细胞浓度;2. 准备3*10^5个细胞/每个反应;3. 细胞样品于400g下离心3-5分钟,去上清,用100μl pbs重悬;4. 轻轻混匀细胞样品,于400g下离心3-5分钟,去上清,用100μl cellstaining buffer重悬;5. 在细胞样品中加入不同浓度梯度的一抗,每种抗体最高浓度为10μg/ml,4倍梯度稀释,最低浓度为0.01μg/ml;6. 37℃下,避光孵育60分钟;7. 细胞样品于400g下离心3-5分钟,去上清,用100μl pbs重悬;8. 轻轻混匀细胞样品,于400g下离心3-5分钟,去上清,用100μl cellstaining buffer重悬;9. 在每个反应组内加入5μg/ml二抗;10. 常温下,避光孵育30分钟;11. 细胞样品于400g下离心3-5分钟,去上清,用100μl pbs重悬;12. 轻轻混匀细胞样品,于400g下离心3-5分钟,去上清,用100μl cellstaining buffer重悬;13. 混匀样品,加入20μl于细胞计数板中,上机检测。注:以上操作可使用ep管或96孔板。图像获取及数据分析1. 选用“台盼蓝计数”进行细胞浓度和活率测定;2. 单荧光模块的程序用于获取fitc通道下alexa fluor 488的图像;3. 每个样品采集1或3个视野(该实验检测1个视野);4. 检测过程中直接呈现数据结果,图像获取和数据分析完成后,导出数据结果。抗体亲和力检测过程如图2。 图2.抗体亲和力检测过程 不同抗体梯度稀释添加剂量选用96孔板测定不同抗体与cho细胞反应的剂量效应实验,包括原研药、抗体药和阴性对照(图3)。一抗浓度按照下表指示梯度降低(10μg/ml-0.01μg/ml)。 图3. 96孔板中抗体浓度. 每孔中有cho细胞(30万个),二抗(5μg/ml)及图示一抗(0.01, 0.039, 0.156, 0.625, 2.5, 10μg/ml).其他孔为空. countstar fl系统图像获取 countstar fl内置的抗体亲和力检测程序进行明场,fitc通道下alexa fluor 488图像的获取。明场的图像作为一个参考标准对荧光场的图像进行分割,进而获取荧光场的信号。不同浓度梯度ab4,最高浓度pck9和002-bmk1样本图像结果如图3所示。 图4. 0.01, 0.039, 0.156, 0.625, 2.5, 10μg/ml ab4与cho细胞反应后的细胞图像.图像显示抗体浓度越高,荧光信号越强. 002-bmk1抗体能特异性的与x蛋白结合,pcsk-9为阴性对照抗体. 图像代表002-bmk1样品有较强的荧光信号,pcsk-9样品基本没有荧光信号. 抗体亲和力定量分析 不同抗原抗体反应呈现的平均荧光强度直接定量评价抗体亲和力大小。稳定表达x蛋白的cho细胞系应用于分析抗体亲和力,countstarfl可直接显示测试结果,并将数据导出进行分析。使用graphpad prism5对抗体的ec50进行分析(fig. 5a)。测试结果显示样品荧光强度随着一抗浓度升高而增加,平均荧光强度曲线代表不同浓度下每个抗体的反应活性,其中pcsk-9为阴性对照抗体,样品基本没有荧光信号。各抗体的logec50结果显示原研药的抗体亲和力比仿制药更好,而仿制药中ab2, ab3, ab4, ab6效果较好,可进行下一步实验(fig. 5b)。countstar fl系统为评价抗体亲和力提供直接可靠的结果。 图5. 抗体亲和力定量分析结果. a.不同浓度梯度抗体下不同抗原抗体反应中平均荧光强度.b.原研药和仿制药的分析结果比较. 总结: countstar fl系统提供了一个快速,直接,容易的方法评价抗体亲和力。此外,它是融合了电子显微镜,图像处理,自动细胞计数于一体的设备。另外,countstar fl提供扩展功能,用户可以根据自身需要进行定制。countstar fl是一款高度可移动的设备,内置多种预设程序,便于用户快速获取准确,稳定,可高度重现的数据。仪器中每个应用模块简单易用,大大简化了常规实验室的工作,给客户提供高质量的科研数据。countstar fl为客户开展抗体亲和力实验提供一个直接可靠的实验结果。