[align=left][color=#000000]作为史上最成功的几款软件之一,MS Excel电子表格(后文简称Excel)由于其易用性和灵活性,被广泛应用于全球各行各业,成为最流行的个人计算机数据处理软件。虽然制药行业不算是Excel的最重度使用者,但从研发到生产,流通,从日常办公到实验室的业务处理,每个环节都可以看到Excel使用的身影。[/color][/align][align=left][/align][align=left]但可惜的是,Excel毕竟是面向普罗大众的软件,并没有针对GxP合规要求专门设计,其本身具有一些固有的安全和审计跟踪缺陷。正是由于这些缺点,Excel在GxP领域内的应用一直是监管机构检查的重点。[/align][align=left][/align][align=left]最近20年,随着行业内各种专业软件的推出以及现有软件的完善,例如LIMS(实验室信息管理系统),CDS(色谱数据系统),ELN(电子实验记录系统),MES(生产执行系统),数据的存储和处理方式有了更多的选择。由此,为了减轻在Excel电子表格应用合规性上的压力,许多制药企业尝试在关键业务领域中逐步“替换”电子表格。由于需要替换的数量不小,加上替代系统也有很多潜在的合规问题需要解决,使得“替换”过程并不顺利。再者,专业软件只能处理其管理范围内的数据,在替换上有一定的局限性,即便是经历了几十年信息化建设的欧美大型药企,想要彻底杜绝Excel的使用也几无可能。Excel仍旧以其易用性和灵活性在药物研究与开发、生产、流通等各个环节扮演着独特的角色。那些早期在Excel应用上做出了诸多努力的企业,功夫并没有白费,通过Excel模板的设计和使用,能够帮助企业梳理自身的工作流程,清理各种基础数据,明确信息化的需求,从而为桌面工具向大型信息系统过渡打下了良好的基础,同时在一些重要环节成为这些信息系统的有益补充,一个将电子表格深入应用的企业在实施大型信息系统的成功率上绝对要远远超出那些连电子表格都用不好的企业。[/align][align=left][/align][align=left]虽然Excel的群众基础特别好,但群众使用Excel的基础却并不是很好(同样适用于word)。对于国内广大药企尤其是中小药企,能够把Excel以及Office中的其他软件用好,在管理水平和效率提升上就可以上一个大的台阶。不顾自身情况一味追求高大上的系统,盲目跟风,做不切实际的预期,其结果一定是费力不讨好,花钱不见疗效。电子表格工具作为大型系统的简单替代方案,投入少,见效快,更新起来也容易,很适合应用于没有信息化基础的企业。然而,这种易用性、灵活性以及Excel在合规上的缺陷,导致在其开发、使用和管理过程中很容易产生问题。同时,Excel作为通用型软件,并未针对GxP合规要求进行专门设计,其本身具有一些固有的安全和审计跟踪缺陷。正是由于这些缺点,Excel在GxP领域内的应用一直是监管机构检查的重点。[/align][align=left][/align][align=left]按照对病人安全、产品质量及数据完整性的影响,分为如下3类:1.高影响的包括用于原料检测、成品检测的电子表格,用于毒理学研究的表格,临床研究统计分析表格等。2.中等影响的包括标签打印和分发数据记录表格,实验趋势分析表等。3.低影响的如生产计划表,培训出席统计表等。因此,在充分了解Excel潜在风险的基础上,对其采用最佳实践的优化设计、验证和控制以确保其合规使用,已成为监管机构认可的主流做法。[/align][align=left][/align][align=left]同时,监管机构内部实验室仍然在大量使用电子表格。FDA所属上级机构HHS就制定了详细的Excel文档检查表,并自2012年初后公布在FDA官网上。这份检查文档的详细程度充分说明了HHS及FDA对Excel风险的充分认识和重视。[/align][align=left][/align][align=left]电子表格风险的来源:[/align][list=1][*]电子表格的设计缺陷以及使用过程中的不受控带来的直接风险;[*]电子表格本身在合规功能上的缺陷带来的风险 [*]企业对电子表格的本质认识不够以及管理上的缺失带来的间接风险 [*]电子表格风险场景分析及其控制措施:[/list][b]风险场景1:模板使用不受控[/b][color=#000000]由于电子表格的普及性,其应用和开发不仅有专业的IT人员,更有大量的业务部门人员参与。极端的混乱情况是每个人都设计自己的计算表格,从而导致计算方式、格式、数值修约等的差异性极大。这种放任自流无任何管理的应用方式在需要合规的GLP,GMP,GCP领域绝对是要禁止的。其后果也是非常糟糕的。[/color][color=#000000]做得规范一些的公司会指定人员进行电子表格的设计和审核,并将设计好的模板统一进行管理和分发。问题往往会出在分发的环节中。电子表格的使用一般会涉及到业务部门的多个人员。我们常常看到主管将电子表格通过邮件、拷贝,或者共享文件夹的方式分发给所属人员。一方面使用人员是否真正使用了这些模板不得而知。另一方面,由于业务流程的变化,或者模板的优化升级,加上文件命名没有版本控制,模板使用人员并不能识别哪个版本是最终版本或者现行版本。采用这种主动分发的方式去很难保证被动接受的终端人员使用的是最新版本,从而导致模板的误用。有些公司虽然意识了这些风险,但采取的措施过于落后,例如将Excel模板的使用限定于某台计算机,由专人在专机上维护电子表格。使用人员只能在该台电脑上使用。这种方法虽然降低了风险,但也大大降低了便利性。[/color][b]建议:[/b][color=#000000]统计公司内部的所有Excel模板,制定命名规则并给予唯一性编号,形成一份电子表格的台帐。同时将模板置于局域网内的共享文件夹中,并真正使用到Excel模板的特性(扩展名为xltx),并将终端计算机的Excel模板目录定位到该共享文件夹。[/color][b]风险场景2:“Save as”另存为的滥用[/b][color=#000000]大家喜欢用“Saveas”(另存为)一部分原因是出于无奈。追根溯源,产生这一现象的原因是Excel模板的设计人员和维护人员对Excel软件掌握得不够深入,对扩展名为.xlsx和.xltx两类文件的作用没有弄清楚。前者是普通的电子表格文件,而后者则是Excel的模板文件。我们看到绝大部分的公司在Excel的使用中都是将设计好的模板直接保存为xlsx文件,而不是xltx文件。这就导致大家获得这些模板并填写完数据后要选择另存为独立的数据文件。手脚稍快,这些所谓的模板很可能被大家误填上了数据。后续就是不断的删数据,录入数据,另存为。由此引起的漏删数据,模板私自修改,文件之间的关系错乱,无法追溯等等问题就在所难免了。此前,WHO的检查专家就对国内一些药企滥用“另存为”功能提出了严厉的批评。[/color][color=#000000]有些公司为了提高模板最新版本的识别度,在现行的Excel模板的文件名末尾加上了诸如“Final”,”最终版”之类的标识,一旦这些措施遇上了“另存为”,也形同虚设,因为每个人都可以把任何表格保存为Final或者“最终版”。[/color][b]建议:[/b][color=#000000]真正把Excel模板的功能使用上,当用户点击“新建”时,能浏览到所有的模板,并由Excel使用这些模板自动为用户创建用于填写数据的文件。这样,用户无需四处复制粘贴和保存那些所谓的模板,避免了错误的同时,提高了效率。在GxP环境中,控制“另存为”菜单的使用。通过加载宏可以实现对另存为的控制,但如果用户通过Excel文件的复制达到制作副本的目的,则控制“另存为”也无能为力,只能依赖更加严格的Excel合规软件实现管控。[/color][b]风险场景3:不受保护的Excel工作薄[/b][color=#000000]不对电子表格做任何保护是较常见的问题,也是电子表格最重要的风险点。虽然在国外这种低级的错误几乎已经绝迹,但在国内还是有很多人不知道电子表格需要保护,或者不知道如何去保护。如果不是这几年计算机系统验证与合规宣传得比较密集,可能还是有一部分人没有意识到电子表格也属于计算机系统,同样是需要进行访问控制的;同我们常见到的色谱数据系统,LIMS系统并没有本质的不同。[/color][color=#000000]设计过电子表格公式的人会明白如果这些公式不加保护,是何等的容易被人无意的修改,导致一连串的错误结果。对电子表格的保护包括工作表级的保护和工作薄的保护。前者是针对单个工作表中的元素进行保护设置,包括单元格的锁定与保护,行和列的编辑。后者是针对包含多个工作表的结构保护。如果你的电子表格包含多个工作表,那么除了每个工作表启用保护外,工作簿也需要启用结构保护。因为未启用工作薄结构保护的电子表格,用户可以删除里面任意一个工作表,而这些工作表之间很可能有数据的关联引用和计算。意外删除工作表同样会导致结果错误。[/color][color=#000000]除了工作表和工作薄的结构不受保护,Excel文件本身的安全性也常常容易被忽视,尤其是重要的模板文件,计算结果文件,从而引起Excel文件被删除或替换。[/color][b]建议:[/b][color=#000000]对工作表内的公式,常量,标准数值,格式,工作薄结构进行保护,对Excel设置打开密码,从而做到一定程度上的访问控制。对公用模板的存放位置进行保护,防止无意的删除或有意的替换。[/color][b]风险场景4:设计缺陷导致的错误[/b][color=#000000]电子表格的设计开发从本质上来说也属于计算机软件开发的范畴,但多数制药企业并不会配备专门的电子表格设计开发人员。电子表格的设计和开发往往由电子表格的使用者承担,这些使用者一般具有一定的Excel使用经验,但多数人员并未经过软件工程及原理或者电子表格设计开发的系统学习,这就可能会导致设计上的各种问题。[/color][color=#000000]设计缺陷导致的错误可能有下边这些情况:1)没有设定数据输入格式的限制导致的计算错误,比如FDA于2014年发布的一篇警告信中就有关于电子表格未做输入格式限制导致统计结果错误的描述;2)电子表格公式错误、公式与方法文件描述不符、修约规则与方法文件描述不符、有效数值保留位数错误、多次修约等导致的计算结果错误;3)电子表格设计时未考虑出错情形的处理,比如将结果判断设置为数值超过指定范围时报告“Fail”,否则报告“Pass”,这种设计将会导致在数据无效或数据错误时也报告出“Pass”的错误结果;4)不同设计开发人员或者同一人员设计开发的不同电子表格未按统一的风格进行数据输入、结果计算、结果输出区域的划分和标识,未使用有明显意义的表头,或者未对重要单元格添加解释性说明的,导致使用过程中的数据输入错误,导致错误的计算结果;5)电子表格没有清晰的名称、基本描述、作者、目的与用途、限制条件等,导致使用者误用电子表格,比如一种产品的结果计算误用了另一品种的表格,导致错误的结论。[/color][b]建议:[/b][color=#000000]参照HHS的检查表以及其它的良好设计规范,制定公司内部的良好设计SOP。对候选人员进行统一的培训和考核,通过培训和考核的人员才能进行电子表格的设计、开发和验证。[/color][b]风险场景5:软件版本差异或设置差异导致的错误[/b][color=#000000]我们都知道,高版本的Excel软件可以向下兼容,不能向上兼容。显然,用高版本软件开发的电子表格不能直接在低版本的软件中使用,企业中一般也不会出现将Excel软件从高版本降级到低版本的情况。[/color][color=#000000]那么,用低版本软件开发的电子表格是否可以直接用于高版本的软件呢?答案也是否定的。Excel软件版本的不同或者设置的不同,可能导致电子表格文件的重大错误。比如在不同的语言设置中,算术运算的表达不一定是相同的(例如在Excel97中,同样一个操作,在设置为英语时表达为“convert”,而在设置为德语时则表达为“Umwandel”)。当在不同语言之间进行切换时,这两种表达并不会自动进行转换,这将导致计算错误。另外一个例子是,在Excel97中,语言设置为英语时的小数点为“.”,而设置为德语时的小数点为“,”,切换语言设置时同样不能自动进行转换。Excel版本不同,其中的计算、控件或者加载项等也可能有细微差别。[/color][color=#000000]如果电子表格中涉及到宏命令的使用,则必须在选项中设置“启用宏”。这样就需要在每台使用电子表格的终端电脑上进行设置,否则在设置为“禁用宏”的电脑上使用带宏命令的电子表格将会导致错误。[/color][color=#000000]随着Excel软件多年来的升级,版本差异或设置差异导致的计算错误被逐步的改进,但微软从来没有申明这些问题已经不复存在,在GxP领域中使用Excel电子表格仍然不能忽视这一问题。[/color][b]建议:[/b][color=#000000]在发布电子表格模板时,对其经过验证的使用环境进行记录(配置管理),这些环境包括操作系统版本、Excel软件版本、语言设置、安全设置、加载项设置等;尽可能在公司范围内统一软件版本;在改变使用环境时,需要对其影响进行评估,并依据评估结果进行必要的再验证或确认。[/color][b]风险场景6:打印的纸质表格无法溯源[/b][color=#000000]电子表格软件本身不具有电子签名功能。在保存电子表格的同时,将电子表格打印为纸质文件签署并保存是普遍的做法。然而,多数公司的SOP并没有细致到规定电子表格文件命名和存储的具体方式,也没有规定纸质文件的命名如何体现对应电子文件的名称和存储位置。随着时间的推移,找到纸质文件对应的电子文件会越来越难。在一些没有对电子文件进行有效备份的公司,在经历了较长的时间后,由于原始电脑的升级换代、故障等,甚至导致电子表格原始文件丢失的情况也不少见。[/color][b]建议:[/b][color=#000000]规范电子表格命名的具体方式,在电子表格名称上体现如批次号、用途等关键信息,通过名称上的关键信息关联到纸质文件;规范电子表格的存储方法和备份,降低电子表格分散存储及备份缺失带来的风险;在设计电子表格模板时,将电子表格的文件名、存储路径、电脑名、用户名、最后保存时间、打印时间等信息加入到页眉/页脚或者表格内其它的合适位置。打印出的纸质文件包含这些信息将更容易地追溯到原始文件。[/color][b]风险场景7:隐匿电子表格的使用行为[/b][color=#000000]在国内制药企业中,隐匿电子表格的使用是比较普遍的现象。在一些将电子表格用作简单数据库使用(如物料管理、质量事件记录等)的公司,由于担心访问控制和审计跟踪缺失受到监管机构的挑战,在迎接监管机构检查前用手抄记录代替电子文件,从而隐匿电子表格的使用。在飞行检查日益密集和严格的环境下,这种做法已不多见。另外一些情况仍然较为常见,比如在进行分析检测的结果计算时,实际是使用电子表格进行的,出于公司内部没有电子表格的控制程序或者没有进行验证等原因,QC及QA部门往往达成隐匿电子表格使用的默契,将电子表格中的计算过程抄录于实验记录上。[/color][color=#000000]隐匿电子表格的使用是在国内监管不严的特定时期存在的不合规现象,做到完全消除实际使用过电子表格的痕迹非常困难,比如不能确保每次打印完毕或者抄录完毕都将电子表格删除,也不太可能不保留实际使用的计算模板而每次新建。在新的监管环境下,隐匿电子表格的使用已经很不明智。[/color][b]建议:[/b][color=#000000]建立电子表格的管理控制规程,对电子表格进行验证。[/color][b]风险场景8:不对电子表格进行验证[/b][color=#000000]FDA涉及到电子表格的警告信中,有超过一半的涉及到使用未验证的电子表格。在国内制药企业中,有一部分尚未启动对电子表格进行验证。另外一些虽然已启动电子表格的验证,由于管理体系不健全的问题(比如电子表格清单不完全),导致电子表格有遗漏,或者使用者私自使用未经验证电子表格的情况。[/color][b]建议:[/b][color=#000000]为电子表格的设计、开发、审核、验证、审批、放行、使用制定完善的规范,制定并维护所有非一次性使用的电子表格清单,确保所有非一次性使用电子表格是经过验证的。[/color][b]风险场景9:缺乏培训和SOP[/b][color=#000000]电子表格使用非常方便,但并不表明所有的电子表格都很简单,一目了然。利用电子表格实现数据存储,自动化处理,数据交换与分析等从简单到复杂的应用不胜枚举。Excel并非计算机系统的编外物种;如何对待实验室、生产中应用的各种计算机系统,我们就应该如何对待这些电子表格模板。我们需要将设计完后的电子表格模板视作一个个独立的应用程序。因此,缺乏相应的SOP和培训一方面容易引起程序的错误使用,另一方面也不符合GxP规范。这里的SOP不是泛泛的所谓电子表格使用规范,就好比我们不会去出具一个模糊的实验室分析软件使用SOP,而应该为每一个特定电子表格制定使用规程。[/color][b]建议:[/b][color=#000000]为每一个特定的电子表格模板制定SOP,或者在模板中添加足够的使用注释和说明,并进行培训。[/color][b]风险场景10:缺少用户识别和审计追踪[/b][color=#000000]Excel电子表格仅可设置文件本身的密码,自身没有用户体系,不能电子化地将操作归属到个人。网上盛传的通过“共享工作薄”实现审计追踪功能有诸多缺陷。首先,从模板创建的工作薄默认是不共享的,用户需要单独为创建的工作薄设置共享和密码保护,从而增加了操作的难度。其二,共享工作薄一旦取消共享,所有的修订记录都会消失,而共享工作薄的保护密码是由使用者自行设定的,这就意味着使用者随时都可以删除其中的审计追踪记录,而操作失误也会导致审计信息的消失。其三,共享工作薄只能记录单元格的修改信息,对于其他的“表格创建,保存”等操作历史无法记录,因此一旦工作薄本身被删除,整个工作薄的历史记录就被全部清除。这个工作薄是否曾经有过都不得而知。[/color][color=#000000]作为数据库使用的Excel电子表格,具备审计跟踪是必需的要求。FDA 2015年的一封警告信中就强调了“The use ofExcel requires many management controls to prevent data alteration,and Excel does not have an audit trail to identify datachanges.”[/color][b]建议:[/b][color=#000000]出于自身管理的需要(比如良好的文件追溯),最好为电子表格文件提供文件层面上的审计跟踪(比如新文件由哪一个已有文件另存而来,原文件状态,新文件的另存者,新旧文件的内容差异对比等)。对于作为数据库使用的电子表格,需要按照法规要求提供完整的单元格级别的审计跟踪(何人何时作何修改)。在这方面,国外已经有成熟的商业化软件实现Excel电子表格的审计追踪和用户权限管理的功能,例如CIMCON公司的eInfotree。[/color][b]风险场景11:缺少电子签名功能[/b][color=#000000]关于电子表格文件的保存,制药企业的普遍做法是这样的:在保存电子表格电子文件的同时,将电子表格打印为纸质文件进行签署并保存。由于Excel软件不具备电子签名功能,在将电子表格打印为纸质文件后,并不能确保保存的电子文件不被修改,比如打开已打印的旧批次电子表格文件,输入新批次的检验数据然后再次保存或打印,这将导致电子文件与纸质文件的不一致,或者找不到对应的电子文件。[/color][b]建议:[/b][color=#000000]建立严密的电子文件保存体系;使用电子文档管理系统;使用加载宏或者第三方插件,实现对已被打印的电子表格文件的保护或者实现对电子表格文件的电子签名。[/color][b]结语[/b][color=#000000]本文介绍了电子表格在GxP环境中使用的主要风险及其应对措施。Excel电子表格使用的合规性一直是FDA检查的重点之一。FDA警告信中涉及到大量关于电子表格不合规使用的问题,占了有关计算机系统警告信总数的四分之一。同时,检查的回溯时间长,以FDA在2017年1月13日发给意大利一家制药企业的警告信为例,其中包含该公司在2014年期间使用“非官方”及不受控电子表格的问题。[/color][color=#000000]由于篇幅限制,可能并未涵盖到全部的风险点,所建议应对措施也仅提供一些解决的方向。各企业需要结合自身情况,建立完备的管理体系和成熟的技术手段,才能实现电子表格在GxP环境下的合规使用。[/color][color=#000000][b][color=#000000][/color][/b][/color][align=left][/align]
[align=left]作为史上最成功的几款软件之一,MS Excel电子表格(后文简称Excel)由于其易用性和灵活性,被广泛应用于全球各行各业,成为最流行的个人计算机数据处理软件。虽然制药行业不算是Excel的最重度使用者,但从研发到生产,流通,从日常办公到实验室的业务处理,每个环节都可以看到Excel使用的身影。[/align][color=#333333][/color][align=left][/align][align=left]但可惜的是,Excel毕竟是面向普罗大众的软件,并没有针对GxP合规要求专门设计,其本身具有一些固有的安全和审计跟踪缺陷。正是由于这些缺点,Excel在GxP领域内的应用一直是监管机构检查的重点。[/align][color=#333333][/color][align=left][/align][align=left]最近20年,随着行业内各种专业软件的推出以及现有软件的完善,例如LIMS(实验室信息管理系统),CDS(色谱数据系统),ELN(电子实验记录系统),MES(生产执行系统),数据的存储和处理方式有了更多的选择。由此,为了减轻在Excel电子表格应用合规性上的压力,许多制药企业尝试在关键业务领域中逐步“替换”电子表格。由于需要替换的数量不小,加上替代系统也有很多潜在的合规问题需要解决,使得“替换”过程并不顺利。再者,专业软件只能处理其管理范围内的数据,在替换上有一定的局限性,即便是经历了几十年信息化建设的欧美大型药企,想要彻底杜绝Excel的使用也几无可能。Excel仍旧以其易用性和灵活性在药物研究与开发、生产、流通等各个环节扮演着独特的角色。那些早期在Excel应用上做出了诸多努力的企业,功夫并没有白费,通过Excel模板的设计和使用,能够帮助企业梳理自身的工作流程,清理各种基础数据,明确信息化的需求,从而为桌面工具向大型信息系统过渡打下了良好的基础,同时在一些重要环节成为这些信息系统的有益补充,一个将电子表格深入应用的企业在实施大型信息系统的成功率上绝对要远远超出那些连电子表格都用不好的企业。[/align][color=#333333][/color][align=left][/align][align=left]虽然Excel的群众基础特别好,但群众使用Excel的基础却并不是很好(同样适用于word)。对于国内广大药企尤其是中小药企,能够把Excel以及Office中的其他软件用好,在管理水平和效率提升上就可以上一个大的台阶。不顾自身情况一味追求高大上的系统,盲目跟风,做不切实际的预期,其结果一定是费力不讨好,花钱不见疗效。[/align][color=#333333][/color][align=left][/align][align=left]电子表格工具作为大型系统的简单替代方案,投入少,见效快,更新起来也容易,很适合应用于没有信息化基础的企业。然而,这种易用性、灵活性以及Excel在合规上的缺陷,导致在其开发、使用和管理过程中很容易产生问题。同时,Excel作为通用型软件,并未针对GxP合规要求进行专门设计,其本身具有一些固有的安全和审计跟踪缺陷。正是由于这些缺点,Excel在GxP领域内的应用一直是监管机构检查的重点。[/align][color=#333333][/color][align=left][/align][align=left]按照对病人安全、产品质量及数据完整性的影响,分为如下3类:1. 高影响的包括用于原料检测、成品检测的电子表格,用于毒理学研究的表格,临床研究统计分析表格等。2. 中等影响的包括标签打印和分发数据记录表格,实验趋势分析表等。3. 低影响的如生产计划表,培训出席统计表等。因此,在充分了解Excel潜在风险的基础上,对其采用最佳实践的优化设计、验证和控制以确保其合规使用,已成为监管机构认可的主流做法。[/align][color=#333333][/color][align=left][/align][align=left]同时,监管机构内部实验室仍然在大量使用电子表格。FDA所属上级机构HHS就制定了详细的Excel文档检查表,并自2012年初后公布在FDA官网上。这份检查文档的详细程度充分说明了HHS及FDA对Excel风险的充分认识和重视。[/align][color=#333333][/color][align=left][/align][align=left]电子表格风险的来源:[/align][color=#333333][/color][list=1][*]电子表格的设计缺陷以及使用过程中的不受控带来的直接风险;[*]电子表格本身在合规功能上的缺陷带来的风险 [*]企业对电子表格的本质认识不够以及管理上的缺失带来的间接风险 [*]电子表格风险场景分析及其控制措施:[/list][color=#333333][/color][align=left][/align][align=left][color=#000000][b]风险场景1:模板使用不受控[/b][/color][/align][color=#333333][/color][align=left]由于电子表格的普及性,其应用和开发不仅有专业的IT人员,更有大量的业务部门人员参与。极端的混乱情况是每个人都设计自己的计算表格,从而导致计算方式、格式、数值修约等的差异性极大。这种放任自流无任何管理的应用方式在需要合规的GLP,GMP,GCP领域绝对是要禁止的。其后果也是非常糟糕的。[/align][color=#333333][/color][align=left][/align][align=left]做得规范一些的公司会指定人员进行电子表格的设计和审核,并将设计好的模板统一进行管理和分发。问题往往会出在分发的环节中。电子表格的使用一般会涉及到业务部门的多个人员。我们常常看到主管将电子表格通过邮件、拷贝,或者共享文件夹的方式分发给所属人员。一方面使用人员是否真正使用了这些模板不得而知。另一方面,由于业务流程的变化,或者模板的优化升级,加上文件命名没有版本控制,模板使用人员并不能识别哪个版本是最终版本或者现行版本。采用这种主动分发的方式去很难保证被动接受的终端人员使用的是最新版本,从而导致模板的误用。有些公司虽然意识了这些风险,但采取的措施过于落后,例如将Excel模板的使用限定于某台计算机,由专人在专机上维护电子表格。使用人员只能在该台电脑上使用。这种方法虽然降低了风险,但也大大降低了便利性。[/align][color=#333333][/color][align=left][b][/b][/align][align=left][b]建议:[/b]统计公司内部的所有Excel模板,制定命名规则并给予唯一性编号,形成一份电子表格的台帐。同时将模板置于局域网内的共享文件夹中,并真正使用到Excel模板的特性(扩展名为xltx),并将终端计算机的Excel模板目录定位到该共享文件夹。[/align][color=#333333][/color][align=left][/align][align=left][b]风险场景2:“Save as”另存为的滥用[/b][/align][color=#333333][/color][align=left]大家喜欢用“Save as”(另存为)一部分原因是出于无奈。追根溯源,产生这一现象的原因是Excel模板的设计人员和维护人员对Excel软件掌握得不够深入,对扩展名为.xlsx和.xltx两类文件的作用没有弄清楚。前者是普通的电子表格文件,而后者则是Excel的模板文件。我们看到绝大部分的公司在Excel的使用中都是将设计好的模板直接保存为xlsx文件,而不是xltx文件。这就导致大家获得这些模板并填写完数据后要选择另存为独立的数据文件。手脚稍快,这些所谓的模板很可能被大家误填上了数据。后续就是不断的删数据,录入数据,另存为。由此引起的漏删数据,模板私自修改,文件之间的关系错乱,无法追溯等等问题就在所难免了。此前,WHO的检查专家就对国内一些药企滥用“另存为”功能提出了严厉的批评。[/align][color=#333333][/color][align=left][/align][align=left]有些公司为了提高模板最新版本的识别度,在现行的Excel模板的文件名末尾加上了诸如“Final”,”最终版”之类的标识,一旦这些措施遇上了“另存为”,也形同虚设,因为每个人都可以把任何表格保存为Final或者“最终版”。[/align][color=#333333][/color][align=left][b][/b][/align][align=left][b]建议:[/b]真正把Excel模板的功能使用上,当用户点击“新建”时,能浏览到所有的模板,并由Excel使用这些模板自动为用户创建用于填写数据的文件。这样,用户无需四处复制粘贴和保存那些所谓的模板,避免了错误的同时,提高了效率。在GxP环境中,控制“另存为”菜单的使用。通过加载宏可以实现对另存为的控制,但如果用户通过Excel文件的复制达到制作副本的目的,则控制“另存为”也无能为力,只能依赖更加严格的Excel合规软件实现管控。[/align][color=#333333][/color][align=left][/align][align=left][b]风险场景3:不受保护的Excel工作薄[/b][/align][color=#333333][/color][align=left]不对电子表格做任何保护是较常见的问题,也是电子表格最重要的风险点。虽然在国外这种低级的错误几乎已经绝迹,但在国内还是有很多人不知道电子表格需要保护,或者不知道如何去保护。如果不是这几年计算机系统验证与合规宣传得比较密集,可能还是有一部分人没有意识到电子表格也属于计算机系统,同样是需要进行访问控制的;同我们常见到的色谱数据系统,LIMS系统并没有本质的不同。[/align][color=#333333][/color][align=left][/align][align=left]设计过电子表格公式的人会明白如果这些公式不加保护,是何等的容易被人无意的修改,导致一连串的错误结果。对电子表格的保护包括工作表级的保护和工作薄的保护。前者是针对单个工作表中的元素进行保护设置,包括单元格的锁定与保护,行和列的编辑。后者是针对包含多个工作表的结构保护。如果你的电子表格包含多个工作表,那么除了每个工作表启用保护外,工作簿也需要启用结构保护。因为未启用工作薄结构保护的电子表格,用户可以删除里面任意一个工作表,而这些工作表之间很可能有数据的关联引用和计算。意外删除工作表同样会导致结果错误。[/align][color=#333333][/color][align=left][/align][align=left]除了工作表和工作薄的结构不受保护,Excel文件本身的安全性也常常容易被忽视,尤其是重要的模板文件,计算结果文件,从而引起Excel文件被删除或替换。[/align][color=#333333][/color][align=left][b][/b][/align][align=left][b]建议:[/b]对工作表内的公式,常量,标准数值,格式,工作薄结构进行保护,对Excel设置打开密码,从而做到一定程度上的访问控制。对公用模板的存放位置进行保护,防止无意的删除或有意的替换。[/align][color=#333333][/color][align=left][/align][align=left][b]风险场景4:设计缺陷导致的错误[/b][/align][color=#333333][/color][align=left]电子表格的设计开发从本质上来说也属于计算机软件开发的范畴,但多数制药企业并不会配备专门的电子表格设计开发人员。电子表格的设计和开发往往由电子表格的使用者承担,这些使用者一般具有一定的Excel使用经验,但多数人员并未经过软件工程及原理或者电子表格设计开发的系统学习,这就可能会导致设计上的各种问题。[/align][color=#333333][/color][align=left][/align][align=left]设计缺陷导致的错误可能有下边这些情况:1)没有设定数据输入格式的限制导致的计算错误,比如FDA于2014年发布的一篇警告信中就有关于电子表格未做输入格式限制导致统计结果错误的描述;2)电子表格公式错误、公式与方法文件描述不符、修约规则与方法文件描述不符、有效数值保留位数错误、多次修约等导致的计算结果错误;3)电子表格设计时未考虑出错情形的处理,比如将结果判断设置为数值超过指定范围时报告“Fail”,否则报告“Pass”,这种设计将会导致在数据无效或数据错误时也报告出“Pass”的错误结果;4)不同设计开发人员或者同一人员设计开发的不同电子表格未按统一的风格进行数据输入、结果计算、结果输出区域的划分和标识,未使用有明显意义的表头,或者未对重要单元格添加解释性说明的,导致使用过程中的数据输入错误,导致错误的计算结果;5)电子表格没有清晰的名称、基本描述、作者、目的与用途、限制条件等,导致使用者误用电子表格,比如一种产品的结果计算误用了另一品种的表格,导致错误的结论。[/align][color=#333333][/color][align=left][b][/b][/align][align=left][b]建议:[/b]参照HHS的检查表以及其它的良好设计规范,制定公司内部的良好设计SOP。对候选人员进行统一的培训和考核,通过培训和考核的人员才能进行电子表格的设计、开发和验证。[/align][color=#333333][/color][align=left][/align][align=left][b]风险场景5:软件版本差异或设置差异导致的错误[/b][/align][color=#333333][/color][align=left]我们都知道,高版本的Excel软件可以向下兼容,不能向上兼容。显然,用高版本软件开发的电子表格不能直接在低版本的软件中使用,企业中一般也不会出现将Excel软件从高版本降级到低版本的情况。[/align][color=#333333][/color][align=left][/align][align=left]那么,用低版本软件开发的电子表格是否可以直接用于高版本的软件呢?答案也是否定的。Excel软件版本的不同或者设置的不同,可能导致电子表格文件的重大错误。比如在不同的语言设置中,算术运算的表达不一定是相同的(例如在Excel 97中,同样一个操作,在设置为英语时表达为 “convert”,而在设置为德语时则表达为“Umwandel”)。当在不同语言之间进行切换时,这两种表达并不会自动进行转换,这将导致计算错误。另外一个例子是,在Excel 97中,语言设置为英语时的小数点为“.”,而设置为德语时的小数点为“,”,切换语言设置时同样不能自动进行转换。Excel版本不同,其中的计算、控件或者加载项等也可能有细微差别。[/align][color=#333333][/color][align=left][/align][align=left]如果电子表格中涉及到宏命令的使用,则必须在选项中设置“启用宏”。这样就需要在每台使用电子表格的终端电脑上进行设置,否则在设置为“禁用宏”的电脑上使用带宏命令的电子表格将会导致错误。[/align][color=#333333][/color][align=left][/align][align=left]随着Excel软件多年来的升级,版本差异或设置差异导致的计算错误被逐步的改进,但微软从来没有申明这些问题已经不复存在,在GxP领域中使用Excel电子表格仍然不能忽视这一问题。[/align][color=#333333][/color][align=left][b][/b][/align][align=left][b]建议:[/b]在发布电子表格模板时,对其经过验证的使用环境进行记录(配置管理),这些环境包括操作系统版本、Excel软件版本、语言设置、安全设置、加载项设置等;尽可能在公司范围内统一软件版本;在改变使用环境时,需要对其影响进行评估,并依据评估结果进行必要的再验证或确认。[/align][color=#333333][/color][align=left][b][/b][/align][align=left][b][color=#000000]风[/color]险场景6:打印的纸质表格无法溯源[/b][/align][color=#333333][/color][align=left]电子表格软件本身不具有电子签名功能。在保存电子表格的同时,将电子表格打印为纸质文件签署并保存是普遍的做法。然而,多数公司的SOP并没有细致到规定电子表格文件命名和存储的具体方式,也没有规定纸质文件的命名如何体现对应电子文件的名称和存储位置。随着时间的推移,找到纸质文件对应的电子文件会越来越难。在一些没有对电子文件进行有效备份的公司,在经历了较长的时间后,由于原始电脑的升级换代、故障等,甚至导致电子表格原始文件丢失的情况也不少见。[/align][color=#333333][/color][align=left][b][/b][/align][align=left][b]建议:[/b]规范电子表格命名的具体方式,在电子表格名称上体现如批次号、用途等关键信息,通过名称上的关键信息关联到纸质文件;规范电子表格的存储方法和备份,降低电子表格分散存储及备份缺失带来的风险;在设计电子表格模板时,将电子表格的文件名、存储路径、电脑名、用户名、最后保存时间、打印时间等信息加入到页眉/页脚或者表格内其它的合适位置。打印出的纸质文件包含这些信息将更容易地追溯到原始文件。[/align][color=#333333][/color][align=left][/align][align=left][b]风险场景7:隐匿电子表格的使用行为[/b][/align][color=#333333][/color][align=left]在国内制药企业中,隐匿电子表格的使用是比较普遍的现象。在一些将电子表格用作简单数据库使用(如物料管理、质量事件记录等)的公司,由于担心访问控制和审计跟踪缺失受到监管机构的挑战,在迎接监管机构检查前用手抄记录代替电子文件,从而隐匿电子表格的使用。在飞行检查日益密集和严格的环境下,这种做法已不多见。另外一些情况仍然较为常见,比如在进行分析检测的结果计算时,实际是使用电子表格进行的,出于公司内部没有电子表格的控制程序或者没有进行验证等原因,QC及QA部门往往达成隐匿电子表格使用的默契,将电子表格中的计算过程抄录于实验记录上。[/align][color=#333333][/color][align=left][/align][align=left]隐匿电子表格的使用是在国内监管不严的特定时期存在的不合规现象,做到完全消除实际使用过电子表格的痕迹非常困难,比如不能确保每次打印完毕或者抄录完毕都将电子表格删除,也不太可能不保留实际使用的计算模板而每次新建。在新的监管环境下,隐匿电子表格的使用已经很不明智。[/align][color=#333333][/color][align=left][b][/b][/align][align=left][b]建议:[/b]建立电子表格的管理控制规程,对电子表格进行验证。[/align][color=#333333][/color][align=left][b][/b][/align][align=left][b]风险场景8:不对电子表格进行验证[/b][/align][color=#333333][/color][align=left]FDA涉及到电子表格的警告信中,有超过一半的涉及到使用未验证的电子表格。在国内制药企业中,有一部分尚未启动对电子表格进行验证。另外一些虽然已启动电子表格的验证,由于管理体系不健全的问题(比如电子表格清单不完全),导致电子表格有遗漏,或者使用者私自使用未经验证电子表格的情况。[/align][color=#333333][/color][align=left][b][/b][/align][align=left][b]建议:[/b]为电子表格的设计、开发、审核、验证、审批、放行、使用制定完善的规范,制定并维护所有非一次性使用的电子表格清单,确保所有非一次性使用电子表格是经过验证的。[/align][color=#333333][/color][align=left][/align][align=left][b]风险场景9:缺乏培训和SOP[/b][/align][color=#333333][/color][align=left]电子表格使用非常方便,但并不表明所有的电子表格都很简单,一目了然。利用电子表格实现数据存储,自动化处理,数据交换与分析等从简单到复杂的应用不胜枚举。Excel并非计算机系统的编外物种;如何对待实验室、生产中应用的各种计算机系统,我们就应该如何对待这些电子表格模板。我们需要将设计完后的电子表格模板视作一个个独立的应用程序。因此,缺乏相应的SOP和培训一方面容易引起程序的错误使用,另一方面也不符合GxP规范。这里的SOP不是泛泛的所谓电子表格使用规范,就好比我们不会去出具一个模糊的实验室分析软件使用SOP,而应该为每一个特定电子表格制定使用规程。[/align][color=#333333][/color][align=left][b][/b][/align][align=left][b]建议:[/b]为每一个特定的电子表格模板制定SOP,或者在模板中添加足够的使用注释和说明,并进行培训。[/align][color=#333333][/color][align=left][b][/b][/align][align=left][b]风险场景10:缺少用户识别和审计追踪[/b][/align][color=#333333][/color][align=left]Excel电子表格仅可设置文件本身的密码,自身没有用户体系,不能电子化地将操作归属到个人。网上盛传的通过“共享工作薄”实现审计追踪功能有诸多缺陷。首先,从模板创建的工作薄默认是不共享的,用户需要单独为创建的工作薄设置共享和密码保护,从而增加了操作的难度。其二,共享工作薄一旦取消共享,所有的修订记录都会消失,而共享工作薄的保护密码是由使用者自行设定的,这就意味着使用者随时都可以删除其中的审计追踪记录,而操作失误也会导致审计信息的消失。其三,共享工作薄只能记录单元格的修改信息,对于其他的“表格创建,保存”等操作历史无法记录,因此一旦工作薄本身被删除,整个工作薄的历史记录就被全部清除。这个工作薄是否曾经有过都不得而知。[/align][color=#333333][/color][align=left][/align][align=left]作为数据库使用的Excel电子表格,具备审计跟踪是必需的要求。FDA 2015年的一封警告信中就强调了“The use of Excel requires many management controls to prevent data alteration, and Excel does not have an audit trail to identify data changes.”[/align][color=#333333][/color][align=left][b][/b][/align][align=left][b]建议:[/b]出于自身管理的需要(比如良好的文件追溯),最好为电子表格文件提供文件层面上的审计跟踪(比如新文件由哪一个已有文件另存而来,原文件状态,新文件的另存者,新旧文件的内容差异对比等)。对于作为数据库使用的电子表格,需要按照法规要求提供完整的单元格级别的审计跟踪(何人何时作何修改)。在这方面,国外已经有成熟的商业化软件实现Excel电子表格的审计追踪和用户权限管理的功能,例如CIMCON公司的eInfotree。[/align][color=#333333][/color][align=left][b][/b][/align][align=left][b]风险场景11[color=#000000]:缺少电子签名功[/color]能[/b][/align][color=#333333][/color][align=left]关于电子表格文件的保存,制药企业的普遍做法是这样的:在保存电子表格电子文件的同时,将电子表格打印为纸质文件进行签署并保存。由于Excel软件不具备电子签名功能,在将电子表格打印为纸质文件后,并不能确保保存的电子文件不被修改,比如打开已打印的旧批次电子表格文件,输入新批次的检验数据然后再次保存或打印,这将导致电子文件与纸质文件的不一致,或者找不到对应的电子文件。[/align][color=#333333][/color][align=left][b][/b][/align][align=left][b]建议:[/b]建立严密的电子文件保存体系;使用电子文档管理系统;使用加载宏或者第三方插件,实现对已被打印的电子表格文件的保护或者实现对电子表格文件的电子签名。[/align][color=#333333][/color][align=left][b][/b][/align][align=left][b]结语[/b][/align][color=#333333][/color][align=left]本文介绍了电子表格在GxP环境中使用的主要风险及其应对措施。Excel电子表格使用的合规性一直是FDA检查的重点之一。FDA警告信中涉及到大量关于电子表格不合规使用的问题,占了有关计算机系统警告信总数的四分之一。同时,检查的回溯时间长,以FDA在2017年1月13日发给意大利一家制药企业的警告信为例,其中包含该公司在2014年期间使用“非官方”及不受控电子表格的问题。[/align][color=#333333][/color][align=left]由于篇幅限制,可能并未涵盖到全部的风险点,所建议应对措施也仅提供一些解决的方向。各企业需要结合自身情况,建立完备的管理体系和成熟的技术手段,才能实现电子表格在GxP环境下的合规使用[/align][color=#464646][/color][align=left][color=#464646][color=#000000][/color][/color][/align]

[align=left]1[b]概述[/b][/align][align=left]Excel电子表格的易用性、灵活性以及Excel软件本身在合规上的缺陷,导致在其开发、使用和管理过程中都存在大量的潜在问题。比如模板文件不受控、使用的版本错误、电子表格文件分散存放不易管理、不受保护、不易溯源等等。[/align][align=left] [/align][align=left][/align][align=left]Excel的合规使用是一个系统工程,涉及Excel模板的设计、开发、部署,验证、使用及管理的整个过程。针对企业自身Excel电子表格的使用情况,建立完备的管理体系和成熟的技术手段,才能实现电子表格在GxP环境下的合规使用。[/align][align=left] [/align][align=left][/align][align=left]电子表格合规概念模型如下图所示:[/align][align=center][img=,504,311]https://ng1.17img.cn/bbsfiles/images/2018/11/201811071016450350_5750_3419387_3.jpg!w504x311.jpg[/img][/align][align=left][/align][align=left]将以上概念模型进一步以思维导图呈现:[/align][align=center][img=,690,352]https://ng1.17img.cn/bbsfiles/images/2018/11/201811071016584850_4889_3419387_3.jpg!w690x352.jpg[/img][/align][align=center][/align][align=center] [/align][align=left][b]2电子表格的合规控制与无纸化应用[/b][/align][align=left][/align][align=left]2.1电子表格文件及内容受控的技术措施[/align][align=left] 2.1.1 电子表格模板使用的可控[/align][align=left]1)建立Excel电子表格模板的集中管理和使用模式[/align][align=left]将电子表格的公共使用模板(Template文件夹)放置在共享存储中,并将所有终端的Excel的默认模板位置映射该存储路径,且只有管理员权限才能对Template文件夹中的文件进行编辑,普通用户只能读取。用户使用特定电子表格时,可以从特定Template文件快速创建出一个功能完全一样的电子表格,这是一种确保所有终端用户始终使用最新版正式电子表格的有效方式。[/align][align=center][img=,690,417]https://ng1.17img.cn/bbsfiles/images/2018/11/201811071017374710_3494_3419387_3.jpg!w690x417.jpg[/img][/align][align=center]Template部署方式示意图[/align][align=left] [/align][align=left][/align][align=left]2)建立Template文件唯一性技术控制措施[/align][align=left]建立技术措施,确保Template文件夹中的Template文件不能被随意复制和私自存储,确保由Template文件创建的子文件不能被再次另存或者被作为模板文件使用。[/align][align=left] [/align][align=left][/align][align=left]3)建立技术控制措施,确保电子表格计算模板仅能直接来源于正式Template文件[/align][align=left]确保所有同一用途的电子表格直接来源于Template文件夹中的正式Template文件,从技术上确保所有使用人员使用的Template文件是唯一的正式文件。[/align][align=left] [/align][align=left][/align][align=left]4)建立技术措施,确保由Template文件创建的电子表格受保护[/align][align=left]建立技术措施或文件审批控制流程,根据不同类型电子表格的具体情况,在不同的节点或触发条件下,自动对电子表格内容或文件本身进行保护,避免数据的丢失、覆盖或修改。[/align][align=left] [/align][align=left][/align][align=left] 2.1.2 电子表格的访问及权限控制[/align][align=left]1)文件层面的访问及权限控制,实现不同的用户对不同电子表格具有不同的权限,比如不可访问、只读、读写等。[/align][align=left] [/align][align=left][/align][align=left]2)工作簿层面的权限控制,实现不同的用户对不同电子表格具有不同的菜单权限,比如特定的用户才能打印、另存、解锁保护等等。[/align][align=left] [/align][align=left][/align][align=left]3)单元格层面的权限控制,不同用户对不同的单元格具有差异化的权限控制。[/align][align=left] [/align][align=left][/align][align=left]4)建立技术控制措施,限制电子表格文件的随意复制。[/align][align=left] [/align][align=left][/align][align=left] 2.1.3 电子表格的规范化存储[/align][align=left]为由不同Template文件生成的电子表格文件设置个性化的存储路径和文件名称规则,由同一个Template文件生成的所有电子表格文件只能按照设定的规则进行存放,实现电子表格的有序的规范的存储,易于管理。[/align][align=left] [/align][align=left][/align][align=left]比如,我们为“含量测定”Template文件(见图)设定三个存储规则:[/align][align=left] [/align][align=left]1)固定存放到根目录\\WIN-HS58US0NHMT\sharefolder\含量测定中;[/align][align=left] [/align][align=left][/align][align=left]2)自动按所检测产品名称生成子文件夹,同一检品的含量测定计算电子表格只能存储于与检品名称对应的子文件夹内;[/align][align=left] [/align][align=left][/align][align=left]3)含量测定电子表格的名称自动强制命名为所检产品对应的批次。那么所有由“含量测定”Template文件生成的电子表格都只能存储在指定根目录下,且自动强制存储在检品名称对应的文件夹内,自动强制以批号命名(见图)。[/align][align=center][img=,690,325]https://ng1.17img.cn/bbsfiles/images/2018/11/201811071017538290_6320_3419387_3.jpg!w690x325.jpg[/img][/align][align=center]“含量测定”Template文件[/align][align=center] [/align][align=center][/align][align=center][img=,690,312]https://ng1.17img.cn/bbsfiles/images/2018/11/201811071018059564_2019_3419387_3.jpg!w690x312.jpg[/img][/align][align=center]强制规范存储示意图[/align][align=left] [/align][align=left][/align][align=left][b]3电子表格文件模板开发与验证[/b][/align][align=left]电子表格文件层面的合规验证服务内容可以用下图概括:[/align][align=center][img=,644,327]https://ng1.17img.cn/bbsfiles/images/2018/11/201811071018204440_2946_3419387_3.jpg!w644x327.jpg[/img][/align][align=left] [/align][align=left][/align][align=left]3.1 模板的设计和开发[/align][align=left]验证过程只是证明电子表格模板的功能满足预期的使用效果、公司内部要求或法规要求,验证本身不能解决问题,而是用来发现问题。从质量源于设计(QbD)的角度出发,前期的设计和开发才真正决定电子表格模板是否满足要求。[/align][align=left] [/align][align=left][/align][align=left]具体的服务内容应包括:[/align][align=left] [/align][align=left]1)电子表格现状评估:逐个评估电子表格的复杂度及GxP影响等级,根据这两项评估结果确定电子表格风险等级,依据风险等级确定其需要进行的设计、开发及验证活动及对应的文档需求。汇总评估结果形成电子表格台账。[/align][align=left] [/align][align=left][/align][align=left]2)需求确认及用户需求说明制定:与使用人员确认电子表格的具体需求,并制定用户需求说明。[/align][align=left] [/align][align=left][/align][align=left]3)电子表格设计/开发:根据用户需求、良好设计开发规范、合规要求进行电子表格的设计、开发和测试(原型论证)。良好的设计体现在清晰的计算流程、输入值的合法验证、错误处理、明确数值精确度和修约规则、工作表和单元格区域的保护、统一的界面风格、文件追溯等。[/align][align=left] [/align][align=left][/align][align=left]4)功能规格说明制定:根据用户需求说明以及经原型论证的电子表格文件,制定功能规格说明。[/align][align=left] [/align][align=left][/align][align=left]5)为风险等级高的电子表格制定培训文档或SOP。[/align][align=left] [/align][align=left][/align][align=left]6)建立电子表格模板设计/开发规范:明确电子表格设计和开发需要遵循的标准,明确参与电子表格的设计、开发和验证的人员需要通过的培训和考核,帮助建立Excel电子表格良好设计、开发、验证的长效机制。[/align][align=left] [/align][align=left][/align][align=left]3.2 电子表格的验证[/align][align=left]1)制定电子表格验证计划。[/align][align=left] [/align][align=left][/align][align=left]2)制定电子表格的验证方案。[/align][align=left] [/align][align=left][/align][align=left]3)实施验证。[/align][align=left] [/align][align=left][/align][align=left]4)制定追踪矩阵。[/align][align=left] [/align][align=left][/align][align=left]5)制定验证报告。[/align][align=left] [/align][align=left][/align][align=left]3.3 电子表格验证交付文件[/align][align=center][img=,580,550]https://ng1.17img.cn/bbsfiles/images/2018/11/201811071018364795_7555_3419387_3.jpg!w580x550.jpg[/img][/align][align=left] [/align][align=left][/align][align=left]4[b]电子表格管理SOP[/b][/align][align=center][img=,580,155]https://ng1.17img.cn/bbsfiles/images/2018/11/201811071018556550_6119_3419387_3.jpg!w580x155.jpg[/img][/align]
我想把一个电子表改成计数器,该如何办到呢???????????
[align=left][b]设计目的[/b][/align][align=left]没有物料管理系统的制药企业,大多在使用Excel电子表格进行试剂管理。但大多数企业使用电子表格的水准并不高,很多仅仅用到了筛选、排序、统计这些简单功能。我们发现,一些效率低下容易出错的做法被普遍使用,比如:[/align][align=left][b]1)使用剪切、黏贴的方式对试剂进行入库、出库操作;[/b][/align][align=left][b]2)使用排序的方式进行数量统计;[/b][/align][align=left][b]3)没有设置任何库存量警示提醒;[/b][/align][align=left][b]4)试剂没有统一格式的便于识别的条码标签,使用手写标签或手动数据录入方式;[/b][/align][align=left][b]5)数据没有任何保护[/b][/align][align=left]小编为大家设计了一款可以避免上述问题的试剂管理电子表格。[/align][align=left][b][i]功能介绍[/i][/b][/align][align=left][b][color=#0070c0]01[/color][color=#0070c0]生成并打印二维码标签[/color][/b][/align][align=left]在“二维码标签”工作表中,输入(手动或黏贴)试剂编号或者需要打印到标签中的任何信息,按Ctrl+D,自动生成二维码标签。[/align][align=left][img=,630,853]https://ng1.17img.cn/bbsfiles/images/2018/09/201809061544515526_6484_3419387_3.jpg!w630x853.jpg[/img] [/align][align=left] [b][color=#0070c0]02[/color][color=#0070c0]数据录入自动锁定[/color][/b][/align][align=left]在“试剂入库”工作表中输入待入库试剂信息,切换至“在库清单”工作表。[/align][align=left]1)“试剂入库”工作表中的待入库试剂信息将自动录入至“在库清单”工作表中;[/align][align=left]2)如有信息不全的或者同一编号已有入库或出库记录的,将不被录入并给出提示信息;[/align][align=left]3)“在库清单”工作表中的试剂信息自动锁定,一旦录入将不能被修改或删除(除非输入管理密码解锁工作表)。[/align][align=left][img=,690,352]https://ng1.17img.cn/bbsfiles/images/2018/09/201809061546154406_5321_3419387_3.jpg!w690x352.jpg[/img] [/align][align=left] [b][color=#0070c0]03[/color][color=#0070c0]自动汇总库存量[/color][/b][/align][align=left]1) 新入库试剂种类在库存量清单中没有记录时,自动在库存量清单中新建一条记录;[/align][align=left]2) 新入库试剂种类在库存量清单中已有记录时,自动更新库存量清单中相应记录的数量;[/align][align=left]3) 试剂出库时,自动在库存量清单中扣除出库数量;[/align][align=left]4) 可以为各种试剂设置警戒数量,当库存量低于警戒数量时自动以警示颜色标记;[/align][align=left]5) 库存量清单自动维护,自动锁定,不能被人为修改或删除。[/align][align=left][img=,690,351]https://ng1.17img.cn/bbsfiles/images/2018/09/201809061547042685_4381_3419387_3.gif!w690x351.jpg[/img] [/align][align=left] [b][color=#0070c0]04[/color][color=#0070c0]扫描条码出库[/color][/b][/align][align=left]在“在库清单”工作表中,将待出库试剂的二维码信息扫描进“扫码出库”列中,在“领用人”列的对应行输入领用人.点击“试剂分发”按钮,进行确认后,出库的试剂将自动从“在库清单”工作表转移至“出库单”工作表。“出库单”工作表自动锁定,不能被人为修改或删除。[/align][align=left][img=,690,349]https://ng1.17img.cn/bbsfiles/images/2018/09/201809061548108066_6087_3419387_3.jpg!w690x349.jpg[/img] [/align][align=left] [b][i]拓展功能[/i][/b][/align][align=left] 大多数制药企业都在使用Excel电子表格管理试剂,只不过一般都是藏着使用:表面上使用纸质的台账,日常的管理实际上使用电子表格。[/align][align=left]很显然,这种使用方式的根源有两个:[/align][align=left]1)[b]电子表格的管理效率比纸质台账高出很多[/b],所以人们偷偷摸摸的也要用;[/align][align=left]2)使用的电子表格未经良好设计或者没有恰当的控制措施,[b]不能满足法规的电子记录要求[/b],比如数据可被随意修改等等。[/align][align=left]小编设计的这个表格,仅仅展示了一些基本功能。还可以开发更丰富的功能,既可提高使用效率,比如将警示库存提醒改为弹出对话框提示或者声音提示,还可以提高合规性,比如实现分级访问控制和权限控制,比如实现审计跟踪或电子签名。感兴趣的读者可联系小编。[/align][align=left][/align][align=left][color=#444444]文章转自微信公众号:[/color][b]实验室信息化与自动化[/b][/align]
帕纳科xrf的分析数据有没有办法导出形成EXCEL电子表格,有大神支支招,感谢感谢!
[align=left][color=#333333]电子表格在制药企业中使用的合规性一直是FDA检查的重点之一, FDA警告信中涉及到大量关于电子表格不合规使用的问题。从趋势上看,自2014年开始,警告信涉及电子表格不合规问题的频次有所降低,说明在欧美等成熟市场中,药企通过多年的努力,在数据完整性上做的越来越好。但另外一方面,以2017年1月13日发给意大利一家制药企业的警告信为例,即使在2014年期间使用”非官方”及不受控电子表格的问题都被挖了出来,其回溯的时间较之前的警告信更长,说明FDA对电子表格的关注非但并未降低反而有所提高。[/color][/align][align=left][color=#333333]CFDA[/color][color=#333333]于2015年5月26日正式发布了GMP法规的新附录之一《计算机化系统》,首次明确提出对计算机化系统的合规要求。2016年9月30日,由CFDA食品药品审核查验中心组织起草的《药品数据管理规范(征求意见稿)》挂网公开征求意见。从上述两份文件不难看出,CFDA对于数据完整性及计算机化系统的合规要求正在全面与FDA接轨。电子表格作为计算机化系统的重要部分及数据完整性的重要载体,毫无疑问今后也将成为CFDA的监管重点。[/color][/align][align=left][color=#333333]对于广大国内药企,无论是向外扩张的需求或是适应国内监管的要求,电子表格的合规性使用都已成为必须要认真面对的问题。[/color][/align][align=left][color=#333333]本文整理了警告信中一些代表性内容,主要有以下几个方面:1)使用到”非正式”或不受控的电子表格;2)没有审计追踪 3)未经验证; 4)数据错误。[/color][/align][color=#333333]具体内容详见下表[/color]:[align=left] [table][tr][td] [b][/b][color=#005000][/color][b][/b][color=#b08000][/color][align=left][b][color=#000000]时间[/color][/b][/align][b][/b][color=#005000][/color][b][/b][color=#b08000][/color] [/td][td][color=#006000] [/color][b][color=#000000]公司or机构[/color][/b][/td][td][color=#006000][/color] [b] 原文[/b] [/td][td] [b]中文摘要 [/b][/td][/tr][tr][td] [align=left][b][color=#333333]2017[/color][color=#333333]年1月13日[/color][/b][/align] [/td][td] [align=left][color=#333333]FACTA Farmaceutici[/color][/align] [/td][td] [align=left][color=#333333]You stored original data in an [/color][color=#333333]“unofficial” and uncontrolled electronic spreadsheet on a shared computer network drive. In response to this letter: Comprehensively evaluate test samples performed by other analysts from January to September,2014, when the unofficial spreadsheet was in use.[/color][/align] [align=left][color=#333333]Evaluate the extent of uncontrolled spreadsheets at your facility.[/color][/align] [/td][td] [align=left][color=#333333]检查发现该公司存在使用共享网络盘中的”非正式”及不受控的电子表格存储原始数据的情况。 FDA要求: 1)综合评估使用过非官方电子表格期间内测试的样品;[/color][/align] [align=left][color=#333333]2[/color][color=#333333])评估不受控电子表格的使用及影响程度。[/color][/align] [/td][/tr][tr][td] [align=left][b][color=#333333]2016[/color][color=#333333]年8月25日[/color][/b][/align] [/td][td] [align=left][color=#333333]Pan Drugs Limited[/color][/align] [/td][td] [align=left][color=#333333]For example, the computer in your quality unit area did not have controls to restrict access and prevent unauthorized changes to data files and folders. All employees had access to your Annual Product Review (APR) spreadsheet. The desktop computer containing the APR was not locked. [/color][/align] [/td][td] [align=left][color=#333333]质量部门中的计算机没有进行控制以限制访问并防止未经授权的更改数据文件和文件夹。例如所有员工都能访问该公司的年度产品回顾(APR)电子表格。[/color][/align] [/td][/tr][tr][td] [align=left][b][color=#333333]2016[/color][color=#333333]年8月3日[/color][/b][/align] [/td][td] [align=left][color=#333333]Ropack, Inc.[/color][/align] [/td][td] [align=left][color=#333333]Failure to validate computer software for its intended use according to an established protocol when computers or automated data processing systems are used as part of production or the quality system, as required by 21 CFR 820.70(i). For example, your firm was utilizing an uncontrolled spreadsheet to track equipment requalification due dates.[/color][/align] [/td][td] [align=left][color=#333333]计算机软件作为产品质量体系的一部分,未按照21 CFR 820.70(i)的要求依据既定方案进行验证。例如该公司使用了一个未受控的电子表格跟踪设备的再确认日期。[/color][/align] [/td][/tr][tr][td] [align=left][b][color=#333333]2015[/color][color=#333333]年12月18日[/color][/b][/align] [/td][td] [align=left][color=#333333]Virbac Corporation[/color][/align] [/td][td] [align=left][color=#333333]Your Complaint SOP states that QA shall maintain the customer complaint report files. Your firm[/color][color=#333333]’s QA unit maintains a separate Excel spreadsheet for those complaints that come directly into the Bridgeton QA unit. You have no centralized system for tracking all your complaints. The use of Excel requires many management controls to prevent data alteration, and Excel does not have an audit trail to identify data changes.[/color][/align] [/td][td] [align=left][color=#333333]该公司 QA部门使用一个单独的Excel表格而非集中式的系统来维护那些直接发到Bridgeton QA部门的投诉。FDA认为使用Excel需要很多管理控制措施来防止数据修改,并且Excel自身没有审计追踪功能来识别数据变更。[/color][/align] [/td][/tr][tr][td] [align=left][b][color=#333333]2015[/color][color=#333333]年10月22日[/color][/b][/align] [/td][td] [align=left][color=#333333]Sandoz International GmbH[/color][/align] [/td][td] [align=left][color=#333333]Two uncontrolled Excel spreadsheets were used to record discrepancies and certain in-process drug quality data.[/color][/align] [/td][td] [align=left][color=#333333]使用两个不受控的Excel电子表格记录偏差和某些药品中控质量数据。[/color][/align] [/td][/tr][tr][td] [align=left][b][color=#333333]2014[/color][color=#333333]年7月21日[/color][/b][/align] [/td][td] [align=left][color=#333333]Med-Mizer, Inc.[/color][/align] [/td][td] [align=left][color=#333333]Also, your firm tracks complaint data on a spreadsheet that contains free form text fields that are not standardized, resulting in an inability to adequately trend the data. For example, when using complaint data from January 1, 2011 to February 19, 2014 to trend for [/color][color=#333333]“Description of Failure” for “6090,” fourteen complaints are shown. However, the spreadsheet contains several different descriptions of the same part failure that when totaled resulted in a total count of forty complaints related to the inline coupler, part #6090.”[/color][/align] [/td][td] [align=left][color=#333333]该公司跟踪投诉数据的电子表格,其中包含自由形式的文本字段,这不规范,导致了数据分析中出现问题。例如,一个管理投诉数据的电子表格,因对同一问题”描述失败”包含几种不同的描述,导致使用表格内部公式计算”描述为失败”问题总数时,将原本的14统计为了40。[/color][/align] [/td][/tr][tr][td] [align=left][b][color=#333333]2013[/color][color=#333333]年9月27日[/color][/b][/align] [/td][td] [align=left][color=#333333]Aarti Drug Limited[/color][/align] [/td][td] [align=left][color=#333333]Additionally, at the Aarti Drug Limited facility (FEI 3009688205), the investigator noticed that the use of the Excel spreadsheets in analytical calculations are neither controlled nor protected from modifications or deletion. The investigator noticed that the calculation for residual solvent for XXX uses an Excel spreadsheet that has not been qualified. We are concerned about the data generated by your QC laboratory from non-qualified and uncontrolled Excel spreadsheets.[/color][/align] [/td][td] [align=left][color=#333333]该公司未对用于分析计算的Excel电子表格进行控制和保护,电子表格可被修改和删除。表格未经验证(例如XXX品种的溶剂残留计算表格non-qualified)。FDA对该公司QC实验室使用未经验证及不受控制的电子表格产生的数据表示担心。[/color][/align] [/td][/tr][tr][td] [align=left][b][color=#333333]2012[/color][color=#333333]年6月13日[/color][/b][/align] [/td][td] [align=left][color=#333333]Compañ ía Internacional de Comercio[/color][/align] [/td][td] [align=left][color=#333333]Specific violations observed during the inspection include, but are not limited, to the following: Your firm has not established appropriate controls designed to assure that laboratory records include all data secured in the course of each test, including graphs, charts, and spectra from laboratory instrumentation, properly identified to show the specific component, drug product container, closure, in-process material, or drug product, and lot tested . Specifically, the inspection revealed that your firm has not established written procedures to control and account for electronically generated worksheets used by analysts to record analytical test results. Analysts in your QC laboratory print an uncontrolled number of worksheets from computers throughout the QC laboratory without supervision.[/color][/align] [/td][td] [align=left][color=#333333]检查中发现该企业没有建立适当的控制措施以保证实验室记录被合适地标识或归属至所属对象,这不符合21 CFR 211.194(a)(4)的要求。 具体地,该公司没有制定书面程序来控制和说明分析人员用以记录测试结果的电子表格。分析人员在QC实验室的电脑上未受监督地打印了数量不受控制的电子表格。[/color][/align] [/td][/tr][tr][td] [align=left][b][color=#333333]2011[/color][color=#333333]年5月16日[/color][/b][/align] [/td][td] [align=left][color=#333333]Aubrey Inc.[/color][/align] [/td][td] [align=left][color=#333333]Failure to validate software used as part of production or the quality system for its intended use according to an established protocol, as required by 21 CFR 820.70(I). For example, your firm did not validate use of an Excel spreadsheet used to calculate the Moisture Vapor Transmission Rate (MVTR) per test procedure XXX Revision B.[/color][/align] [/td][td] [align=left][color=#333333]计算机软件(例如用于计算MVTR的Excel电子表格),作为产品质量体系的一部分,未按照21 CFR 820.70(i)的要求依据既定方案进行验证。[/color][/align] [/td][/tr][tr][td] [align=left][b][color=#333333]2010[/color][color=#333333]年10月12日[/color][/b][/align] [/td][td] [align=left][color=#333333]Advanced Testing Laboratory, Inc.[/color][/align] [/td][td] [align=left][color=#333333]We observed 8 of 9 worksheets where one or more tabs with formula cells were not locked. These worksheets were used for analyzing raw data from drug component and product samples, including XXX. Your firm[/color][color=#333333]’s SOP 100-G-0110, “Creation and Use of Templates,” stated that cells, in which data is entered, must be locked within their electronic template. In your response, your firm states that you will enforce the existing procedure by reviewing the current inventory of electronic data files and disposing of non-compliant spreadsheets. In addition, you will retrain analysts on the current procedure. Your response, however, is inadequate because you do not assess whether the raw data results, generated using unlocked templates, are valid.[/color][/align] [/td][td] [align=left][color=#333333]该公司用于分析原料药及制剂样品原始数据的大多数(9个中的8个)电子表格中,均存在一个或多个带公式单元格未被锁定的情况,而这与法规要求及该公司的SOP均不符。 在该公司对483的答复中,承诺将加强对现有程序的执行、梳理现有表格并处理不合规表格、同时将对分析人员进行重新培训。但FDA认为其答复是不够的,因为没有对使用未锁定表格处理的原始数据结果进行有效性评估。[/color][/align] [/td][/tr][tr][td] [align=left][b][color=#333333]2010[/color][color=#333333]年6月10日[/color][/b][/align] [/td][td] [align=left][color=#333333]Medefil, Incorporated[/color][/align] [/td][td] [align=left][color=#333333]Your firm has no procedures for controlling laboratory worksheets including changes to worksheets, issuance of laboratory worksheets, and reconciliation of laboratory worksheets. The worksheet [/color][color=#333333]“Internal Communication - Batch Release Information” by the warehouse, which is used to identify released product, was created after XXX documented release of finished product for Heparin I.V. Flush Syringes and Normal Saline I.V. Flush Syringes prior to obtaining media fill results. This sheet is used to communicate batch release information to warehouse operations. Use of this sheet is not documented in any Medefil procedure nor is control over this sheet documented.[/color][/align] [/td][td] [align=left][color=#333333]该公司没有实验室电子表格的控制(发行、变更、一致性控制等)程序。 例如仓库用于识别放行产品的某工作表,它的使用既没有在任何的程序中记录,也没有在工作表本身的记录文件中收到控制。[/color][/align] [/td][/tr][tr][td] [align=left][b][color=#333333]2010[/color][color=#333333]年4月20日[/color][/b][/align] [/td][td] [align=left][color=#333333]Capricorn Pharma, Inc.[/color][/align] [/td][td] [align=left][color=#333333]Your firm has failed to exercise appropriate controls over computer or related systems to assure that changes in master production and control records, or other records, are instituted only by authorized personnel [21 C.F.R [/color][color=#333333]§ 211.68(b)]. Your firm’s laboratory analysts have the ability to access and modify the formulas in the Excel spreadsheets used to calculate assay results for Guaifenesin and XXX drug products. Due to this unrestricted access, there is no assurance that the formulas in the Excel preadsheets are accurate and valid.[/color][/align] [/td][td] [align=left][color=#333333]该公司未能对计算机或相关系统实施适当的控制,以确保主生产和控制记录或其他记录的变更仅由授权人员实施。 例如该公司的实验室分析人员能访问和修改用于计算检测结果的Excel电子表格中的公式。由于这种不受限制的访问,Excel电子表格的准确性和有效性得不到保障。[/color][/align] [/td][/tr][tr][td] [align=left][b][color=#333333]2009[/color][color=#333333]年10月5日[/color][/b][/align] [/td][td] [align=left][color=#333333]Phoenix Bio-Tech Corporation[/color][/align] [/td][td] [align=left][color=#333333]Failure to validate computer software for its intended use according to an established protocol when computers or automated data processing systems are used as part of production or the quality system, as required by 21 CFR 820.70(i). We have reviewed your responses and have concluded that they are inadequate because a copy of your revised procedures and the Excel spreadsheet validation protocols/procedures and reports were not provided. It is unclear how you plan to document quality system records that were previously documented in the (b)(4) system.[/color][/align] [/td][td] [align=left][color=#333333]计算机软件(含Excel等自动数据处理系统),作为产品质量体系的一部分,未按照21 CFR 820.70(i)的要求依据既定方案进行验证。 因该公司未提供修订程序和Excel电子表格验证方案/程序和报告的相关资料。FDA评估认为其对483答复不够充分。[/color][/align] [/td][/tr][tr][td] [align=left][b][color=#333333]2009[/color][color=#333333]年4月27日[/color][/b][/align] [/td][td] [align=left][color=#333333]Hill Dermaceuticals, Inc.[/color][/align] [/td][td] [align=left][color=#333333]Your laboratory records did not include a record of all calculations performed in connection with laboratory tests as required by 21 CFR [/color][color=#333333]§ 211.194(a)(5). For example, laboratory notebook #7, page 49, documents the assay results, but not the calculations performed in Test number DSFS D-13 and Test number TG 521 for the analysis of XXX, lot #HI7908. The notebook does not document reference to the spreadsheet calculation used to generate the results. In addition, the assay results generated by the spreadsheet were not verified for accuracy. Your response dated February 16, 2009, states that you have established procedures to ensure that calculations of method validation studies are recorded. The Records Management SOP, Section 5.7.4.7, states that the procedures shall define what and how data is to be recorded in respective logbooks. However, this SOP omits instructions to include in the notebook the reference to the spreadsheet calculation used to generate the results, as well as the raw data and calculations. In addition, you continued to release products based on assay results generated by the spreadsheet that have not been verified for accuracy.[/color][/align] [/td][td] [align=left][color=#333333]记录本仅记录了检验结果,没有记录计算过程,而且没有引用执行计算生成结果的电子表格。此外,用电子表格计算产生的检验结果没有验证其准确性。 该公司在对483的答复中声明已建立程序用于确保方法验证研究的计算被记录,其记录管理SOP规定了什么样的数据应怎样被记录在各自的日志中。 但检察官认为该公司的回复忽略了483中的指示,其SOP未规定在记录本中引用用于计算的电子表格(含原始数据及计算)。此外,在未验证准确性的情况下,该公司继续使用电子表格计算检验结果用于产品放行。[/color][/align] [/td][/tr][tr][td] [align=left][b][color=#333333]2007[/color][color=#333333]年5月17日[/color][/b][/align] [/td][td] [align=left][color=#333333]Quantimetrix Corporation[/color][/align] [/td][td] [align=left][color=#333333]Software used as part of the production quality system was not validated for its intended use according to an established protocol . Specifically, Spreadsheets intended to check for outliers and calculate mean, SC, % CV, value assignments for finished devices. [/color][/align] [/td][td] [align=left][color=#333333]用于检查异常值,计算平均值、SC、%CV等的电子表格,作为产品质量体系的一部分,未按照21 CFR 820.70(i)的要求依据既定方案进行验证。[/color][/align] [/td][/tr][tr][td] [align=left][b][color=#333333]2007[/color][color=#333333]年5月9日[/color][/b][/align] [/td][td] [align=left][color=#333333]TOSOH AIA, Inc[/color][/align] [/td][td] [align=left][color=#333333]the method for tracking (i .e . Microsoft Excel) the number of samples placed in the incubator was unauthenticated.[/color][/align] [/td][td] [align=left][color=#333333]用于恒温箱中样品数量管理的方法(如微软Excel)未经验证。[/color][/align] [/td][/tr][tr][td] [align=left][b][color=#333333]2006[/color][color=#333333]年1月17日[/color][/b][/align] [/td][td] [align=left][color=#333333]National Genetics Institute[/color][/align] [/td][td] [align=left][color=#333333]There are no data to demonstrate that the quality control/quality assurance spreadsheets used for tracking and trending various quality metrics have been properly validated (installation qualification, operational qualification, and performance qualification) and are performing as intended.[/color][/align] [/td][td] [align=left][color=#333333]没有数据证明用于跟踪和监控各种质量指标的QC/QA电子表格已被正确地验证(IQ,OQ,PQ),不能证明电子表格的运行状况符合预期。[/color][/align] [/td][/tr][tr][td] [align=left][b][color=#333333]2003[/color][color=#333333]年12月23日[/color][/b][/align] [/td][td] [align=left][color=#333333]Eldon Biologicals A/S[/color][/align] [/td][td] [align=left][color=#333333]Failure to establish and maintain adequate procedures for implementing corrective and preventive action, as required by 21 CFR 820.100(a) and (b). For-example: b. Microsoft 2000 Excel spreadsheet software used manufacturing has not been validated for the purpose of generating a worksheet for formulation of reagents. No documentation was found to establish or verify corrections made to the program. Failure to validate computer software for its intended use according to an established protocol, as required by 21 CFR 820.70(i). For example the Microsoft 2000 Excel spreadsheet software program was not validated for formulation of reagents and was seen to give incorrect data[/color][/align] [/td][td] [align=left][color=#333333]1[/color][color=#333333])该公司未按照21 CFR 820.70(i)的要求根据既定的方案验证Excel电子表格软件(该表格用于生产中制定试剂配方表),并且发现有错误数据。 2)检查中未发现就上述问题建立或确认改正措施的文件。说明该公司未能按21 CFR 820.100(a)和(b)的要求建立和保持实施CAPA的适当的程序。[/color][/align] [/td][/tr][tr][td] [align=left][b][color=#333333]2001[/color][color=#333333]年7月10日[/color][/b][/align] [/td][td] [align=left][color=#333333]EP MedSystems[/color][/align] [/td][td] [align=left][color=#333333]Your firm failed to validate several computer databases that are used for quality functions including your Access database, your XXX software, and your MS Excel spreadsheet program as required by 21 CFR 820.70(i).[/color][/align] [/td][td] [align=left][color=#333333]该公司未按照21 CFR 820.70(i)的要求验证用于质量功能的几个计算机数据库、XXX软件及微软Excel电子表格程序。[/color][/align] [/td][/tr][/table][/align]
怎么把icp测量结果导出成电子表格,目前都是通过一个一个的输入,即慢同时也容易出错
[b]全国专业技术人员计算机应用能力考试用书——Excel 2003中文电子表格辽宁人民出版社,辽宁电子出版社2005年11月[/b]
[align=left][img=,690,331]https://ng1.17img.cn/bbsfiles/images/2019/06/201906242006271074_8109_3419387_3.jpg!w690x331.jpg[/img][/align][align=left]Excel表格在实验室的应用非常广泛,它的身影不仅出现在GMP实验室,几乎所有类型的实验室都是Excel表格的重度使用者,其中包含有资质的第三方检测实验室,如通过CNAS认证或有计划通过CNAS认证的实验室,他们对Excel表格的使用包括但不限于:实验数据的计算,各种台账的管理,实验记录管理等等方面。那么,对于通过CNAS认证或者有意向申请CNAS认证的实验室,对于Excel的合规使用有明确的要求吗?![/align][align=left] [/align][align=left]我们知道,GMP实验室电子数据管理,各国监管机构都有明确的法规要求。同样的,对于有CNAS认证或者有意向申请CNAS认证的实验室,其电子数据的管理同样有相关的规定:[/align][align=left] [/align][align=left][b][i][color=#5f9cef][/color][/i][/b]的第7.5章节“技术记录”之“7.5.2 a”项下:当用电子方式储存记录时,对记录的修改应由授权人员进行,并记录修改人、修改时间、修改前和修改后的内容,必要时,应注明修改的原因;[/align][align=left] [/align][align=left][b][i][color=#5f9cef][/color][/i][/b]的第4.13章节“记录的控制”之“4.13.1.4”项下: 实验室使用信息管理系统(LIMS) 时, 应确保该系统满足所有相关要求,包括审核路径、数据安全和完整性等。 实验室应对LIMS与相关认可要求的符合性和适宜性进行完整的确认,并保留确认记录;对LIMS的改进和维护应确保可以获得先前产生的记录。[/align][align=left] [/align][align=left]从CNAS相关要求可以看出,对于电子方式存储的记录,其和GMP对计算机化系统的要求大同小异,其中关于“记录的修改应由授权人员进行,并记录修改人、修改时间、修改前和修改后的内容,必要时,应注明修改的原因”的相关描述和GMP要求是无异的。通俗的讲就是要有权限管理和审计追踪控制。[/align][align=left] [/align][align=left]对于规模不大的CNAS实验室,资源和其他各方面上LIMS条件不成熟,用Excel几乎是替代的理想选择,可解决方方面面的问题,例如实验室的各种自动计算,合格与否的判断,各种数据的管理。即便是有LIMS的单位,由于LIMS的灵活性不够,管理也无法覆盖到实验室的所有事务,而且调整改变太麻烦,采用电子表格管理也是对于LIMS的良好补充。微软的整个Office 系列均稳定,成熟,功能强大,灵活可变,实验室的人员自己动手就能丰衣足食,利用电子表格的强大功能实现无纸化,提高实验室工作和管理的效率。[/align][align=left] [/align][align=left]那么,如果我们在CNAS认证的实验室使用Excel表格,要求是同样的,需要有必要的权限管理和审计追踪控制。此时, Excel合规插件eInfotree即能够完美契合CNAS认证实验室。[/align][align=left] [/align][align=left][b]eInfotree核心功能一:限制性访问[/b][/align][align=left] [/align][align=left][b][color=#00b0f0]▷ [/color][/b][color=#0070c0] [/color][b][color=#5f9cef]授权人员才能打开[/color][color=#5f9cef]Excel[/color][color=#5f9cef]电子表格,打开电子表格时需要使用唯一地用户名和密码;[/color][/b][/align][align=left] [/align][align=left][b][color=#00b0f0]▷ [/color][color=#5f9cef]根据用户或者用户组配置[/color][color=#5f9cef]Excel[/color][color=#5f9cef]电子表格的读写权限;[/color][color=#00b0f0][/color][/b][/align][align=left] [/align][align=left][b][color=#00b0f0]▷ [/color][color=#5f9cef]根据用户或者用户组配置对[/color][color=#5f9cef]Excel[/color][color=#5f9cef]菜单的访问权限,从而控制用户使用[/color][color=#5f9cef]Save as [/color][color=#5f9cef]和[/color][color=#5f9cef]Print[/color][color=#5f9cef]等关键功能。[/color][color=#00b0f0][/color][/b][/align][align=left][img=,690,306]https://ng1.17img.cn/bbsfiles/images/2019/06/201906242005189541_1861_3419387_3.jpg!w690x306.jpg[/img][/align][align=left] [/align][align=left][b]eInfotree核心功能二:审计追踪[/b][/align][align=left] [/align][align=left][b][color=#00b0f0]▷ [/color][color=#5f9cef]记录[/color][color=#5f9cef]Excel[/color][color=#5f9cef]电子表格中单元格级别的任何修改,包括修改人、修改时间、修改类型、修改前和修改后的内容;[/color][color=#00b0f0][/color][/b][/align][align=left] [/align][align=left][b][color=#00b0f0]▷ [/color][color=#5f9cef]记录用户登录,登出,非法登录尝试,密码变更与锁定的审计追踪记录。[/color][color=#00b0f0][/color][/b][/align][align=left] [/align][align=left][b][color=#00b0f0]▷ [/color][color=#5f9cef]配置修改原因的可选项,审计追踪显式标记。[/color][color=#00b0f0][/color][/b][/align][align=left][img=,556,313]https://ng1.17img.cn/bbsfiles/images/2019/06/201906242005324288_8859_3419387_3.jpg!w556x313.jpg[/img][/align][align=left] [/align][align=left][b]eInfotree核心功能三:电子签名[/b][/align][align=left] [/align][align=left][b][color=#00b0f0]▷ [/color][color=#5f9cef]支持电子签名,签名后可根据配置锁定单元格,工作表或工作簿;[/color][/b][/align][align=left] [/align][align=left][b][color=#00b0f0]▷ [/color][color=#5f9cef] [/color][color=#5f9cef]支持线上审批工作流程,通过邮件自动将待审批的;[/color][color=#5f9cef][/color][/b][/align][align=left] [/align][align=left][b][color=#00b0f0]▷ [/color][color=#5f9cef] [/color][color=#5f9cef]支持实验室实现基于[/color][color=#5f9cef]Excel[/color][color=#5f9cef]电子表格的无纸化办公模式。[/color][color=#5f9cef][/color][/b][/align][align=left][img=,690,332]https://ng1.17img.cn/bbsfiles/images/2019/06/201906242006128689_797_3419387_3.jpg!w690x332.jpg[/img][/align]
如题,有人有“不同温度下标准滴定溶液的体积补正值”的电子表格吗?帮忙传上来一份呀?
絮用纤维检测报告表格?哪位朋友对絮用纤维GB18383-2007比较了解,有没有絮用纤维检测报告的电子表格发给我一份
[color=#31424e][/color][align=left]电子表格软件是使用最广泛,最受各种企业青睐的软件之一。电子表格软件中的杰出者Excel以其易用性和灵活性在各行各业都有十分广泛的应用。用户往往不需要什么培训或使用经验就可以独立操作Excel软件。同时,灵活性和应用的广泛性也使得在应用开发和操作时出现错误的概率大大增加。最新的调查表明,超过90%的电子表格都存在错误。由于Excel并非是专为合规环境而设计的,因此对电子表格和其产生的数据进行验证也变得更加困难。在GxP环境中(GCP、GMP、GLP),Excel等电子表格的使用需要受控,并且需要采用系统的方法进行开发和验证确认,以保证数据的合法性。除了进行验证和确认,通过Excel 及其中的宏程序所计算生成的记录属于电子记录,因此Excel在合规环境下的使用还需要符合ER/ES(电子记录/电子签名)的相关要求,而Excel与生俱来的在安全和审计跟踪方面缺陷使得很多公司在使用时一直心存疑虑。微软公司于2013年发布了最新的SharePoint与Office在符合Part11方面的说明,但鉴于国内采用SharePoint的用户数量并不多,我们这里说明的仍是单机版Excel在合规方面存在的问题。[/align][color=#333333][/color][align=left][/align][align=left]Excel最大的问题在于符合21CFR Part11的要求。21 CFR Part 11主要是关于电子记录和电子签名方面的法规,其主要要求包括:[/align][color=#333333][/color][list][*]GxP下使用经验证的软件和计算机系统[*]用户无关,由计算机自动生成的时间标记的审计跟踪[*]系统和数据安全性,数据完整性,限制性访问[*]将手写签名或电子签名与电子记录绑定[*]准确、完整、安全地保存电子记录[/list][color=#333333][/color][align=left][/align][align=left]相比于以前的解释,FDA在2003年发布的新的关于Part11的最终指导缩小了其应用范围,但在影响产品质量和安全以及记录完整性方面进一步强调了基于风险的评估。由电子表格计算生成的记录都属于这一类,例如,在很多药厂电子表格被用于药品生产过程中的批次放行。[/align][align=left][/align][b][color=#333333]电子表格在在合规环境中遇到的问题[/color][color=#333333][/color]访问安全性[/b][color=#333333][/color][align=left]电子表格软件大多安装在个人电脑和服务器上,通常提供给所有用户使用。几乎每个人都可以访问。质量保证部门对于到底有多少电子表格应用在了合规环境下很难掌握确切的数据。[/align][b]变更控制[/b][color=#333333][/color][align=left]首先,电子表格中的内容相对而言比较容易被修改。而且通常这种更改没有记录,后续也不会做任何的测试。其次电子表格的使用环境很难去控制。每一个电子表格都是基于特定的计算机配置去开发的,这个配置包括开发所用计算机的操作系统及所用的Excel版本。就拿笔者来说,当前使用的是Windows8.1的OS,Excel用的是2013.尽管如此,我编辑的这个电子表格可以发布给其他的用户使用,而这些用户的系统可能是Windows7/10/XP ,而Office也有可能是2010或是2007,非常自由,但电子表格的使用环境还是发生了变化的。[/align][color=#333333][/color][align=left]再次,电子表格的文件版本很难去控制,即便是一台计算机中也可能在不同文件夹中存放在不同版本的Excel文件,更不说在一个公司的范围内,各台个人计算机,服务器,网络磁盘都会有Excel不同版本的复制品。[/align][b]电子记录/电子签名方面的缺陷[/b][color=#333333][/color][align=left]通常情况下,电子表格程序不符合所有相关规定。特别是,21 CFR Part 11中的相关条款,同样也不符合中国GMP最新附录”计算机化系统”的要求,例如安全性要求、审计跟踪的要求,这是单机版Excel与生俱来的缺陷。[/align][b]人员资格[/b][color=#333333][/color][align=left]最新的GMP附录《计算机化系统》第三章”人员”对计算机化系统的人员的职责和资质给出了相关要求。而对普通的商业电子表格程序来说,任何人都可以开发电子表格计算和使用相关电子表格。虽然在电子表格中定义计算公式也算是是软件开发的范畴,但设计这些计算公式并不需要软件开发技能。自定义的公式可以方便地加入到Excel的公式库中。[/align][b]验证与确认[/b][color=#333333][/color][align=left]很少会有人意识到Excel的计算应该进行验证。我们往往会因为碰到某个问题临时定义个公式算一下,这种临时用的电子表格都是一次性的,这种情况大家不可能会去考虑做验证。事实上也确实如此,对于一次性的电子表格只需要进行细致的检查,不需要验证。但对于那种反复使用的电子表格,验证就是必须的了。[/align][b]缺乏文档的支持[/b][color=#333333][/color][align=left]通常情况下,电子表格的开发者也是使用者,很少会认为自己开发给自己用还会需要什么文档。[/align]
《Excel与化学化工试验数据处理》【作 者】 胡亮, 杨大锦编著【丛书名】 化学化工中计算机应用技术丛书【页 数】 298页【尺 寸】 24cm【DU 号】 000003153722【出版社】: 化学工业出版社【主题词】: 电子表格系统(学科 应用学科 化学工业学科 化学实验学科 数据处理)【ISBN号】 7-5025-2992-6 7-89995-617-x【出版日期】: 2004 【内容简介】微软公司的Excel是集文字、数据、图表处理于一体的,并能进行数据计算和统计分析的电子表格软件。其操作简单,所见即所得。 本书简要介绍Excel电子表格应用基础知识,并在此基础上结合大量化学化工实例,重点介绍Excel试验数据分析及应用,能满足化学化工工作者进行试验设计和数据处理工作的需要。 附赠光盘中根据书中出现的实例和有关Excel电子表格图示,按照篇章整理出了相应的Excel电子表格,方便与书中实例对照学习。同时以Excel电子表格的形式,摘录了部分实验用表,方便参考。 本书适用于化学化工科技工作者和科研人员阅读,也可作为化学化工相关专业教师、学生用教材。
[align=left]对于类似Excel电子表格类的应用程序,在合规领域GxP(GLP、GMP、GCP)使用时,必须是受控的和经过验证确认的。人们通常有一些误区。一种极端是认为Excel具有很多缺陷,不能在合规环境中使用,另外一个极端是认为Excel这种在全球商业领域广泛应用的软件必然是经过实践检验的,受到公认的,不需要验证了,但FDA恰恰没有对任何软件给予这种免于验证的豁免权,当然也没有说Excel就完全不能在其监管领域中使用,相反,在FDA所属的一些实验室也大量使用了Excel。这么好用的软件,谁能经经受得住诱惑呢。[/align][align=left][/align][align=left]出于担心Excel在合规环境中应用的质疑,很多企业尽量避免在法规监管的重要领域使用Excel表格,而用其他系统替代。这种办法确实有一些成功的案例,但开销大,时间长。除了极少数公司能完全替换掉Excel,绝大部分公司仍然或多或少地在使用Excel。大家一方面对自己设计的Excel产出的数据信心满满,但面对检察官和审计人员时,却又发现很难证明其可信度。[/align][align=left][/align][align=left]还有一个误区是,通过风险评估去规避验证确认环节。的确,计算机系统的验证提倡基于风险的验证,我们无需在低风险软件应用上去浪费过多的精力,但并不能说我们自己去评估自己所用的Excel表格,并自认为是低风险的,以此作为不验证的理由。更何况,统计表明,高达94%的Excel表格都包含或多或少的错误。[/align][align=left][/align][align=left]如果我们去关注FDA发放的483警告性,就会发现关于电子表格方面的警告信非常多,这并不奇怪,一是Excel的应用实在是太广泛了,我们每天都接触和应用大量的电子表格,多了自然就会出问题。另一个原因就是缺少对电子表格进行验证确认的管理上的支持,大家都往往忽视这一块。[/align][align=left][/align][align=left]FDA的检查官和QA审计员也十分清楚电子表格类的程序通常并没有在好的受控条件下运行,而且在安全性和审计跟踪功能方面有缺陷。对于一款桌面级的工具性软件,我们本不应该苛求更多,这也不是Excel设计使用的初衷。但既然我们将其应用在GxP环境下,又必须考虑合规性的问题。[/align][align=left][b][/b][/align][align=left][b]什么样的电子表格需要进行验证/确认?[/b][/align][color=#333333][/color][align=left]从使用方式上,电子表格可以分为个人使用的和公用的。所谓个人使用的,是指个人临时创建的电子表格或者使用个人制作好的模板创建的电子表格,对数据作临时性处理的情况。这种电子表格应该仅供个人使用,往往不会涉及过于复杂的表格结构,不会包含复杂的计算公式,宏、颜色标记、单元格保护和使用说明。因为这类电子表格毕竟是个人使用,需要在哪里输入数据,公式在哪里,哪里不能改动自己都比较清楚,上述这些特性都不需要。而我们在工作中,特别是在规范环境中,应用的一般是循环使用的,也就是那种设计精良的计算模板,通用性强,功能强大,方便好用,往往作为程式化的数据处理和报告工具。这两类电子表格只要用于与质量相关的活动,都必须进行验证,根据使用的风险决定验证的深度。对于公用的电子表格,特别是当一个标准的计算方式在很长一段时间里都要重复地被多人使用,那么我们就需要考虑对其进行严格的验证确认,因为这种方式一旦出现错误,将产生长期和持续的影响。对于个人使用的电子表格,则需要根据其是从模板创建还是临时创建决定其验证方式和深度。[/align][color=#333333][/color][align=left][/align][align=left]从功能上讲,电子表格可以分为仅仅存储数据的电子表格和具有数据处理的电子表格两种。很多人有一个误解,就是只需要对做数据处理的电子表格进行验证,而作为数据存储的电子表格则不需要。然而,你从任何一部国内外法规中都找不出对这两种不同电子表格区分对待的条款。美国医疗器械质量体系法规(QSR)是这样规定的:如果电子表格或数据库用于创建,维护,归档,修改,检索或传输QSR或任何其它FDA法规要求的数据或记录,那么就需要按其预期用途进行验证。从计算机系统验证/确认的角度也是能够理解的,绝大多数计算机系统都同时包括了数据存储与计算处理的功能,不同的系统只不过会各有其侧重点。我们不会因为某个系统只存储数据就不去做验证,何况这还是一种电子记录呢。总之,是否做验证的判断的标准是该系统对产品质量、患者安全、数据完整性是否有影响以及影响的大小。[/align][align=left][/align][b]电子表格验证的内容[/b][color=#333333][/color][align=left]所谓验证的内容,也就是验证的范围,千万不要尝试去验证整个Excel,Excel是这个世界上最优秀的软件之一,可以称得上博大精深,几乎应用于全球每一个行业,你想验证整个Excel,似乎不太现实。其实对于这个问题,FDA已经给出了答案,既只需要验证你用Excel软件根据业务需求创建的电子表格中的内容。[/align]电子表格软件作为计算机系统中的一种,其验证的目的同样是:建立文件来证明系统的开发符合质量工程的原则,能够提供满足用户需求的功能并且能够长期稳定工作的过程。这里的系统是指根据需求制作的电子表格和宏程序,而非Excel本身。由此衍生,对电子表格的验证与确认是为了确保所有的操作和产生的数据,以及通过电子表格执行的计算,数据检查,以及动态生成的图表都是合规有效的。以往那种仅仅用手持计算器对Excel表格中的公式进行计算比较的方式在新版GMP对计算机系统验证要求的背景下就太显单薄了。[color=#333333][/color][align=left][/align][align=left]电子表格的验证与确认主要是两方面的内容,一方面是Excel的设计开发过程与Excel本身是否符合业务需求。业务需求主要包括Excel中的计算公式,数据引用、数据检查,数据格式、数据精度的验证。对于公式而言,我们需要验证的是公式中包含多个Excel标准库函数或者使用了VBA自定义函数的,或者使用了逻辑运算符if then的,而Excel中自带的单个标准函数比如求平均数,最小值,最大值就不需要专门去验证了,我们默认这些自带的函数随着Excel产品开发完成已经验证确认过了。对于数据引用关系,这里包括公式中的数据位置引用和图表对数据组的引用,我们不用去考究数据传递过程中是否有问题,但必须能够说明表格中的数据列与图之间的对应关系是正确的。[/align][color=#333333][/color][align=left][/align][align=left]电子表格验证的另一方问题包括安全的数据存储,单元格和文件的安全、ER/ES(电子记录/电子签名 Part11要求)缺陷的弥补,审计跟踪,访问控制等。[/align]验证与确认功能是十分消耗资源与时间的,因此我们需要权衡对Excel电子表格验证是否有必要,除了对每一个电子表格进行实际的验证,必须建立操作说明用于指导如何使用电子表格开展日常工作。[b]验证的方法[/b]电子表格的结构从本质上就是一种计算机程序。我们同样要遵循计算机系统验证基于风险评估的方法,验证的深度应该与风险的分类相匹配。对于复杂的电子表格模板,如果里面包含了大量复杂公式组合与逻辑函数的使用,这就相当于是一个编程开发过程。定制软件的编码过程也是一个个函数,加上计算法则和逻辑判断构成的,更不用说包含宏程序的开发。此时,我们可以套用企业内部自定义开发软件的验证流程,也就是GAMP中第五类软件的验证方式,但在验证的深度和广度上可以做适当的取舍,例如我们可以把URS和FS合并,或者将OQ与PQ合并起来。[color=#333333][/color][align=left]我们需要把所有需要在合规环境中(GMP、GLP)用到的Excel表格登记造册,对这些Excel表格根据其所用到的数据,电子表格的功能,产生的数据报告进行风险评估。最终得到的Excel表格目录需要为每一个Excel表格按照优先级进行排序,这样做的好处是可以将验证的精力更多的放在那些业务风险和合规风险最高的电子表格上。合规性的风险与Excel表格本身设计的复杂性并无相关性。优先验证那些简单的,但风险高的,也能让验证人员更快地了解验证流程。[/align][align=left][/align][align=left][b]验证过程文档准备[/b][/align][color=#333333][/color][align=left]计算机系统的验证过程需要文档来提供证据证明验证过程是合理的,证据是充分的。正确和完整的文档对于检查非常重要。它还允许未参与M&S开发和测试的人了解和审查程序。电子表格的验证一般应提供下列文件:[/align][color=#333333][/color][list=1][*] 公司验证总计划[*] 宏和电子表格信息[*] 宏和电子表格在规范的环境使用、验证,变更控制的标准操作规程[*] 使用电子表格的系统清单目录,其中列出授权用户,计算机硬件,系统软件,电子表格程序和版本,电子表格文件的名称和版本的位置[*] 验证计划(Validation Plan)[*] 需求规格(URS)[*] 设计规范(DS)[*] 设计审查报告[*] 包含注释的代码[*] 代码审查报告[*] 测试计划和测试方案[*] 安装报告(IQ)[*] 变更控制报告[*] 历史记录[*] 验证报告[/list][b]总结:[/b]电子表格,特别是Excel作为全世界应用最广泛的软件之一,在法规监管的制药,临床,医疗器械的研发和生产领域都有广泛的应用。Excel的易用性和出色的功能为日常工作提供了巨大的便利,大为提高我们的日常工作效率。相对于其他的一些软件和信息化系统,人们更乐意使用Excel作为其最常用的数据处理工具,并在Excel的基础上发挥自身的主动性创造了丰富多彩的应用。当然,我们也不能忽视Excel灵活性背后所存在的问题,特别是在国内外GMP愈加注重计算机系统的可靠性和数据完整性的背景下,我们应该结合现有的使用情况,进行差距分析和风险评估,并制定积极的整改计划,这对于我们规范Excel在公司内部的使用,提升Excel的使用水平,降低风险也是十分有益的。

电子表格是各行业使用最广泛的软件之一。电子表格软件中的杰出者Excel以其易用性和灵活性在各行各业都有十分广泛的应用。小到一些基本的计算,大到业务智能,Excel是提高工作效率的重要工具。用户往往不需要什么培训或使用经验就可以独立操作Excel软件。正是由于其灵活性和应用的广泛性,其在开发和操作时出现错误的可能性也大大增加,并且对电子表格和其产生的数据进行验证也变得更加困难。最新的调查表明,超过90%的电子表格都存在错误。在合规环境中,也就是在GxP环境中(GCP、GMP、GLP),Excel使用十分广泛,例如很多药物生产中的批次放行就是基于Excel来做的。但Excel并非是专为合规环境而设计的,通过Excel 及其中的宏程序所计算生成的记录属于电子记录,因此必须符合FDA 21 CFR Part 11的相关规则另外,Excel的使用必须受控,并且需要采用系统的方法进行开发和验证确认,以保证数据的正确性与合法性。除了进行验证和确认,Excel在合规环境下的使用还需要满足ER/ES(电子记录/电子签名)的相关要求,而Excel与生俱来的在安全、审计跟踪、限制访问等方面缺陷使得一些人士甚至认为Excel不能用在合规领域。微软于2013年发布了最新的SharePoint在符合Part11方面的说明,但其主要考察Excel版本之间差别控制,而没有去体现单元格级别的变更记录,同时鉴于国内采用SharePoint的用户少之又少,我们这里借鉴国外公司的经验谈谈Excel合规化使用的一些方法。1 Excel应用于合规环境的基本策略Ÿ 充分利用Excel内置的安全机制和相关功能,并采用Excel功能扩展插件实现限制性访问和审计跟踪,弥补合规性缺陷,这样不对现有工作方式产生任何影响。Ÿ 为电子表格程序的开发、使用、文档编制提供基础设施和环境,策略以及操作规程Ÿ 采用系统化的方法验证电子表格的计算公式和宏。以上策略应该体现到公司相关的政策,验证总计划,系统目录、宏和电子表格开发和应用的规程中。1.1公司层面策略的制定公司或组织需要制定用于电子表格程序开发的规章制度。针对这一部分的规章制度将作为公司整体合规和质量政策的一部分,可单独成文。该政策应该获得管理层的支持,并传达给所有员工,包括以下内容:Ÿ 在GxP下使用的所有电子表格及相关的宏的开发和使用必须遵循标准操作程序。Ÿ 所有在用的电子表格和宏都应注册登记。Ÿ 所有宏和电子表格应按照标准规程进行验证。Ÿ 变更应遵循既定的变更控制程序。Ÿ 安全措施以及其他与合规相关的电子表格功能都应启用。Ÿ 宏和电子表格程序应妥善保护以防止意外的修改。1.2合规总计划的制定公司政策主要是为了阐明目标,具体的落实则通过拟定合规总计划进行实施。为了进一步说明目标和需要采取的措施,计划中应该采用相关的范例以作说明。合规总计划应当包括如下内容:Ÿ 计划的目标、项目背景、范围、所涉及的用户Ÿ 所有必须遵守合规政策的电子表格的目录Ÿ 责任分配,表格由谁开发,由谁验证Ÿ 需要执行的SOP列表Ÿ 对宏和电子表格的一般要求列表1.3系统清单所有的应用于计算的电子表格程序都应该登记。登记信息包括电子表格程序本身的信息,操作系统,计算机硬件,应用程序,授权用户列表。这些信息有任何更改都要更新。http://ng1.17img.cn/bbsfiles/images/2016/01/201601131606_581716_1603327_3.png1.4统一软件版本企业里计算机操作系统和Excel的版本过多,会造成管理上的负担,更不利于合规环境下的监管。尤其是版本过老,失去了厂商的技术支持更容易受到病毒和漏洞侵袭程序的干扰。即便是不能马上统一所有的软件版本,我们也需要设定一个时间上的期限。标准化的操作系统和电子表格软件(包括其版本)有助于减少下列情况的发生:Ÿ 安装和使用时所需要的用户信息Ÿ 验证工作量Ÿ 安装和使用过程中的技术支持Ÿ 版本之间不兼容性引起的错误1.5规范软件开发宏和电子表格的开发应该尽可能标准化。下面是一些应当标准化的项目:Ÿ 设计规范Ÿ 命名规范,如rt_data_entry,std_resultsŸ 代码编写规范Ÿ 代码注释,例如头文件注释Ÿ 公式编辑Ÿ 单元格的颜色,例如统一需要输入数据的单元格的背景色Ÿ 电子表格注释(如文件名,版本)Ÿ 验证和测试1.6日常使用电子表格在应用过程中所出现的错误大部分不是因为程序不合格或测试不充分,而是源于日常工作中的不当使用。有多种原因导致这种情况发生。Ÿ 使用电子表格的新用户未经任何培训Ÿ 用户使用了未经授权的电子表格Ÿ 用户输入错误的数据以上问题可以克服或最小化。Excel的应非常普遍,界面也十分友好,绝大部分用户会认为他们不需要任何培训就可以上手。有这种认识对于电子表格软件本身没有可质疑的地方,但对于某个具体的Excel电子表格模板的使用却不尽如此。一些制作精良的电子表格模板的复杂程度不亚于一个全新的软件。对电子表格研究略深的人都会有更清醒的认识。因此,在使用某个成熟的电子表格模板前,用户至少要阅读说明书并了解可能出现的问题。1.7文档的要求正确和完整的文档对于检查非常重要。它能帮助未参与电子表格模板开发的人了解和审查程序。完整的文档应包括:Ÿ 公司验证总计划Ÿ 宏和电子表格信息Ÿ 宏和电子表格在规范的环境使用、验证,变更控制的标准操作规程Ÿ 使用电子表格的系统清单目录,其中列出授权用户,计算机硬件,系统软件,电子表格程序和版本,电子表格文件的名称和版本的位置Ÿ 验证项目的计划Ÿ 需求规格Ÿ 设计规范Ÿ 设计审查报告Ÿ 包含注释的代码Ÿ 代码审查报告Ÿ 测试计划和测试方案Ÿ 安装报告Ÿ 变更控制报告Ÿ 历史记录Ÿ 验证报告Ÿ 对照CFR Part11所做的评估,差距分析,风险评估和积极的整改计划。2 总结Excel可以说是在各行各业的工作中用到最多的软件。众多导入,导出操作都离不开Excel作为数据的载体。其易用性和可扩展性让其从小到一般的计算、统计到高级的数据可视化,模拟分析、业务智能等高端应用几乎无所不能。我们很难想象在现代社会里某一个行业完全不使用Excel的情景。对于受FDA、CFDA监管的制药领域同样如此。综合国外企业在监管环境下的使用经验,利用Excel的强扩展性制作的辅助性功能同样能满足法规的要求。
推荐教学仪器管理系统 2005.0725 运行环境 Win9x/Me/NT/2000/XP 教学仪器管理系统适合学校或教委统计教学仪器设备,如:某个日期段的盘存数、金额等统计数据,生成的报表是电子表格形式,可以用电子表格EXCEL打开编辑排版。 该软件附带国家颁布的物理、化学、生物等各类仪器的编号表,在学校的“两基”检查时很方便快速地统计出所选年度的教学仪器结存帐报表。 希望你能喜欢[~85992~]
虽然教材中都可查到酸碱常数,但当你手里没有书时,或书中的常数太少时,可以从附件的电子表格中直接查到你要的数据。[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=147559]弱酸弱碱离解常数[/url]
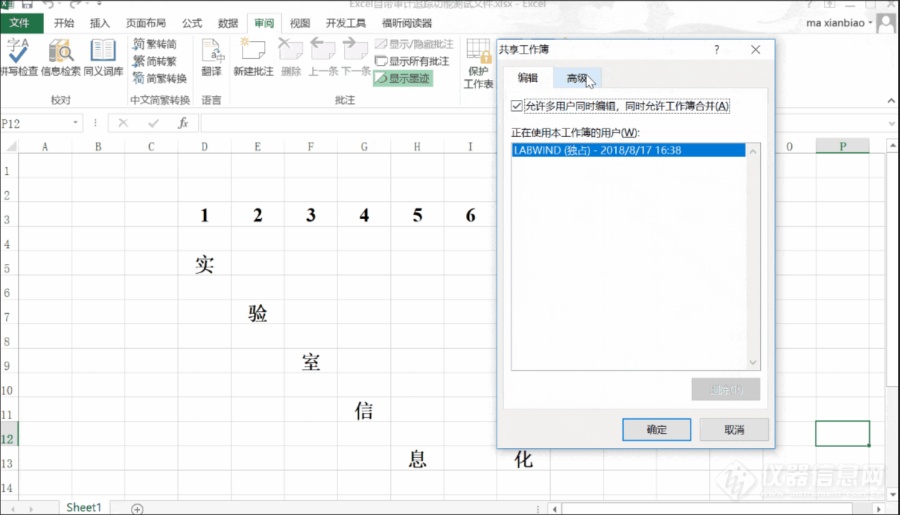
Excel因其方便易用,备受各行各业青睐,制药行业也不例外。然而用作合规用途的电子表格无法符合制药法规要求,特别的,缺乏审计追踪这个合规要素。网上一种流传甚广的做法是通过共享工作簿实现审计追踪功能。笔者在仔细研究了这种方法之后,发现有如下缺陷,希望引起业界注意。[b]缺陷一取消工作簿共享,审计追踪丢失[/b]FDA 21 CFR Part 11要求:使用安全的,计算机生成的审计追踪来独立记录操作人员对电子记录的创建、修改或删除,而且审计追踪信息不能被删除。通过共享工作簿方式实现对单元格录入,修改的审计追踪,会在自动生成的工作表“历史记录”中显示。但是,如果取消对工作簿的共享,工作表“历史记录”将立刻被删除,其记录的审计追踪信息也会被删除而且无法恢复。不加控制的对审计追踪信息的删除,无法确保数据可靠性。[align=left][img=,690,395]https://ng1.17img.cn/bbsfiles/images/2018/08/201808211712354226_4955_3419387_3.jpg!w690x395.jpg[/img][/align][align=left]图1 通过共享工作簿实现审计追踪[/align][align=left][img=,690,397]https://ng1.17img.cn/bbsfiles/images/2018/08/201808211714105288_3112_3419387_3.jpg!w690x397.jpg[/img][/align][align=left]图2 取消工作簿共享审计追踪消失[/align][align=left][/align][align=left][b]缺陷二可在Excel中随意修改操作者姓名[/b]FDA法规要求审计追踪能够真实反映操作人员对电子记录的任何修改。然而Excel表格可以任意修改用户名信息,从而导致审计追踪中操作者随之改变,但是实际上整个操作过程只有一个人。通过修改用户名,就可以模拟出另外一个操作人的操作记录,这样审计追踪就无法真实追踪操作者身份。如果真的以这份修订记录为依据,大家就准备随时帮别人背锅吧,陷害人的手段原来还能这样。[img=,690,395]https://ng1.17img.cn/bbsfiles/images/2018/08/201808211715099828_1222_3419387_3.jpg!w690x395.jpg[/img][/align]图3 任意修改用户名虚拟操作人员[b]缺陷三 审计追踪随工作簿的删除而被删除[/b]由于审计追踪信息,即“历史记录”是以一个工作表的形式存在于工作簿中,操作人员若删除工作簿,所有包含在工作簿中的工作表将会被删除,包括这个叫“历史记录”的审计追踪表格。[b]缺陷四 审计追踪信息不全面[/b]Excel的审计追踪功能对电子表格的修改追踪并不全面,其审计追踪无法记录操作人员进入和退出电子表格,保存和另存电子表格,修改操作者姓名等操作。[b]Excel合规使用解决方案[/b]实现电子表格的合规使用,最靠谱的方法还是要借助第三方合规插件。eInfotree合规插件是目前电子表格合规的最佳解决方案。它能够弥补标准Excel在合规使用上的先天不足。就审计追踪要素而言,eInfotree能够做到记录对电子表格的任何修改:用户的登录,登出,对电子表格的任何操作都能追踪到单元格级别,并且审计追踪信息无法被删除,篡改;同时能够实现限制性访问:采用唯一的用户名和密码,实现密码生命周期管理,多级别访问控制;还能够设置电子签名工作流,实现记录无纸化,为制药企业电子表格的合规使用保驾护航。
不知道哪位大侠有非离子表面活性剂的制造、性能和分析这本书的电子版,能否传一下共享谢谢哦!最近查参考文献查到的,急用哦! 好像风怜香有在目录上提过,不知您有没时间帮忙传一下呢?
美国伯乐酶标仪,数据如何子电子表格保存下来
我们在检测数据中客户需要我们提供Sr值(Sr可能是法语),不知是否就是CV值或者电子表格中的STDEVPA计算值?
请教各位:计量认证允许日常管理例如来样登记直接是用电脑上记录的电子表格吗?
CNAS-CL18提出恒温恒湿要求由连续记录的电子温湿度记录仪来监控,但是数据导出后是电子表格的形式,打出来有说服力吗?
1.非计算机系统的人工记录是指手写还是录入到电子表格2. 7.11.6应对计算和数据传送进行适当和系统的检查,这里边的计算指的是人工计算还是电脑程序计算?
现在需要导出今年1至8月的分析结果数据,ARL4460和3460的,怎么样把他们的数据导出,转换为电子表格,进行筛选统计。。。。。请高手指点,再此谢过
温湿度环境要求用连续记录的电子温湿度记录仪来控制,但是记录如何做的?一个是导出来的是电子表格形式,能够改动。二是导出来的温湿度记录是每隔5min记录一次,如果每天打印的话太浪费了。不知道其他实验室是怎么做的?

我们使用的是SATERAM DSC7仪器,做的是用蒸馏水配的5%NaCl,分别做了没有通甲烷的和150bar,200bar的甲烷气,在15度等温,然后在降到—40度,然后再等温,然后再升到十五度,因为我们的软件比较老,几个曲线不能在一张图中绘制,所以我用的是电子表格处理的,然后在电子表格里面稍微调整了一下曲线以便察看,向上是放热。我们主要是考察在高压低温下天然气水合物的形成状况。在空白没有通甲烷的情况下,降温曲线出了几个峰都不知道是怎么回事,因为里面就只有氯化钠啊,难道是水合物形成了?然而在升温阶段就出了两峰,这两个峰有后面那个是水溶解的峰,前面一个不知道,麻烦大家帮我看看吧,谢谢。。[img]http://ng1.17img.cn/bbsfiles/images/2010/02/201002011038_199970_1979959_3.jpg[/img]
最近遇到一个问题,一个真皮材料,用在电子表的表带,测试ROHS,结果六价铬检出1000多。而采用ISO 17075的方法,结果为未检出。请大家帮忙分析下原因。到底哪种方式更合理,结果更准确。
卵子表面争相受精的精子在扫描隧道电子显微镜下观察到的人体微观结构,可以分辨1-5纳米(1纳米相当于10亿分之一米)直径的细节,让人一睹难得一见的身体细节。后边你还将看到从精子+卵子到胎儿的整个孕育过程。http://www.people.com.cn/mediafile/pic/20110923/26/5555686583589404494.jpg这张照片中,许多精子正争相争取为卵子授精。