为探究生物进程的分子机制,需要确定介导这个过程的蛋白质-蛋白质间的相互作用。研究蛋白质间相互作用的主要技术总结如下:一、酵母双杂交系统酵母双杂交系统是当前广泛用于蛋白质相互作用组学研究的一种重要方法。其原理是当靶蛋白和诱饵蛋白特异结合后,诱饵蛋白结合于报道基因的启动子,启动报道基因在酵母细胞内的表达,如果检测到报道基因的表达产物,则说明两者之间有相互作用,反之则两者之间没有相互作用。将这种技术微量化、阵列化后则可用于大规模蛋白质之间相互作用的研究。在实际工作中,人们根据需要发展了单杂交系统、三杂交系统和反向杂交系统等。Angermayr等设计了一个SOS蛋白介导的双杂交系统。可以研究膜蛋白的功能,丰富了酵母双杂交系统的功能。此外,酵母双杂交系统的作用也已扩展至对蛋白质的鉴定。二、噬茵体展示技术在编码噬菌体外壳蛋白基因上连接一单克隆抗体的DNA序列,当噬菌体生长时,表面就表达出相应的单抗,再将噬菌体过柱,柱上若含目的蛋白,就会与相应抗体特异性结合,这被称为噬菌体展示技术。此技术也主要用于研究蛋白质之间的相互作用,不仅有高通量及简便的特点,还具有直接得到基因、高选择性的筛选复杂混合物、在筛选过程中通过适当改变条件可以直接评价相互结合的特异性等优点。目前,用优化的噬菌体展示技术,已经展示了人和鼠的两种特殊细胞系的cDNA文库,并分离出了人上皮生长因子信号传导途径中的信号分子。三、等离子共振技术表面等离子共振技术(SurfacePlasmonResonance,SPR)已成为蛋白质相互作用研究中的新手段。它的原理是利用一种纳米级的薄膜吸附上“诱饵蛋白”,当待测蛋白与诱饵蛋白结合后,薄膜的共振性质会发生改变,通过检测便可知这两种蛋白的结合情况。SPR技术的优点是不需标记物或染料,反应过程可实时监控。测定快速且安全,还可用于检测蛋白一核酸及其它生物大分子之间的相互作用。四、荧光能量转移技术荧光共振能量转移(FRET)广泛用于研究分子间的距离及其相互作用;与荧光显微镜结合,可定量获取有关生物活体内蛋白质、脂类、DNA和RNA的时空信息。随着绿色荧光蛋白(GFP)的发展,FRET荧光显微镜有可能实时测量活体细胞内分子的动态性质。提出了一种定量测量FRET效率以及供体与受体间距离的简单方法,仅需使用一组滤光片和测量一个比值,利用供体和受体的发射谱消除光谱间的串扰。该方法简单快速,可实时定量测量FRET的效率和供体与受体间的距离,尤其适用于基于GFP的供体受体对。五、抗体与蛋白质阵列技术蛋白芯片技术的出现给蛋白质组学研究带来新的思路。蛋白质组学研究中一个主要的内容就是研究在不同生理状态下蛋白水平的量变,微型化,集成化,高通量化的抗体芯片就是一个非常好的研究工具,他也是芯片中发展最快的芯片,而且在技术上已经日益成熟。这些抗体芯片有的已经在向临床应用上发展,比如肿瘤标志物抗体芯片等,还有很多已经应用再眼就的各个领域里。六、免疫共沉淀技术免疫共沉淀主要是用来研究蛋白质与蛋白质相互作用的一种技术,其基本原理是,在细胞裂解液中加入抗兴趣蛋白的抗体,孵育后再加入与抗体特异结合的结合于Pansobin珠上的金黄色葡萄球菌蛋白A(SPA),若细胞中有正与兴趣蛋白结合的目的蛋白,就可以形成这样一种复合物:“目的蛋白—兴趣蛋白—抗兴趣蛋白抗体—SPA\|Pansobin”,因为SPA\|Pansobin比较大,这样复合物在离心时就被分离出来。经变性聚丙烯酰胺凝胶电泳,复合物四组分又被分开。然后经Westernblotting法,用抗体检测目的蛋白是什么,是否为预测蛋白。这种方法得到的目的蛋白是在细胞内天然与兴趣蛋白结合的,符合体内实际情况,得到的蛋白可信度高。但这种方法有两个缺陷:一是两种蛋白质的结合可能不是直接结合,而可能有第三者在中间起桥梁作用;二是必须在实验前预测目的蛋白是什么,以选择最后检测的抗体,所以,若预测不正确,实验就得不到结果,方法本身具有冒险性。七、pull-down技术蛋白质相互作用的类型有牢固型相互作用和暂时型相互作用两种。牢固型相互作用以多亚基蛋白复合体常见,最好通过免疫共沉淀(Co-IP)、Pull-down技术或Far-western法研究。Pull-down技术用固相化的、已标记的饵蛋白或标签蛋白(生物素-、PolyHis-或GST-),从细胞裂解液中钓出与之相互作用的蛋白。通过Pull-down技术可以确定已知的蛋白与钓出蛋白或已纯化的相关蛋白间的相互作用关系,从体外传路或翻译体系中检测出蛋白相互作用关系。
[size=5]求助有关金属与蛋白质相互作用的中文文献[/size]
用荧光做有关药物与蛋白质相互作用,对药物有什么限制,比如光谱性质,药物发挥作用的机制,对于做这方面研究的意义我其实也不太明白,有大侠给点指导[em06]
记者前天从中科院上海药物所获悉,该所蒋华良研究员等发明出一套预测蛋白质—蛋白质相互作用的新方法,预测精确性大于80%。这项计算生物学重要成果发表于国际著名期刊《美国科学院院刊》(PNAS)本月在线版上。 蛋白质-蛋白质相互作用(PPI)决定着几乎所有的生物功能。目前,大多数蛋白质相互作用预测法都依赖于大量同源蛋白信息或蛋白相互作用标识物信息,应用范围有限;而新方法可仅依据蛋白质的序列信息,研究任意新蛋白的功能,或预测老蛋白的新功能,并可用于新药设计,对基因组研究也具有十分重要的意义。研究人员经过两年努力,用超过1.6万对实验测定了蛋白质相互作用结果,构建出通用性PPI预测模型
[font=宋体]蛋白质纯化系统是一种用于从混合物中纯化目标蛋白的设备和方法。它结合了多种技术和步骤,可以有效地分离和纯化蛋白质,提供高纯度和高活性的目标蛋白。蛋白质纯化系统是实现蛋白质纯化的关键装置,它结合了各种分离、富集和纯化方法,帮助科研工作者实现蛋白质的高纯度提取。[/font][font=宋体] [/font][font=宋体][b]蛋白质纯化系统的基本原理[/b][/font][font=宋体]蛋白质纯化系统主要依据蛋白质的特性利用不同的物理化学方法进行分离和纯化。下面将介绍几种常见的蛋白质纯化系统的基本原理。[/font][font=宋体] [/font][font=宋体][font=宋体]①[url=https://cn.sinobiological.com/resource/protein-review/protein-purification-by-ac][b]亲和层析[/b][/url][/font][/font][font=宋体]亲和层析是一种基于蛋白质的特异性与配体的亲和性相互作用来实现分离和纯化的方法。在亲和层析过程中,蛋白质溶液通过填充有配体的柱子,与配体结合形成复合物,而非特异性结合的其他组分被洗脱。最后,通过改变条件来破坏蛋白质与配体的结合,从而使得目标蛋白质得以纯化。[/font][font=宋体] [/font][font=宋体]②凝胶过滤层析[/font][font=宋体]凝胶过滤层析是一种基于蛋白质大小差异来进行分离的方法。在凝胶过滤层析中,待纯化的蛋白质溶液通过一系列的凝胶层析柱,大分子的蛋白质不能进入凝胶颗粒的内部,而小分子的蛋白质则可以进入凝胶颗粒内部。通过调整凝胶的孔径,可以实现对目标蛋白质的选择性分离和纯化。[/font][font=宋体] [/font][font=宋体][font=宋体]③[url=https://cn.sinobiological.com/resource/protein-review/protein-purification-by-iec][b]离子交换层析[/b][/url][/font][/font][font=宋体][font=宋体]离子交换层析是一种基于蛋白质与固定在柱子上的离子交换基的电荷相互作用来实现分离和纯化的方法。在离子交换层析中,蛋白质溶液通过带有离子交换基的柱子,与柱子上的离子交换基之间发生相互作用。通过改变溶液的离子浓度和[/font][font=Calibri]pH[/font][font=宋体]值,可以实现对蛋白质的选择性吸附和洗脱。[/font][/font][font=宋体] [/font][font=宋体]④逆流层析[/font][font=宋体]逆流层析是一种基于分子质量和电荷差异来实现蛋白质分离和纯化的方法。在逆流层析中,蛋白质溶液通过填充有逆流层析介质的柱子,溶液在反向流动的情况下通过层析柱。由于不同蛋白质之间的分子质量和电荷差异,它们在逆流层析介质中的移动速度不同,从而实现对蛋白质的分离和纯化。[/font][font=宋体] [/font][font=宋体][b]蛋白质纯化系统的应用[/b][/font][font=宋体]蛋白质纯化系统在生物医药领域有着广泛的应用,下面将介绍几个常见的应用场景。[/font][font=宋体] [/font][font=宋体]①药物研发[/font][font=宋体]蛋白质纯化系统在药物研发中起到了非常重要的作用。通过蛋白质纯化系统,科研人员可以从复杂的生物样品中高效纯化出目标蛋白质,为药物研发提供了可靠的原料和工具。蛋白质纯化系统不仅可以提高药物研发的效率,还可以确保药物的纯度和质量,从而提高药物的疗效和安全性。[/font][font=宋体] [/font][font=宋体]②生物学研究[/font][font=宋体]在生物学研究中,蛋白质纯化系统被广泛应用于蛋白质相互作用研究、蛋白质结构解析和功能分析等方面。通过蛋白质纯化系统,科研人员可以从不同的细胞和组织中提取目标蛋白质,进一步研究它们之间的相互关系和作用机制。蛋白质纯化系统还可以用于蛋白质结构解析,帮助科学家揭示蛋白质的三维结构以及其功能。[/font][font=宋体] [/font][font=宋体]③临床诊断[/font][font=宋体]蛋白质纯化系统在临床诊断中也起到了重要的作用。通过蛋白质纯化系统,医生可以从患者的生物样本中纯化出特定的蛋白质标志物,用于疾病早期诊断、病情监测和治疗评估等方面。蛋白质纯化系统在临床诊断中的应用可以帮助医生及早发现疾病,提高诊断的准确性和效率。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体]蛋白质纯化系统是实现蛋白质纯化的重要装置,它结合了多种分离、富集和纯化方法,帮助科研人员高效地提取目标蛋白质。蛋白质纯化系统的应用广泛,不仅在药物研发、生物学研究和临床诊断等领域发挥重要作用,还为科学家揭开蛋白质的结构和功能提供了有力的支持。通过不断的技术创新和优化,蛋白质纯化系统将更好地满足科研和临床的需求,推动生物医药领域的发展。[/font][font=Calibri] [/font]
朊蛋白与免疫系统相互作用的新发现http://www.bioon.com/biology/UploadFiles/201112/2011123113381385.jpg 12月29日,据《每日科学》报道,痒病是一种神经退行性疾病,它可以作为其他由蛋白积累致组织畸形(蛋白质病)疾病的模型,如阿尔兹海默氏病和帕金森氏病。有关这些基因的许多问题仍然悬而未决。在一个新的博士论文研究中,发现了数个与阮蛋白(PrPSc,与疾病的发展有关)摄取相关的因子以及朊蛋白是如何与肠道内的免疫细胞相互作用。 羊瘙痒病属于一组被称为"传染性海绵状脑病(TSE)"的疾病,因为它们可以在动物个体之间传播,并导致大脑产生海绵状、退行性改变。这些疾病不仅折磨羊,还折磨牛(牛海绵状脑病,又称疯牛病,BSE)、鹿(鹿慢性消耗性疾病,又称疯鹿病,CWD)以及人类(克雅氏病CJD)。它们在一定程度上也可以在物种见传播,在20世纪90年代,超过200人经由食物感染而患上了克雅氏病。 传染性海绵状脑病(TSE),或者称阮病毒疾病,被认为是感染了一种能致病的蛋白质变体--朊蛋白,它是机体细胞的正常组成部分,在脑中含量最为丰富。一般而言,阮病毒疾病可能是传染的、遗传的或偶发/自发的。当正常的朊蛋白突变成致病的变种,疾病便发生了,变种朊蛋白在空间结构上与健康的朊蛋白不同。由于变种的朊蛋白具有不同的空间结构,机体细胞很难降解它,因此它就一直在积累。 因为朊蛋白(PrPSc)是在疾病早期在肠道系统的淋巴组织中被发现,推测它是经由肠胃道传染。在兽医学家Caroline Piercey Akesson博士研究杂交仪期间,研究了朊蛋白在肠道内的吸收,从而对疾病发展的早期阶段所发生的过程有了新的了解。与早先的推测相反,她通过免疫电镜证明阮蛋白不是直接从肠道转运到肠道相关的的淋巴组织。相反,她发现朊蛋白自由地穿过或穿进肠道淋巴组织之外的淋巴细胞。 树突状细胞据推测发挥着"看门人"的作用,它决定机体能容忍什么以及当面对外来物时该策划哪一种免疫防御反应。Akeeson的目标之一就是树突细胞与朊蛋白摄取之间的相互作用。首先,需要了解正常的羊肠道内树突状细胞的特点;其次,去调查哪一类型的细胞与阮病毒的摄取有关。 她的研究结果表明,不是树突状细胞,而是巨噬细胞负责朊蛋白的摄取。Akesson的研究揭示,朊蛋白利用了肠道中大分子物质摄取的正常生理通道,这可能对机体的免疫监视系统有显著影响。一个可能的后果就是免疫耐受被激活,从而阻碍了肠道对所吸收的朊蛋白的正常免疫反应。 今后的研究能够揭示免疫细胞是如何运输朊蛋白及机体是如何处理朊蛋白,这将具有非常重要的意义,不仅是为了提供更多的关于痒病的知识,还为研究人类和其他动物中神经退行性蛋白质病提供重要见解。 Caroline Piercey Akesson于12月20日在挪威兽医科学系进行了博士论文答辩,论文的题目是:研究阮病毒的摄取及其与羊肠道中免疫细胞的早期相互作用。
褚福亮,王福生, 中国人民解放军第302医院全军艾滋病与病毒性肝炎重点实验室 北京市 100039项目负责人 王福生, 100039 ,北京市丰台路26号, 中国人民解放军第302医院全军艾滋病与病毒性肝炎重点实验室. fswang@public.bta.net.cn电话:010-66933332 传真:010-63831870收稿日期 2002-08-15 接受日期 2002-09-03摘要新近广泛应用蛋白质芯片(ProteinChipâ Array)系统成功鉴定出了一些重要疾病(如肿瘤和危害性较大的传染病)新的、特异性的生物标记(biomarkers),后者不仅在生物医学的基础方面具有重要的科学价值,而且在临床疾病的诊断、治疗和预防发挥重要的指导作用,显示了良好的发展前景.本文就表面增强的激光解析电离-飞行时间-质谱(SELDI-TOF-MS)相关的原理、特点、在临床和基础研究中的应用新进展和未来的发展趋势做一综述.此外,我们就蛋白质谱分析技术在病毒性肝炎、肝硬化和肝癌等一系列肝病方面的应用策略和前景进行了分析.褚福亮,王福生. 蛋白质谱分析方法特点及其在蛋白组学研究领域中的应用.世界华人消化杂志 2002 10(12):1431-14350 引言人类基因组计划已经进入后基因组时代-即功能基因组时代[1],作为基因功能的直接体现者-蛋白质,及其之间的相互作用越来越引起基础和临床科学家们的关注[2-6] .因为要彻底了解生命的本质,只把基因测出来还是不够的,还必须要了解其在生物生长、发育、衰老和整个生命过程中的功能、不同蛋白质之间的相互作用以及他们与疾病发生、发展和转化的规律[7-14] .正因为如此,有关上述问题的蛋白质组学研究成了今天生命科学最重要的焦点之一[15] .为了阐明蛋白质在上述生命现象中的作用和相关机制,人们设计了许多新的方法技术,如:二维电泳、质谱分析、微距阵列、酵母双杂交和噬菌体展示等,这些方法在一些特定的情况下,虽然显示出了他们各自不同的优点,但是同样也存在着较大的局限性,难以开展大规模、超微量、高通量、全自动筛选蛋白质等方面的分析,因而设计更全面、同时研究多种蛋白质相互作用的技术,在功能基因组和蛋白组学的研究中建立一个更有效的技术平台,成为本领域中优先关注的问题[16] .近来,美国Ciphergen(赛弗吉)公司研制的ProteinChipâ Array的仪器,并建立了一种新的蛋白质飞行质谱-表面增强的激光解析离子化-飞行时间-质谱(surface-enhanced laser desorption/inionation-time of flight-mass spectra, SELDI-TOF-MS),已取得可喜的进展,筛选出了许多与疾病相关的新型生物标志,不仅为临床疾病的诊断和治疗等提供了新的选择,而且在基础科学、新药研制和疾病预防等方面具有广泛的应用前景[16-18] .本文就SELDI-TOF-MS相关的原理、特点、在临床和基础研究中的应用新进展和未来的发展趋势做一综述.1 ProteinChipâ Array系统和SELDI-TOF-MS的特点1.1 蛋白质芯片系统的组成和原理 蛋白质芯片系统由三部分组成:蛋白质芯片、芯片阅读器和芯片软件.供研究用芯片上有6-10芯池,不同的芯片表面上的化学物质不同,芯片表面分为两大类:一类为化学类表面,包括经典的色谱分析表面,如:结合普通蛋白质的正相表面,用于反相捕获的疏水表面,阴阳离子交换表面和捕获金属结合蛋白的静态金属亲合捕获表面;另一类称为生物类,特定的蛋白质共价结合于预先活化的表面阵列,可以用来研究传统的抗体一抗原反应,DNA和蛋白质作用,受体、配体作用和其他的一些分子之间的相互作用[19] . 根据检测目的不同,可以选用不同的芯片,或者自己设计芯片.将样本和对照点到芯池上以后,经过一段时间的结合反应,用缓冲液或水洗去一些不结合的非特异分子,再加上能量吸收分子(energy absorbing molelule,EAM)溶液,使样本固定在芯片表面.当溶液干燥后,一个含有分析物和大量能量吸收分子“晶体”就形成了.能量吸收分子对于电离来说非常重要.经过以上步骤,就可经把芯片放到芯片阅读器中进行质谱分析. 在阅读器的固定激光束下,芯片上、下移动,使样本上每一个特定点都被“读”到.激光束的每一次闪光释放的能量都聚集在该区一个非常小的点上(focused laser beam,聚焦激光束).这样,每个区都含有丰富的,可寻址(addressable)的位置.蛋白质芯片处理软件精确控制激光寻读过程.当样本受到激发,就开始电离和解除吸附.不同质量的带电离子在电场中飞行的时间长短不同,计算检测到的不同时间,就可以得出质量电荷比,把他输入电脑,形成图像[19].Ball et al [20]采用一种称为人工神经网络(artifical neural network,ANN)的算法处理出现的成千上万的峰,鉴定出三个分子量为13 454、13 457和14 278的生物标记分子,使疾病预测率达到97.1 %.1.2 ProteinChipâ Array芯片和SELDI-TOF-MS的特点 新型蛋白芯片与以往的蛋白芯片不同之处:SELDI-TOF-MS,他是在MALDI(matrix-assisted laser desorption/inionation)[21,22]基础上,改进后实行表面增强的飞行质谱.SELDI-TOF-MS优于MALDI-TOF表现为他不会破坏蛋白质,或使样本与可溶的基质共结晶来产生质谱信号.对SELDI-TOF来说,可以直接将血清、尿液、组织抽取物等不需处理直接点样检测[40] 由于一部分非特异结合的分析物被洗去,因而出现的质峰非常一致,有利于后期分析[23,24] . 与二维电泳相比:二维电泳分析蛋白质的分子量在30 KDa以上时电泳图谱较清楚,对在组织抽提物中占很大比例的低丰度的蛋白质不能被检出;其次,二维电泳胶上的蛋白质斑点很大一部分包含一种以上的蛋白质;而且,二维电泳耗时长,工作量大,对象染色转移等技术要求高,不能完全实现自动化.而SELDI-TOF在200 Da-500 KDa区间都可以给出很好的质谱,对一个样本的分析在几十分钟内就可以完成[19],处理的信息量远远大于二维电泳;对于低丰度物质,即使浓度仅attomole(10-18)的分子,只要与表面探针结合,就可以检测到,这也是二维电泳所不具备的[24,25] . 对于微距阵蛋白芯片来说,需要一种不破坏折叠的蛋白质构象的固定技术,再与另外的蛋白质反应,经检测莹光来观察蛋白质之间的作用[26] .而基于SELDI-TOF-MS的ProteinChip分析蛋白质不需溶解、不需染色、廉价、针对性强. 因而蛋白质芯片仪具有以下优势:(1)可直接使用粗样本,如:血清、尿液、细胞抽提物等[27] .(2)使大规模、超微量、高通量、全自动筛选蛋白质成为可能;(3)他不仅可发现一种蛋白质或生物标记分子,而且还可以发现不同的多种方式的组合蛋白质谱,可能与某种疾病有关[28] (4)推动基因组学发展,验证基因组学方面的变化,基于蛋白质特点发现新的基因.可以推测疾病状态下,基因启动何以与正常状态下不同,受到那些因素的影响,从而跟踪基因的变化[2,14,15] . 其存在的问题:对于不同的样本,根据检测的目标采取或者设计几种芯片,理论上可以把所有的相同性质蛋白质捕获,但是实际上仍有少量的分子没与表面探针结合.使用SELDI-TOF-MS,仅能给出蛋白质的分子量,不能给出C端、N端的序列,也没法知道蛋白质的构型,因此需要将蛋白质充分纯化后,用蛋白酶消化芯片上的蛋白质,分析肽段,再用生物信息学方法鉴定蛋白质序列[18,24] .另外,在国内,该芯片费用较高,分析质谱需要大量后续工作支持.
[font=宋体]离子交换层析是一种在生物化学和生物技术领域中广泛使用的分离和纯化技术。它基于离子间的相互作用,特别是离子与固定在层析介质上的带电基团之间的相互作用,从而实现对混合物中不同离子的分离。以下将详细介绍离子交换层析的步骤及其作用。[/font][font=宋体] [/font][b][font=宋体]一、步骤[/font][/b][font=宋体][font=Calibri]1[/font][font=宋体]、预处理:在开始离子交换层析之前,通常需要对样品进行预处理,以去除大颗粒杂质和不需要的成分。这通常包括离心、过滤和可能的浓缩步骤。[/font][/font][font=宋体][font=Calibri]2[/font][font=宋体]、选择合适的离子交换剂:离子交换剂是层析过程的核心。根据待分离离子的性质(如电荷、大小和与交换剂的亲和力)选择合适的离子交换剂。常见的离子交换剂包括阳离子交换剂和阴离子交换剂。[/font][/font][font=宋体][font=Calibri]3[/font][font=宋体]、平衡离子交换剂:在将样品加载到离子交换柱之前,需要用适当的平衡溶液(通常是水或盐溶液)冲洗离子交换剂,以去除可能存在的杂质并确保离子交换剂处于最佳状态。[/font][/font][font=宋体][font=Calibri]4[/font][font=宋体]、加载样品:将预处理过的样品加载到离子交换柱上。样品中的离子会与离子交换剂上的带电基团发生相互作用。[/font][/font][font=宋体][font=Calibri]5[/font][font=宋体]、洗脱:用洗脱液(通常是盐溶液,其浓度逐渐增加)将结合的离子从离子交换剂上洗脱下来。这一步骤是离子交换层析中最为关键的一步,因为它决定了不同离子之间的分离效果。[/font][/font][font=宋体][font=Calibri]6[/font][font=宋体]、收集和分析:收集洗脱下来的各个组分,并进行分析,以确定每个组分中包含的离子种类和浓度。常见的分析方法包括电导率测量、紫外[/font][font=Calibri]-[/font][font=宋体]可见光谱和质谱等。[/font][/font][font=宋体][font=Calibri]7[/font][font=宋体]、后处理:根据需要对收集到的组分进行进一步的处理,如浓缩、脱盐或重新配制等。[/font][/font][b][font=宋体] [/font][font=宋体]二、作用[/font][/b][font=宋体]离子交换层析在生物化学和生物技术领域有着广泛的应用,主要作用包括:[/font][font=宋体] [/font][font=宋体][font=Calibri]1[/font][font=宋体]、分离和纯化蛋白质:离子交换层析可用于从复杂的混合物中分离和纯化蛋白质,这对于后续的生物化学研究和药物开发至关重要。[/font][/font][font=宋体][font=Calibri]2[/font][font=宋体]、去除杂质:离子交换层析能够有效地去除样品中的离子杂质,提高样品的纯度。[/font][/font][font=宋体][font=Calibri]3[/font][font=宋体]、样品制备:在进行其他分析或实验之前,离子交换层析可用于样品的制备和预处理。[/font][/font][font=宋体][font=Calibri]4[/font][font=宋体]、研究蛋白质与离子的相互作用:通过离子交换层析,可以研究蛋白质与不同离子之间的相互作用和亲和力,这对于理解蛋白质的生物学功能和调控机制具有重要意义。[/font][/font][font=宋体] [/font][b][font=宋体][font=宋体]三[/font] [font=宋体]、应用领域[/font][/font][/b][font=宋体]离子交换层析法在许多领域得到广泛应用:[/font][font=宋体]●生物制药:用于药物蛋白质的纯化,确保生物制剂的质量和稳定性。[/font][font=宋体]●生物学研究:在分离和纯化特定电荷性质的蛋白质时被广泛使用,尤其在基因表达和蛋白质互作研究中。[/font][font=宋体]●食品工业:用于提取和纯化食品中的蛋白质,改善食品的质地和口感。[/font][font=宋体]●环境监测:可用于从环境样品中分离和检测特定蛋白质,例如水体中的生物标志物。离子交换层析法凭借其良好的选择性和高效性,是生物分离和纯化领域不可或缺的重要工具。[/font][font=宋体] [/font][font=宋体][font=宋体]更多详情可以关注:[url=https://cn.sinobiological.com/resource/protein-review/protein-purification-by-iec][b]离子交换层析蛋白纯化[/b][/url][/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/protein-purification-by-iec[/font][/font][b][font=宋体] [/font][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b]
基因组(genome)包含的遗传信息经转录产生mRNA,一个细胞在特定生理或病理状态下表达的所有种类的mRNA称为转录子组(transcriptome)。很显然,不同细胞在不同生理或病理状态下转录子组包含的mRNA的种类不尽相同。mRNA经翻译产生蛋白质,一个细胞在特定生理或病理状态下表达的所有种类的蛋白质称为蛋白质组(proteome)。同理,不同细胞在不同生理或病理状态下所表达的蛋白质的种类也不尽相同。蛋白质是基因功能的实施者,因此对蛋白质结构,定位和蛋白质-蛋白质相互作用的研究将为阐明生命现象的本质提供直接的基础。生命科学是实验科学,因此生命科学的发展极大地依赖于实验技术的发展。以DNA序列分析技术为核心的基因组研究技术推动了基因组研究的日新月异,而以基因芯片技术为代表的基因表达研究技术为科学家了解基因表达规律立下汗马功劳。在蛋白质组研究中,二维电泳和质谱技术的黄金组合又为科学家掌握蛋白质表达规律再铸辉煌。蛋白质组学(proteomics)就是指研究蛋白质组的技术及这些研究得到的结果。蛋白质组学的研究试图比较细胞在不同生理或病理条件下蛋白质表达的异同,对相关蛋白质进行分类和鉴定。更重要的是蛋白质组学的研究要分析蛋白质间相互作用和蛋白质的功能。蛋白质组学的研究内容包括:1.蛋白质鉴定:可以利用一维电泳和二维电泳并结合Western等技术,利用蛋白质芯片和抗体芯片及免疫共沉淀等技术对蛋白质进行鉴定研究。2.翻译后修饰:很多mRNA表达产生的蛋白质要经历翻译后修饰如磷酸化,糖基化,酶原激活等。翻译后修饰是蛋白质调节功能的重要方式,因此对蛋白质翻译后修饰的研究对阐明蛋白质的功能具有重要作用。3.蛋白质功能确定:如分析酶活性和确定酶底物,细胞因子的生物分析/配基-受体结合分析。可以利用基因敲除和反义技术分析基因表达产物-蛋白质的功能。另外对蛋白质表达出来后在细胞内的定位研究也在一定程度上有助于蛋白质功能的了解。Clontech的荧光蛋白表达系统就是研究蛋白质在细胞内定位的一个很好的工具。4.对人类而言,蛋白质组学的研究最终要服务于人类的健康,主要指促进分子医学的发展。如寻找药物的靶分子。很多药物本身就是蛋白质,而很多药物的靶分子也是蛋白质。药物也可以干预蛋白质-蛋白质相互作用。在基础医学和疾病机理研究中,了解人不同发育、生长期和不同生理、病理条件下及不同细胞类型的基因表达的特点具有特别重要的意义。这些研究可能找到直接与特定生理或病理状态相关的分子,进一步为设计作用于特定靶分子的药物奠定基础。不同发育、生长期和不同生理、病理条件下不同的细胞类型的基因表达是不一致的,因此对蛋白质表达的研究应该精确到细胞甚至亚细胞水平。可以利用免疫组织化学技术达到这个目的,但该技术的致命缺点是通量低。LCM技术可以精确地从组织切片中取出研究者感兴趣的细胞类型,因此LCM技术实际上是一种原位技术。取出的细胞用于蛋白质样品的制备,结合抗体芯片或二维电泳-质谱的技术路线,可以对蛋白质的表达进行原位的高通量的研究。很多研究采用匀浆组织制备蛋白质样品的技术路线,其研究结论值得怀疑,因为组织匀浆后不同细胞类型的蛋白质混杂在一起,最后得到的研究数据根本无法解释蛋白质在每类细胞中的表达情况。虽然培养细胞可以得到单一类型细胞,但体外培养的细胞很难模拟体内细胞的环境,因此这样研究得出的结论也很难用于解释在体实际情况。因此在研究中首先应该将不同细胞类型分离,分离出来的不同类型细胞可以用于基因表达研究,包括mRNA和蛋白质的表达。LCM技术获得的细胞可以用于蛋白质样品的制备。可以根据需要制备总蛋白,或膜蛋白,或核蛋白等,也可以富集糖蛋白,或通过去除白蛋白来减少蛋白质类型的复杂程度。相关试剂盒均有厂商提供。蛋白质样品中的不同类型的蛋白质可以通过二维电泳进行分离。二维电泳可以将不同种类的蛋白质按照等电点和分子量差异进行高分辨率的分离。成功的二维电泳可以将2000到3000种蛋白质进行分离。电泳后对胶进行高灵敏度的染色如银染和荧光染色。如果是比较两种样品之间蛋白质表达的异同,可以在同样条件下分别制备二者的蛋白质样品,然后在同样条件下进行二维电泳,染色后比较两块胶。也可以将二者的蛋白质样品分别用不同的荧光染料标记,然后两种蛋白质样品在一块胶上进行二维电泳的分离,最后通过荧光扫描技术分析结果。胶染色后可以利用凝胶图象分析系统成像,然后通过分析软件对蛋白质点进行定量分析,并且对感兴趣的蛋白质点进行定位。通过专门的蛋白质点切割系统,可以将蛋白质点所在的胶区域进行精确切割。接着对胶中蛋白质进行酶切消化,酶切后的消化物经脱盐/浓缩处理后就可以通过点样系统将蛋白质点样到特定的材料的表面(MALDI-TOF)。最后这些蛋白质就可以在质谱系统中进行分析,从而得到蛋白质的定性数据;这些数据可以用于构建数据库或和已有的数据库进行比较分析。实际上像人类的血浆,尿液,脑脊液,乳腺,心脏,膀胱癌和磷状细胞癌及多种病原微生物的蛋白质样品的二维电泳数据库已经建立起来,研究者可以登录www.expasy.ch/www/tools.html等网站进行查询,并和自己的同类研究进行对比分析。Genomic Solution可以为研究者提供除质谱外的所有蛋白质组学研究工具,包括二维电泳系统,成像系统及分析软件,胶切割系统,蛋白质消化浓缩工作站,点样工作站等;同时还可以提供相关试剂和消耗品。LCM-二维电泳-质谱的技术路线是典型的一条蛋白质组学研究的技术路线,除此以外,LCM-抗体芯片也是一条重要的蛋白质组学研究的技术路线。即通过LCM技术获得感兴趣的细胞类型,制备细胞蛋白质样品,蛋白质经荧光染料标记后和抗体芯片杂交,从而可以比较两种样品蛋白质表达的异同。Clontech最近开发了一张抗体芯片,可以对378种膜蛋白和胞浆蛋白进行分析。该芯片同时配合了抗体芯片的全部操作过程的重要试剂,包括蛋白质制备试剂,蛋白质的荧光染料标记试剂,标记体系的纯化试剂,杂交试剂等。对于蛋白质相互作用的研究,酵母双杂交和噬菌体展示技术无疑是很好的研究方法。Clontech开发的酵母双杂交系统和NEB公司开发的噬菌体展示技术可供研究者选用。关于蛋白质组的研究,也可以将蛋白质组的部分或全部种类的蛋白质制作成蛋白质芯片,这样的蛋白质芯片可以用于蛋白质相互作用研究,蛋白表达研究和小分子蛋白结合研究。Science,Vol.293,Issue 5537,2101-2105,September 14,2001发表了一篇关于酵母蛋白质组芯片的论文。该文主要研究内容为:将酵母的5800个ORF表达成蛋白质并进行纯化点样制作芯片,然后用该芯片筛选钙调素和磷脂分子的相互作用分子。最后有必要指出的是,传统的蛋白质研究注重研究单一蛋白质,而蛋白质组学注重研究参与特定生理或病理状态的所有的蛋白质种类及其与周围环境(分子)的关系。因此蛋白质组学的研究通常是高通量的。适应这个要求,蛋白质组学相关研究工具通常都是高度自动化的系统,通量高而速度快,配合相应分析软件和数据库,研究者可以在最短的时间内处理最多的数据。
云唐蛋白质检测仪是一种用于测定食品、生物样品等中蛋白质含量的仪器设备。它在食品科学、生物学、医学和生化等领域具有重要作用,以下是其主要作用: 食品质量控制: 在食品工业中,蛋白质是食品的主要组分之一,其含量影响着食品的口感、质地、营养价值等。蛋白质检测仪可以用于监测食品样品中的蛋白质含量,确保产品的质量稳定性和一致性。 生物学研究: 在生物学研究中,蛋白质是细胞功能和结构的重要组成部分。蛋白质检测仪可以帮助研究人员测定生物样品(如细胞提取物、血清等)中蛋白质含量,从而深入了解细胞的生物学特性和疾病机制。 医学诊断: 在临床医学中,某些疾病的发展可能会导致血清蛋白质含量的改变。蛋白质检测仪可以用于测定血液和尿液中的蛋白质含量,帮助医生进行疾病诊断和监测。 药物研发: 药物研发过程中,蛋白质的定量分析是评估药物效果的重要环节。蛋白质检测仪可以用于分析药物与蛋白质的相互作用,评估药物对蛋白质的影响。 生化实验: 在生化实验室中,蛋白质检测仪常用于定量测定蛋白质样品,用于分析实验数据和评估实验结果的可靠性。 环境监测: 在环境科学领域,蛋白质检测仪可以用于监测水体、土壤等环境中蛋白质的含量,从而评估环境质量。
英国科学家已经研发出了一种新方法,利用“智能材料”来使蛋白质结晶,这种智能材料能记住分子的形状和“性格”。科学家们表示,发表于6月20日《美国国家科学院院刊》上的这项最新技术,有望通过帮助科学家确定靶向蛋白的结构从而研发出新药。 研发新药的过程一般如下:科学家们会先找出一个与疾病有关的蛋白质;接着设计出一个能同该蛋白质相互作用的分子,来刺激或者阻止该蛋白质的功能。为了做到这一点,需要首先了解目标蛋白质的结构。 一项名为X射线晶体学的技术能被用来分析一个蛋白质晶体内原子的排列,但是,让蛋白质从溶液中析出并形成晶体是一个主要的障碍。随着科学家们在基因组学和蛋白质组学领域不断取得新进展,可以作为潜在靶向药物的蛋白质的数量呈指数级增加,科学家们使用了很多蛋白质进行试验,然而目前的方法获得有用晶体的成功率不足20%。
曲拉通X-114溶液分析蛋白质应选用那种分析柱,我用C8柱,但是谱图基线不稳定,可能是强保留性物质,请专家高手为小弟分析原因,看选择那种柱子合适! 十分感谢!
能不能用NMR来测定蛋白质水溶液中氢键强度的变化抑或说,在蛋白质的变性过程中,氢键强度能不能够测定?并且能用某种试剂完全屏蔽氢键的作用吗。。
我将需要浓缩的蛋白质溶液在-20℃下冷冻20h后在室温下冷却,结果蛋白质形成絮状析出,而且析出的蛋白质能用砂芯过滤器过滤得到比较干的滤饼。这样等到的蛋白质变性了吗?低温可使蛋白质浓缩凝胶析出,这样的蛋白质与之前没处理的蛋白质溶液相比变性了吗?
蛋白质折叠病 ▲许多疾病,如阿兹海默症(Alzheimer's),疯牛病(Mad Cow, BSE),可传播性海绵状脑病(CJD),肌萎缩性脊髓侧索硬化症(ALS),还有帕金森氏症(Parkinson's)等正是由于一些细胞内的重要蛋白发生突变,导致蛋白质聚沉或错误折叠而造成的。因此,深入了解蛋白质折叠与错误折叠的关系对于这些疾病的致病机制的阐明以及治疗方法的寻找将大有帮助。 ▲基因组序列的发展使我们得到了大量的蛋白质序列,结构信息的获得对于揭示它们的生物学功能是十分重要的。依靠现有手段(X-ray晶体衍射、NMR及电镜)测定蛋白质的结构需要较长的时间,因此结构解析的步伐已落后于发现新蛋白的步伐。而结构预测的方法虽然速度较快,但可靠性并不高,只有当我们对于维持蛋白质结构,驱动蛋白质折叠的理化因素更为了解,这一方法才可能有根本的改进。另外,我们对于蛋白质相互作用、配体与蛋白质的作用等结构与功能关系的研究也有赖于蛋白质折叠机制的阐明。【蛋白质折叠与“折叠病” 】 人们对由于基因突变造成蛋白质分子中仅仅一个氨基酸残基的变化就引起疾病的情况已有所了解,即所谓“分子病”,如地中海镰刀状红血球贫血症就是因为血红蛋白分子中第六位的谷氨酸突变成了颉氨酸。现在则发现蛋白质分子的氨基酸序列没有改变,只是其结构或者说构象有所改变也能引起疾病,那就是所谓“构象病”,或称“折叠病”。 大家都知道的疯牛病,它是由一种称为Prion的蛋白质的感染引起的,这种蛋白质也可以感染人而引起神经系统疾病。在正常机体中,Prion是正常神经活动所需要的蛋白质,而致病Prion与正常Prion的一级结构完全相同,只是空间结构不同。这一疾病的研究涉及到许多生物学的基本问题。一级结构完全相同的蛋白质为什么会有不同的空间结构,这与Anfinsen原理是否矛盾?显然这里有蛋白质的能量和稳定性问题。 从来认为蛋白结构的变化来自于序列的变化,而序列的变化来自于基因的变化,生命信息从核酸传递到蛋白。而致病Prion的信息已被诺贝尔奖获得者普鲁辛纳证明不是来自基因的变化,致病蛋白Prion导致正常蛋白Prion转变为致病的折叠状态是通过蛋白分子间的作用而感染!这种相互作用的本质和机制是什么?仅仅改变了折叠状态的分子又如何导致严重的疾病?这些问题都不能用传统的概念给予满意的解释,因此在科学界引起激烈的争论,有关研究的强度和竞争性也随之大大增强。 由于蛋白质折叠异常而造成分子聚集甚至沉淀或不能正常转运到位所引起的疾病还有老年性痴呆症、囊性纤维病变、家族性高胆固醇症、家族性淀粉样蛋白症、某些肿瘤等等。由于分子伴侣在蛋白质折叠中至关重要的作用,分子伴侣本身的突变显然会引起蛋白质折叠异常而引起折叠病。随着蛋白质折叠研究的深入,人们会发现更多疾病的真正病因和更针对性的治疗方法,设计更有效的药物。现在发现有些小分子可以穿越细胞作为配体与突变蛋白结合,从而使原已失去作战能力的突变蛋白逃逸“蛋白质质量控制系统”而“带伤作战”。这种小分子被称为“药物分子伴侣”,有希望成为治疗“折叠病”的新药。 新生肽的折叠问题或蛋白质折叠问题不仅具有重大的科学意义,除了上面提到的在医学上的应用价值外,在生物工程上具有极大的应用价值。基因工程和蛋白工程已经逐渐发展成为产值以数十亿美元计的大产业,进入21世纪后,还将会有更大的发展。但是当前经常遇到的困难,是在简单的微生物细胞内引入异体DNA后所合成的多肽链往往不能正确折叠成为有生物活性的蛋白质而形成不溶解的包含体或被降解。这一“瓶颈”问题的彻底解决有待于对新生肽链折叠更多的认识。
蛋白质组学研究的一般工具与方法随着人类基因组计划取得巨大的成功和许多物种基因组测序的完成,仅仅靠基因组的序列来试图阐明生命现象是远远不够的,因此,研究重心已经开始从揭示生命的所有遗传信息转移到在分子整体水平对功能的研究上,生命科学已实质性地跨入了后基因组时代。 尽管现在已经有多个物种的基因组被测序,但这些基因组中通常有一半以上基因的功能是未知的。目前功能基因组研究中所采用的策略,如微阵列法(microarray)(Wodicka et al., 1997)、基因芯片(gene chips)(Ramsay et al., 1998)、基因表达序列分析(SAGE)(Velculescu et al., 1995)等,都是从细胞中mRNA的角度来考虑的。但事实上,从DNA、mRNA到蛋白质存在三个层次的调控,mRNA自身也存在着贮存、转运和降解等问题,从mRNA角度考虑,实际上仅包括了转录水平调控,并不能全面代表蛋白质表达水平。实验也证明,组织中mRNA丰度与蛋白质丰度的相关性并不好,尤其对于低丰度蛋白质来说,相关性更差。蛋白质复杂的翻译后修饰,蛋白质的亚细胞定位或迁移,蛋白质-蛋白质相互作用则几乎无法从mRNA水平来判断(曾嵘,夏其昌,2002)。新生肽链合成后存在多种加工、修饰过程,蛋白质间也存在类似于mRNA分子内的剪切、拼接,研究证明基本元件“intein”广泛存在于蛋白质中(Perler et al., 1997)。基因与其编码产物蛋白的线性对应关系只存在于新生肽链而不是最终的功能蛋白质中。 蛋白质是生理功能的执行者和生命现象的直接体现者,对蛋白质结构和功能的研究将直接阐明生命在生理或病理条件下的变化机制;蛋白质本身的存在形式和活动规律,如翻译后修饰、蛋白质间相互作用及蛋白质构象等问题,仍依赖于直接对蛋白质的研究来解决。因此要对生命的复杂活动有全面和深入的认识,必然要在整体、动态、网络的水平上对蛋白质进行研究(钱小红,贺福初,2003)。 蛋白质组学研究中常用的技术体系 方法学上,二维凝胶电泳-质谱仍然是目前最流行和可靠的技术平台(Rabilloud et al., 2000)。其一般过程是:细胞或组织样品——样品制备——二维凝胶电泳(2D-PAGE)分离蛋白质——计算机辅助分析2D-PAGE图象——对感兴趣的蛋白质进行酶解——质谱分析——数据库检索——蛋白质鉴定——分析蛋白质在细胞与组织中的表达情况。 2-D PAGE 样品制备 2D-PAGE 的操作流程基本上实现了程序化。但是,样品制备是一个非常关键与复杂的过程。成功的2D-PAGE取决于对样品中蛋白质有效的抽提和它的溶解性。与核酸不同,目前没有一种通用的方法适用于所有的蛋白质,来源不同的蛋白质都受到自身蛋白质制备方法的挑战。 正确的样品制备方法从收集样品开始时就要防止样品的裂解和被蛋白水解酶降解(Rabilloud et al., 2000)。要尽可能溶解更多的蛋白,并且在2D-PAGE过程中保持它的溶解性,阻止蛋白质的人为修饰。在样品制备过程中,各个实验室也通过实验建立了更为可行的方法。目前通过建立分步提取方法可以有效地提取出更多的蛋白质(兰彦等,2001)。另一种对蛋白质采用预分离的方法称为“多间隔电解法(multi-compartment-electrolyser)”,采用这种方法后,分辨率和胶的质量均明显改善(Herbert et al., 2000)。 但是,由于生物样品的多样性和复杂性,目前所采用的样品制备方法具有局限性。其它物质对蛋白质样品制备存在干扰。核酸通过与蛋白质结合,增加样品黏度而干扰等点聚焦(IEF)分离的效果。当然,通过实验探索,采取一些措施可以减轻它的干扰。例如,在样品制备过程中加入非特异性的核酸酶或RNase与DNase的混合物,在等电聚焦时将每个胶条的电流限制在50mA以内通常可以消除其影响。脂类物质的影响可以通过利用有机溶剂的方法将其去除,但是这常常会导致蛋白质的不可逆沉淀。除了蛋白质的降解之外,糖基化是蛋白质的最重要的人工修饰,样品中的尿素在这一过程中起着非常重要的作用。样品中的尿素在降解的过程中会形成能够与蛋白质的氨基反应的氰酸盐,这种结果会导致蛋白质带有更多的正电荷。所以,在2D-PAGE中要用新鲜的尿素溶液,在等电聚焦过程中要控制温度不能太高(Beranova-Giorgianni, 2003)。但是,目前还没有一种简单有效的方法来去除样品中的多糖。 样品分离和分析 样品制备完成后运用IEF和SDS-PAGE电泳对它进行分离,常采用银染和考马斯亮兰染色即可观察到具有许多蛋白质斑点的凝胶图像。等电聚焦电泳与SDS-PAGE的具体操作步骤已经实现了程序化,均有详细操作流程参考,但是由于样品的不同,不同样品的具体条件还需要试验探索。第二相SDS-PAGE运行结束,染色完毕后,利用计算机软件对凝胶图像进行分析,如PD-QUEST软件,LIPS,HERMES,GEMINI等,对凝胶图像上的蛋白质斑点进行匹配,对图像进行数字化处理等分析(贾宇峰等,2001),对感兴趣的蛋白质采用质谱分析。 低丰度蛋白质的检测 低丰度蛋白在蛋白质组学研究中常常是人们非常感兴趣的,因为细胞或组织中的一些生物活性物质,如细胞分泌的一些活性物质,受体等表达量都非常低。按照一般电泳的上样量,这些小分子是根本看不到的,但如果单纯地增加上样量,细胞或组织中的大量表达的蛋白就会将其覆盖,而且上样量过大也会影响电泳结果。所以对这些低丰度的样品可以进行富集,富集的方法可以通过层析,如亲和层析,离子交换层析等方法,还可以通过利用样品等电点性质等方法将pH范围相近的蛋白质富集(Santoni et al., 2000; Beranova-Giorgianni, 2003)。
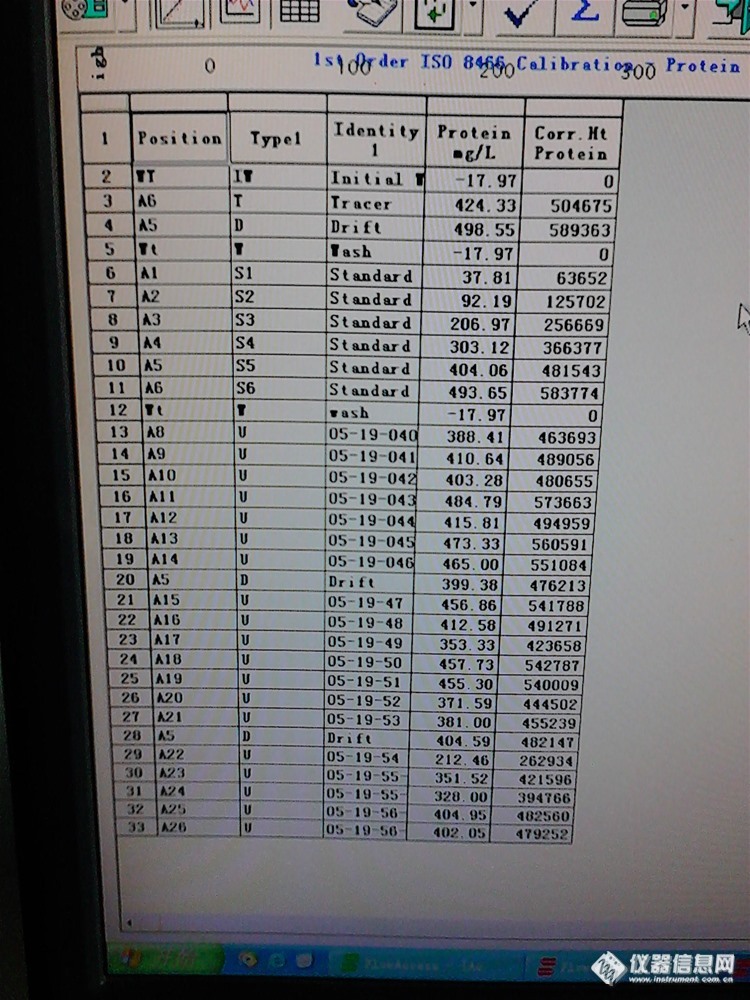
蛋白质是生命的基础 , 人体的重要组成成分。它不仅是一种重要的供能物质 , 更主要的作用是促进生长发育和新陈代谢。但婴幼儿过量的摄入蛋白质会增加 肾脏的负担,因此蛋白质的摄入要根据营养状况、生长发育要求达到供求平衡 。乳及乳制品是婴幼儿摄取蛋白质的主要来源, 安徽阜阳 “毒奶粉 ”事件就是因为婴幼儿食用了蛋白质含量极低的劣质奶粉 ,所以对乳及乳制品中蛋白质含量的监控极为重要. 目前我国测定乳及乳制品中蛋白质的方法主要为凯氏定氮滴定法、凯氏定氮比色法, 但是这两种方法繁琐、费时。连续流动分析法测定乳及乳制品中蛋白质含量,对于批量样品,该方法具有很大的优势,不但简便快捷、而且准确度和灵敏度度也有很大的提高。1.实验部分1. 1 仪器与原理SAN+ +四通道连续流动分析仪 (荷兰SKALAR公司)蛋白质分析模块。原理:自 动测定蛋白质基于改良后的贝特勒反应即经过相互分离后对氨进行分析。消化后 的样品用酸式盐溶液稀释定容,铵盐通过与水杨酸钠反应氯化为一氯化胺, 通过氧化和氧化偶合后形成绿色配合物,反应是以硝普钠为催化剂,次氯酸钠溶液被用于提供氯, 在波长630 nm处检测。1. 2样品前处理准确吸取 液态奶 (或称取固 态奶 ), 同时准备空白样 分别置于 250 mlVELP消化管中 , 加入以1: 10混匀的 CuSO4和K2SO4混合催化剂, 再加入20 ml浓 H2SO4,于蛋白质自动消化仪中消化,最后消化至蓝绿色, 冷却至室温后用蒸馏水定容至100 ml。1.3试剂和标准的配置酸性氯化钠溶液: 称取100 g氯化钠用800 ml水溶解[
physorg.com网站2007年4月13日报道:来自美国能源部Argonne国家实验室以及Notre Dame大学的科学家们最近成功的利用X射线散射技术找到了溶液中的金属离子是如何发生相互作用的。详细结果发表在最新的《Inorganic Chemistry》上。这些发现有着重要意义,因为它能帮助科学家更好了解核废料以及其它工业产物中的金属离子是如何影响环境的。 Argonne实验室的Suntharalingam Skanthakumar表示:“科学家长期以来一直有一个疑问,那就是溶液中金属离子的行为。对于这些金属相互作用的直接测量显示,在溶液体系结构和固态环境之间存在长程的交互作用和强相关性。” 而Argonne实验室的另一位科学家Lynda Soderholm则说:“我们已经掌握了关于四价水解锕类金属的详细结构和化学信息,结果表明原子相互作用细节和我们之前想象的很不一样。金属离子水解是水化学中最基本也是最重要的反应之一。” 此项研究的实验是在Argonne的APS进行的。周长1104米的APS加速器足够容纳一个棒球场,其中的复杂仪器设备能加速并储存一束电子,这作为APS的X射线源。在科学家的实验中,一束细的高能X射线来轰击溶液中的离子,当X射线被散射出来,特殊的CCD就能探测出二维的散射模式。 博士后Richard E. Wilson说:“下一步我们将分析周期表中的钍等金属,最终目标是预言金属污染物的反应状况,并确定它们对于环境的影响。”此项研究结合了多个学科的学者,包括物理学家、化学家和地质学家。来源:教育部科技发展中心网站
BIA是英语“Biomolecular Interaction Analysis” 的缩写,BIA提供了实时观察生物分子间相互作用的技术。通过它能观察两种分子结合的特异性,能知道两种分子的结合有多强,还能了解生物分子的结合过程共有多少个协同者和参与者。BIA可以让得到用其他技术方法难以得到的结果,因为它可以实时反映分子结合过程中每一秒变化的情况。无需借助标记物进行分析使BIA广泛应用于各类生物体系的测定,从各类小分子化合物、多肽、蛋白质、寡核苷酸和寡聚糖直至类脂、噬菌体、病毒和细胞。一、 动力学常数的测定BIA可以用来分析不同抗体与抗原的结合与解离常数,相对与以前其它检测抗体效价的方法,BIA不仅快速,可以准确定量,和可以让你看到整个结合和解离的动态过程。二、浓度的测量三、分子相互作用模式的研究我们想知道两分子之间相互作用的比例,结合位点,抗原决定族的位点,都可以用BIA来完成。研究突变后活力大小的变化,研究复合物形成次序等等。四、蛋白质功能分析复合物的组装可以看成研究蛋白功能的一个例子。也可以设计其它的一些实验,只要前后芯片表面的质量有变化就可以利用BIA技术来检测。详情请见:[URL=http://biotech.ustc.edu.cn/html/yiqijieshao/2006/0727/2.html]http://biotech.ustc.edu.cn/html/yiqijieshao/2006/0727/2.html[/URL]
蛋白质是荷兰科学家格里特在1838年发现的,它是生物体内一种极重要的高分子有机物。没有蛋白质就没有生命,它是与生命及与各种形式的生命活动紧密联系在一起的物质。人体的生长、发育、运动、遗传、繁殖等一切生命活动都离不开蛋白质,因此对于蛋白质的研究显得极其重要与急迫。AFM 对于蛋白质的研究是一个极好的工具,它可以测量蛋白质空间结构,表征蛋白质的结构与功能、了解分子间的相互作用等等。样品制备当用AFM对蛋白质进行观察时,样品制备很重要。蛋白质样品的制备原则与粉体材料基本相同,也需要固定到基片上,只是要研究一些活体蛋白时,必须为之提供一定的生理环境,如生理缓冲液,所以大多需要在溶液中进行研究,如成像,测定力曲线以研究其构形,构像转变等特性.所以应该选择合适的方法在固定蛋白质样品的同时仍能保持其生物特性。具体要求和方法如下:样品制备要求样品表面平整, 高度起伏≤10一20μm;表面有一定的硬度;基底面平滑;样品在基底表面要求相对均匀、分散等。样品制备过程蛋白质样品制备过程有两种方法蛋白质吸附固定法: 使用在中性条件下带负电云母片、玻璃及氧化硅为基底,将一定浓度的带正电的蛋白质溶液滴加于云母表面,蛋白便可很容易通过吸附固定吸附于云母表面蛋白质共价固定法: 在某些特定的条件下,蛋白分子需要通过共价吸附才能检测到。利用蛋白质分子上的氨基与疏基丙酸的羧基形成肽键连接的原理,进行蛋白质的固定。
我是做蛋白质SDS-PAGE电泳的。蛋白质样品用碘乙酸溶液处理后如何除去过量的碘乙酸?1、取约1 mg的总蛋白样品放入离心管中,加入1ml 6M 的尿素溶液,得到1 mg/mL的蛋白溶液。2、加入20微升1M的巯基乙醇到上述离心管中,震荡混合5秒钟。3、将上述离心管恒温在37oC条件下反应1小时 (以还原蛋白中的双硫键)。4、加入25µ L 1M新鲜配制在1M NaOH中的碘乙酸,在避光、室温条件下放置30 分钟。(烷基化将巯基保护起来) 接下来我准备做SDS-PAGE还原电泳,我不清楚样品中的过量碘乙酸对电泳有没有影响?应该怎么除掉?求高人指点![em0808][em0808][em0808][em0808][em0808]
请教:双缩脲反应测定蛋白质含量时,绘制标准曲线时需要标准蛋白溶液,标准蛋白溶液要用什么蛋白质?我见有用酪蛋白的,可以用胶原蛋白吗?谢谢……
一、 前言基因工程已令人难以置信的扩展了我们关于有机体DNA序列的认识。但是仍有许多新识别的基因的功能还不知道,也不知道基因产物是如何相互作用从而产生活的有机体的。功能基因组试图通过大规模实验方法来回答这些问题。但由于仅从DNA序列尚不能回答某基因的表达时间、表达量、蛋白质翻译后加工和修饰的情况、以及它们的亚细胞分布等等,因此在整体水平上研究蛋白质表达及其功能变得日益显得重要。这些在基因组中不能解决的问题可望在蛋白质组研究中找到答案。蛋白质组研究的数据与基因组数据的整合,将会在后基因组研究中发挥重要作用。目前蛋白质组研究采用的主要技术是双向凝胶电泳和质谱方法。双向凝胶电泳的基本原理是蛋白质首先根据其等电点,第一向在pH梯度胶内等电聚焦,然后转90度按他们的分子量大小进行第二向的SDS-PAGE分离。质谱在90年代得到了长足的发展,生物质谱当上了主角,蛋白质组学又为生物质谱提供了一个大舞台。他们中首选的是MALDI-TOF,其分析容量大,单电荷为主的测定分子量高达30万,干扰因素少,适合蛋白质组的大规模分析。其次ESI为主的LC-MS联机适于精细的研究。本文将简介几种常用的生物质谱技术,并着重介绍生物质谱技术在蛋白质组学各领域的应用。此贴与http://bbs.instrument.com.cn/shtml/20081130/1613156/重复,请版友在发帖前先搜索一下,以免重复发帖,谢谢!
有奖问答:当调节溶液pH值,使蛋白质分子的正、负离子数目相等,此时溶液的pH值即为该蛋白质的?
蛋白质纯化及复性 重组蛋白在大肠杆菌(E. coli)高效表达时,往往以不溶的、无活性的蛋白聚集体,即包涵体(inclusion body)的形式存在于细胞内。必须从细胞内分离出包涵体,采用高浓度变性剂(如7.0mol/L盐酸胍、8.0mol/L脲)溶解包涵体,然后除去变性剂或降低变性剂的浓度,使包涵体蛋白得以复性,最后再用色谱法使目标蛋白质得到纯化。其中包涵体蛋白的复性和纯化是整个过程中的核心。 目前重组蛋白生产中普遍存在的问题是:(1)复性效率低。传统的复性方法稀释法和透析法。稀释复性法对样品几十倍,甚至上百倍的稀释会使样品的体积急剧增大,给后续的分离纯化带来很大的困难,而且复性过程中需要较大的复性容器。透析法耗时较长,而且要多次更换透析溶液。这两种方法的共同缺点是蛋白质在复性过程中会发生聚集而产生大量沉淀,复性效率低,通常蛋白质的活性回收率只有5~20%,而且复性后的蛋白质溶液中含有大量的杂蛋白,需要进行进一步的分离纯化。(2)工艺路线烦琐,生产周期长。在传统的重组蛋白质分离纯化工艺中,大多采用经典的软凝胶分离介质,由于这种介质的颗粒较大,分离效率较差,因此常常需要采用多种不同模式的色谱操作联用对目标蛋白质进行纯化,才能得到纯度符合一定标准的目标蛋白质。另外,这种色谱介质的耐压性很差,只能在流速较低的情况下进行操作,分离纯化时间较长。分离纯化步骤多和分离时间长使得蛋白质的质量回收率和活性回收率很低。而且在传统的重组蛋白质生产工艺中,蛋白质的复性和纯化是生产过程中两个独立的单元操作,也在很大程度上制约着生产效率。(3)生产成本高,设备投资大。由于复性和分离纯化分别单独进行,而且分离纯化步骤多,每一步都需要有与之配套的设备,致使设备投资大,生产成本高。随着生产规模的增加,这种弊端会愈来愈严重。 1991年耿信笃教授首先将高效疏水相互作用色谱(HPHIC)用于变性蛋白的复性,很好的解决了上述问题,现已成功用于重组人干扰素-g(rhIFN-g)、重组人干扰素-a(rhIFN-a)、人粒细胞集落刺激因子(rhG-CSF)、重组人胰岛素原(proinsulin)、重组牛朊病毒(prion)等重组蛋白以及溶菌酶和核搪核酸酶等标准模型蛋白的复性与同时纯化中。目前,排阻色谱法、离子交换色谱法和亲合色谱法也已用于蛋白质的复性和同时纯化中。与传统的稀释法及透析法比较,用色谱法进行蛋白复性的优点是:①在进样后可很快除去变性剂;②由于色谱固定相对变性蛋白质的吸附,可明显地减少、甚至完全消除复性过程中蛋白质聚集体和沉淀的产生,从而提高蛋白质复性的质量和活性回收率;③在蛋白质复性的同时可使目标蛋白质与杂蛋白分离以达到纯化的目的,使复性和纯化同时进行;④便于回收变性剂,以降低废水处理成本。简言之,色谱法复性可以提高蛋白质的活性和质量回收率,将蛋白复性和纯化集成在一步操作完成,缩短了操作步骤和生产时间,减少了设备投资,使生产成本大大降低,已经引起了全世界范围内许多生化研究者和重组蛋白药物生产厂家的关注。由于高效液相色谱(HPLC)分离效率高,往往在一步操作中便可得到纯度符合要求的蛋白质,而且分离速度快,在应用方面具有更大的优势。
一、 前言 基因工程已令人难以置信的扩展了我们关于有机体DNA序列的认识。但是仍有许多新识别的基因的功能还不知道,也不知道基因产物是如何相互作用从而产生活的有机体的。功能基因组试图通过大规模实验方法来回答这些问题。但由于仅从DNA序列尚不能回答某基因的表达时间、表达量、蛋白质翻译后加工和修饰的情况、以及它们的亚细胞分布等等,因此在整体水平上研究蛋白质表达及其功能变得日益显得重要。这些在基因组中不能解决的问题可望在蛋白质组研究中找到答案。蛋白质组研究的数据与基因组数据的整合,将会在后基因组研究中发挥重要作用。 目前蛋白质组研究采用的主要技术是双向凝胶电泳和质谱方法。双向凝胶电泳的基本原理是蛋白质首先根据其等电点,第一向在pH梯度胶内等电聚焦,然后转90度按他们的分子量大小进行第二向的SDS-PAGE分离。质谱在90年代得到了长足的发展,生物质谱当上了主角,蛋白质组学又为生物质谱提供了一个大舞台。他们中首选的是MALDI-TOF,其分析容量大,单电荷为主的测定分子量高达30万,干扰因素少,适合蛋白质组的大规模分析。其次ESI为主的 LC-MS联机适于精细的研究。本文将简介几种常用的生物质谱技术,并着重介绍生物质谱技术在蛋白质组学各领域的应用。 二、 生物质谱技术 1.电喷雾质谱技术(ESI) 电喷雾质谱技术( Electrospray Ionization Mass Spectrometry , ESI - MS) 是在毛细管的出口处施加一高电压,所产生的高电场使从毛细管流出的液体雾化成细小的带电液滴,随着溶剂蒸发,液滴表面的电荷强度逐渐增大,最后液滴崩解为大量带一个或多个电荷的离子,致使分析物以单电荷或多电荷离子的形式进入气相。电喷雾离子化的特点是产生高电荷离子而不是碎片离子, 使质量电荷比(m/ z) 降低到多数质量分析仪器都可以检测的范围,因而大大扩展了分子量的分析范围,离子的真实分子质量也可以根据质荷比及电荷数算出。本帖与http://bbs.instrument.com.cn/shtml/20081130/1613156/重复,故锁帖!请版友在发帖前先搜索一下,以免出现重复贴。谢谢!斑竹您给的重复贴链接有误,并且我写贴前已经搜索了标题。SORRY,请LZ检索一下这个网址,开始那个是弄错了。
请教各位高手:含有蛋白质的溶液如何进行吸收光谱试验?我的是 Ca2+和清蛋白的水溶液,在吸收光谱测量含量时,偏差较大,估计清蛋白的影响,请问有什么办法消除白蛋白的影响么?谢先!!
[align=center]蛋白质热稳定性的研究机理[/align][align=center]西安国联质量检测技术股份有限公司[/align][align=center]食品事业部:魏娜[/align] 疏水作用被认为是决定蛋白质结构的主要作用力。蛋白质的天然结构是由以下类型的共同作用力维持其结构的热稳定性(例如,H键,离子键和范德华力)。德国专家Dil回顾了支持这一理论的证据:(一)非极性溶剂使蛋白质变性 (二)疏水残基可以很典型的把核心部位分开,在其核心部位他们在很大程度上避免了与接触水 (三)在蛋白质核心部位的残基和疏水基团比任何其他一种残基具有更坚固的保守区和结构(核心部位疏水残基的取代物一般比任何一种代替物更具有破坏性)。(四)蛋白质展开涉及大量增加的热容量。给定的疏水作用的中心对在蛋白质折叠也有一定的影响,很容易以为疏水作用还是负责蛋白稳定性的主要动力。在过去20年里,序列、结构和诱变等信息的积累证实了疏水作用,事实上,更是蛋白质稳定性的主要动力。两个观察报告指出常温的和极端嗜热的微生物的同源体具有相同的最基本的稳定性,这种稳定性由保守的蛋白质核心提供:(1)疏水相互作用以及中心残基所影响的二级结构比特征区域表面更保守。(2)在有溶解能力的被暴露的区域发现了大量稳定的代替物(可以在常温及极端嗜热蛋白质结构的比较以及在蛋白质定向突变的实验中观察到)。常温以及嗜热蛋白质同源体的核心具有高度的相似性,这些性质表明常温蛋白质尽可能高效的与那些在核心外部的没有太多空间稳定性的蛋白质进行折叠。极端嗜热蛋白质稳定的相互作用经常在蛋白质的不保守区被发现。如下所示,如表面离子对减少了溶剂暴露疏水面,和与之稳定结合(即N和C末端以及氨基酸循环)的蛋白质表面似乎有助于极端嗜热蛋白质的热稳定性。 在近年来足够的实验证据(如序列,诱变,结构,和热力学)被积累,但没有一个单一的机理可以解释极端嗜热蛋白质的显著的稳定性。增加的热稳定性可以在数量很少的精确突变中找到,这样的突变常常不遵循任何一种固定的法则。[b] 氨基酸组成和内在倾向[/b]蛋白质的氨基酸组成长期以来被认为与其热稳定性有关。第一个数据分析对比了常温和极端嗜热蛋白质的氨基酸组成,发现趋向于Gly→Ala,Lys→Arg的替换,嗜温蛋白质的组成中含有大量Ala,主要是由于Ala最易于螺旋结构的形成。随着更多实验数据的积累(尤其是,全基因组序列的测序 ),通常的嗜热适应规则不能依据显著性差异来定义蛋白质中氨基酸的组成已经变得越来越明显了。通过对8个常温和7个极端嗜热微生物的基因组序列的对比得出常温和极端嗜热蛋白质的残基存在这种趋势的差异(如表4所示)。另外发现,极端嗜热蛋白质比常温蛋白质带有更多的带电残基(多3.24%),以及较少的极性未荷电残基(-4.98% 特别是谷氨酰胺,-2.21%)。嗜热蛋白质比常温蛋白质还含有更多的疏水残基和芳香残基。从基因组测序中获得的这些数据不能普遍化,在极端嗜热的微生物基因组中自身存在着很多的突变。敏捷气热菌实际上比在表4中列出的嗜温菌含有有更少的带电残基(23.64%),更少的大体积的疏水残基(27.29%),以及更少的芳香性残基(7.42%)。相反,敏捷气热菌含有较多的Ala,Gly,Pro,Ser,和Thr残基。因此,极端嗜热蛋白质的氨基酸组成可能经常和突变性有关,而不是与其适应高温的指标有关。蛋白质中氨基酸残基的分布与其相互作用比氨基酸残基的组成对蛋白质的热稳定性更相关。这两种同源蛋白酶解淀粉芽孢杆菌枯草杆菌蛋白酶BPN9和普通高温放线菌嗜热蛋白酶包含数量相同的带电残基,但嗜常温酶的嗜热蛋白酶包含比八个更多的离子对。有关的想法,蛋白质的稳定性取决于稳定的紧密包裹的疏水内核,个别残基的固有倾向是参与螺旋或链结构,这作为一个潜在的稳定机制被研究。比较嗜温和嗜热蛋白结构,Facchiano等人观察到嗜热蛋白质的螺旋结构通常比的嗜温蛋白质更稳定。他们检测到的唯一的趋势是在嗜热蛋白质的螺旋(二支链残基没有得到很好的耐受性螺旋线性残留有)中C[sub]β[/sub]分支残基的减少(Val,Ile,和Thr)。许多实例存在于未遵循这一趋势。该P.球菌和T. litoralisGDHs包含更多数量的Ile。如果将Leu和Ile残基进行比较,这两个残基具有最高的(和等同的)部分特定卷。在蛋白质中,Leu侧链最常发现两种旋转异构体的构象(180°和300°×1),但不是在一个与X1 =60°。在Ile侧链频繁采用四种不同的旋转异构体的构象,以及三个X1值被发现。随着这种构象的柔性,Ile可能能够更好地填补在蛋白质内核折叠时出现的空缺。Dil还指出,环境的影响(例如,盐桥的形成,芳烃相互作用,疏水表面的包埋,以及填充膜腔)可以作为重要内在的螺旋倾向。在许多情况下,二级结构在蛋白质结构不对应于所找到的二级结构预测的内在倾向,表明该固有倾向不足以解释蛋白质中α-螺旋的稳定性。Arg残基的几个特性表明,他们将比Lys残基更好地适应高温:该Argδ-胍基部分由于其高的pKa和共振稳定而降低的化学反应活性。δ-胍基部分比Lys氨基为带电的相互作用提供了更多的表面积。Arg参与多种非共价相互作用的能力。因为在Arg侧链比Lys少一个亚甲基,它具有开发较少不利触点的电位与溶剂。最后,因为它的pKa值(约12)是Lys的1倍以上(11.1),在温度升高的时候,精氨酸更容易保持离子对和净正电荷(因为温度的增加,pKa值下降)(252,354)。在嗜温菌的蛋白质池和在表中列出超嗜4(0.73+ - 0.37和0.87+ - 0.60,分别)平均精氨酸/赖氨酸的比率与大标准偏差相关。(其中超嗜热,精氨酸/赖氨酸的比率范围从Aquifex0.52超嗜热菌蛋白到2.19敏捷气热菌。)这些结果表明,如果增加精氨酸确实会变得稳定,这种机制是不能够普遍使用于极端嗜热菌中。[b] 二硫键 [/b]二硫键被认为主要是通过降低蛋白质裂解状态的熵维持蛋白质的稳定。当两个半胱氨酸键断裂时,二硫键的熵效应成比例地以对数方式增加残基的数量。 因为在高温下,半胱氨酸和二硫键的敏感性遭到破坏,,100℃被认为是蛋白质维持二硫键稳定性的上限。这一概念是基于这样一个事实,早期的研究描述蛋白质活性的研究机理,在那个时期仅形成了一种可利用的酶:常温酶。这些研究确定了所有蛋白质研究,研究包括的二硫键在100℃时β-消除有相同的速率。这个速率不依赖于蛋白质的结构并且在pH=8.0(半衰为1小时)比在pH =6.0(半衰期为12.4小时)时速度快。这些研究的限制是在100℃时所有蛋白质是在展开状态时进行研究的。在最近包括二硫键的蛋白质的描述中,在100℃时这些蛋白质具有最大的活性和稳定性,表明在100℃时二硫键维持了这些蛋白质的稳定性并且构象环境和溶剂可被决定因素保护,防止破坏二硫键。当描述大肠杆菌时,S.solfataricus 5’-甲硫腺苷磷酸化酶形成了不正确,不稳定的二硫键。这一观察间接反映了,二硫键在天然酶中表现出的稳定性。嗜火液丝氨酸蛋白酶被描述为包含8半胱氨酸(无存在于枯草杆菌蛋白酶BPN')。处理二硫苏糖醇从半衰期为90 小时 85℃,减少到少于2小时。在高温下二硫苏糖醇不稳定进一步表明这种酶的确含有二硫键并且它们是高度不稳定的。这种酶在半衰期为6小时 温度为105℃ pH=9.0时,要比它在蛋白质展开中pH=8.0 半衰期为1小时二硫键计算的长,表明这种酶的二硫键通过蛋白质中二硫键的无法靠近以保护二硫键不被破坏。因此,不是所有的二硫键对热稳定破坏具有相同的易感性。[align=center][b]疏水作用[/b][/align] 在极端嗜热蛋白质中,疏水作用是蛋白质热稳定性的一个机理。平均增加1.3千卡/摩尔(±0.5)的稳定性对于增加甲基埋在蛋白质折叠(取决于腔产生突变,这种突变中,大的脂族残基被替换为一个较小的脂族残基)。当突变产生了往往需要局部重排的不利的范德华力作用时,突变试图填充凹处往往是更不稳定的。疏水性相互作用在蛋白质结晶中的热稳定作用的,实验证据是可用于确认所述极端嗜热蛋白质中疏水作用的区域。存在于沃氏甲烷球菌和M.jannaschiladenylate激酶中的这种酶嵌合体的结构的稳定部分表明,更大和更具极端嗜热酶疏水酶核心(这是由于增加的脂肪族残基含量和脂族侧链体积)可能是负责分枝詹氏甲烷球菌的腺苷酸激酶的热稳定性。该从嗜热栖热菌3-异丙基苹果酸脱氢酶热包含亚基间的疏水相互作用的没有在大肠杆菌中酶存在。嗜三异丙基脱氢酶Leu246Glu/ Val249Met和大肠杆菌Glu256Leu/Met259Val突变衍生物构建了动摇并稳定在栖热和大肠杆菌酶,分别的突变体和野生型的聚丙烯酰胺凝胶电泳在尿素的存在下酶表明,疏水性相互作用使二聚体解离更有抵抗力。[b]氢键[/b]由于氢键的作用使得核糖核酸酶T1趋于稳定。核糖核酸酶T1平均长度86 H键。他们的核糖核酸酶T1稳定(约贡献110千卡/摩尔,如通过诱变和展开实验确定),H键贡献(307)1.3千卡/摩尔能力。因为识别H键的高度依赖于距离截止和因为一批超嗜热蛋白质结构没有被细化到足够高的分辨率,通过结构研究的热稳定性H键的作用分析没有提供明确的答案。一项研究由唐纳等人完成的。H键使得蛋白质的热力学稳定:(i)关联的去溶剂化罚与掩埋诸如H键小于去溶剂化罚掩埋离子对的(即包括两个电荷的残基),和(ii)一个充电中立H键的焓奖励是大于由于中性中性H键的电荷 - 偶极相互作用。chargedneutral之间的这种相关性H键和GAPDH稳定性表明的作用在稳定蛋白质电荷的残基可以不限于形成离子对。带电中性h的人数增加债券还发现了T. maritima的铁氧还蛋白(表5)。这些H键或者稳定转弯或锚的结构变为另一个。[b]离子对[/b]因为离子对通常存在于在少量蛋白质和因为它们不是高度保守的,它们是不驱动在蛋白质折叠的力。去溶剂化作用8筒体螺旋A8和A1)还通过测试SDM。在85.5°C,突变Arg241Ala增加酶变性率几乎3.酶的EA的一个因素展开在85℃下降3.2千焦耳/摩尔,这表明Arg241-Glu73对参与的动力学稳定这种酶。在P.球菌确定的离子对网络,P. kodakaraensis,和T. litoralis的GDH的结构进行了研究由SDM。这三种酶是83至87%相同,但它们的thermostabilities减小的方向P.球菌GDH。P. kodakaraensis GDH。T. litoralis的GDH。它们都含有相同的18离子对网络在它们的六聚体界面。突变Glu158Gln,其中去掉2离子对的该网络的中心,显著不稳定P. kodakaraensisGDH的。一个离子,包括六对网络被控残留物只存在于P.球菌GDH。相同的离子对网络在P.kodakaraensis GDH和T. litoralis的创建GDH由SDM。这两种酶是由新稳定的介绍离子对网络(280,348)。这些研究证实离子对网络在巴斯德球菌,P的作用kodakaraensis和T. litoralis的GDH thermostabilities。 Lebbink等。 (203)介绍了16个残基的离子对网络的在T. maritima的GDH亚基界面来创建一个界面类似于在体育球菌的GDH在18离子对网络。该三不稳定的突变组合产生了三重突变酶(Ser128Arg-Thr158Glu-Asn117Arg),这是稍微更稳定和嗜热比野生型酶。这个结果示出合作的高级别存在这种离子对网络的不同成员之间。该结果还支持18个残基的离子对的作用网络中的P.球菌GDH稳定。在早先的研究中,Tomschy等。(337)已拆除2位于两个α-螺旋在T. maritima的表面上的离子对GAPDH。由于这些突变不影响所述酶稳定性,作者得出结论认为,表面离子对不能被认为是热适应的总体战略。选择在本研究Bothion对分别螺旋内的离子对。这些2双可能已经位于蛋白质领域的人过约束,而不是蛋白质的地区之一最容易展开。与此相反,在其它实施例上述说明的热稳定效果非本地离子对和离子对网络,连接不相邻的残基(和二级结构)的序列中。离子配对中的作用的附加的,间接的证据热稳定性是来自基因组测序。与嗜热蛋白质带电残基相比,常温蛋白,主要是在不带电荷的极性为代价残留物。[b]脯氨酸及脯氨酸展开过程中的熵的减少[/b]Matthews等人提出已知的蛋白质三维结构可以通过展开时他们的熵的减少维持稳定。在展开状态下,甘氨酸是带有最高构象熵的残基,没有C[sub]β[/sub]。脯氨酸,可以采用只有几个配置并限制允许前述残余物的配置(313),具有最低的构象熵。因此,该突变Gly3Xaa或Xaa3Pro应该减少熵及的蛋白质的展开状态稳定的蛋白质,只要作为改造的残留不引入不利菌株中的蛋白质的结构。这一技术已被用来工程师酶是热力学更稳定。例如,杆状stearothermophilus中性蛋白酶失活通过自溶,其中针对特定柔性表面环(残基63到69)(93)。脯氨酸在循环中引入使其不易展开。只有定位65至69是适合脯氨酸替换。在其他位置,一脯氨酸将消除非共价相互作用,产生构象株,或有不恰当的扭转角度。许多嗜热和嗜热蛋白也利用这个稳定机构(255)。Pro177和Pro316在两个N个末端螺旋和Pro24中的B-转弯位置2被证明是稳定(215)。(脯氨酸分别在相应的引入地点在拜氏梭菌的酶。)至少有其中仅发生在嗜热芽孢杆菌脯氨酸22位置寡聚1,6-葡糖苷酶。其中大多数脯氨酸是在位置2的溶剂暴露B-圈(七个脯氨酸的),在循环内的线圈(9人),或在N帽一个螺旋在桶结构(其中四个)。脯氨酸是在嗜温的相应位置引入蜡状芽孢杆菌寡-1,6-葡糖苷酶。热稳定性一般随着引入脯氨酸的数量。稳定性增长最为显著时添加的脯氨酸位置两个B-转弯或在一个螺旋瓶盖ñ 。少稳定的突变可能引入不利范德范德华相互作用或删除稳定H键(361)。在那不勒斯栖热袍木糖异构酶包含两个脯氨酸在参与亚基间的相互作用是一个循环。这些脯氨酸缺席在不太稳定的Thermoanaerobacteriumthermosulfurigenes酶。动力学稳定性两个T的性能thermosulfurigenes木糖异构酶突变体Gln58Pro和Ala62Pro说明如何重要突变位置为SDM(313)的结果。两Gln58和Ala62有骨干二面角这使得为脯氨酸,既不参与非共价稳定相互作用,以及Asp57和Lys61不得不二面角那允许前面的脯氨酸残留。的构象在Gln58侧链非常接近的脯氨酸吡咯烷酮环,并且因此没有构象菌株由临介绍 突变Gln58Pro稳定的蛋白质主要是通过降低展开的熵。相反,突变Ala62Pro之间创建一个卷的干扰脯氨酸吡咯烷酮环(镉原子)和Ly61侧链(CB原子),这可能导致不稳定的构象变化。突变Ala62Pro降低了酶的T1 /2为85℃下的10倍。[b] 构象应变作用力的作用[/b]左手螺旋构象的残基(Φ=40至60°,Ψ=20〜 80°)有着末端构象稳定性除非它们通过分子内的非共价相互作用来稳定。(左旋螺旋构象非甘氨酸残基被认为比右旋结构少0.52.0千卡/摩尔而不太稳定)。在左手螺旋构象的残基中,β- 碳和羰基氧的紧密相连在蛋白质结构中产生了一个局部的构象张力。左手螺旋构象的两个残基,谷氨酸15在枯草芽胞杆菌的DNA结合蛋白HU和赖氨酸95大肠杆菌核糖核酸酶H1,在旋转区域,是通过在嗜热酶的相应部分甘氨酸残基取代。突变体谷氨酸15甘氨酸和赖氨酸95甘氨酸分别在枯草杆菌DNA结合蛋白HU和大肠杆菌RNA酶H1,消除在左旋螺旋构象中由残基产生的构象张力,以及两种蛋白质的热力学稳定性的显著增加。在这两个例子中,由于构象张力的释放增加的蛋白质的稳定,通过它的稳定性影响二级结构的相互作用被加强。大肠杆菌核糖核酸酶H1包含两个额外左旋螺旋构象的非甘氨酸残基。残基色氨酸90和天冬酰胺100,而相比之下,赖氨酸95,酶内部的点,并且它们弥补了极性或疏水的相互作用。左旋螺旋构象中,常温的铁氧还蛋白含有三个残基在他们簇结合区域。在海栖热袍菌和T. litoralis的同系物中,簇结合区域的空间位阻通过具有三个甘氨酸残基的左旋螺旋构象的残基取代物被释放。这三个甘氨酸残基都涉及了拥有硫原子簇的H键。其他类型的构象张力释放作为稳定机制已经被提及。例如在α-螺旋中,具有低螺旋倾向的残基可以通过具有高螺旋倾向的残基被替换。这样的替代物通常发生在残基的侧链没有得到很好的安置的α-螺旋时。位于α-螺旋的一个特殊取代物是C末端(或C帽)。因为它缺乏了的支链以允许它采用没有张力的左手螺旋构象,并且由于主链羰基氧可以与溶剂分子形成氢键,所以在C帽甘氨酸是最有利的残基。该P.furiosus柠檬酸合成酶至少包含了7个具有C-帽的甘氨酸螺旋。他们的对稳定性的影响仍是未知的。虽然,在一般情况下,这些构象张力释放的类型不被期望提供显著的稳定性,并且它们在极端嗜热蛋白结构中没有扮演细致的角色。他们还与其他稳定机制相竞争(如倾向疏水相互作用,H键,或离子对)。[b] 螺旋偶极作用力对结构稳定的作用[/b]螺旋偶极可以通过邻近N-末端带负电荷的残基,以及邻近C-末端带正电荷的残基维持稳定。在S.solfataricus吲哚-3-甘油磷酸合成酶中,螺旋的偶极。也被稳定在杆状stearothermophilus和海栖热袍菌PGKs中:常温酶只有9 N帽和12 C帽(猪PGK)和10 N帽9 C帽(酵母PGK)通过相反的电荷被稳定。嗜热脂肪芽孢PGK数量稳定的N和C帽提高到16 N帽和13 C和在海栖热袍菌的PGK的提高到17 N帽和14C帽。尼克尔森等人展示N帽可通过约0.8千卡/摩尔增加酶的△Gstab。虽然,在一般情况下,N和C帽子和其他稳定的以及不稳定机制相竞争(例如,倾向H键或离子对)。[b]金属键对稳定性的影响[/b]长久以来,金属键以稳定和激活酶而众所周知。木糖异构酶连接两个金属离子(选自Co[sup]2+[/sup],Mg[sup]2+[/sup]和Mn[sup]2[/sup][sup]+[/sup])。一种阳离子是直接参与催化 第二种主要是结构。两种金属结合位点具有不同的特异性,并且一种阳离子与另一种阳离子的替换经常显著的改变酶的活性,底物特异性,热稳定性。存在和不存在于地衣芽孢杆菌木糖异构酶的金属键其酶稳定性的研究稳定结果表明的演变动力学稳定性遵循的热力学稳定性以及这两种类型的稳定性是金属呈现出的固有的功能。这些观察表明,主要稳定力与呈现在全酶中的金属相连。 对于金属在极端嗜热蛋白质中的稳定性起的作用的间接证据是在酶中除去金属遇到困难。α-淀粉酶特殊结合Ca[sup]2[/sup][sup]+[/sup]。α-淀粉酶催化位点位于两个领域的分裂结构之间(具有8管和一个回路)。属于这两个领域的配体相调整,Ca[sup]2[/sup][sup]+[/sup]配体对酶的催化活性和热稳定性是必不可少。巴斯德球菌胞外α-淀粉酶最初描述为Ca[sup]2[/sup][sup]+[/sup]无关的酶,因为室温下EDTA处理对其活性没有任何影响。进一步鉴定表明,这种酶包含至少两个Ca[sup]2[/sup][sup]+[/sup]阳离子,这种阳离子在70℃以下不能被EDTA去除。在90℃下处理EDTA30分钟除去大约60%至70%的结合的Ca[sup]2[/sup][sup]+[/sup]。Thermococcus profundusα-淀粉酶做出类似的观察结果(约80%相同的P.furiosua,胞外α-淀粉酶)。这种酶被激活并通过Ca[sup]2[/sup][sup]+[/sup]使其稳定,但室温处理EDTA对活性没有任何影响。 一些嗜热和极端嗜热酶曾被描述为含有金属原子,这些原子不出现在它们同源的常温酶中。来自于Sulfolobus sp.de 铁氧化还原蛋白张力7包含一个额外的40残基的N-末端延伸,这个延伸通过Zn结合位点被连接到核心蛋白上。锌原子通过N-末端结构域的三个组氨酸残基与核心结构域的1个天冬氨酸残基相连接。这种结构(N-末端延伸加锌结合位点)是不存在于真细菌同源微生物中的但是被保存在所有其他的嗜热嗜酸菌中 。逐行N末端缺失和两三个定向突变的配体表明,N端延伸和这两个锌原子对热力学稳定性很重要。虽然,它们的存在或缺失没有任何影响,但是影响着铁氧还蛋白功能。锌原子是负责9°C增加Tm值。它是如此的紧密结合在蛋白质内,在没有移除这两个FeS时锌原子不能被移除。普通嗜热放线菌枯草杆菌蛋白酶型丝氨酸蛋白酶的嗜热蛋白酶包含了三个Ca[sup]2[/sup][sup]+[/sup]结合位点 它们中的一个不出现在其常温酶同系物中(331)。嗜热酶的嗜热同系物,芽孢杆菌AK1蛋白酶比嗜热酶包含更多的Ca[sup]2[/sup][sup]+[/sup],并且它比在嗜热酶中出现的Ca[sup]2[/sup][sup]+[/sup]具有更显著的动力学稳定(半衰期为15小时80℃下与19分钟为嗜热酶)。因为Ca[sup]2[/sup][sup]+[/sup]优先与羧酸盐以及其他含氧等配体结合(它是最有可能被位于蛋白质表面上的金属配位体),这种金属比其他金属在蛋白质稳定性可能扮演更显著的稳定作用。[b] 蛋白质翻译后的修饰作用[/b] 蛋白质糖基化广泛存在于真核生物的酶上,以及一些细菌的胞外酶被糖基化。只有几个例子是公知的被糖基化的极端嗜热蛋白,并且它们的碳水化合物部分还没有被广泛表征。虽然,大多数的酶被糖基化(细菌,古细菌和真核微生物),但在细菌中仍然保留了其催化作用和稳定性。一些研究使用天然糖基化的真核生物蛋白质表明,糖基化可能在不影响蛋白质折叠的方式或它们的构象下造成显著地热稳定作用。较高倾向去糖基化的酶在热失活下聚集,表明糖基化也可以防止部分折叠或来自于聚合蛋白质的展开。牛科胰核糖核酸酶A和核糖核酸酶B区别仅在于连接核糖核酸酶B的Asn34部分的碳水化合物不同。这碳水化合物解释说明了核糖核酸酶B更高的动力学以及热力学稳定性。先进的碳水化合物部分的假说表明,稳定性的不同是由于在第一个糖单元连接到Asn34。 糖基化对热稳定性的影响两个杆菌β-葡聚糖酶在大肠杆菌和酿酒酵母的表达。这两个之一酶在70℃时,通过糖基化有强烈的动力学稳定性,其最佳动力学稳定活性温度更高。对热稳定水平比对糖基化的程度更依赖于碳水化合物部分在蛋白质中的位置。虽然在自然界中糖基化可能不是大众的热稳定方法,上述被引用的几个例子表明,对于酶的热稳定或是溶解,糖基化可能代表了一种替代方法。 翻译后赖氨酸甲基化(形成于 N-ε-单甲基赖氨酸)已经描述为许多硫化的蛋白。天然的小的来自的 S.嗜酸热的DNA结合蛋白Sac7d(单甲基化赖氨酸 Lys5和Lys7)在100℃下发生可逆地变性(pH为7.0)。该重组Sac7d在92.7℃下变性。天然和重组的Sac7d之间的Tm 7°C的区别已被归因于赖氨酸的甲基化,赖氨酸的甲基化不存在于重组蛋白之中。由于Sso7d的稳定性(在S.Sulfolobus中是Sac7d的同系物)是不依赖于甲基化的,赖氨酸的甲基化在Sulfolobales是否是一般的热稳定机制。[b]盐离子的稳定性[/b]无机盐稳定蛋白有两种方式:(ⅰ)通过特定的影响,其中,金属离子于一个构象方式的蛋白质相互作用(参见“金属键”),(ii)通过一般盐的影响,主要影响水活性。 Thauer以及他的同事研究了盐对热稳定性的影响以及5种如甲烷噬热菌产甲烷的酶的活性(36,37,181,224,225)。然而这5种酶通过盐被激活以及机械的被稳定,盐影响的程度是酶的依赖性。 K[sup]+[/sup]和NH[sup]4[/sup][sup]+[/sup]通常比其他阳离子更有效地稳定酶。所有的阴离子,SO4[sup]2[/sup][sup]-[/sup]和HPO4[sup]2[/sup][sup]-[/sup]有最强的激活效应。酶盐的要求并不总是由细胞内盐浓度满足。分枝如甲烷噬热菌细胞内的盐浓度(大于1M钾加1M的环状2,3-二磷酸甘油酸)似乎对MkCH活性有利(最大浓度为1.5M盐)在其稳定(最佳浓度低于0.1M盐)。盐对来自于如甲烷噬热菌,M.thermoautotrophicum, Archaeoglobus fulgidus以及Methanosarcinabarkeri的CHOtetrahydrormethanopterin(H4MPT)甲酰基转移酶的影响进行比较。通过盐在甲酰基转移酶活性的不同是与在不同的生物体细胞内cDPG浓度直接相关。通过盐按照MkFT的活性分析了MkFT的结构。两种功能被提出相关的性质:(一)在疏水性表面MkFT呈现出下降的趋势,以及亚基间的界面在很大程度上是疏水的 和(ii)四聚体表面呈现与24个基本过量的负电荷残基(48个残基)。酸性残基可以形成较强的氢键和多H键的水分子,确保这些残基与无机阳离子或水竞争。所有的残基中,谷氨酸具有结合水分子的最高容量。48个表面带负电荷的,33个是谷氨酸和15是天冬氨酸。高易溶的盐浓度被认为由于在负电荷残基表面增加的无机阳离子增加了表面离子作用,并且间由于盐析的影响提高了亚基疏水相互作用效果。MkFT寡聚物构象显示出了需要比磷酸钾更高的NaCl浓度(更强易溶的盐),表明在MkFT热稳定中盐析的影响起主导作用。这种蛋白质可能有演变为最佳地稳定性表现在高的胞内盐浓度中。 当在98℃时,如甲烷噬热菌细胞中含有约的1M cDPG。cDPG中的钾盐,2,3-DPG以及磷酸盐在激活如甲烷嗜热酶环化酶中同样有效。然而,在同等离子浓度cDPG比在稳定的MkFT中更有效。在如甲烷噬热菌中,cDPG浓度对MkCH和MkFT的活性以及稳定性是最佳的。合成CDPG需要4 分子ATP。在这个合成的最后反应是唯一一个能够放出足够的能量来驱使合成cDPG而非其前体2,3-DPG。此外,在pH=7.0,cDPG是三阴离子,而2,3-DPG是五阴离子 因此cDPG比2,3-DPG在离子强度方面有更小的影响。[color=#ff0000] [/color]M. fervidus[color=#ff0000] [/color]磷酸甘油醛脱氢酶(GAPDH)本质上动力学稳定仅达到75℃。通过盐来研究这种酶的热稳定性表明,相对于盐的效果—K[sub] 3[/sub] PO[sub] 4[/sub]Na[sub]3[/sub]PO[sub]4[/sub][sub] [/sub]K[sub]2[/sub]SO[sub]4[/sub]Na[sub]2[/sub]SO[sub]4[/sub]KCLNaCL—都与他们保持一致各自的能力以减少酶在水溶液中的溶解度。它们的盐析影响了他们活性的分布。 M. fervidus GAPDH可能由cDPG被稳定在体内,它以约为0.2〜 0.3M出现在生物体中。有趣的是,其他的M.fervidus酶是唯一依赖于低于生物体的最佳生长温度的以维持稳定,这表明在该生物体中通过盐的稳定性是共同的机制。 [b]压力的影响[/b] 因为许多高温环境同样也是高压环境并且因为微生物无法逃避压力和温度,所有的大分子细胞成分必须能适应高的压力。因此,并不奇怪的是找到极端嗜生物体也是嗜压微生物(如嗜热barophilus),并发现通过高压使这种酶被稳定以及被激活(例如,M。詹氏甲烷球菌的蛋白酶和氢化酶)。通过压力这种稳定性背后的理论说明压力有利于体积最小的结构。蛋白质主要通过疏水被稳定因此,预计在高呀下被稳定,而通过离子相互作用被稳定的蛋白质应该是不稳定的。例如,P.furiosus 红素氧还蛋白主要是由静电相互作用稳定。这种酶在高压力不稳定。由于许多化学反应在高温高压进行的,在高压下酶的稳定性可能很大程度上对生物催化作用有利。
一、 前言[1,2]基因工程已令人难以置信的扩展了我们关于有机体DNA序列的认识。但是仍有许多新识别的基因的功能还不知道,也不知道基因产物是如何相互作用从而产生活的有机体的。功能基因组试图通过大规模实验方法来回答这些问题。但由于仅从DNA序列尚不能回答某基因的表达时间、表达量、蛋白质翻译后加工和修饰的情况、以及它们的亚细胞分布等等,因此在整体水平上研究蛋白质表达及其功能变得日益显得重要。这些在基因组中不能解决的问题可望在蛋白质组研究中找到答案。蛋白质组研究的数据与基因组数据的整合,将会在后基因组研究中发挥重要作用。目前蛋白质组研究采用的主要技术是双向凝胶电泳和质谱方法。双向凝胶电泳的基本原理是蛋白质首先根据其等电点,第一向在pH梯度胶内等电聚焦,然后转90度按他们的分子量大小进行第二向的SDS-PAGE分离。质谱在90年代得到了长足的发展,生物质谱当上了主角,蛋白质组学又为生物质谱提供了一个大舞台。他们中首选的是MALDI-TOF,其分析容量大,单电荷为主的测定分子量高达30万,干扰因素少,适合蛋白质组的大规模分析。其次ESI为主的[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]联机适于精细的研究。本文将简介几种常用的生物质谱技术,并着重介绍生物质谱技术在蛋白质组学各领域的应用。
请教大家:对保存在PBS溶液中的蛋白质样品,要进质谱。但是不知通过什么样的前处理方式,才能去掉蛋白质溶液中的磷酸盐呢?谢谢!