——胡丽涛、王治国目的 为凝血酶原时间(PT)和活化部分凝血酶时间(APTT)检测提供指南。方法 主要参考美国临床和实验室标准化研究院(CLSI)H47-A2文件相关内容,并结合具体的实际进行总结。结果 PT和APTT检测受到检验前、中和后各种变异的影响。通过检测技术的标准化提高检测的重复性,通过设定性能目标来确保检测的临床相关性。PT检测可用于检测肝素治疗,实验室应该建立肝素治疗范围。结论 对于疑似血液凝固障碍的患者评估,PT和APTT是非常重要的实验室筛查检测。在实际工作中要严格按照操作规程和厂家说明,保证结果的准确可靠,为临床提供诊疗依据。凝血酶原时间;部分活化凝血酶时间;国际标准化比值;校准 自从Quick在1953年首次描述了凝血酶原时间(PT),PT在可疑凝血障碍的患者评估方面成为了一项非常重要的实验室筛查检测,也是实验室最常见的凝血检测。尽管PT最先被描述成一种凝血酶原或凝血因子Ⅱ的特异性一步法检测,但是PT对凝血系统的共同途径和外源性途径所涉及到的任何凝血因子(凝血因子Ⅱ、Ⅴ、Ⅶ、Ⅹ和纤维蛋白原)及因子抑制物的定量或定性的异常都非常敏感。同时,PT也是严重肝脏疾病或慢性肝病的一项适当指标,还是用于监测维生素K治疗最常用的指标。 PT检测的主要试剂凝血活酶是一种磷脂或组织制剂,通常为人源性或动物源性或人和动物的混合材料制成的各种商业化的制剂。这些商业化的凝血活酶制剂在其减少凝血因子的反应性方面存在差异,影响了其使用,特别是在维生素K治疗的检测过程中。 APTT对内源性凝血途径和共同途径的定量和定性异常敏感。是除PT之外,常规实验室最常进行的凝血检测。APTT对内源性凝血途径凝血因子缺乏(凝血因子Ⅷ、Ⅸ、Ⅺ、Ⅻ、前激肽释放酶和高分子激肽原)尤为敏感。APTT检测通常用于监测低分子肝素抗凝治疗。APTT还用于检测其他类型的病理型血液凝固抑制物,最常见的是狼疮抗凝物质(LA)。APTT用于凝血因子替代治疗。APTT的检测试剂是促凝物、磷脂和接触激活剂组成的混合物。磷脂可能来源于人、动物或者植物。激活剂的种类也很多,如硅藻土、高岭土、微粉化的硅土和鞣花酸等。 一般,当凝血因子的活性低于参考区间的95%置信限水平时APTT会延长。但是,大量的研究表明不同的APTT试剂对于轻度和中度的凝血因子缺乏的反应程度存在一定的区别,特别是Ⅷ和Ⅸ因子缺乏。有相似的报道APTT对循环狼疮抗凝物质有不同的敏感性。同样,有文献报道商品化的APTT试剂对肝素的反应性不同,使得APTT值存在显著差异。
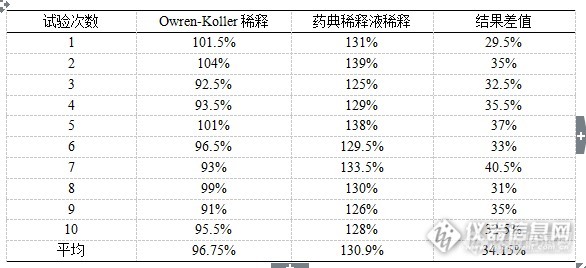
RT 单位买了台凝血分析仪,想了解一些他的工作原理是什么?
[align=center][/align][align=left][b] 摘要:目的 [/b]确立不同稀释液对凝血因子效价检测的影响,研究因子效价检测的稀释方法,从而完善因子类血液制品效价检测的方法。 [b]方法 [/b]对同一批和连续生产的10批人凝血因子Ⅷ、人凝血酶原复合物样品进行全自动血凝仪法的效价检测,分别选用全自动血凝仪稀释液和含1%人血白蛋白稀释液进行检测,统计10次以上的检测结果以确定不同稀释液之间的差别。 [b]结果 [/b]本实验确定了在人凝血因子Ⅷ的效价检测中,采用不同的稀释液对每1 ml约含1.00 IU人凝血因子Ⅷ的样品进行稀释,无论是对同一批质控品的测定还是对连续批次样品的测定,检测结果之间存在较大的差别。而在人凝血酶原复合物人凝血因子Ⅸ的效价检测中,采用不同的稀释液对每1 ml约含1.00 IU人凝血因子Ⅸ的样品进行稀释,同一批质控品和连续批次样品检测结果之间差别较小。[b]结论 [/b]因子类血液制品效价检测时,同一样品采用不同的稀释液进行稀释检测结果可能存在较大差别,应对血凝仪是否可用于因子类血液制品进行评估,并应建立起正确的检测操作规程。[/align][b] 关键词: [/b]凝血因子; 稀释液; 效价测定 目前国内血液制品的生产是以健康人血浆为原料,经过分离纯化和病毒灭活制成,主要分为三大类,人血白蛋白、人免疫球蛋白类产品、人凝血因子类产品。国内已上市或在研的人凝血因子类产品主要有人凝血因子Ⅷ、人凝血酶原复合物、人纤维蛋白原、人纤维蛋白粘合剂、人凝血因子Ⅸ、人抗凝血酶Ⅲ等。人凝血因子Ⅷ主要用于防治甲型血友病和获得性凝血因子Ⅷ缺乏而致的出血症状病人的手术治疗。人凝血酶原复合物主要有效成分为人凝血因子Ⅱ、Ⅶ、Ⅸ、Ⅹ,主要用于治疗主要用于乙型血友病、 维生素K依赖的凝血因子缺乏症等病症的治疗。 人凝血因子Ⅸ主要用于防治乙型血友病和获得性凝血因子Ⅸ缺乏而致的出血症状病人的手术治疗。因子类血液制品是血液中凝血因子的高纯度浓缩物,在进行效价测定时需要对样品进行稀释,而稀释液中蛋白含量的不同对其检测结果有着影响。因子效价测定方法有一期法、二期法和发色底物法。一期法是目前应用最广泛的检测方法,系用人凝血因子缺乏血浆为基质,在APTT试剂和氯化钙的参与下,根据凝血因子国家标准品和供试品的凝集时间来计算供试品中的人凝血因子效价,实际检测过程中将基于一期法原理的人凝血因子效价测定法分为三种方法,即手工法、半自动血凝仪法、全自动血凝仪法。全自动血凝仪只是对一期法中各反应试剂的加入顺序进行了修订以便实现仪器的自动操作。相对于手工法检测,消除了很多主观因素。在日常工作中,当使用不同种类的稀释剂而采用相同的检测原理和方法进行效价测定应不会对测定结果产生影响,但实际工作中发现使用不同种类的稀释剂对效价测定结果有一定的影响。在人凝血因子Ⅷ效价检测过程中,采用手工法、半自动血凝仪法、全自动血凝仪法进行人凝血因子Ⅷ效价的比对试验,发现手工法、半自动血凝仪法检测结果一致,这两种方法比全自动血凝仪法的检测结果高20%以上。血液制品的原料来源于人血浆,受原料限制,一直较为稀缺,尤其是当前人凝血因子Ⅷ的生产量远远无法满足血友病患者的需求[sup][[/sup][sup]1-5[/sup][sup]][/sup],不同检测方法间20%以上的检测差别可能影响20%的产品收率,所以建立起因子类产品效价准确的检测至关重要。[b][b]1 实验仪器与试剂1.1 仪器[/b][/b]Stago-compact全自动血凝仪(法国Diagnostica Stago公司),漩涡振荡器(美国Thermo Scientific公司)。[b][b]1.2 试剂[/b][/b]人凝血因子Ⅷ缺乏血浆(法国Diagnostica Stago公司),人凝血因子Ⅸ缺乏血浆(法国Diagnostica Stago公司),APTT试剂(法国Diagnostica Stago公司),Owren-Koller(稀释液)(法国Diagnostica Stago公司),0.025 mol/L氯化钙溶液(法国Diagnostica Stago公司),Desorb U(清洗液)(法国Diagnostica Stago公司),人凝血因子Ⅷ国家标准品(批号20100101),人凝血酶原复合物国家标准品(批号20130306),生理氯化钠溶液(石家庄四药有限公司),咪唑(天津市巴斯夫化工有限公司),氯化钠(天津市巴斯夫化工有限公司),枸橼酸钠(台山新宁制药有限公司),人血白蛋白(公司自产)。[b][b]2 方法2.1 人凝血因子Ⅷ不同稀释液稀释效价测定2.1.1 人凝血因子Ⅷ供试品Owren-Koller(稀释液)稀释效价测定方法[/b][/b] 人凝血因子Ⅷ国家标准品的定标:取1支人凝血因子Ⅷ国家标准品,加入1.0 ml纯化水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml含1.00 IU人凝血因子Ⅷ,将Desorb U(清洗液)、复溶后的人凝血因子Ⅷ缺乏血浆、0.025 mol/L氯化钙溶液、APTT以及每1ml含1.00 IU的人凝血因子Ⅷ标准品溶液分别装入全自动血凝仪的试剂抽屉,将Owren-Koller(稀释液)装入全自动血凝仪的样本抽屉,按照《Stago-compact全自动血凝仪标准操作规程》选择人凝血因子Ⅷ效价测定定标程序进行定标,仪器自动将装入的人凝血因子Ⅷ标准品溶液再进行2倍、4倍、8倍稀释,建立人凝血因子Ⅷ标准品溶液效价(分别为1.00 IU/ml、0.50 IU/ml、0.25 IU/ml、0.13 IU/ml)的对数对其相应凝固时间对数的直线回归方程。人凝血因子Ⅷ供试品效价测定:取人凝血因子Ⅷ供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml约含1.00 IU人凝血因子Ⅷ,再用Owren-Koller(稀释液)做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅷ效价测定选项进行测定。[b][b]2.1.2 人凝血因子Ⅷ供试品药典稀释液稀释效价测定方法[/b][/b] 人凝血因子Ⅷ国家标准品的定标同2.1.1人凝血因子Ⅷ供试品效价测定:取人凝血因子Ⅷ供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml约含1.00 IU人凝血因子Ⅷ,再用药典稀释液(取1体积的3.8%枸橼酸钠加入5体积咪唑缓冲液混合,加适量20%人血白蛋白至终浓度为1%配制而成)做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅷ效价测定选项进行测定。[b][b]2.2 人凝血酶原复合物人凝血因子Ⅸ不同稀释液稀释效价测定2.2.1 人凝血酶原复合物供试品Owren-Koller(稀释液)稀释效价测定方法[/b][/b] 人凝血因子Ⅸ国家标准品的定标:取1支人凝血酶原复合物国家标准品,加入1.0 ml纯化水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml含1.00 IU人凝血因子Ⅸ,将Desorb U(清洗液)、复溶后的人凝血因子Ⅸ缺乏血浆、0.025 mol/L氯化钙溶液、APTT以及每1ml含1.00 IU的人凝血因子Ⅸ标准品溶液分别装入全自动血凝仪的试剂抽屉,将Owren-Koller(稀释液)装入全自动血凝仪的样本抽屉,按照《STAGO Compact全自动血凝仪标准操作规程》选择人凝血因子Ⅸ效价测定定标程序进行定标,仪器自动将装入的人凝血因子Ⅸ标准品溶液再进行2倍、4倍、8倍稀释,建立人凝血因子Ⅸ标准品溶液效价(分别为1.00 IU/ml、0.50 IU/ml、0.25 IU/ml、0.13 IU/ml)的对数对其相应凝固时间对数的直线回归方程。 人凝血酶原复合物供试品效价测定:取人凝血酶原复合物供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml约含1.00 IU人凝血因子Ⅸ,再用Owren-Koller(稀释液)做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅸ效价测定选项进行测定。[b][b]2.2.2 人凝血酶原复合物供试品药典稀释液稀释效价测定方法[/b][/b] 人凝血因子Ⅸ国家标准品的定标同2.1.1。人凝血酶原复合物供试品效价测定:取人凝血酶原复合物供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml约含1.00 IU人凝血因子Ⅸ,再用药典稀释液(取1体积的3.8%枸橼酸钠加入5体积咪唑缓冲液混合,加适量20%人血白蛋白至终浓度为1%配制而成)做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅸ效价测定选项进行测定。[b][b]3 结果3.1 人凝血因子Ⅷ不同稀释液稀释效价测定结果[/b][/b] 2015ZK0801批人凝血因子Ⅷ为泰邦公司人凝血因子Ⅷ产品的质控品,取自正常生产的产品,用国家标准品标定后用作工作质控品。在进行人凝血因子Ⅷ效价测定时,分别用Owren-Koller(稀释液)和药典稀释液(取1体积的3.8%枸橼酸钠加入5体积咪唑缓冲液混合,加适量20%人血白蛋白至终浓度为1%配制而成)对每1 ml约含1.00 IU人凝血因子Ⅷ进行再稀释。检验结果见表1,效价检测结果为效价标示量的百分比。[align=center]表1 FⅧ质控品两种稀释液检测结果对比[/align][align=center][img=,586,268]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141920_02_1626619_3.png[/img][/align]用柱形图表示,如图1:[align=center][img=,488,300]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141921_02_1626619_3.png[/img][/align][align=center]图1 FⅧ质控品两种稀释液检测结果对比[/align] 选取泰邦公司生产的连续10个批次的人凝血因子Ⅷ产品,进行人凝血因子Ⅷ效价测定,分别用Owren-Koller(稀释液)和药典稀释液(取1体积的3.8%枸橼酸钠加入5体积咪唑缓冲液混合,加适量20%人血白蛋白至终浓度为1%配制而成)对每1 ml约含1.00 IU人凝血因子Ⅷ进行再稀释。检验结果见表2,效价检测结果为效价标示量的百分比。[align=center]表2 连续10批FⅧ两种稀释液检测结果对比[/align][align=center][img=,580,273]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141921_03_1626619_3.png[/img][/align]用柱形图表示,如图2:[align=center][img=,499,310]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141922_01_1626619_3.png[/img][/align][align=center]图 2 连续10批FⅧ两种稀释液检测结果对比[/align][b][b]3.2 人凝血酶原复合物不同稀释液稀释效价测定结果[/b][/b] 2015ZK0901批人凝血酶原复合物为泰邦公司人凝血酶原复合物产品的质控品,取自正常生产的产品,用国家标准品标定后用作工作质控品。在进行人凝血酶原复合物人凝血因子Ⅸ效价测定时,分别用Owren-Koller(稀释液)和药典稀释液(取1体积的3.8%枸橼酸钠加入5体积咪唑缓冲液混合,加适量20%人血白蛋白至终浓度为1%配制而成)对每1 ml约含1.00 IU人凝血因子Ⅸ进行再稀释。检验结果见表3,效价检测结果为效价标示量的百分比。[align=center]表3 PCC质控品两种稀释液检测结果对比[/align][align=center][img=,580,269]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141923_01_1626619_3.png[/img][/align]用柱形图表示,如图3:[align=center][img=,548,288]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141923_02_1626619_3.png[/img][/align][align=center]图3 PCC质控品两种稀释液检测结果对比[/align] 选取泰邦公司生产的连续10个批次的人凝血酶原复合物产品,进行人凝血酶原复合物人凝血因子Ⅸ效价测定,分别用Owren-Koller(稀释液)和药典稀释液(取1体积的3.8%枸橼酸钠加入5体积咪唑缓冲液混合,加适量20%人血白蛋白至终浓度为1%配制而成)对每1 ml约含1.00 IU人凝血因子Ⅸ进行再稀释。检验结果见表4,效价检测结果为效价标示量的百分比。[align=center]表4 连续10批PCC两种稀释液检测结果对比[/align][align=center][img=,573,259]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141947_01_1626619_3.png[/img][/align]用柱形图表示,如图4:[align=center][img=,548,327]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141947_03_1626619_3.png[/img][/align][align=center]图4 连续10批PCC两种稀释液检测结果对比[/align][b][b]4 讨论[/b][/b] 本实验确定了在人凝血因子Ⅷ的效价检测中,采用不同的稀释液对每1 ml约含1.00 IU人凝血因子Ⅷ的样品进行稀释,无论是对同一批质控品的测定还是对连续批次样品的测定,检测结果之间存在较大的差别,另外对FⅧ质控品两种稀释液检测结果运用软件SPSS17.0进行均值单因素ANOVA比较,计算P值,P<0.05表明两种方法的结果有显著性差异,含有蛋白的稀释液的检测结果明显高于不含蛋白的稀释液。而在人凝血酶原复合物人凝血因子Ⅸ的效价检测中,采用不同的稀释液对每1 ml约含1.00 IU人凝血因子Ⅸ的样品进行稀释,同一批质控品和连续批次样品检测结果之间差别较小,另外对PCC质控品两种稀释液检测结果运用软件SPSS17.0进行均值单因素ANOVA比较,计算P值,P>0.05表明两种方法的结果无显著性差异。在使用全自动血凝仪进行人凝血因子Ⅷ和人凝血酶原复合物等因子类血液制品效价检测时,一般按照仪器的使用说明书和配套试剂进行稀释检测,但是忽视了血凝仪的开发目的是用于临床血浆样品的检测,而血浆与高纯度的血液制品浓缩物是不同的,用检测血浆样品的方法进行因子类血液制品的效价检测可能影响检测结果。因子类血液制品效价检测时,同一样品采用不同的稀释液进行稀释检测结果可能存在较大差别,应对血凝仪是否可用于因子类血液制品进行评估,并应建立起正确的检测操作规程。因子类血液制品采用不同的稀释液进行稀释检测结果可能存在较大差别可能跟产品本身的性质有关,因子类血液制品经过分离、纯化,去除了众多的杂质蛋白,为高纯度的浓缩物,活性较高,但蛋白质含量较低,人凝血因子Ⅷ的蛋白质含量约为0.1%,人凝血酶原复合物的蛋白质含量约为2.3%,而临床血浆样本的蛋白质含量约为5%,, 人凝血因子Ⅷ加入含1%人血白蛋白的稀释液后对FⅧ效价测定影响较大,PCC中加入含1%人血白蛋白的稀释液后对FⅨ效价测定影响较小,可能是人凝血因子Ⅷ的蛋白质含量远小于血凝仪设计用于检测的血浆样本的蛋白含量,故建立不同蛋白质浓度梯度的稀释液对因子效价进行测定,从而确认蛋白质浓度对因效价测定的影响。[b]参考文献:[/b]Cheng E, Jinzenji D, Lorthiois AP, et al. Purification of coagulation factorⅧ using chromatographic methods. Direct chromatography of plasma in anion exchange resins . Biotechnol Lett, 2010, 32(9):1207-1214.李策生, 周志军, 胡勇, 等. 人凝血因子Ⅷ中试纯化工艺的质量控制 .中国生物制品学杂志, 2013, 26(10):1508-1512.冉曙光, 刘文芳, 赵辉. 凝血因子Ⅷ浓缩物的制备及安全性和有效性 .中国输血杂志, 2008, 21(2):156-159.倪道明, 朱威. 血液制品 . 北京: 人民卫生出版社, 2013:21.王卓, 赵雄, 吕茂民, 等. 血液制品的现状与展望 . 生物工程学报, 2011, 27(5):730-746.[b] [/b]
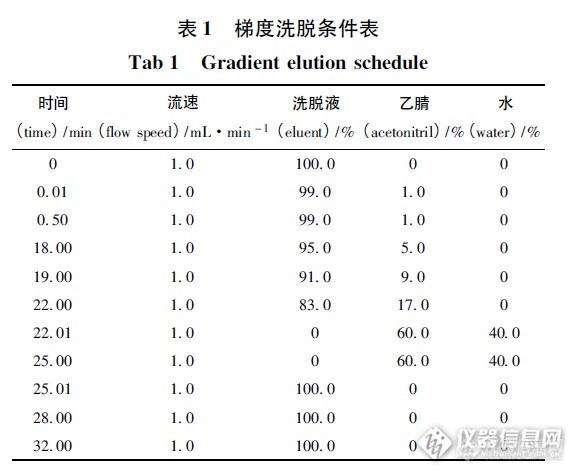
人凝血因子VIII中氨基酸含量测定摘要 目的: 建立用高效液相色谱法测定人凝血因子VIII中氨基酸含量。方法: 采用6 - 氨基喹啉- N - 羟基琥珀酰亚氨基氨基甲酸酯( AQC) 为衍生剂,与氨基酸柱前衍生后,用Agilent 1200 高效液相色谱仪,AccQ·Tag C18柱( waters 150 mm ×3. 9 mm,4 μm) ,以水Eluent( 醋酸盐- 磷酸盐缓冲液) 稀释液和乙腈进行梯度洗脱,检测波长为248 nm,柱温37 ℃,进样量10μL。结果: 各氨基酸在32 min 内测定完毕,回收率为98.7% ~ 101.5%。RSD 均小于1. 5%。结论: 本法分离度好,快速、简便,可作为产品的质量控制方法。关键词: 6 - 氨基喹啉- N - 羟基琥珀酰亚氨基氨基甲酸酯; 人凝血因子VIII; 甘氨酸; 衍生物; 梯度洗脱; 高效液相色谱法;氨基酸; 含量测定人凝血因子VIII,本品对缺乏人凝血因子礓所致的凝血机能障碍具有纠正作用,主要用于防治甲型血友病和获得性凝血因子Ⅷ缺乏而致的出血症状及这类病人的手术出血治疗。该药物制备过程中使用了氨基酸( 精氨酸、丙氨酸、甘氨酸、组氨酸、盐酸赖氨酸、脯氨酸 等) 做稳定剂,为了保证药品质量和用药安全,应对其中氨基酸的含量进行控制。该法依据过量的6 - 氨基喹啉基- N - 羟基琥珀酰亚氨基氨基甲酸酯( AQC) 在一定条件和氨基酸形成稳定的衍生产物( 柱前衍生) ,用高效液相色谱法测定衍生产物,根据衍生产物的含量计算人凝血因子中各氨基酸的含量。1 仪器和试药1200 高效液相色谱系统( 美国Agilent 公司) ,配置低压四元梯度泵、1314B 紫外吸收检测器、自动进样器、柱温箱、Chemistations 化学工作站; Sartorius CP225D 电子微量天平( 德国Sartorius 公司) ; SartoriusPB - 21 型pH 计( 德国Sartorius 公司) ; LDZ5 -2 低速自动平衡离心机( 上海医用离心机厂) 等。各标准品均来自于中国食品药品检定研究院2 色谱条件及系统适用性试验色谱柱: Waters AccQ·Tag C18色谱柱( 3. 9 mm ×150 mm) ; 流动相: 水为溶剂D,Eluent( 醋酸盐- 磷酸盐缓冲液) 稀释液( A) - 乙腈( B) - 水( D) ,柱温:37 ℃; 检测波长: 248 nm。精密量取对照品溶液与供试品溶液10 μL,分别注入液相色谱仪,记录色谱图32 min。梯度洗脱条件表见表1。http://ng1.17img.cn/bbsfiles/images/2015/08/201508311802_563771_1637386_3.png
摘要: 目的 对人凝血因子Ⅷ酸沉淀过程效价和总蛋白建立近红外模型,实现效价和总蛋白的快速检测,并以此确定酸沉终点。 方法 实验室模拟人凝血因子Ⅷ酸沉淀过程,对不同酸沉程度下的效价和总蛋白进行测定,同时采集近红外光谱,建立模型。结果 酸沉淀过程中FⅧ比活性达到最高时的pH值并不固定,在6.1-6.5范围内波动,所以将固定的pH值作为酸沉淀的终点并不能达到最佳的效果。结论 建立的人凝血因子Ⅷ酸沉过程中效价和总蛋白模型,固定加酸法不能准确判断酸沉最佳终点,所建立的近红外分析模型为在线实时监控溶解液中的FⅧ比活性提供参考方案。 关键词:近红外光谱分析技术 人凝血因子Ⅷ 酸沉 效价 总蛋白人凝血因子Ⅷ(coagulationfactor Ⅷ,FⅧ)是治疗甲型血友病和获得性凝血因子Ⅷ缺乏而致的出血症状等的不可或缺的药品,而目前国内生产工艺相对落后,在国内29家血液制品企业中仅有4家有能力生产FⅧ,采用离子交换层析法从人血浆冷沉淀中分离纯化FⅧ的生产工艺,收率低(平均9%)、比活低。因此,针对生产现状,将现代过程分析与控制技术引入到FⅧ生产过程中的关键环节当中,增加对生产工艺过程的了解,有效控制工艺过程,提升FⅧ的收率及比活性。生产人凝血因子Ⅷ以人血浆的冷沉淀为原料,一般用含肝素钠的溶解液溶解,溶解液pH为7.2±0.1。溶解完全后依据不同蛋白质的等电点不同,加0.05M的醋酸溶液进行酸沉淀,使以纤维蛋白原为主的大量杂蛋白沉淀出来,而FⅧ大部分保留在上清液中,从而大大提升溶液的FⅧ比活性。在生产中,酸沉淀终点的控制依据经验以溶液的pH值为参考,当溶液的pH值为6.3±0.1时加酸过程终止,此时上清液中的蛋白含量较低而FⅧ的活性损失较少,因此能够得到FⅧ比活性高的产品。但是单纯以pH值为控制参数的终点控制方法,不一定能够保证不同批次的酸沉淀过程都达到最理想的状态,本试验将对FⅧ的酸沉淀过程进行分析,以检验是否不同批次溶解液的FⅧ比活性在pH=6.3时都达到最高值,并试图找到与比活性直接相关的物料参数——蛋白质含量作为酸沉淀终点的控制标准,使溶解液中FⅧ的比活提升和活性损失达到更均衡的状态。同时,利用近红外光谱分析技术,建立溶解液蛋白含量的PLS定量分析模型,进行蛋白含量的实时监控,从而实现以新参数为指标的酸沉淀终点控制。1 材料1.1 试剂 冷沉淀溶解液(山东泰邦生物制品有限公司),批号分别为201435、201436、201437、201438、201439,每批留样200mL;BCA试剂盒(碧云天生物技术研究所);凝血因子Ⅷ促凝活性检测试剂盒(成都协和生物技术中心);醋酸(国药集团化学试剂有限公司,分析纯);三蒸水。1.2 仪器 Antaris II傅里叶变换近红外光谱仪(美国ThermoFhisher公司);PB-10酸度计(德国sartorius公司);BF300恒流泵(保定齐力恒流泵有限公司);JB-3A型恒温磁力搅拌器(上海雷磁创益仪器仪表有限公司);Legendmicro 17R离心机(美国ThermoFhisher公司);TW12恒温水浴箱(德国Julabo公司);3001-1890酶标仪(美国ThermoFhisher公司)。2 方法2.1 样品的制备2.1.1 配制醋酸溶液 量取醋酸约3.0mL,加入适量蒸馏水中,然后加蒸馏水至1.0L,得到浓度约为0.05M的醋酸溶液,混匀后用0.22 μm膜过滤。2.1.2 酸沉淀过程 参照实际生产过程,在实验室进行小试规模的酸沉淀过程。将超低温冻存的冷沉淀溶解液约100mL放至室温融化,缓慢倒入烧杯中,将烧杯置于低温水浴中,用酸度计监测溶解液的pH值和温度,然后以1mL/min的速度滴加配制好的醋酸溶液,边加边搅拌,使溶液的pH值由7.2左右降低至5.9左右,此过程中溶解液的温度由室温(25℃)均匀降低至15 ℃。重复进行此实验10次,每次实验过程之间保证相同的环境温度、水浴温度、醋酸浓度、加酸速度和搅拌速度。每次酸沉淀过程中pH值每变化0.1取样800μL,取样后立即进行离心(10000 rpm,5min),保留上清液作为样品,进行后面的光谱采集和蛋白含量及FⅧ效价的测定。2.2 近红外光谱的采集 选择AntarisII光谱仪的透射模块进行上清液光谱的采集。选用4 mm光程的比色皿,加样量约为400μL,光谱扫描范围为10000-4000 cm-1,扫描次数为32次,分辨率为8cm-1,以空气为参比进行采集,每隔1小时校正一次背景,测量环境为室温,湿度30%-50%。2.3 FⅧ效价的测定 使用凝血因子Ⅷ促凝活性检验试剂盒对上清液中的FⅧ效价进行检测,试剂盒中包含正常凝血质控血浆、缺凝血因子Ⅷ血浆,APTT试剂b/a、稀释液、CaCl2溶液,现用现配。2.3.1 标准曲线的制作 除氯化钙溶液在37℃水浴预热外,其余样品、试剂均置冰水浴中。 1)将正常凝血质控血浆用稀释液1作1/2、1/5、1/10、1/20、1/40、1/80倍比稀释,其对应FⅧ:C百分活性为500%、200%、100%、50%、25%、12.5%。 2)取某一稀释度正常凝血质控血浆0.1mL、缺凝血因子Ⅷ血浆0.1 mL、APTT试剂0.1mL于透明小试管,混匀后即置37℃水浴温浴10min。 3)迅速加入氯化钙溶液0.1mL,同时启动秒表,在水浴中以1-2次/秒的频率摇动小试管,当观察到凝固出现时,立刻停表记录凝固时间。 4)以不同稀释度正常凝血质控血浆FⅧ:C百分活性为X,对应的凝固时间(秒)为Y,按照统计学方法作直线回归方程,方程形式为Y=blog X+ a,即得标准曲线。2.3.2 样品效价的测定 1)将上清液用稀释液1作1/100倍稀释,即取10µL样品液加稀释液990µL,以此代替标准曲线制作项中某一稀释度正常凝血质控血浆,按照同样方法测定凝固时间。 2)将样品凝固时间(秒)代入标准曲线方程,计算X值,即得样品FⅧ:C百分活性水平。2.4 总蛋白含量的测定样品上清液中总蛋白质的含量测定采用Bicinchoninicacid(BCA)法。BCA法是应用较为广泛的蛋白定量方法之一,其原理是在碱性条件下,蛋白质与Cu2+络合,使之还原成Cu1+,Cu1+可与BCA形成稳定的蓝紫色复合物,复合物在561nm处有强吸收且吸收值与蛋白浓度成正比。BCA法原理与Lowery法相似,但是灵敏度高,操作简单,稳定性好,干扰物质对其影响也较小。2.4.1 配制工作溶液 将BCA试剂盒铜试剂按照体积比50:1混合,得到嫩绿色的标准工作试剂(WorkingReagent,WR),WR在室温条件下十分稳定。2.4.2 配制标准蛋白溶液配制0.5 mg/mL的BSA蛋白溶液,在96孔板中用PBS缓冲液对BSA溶液进行稀释,得到相同体积的BSA标准溶液0、25、50、100、200、300、400、500μg/mL,每个浓度的BSA标准溶液再各加200μL WR。具体稀释方案如表1所示。2.4.3 测定蛋白浓度每个样品取2 μL置于96孔板中,加18μL PBS缓冲液,然后加200 μL WR,在37℃培养箱中放置30min。将反应温度冷却至室温,用酶标仪测定标准蛋白溶液和样品溶液在561 nm处的吸光度值,绘制标准曲线,计算样品的蛋白浓度。表1 标准蛋白溶液和待测样品的加样量和比例 孔数 蛋白浓度(μg/mL) 标准或待测蛋白溶液体积(μL) PBS缓冲液体积(μL) WR体积(μL) 1 0 [ali
蕲蛇蛇毒中凝血酶样酶的分离纯化与特性[~119829~][~119828~]
【序号】:1【作者】: 于佳鑫【题名】:壳聚糖止血粉促凝血作用的实验研究【期刊】:影像研究与医学应用. 【年、卷、期、起止页码】:2018,2(05)【全文链接】:https://kns.cnki.net/kcms/detail/detail.aspx?dbcode=CJFD&dbname=CJFDLAST2018&filename=YXYY201805159&uniplatform=NZKPT&v=PHm7p9Rc2CgPScGXeXyvUFix-WBMA12jeytsIyDnJZXLw-WSRFCaK9jDGAkjOwc9
[b][font=inherit]项目概况[/font][/b]HPV试剂、生化凝血和血常规试剂采购项目招标项目的潜在投标人应在全国公共资源交易平台(陕西省西安市)网站〖首页〉电子交易平台〉陕西政府采购交易系统〉企业端〗获取招标文件,并于 2022年12月29日 09时30分 (北京时间)前递交投标文件。[b][font=inherit]一、项目基本情况[/font][/b]项目编号:SXZBXA2022-37项目名称:HPV试剂、生化凝血和血常规试剂采购项目采购方式:公开招标预算金额:3,350,000.00元采购需求:合同包1(诊断试剂):合同包预算金额:3,350,000.00元合同包最高限价:3,350,000.00元[table=100%][tr][td]品目号[/td][td]品目名称[/td][td]采购标的[/td][td]数量(单位)[/td][td]技术规格、参数及要求[/td][td]品目预算(元)[/td][td]最高限价(元)[/td][/tr][tr][td]1-1[/td][td]诊断用生物试剂盒[/td][td]HPV试剂、生化检测试剂、凝血和血常规检测试剂[/td][td]1(批)[/td][td]详见采购文件[/td][td]3,350,000.00[/td][td]3,350,000.00[/td][/tr][/table]本合同包不接受联合体投标合同履行期限:具体时间以合同上签订时间为准。
建立了使用石墨炉原子吸收分光光度法检测人凝血因子VIII中铝含量的分析方法,探讨了以非离子表面活性剂Triton X-100,基体改进剂,干燥温度和气体流量对实验结果的影响.在最佳工作条件下,铝的检测限为0.8μg/l;样品测得的相对标准偏差(n=6)为5.6%,加标回收率94.5%~103.5 %。方法适合人凝血因子VIII中铝离子残留量的分析测定。关键词:铝;石墨炉原子吸收分光光度法;人凝血因子VIII,残留量 铝是一种人体非必需的微量元素, 如果摄入过多, 将会严重影响人体的神经系统, 不仅使老年人易患痴呆病,还会引发慢性肾功能损害等病症, 故世界卫生组织及欧洲药典等均将铝含量的测定作为成品检定项目之一。 人凝血因子VIII辅料中加入Al2O3作为吸附剂,因此其在制剂中需对其残留量进行检测。由于其制剂成分复杂、有机物干扰严重、某些样品中的铝含量极低, 有些分析方法检出限达不到要求。石墨炉原子吸收光谱法是铝残留量分析中常用的方法之一。 本文采用非离子表面活性剂Triton X-100,基体改进剂硝酸镁 ,建立了石墨炉原子吸收分光光度法检测人凝血因子VIII中铝离子残留量的分析方法。1 实验部分1 .1 仪器与试剂ICE 3400GF 型原子吸收光谱仪(美国Thermo公司):ID100 自动稀释器,Chill I冷却水系统,GFS35Z石墨炉,自参比单光束塞曼系统, GFS 石墨炉自动进样器, 涂层石墨管(Extended Lifetime Cuvettes);铝空心阴极灯;ELGA Q15 纯水机。HNO3为MOS级;100μg/mL铝元素标准溶液(GSB 04-1713-2004) , 标准工作溶液均由以上溶液经超纯水逐级稀释而成的;稀释液:1%(v/v)硝酸+0.01%(v/v)Triton X-100(化学纯试剂);2.5g/L Mg(NO3)2 基体改进剂:称取0.25g分析纯Mg(NO3)2到PPE塑料烧杯中, 用超纯水溶解定容至100mL PPE塑料容量瓶中。实验所用水为电阻率为18.2 MΩ·cm 的超纯水。1 .2 样品预处理1.2.1 供试品溶液 精密量取供试品溶液0.2ml,加稀释液2.3ml。1.2.2 混合溶液 精密量取供试品溶液0.2ml,加入100μg/L标准铝溶液0.50ml,再加稀释液1.8ml。1 .3 实验方法准确移取稀释液、供试品溶液、混合溶液倒入自动进样器的样品杯中, 再通过自动进样器进样后由石墨炉原子吸收光谱仪进行铝含量的测定。1 .4 仪器工作条件石墨炉原子吸收光谱仪测定铝时的工作参数设置和石墨炉升温程序见表1 和表2 。表1 石墨炉原子吸收光谱仪的操作参数Tab.1 Operating parameters for GFAAS电流 I/mA测定波长 λ/nm缝隙宽度 l/nm测定模式进样量 V/µL基体改进剂8309.30.5峰高102.5g/L Mg(NO3)2 表2 石墨炉升温程序Tab.2 Graphite furnace heating program步骤程序温度 ℃时间 s斜坡 ℃/s气体类型气体流量 l/min1干燥8010.00氩气0.22干燥1105.03氩气0.13干燥2205.01氩气0.24灰化150010.00氩气0.15原子化26005.00氩气06清除26505.00氩气0.3 1 .5 工作曲线的制作将0
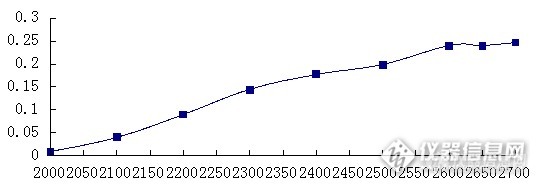
摘要:目的 建立一种快速测定人凝血因子Ⅷ冷冻干燥过程中水分含量的方法。 方法 首先采用卡尔费休容量滴定法测定不同冻干程度的人凝血因子Ⅷ的水分含量,做为一级数据,并同时采集样品的近红外光谱;采用K-S方法对样品集进行划分,学生化残差-杠杆值去除异常样品,考察不同的光谱预处理方法,利用iPLS和GA对建模波段进行选择,以R2、RMSEC、RMSECV、RMSEP值为模型评价指标。 结果 所建立模型的主要参数为R2=0.918,RMSEC=0.2141,RMSECV =0.4102,RMSEP=0.3848,线性较好,光谱与样品的水分含量有较好的相关性。结论 建立的FⅧ成品的水分含量模型满足生产需求,是一种快速无损的检测方法,同时减少了FⅧ样品和卡尔费休试剂等的损耗,是一种十分经济有效的方法。关键词:近红外光谱分析技术 人凝血因子Ⅷ 水分 冻干血液制品在医疗急救和某些特定遗传疾病治疗上具有其他药品无法替代的作用,但我国当前整个血液制品行业长期处于供不应求的状态,因此提高血浆综合利用率、增加各产品的收率是解决现状的一个必要举措。其中人凝血因子Ⅷ(coagulation factor Ⅷ, FⅧ)是治疗甲型血友病和获得性凝血因子Ⅷ缺乏而致的出血症状等不可或缺的药品,而目前国内生产工艺相对落后,少数企业有能力生产FⅧ。水分是确保产品质量的一个重要参数,它的含量和存在形式对FⅧ的结构和功能影响很大,直接关系到FⅧ产品的稳定性。在生产中,通过冷冻干燥使FⅧ制剂的水分含量在3.0%以下。但是冻干过程无法取样,只能依据经验,通过观察冻干曲线对冻干条件和冻干时间进行控制,无法直接对产品水分含量进行判定;而产品的水分含量测定采用常规的卡氏水分测定方法,具有破坏性切费时费力,而且测定结果无法代表整批产品的特性。近红外光谱分析技术(Near InfraredSpectroscopy,NIRS)是当前最重要的一种PAT技术,它是指应用波长范围在780-2526nm波长范围内的电磁波的一种光谱学方法,在制药、医学诊断、食品和农产品的质量控制,天文学以及治疗医学等领域都有应用。本实验室采用近红外光谱分析技术,对产品进行快速、无损隔瓶测定,并可以实现多点测控,测定冻干产品中的水分含量,以判断干燥终点。1 材料1.1 试剂人凝血因子Ⅷ(冻干剂,200IU/瓶,山东泰邦生物制品有限公司);甲醇(分析纯,国药集团化学试剂有限公司);卡尔·费休试剂(KFR-06型,天津市科密欧化学试剂有限公司);注射用水。1.2 仪器Antaris Ⅱ傅里叶变换近红外光谱仪(美国Thermo Fisher scientific公司),附件配置:积分球漫反射检测器;KF-4型自动水分测定仪(南京科环分析仪器有限公司);Alpha 1-2 LD实验室型冻干机(德国Christ公司);VD-53真空干燥箱(德国Binder公司);EL204电子天平(METTLER TOLEDO公司)。2 方法2.1 样品的制备取若干瓶FⅧ冻干剂,每瓶加10mL注射用水溶解完全,置于-80℃超低温冰箱预冻2h以上。开启冻干机,使冷阱降温至-55℃,并将真空泵预热。取出预冻完全的FⅧ,放置在干燥室内的搁板上,抽真空开始升华干燥,干燥过程中搁板温度约为-20℃,真空度为10Pa。升华干燥的时间为12-48h不等,到时间后关闭真空泵,通过真空密封阀门使干燥室通气,取出样品。选取部分升华干燥时间在24h以上的样品,转移至真空干燥箱内,进行解析干燥,其余样品封盖密封保存。解析干燥的温度为32℃,真空度为10Pa,干燥时间为5-24h不等。干燥结束后取出样品,压盖密封保存。最终共得到88个样品,通过控制干燥时间的不同使获得的样品拥有不同的水分含量,而且能够涵盖使用该模型预测样品水分时可能遇到的浓度范围,以保证未知样品水分含量的预测是通过模型内插进行分析的,从而使模型具有有效性和实用性。2.2 光谱的采集本实验使用Antaris Ⅱ傅里叶变换近红外光谱仪,包括带InGaAs检测器的积分球漫反射分析模块,采用仪器自带的RESULT-Intergration软件编写采集光谱的工作流程。仪器的主要工作参数为:光谱扫描范围为10000cm-1-4000cm-1,分辨率为8cm-1,光谱扫描次数为32,每个样品在不同部位采集3张光谱。近红外漫反射光谱吸收强度设定为lg(1/R)。启动仪器,预热至少30分钟,检查仪器各项性能是否正常。采用仪器自带的RESULT-Operation采集光谱,调用编写好的工作流程,将装有样品的西林瓶直接放在通光孔并固定位置,即可采集样品的傅里叶变换近红外光谱数据。2.3 水分含量的测定依据《中国药典》三部附录VII D 水分测定法第一法—卡尔费休容量滴定法,测定样品的水分含量。2.4 建立校正模型在MATLAB中运行PLS_Toolbox工具箱进行数据处理,采用PLS建立FⅧ冻干过程中水分含量的定量分析模型。用K-S分类的方法将样品划分为校正集和验证集。根据学生化残差和杠杆值等统计指标识别并去除异常样品。对光谱数据进行必要的平滑、求导等预处理,以消除噪声和基线漂移等的影响。使用iPLS和GA等方法选择光谱区间,优选与水分含量相关性强的谱区,减少无效信息的使用。3 结果3.1 样品制备及水分含量测定结果共制备得到88个样品,水分含量范围为1.00%-5.30%。其中1-60号样品只进行了不同时间的升华干燥,水分含量在2.04%-5.30%之间;61-88号样品在升华干燥后进行了不同时间的解析干燥,水分含量在1.00%-2.75%之间。3.2 样品的近红外光谱所有88个样品的原始近红外漫反射光谱如图1所示。从图中可发现,样品光谱的基线漂移十分严重,所以必须进行适当的预处理,以消除基线漂移以及光谱噪声等的影响。水分子的O-H在近红外谱区有两个特征谱带:5150cm-1的组合频吸收和6950cm-1的OH伸缩振动一级倍频吸收。这两个特征吸收是建模时选择光谱区间的重要依据。data:image/png;base64,iVBORw0KGgoAAAANSUhEUgAAAz4AAAF2CAMAAACYgb3CAAAAAXNSR0ICQMB9xQAAALpQTFRFAAAAAAA6AABmAAD/ADo6ADqQAH8AAGa2AL+/OgAAOgA6OgBmOjoAPz8/Ojo6OjpmOjqQOmZmOma2OpCQOpC2OpDbZgAAZgA6ZgBmZjoAZjqQZmY6ZmZmZma2ZpCQZrbbZrb/kDoAkDo6kDpmkGZmkGaQkJA6kJBmkLaQkNvbkNv/vwC/tmYAtmY6tmZmtpA6v78Atv+2tv//25A627a22//b2////wAA/7Zm/7a2/9uQ//+2///b////FbtuvwAAAAlwSFlzAAAWJQAAFiUBSVIk8AAAABl0RVh0U29mdHdhcmUATWljcm9zb2Z0IE9mZmljZX/tNXEAADorSURBVHja7Z0Ngxs5cp5nDzkI6wscx8nuXRyfrb2LE1vQXWApWSiS8P//VvBWAWh0s5tfQ3JmyLd2NcOPZqPJwcP6QKHqKVMolDPliR8BhUJ8KBTiQ6EQHwqF+FAoFOJDoRAfCoX4UCjEh0IhPhQKhfhQKMSHQiE+FArxoVAoxIdCIT4UCvGhUIgPhUJ8KBQK8aFQiA+FQnwoFOJDoVCID4XytvD59sfy4+uPT+/5WVOIz4ny9cd35ecXwkMhPmeIaJ/PTz98wGAUysvKm8Sn/rrOW3iZ98Wh3tRQbxqfv3xQfPjX51AvOdSbxOfL+68/qvHGvz6HIj78k3Ao4kN8OBTxIT4cikMRHw7Fod7YUPeKD4VCfCgU4kN8KMSH+FCID/GhEB/iQ6EQHwqF+BAfCvEhPhTiQ3woFOJDoRAf4kMhPsSHQnyID4X4EB8KhfhQKMSH+FCID/GhEB/iQ6EQHwqF+BAfCvEhPhTiQ3woxIf4UCjEh0IhPsSHQnyID4X4EB8K
如果测定全血中毒鼠强,对血有没有特别要求呢?一定要用不抗凝血吗?还是抗凝血呢?感觉都可以用吧?测定步骤是这样的,离心,取血清,加2ml乙酸乙酯,萃取10min,再加2ml乙酸乙酯,萃取10min,氮吹仪浓缩至0.5ml,进气质定性或定量。
如果测定全血中毒鼠强,对血有没有特别要求呢?一定要用不抗凝血吗?还是抗凝血呢?感觉都可以用吧?测定步骤是这样的,离心,取血清,加2ml乙酸乙酯,萃取10min,再加2ml乙酸乙酯,萃取10min,合并萃取液于氮吹仪浓缩至0.5ml,进气质定性或定量。
1. 原理 凝聚胺(polymatching)法首先利用低离子介质降低溶液的离子强度,减少红细胞周围的阳离子云,促进血清(浆)中的抗体与红细胞相应抗原结合,再加入带亚电荷的高价阳离子多聚物-凝聚胺溶液,中和红细胞表面的负电荷,缩短细胞间距,形成可逆的非特异性聚集,并使IgG型抗体直接凝集红细胞。加入中和液后,仅由凝聚胺引起的非特异性聚集,会因电荷中和而分散,而由抗体介导的特异性凝集则不会分散。2. 标本采集:2.1 标本种类:抽取静脉血3-4ml待凝固后分离血清,将细胞配成5%盐水悬液将供血者血样以同样方法分离血清(浆)和红细胞悬液。2.2 标本要求:抗凝和干燥管均可,如用抗凝血主张用EDTAK2(mg/dz)抗凝标本应无溶血,切标签齐全。3. 标本储存:急诊标本30分钟内完成操作,标本应至4℃冰箱保存7天。4. 标本运输:室温运输。5. 标本拒收标准:细菌污染。溶血标本,标签不齐全不能作测定。6. 试剂:6.1 试剂名称:凝聚胺试剂(polymatching)6.2 试剂生产厂家:(台资)珠海贝索生物技术有限公司。6.3 试剂组成:试剂1. 低离子介质(LowLonic Medium,LIM).试剂打开使用后,可置室温贮存,未开封者2-10度贮存,有效期为2年。试剂2. 凝聚胺溶液(PolybreneSolution).贮存及有效期同上。试剂3. 重悬液(ResuspendingSolution).贮存及有效期同上。试剂4. 8.5%生理盐水。7. 仪器:7.1 血型血清索离心机:XTL-4.7 上海离心机械研究所7.2 离心机:上海手术器械厂7.3 电热恒温水箱:北京长源实验设备厂7.4 显微镜:OLYMPUS(日本)8. 操作步骤及结果判断:8.1 供受者红细胞用生理盐水配成3-5%的细胞悬液。加样量均为:血清2滴,红细胞悬液1滴。主管:受血者血清+供者红细胞悬液;次管:受者红细胞悬液+供者血清;(阴阳对照管另设)。8.2 各管分别加低离子介质0.6ml混匀置室温1分钟。加凝聚胺溶液2滴,混匀,置室温15秒。8.3 1000g(3000rpm),离心18秒,弃上清液,管底保留约2滴液体。轻摇试管,观察是否形成凝块。如未形成凝块,则重做前面试验。8.4 加入2滴重悬液,轻轻混合,肉眼或显微镜下观察结果。8.5 凝块在1分钟内分散,试验结果为阴性,供受者血液配合;反之,如依照为不同强度的凝块,试验结果判为阳性,供受者血液不配合。实验结果必须在3分钟内判读。9. 操作性能: 快速简便,特异性强,灵敏度较高,重复性好。10. 超出范围结果处理:10.1 细胞自凝: 在冬天气温较低时,某些病人血清中含有冷凝集素而导致交叉配血假阳性;遇此现象可用37℃-40℃生理盐水洗涤红细胞并置37℃水溶中轻轻摇动,观察结果。10.2 若病人血清(血浆)含有肝素,如洗肾患者能影响配血,须多加4-6滴polybrene溶液以中和肝素。10.3 红细胞悬液为5%为宜,过浓或过淡可使抗原抗体比例不适当,反应不明显易误判。10.4 各种原因引起的红细胞溶解,误判为不凝集,部分溶血时,可溶性血型物质中和了相应的抗体。11. 方法局限性:11.1 试管,滴管吸头和玻片必须清洁干燥,防止溶血。11.2 操作方法应按规定,先加血清,然后再加红细胞悬液,以便容易核实是否漏加血清。11.3 离心时间不宜过长或过短,速度不宜过快或过慢,以防假阳性或假阴性结果。11.4 观察时应注意红细胞呈特异性凝集,继发性凝固及线状排列的区别。

http://ng1.17img.cn/bbsfiles/images/2011/05/201105281415_296633_1609805_3.jpg献血毕竟也是“出血”。我们知道,一般急性失血500ml,就会出现头昏、心慌、乏力,失血1000ml就会出现休克。正常成人的血液总量大约有4000~5000ml,倘若一次失血超过20%(也就是800~1000ml)就可能有生命危险。因此,献血者有些顾虑是正常的,但是献血对身体的具体影响会大到什么地步呢?血液中的主要成分包括红细胞、血小板、白细胞和血浆。红细胞的主要作用是运送氧气和二氧化碳——这可谓是血液最重要的功能。人体的组织器官,缺氧超过几分钟就会发生不可逆的损伤。而细胞所需要的氧几乎都是由红细胞运送的。大量失血之所以会要人命,主要就是因为红细胞会不够用。血小板和血浆中的十几种凝血因子共同参与凝血的工作。如果血小板减少的话,人就可能出血不止,甚至出现自发出血,也就是你什么都不做,血自己就渗出来了。白细胞主要参与免疫反应,说白了就是抵抗外来入侵者、以及清除内部叛乱者——肿瘤细胞。但是这个免疫反应绝对不是白细胞一个人在战斗,还需血浆中的各种免疫成分协作。
抗凝血药血栓疾病需抗凝,肝素作用强快灵,抗凝适用体内外,鱼精蛋白拮抗快,双香豆素仅体内,过量中毒加维K,枸橼酸钠用体外,大量输血防低钙。
用注射器抽取血淋巴每只蟹0.5mL移入装有0.5mLACD抗凝剂的ePpendorf管中。为什么抽的血和抗凝剂要一样多,谢谢
春节前的一则药品召回通知引发了市场关注。2月17日,北京市食药监局在其官网发布通知称,北京华润高科天然药物有限公司(以下简称华润高科)生产的舒血宁注射液存在安全风险,要求该公司对相关批次药品实施召回,且在整改期间不得生产、销售和使用。 记者致电位于北京延庆的华润高科公司,其一位工作人员证实,北京食药监局确实下发了整改通知,目前公司的舒血宁已经停产,但还有产品库存。 据了解,华润高科是华润三九旗下全资子公司,以生产天然药物液体制剂为主,现为华润三九在北京的中药处方药制剂生产基地。 涉事产品为“核心品种” 北京市食药监督管理局的通知显示,监督管理部门在市场监督检查过程中发现华润高科生产的舒血宁注射液存在安全风险,结合生产现场检查情况,为保证用药安全,对其提出相关批次药品召回,库存产品暂停销售、使用以及企业整改期间停止生产销售等要求。 华润高科官网资料显示:舒血宁注射液源于承接的国家保密计划研制的“6911”注射液,1970年经北京市卫生局革命领导小组批准在国内首家上市,上市后由于其在治疗心脑血管疾病中的冠心病、心绞痛、脑缺血、脑动脉硬化、急性脑梗塞、高粘血症等方面的优异表现获得临床大夫的一致好评。 目前,全国舒血宁注射剂销售市场中,神威药业的销量排第一,其次为华润三九,第三位是上海医药,其中华润高科的舒血宁注射剂年产量已接近1亿支。 中药注射液存滥用问题 对于此次事件原因,有人推测,“应该是存在质量问题,否则不会实施召回,比如某一批原材料重金属超标或者混入其他物质,因为现在很多药材种植大量使用农药,导致重金属超标。” 事实上,包括舒血宁在内的中药注射液还存在被滥用的问题。2013年,中国医疗保险研究会发布的一份《2009~2011年全国城镇基本医疗保险参保住院患者中药利用情况分析》(简称《分析》)报告显示,舒血宁注射剂超适应症使用发生费用12亿多元,属最被滥用的一种中药注射剂。 此外,中药注射剂不良反应较多等问题同样在医药界备受争议。2014年10月,国家食药监总局发布的《2013年药品不良反应监测年度报告》显示,中药注射剂不良反应报告数量增长17%,舒血宁注射剂位列前十位。2014年11月,国家食药总局还根据监测评价结果,决定对舒血宁注射液的说明书进行修订,要求相关药品生产企业增加警示语,指定不良反应内容、禁忌内容、注意事项等内容。 中药注射剂最大的特点就是有效成分和无效成分都在一起,有效成分起作用,无效成分对人体有伤害,但是这些都没有大量临床数据,不知道是人为造成还是客观造成,所以各方是各执一词,致使单纯讨论安全和不安全变得没有意义。 舒血宁注射液,你了解多少呢?华润高科生产的舒血宁注射液存在安全风险,那其他厂家生产的舒血宁没有发现吗?中药注射剂,能顶多久呢??
[img=,690,975]https://ng1.17img.cn/bbsfiles/images/2019/07/201907221754166749_5746_3389662_3.jpeg!w690x975.jpg[/img][img=,690,975]https://ng1.17img.cn/bbsfiles/images/2019/07/201907221754272172_4339_3389662_3.jpeg!w690x975.jpg[/img][img=,690,975]https://ng1.17img.cn/bbsfiles/images/2019/07/201907221754375930_7082_3389662_3.jpeg!w690x975.jpg[/img][img=,690,975]https://ng1.17img.cn/bbsfiles/images/2019/07/201907221754478170_9409_3389662_3.jpeg!w690x975.jpg[/img][img=,690,975]https://ng1.17img.cn/bbsfiles/images/2019/07/201907221754579270_6088_3389662_3.jpeg!w690x975.jpg[/img][img=,690,975]https://ng1.17img.cn/bbsfiles/images/2019/07/201907221755077660_5040_3389662_3.jpeg!w690x975.jpg[/img][img=,690,975]https://ng1.17img.cn/bbsfiles/images/2019/07/201907221755154062_8177_3389662_3.jpeg!w690x975.jpg[/img][img=,690,975]https://ng1.17img.cn/bbsfiles/images/2019/07/201907221755231932_519_3389662_3.jpeg!w690x975.jpg[/img][img=,690,975]https://ng1.17img.cn/bbsfiles/images/2019/07/201907221755316494_3561_3389662_3.jpeg!w690x975.jpg[/img][img=,690,975]https://ng1.17img.cn/bbsfiles/images/2019/07/201907221755387771_4933_3389662_3.jpeg!w690x975.jpg[/img][img=,690,975]https://ng1.17img.cn/bbsfiles/images/2019/07/201907221755454692_9457_3389662_3.jpeg!w690x975.jpg[/img][img=,690,975]https://ng1.17img.cn/bbsfiles/images/2019/07/201907221755534545_1492_3389662_3.jpeg!w690x975.jpg[/img][img=,690,975]https://ng1.17img.cn/bbsfiles/images/2019/07/201907221756015254_5487_3389662_3.jpeg!w690x975.jpg[/img][img=,690,975]https://ng1.17img.cn/bbsfiles/images/2019/07/201907221756105492_8859_3389662_3.jpeg!w690x975.jpg[/img][img=,690,975]https://ng1.17img.cn/bbsfiles/images/2019/07/201907221756194351_7987_3389662_3.jpeg!w690x975.jpg[/img][img=,690,975]https://ng1.17img.cn/bbsfiles/images/2019/07/201907221756271199_1141_3389662_3.jpeg!w690x975.jpg[/img][img=,690,975]https://ng1.17img.cn/bbsfiles/images/2019/07/201907221756346232_4807_3389662_3.jpeg!w690x975.jpg[/img][img=,690,975]https://ng1.17img.cn/bbsfiles/images/2019/07/201907221756407302_4758_3389662_3.jpeg!w690x975.jpg[/img][align=center][b][/b][/align]
[b]中文摘要:目的[/b] 确立因子类血液制品中蛋白质含量对效价检测结果的影响,从而完善因子类血液制品效价检测的方法。[b]方法 [/b]选取不同蛋白质浓度梯度的稀释液对同一供试品进行稀释来确定蛋白质影响的规律。 [b]结果 [/b]建立起人凝血因子Ⅷ、人凝血酶原复合物的全自动血凝仪因子效价检测方法,根据效价检测反应体系中蛋白浓度对检测结果的影响,建立因子类血液制品效价全自动血凝仪检测的方法。[b]结论 [/b]建立的两种稀释方法均消除了样品中蛋白质含量的不同对检测结果的影响,提高了检测的准确性,不但可以适用于现在产品的效价检测,而且适用于随着生产工艺的提升生产的更高纯度、低蛋白含量的FⅧ和PCC,同时也是对中国药典标准的补充。[b]关键词[/b]:人凝血因子Ⅷ;人凝血酶原复合物;效价;蛋白含量 人凝血因子Ⅷ、人凝血酶原复合物、人凝血因子Ⅸ等因子类血液制品,是以健康人血浆为原料,经分离纯化和病毒灭活制成,在临床上主要用于各种凝血因子缺乏的治疗,这些因子类血液制品的凝血因子效价是药品有效性的指标,凝血因子效价的测定也是药品质量检测中的关键检测项目。血液制品生产企业及各级检测机构一般采用全自动血凝仪并按照仪器使用说明来进行因子效价的检测,然而在不同检测方法结果比对中,发现全自动血凝仪检测结果与中国药典中一期法的检测结果在部分因子效价检测中存在检测差异,差异可能是样品稀释中使用的稀释液的蛋白含量不同引起的,故本课题主要研究因子类血液制品中蛋白质含量对效价检测结果影响。通过蛋白含量对因子效价检测影响的研究建立起的全自动血凝仪因子效价检测方法,消除了产品本身性质的影响,可以准确进行因子效价的测定,方法的建立不但可以准确控制因子类血液制品的质量,保证生产企业持续稳定生产出质量均一的药品,而且可以减少因子类产品在临床使用中的风险。[b]1 实验仪器与试剂[b]1.1 仪器[/b][/b]Stago-compact全自动血凝仪(法国Diagnostica Stago公司),漩涡振荡器(美国Thermo Scientific公司)。[b][b]1.2 试剂[/b][/b]人凝血因子Ⅷ缺乏血浆(法国Diagnostica Stago公司),人凝血因子Ⅸ缺乏血浆(法国Diagnostica Stago公司),APTT试剂(法国Diagnostica Stago公司),Owren-Koller(稀释液)(法国Diagnostica Stago公司),0.025 mol/L氯化钙溶液(法国Diagnostica Stago公司),Desorb U(清洗液)(法国Diagnostica Stago公司),人凝血因子Ⅷ国家标准品(批号20100101),人凝血酶原复合物国家标准品(批号20130306),生理氯化钠溶液(石家庄四药有限公司),咪唑(天津市巴斯夫化工有限公司),氯化钠(天津市巴斯夫化工有限公司),枸橼酸钠(台山新宁制药有限公司),人血白蛋白(公司自产)。[b][b]2 方法 2.1 人凝血因子Ⅷ不同蛋白质浓度梯度稀释效价测定[/b][/b] 人凝血因子Ⅷ国家标准品的定标:取1支人凝血因子Ⅷ国家标准品,加入1.0 ml纯化水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml含1.00 IU人凝血因子Ⅷ,将Desorb U(清洗液)、复溶后的人凝血因子Ⅷ缺乏血浆、0.025 mol/L氯化钙溶液、APTT以及每1 ml含1.00 IU的人凝血因子Ⅷ标准品溶液分别装入全自动血凝仪的试剂抽屉,将Owren-Koller(稀释液)装入全自动血凝仪的样本抽屉,按照《Stago-compact全自动血凝仪标准操作规程》选择人凝血因子Ⅷ效价测定定标程序进行定标,仪器自动将装入的人凝血因子Ⅷ标准品溶液再进行2倍、4倍、8倍稀释,建立人凝血因子Ⅷ标准品溶液效价(分别为1.00 IU/ml、0.50 IU/ml、0.25 IU/ml、0.13 IU/ml)的对数对其相应凝固时间对数的直线回归方程。 不同蛋白质浓度梯度稀释液制备:选取全自动血凝仪的稀释液Owren-Koller、生理氯化钠溶液、取1体积的3.8%枸橼酸钠加入5体积咪唑缓冲液混合液分别定义为稀释液1、稀释液2、稀释液3。向3种稀释液中分别加入人血白蛋白,使其中人血白蛋白的浓度分别为0、0.5%、1%、3%、5%。 人凝血因子Ⅷ供试品效价测定:取人凝血因子Ⅷ供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml约含1.00 IU人凝血因子Ⅷ,再用含不同蛋白浓度的稀释液做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅷ效价测定选项进行测定。[b][b]2.2 人凝血因子Ⅷ人凝血因子缺乏血浆稀释效价测定[/b] [/b]人凝血因子Ⅷ国家标准品的定标:取1支人凝血因子Ⅷ国家标准品,加入1.0 ml纯化水复溶,轻轻混匀,用人凝血因子Ⅷ缺乏血浆将其稀释成每1ml含1.00 IU人凝血因子Ⅷ,将Desorb U(清洗液)、复溶后的人凝血因子Ⅷ缺乏血浆、0.025 mol/L氯化钙溶液、APTT以及每1 ml含1.00 IU的人凝血因子Ⅷ标准品溶液分别装入全自动血凝仪的试剂抽屉,将Owren-Koller(稀释液)装入全自动血凝仪的样本抽屉,按照《Stago-compact全自动血凝仪标准操作规程》选择人凝血因子Ⅷ效价测定定标程序进行定标,仪器自动将装入的人凝血因子Ⅷ标准品溶液再进行2倍、4倍、8倍稀释,建立人凝血因子Ⅷ标准品溶液效价(分别为1.00 IU/ml、0.50 IU/ml、0.25 IU/ml、0.13 IU/ml)的对数对其相应凝固时间对数的直线回归方程。 人凝血因子Ⅷ供试品效价测定:取人凝血因子Ⅷ供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用人凝血因子Ⅷ缺乏血浆将其稀释成每1 ml约含1.00 IU人凝血因子Ⅷ,再用Owren-Koller(稀释液)做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅷ效价测定选项进行测定。[b][b]2.3 人凝血酶原复合物人凝血因子Ⅸ不同蛋白质浓度梯度稀释效价测定[/b][/b] 人凝血因子Ⅸ国家标准品的定标:取1支人凝血酶原复合物国家标准品,加入1.0 ml纯化水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml含1.00 IU人凝血因子Ⅸ,将Desorb U(清洗液)、复溶后的人凝血因子Ⅸ缺乏血浆、0.025 mol/L氯化钙溶液、APTT以及每1 ml含1.00 IU的人凝血因子Ⅸ标准品溶液分别装入全自动血凝仪的试剂抽屉,将Owren-Koller(稀释液)装入全自动血凝仪的样本抽屉,按照《Stago-compact全自动血凝仪标准操作规程》选择人凝血因子Ⅸ效价测定定标程序进行定标,仪器自动将装入的人凝血因子Ⅸ标准品溶液再进行2倍、4倍、8倍稀释,建立人凝血因子Ⅸ标准品溶液效价(分别为1.00 IU/ml、0.50 IU/ml、0.25 IU/ml、0.13 IU/ml)的对数对其相应凝固时间对数的直线回归方程。 不同蛋白质浓度梯度稀释液制备同2.1。 人凝血酶原复合物供试品效价测定:取人凝血酶原复合物供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml约含1.00 IU人凝血因子Ⅸ,再用含不同蛋白浓度的稀释液做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅸ效价测定选项进行测定。[b][b]2.4 人凝血酶原复合物人凝血因子Ⅸ人凝血因子缺乏血浆稀释效价测定[/b][/b] 人凝血因子Ⅸ国家标准品的定标:取1支人凝血酶原复合物国家标准品,加入1.0 ml纯化水复溶,轻轻混匀,用人凝血因子Ⅸ缺乏血浆将其稀释成每1 ml含1.00 IU人凝血因子Ⅸ,将Desorb U(清洗液)、复溶后的人凝血因子Ⅸ缺乏血浆、0.025 mol/L氯化钙溶液、APTT以及每1 ml含1.00 IU的人凝血因子Ⅸ标准品溶液分别装入全自动血凝仪的试剂抽屉,将Owren-Koller(稀释液)装入全自动血凝仪的样本抽屉,按照《Stago-compact全自动血凝仪标准操作规程》选择人凝血因子Ⅸ效价测定定标程序进行定标,仪器自动将装入的人凝血因子Ⅸ标准品溶液再进行2倍、4倍、8倍稀释,建立人凝血因子Ⅸ标准品溶液效价(分别为1.00 IU/ml、0.50 IU/ml、0.25 IU/ml、0.13 IU/ml)的对数对其相应凝固时间对数的直线回归方程。 人凝血酶原复合物供试品效价测定:取人凝血酶原复合物供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用人凝血因子Ⅸ缺乏血浆将其稀释成每1 ml约含1.00 IU人凝血因子Ⅸ,再用Owren-Koller(稀释液)做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅸ效价测定选项进行测定。[b][b]3 结果3.1 人凝血因子Ⅷ不同蛋白质浓度梯度稀释效价测定结果[/b][/b] 选取2015ZK0801批人凝血因子Ⅷ进行了不同蛋白质浓度梯度稀释效价测定,不同浓度稀释液分别测定10次。人血白蛋白的浓度分别为0、0.5%、1%、3%、5%的稀释液1、稀释液2、稀释液3的效价检测结果分别见表1、2、3,效价检测结果为效价标示量的百分比。[align=center]表1 FⅧ质控品不同蛋白浓度梯度稀释液1检测结果[/align][align=center][/align][align=center][img=,590,266]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142017_01_1626619_3.png[/img][/align][align=center]表2 FⅧ质控品不同蛋白浓度梯度稀释液2检测结果 [/align][align=center][img=,586,260]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142019_01_1626619_3.png[/img][/align][align=center]表3 FⅧ质控品不同蛋白浓度梯度稀释液3检测结果 [/align][align=center][img=,585,261]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142019_02_1626619_3.png[/img][/align]人凝血因子Ⅷ质控品2015ZK0801批用不同蛋白质浓度梯度的稀释液1、稀释液2、稀释液3稀释效价检测结果平均值用折线图表示,如图1:[align=center]图1 FⅧ质控品不同蛋白质浓度检测结果对比[/align][align=center][img=,548,295]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142019_03_1626619_3.png[/img][/align] 选取2批国外产人凝血因子Ⅷ和VWF混合制剂进行了不同蛋白质浓度梯度稀释效价测定,人血白蛋白的浓度分别为0、0.5%、1%、3%、5%的稀释液1、稀释液2、稀释液3的效价检测结果见表4、5,效价检测结果为效价标示量的百分比。[align=center]表4 658668A批制剂FⅧ检测结果[/align][align=center][img=,585,99]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142020_01_1626619_3.png[/img][/align][align=center]表5 A3B1814批制剂FⅧ检测结果[/align][align=center][img=,577,97]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142021_01_1626619_3.png[/img][/align]FⅧ效价检测结果用折线图表示,如图2、3:[align=center][img=,563,299]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142029_01_1626619_3.png[/img][/align][align=center]图2 658668A批不同蛋白质浓度检测结果对比[/align][align=center][img=,567,287]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142030_01_1626619_3.png[/img][/align][align=center][/align][align=center]图3 A3B1814批不同蛋白质浓度检测结果对比[/align][b][b]3.2 人凝血酶原复合物不同蛋白质浓度梯度稀释效价测定结果[/b][/b] 选取2015ZK0901批人凝血酶原复合物进行了不同蛋白质浓度梯度稀释人凝血因子Ⅸ效价测定,不同浓度稀释液分别测定10次。人血白蛋白的浓度分别为0、0.5%、1%、2%、3%、4%、5%的稀释液1、稀释液2、稀释液3的效价检测结果分别见表6、7、8,效价检测结果为效价标示量的百分比。[align=center]表6 PCC质控品不同蛋白浓度梯度稀释液1检测结果[/align][align=center][img=,583,269]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142031_01_1626619_3.png[/img][/align][align=center]表7 PCC质控品不同蛋白浓度梯度稀释液2检测结果[/align][align=center][img=,586,260]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142031_02_1626619_3.png[/img][/align][align=center]表8 PCC质控品不同蛋白浓度梯度稀释液3检测结果[/align][align=center][img=,593,263]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142043_01_1626619_3.png[/img][/align]人凝血酶原复合物质控品2015ZK0901批用不同蛋白质浓度梯度的稀释液1、稀释液2、稀释液3稀释FⅨ效价检测结果平均值用折线图表示,如图4:[align=center][img=,556,300]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142032_01_1626619_3.png[/img][/align][align=center]图4 PCC质控品不同蛋白质浓度FⅨ检测结果对比[/align][b][b]3.3 人凝血因子Ⅷ人凝血因子缺乏血浆稀释效价测定结果[/b][/b]选取2015ZK0801批人凝血因子Ⅷ进行了人凝血因子缺乏血浆稀释效价测定,共测定10次。效价检测结果见表9,效价检测结果为效价标示量的百分比。[align=center]表9 FⅧ质控品人凝血因子缺乏血浆稀释检测结果[/align][align=center][img=,579,74]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142032_02_1626619_3.png[/img][/align]选取2批国外产人凝血因子Ⅷ和VWF混合制剂进行了人凝血因子缺乏血浆稀释效价测定。效价检测结果见表10,效价检测结果为效价标示量的百分比。[align=center]表10 国外产品人凝血因子缺乏血浆稀释检测结果[/align][align=center][img=,578,77]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142036_01_1626619_3.png[/img][/align][b][b]3.4 人凝血酶原复合物人凝血因子Ⅸ人凝血因子缺乏血浆稀释效价测定结果[/b][/b]选取2015ZK0901批人凝血酶原复合物进行了人凝血因子缺乏血浆稀释人凝血因子Ⅸ效价测定,共测定10次。效价检测结果见表11,效价检测结果为效价标示量的百分比。[align=center]表11 PCC质控品人凝血因子缺乏血浆稀释检测结果[/align][align=center][img=,582,89]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142047_01_1626619_3.png[/img][/align][b][b]4 讨论[/b][/b] 本实验中对人凝血因子Ⅷ和人凝血酶原复合物分别用不同蛋白浓度梯度的稀释液进行了效价测定,另外用人凝血因子缺乏血浆稀释后进行了效价测定。因子效价测定中,稀释液1、稀释液2、稀释液3中加入相同浓度的人血白蛋白后,得到的因子效价检测结果没有差异,说明全自动血凝仪的稀释液Owren-Koller、生理氯化钠溶液、取1体积的3.8%枸橼酸钠加入5体积咪唑缓冲液混合液作为稀释液时没有区别。 人凝血因子Ⅷ、人凝血酶原复合物不同蛋白浓度梯度效价测定时,随着稀释液中蛋白质含量的增高,效价检测结果也不断升高,但在人凝血因子Ⅷ效价测定中,采用蛋白质含量为1%、3%的稀释液时,效价检测结果间均无显著差别,在人凝血酶原复合物人凝血因子Ⅸ效价测定中,采用蛋白质含量为0、0.5%、1%的稀释液时,效价检测结果间均无显著差别。另外,人凝血因子Ⅷ进行人凝血因子缺乏血浆稀释效价测定效价检测结果与采用蛋白质含量为1%、3%的稀释液得到的检测结果也无显著差异,人凝血酶原复合物人凝血因子缺乏血浆稀释人凝血因子Ⅸ效价检测结果与采用蛋白质含量为0、0.5%、1%的稀释液得到的检测结果也无显著差异。另外,国外生产的人凝血因子Ⅷ和VWF的混合制剂FⅧ效价的检测结果及血浆、稀释液的影响同泰邦公司产品一致。[b]参考文献[/b][align=left] 邬杨斌, 余蓉. 凝血因子Ⅸ复合物的研制 . 华西药学杂志, 2000, 15(3):177-179. Pabinger I, Brenner B, Kalina U, et al. Prothrombin complex concentrate(Beriplexw P/N)for emergency anticoagulation reversal: A prospective multinational clinical trial . J Thromb Haemost, 2008, 6(4):622-631. Kiman E, Elela AA, Ramsis N, et al. Evaluation of the coagulation factors activity of Cryosupernatant . Suez Canal Univ Med J, 2003, 6(2):247-258.Tullis JL, Melin M, Jurigian P. Clinical use of human Prothrombin complexes . N Engl J Med, 1965, 73(13):667-674.马莉, 孙盼, 李长清, 等. 去冷沉淀血浆的质量分析 . 中国生物制品学杂志, 2013, 26(1):81-83.魏舒, 时凯, 刘国荣, 等. 冻干人凝血酶原复合物的生产工艺研究 . 中国输血杂志, 2008, 21(10):282-284.Samama CM. Prothrombin complex concentrates: a brief review . Eur J Anaesthesiol, 2008, 25(10):784-789.焦丽华, 代旭兰, 刘文芳. 凝血酶原复合物的制备及其临床应用进展 .中国输血杂志, 2008, 21(9):737-741.[/align][b] [/b]
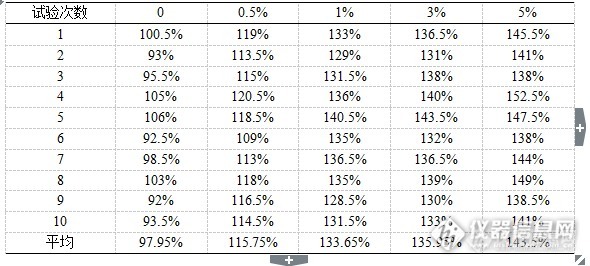
[b]中文摘要:目的[/b] 确立因子类血液制品中蛋白质含量对效价检测结果的影响,从而完善因子类血液制品效价检测的方法。[b]方法 [/b]选取不同蛋白质浓度梯度的稀释液对同一供试品进行稀释来确定蛋白质影响的规律。 [b]结果 [/b]建立起人凝血因子Ⅷ、人凝血酶原复合物的全自动血凝仪因子效价检测方法,根据效价检测反应体系中蛋白浓度对检测结果的影响,建立因子类血液制品效价全自动血凝仪检测的方法。[b]结论 [/b]建立的两种稀释方法均消除了样品中蛋白质含量的不同对检测结果的影响,提高了检测的准确性,不但可以适用于现在产品的效价检测,而且适用于随着生产工艺的提升生产的更高纯度、低蛋白含量的FⅧ和PCC,同时也是对中国药典标准的补充。[b]关键词[/b]:人凝血因子Ⅷ;人凝血酶原复合物;效价;蛋白含量 人凝血因子Ⅷ、人凝血酶原复合物、人凝血因子Ⅸ等因子类血液制品,是以健康人血浆为原料,经分离纯化和病毒灭活制成,在临床上主要用于各种凝血因子缺乏的治疗,这些因子类血液制品的凝血因子效价是药品有效性的指标,凝血因子效价的测定也是药品质量检测中的关键检测项目。血液制品生产企业及各级检测机构一般采用全自动血凝仪并按照仪器使用说明来进行因子效价的检测,然而在不同检测方法结果比对中,发现全自动血凝仪检测结果与中国药典中一期法的检测结果在部分因子效价检测中存在检测差异,差异可能是样品稀释中使用的稀释液的蛋白含量不同引起的,故本课题主要研究因子类血液制品中蛋白质含量对效价检测结果影响。通过蛋白含量对因子效价检测影响的研究建立起的全自动血凝仪因子效价检测方法,消除了产品本身性质的影响,可以准确进行因子效价的测定,方法的建立不但可以准确控制因子类血液制品的质量,保证生产企业持续稳定生产出质量均一的药品,而且可以减少因子类产品在临床使用中的风险。[b]1 实验仪器与试剂[b]1.1 仪器[/b][/b]Stago-compact全自动血凝仪(法国Diagnostica Stago公司),漩涡振荡器(美国Thermo Scientific公司)。[b][b]1.2 试剂[/b][/b]人凝血因子Ⅷ缺乏血浆(法国Diagnostica Stago公司),人凝血因子Ⅸ缺乏血浆(法国Diagnostica Stago公司),APTT试剂(法国Diagnostica Stago公司),Owren-Koller(稀释液)(法国Diagnostica Stago公司),0.025 mol/L氯化钙溶液(法国Diagnostica Stago公司),Desorb U(清洗液)(法国Diagnostica Stago公司),人凝血因子Ⅷ国家标准品(批号20100101),人凝血酶原复合物国家标准品(批号20130306),生理氯化钠溶液(石家庄四药有限公司),咪唑(天津市巴斯夫化工有限公司),氯化钠(天津市巴斯夫化工有限公司),枸橼酸钠(台山新宁制药有限公司),人血白蛋白(公司自产)。[b][b]2 方法2.1 人凝血因子Ⅷ不同蛋白质浓度梯度稀释效价测定[/b][/b] 人凝血因子Ⅷ国家标准品的定标:取1支人凝血因子Ⅷ国家标准品,加入1.0 ml纯化水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml含1.00 IU人凝血因子Ⅷ,将Desorb U(清洗液)、复溶后的人凝血因子Ⅷ缺乏血浆、0.025 mol/L氯化钙溶液、APTT以及每1 ml含1.00 IU的人凝血因子Ⅷ标准品溶液分别装入全自动血凝仪的试剂抽屉,将Owren-Koller(稀释液)装入全自动血凝仪的样本抽屉,按照《Stago-compact全自动血凝仪标准操作规程》选择人凝血因子Ⅷ效价测定定标程序进行定标,仪器自动将装入的人凝血因子Ⅷ标准品溶液再进行2倍、4倍、8倍稀释,建立人凝血因子Ⅷ标准品溶液效价(分别为1.00 IU/ml、0.50 IU/ml、0.25 IU/ml、0.13 IU/ml)的对数对其相应凝固时间对数的直线回归方程。 不同蛋白质浓度梯度稀释液制备:选取全自动血凝仪的稀释液Owren-Koller、生理氯化钠溶液、取1体积的3.8%枸橼酸钠加入5体积咪唑缓冲液混合液分别定义为稀释液1、稀释液2、稀释液3。向3种稀释液中分别加入人血白蛋白,使其中人血白蛋白的浓度分别为0、0.5%、1%、3%、5%。 人凝血因子Ⅷ供试品效价测定:取人凝血因子Ⅷ供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml约含1.00 IU人凝血因子Ⅷ,再用含不同蛋白浓度的稀释液做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅷ效价测定选项进行测定。[b][b]2.2 人凝血因子Ⅷ人凝血因子缺乏血浆稀释效价测定[/b] [/b]人凝血因子Ⅷ国家标准品的定标:取1支人凝血因子Ⅷ国家标准品,加入1.0 ml纯化水复溶,轻轻混匀,用人凝血因子Ⅷ缺乏血浆将其稀释成每1ml含1.00 IU人凝血因子Ⅷ,将Desorb U(清洗液)、复溶后的人凝血因子Ⅷ缺乏血浆、0.025 mol/L氯化钙溶液、APTT以及每1 ml含1.00 IU的人凝血因子Ⅷ标准品溶液分别装入全自动血凝仪的试剂抽屉,将Owren-Koller(稀释液)装入全自动血凝仪的样本抽屉,按照《Stago-compact全自动血凝仪标准操作规程》选择人凝血因子Ⅷ效价测定定标程序进行定标,仪器自动将装入的人凝血因子Ⅷ标准品溶液再进行2倍、4倍、8倍稀释,建立人凝血因子Ⅷ标准品溶液效价(分别为1.00 IU/ml、0.50 IU/ml、0.25 IU/ml、0.13 IU/ml)的对数对其相应凝固时间对数的直线回归方程。 人凝血因子Ⅷ供试品效价测定:取人凝血因子Ⅷ供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用人凝血因子Ⅷ缺乏血浆将其稀释成每1 ml约含1.00 IU人凝血因子Ⅷ,再用Owren-Koller(稀释液)做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅷ效价测定选项进行测定。[b][b]2.3 人凝血酶原复合物人凝血因子Ⅸ不同蛋白质浓度梯度稀释效价测定[/b][/b] 人凝血因子Ⅸ国家标准品的定标:取1支人凝血酶原复合物国家标准品,加入1.0 ml纯化水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml含1.00 IU人凝血因子Ⅸ,将Desorb U(清洗液)、复溶后的人凝血因子Ⅸ缺乏血浆、0.025 mol/L氯化钙溶液、APTT以及每1 ml含1.00 IU的人凝血因子Ⅸ标准品溶液分别装入全自动血凝仪的试剂抽屉,将Owren-Koller(稀释液)装入全自动血凝仪的样本抽屉,按照《Stago-compact全自动血凝仪标准操作规程》选择人凝血因子Ⅸ效价测定定标程序进行定标,仪器自动将装入的人凝血因子Ⅸ标准品溶液再进行2倍、4倍、8倍稀释,建立人凝血因子Ⅸ标准品溶液效价(分别为1.00 IU/ml、0.50 IU/ml、0.25 IU/ml、0.13 IU/ml)的对数对其相应凝固时间对数的直线回归方程。 不同蛋白质浓度梯度稀释液制备同2.1。 人凝血酶原复合物供试品效价测定:取人凝血酶原复合物供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml约含1.00 IU人凝血因子Ⅸ,再用含不同蛋白浓度的稀释液做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅸ效价测定选项进行测定。[b][b]2.4 人凝血酶原复合物人凝血因子Ⅸ人凝血因子缺乏血浆稀释效价测定[/b][/b] 人凝血因子Ⅸ国家标准品的定标:取1支人凝血酶原复合物国家标准品,加入1.0 ml纯化水复溶,轻轻混匀,用人凝血因子Ⅸ缺乏血浆将其稀释成每1 ml含1.00 IU人凝血因子Ⅸ,将Desorb U(清洗液)、复溶后的人凝血因子Ⅸ缺乏血浆、0.025 mol/L氯化钙溶液、APTT以及每1 ml含1.00 IU的人凝血因子Ⅸ标准品溶液分别装入全自动血凝仪的试剂抽屉,将Owren-Koller(稀释液)装入全自动血凝仪的样本抽屉,按照《Stago-compact全自动血凝仪标准操作规程》选择人凝血因子Ⅸ效价测定定标程序进行定标,仪器自动将装入的人凝血因子Ⅸ标准品溶液再进行2倍、4倍、8倍稀释,建立人凝血因子Ⅸ标准品溶液效价(分别为1.00 IU/ml、0.50 IU/ml、0.25 IU/ml、0.13 IU/ml)的对数对其相应凝固时间对数的直线回归方程。 人凝血酶原复合物供试品效价测定:取人凝血酶原复合物供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用人凝血因子Ⅸ缺乏血浆将其稀释成每1 ml约含1.00 IU人凝血因子Ⅸ,再用Owren-Koller(稀释液)做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅸ效价测定选项进行测定。[b][b]3 结果3.1 人凝血因子Ⅷ不同蛋白质浓度梯度稀释效价测定结果[/b][/b] 选取2015ZK0801批人凝血因子Ⅷ进行了不同蛋白质浓度梯度稀释效价测定,不同浓度稀释液分别测定10次。人血白蛋白的浓度分别为0、0.5%、1%、3%、5%的稀释液1、稀释液2、稀释液3的效价检测结果分别见表1、2、3,效价检测结果为效价标示量的百分比。[align=center]表1 FⅧ质控品不同蛋白浓度梯度稀释液1检测结果[/align][align=center][img=,590,266]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142017_01_1626619_3.png[/img][/align][align=center]表2 FⅧ质控品不同蛋白浓度梯度稀释液2检测结果 [/align][align=center][img=,586,260]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142019_01_1626619_3.png[/img][/align][align=center]表3 FⅧ质控品不同蛋白浓度梯度稀释液3检测结果 [/align][align=center][img=,585,261]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142019_02_1626619_3.png[/img][/align]人凝血因子Ⅷ质控品2015ZK0801批用不同蛋白质浓度梯度的稀释液1、稀释液2、稀释液3稀释效价检测结果平均值用折线图表示,如图1:[align=center]图1 FⅧ质控品不同蛋白质浓度检测结果对比[/align][align=center][img=,548,295]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142019_03_1626619_3.png[/img][/align] 选取2批国外产人凝血因子Ⅷ和VWF混合制剂进行了不同蛋白质浓度梯度稀释效价测定,人血白蛋白的浓度分别为0、0.5%、1%、3%、5%的稀释液1、稀释液2、稀释液3的效价检测结果见表4、5,效价检测结果为效价标示量的百分比。[align=center]表4 658668A批制剂FⅧ检测结果[/align][align=center][img=,585,99]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142020_01_1626619_3.png[/img][/align][align=center]表5 A3B1814批制剂FⅧ检测结果[/align][align=center][img=,577,97]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142021_01_1626619_3.png[/img][/align]FⅧ效价检测结果用折线图表示,如图2、3:[align=center][img=,563,299]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142029_01_1626619_3.png[/img][/align][align=center]图2 658668A批不同蛋白质浓度检测结果对比[/align][align=center][img=,567,287]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142030_01_1626619_3.png[/img][/align][align=center]图3 A3B1814批不同蛋白质浓度检测结果对比[/align][b][b]3.2 人凝血酶原复合物不同蛋白质浓度梯度稀释效价测定结果[/b][/b] 选取2015ZK0901批人凝血酶原复合物进行了不同蛋白质浓度梯度稀释人凝血因子Ⅸ效价测定,不同浓度稀释液分别测定10次。人血白蛋白的浓度分别为0、0.5%、1%、2%、3%、4%、5%的稀释液1、稀释液2、稀释液3的效价检测结果分别见表6、7、8,效价检测结果为效价标示量的百分比。[align=center]表6 PCC质控品不同蛋白浓度梯度稀释液1检测结果[/align][align=center][img=,583,269]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142031_01_1626619_3.png[/img][/align][align=center]表7 PCC质控品不同蛋白浓度梯度稀释液2检测结果[/align][align=center][img=,586,260]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142031_02_1626619_3.png[/img][/align][align=center]表8 PCC质控品不同蛋白浓度梯度稀释液3检测结果[/align][align=center][img=,593,263]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142043_01_1626619_3.png[/img][/align]人凝血酶原复合物质控品2015ZK0901批用不同蛋白质浓度梯度的稀释液1、稀释液2、稀释液3稀释FⅨ效价检测结果平均值用折线图表示,如图4:[align=center][img=,556,300]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142032_01_1626619_3.png[/img][/align][align=center]图4 PCC质控品不同蛋白质浓度FⅨ检测结果对比[/align][b][b]3.3 人凝血因子Ⅷ人凝血因子缺乏血浆稀释效价测定结果[/b][/b]选取2015ZK0801批人凝血因子Ⅷ进行了人凝血因子缺乏血浆稀释效价测定,共测定10次。效价检测结果见表9,效价检测结果为效价标示量的百分比。[align=center]表9 FⅧ质控品人凝血因子缺乏血浆稀释检测结果[/align][align=center][img=,579,74]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142032_02_1626619_3.png[/img][/align]选取2批国外产人凝血因子Ⅷ和VWF混合制剂进行了人凝血因子缺乏血浆稀释效价测定。效价检测结果见表10,效价检测结果为效价标示量的百分比。[align=center]表10 国外产品人凝血因子缺乏血浆稀释检测结果[/align][align=center][img=,578,77]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142036_01_1626619_3.png[/img][/align][b][b]3.4 人凝血酶原复合物人凝血因子Ⅸ人凝血因子缺乏血浆稀释效价测定结果[/b][/b]选取2015ZK0901批人凝血酶原复合物进行了人凝血因子缺乏血浆稀释人凝血因子Ⅸ效价测定,共测定10次。效价检测结果见表11,效价检测结果为效价标示量的百分比。[align=center]表11 PCC质控品人凝血因子缺乏血浆稀释检测结果[/align][align=center][img=,582,89]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142047_01_1626619_3.png[/img][/align][b][b]4 讨论[/b][/b] 本实验中对人凝血因子Ⅷ和人凝血酶原复合物分别用不同蛋白浓度梯度的稀释液进行了效价测定,另外用人凝血因子缺乏血浆稀释后进行了效价测定。因子效价测定中,稀释液1、稀释液2、稀释液3中加入相同浓度的人血白蛋白后,得到的因子效价检测结果没有差异,说明全自动血凝仪的稀释液Owren-Koller、生理氯化钠溶液、取1体积的3.8%枸橼酸钠加入5体积咪唑缓冲液混合液作为稀释液时没有区别。 人凝血因子Ⅷ、人凝血酶原复合物不同蛋白浓度梯度效价测定时,随着稀释液中蛋白质含量的增高,效价检测结果也不断升高,但在人凝血因子Ⅷ效价测定中,采用蛋白质含量为1%、3%的稀释液时,效价检测结果间均无显著差别,在人凝血酶原复合物人凝血因子Ⅸ效价测定中,采用蛋白质含量为0、0.5%、1%的稀释液时,效价检测结果间均无显著差别。另外,人凝血因子Ⅷ进行人凝血因子缺乏血浆稀释效价测定效价检测结果与采用蛋白质含量为1%、3%的稀释液得到的检测结果也无显著差异,人凝血酶原复合物人凝血因子缺乏血浆稀释人凝血因子Ⅸ效价检测结果与采用蛋白质含量为0、0.5%、1%的稀释液得到的检测结果也无显著差异。另外,国外生产的人凝血因子Ⅷ和VWF的混合制剂FⅧ效价的检测结果及血浆、稀释液的影响同泰邦公司产品一致。[b]参考文献[/b][align=left] 邬杨斌, 余蓉. 凝血因子Ⅸ复合物的研制 . 华西药学杂志, 2000, 15(3):177-179. Pabinger I, Brenner B, Kalina U, et al. Prothrombin complex concentrate(Beriplexw P/N)for emergency anticoagulation reversal: A prospective multinational clinical trial . J Thromb Haemost, 2008, 6(4):622-631. Kiman E, Elela AA, Ramsis N, et al. Evaluation of the coagulation factors activity of Cryosupernatant . Suez Canal Univ Med J, 2003, 6(2):247-258.Tullis JL, Melin M, Jurigian P. Clinical use of human Prothrombin complexes . N Engl J Med, 1965, 73(13):667-674.马莉, 孙盼, 李长清, 等. 去冷沉淀血浆的质量分析 . 中国生物制品学杂志, 2013, 26(1):81-83.魏舒, 时凯, 刘国荣, 等. 冻干人凝血酶原复合物的生产工艺研究 . 中国输血杂志, 2008, 21(10):282-284.Samama CM. Prothrombin complex concentrates: a brief review . Eur J Anaesthesiol, 2008, 25(10):784-789.焦丽华, 代旭兰, 刘文芳. 凝血酶原复合物的制备及其临床应用进展 .中国输血杂志, 2008, 21(9):737-741.[/align][b] [/b]
原理:在确定量的血浆样本经过一定时间的加温后,加入试剂。加入试剂后,采用波长为660nm的光照射样本。凝血过程(纤维蛋白原转化为纤维蛋白)中血的浑浊度可以通过测量散射光光强度的改变来测定。从散射光光强度的测定,可以做出凝血曲线,通过PercentageDetection Method方法求得凝血时间。一、仪器:(一)型号:Sysmex CA—1500自动血液凝血分析仪(二)分析和计算参数:1.处理量:约120个测试/小时2.所需样本量:10μl 3.检验时间:在最长检验时间之内测出结果,典型最长检验时间:100秒4.重复性:CV≤4%5. 计算参数:纤维蛋白原浓度(Fbg)二、试剂及配套品:(一)试剂:1. 凝血酶试剂(Thrombin Reagent)(1)商标:德灵(DADE BEHRING)(2)包装规格:Pack for 10×1ml(3)代码:B4233 G25 E0533 (961) W(4)成分:牛凝血酶冻干粉(lyophilized preparation of bovine thrombin)(近似100 NIH units/ml)
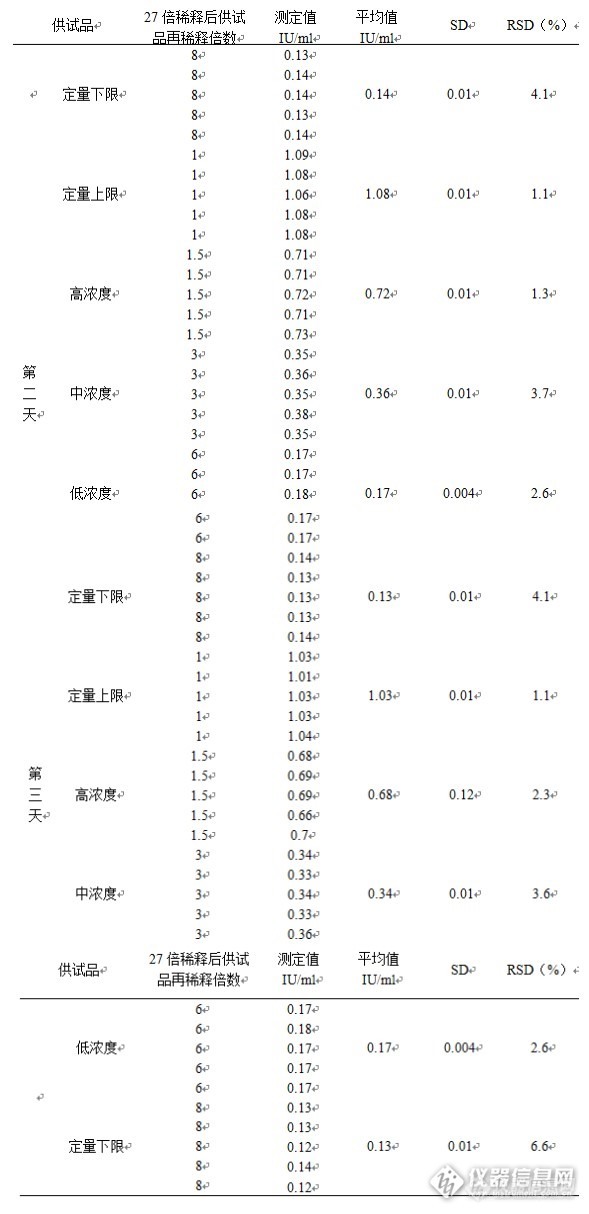
[align=center][b]因子类血液制品效价的检测方法验证[/b][/align][align=left][b]中文摘要[/b]:[b]目的 [/b]验证全自动凝血仪应用于因子类血液制品效价测定时方法的准确性 [b]方法[/b]根据生物制品质量控制分析方法验证技术审评一般原则及《中国药典》2015年版通则9012生物样品定量分析方法验证指导原则,通过线性关系,准确度,精密度(重复性、日间精密度),专属性对本方法进行方法学验证。[b]结果[/b]两种稀释方法的因子效价检测所进行的线性关系,准确度,精密度、日间精密度、专属性验证均符合方法学验证的标准。[b]结论[/b]两种稀释方法适用于因子效价的检测。效从价检测方法的建立可应用于因子类血液制品生产的中间过程控制,通过准确的效价检测可以对中间各个生产环节的中间产品进行指导,可以精确分析各生产环节的效价损耗量,而制定解决方案,提高整个生产过程的产品收率,在半成品的配制环节,可对产品的总效价进行精确控制,从而提高产品质量的均一性,整体提高产品的质量水平。[/align][b]关键词: 因子类血液制品;效价检测; 方法学验证[/b]通过蛋白质含量对凝血因子效价检测影响的研究,发现在供试品稀释中使用含不同蛋白质浓度的稀释液导致因子效价测定的差异。而在制药企业和检测机构中,为追求检测方法的简单化、仪器化和数据可追溯性,大部分采用了全自动血凝仪,并按照血凝仪的使用说明书进行了因子类血液制品的效价检测。选用蛋白浓度为1%的药典稀释液和用人凝血因子缺乏血浆进行预稀释两种方法对人凝血因子进行效价检测全自动血凝仪法通过线性关系,准确度,精密度(重复性、日间精密度),专属性对本方法进行方法学验证。效价检测方法的建立可应用于因子类血液制品生产的中间过程控制,通过准确的效价检测可以对中间各个生产环节的中间产品进行指导,可以精确分析各生产环节的效价损耗量,从而制定解决方案,提高整个生产过程的产品收率,在半成品的配制环节,可对产品的总效价进行精确控制,从而提高产品质量的均一性,整体提高产品的质量水平。[b] 1 实验仪器与试剂1.1 仪器[/b]Stago-compact全自动血凝仪(法国DiagnosticaStago公司),漩涡振荡器(美国ThermoScientific公司)。[b]1.2 试剂人凝血因子Ⅷ国家标准品(批号20100101),人凝血酶原复合物国家标准品(批号20130306),药典稀释液(取1体积的3.8%枸橼酸钠加入5体积咪唑缓冲液混合,加适量20%人血白蛋白至终浓度为1%),Owren-Koller(稀释液)。2 方法2.1 蛋白含量1%的药典稀释液稀释人凝血因子Ⅷ效价检测方法验证2.1.1线性关系[/b]取复溶后的人凝血因子Ⅷ国家标准品,用生理氯化钠溶液将其稀释成每1 ml含1.00 IU人凝血因子Ⅷ,按照Stago全自动血凝仪操作规程选择人凝血因子Ⅷ效价测定定标程序操作,仪器自动将装入的人凝血因子标准品溶液稀释至1.00 IU/ml、0.50IU/ml、0.25IU/ml、0.13IU/ml,连续定标3次。定标完成后,仪器建立人凝血因子Ⅷ标准品溶液效价(IU/ml)的对数对其相应的凝固时间(秒)对数的直线回归方程,记录相关系数R值,应不低于0.99。[b]2.1.2 准确度[/b]将生理氯化钠溶液稀释至1 IU/ml的人凝血因子Ⅷ溶液放入STAGO全自动血凝仪中定标,另取用药典稀释液再稀释1.5倍,3倍,6倍,8倍的标准品溶液(标准曲线范围内高、中、低三个稀释度和定量下限)作为待测样品,按照操作规程进行测定,测定3次,并计算回收率,高、中、低浓度标准品回收率应在85%~115%范围内,定量下限标准品回收率应在80%~120%范围内。[b]2.1.3 精密度[/b]取2015ZK0801批人凝血因子Ⅷ质控品,用灭菌注射用水复溶后,用生理氯化钠溶液将其进行27倍稀释,再用药典稀释液稀释1倍,1.5倍,3倍,6倍,8倍,分别作为标准曲线范围内定量上限,高、中、低三个稀释度和定量下限。每一个稀释度重复测定5次。计算每一浓度测定结果的均值、SD和RSD值,高、中、低浓度标准品回收率应在85%~115%范围内,定量上、下限标准品回收率应在80%~120%范围内。[b]2.1.4 日间精密度[/b]在不同的三天分别按照2.1.3进行精密度的测定。[b]2.1.5 专属性[/b]为确保当制品中含有其它组分,如杂质、降解物、添加物(如缓冲液、赋形剂、稳定剂)等存在时,能够准确可靠测定供试品的能力而进行分析方法的专属性验证。取人凝血因子Ⅷ生产过程中的配制平衡液(含与人凝血因子Ⅷ中相同含量的氯化钠、枸橼酸钠、甘氨酸、甘露醇等),以此作为不含人凝血因子Ⅷ的基质溶液,进行人凝血因子Ⅷ效价的检测,其检测结果应低于方法定量下限,并对用基质溶液稀释的高浓度和低浓度的标准品进行检测,要求至少80%以上的标准品的准确度在±20%范围内。[b]2.2 人凝血因子缺乏血浆进行预稀释人凝血因子Ⅷ效价检测方法验证2.2.1 线性关系[/b]取复溶后的人凝血因子Ⅷ国家标准品,用人凝血因子Ⅷ缺乏血浆将其稀释成每1 ml含1.00 IU人凝血因子Ⅷ,按照Stago全自动血凝仪操作规程选择人凝血因子Ⅷ效价测定定标程序操作,仪器自动将装入的人凝血因子标准品溶液稀释至1.00 IU/ml、0.50IU/ml、0.25IU/ml、0.13IU/ml,连续定标3次。定标完成后,仪器建立人凝血因子Ⅷ标准品溶液效价(IU/ml)的对数对其相应的凝固时间(秒)对数的直线回归方程,记录相关系数R值,应不低于0.99。[b]2.2.2 准确度[/b]将人凝血因子Ⅷ缺乏血浆稀释至1 IU/ml的人凝血因子Ⅷ溶液放入STAGO全自动血凝仪中定标,另取用Owren-Koller(稀释液)再稀释1.5倍,3倍,6倍,8倍的标准品溶液(标准曲线范围内高、中、低三个稀释度和定量下限)作为待测样品,按照操作规程进行测定,测定3次,并计算回收率,高、中、低浓度标准品回收率应在85%~115%范围内,定量下限标准品回收率应在80%~120%范围内。[b]2.2.3 精密度[/b]取2015ZK0801批人凝血因子Ⅷ质控品,用灭菌注射用水复溶后,用人凝血因子Ⅷ缺乏血浆将其进行27倍稀释,再用Owren-Koller(稀释液)稀释1倍,1.5倍,3倍,6倍,8倍,分别作为标准曲线范围内定量上限,高、中、低三个稀释度和定量下限。每一个稀释度重复测定5次。计算每一浓度测定结果的均值、SD和RSD值,高、中、低浓度标准品回收率应在85%~115%范围内,定量上、下限标准品回收率应在80%~120%范围内。[b]2.2.4 日间精密度[/b]在不同的三天分别按照2.2.3进行精密度的测定。[b]2.2.5 专属性[/b]为确保当制品中含有其它组分,如杂质、降解物、添加物(如缓冲液、赋形剂、稳定剂)等存在时,能够准确可靠测定供试品的能力而进行分析方法的专属性验证。取人凝血因子Ⅷ生产过程中的配制平衡液(含与人凝血因子Ⅷ中相同含量的氯化钠、枸橼酸钠、甘氨酸、甘露醇等),以此作为不含人凝血因子Ⅷ的基质溶液,进行人凝血因子Ⅷ效价的检测,其检测结果应低于方法定量下限,并对用基质溶液稀释的高浓度和低浓度的标准品进行检测,要求至少80%以上的标准品的准确度在±20%范围内[b]2.3 蛋白含量1%的药典稀释液稀释人凝血酶原复合物效价检测方法验证2.3.1 线性关系[/b]取复溶后的人凝血酶原复合物国家标准品,用生理氯化钠溶液将其稀释成每1 ml含1.00 IU人凝血因子Ⅸ,按照Stago全自动血凝仪操作规程选择人凝血因子Ⅸ效价测定定标程序操作,仪器自动将装入的人凝血因子Ⅸ标准品溶液稀释至1.00 IU/ml、0.50IU/ml、0.25IU/ml、0.13IU/ml,连续定标3次。定标完成后,仪器建立人凝血因子Ⅸ标准品溶液效价(IU/ml)的对数对其相应的凝固时间(秒)对数的直线回归方程,记录相关系数R值,应不低于0.99。[b]2.3.2 准确度[/b]将生理氯化钠溶液稀释至1 IU/ml的人凝血因子Ⅸ溶液放入STAGO全自动血凝仪中定标,另取用药典稀释液再稀释1.5倍,3倍,6倍,8倍的标准品溶液(标准曲线范围内高、中、低三个稀释度和定量下限)作为待测样品,按照操作规程进行测定,测定3次,并计算回收率,高、中、低浓度标准品回收率应在85%~115%范围内,定量下限标准品回收率应在80%~120%范围内。[b]2.3.3 精密度[/b]取2015ZK0901批人凝血酶原复合物质控品,用灭菌注射用水复溶后,用生理氯化钠溶液将其进行15倍稀释,再用药典稀释液稀释1倍,1.5倍,3倍,6倍,8倍,分别作为标准曲线范围内定量上限,高、中、低三个稀释度和定量下限。每一个稀释度重复测定5次。计算每一浓度测定结果的均值、SD和RSD值,高、中、低浓度标准品回收率应在85%~115%范围内,定量上、下限标准品回收率应在80%~120%范围内。[b]2.3.4 日间精密度[/b]在不同的三天分别按照2.3.3进行精密度的测定。[b]2.3.5 专属性[/b]为确保当制品中含有其它组分,如杂质、降解物、添加物(如缓冲液、赋形剂、稳定剂)等存在时,能够准确可靠测定供试品的能力而进行分析方法的专属性验证。取人凝血酶原复合物生产过程中的配制平衡液(含与人凝血酶原复合物中相同含量的氯化钠、枸橼酸钠、甘氨酸等),以此作为不含人凝血酶原复合物的基质溶液,进行人凝血因子Ⅸ效价的检测,其检测结果应低于方法定量下限,并对用基质溶液稀释的高浓度和低浓度的标准品进行检测,要求至少80%以上的标准品的准确度在±20%范围内。[b]2.4 人凝血因子缺乏血浆进行预稀释人凝血酶原复合物效价检测方法验证2.4.1 线性关系[/b]取复溶后的人凝血酶原复合物国家标准品,用人凝血因子Ⅸ缺乏血浆将其稀释成每1 ml含1.00 IU人凝血因子Ⅸ,按照Stago全自动血凝仪操作规程选择人凝血因子Ⅸ效价测定定标程序操作,仪器自动将装入的人凝血因子Ⅸ标准品溶液稀释至1.00 IU/ml、0.50 IU/ml、0.25 IU/ml、0.13 IU/ml,连续定标3次。定标完成后,仪器建立人凝血因子Ⅸ标准品溶液效价(IU/ml)的对数对其相应的凝固时间(秒)对数的直线回归方程,记录相关系数R值,应不低于0.99。[b]2.4.2 准确度[/b]将人凝血因子Ⅸ缺乏血浆稀释至1 IU/ml的人凝血因子Ⅸ溶液放入STAGO全自动血凝仪中定标,另取用Owren-Koller(稀释液)再稀释1.5倍,3倍,6倍,8倍的标准品溶液(标准曲线范围内高、中、低三个稀释度和定量下限)作为待测样品,按照操作规程进行测定,测定3次,并计算回收率,高、中、低浓度标准品回收率应在85%~115%范围内,定量下限标准品回收率应在80%~120%范围内。[b]2.4.3 精密度[/b]取2015ZK0901批人凝血酶原复合物质控品,用灭菌注射用水复溶后,用人凝血因子Ⅸ缺乏血浆将其进行15倍稀释,再用Owren-Koller(稀释液)稀释1倍,1.5倍,3倍,6倍,8倍,分别作为标准曲线范围内定量上限,高、中、低三个稀释度和定量下限。每一个稀释度重复测定5次。计算每一浓度测定结果的均值、SD和RSD值,高、中、低浓度标准品回收率应在85%~115%范围内,定量上、下限标准品回收率应在80%~120%范围内。2.4.4 日间精密度在不同的三天分别按照2.4.3进行精密度的测定。[b]2.4.5 专属性[/b]为确保当制品中含有其它组分,如杂质、降解物、添加物(如缓冲液、赋形剂、稳定剂)等存在时,能够准确可靠测定供试品的能力而进行分析方法的专属性验证。取人凝血酶原复合物生产过程中的配制平衡液(含与人凝血酶原复合物中相同含量的氯化钠、枸橼酸钠、甘氨酸等),以此作为不含人凝血酶原复合物的基质溶液,进行人凝血因子Ⅸ效价的检测,其检测结果应低于方法定量下限,并对用基质溶液稀释的高浓度和低浓度的标准品进行检测,要求至少80%以上的标准品的准确度在±20%范围内。[b]3 结果3.1 蛋白含量1%的药典稀释液稀释人凝血因子Ⅷ效价检测方法验证3.1.1 线性关系结果[/b]用生理氯化钠溶液稀释的每1 ml含1.00 IU人凝血因子Ⅷ标准品进行Ⅷ效价测定定标,三次直线回归方程相关系数R值结果见表1。[align=center]表1 生理氯化钠稀释FⅧ定标R值检测结果[/align][align=center][img=,573,138]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141653_01_1626619_3.png[/img][/align][align=left][b]3.1.2 准确度结果[/b][/align][align=left]用生理氯化钠溶液稀释的每1 ml含1.00 IU人凝血因子Ⅷ后再用药典稀释液再稀释1.5倍,3倍,6倍,8倍的标准品溶液的检测结果见表2。[/align][align=center]表2 准确度检测结果[/align][align=center][img=,570,335]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141654_01_1626619_3.png[/img][/align][b]3.1.3 精密度结果[/b]2015ZK0801批人凝血因子Ⅷ质控品用生理氯化钠溶液稀释27倍后再用药典稀释液再稀释1倍,1.5倍,3倍,6倍,8倍的检测结果见表3。[align=center]表3 精密度检测结果[/align][align=center][img=,571,422]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141656_01_1626619_3.png[/img][/align][align=center][img=,566,290]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141657_01_1626619_3.png[/img][/align][b]3.1.4 日间精密度结果[/b]在不同的三天2015ZK0801批人凝血因子Ⅷ质控品用生理氯化钠溶液稀释27倍后再用药典稀释液再稀释1倍,1.5倍,3倍,6倍,8倍的检测结果见表4。[align=center]表4 日间精密度检测结果[/align][align=center][img=,571,470]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141703_01_1626619_3.png[/img][/align][align=center][img=,589,1214]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141713_01_1626619_3.jpg[/img][/align][b]3.1.5 专属性结果[/b]将生理氯化钠溶液稀释至1 IU/ml的人凝血因子Ⅷ溶液定标后,取不含人凝血因子Ⅷ的基质溶液,进行人凝血因子Ⅷ效价的检测,并对用基质溶液稀释的高浓度和低浓度的标准品进行检测,检测结果见表5。[align=center]表5 专属性检测结果[/align][align=center][img=,565,239]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141714_01_1626619_3.png[/img][/align][b]3.2 人凝血因子缺乏血浆进行预稀释人凝血因子Ⅷ效价检测方法验证3.2.1 线性关系结果[/b]用人凝血因子Ⅷ缺乏血浆稀释的每1 ml含1.00 IU人凝血因子Ⅷ标准品进行Ⅷ效价测定定标,三次直线回归方程相关系数R值结果见表6。[align=center]表6 人凝血因子缺乏血浆稀释FⅧ定标R值检测结果[/align][align=center][img=,567,135]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141716_01_1626619_3.png[/img][/align][b]3.2.2 准确度结果[/b]用人凝血因子Ⅷ缺乏血浆稀释的每1 ml含1.00 IU人凝血因子Ⅷ后用Owren-Koller(稀释液)再稀释1.5倍,3倍,6倍,8倍的标准品溶液的检测结果见表7。[align=center]表7 准确度检测结果[/align][align=center][img=,569,300]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141717_01_1626619_3.png[/img][/align][b]3.2.3 精密度结果[/b]2015ZK0801批人凝血因子Ⅷ质控品用人凝血因子Ⅷ缺乏血浆稀释27倍后再用Owren-Koller(稀释液)再稀释1倍,1.5倍,3倍,6倍,8倍的检测结果见表4-8。[align=center]表8 精密度检测结果[/align][align=center][img=,566,570]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141720_01_1626619_3.png[/img][/align][b]3.2.4 日间精密度结果[/b]在不同的三天2015ZK0801批人凝血因子Ⅷ质控品用人凝血因子Ⅷ缺乏血浆稀释27倍后再用Owren-Koller(稀释液)再稀释1倍,1.5倍,3倍,6倍,8倍的检测结果见表9。[align=center]表9 日间精密度检测结果[/align][align=center][img=,588,1701]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141726_02_1626619_3.jpg[/img][/align][b]3.2.5 专属性结果[/b]将人凝血因子Ⅷ缺乏血浆稀释至1 IU/ml的人凝血因子Ⅷ溶液定标后,取不含人凝血因子Ⅷ的基质溶液,进行人凝血因子Ⅷ效价的检测,并对用基质溶液稀释的高浓度和低浓度的标准品进行检测,检测结果见表10。[align=center]表10 专属性检测结果[/align][align=center][img=,569,238]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141728_01_1626619_3.png[/img][/align][b]3.3 蛋白含量1%的药典稀释液稀释人凝血酶原复合物效价检测方法验证3.3.1 线性关系结果[/b]用生理氯化钠溶液稀释的每1 ml含1.00 IU人凝血因子Ⅸ标准品进行Ⅸ效价测定定标,三次直线回归方程相关系数R值结果见表11。[align=center]表11 生理氯化钠稀释FⅨ定标R值检测结果[/align][align=center][img=,571,139]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141729_01_1626619_3.png[/img][/align][b]3.3.2 准确度结果[/b]用生理氯化钠溶液稀释的每1 ml含1.00 IU人凝血因子Ⅸ后再用药典稀释液再稀释1.5倍,3倍,6倍,8倍的标准品溶液的检测结果见表12。[align=center]表12 准确度检测结果[/align][align=center][img=,571,274]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141730_01_1626619_3.png[/img][/align][b]3.3.3 精密度结果[/b]2015ZK0901批人凝血酶原复合物用生理氯化钠溶液稀释15倍后再用药典稀释液再稀释1倍,1.5倍,3倍,6倍,8倍的检测结果见表13。[align=center]表13 精密度检测结果[/align][align=center][img=,572,506]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141731_01_1626619_3.png[/img][/align][b]3.3.4 日间精密度结果[/b]在不同的三天2015ZK0901批人凝血酶原复合物质控品用生理氯化钠溶液稀释15倍后再用药典稀释液再稀释1倍,1.5倍,3倍,6倍,8倍的检测结果见表14。[align=center]表14 日间精密度检测结果[/align][align=center][img=,590,1702]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141737_01_1626619_3.jpg[/img][/align][align=left][b]3.3.5 专属性结果[/b][/align]将生理氯化钠溶液稀释至1 IU/ml的人凝血因子Ⅸ溶液定标后,取不含人凝血酶原复合物的基质溶液,进行人凝血因子Ⅸ效价的检测,并对用基质溶液稀释的高浓度和低浓度的标准品进行检测,检测结果见表15。[align=center]表15 专属性检测结果[/align][align=center][img=,566,236]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141739_01_1626619_3.png[/img][/align][b]3.4 人凝血因子缺乏血浆进行预稀释人凝血酶原复合物效价检测方法验证3.4.1 线性关系结果[/b]用人凝血因子Ⅸ缺乏血浆稀释的每1 ml含1.00 IU人凝血因子Ⅸ标准品进行Ⅸ效价测定定标,三次直线回归方程相关系数R值结果见表16。[align=center]表16 人凝血因子缺乏血浆稀释FⅨ定标R值检测结果[/align][align=center][img=,567,133]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141740_01_1626619_3.png[/img][/align][b]3.4.2 准确度结果[/b]用人凝血因子Ⅸ缺乏血浆稀释的每1 ml含1.00 IU人凝血因子Ⅸ后用Owren-Koller(稀释液)再稀释1.5倍,3倍,6倍,8倍的标准品溶液的检测结果见表17。[align=center]表17 准确度检测结果[/align][align=center][img=,568,274]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141741_01_1626619_3.png[/img][/align][b]3.4.3 精密度结果[/b]2015ZK0901批人凝血酶原复合物质控品用人凝血因子Ⅸ缺乏血浆稀释15倍后再用Owren-Koller(稀释液)再稀释1倍,1.5倍,3倍,6倍,8倍的检测结果见表18。[align=center]表18 精密度检测结果[/align][align=center][img=,571,576]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141742_01_1626619_3.png[/img][/align][b]3.4.4 日间精密度结果[/b]在不同的三天2015ZK0901批人凝血酶原复合物质控品用人凝血因子Ⅸ缺乏血浆稀释15倍后再用Owren-Koller(稀释液)再稀释1倍,1.5倍,3倍,6倍,8倍的检测结果见表19。[align=center]表19 日间精密度检测结果[/align][align=center][img=,588,1756]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141747_01_1626619_3.jpg[/img][/align][b]3.4.5 专属性结果[/b]将人凝血因子Ⅸ缺乏血浆稀释至1 IU/ml的人凝血因子Ⅸ溶液定标后,取不含人凝血酶原复合物的基质溶液,进行人凝血因子Ⅸ效价的检测,并对用基质溶液稀释的高浓度和低浓度的标准品进行检测,检测结果见表20。[align=center]表20 专属性检测结果[/align][align=center][img=,568,240]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141748_01_1626619_3.png[/img][/align][b]4讨论[/b]本章对人凝血因子Ⅷ、人凝血酶原复合物中的FⅨ效价测定方法进行了方法学验证,供试品因子效价的测定可采用两种不同的稀释方法进行,先用生理氯化钠溶液稀释至(约)1 IU/ml再用药典稀释液进行稀释或者先用凝血因子缺乏血浆稀释至(约)1 IU/ml再用Owren-Koller(稀释液)稀释。两种稀释方法的因子效价检测所进行的线性关系,准确度,精密度、日间精密度、专属性验证均符合方法学验证的标准,适用于因子效价的检测。其中先用生理氯化钠溶液稀释至(约)1 IU/ml再用药典稀释液进行稀释检测方法适用于开放型(可使用不同厂家试剂)的血凝仪,且所用稀释剂价格低廉,降低了检测成本;而先用凝血因子缺乏血浆稀释至(约)1 IU/ml再用Owren-Koller(稀释液)稀释适用于Stago全自动血凝仪这种封闭式(只能使用本厂配套试剂)的血凝仪,且由于使用凝血因子缺乏血浆这种价格昂贵的试剂提高了检测成本。[b]参考文献[/b] 王卓, 赵雄, 吕茂民, 等. 血液制品的现状与展望 . 生物工程学报, 2011, 27(5):730-746. Newman J, et al. Methods for the productionof clinically effective intermediate and high-factor-Ⅷconcentrates . Brit J Haemat, 1971, 21:1. 王箐舟, 赵卉, 王威, 等. 第四批人凝血因子Ⅷ国家标准品制备和标定 .中国药品标准, 2013,14(3):188-190. 刘大英, 沈琦, 云志宏. 血浆和中纯FⅧ国家标准品FⅧ: C检测结果及分析. 中国输血杂志, 1995,8(2):87-88.
西红柿颜色鲜艳、味道可口、食法多样,是人们餐桌上常见的平民化蔬菜。不仅味道酸甜可口,而且还含有不少对人体有益的元素,常吃西红柿,可达到祛斑、美白、降血压、防癌等多重养生功效。然而,吃西红柿的好吃虽然有不少,但食用上还是要多加注意,否则很容易出事的哦。 服用抗凝血药物时不能吃 维生素K主要作用是催化肝中凝血酶原以及凝血活素的合成,维生素K不足时,由于限制了凝血酶原的合成而使凝血时间延长,造成皮下和肌肉出血。而西红柿则刚好含有较丰富的维生素K,因此服用肝素、双香豆素等抗凝血药物时不宜食用。 不要空腹食用 西红柿含有大量可溶性收敛剂等成分,与胃酸发生反应,凝结成不溶解的块状物,这些硬块可能将胃的出口幽门堵塞,引起胃肠胀满、疼痛等不适症状。 吃成熟的西红柿 尚未成熟的青西红柿含有生物碱甙(龙葵碱)其形状为针状结晶体,进食以后轻则口腔感到苦涩,严重的时候还会出现中毒现象。所以生的西红柿最好就不要吃了。 不宜长久加热烹制后食用 长久加热烹制后就失去了原有的营养与味道,因番茄红素遇光、热和氧气容易分解,失去保健作用。因此,烹调时应避免长时间高温加热。
一:综述 1985-1988年在浙江省发现四名血友病人因使用进口凝血VIII因子而感染艾滋病。因为得不到及时的治疗,他们早已过世。1987年中国卫生部,海关,外交部联合发文禁止进口血制品(白蛋白除外)。在1996年前中国的血友病患者使用的都是其国产的凝血VIII因子制剂,主要生产厂家是国家卫生部直属机构,上海生物制品研究所。据该研究所一位负责说,大约生产了二十万瓶药物。有一万多客户购销。 上世纪90年代初期在中国内地开始的非法采血,在河南等省造成了艾滋病大面积扩散。而这些收集起来的血浆,流入了医院、流入了生产血制品的厂家。 部分存在着HIV病毒的血浆制成凝血VIII因子制剂,流进了中国血友病人的血管。 二:血友病简介 血友病是一种遗传性的血液凝结方面的疾病,在中国的发病率大约是为每十万个男性中有5人为病人,照此推算,中国13亿人口中约有6.5至7万名血友病患者。(主要为甲型—缺8因子和乙型--缺9因子)。 血友病患者由于自身缺乏足够的凝血Ⅷ因子,经常会因一点小伤或者自然出血不止,在出血时必须及时输血,血浆和输血制品———人凝血Ⅷ因子制剂。如不即时输血和凝血Ⅷ因子制剂,将会导致出血不止,引发关节畸变,严重时会危及生命。而输入凝血Ⅷ因子制剂,能迅速缓解病情。所以凝血因子是血友病人经常使用的以保障生命安全的唯一药品。 三:凝血VIII因子生产情况 一九八二年上海生物制品研究所研制出了冻干人凝血Ⅷ因子制剂并生产(卫制82沪(6)13号),经上海瑞金医院,第三人民医院等单位临床应用,证明对血友病甲型患者有显著疗效。当时的宣传是“药到病除,使用安全,无副作用,制剂的纯度和活性已达到国际同类制剂的水平”。 这一科研成果经过有关媒体宣传,使全国的血友病甲型患者看到了希望,大家都争先恐后地在上海生物制品研究所购买了大量的这种冻干人凝血Ⅷ因子制剂,以进行疾病的治疗和预防。 有部分病人反映,他们也曾今使用过成都生物制品公司,广西一家生物生产厂家在八十年代后期至九十年代初期生产的凝血因子制剂。 至今,血友病人在突发性出血或手术中,因即时得不到凝血因子的补充或经济原因,(凝血因子价格昂贵)在部分省直大型医院或血站通过输注血浆或在血浆中提凝血因子(冷沉淀)用于临床治疗血友病。所以至今还存在着输血感染HIV和其它病毒的危险性。 四:相关文件及法规 一九八五年我国发现了首例艾滋病毒感染者。国务院在一九八七年十二月二十六日就此批准了《艾滋病监督管理的若干规定》,上海市人民政府于一九八八年十二月二十二日也批准颁发了《上海市艾滋病监测实施办法》二者的第十一条同时规定:血液和血液制品必须进行艾滋病病毒抗体监测。 而上海生物制品研究所所生产的冻干人凝血Ⅷ因子是未经病毒去除或灭活工艺处理的,该所生产的冻干人凝血Ⅷ因子制剂存在着传播艾滋病毒和丙型,乙型肝炎的严重危险。 为此,国家卫生部在一九九五年颁发了1995第(55)号文件:《关于禁止生产和临床使用未经病毒去除或灭活的凝血因子类血制品的通知》,上海生物制品研究所停止了生产,但仍然销售其产品。明知故犯,无视国家法规,从而导致了这场全国血友病患者雪上加霜的特大灾难。 五:感染者的发现 1998年上海发现血友病人感染艾滋病患者。经病人相互传递信息和媒体报道后,上海地区曾经使用过上海生物制品研究所凝血因子产品的血友病人相继做了检查,现在已经发现感染艾滋病患者64名。已知死亡4人。其中不少患者家属及小孩也被感染其HIV病毒。 2000年上海血友病感染者集体法律诉讼上海生物制品研究所,要求其公开道歉,承认错误并做出赔偿,但上海生物制品研究所拒绝对此承担责任。2001年底,上海的感染者得到了上海市政府的人道救助及疾病的全面免费治疗。 2003年6月来自湖南,辽宁,吉林,黑龙江省,五位血友病感染者。诉讼上海生物制品研究所。上海市长宁区法院受理了他们的诉讼请求。进行了法庭调查,但没有结果。国内媒体相继做了相关报道。至使全国各地曾经使用过上海生物制品研究所凝血VIII因子的血友病人极度恐慌。各省,市相继发现感染者。 六:政府的关注 2003年11月,全国部分血友病感染者联名至信温家保总理和吴仪副总理,反映中国血友病感染者的情况,希望能够得到政府的救治和关怀,法律给予的公证。 2003年12月卫生部办公厅发布了162号文件:《关于做好血友病患者感染艾滋病有关救治问题的通知》。促请湖南,安徽,陕西。辽宁,吉林,黑龙江等当地卫生厅予以重视,参照上海血友病感染者的救治方法,解决好患者们免费治疗和生活救助事宜。但是,各地方政府以发生地不在当地,责任人明确及种种理由,拒绝对血友病感染者进行治疗和生活救助。 各地的感染者分别上访或写信致当地省长,卫生厅长。请求治疗及生活救助。 2004年7月在泰国国际艾滋病大会上,血友HIV感染者阚志明向卫生部王陇德副部长递交了中国血友病感染HIV情况报告,与CDC性艾中心主任沈洁进行了交流。在卫生部、CDC及沈洁主任亲自关心下,目前,各省已知的血友病HIV感染者全部获到了抗HIV药物免费治疗,而生活救助除上海、苏州外,没有一个地方得到了施行。 七:面临的问题 1、自从2001年底首批血友病HIV感染者使用抗病毒药至今已有4年了,现面临耐药和换药的问题。现在血友病HIV感染者使用的药为:施多宁(EFV)+拉美夫定(3TC)+塞瑞特(D4T) 少数病人用的是施多宁(EFV)+双汰芝(3TC+AZT)如何换药,换什么药,是目前最紧要的问题,须尽早找出方案后并储备药品。 2、部分地区的病人无法按时获得全套的抗病毒药。CDC、医院储备的抗病毒药少。 3、除上海外,HIV病毒载量、CD4检测,各地都得不到免费。 4、因HIV的破坏,感染者凝血因子的使用增多。而病人无力承担。 5、感染者100%都有丙型肝炎。 6、血友病HIV感染者的人数少,分布零散,医生对血友病HIV感染者的治疗知识和经验缺乏,对血友病感染者的发病特征不明确,导致治疗效果差,而产生的药物副作用无法及时加以预防和治疗。 7、生活困难。HIV检测费用高,凝血因子昂贵是最大的经济负担。 八:目前的情况: 现发现十三个省二个直辖市感染者108人。其中上海64人,北京2人,湖南4人,陕西2人,四川1人,贵州1人,浙江6人,江苏9人,湖北1人,黑龙江4人,辽宁3人,吉林1人,安徽4人,广东3人,江西2人,山东1人。(附名单) 血友病人感染HIV患者的发现是通过病人们相互信息和网络的认识。感染人群基本以城市人口为主,没有发现农村感染者,原因是凝血因子价格昂贵。 目前,浙江,江苏,安徽,湖南。广东,浙江全国各地都有血友病患者因肺炎,腹泻,大出血等症状导致死亡的消息。 报告人:阚志明 2005年7月31日 本人联系方式: QQ:58079623 mail:xiaokan@xueyou.org
【序号】:1【作者】:蒋忠 马正良【题名】:终未期肝硬化肝移植术中凝血功能的调控【期刊】:临床麻醉学杂志 【年、卷、期、起止页码】:2008 24(4) 【全文链接】:[url]http://d.wanfangdata.com.cn/Periodical_lcmzxzz200804007.aspx[/url]【序号】:2【作者】:张新友 余小舫【题名】:肝移植术时凝血功能障碍的处理【期刊】: 临床血液学杂志 【年、卷、期、起止页码】:2008 21(1) 【全文链接】:[url]http://d.wanfangdata.com.cn/Periodical_lcxyxzz200801007.aspx[/url]【序号】:3【作者】:刘永勤 杨亚红【题名】:原位肝脏移植术中血流动力学及凝血功能变化研究【期刊】: 人民军医【年、卷、期、起止页码】:2008 51(10) 【全文链接】:[url]http://d.wanfangdata.com.cn/Periodical_rmjy200810012.aspx[/url]【序号】:4【作者】:董兰 雷志礼【题名】:40例原位肝移植手术病人术中凝血功能的分析【期刊】:临床麻醉学杂志 【年、卷、期、起止页码】:2004 20(10) 【全文链接】:[url]http://d.wanfangdata.com.cn/Periodical_lcmzxzz200410018.aspx[/url]【序号】:5【作者】:陶国才 易斌【题名】:背驮式肝移植术中凝血功能变化【期刊】: 重庆医学 【年、卷、期、起止页码】: 2002年31卷10期【全文链接】:[url]http://www.cqvip.com/qk/93197a/2002010/6918514.html[/url]
血浆速冻技术的新进展血浆是抗凝全血经物理方法分离制备的一种血液成分,其临床应用是现代成分输血的重要组成部分,尤其是新鲜冰冻血浆(PPT),在临床治疗中更有其重要的作用。血浆是多种血浆蛋白质的混合物,其中包含白蛋白、免疫球蛋白和凝血因子类蛋白。为了有效的保护血浆内的有效成分,特别是凝血因子,并随着我国成分输血技术的发展,新鲜冰冻血浆及冷沉淀的制备技术及应用随之也越来越广泛。目前我国《血站基本标准》实施细则中第92条规定:制备新鲜冰冻血浆时,抗凝剂为CPD、CP2D、CPDA-1的血液应在8小时内分离并速冻;抗凝剂为ACD的血液应在6小时内分离并速冻。其质量要求: 含有全部凝血因子。血浆蛋白为6~8g/%;纤维蛋白原0.2~0.4g%;Ⅷ因子含量:≥0.7 IU/ml 规格。可以看出,时间和温度是制备出质量合格的新鲜冰冻血浆两个关键点,尤其是对于活性很高的凝血因子VIII和V,时间和温度是影响其活性的重要因素。中国医学检验杂志1995年3月第18卷第2期《血浆凝血因子测定的影响因素探讨》,作者通过对比经过不同温度和时间后FVIII含量发现:32℃条件下6小时活性只有48%,24小时5%4℃条件下6小时活性有95%,24小时剩29%。由于在血浆结冰过程中,凝血因子VIII含量与时间呈指数下降关系,所以速冻时间越短,凝血因子VIII和V的损失也就越小。国际上通用的标准是1个小时内速冻完成,如果能在30分钟内完成速冻,那么效果将会更好。因此要保证新鲜冰冻血浆及冷沉淀等成分的疗效,必需在采供血过程中控制好冷链和时间链,其中血浆速冻技术是其中一个重要环节,速冻的时间和效果将直接关系到血浆及冷沉淀产品的质量和疗效。 随着《中华人民共和国献血法》的实施和无偿献血的深入开展,血站的采血方式已由有偿献血时代的站内采血为主转向站外无偿流动采血。要达到采血后6h(或8 h)内分离血浆并冻结有时存在一定的困难。因此为保证临床使用新鲜冰冻血浆、血浆冷沉淀的质量尽可能的缩短血浆速冻的时间就显的尤为重要了。我国血站采用的血浆速冻技术主要经过了以下几个发展阶段:1、用超低温冰箱来进行血浆速冻。此种方法的主要不足在于:冰箱内空间有限,将血浆叠加在一起,上下接触不均匀。冰箱制冷效率有限,速冻时间较长(通常需要6-8h)。显然是达不到要求的。2、强制对流型速冻机。最初的血浆速冻设备我们称为强制对流型速冻机(blast freezer)。该类设备的设计思路来源于普通冰箱,也是使用空气作为冷媒。通过更强的制冷功率来得到低温空气,并且使冷空气快速的流动,加快冷空气与溶液的热交换来实现快速冻结的目的,因此,也称之为“冷风制冷”。由于这类设备内冷空气流动速度比冰箱内空气流动速度有了很大提高,使得制冷效果得到提高,缩短了血浆冻结的时间。对于超低温冰箱来说,这种方式使得速冻的时间已经得到了大大的缩短,但由于关键技术的不足,其速冻时间通常都需要2h。3、平板接触式速冻机。这类设备是根据最新的平板接触制冷技术制造而成。它通过改变传统的“空气”冷媒,用特制不锈钢作为冷媒,加快血浆热交换实现速冻,从而达到缩短速冻时间的目的。今天,我们来讲讲血浆速冻技术的新进展:平板接触式血浆速冻技术。平板接触式速冻(contact plate freezing)。该技术通过高效压缩机使金属板稳定在-50℃的温度,血浆袋通过与-50℃的低温金属板直接接触进行热传递,由于空气的热传导率仅为0.28 w/m•k,而金属的热传导率为58.02w/m•k是空气的上百倍。因此使得降温效率得到极大的提高,降温过程所需时间更少,因此可以得到更多的凝血因子,得到更好质量的新鲜冰冻血浆。平板接触式速冻技术,虽然出现的时间不长,但是它已经以其强大的技术优势已经在国际上占据了血浆速冻市场40%的份额。
科技日报 2013年10月18日 星期五 科技日报讯 据物理学家组织网10月16日报道,一个人若久坐飞机、手术恢复过程中长时间卧病在床,会形成危及生命的血凝块。由于没有快速而简便的诊断方法,往往会导致中风或心脏疾病。为了改变这种状况,美国麻省理工学院一个工程师团队基于纳米技术开发出一种简单的尿检试纸,可快速检测出血液中的凝块。 血液凝固是由一系列复杂的级联蛋白质相互作用,以形成一种能密封伤口的纤维蛋白质。这个过程中的最后一步纤维蛋白原转化为纤维蛋白,由一种叫做凝血酶的酶控制。该研究被最新一期的美国化学会《ACS纳米》杂志描述为一种非侵入式诊断,其依靠纳米粒子检测一个关键凝血因子即凝血酶的存在。既有的血液测试以纤维蛋白副产物为标记物,不能连贯地检测到新凝块的形成,而新方法以凝血酶为标记物,可用一种可注射的纳米粒子快速识别。 实验使用了已获美国食品和药物管理局批准的氧化铁纳米粒子、涂有专门与凝血酶肽(短蛋白质)相互作用的多肽。纳米粒子被注入老鼠体内后,会经过整个鼠体。当粒子遇到凝血酶,凝血酶在特定的位置上裂解肽类,释放的片段最终顺着动物的尿液排泄。 在处理收集的尿液样本时,他们采用含有特定多肽标记物抗体的碎片识别这些蛋白质片段,发现尿液中这些标记物的数量与凝固在小鼠肺中的血液凝块水平成正比。去年发布的系统版本,是利用质谱仪对片段质量分析来进行区分;而最新版本用抗体测试样本,更为简单且便宜。 这种尿样测试有两种应用前景:一是在急诊室用来筛查可能有血块症状的患者,允许医生迅速分诊并确定其是否需要更多的测试。另一应用是监测具有高危血栓的患者,例如手术后不得不卧床康复的病人。这种尿液试纸测试如同怀孕测试,医生可在病人术后回家时开给他们。此外,这项技术也可以用于预测血栓的复发。 麻省理工学院德什潘德技术创新中心将出资实现这项技术商业化。(华凌)
据新华社华盛顿8月29日电 美国研究人员日前报告说,对接受手术或放疗的前列腺癌患者而言,日常坚持服用阿司匹林可降低其长期死亡率。 此前有研究表明,阿司匹林及其他抗凝血药物能抑制肿瘤生长和转移,但相关临床数据却非常有限。在新研究中,得克萨斯大学西南医学中心等机构的研究人员以近6000名接受手术或放疗的前列腺癌患者为对象进行分析,其中约2200人日常服用阿司匹林、华法林或波立维等抗凝血药。 研究人员发现,日常服用抗凝血药的前列腺癌患者群体的10年死亡率为3%,而未服用群体的死亡率为8%,前者的癌症复发率和骨转移率也明显较低。进一步的分析表明,前列腺癌患者所获的上述益处主要来自阿司匹林,而不是其他两种抗凝血药。 相关研究报告本周已发表在美国《临床肿瘤学杂志》上。研究人员表示,新研究表明,作为一种耐受性良好的常用处方药,阿司匹林可以改善前列腺癌的治疗结果,但向前列腺癌患者推荐服用阿司匹林之前还需进行更多研究。(记者任海军)
问:在ELISA试剂盒实验前我们需要的基本试剂有哪些?答:捕获抗体检测抗体链霉亲和素-HRP标准品96孔酶标板:选择具有中等或高吸附力的酶标板,禁止使用培养板包被溶液:0.1M的PBS或者TBS,PH9.6 0.05M碳酸盐缓冲液阻断溶液:含3%BSA的TTBS或PBS,或者含有3-5%血清的PBS标准品/标本稀释液:含1%BSA的TTBS或PBS洗液:含0.02%吐温20的0.002M咪唑盐溶液或者PH7.4的PBS溶液底物溶液:两组份或者一组份的TMB显色液终止液:2N的硫酸或者1%HCl溶液封板膜问:elisa试剂盒血清标本采集需要注意什么呢?答:1) 要注意避免出现严重溶血。血红蛋白中含有血红素基团,其有类似过氧化物的活性,因此,在以HRP为标记酶的ELISA测定中,如血清标本中血红蛋白浓度较高,则其就很容易在温育过程中吸附于固相,从而与后面加入的HRP底物反应显色。2) 样本的采集及血清分离中要注意尽量避免细菌污染,一则细菌的生长,其所分泌的一些酶可能会对抗原抗体等蛋白产生分解作用;二则一些细菌的内源性酶如大肠杆菌的β-半乳糖苷酶本身会对用相应酶作标记的测定方法产生非特异性干扰。3) 血清标本如是以无菌操作分离,则可以在2~8℃下保存一周,如为有菌操作,则建议冰冻保存。样本的长时间保存,应在-70℃以下。4) 冰冻保存的血清标本须注意避免因停电等造成的反复冻融。标本的反复冻融所产生的机械剪切力将对标本中的蛋白等分子产生破坏作用,从而引起假阴性结果。此外,冻融标本的混匀亦应注意,不要进行剧烈振荡,反复颠倒混匀即可。5) 标本在保存中如出现细菌污染所致的混浊或絮状物时,应离心沉淀后取上清检测。问:测抗体可以用什么方法,有操作步骤么,谢谢。答:捕获法测IgM抗体 血清中针对某些抗原的特异性IgM常和特异性IgG同时存在,后者会干扰IgM抗体的测定。因此测定IgM抗本多用捕获法,先将所有血清IgM(包括异性IgM和非特异性IgM)固定在固相上,在去除IgG后再测定特异性IgM。操作步骤如下: (1)将抗人IgM抗体连接在固相载体上,形成固相抗人IgM。洗涤。 (2)加入稀释的血清标本:保温反应后血清中的IgM抗体被固相抗体捕获。洗涤除去其他免疫球蛋白和血清中的杂质成分。 (3)加入特异性抗原试剂:它只与固相上的特异性IgM结合。洗涤。 (4)加入针对特异性的酶标抗体:使之与结合在固相上的抗原反应结合。洗涤。 (5)加底物显色:如有颜色显示,则表示血清标本中的特异性IgM抗体存在,是为阳性反应。 问:血清的类别有哪些还有要怎么鉴别呢?答:血清的类别:胎牛血清、透析型胎牛血清 、天然低IGG胎牛血清 、干细胞培养胎牛血清 、特殊用途胎牛血清 、活性炭/葡萄糖处理胎牛血清 、胎牛血清替代物 、小牛血清 、新生牛血清 、加强型小牛血清 、补铁小牛血清 、成牛血清 、供体马血清 、兔血清 、鸡血清 、猪血清 、马血清 、其他动物血清 、合成血清替代品鉴别方法:血液凝固析出的淡黄色透明液体。如将血液自血管内抽出,放入试管中,不加抗凝剂,则凝血反应被激活,血液迅速凝固,形成胶冻。凝血块收缩,其周围所析出之淡黄色透明液体即为血清,也可于凝血后经离心取得。在凝血过程中,纤维蛋白原转变成纤维蛋白块,所以血清中无纤维蛋白原,这一点是与血浆最大的区别。而在凝血反应中,血小板释放出许多物质,各凝血因子也都发生了变化。这些成分都留在血清中并继续发生变化,如凝血酶原变成凝血酶,并随血清存放时间逐渐减少以至消失。这些也都是与血浆区别之处。但大量未参加凝血反应的物质则与血浆基本相同。为避免抗凝剂的干扰,血液中许多化学成分的分析,都以血清为样品。
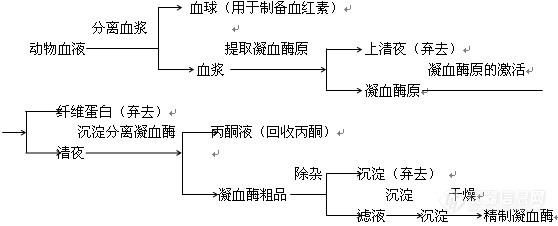
[font=黑体][color=#fe2419]本文为[font=Arial]hchemh[/font][font=宋体]原创作品,本作者是该作品唯一合法使用者,该作品暂不对外授权转载。[/font][/color][font=Arial][/font][size=3][font=宋体]其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现的,均属侵权违法行为。[/font][b][font=Arial][/font][/b]摘 要:[/size][/font][size=3] [font=楷体_GB2312]本实验分别[/font][/size][size=3][font=楷体_GB2312]采用多种方法对人体血液的部分化学成分进行了分析测定。经实验分析鉴定,可知人体血液中凝血酶和血红素的含量。这为以后对于血液成分的进一步研究奠定基础。这个实验是我在学校的时候做的,说到为什么要做这个实验,纯属有现成的样品,却没有可做的实验,于是听毛主席的话:浪费可耻!于是就想着做了这个实验,现在拿出来现眼也是因为抵制不了原创大赛的层层诱惑,可以奖品许愿现在又开始了大乐透,让我就豁出去,分享下自己的实验过程和方法吧!大家板砖轻拍哈!!先说说这次提取的血液中有效成分是什么,由于实验条件的限制,这次我们主要提取两种有效成分,那就是[/font][/size][font=黑体][size=3]凝血酶和血红素!![/size][/font][align=center][b]=================写在前面,背景知识介绍=======================[/b][/align][font=新宋体][b][size=4]凝血酶[/size][/b]是机体凝血系统的天然组分,是由[/font][font=新宋体]前体凝血酶原激活剂激活而转化成具有活性的凝血酶。[/font][color=black][font=宋体]正常血浆中存在无活性的凝血酶原,[/font][/color][color=black][font=宋体]通过对血液提取可以得到凝血酶原,经激活后上清液于沉淀分离即可得到凝血酶。[/font][/color][color=black][font=宋体]凝血酶[/font][/color][font=宋体]是一种糖蛋白,凝血酶[/font][font=宋体]([/font][font=Times New Roman,serif]thrombi,E.C,3.4.21.5[/font][font=宋体])[/font][font=宋体][/font][font=宋体]是由两条肽链之间以二硫键相连接,为蛋白水解酶。形状呈无定形粉末,易溶于水,难溶于乙醇、丙酮、乙醚等有机溶剂,但储存于[/font][font=Times New Roman,serif]2~8[/font][font=宋体]℃很稳定,水溶液室温[/font][font=Times New Roman,serif]8[/font][font=宋体]小时失活。遇热稀酸、碱、金属等活力降低。[/font][font=新宋体] 凝血酶可直接作用于血浆纤维蛋白,加速不溶性纤维蛋白凝块的生成,促进血液凝固。常以干粉或溶液局部应用于伤口或手术处,以控制毛细血管渗血。较多用于骨出血、扁桃体摘除和拔牙等。也可口服,用于胃和十二指肠出血。目前凝血酶的应用范围正日渐扩大,由单纯的局部外敷到外科手术、鼻、喉、口腔、妇产、泌尿急消化道等部位出血的止血,也可以作为多种外用止血药物的重要原料,其止血效果优于“对氨基苯甲酸”、“止血坏酸”、“止血敏”等通过注射后须经血管收缩而起止血作用的药物,故深受广大用户欢迎。据悉,国际新型高效局部止血药物—凝血酶将广泛应用于临床,是目前十分紧俏的凝血酶身价倍增,更趋紧缺。目前我国进口的凝血酶是从牛血中提取的。[/font][font=新宋体]凝血酶是机体凝血系统中的天然成分,国外主要在低温条件下从人或牛血液中提取凝血酶原,在经激活物激活而成凝血酶。其工艺流程为:[img]http://ng1.17img.cn/bbsfiles/images/2010/08/201008251635_238813_1947624_3.jpg[/img][/font][b][size=4][color=black][font=宋体]血红素[/font][/color][/size][/b][color=#333333][font=新宋体][/font][/color][color=black][font=宋体]是含铁卟啉衍生物,是由原卟啉和一个铁离子构成。如下图[img]http://ng1.17img.cn/bbsfiles/images/2010/08/201008251644_238816_1947624_3.jpg[/img][/font][/color][font=新宋体]在食品行业中,血红素可代替熟肉中得发色剂亚硝酸盐及人工合成色素。它可使肉制品产生一种诱人的鲜艳红色,增加其外观美感。更重要的是使用血红素可减少亚硝酸盐的致癌作用。在制药行业中,血红素可作为半合成胆红素原料,而且是制备抗癌的特效药。另外,血红素在临床上作为补铁剂,可治疗因缺铁引起的贫血症(在儿童、妇女中常见)。目前临床上用的非血红素补铁剂,主要从植物性食物中提取,以氢氧化铁络合物形式存在。这种铁络合物在人体中吸收率很低,并含有对人体有害的成分,而血红素补铁剂(即亚铁血红素)可直接被人体吸收,吸收率高达10%~20%。我国民间早有吃血治疗贫血的经验,但原血有异味,易腐败变质,难以作为补铁剂用于临床。从雪中提取血红素,可解决这一问题。血红素补铁剂将取代目前常用的补铁剂,成为深受欢迎的一代产品。[/font][color=black][font=宋体][/font][/color][font=新宋体]血液中的血红蛋白是由4分子亚铁血红素和分子珠蛋白结合而成的。再Ph3时,亚铁血红素与珠蛋白结合最疏松。更据此性质,提取实现从血液中分离出血球液,然后加水将血球液溶解(即溶血),调节Ph至3.0左右,加入适量丙酮,可是蛋白质凝固,亚铁血红素则溶于丙酮液中。此时若加入乙酸钠和鞣酸,即可使血红素沉淀析出。如加入羧甲纤维素(CM-C)阳离子交换剂,血红素可被CM-C吸附,然后过滤,就可以分离出血红素。[/font][b][color=black][font=新宋体][/font][/color][/b][img]http://ng1.17img.cn/bbsfiles/images/2010/08/201008251646_238819_1947624_3.jpg[/img][color=#333333][font=新宋体]用碱处理氯高铁血红素,使之变成羟高铁血红素,将此化合物还原就可得到血红素。它的吸收光谱的主要吸收带在581(α带),545(β带),415(γ带)毫微米.中心的铁原子显有进一步和二个碱基形成配位键的八面体的强烈倾向[/font][/color][b][size=4][font=新宋体][/font][/size][/b][color=#333333][font=新宋体] [/font][/color][color=#333333][font=新宋体]特别是和吡啶、喹啉、烟碱、4-甲基咪唑等三级氨基的二个构成比较稳定的血色原(例如吡啶血色原).这时基于铁原子的3d电子能级结构的永久磁性消失.它的主吸收带为尖峰,在557、525、430毫微米附近.如果把氰酸作为碱基,就生成一个氰酸和二个结合体.还常和蛋白质结合,吸收带多在560、530、430毫微米附近,一般说血红素和血色原自动氧化性强.能和氧发生反应,容易被氧化成三价铁的羟高铁血红素.但一如血红蛋白那样,可与蛋白质(珠蛋白)中的组氨酸结合,被包围在疏水环境里时是比较稳定的,很难发生自动氧化。[/font][/color][font=新宋体][/font][align=center][b]=====================华丽丽的分割,下面介绍我的试验方法=========================[/b][/align][font=楷体_GB2312]1.2[/font][font=楷体_GB2312]实验方法[/font][font=新宋体]1.2.1[/font][font=新宋体]凝血酶的制备 [/font][color=black][font=宋体]取血球研磨后称[/font][/color][color=black]10g[/color][color=black][font=宋体],加入蒸馏水,搅拌[/font][/color][color=black]30min[/color][color=black][font=宋体],使血球溶血,,再加入[/font][/color][color=black]5[/color][color=black][font=宋体]倍体积的氯仿,滤去纤维收集滤液。将上述除去纤维的血球一移入量筒加[/font][/color][color=black]4[/color][color=black][font=宋体]-[/font][/color][color=black]5[/color][color=black][font=宋体]倍体积的丙酮溶液。用[/font][/color][color=black]1mol/L[/color][color=black][font=宋体]盐酸校正[/font][/color][color=black]PH[/color][color=black][font=宋体]至[/font][/color][color=black]2[/color][color=black][font=宋体]-[/font][/color][color=black]3[/color][color=black][font=宋体],搅拌抽提[/font][/color][color=black]10min[/color][color=black][font=宋体],然后过滤收集沉淀。将上述溶液装入蒸馏瓶中,水溶蒸馏回收丙酮([/font][/color][color=black]t [/color][color=black][font=宋体]控在[/font][/color][color=black]60[/color][color=black][font=宋体]℃左右)待滤液浓缩至干时,既有沉淀析出。收集沉淀并称重。此即为血红素粗品。将血红素[/font][/color][color=black]4[/color][color=black][font=宋体]倍量的吡啶、[/font][/color][color=black]7[/color][color=black][font=宋体]倍量的氯仿倒入瓶中,然后加入粗品血红素,充分振荡[/font][/color][color=black]30min[/color][color=black][font=宋体],过滤后收集滤液。滤渣用氯仿洗涤,合并两次滤液。先把适量的冰醋酸加热至沸腾后,加入各占[/font][/color][color=black]1/7[/color][color=black][font=宋体]体积(相对于冰醋酸而言)的饱和氯化钠溶液和盐酸,随后加入滤液,搅匀后过滤,滤渣用氯仿洗涤,合并两次滤液,用旋转蒸馏器蒸馏。收集蒸馏剩物记得到产品。[/font][/color][color=black][font=新宋体][/font][/color][font=新宋体] [/font][font=新宋体]分离血浆、提取凝血酶原:取人血液,按1Kg人血液加3.8g柠檬酸三钠投料,脚板均匀,装入离心管中,以3000r/min的速度离心15min,分出血球(可供制备血红素),收集血浆。(已完成)吸取上清血浆40mL,加蒸馏水到400Ml(360mL),用2%的乙酸调Ph5.3,静置数分钟,出现絮状物后,在离心机上以3000r/min的速度离心15min,弃去上清液,取沉淀物沉重,此即为凝血酶原。[/font][font=新宋体] [/font][font=新宋体]凝血酶原的激活:在30℃条件下,将凝血酶原溶于1~2倍的0.9%氯化钠溶液中,脚板均匀,加入占凝血酶原质量1.5%的氯化钙,搅拌15min。在4℃下静置1.5小时,保证凝血酶原转化为凝血酶。[/font][font=新宋体] [/font][font=新宋体]沉淀分离凝血酶原:将激活的凝血酶溶液用离心机以3000r/min的速度离心15min,弃去沉淀。上清夜于量筒内,加入等量的预冷至4℃的丙酮,搅拌均匀,在冰箱中放置分层。然后用力离心机分离,收集沉淀,上清液可供回收丙酮。沉淀分别用95%乙醇和污水乙醇洗涤,放置在干燥器中干燥,即得凝血酶粗品。[/font][font=新宋体]计算:[/font][i][font=新宋体]凝血酶得率=凝血酶干重g/血清Ml * 100%[/font][/i][font=新宋体]1.2.2[/font][font=新宋体]血红素的制备[/font][font=新宋体]1.2.2.1[/font][font=新宋体]血红素的粗制[/font][font=新宋体] [/font][font=新宋体]分离后溶血:称取50g血球,边研磨边加蒸馏水至100Ml,搅拌30min,使血球溶血,在加入2倍体积的氯仿,滤去纤维,收集滤液。[/font][font=新宋体] [/font][font=新宋体]抽提:用离心机以3000r/min的速度离心10min,弃去沉淀,取上清液,即为红色溶血液,加5倍体积的丙酮溶液,(其中含丙酮体积3%的盐酸)。用1mol/L的演算校正Ph至2~3,搅拌均匀,然后过滤,收集滤液。[/font][font=新宋体] [/font][font=新宋体]蒸馏:将上述溶液于水浴上蒸馏回收丙酮(温度控制在60℃左右),待滤液浓缩至干时,既有沉淀析出。[/font][font=新宋体] [/font][font=新宋体]干燥:把产品干燥后,可得无定性黑绿色粉末状物,装入瓶中保存。 [/font][font=新宋体]1.2.2.2[/font][font=新宋体]血红素的精制[/font][font=新宋体] [/font][font=新宋体]提取:先将血红素4倍量的吡啶、7倍量的氯仿倒入瓶中,然后加入粗品血红素,充分振荡30min,过滤后收集滤液。滤渣用氯仿洗涤,合并两次滤液。[/font][font=新宋体] [/font][font=新宋体]沉淀、静置过夜、洗涤干燥:先把适量冰醋酸加热至沸腾后,加入各1/7体积(相对于冰醋酸来而言)的饱和氯化钠和盐酸,随后加入滤液,搅匀后过滤,滤渣用氯仿洗涤,合并两次滤液,静置过夜,过滤收集滤饼,干燥,即得产品。[/font][font=新宋体][/font][font=新宋体]计算:[/font][font=新宋体] [/font][i][font=新宋体]血红素得率=黑绿色血红素g/血球重g *100%[/font][/i][align=center][font=新宋体][b]=======================结果计算及分析====================[/b][/font][/align][i][font=新宋体]2.[/font][/i][font=新宋体]结果与分析[/font][font=新宋体]2.1[/font][font=新宋体]凝血酶制备:[/font][img]http://ng1.17img.cn/bbsfiles/images/2010/08/201008251651_238820_1947624_3.jpg[/img][font=新宋体]凝血酶原(Ⅱ,prothrombin)是含582氨基酸残基的酶原,被因子Xa在Arg-Thr及Arg-Ile处切开,切除N