两会声音:癌症的早筛早诊早治必须重视!
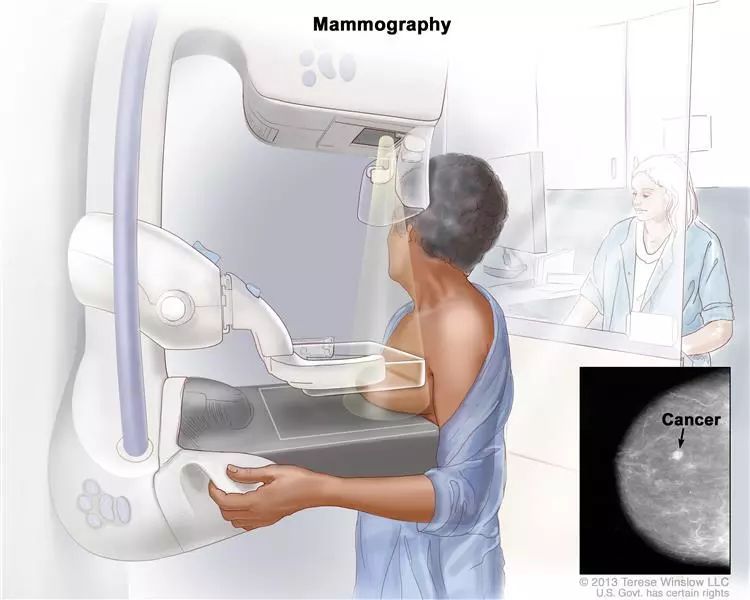
p 李克强总理在作2019年政府工作报告中指出——/pp style="text-align: center"img src="https://img1.17img.cn/17img/images/201903/uepic/19d94137-c510-4829-b67b-fcc014d2be13.jpg" title="1.jpg" alt="1.jpg" width="603" height="336" style="width: 603px height: 336px "//pp style="text-align: center "strong图片来源:中国政府网/strong/pp 这是国家层面再一次对癌症防治提出了要求!为了自身健康,我们每一个人都要高度重视起来!/pp 早期癌症治愈率可达90%以上,早诊早治是国际公认对抗癌症的最有效手段,很多发达国家已经从中受益。最新版美国癌症年度报告显示,过去20年美国癌症死亡率已经下降27%,即已有超过210万人免于死于癌症,且癌症患者5年生存率已达64%。/pp 去年7月,美国癌症中心发布了未来10年肿瘤一级抗击计划,称为“2030癌症预防和死亡率下降蓝图”,详细分析了1930-2010年80年间美国癌症死亡率先升后降的变化,癌症筛查被再次强调。/pp 相比之下,我国癌症检出率比发达国家低3-4倍,患者5年生存率仅为31%,不到美国的一半。”/pp style="text-align: center "span style="color: rgb(0, 0, 0) "strong美国癌症研究院:四大有效的筛查方式!/strong/span/pp 癌症的筛查是降低发病率和死亡率的关键一环,但并非所有的筛查测试都有帮助,有一些筛查存在风险,那么哪些筛查才是真正有效的,又有哪些人群最应该接受筛查呢?近日,美国癌症研究院公布了四类最有效的筛查方式,我们一起来看下。/pp NCI推荐的有效癌症筛查是指能够早期发现癌症,并经过证实可以降低死亡率的检测方式!/pp strong一,结肠镜检查和粪便检查/strong/pp 大部分结直肠癌症状会被忽视或误诊为其他疾病,例如病毒感染或肠易激综合症时,往往错过了癌症最佳的治疗时期,当确诊时往往已经到达晚期。/pp 美国癌症协会报告称,“span style="color: rgb(192, 0, 0) "只有39%的CRC患者被诊断为局限期疾病(最早阶段尚未扩散到附近组织),其五年生存率为90% 而晚期患者的五年生存率仅为14%。/span”/pp 最近,著名临床医学杂志《柳叶刀》发表最新研究,一次肠癌筛选检查可以使发生肠癌的风险降低超过三分之一,并且可以挽救无数的生命。/pp style="text-align: center"img src="https://img1.17img.cn/17img/images/201903/uepic/4490f73e-2753-45ef-afe3-d0963e2f2058.jpg" title="2.jpg" alt="2.jpg" width="494" height="554" style="width: 494px height: 554px "//pp span style="color: rgb(0, 0, 0) "结肠镜检查:将一根细的发光管插入肛门和直肠并进入结肠,以寻找异常区域。/span/pp span style="color: rgb(255, 255, 255) " span style="background-color: rgb(192, 0, 0) "strong哪些人群需要筛查:/strong/span/span/pp 1. 长期摄入高脂、高蛋白、高热量食物的人;/pp 2. 40岁以上,长期摄入酒精、油炸食品等;/pp 3. 有慢性溃疡性结肠炎、大肠腺瘤、家族性结肠腺瘤病、大肠息肉等慢性溃疡性结肠炎者;/pp 4. 有大肠癌家族史者。/pp strong二,低剂量螺旋CT/strong/pp 早期肺癌常常无明显症状,多数因体检发现。当病情发展到中晚期时,常出现刺激性干咳,痰中带血、胸痛、发热、气促等表现。/pp 美国癌症研究院已经对三种筛查进行了研究,包括低剂量 螺旋CT扫描(LDCT扫描),胸部X光和痰细胞学,其中只有低剂量螺旋CT筛查肺癌的测试被证明可以减少55至74岁重度吸烟者的肺癌死亡率。胸部X线检查,痰细胞学检查都不能降低死于肺癌的风险。/pp span style="background-color: rgb(192, 0, 0) color: rgb(255, 255, 255) "哪些人群需要筛查:/span/pp 1. 长期受环境污染,长期吸烟者、吸二手烟(被动吸烟)者;/pp 2. 慢性肺部疾病(肺结核、矽肺、尘肺等);/pp 3. 人体内在因素(如家族遗传、免疫机能降低以及内分泌功能失调等)。/pp strong三,乳腺X光检查/strong/pp 25年之间,美国乳腺癌的死亡率下降了39%,应归功于乳腺筛查的普及、治疗效果的提高、肥胖减缓。多种因素,共同减少乳腺癌。/pp 在我国,乳腺癌是城市地区女性高发的第一大癌症,大城市的发病风险是小城市的2倍。/pp 乳腺X线检查已被证明可以减少40至74岁女性的死亡率,特别是50岁以上的女性。乳房X光检查是乳腺癌最常见的筛查方法。但对于乳房组织致密的女性,乳腺X线摄影不太可能发现乳腺肿瘤。/pp style="text-align: center"img src="https://img1.17img.cn/17img/images/201903/uepic/f0d2d621-09e7-4ebc-964a-4e6d058ffcc5.jpg" title="3.jpg" alt="3.jpg" width="582" height="465" style="width: 582px height: 465px "//pp 乳房X光摄影:将乳房压在两块板之间。X射线用于拍摄乳房组织。/pp span style="color: rgb(255, 255, 255) background-color: rgb(192, 0, 0) "哪些人群适合筛查:/span/pp 未育或≥35岁初产妇;/pp 月经初潮≤12岁,或行经≥42年的妇女;/pp 一级亲属在50岁前患乳腺癌者;/pp 两个以上一级或二级亲属在50岁以后患乳腺癌或卵巢癌者;/pp 对侧乳腺癌史或经乳腺活检证实为重度非典型增生或乳管内乳头状瘤病者;/pp 胸部放射治疗史(≥10年)者。/pp strong四,巴氏试验和人乳头瘤病毒(HPV)检测/strong/pp 宫颈癌是一种在子宫颈中形成恶性(癌)细胞的疾病。人乳头瘤病毒(HPV)感染是宫颈癌的主要危险因素。使用巴氏试验筛查子宫颈癌自1950年以来减少了新发宫颈癌病例数和宫颈癌死亡人数。/pp 这些测试可单独使用或组合使用,可以早期发现和预防宫颈癌。它们可以预防疾病,因为它们可以在癌症发生之前发现异常细胞。比如,在某些巴氏试验阳性结果后,可以进行HPV试验。/pp span style="color: rgb(255, 255, 255) background-color: rgb(192, 0, 0) "哪些人群适合筛查:/span/pp 已婚或有性生活史3年的女性;/pp 口服避孕药。/pp 当然,癌症的筛查方式远不止这些,比如还有超声检查,PET检查等,大家还是要咨询权威的机构,根据自身的情况选择最佳的筛查方案。/p