我们实验室的小型仪器(测定水样)型号分别为:HACH 2100AN浊度仪、HACH Sension3 PH计、YSI3200型电导率仪和YSI溶解氧仪,每半年一次期间核查,想请教各位大侠,平时都是怎么做的,怎么根据核查校准的数据判断仪器是否合格?
请问各位专家,何为"总离子浓度"?和TDS(总溶解性固体)或电导率是一个概念吗,有可以直接测量‘总离子浓度“的仪器吗?
新手咨询:新到上海雷磁JPSL-605F溶解氧测定仪,说明书上有说零度及满度标定,请问溶解氧测定仪是否每次测之前都要标定?还是说定期标定就可以了?(周期多久)。溶解氧测定有些什么注意事项?还有这台仪器标配没有温度探头,但有个接口,这个是否必须?就是说溶解氧的测定是否像pH,电导率等指标样要校正到25°的值?
我公司水质自动监测站安装的德国科泽K100溶解氧,我们自己做了一个测量罐,装上去以后发现数据老不稳定,很多时候是0,而装在同一个罐的也是科泽K100的电导率却没有问题,请各路大侠指点迷津..我知道一点好象溶解氧的安装环境要流量和流速.....
对于地下水来说,电导率高,溶解性总固体也高,当然(PH相近).我们有一批地下水水样,溶解性总固体异常高,而电导率没有那么高.如一样品:电导率:0.76微西/cm,溶解性总固体:1800mg/L.另一样品:电导率:0.78微西/cm,溶解性总固体:570mg/L.如何解释???
测溶解性总固体费时,既然与电导率存在比例关系,能否通过测电导的方式来换算出溶解性总固体?
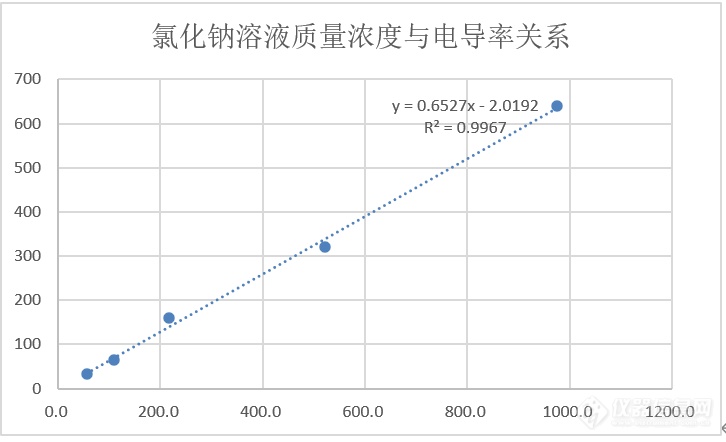
[align=center][b][font=宋体]探究[/font][font=宋体]水质中总溶解固体与电导率关系[/font][/b][/align][align=center][font=宋体]吕炎 张艳艳 刘翔 王柳[/font][/align][align=center][font=宋体](万华化学(宁波)有限公司,浙江省宁波市 315812)[/font][/align][b][font=楷体][color=black]摘要:[/color][/font][/b][font=楷体][color=black]本文[/color][/font][font=楷体][color=black]通过实验[/color][/font][font=楷体][color=black]发现电导率与总溶解固体含量(TDS)之间的关系系数不是固定值0.5,因此在实际生产过程中,不可采用测定电导率值来折算总溶解固体含量(TDS)。同时本文来通过数学建模的方法,完成水质电导率与总溶解固体含量(TDS)之间的关系,用于相似组分条件下的电导率与总溶解固体含量(TDS)折算。[/color][/font][b][font=楷体][color=black]关键词[/color][/font][font=楷体]:[/font][/b][font=楷体][color=black]电导率 总溶解固体 数学建模[/color][/font][b][font='Times New Roman',serif] [/font]1、背景[/b][align=left][font=楷体][color=black]循环水、锅炉水作为工业生产过程中常见的工业用水,在日常使用中,为保证水质安全,常会添加一些阻垢剂、缓蚀剂、抑泡剂等,这些助剂多为盐类物质,工艺生产过程中,为更好地控制助剂添加量,需要测定工业用水中总溶解固体(TDS)的含量。但目前国家标准中采用重量法分析总溶解固体(TDS)的含量,但该方法存在操作繁琐、耗时长等特点,影响样品的分析效率。目前市场上存在TDS计用于测定总溶解固体(TDS)含量,该方法主要通过测定溶液中电导率来折算溶液中存在的溶解性固体含量。一般情况下,[/color][/font][color=black][url=https://baike.baidu.com/item/%E7%94%B5%E5%AF%BC%E7%8E%87/1016751?fromModule=lemma_inlink][font=楷体][color=black]电导率[/color][/font][/url][/color][font=楷体][color=black]越高,盐份越高,TDS越高,实验室中也会采用“1ppmTDS=2[/color][/font][color=black][url=https://baike.baidu.com/item/%CE%BCS/cm/5625737?fromModule=lemma_inlink][font=楷体][color=black]μS/cm[/color][/font][/url][/color][font=楷体][color=black]”[/color][/font][color=black] [/color][font=楷体][color=black]的关系,测定溶液电导率间接测定总溶解固体(TDS)含量。[/color][/font][/align][align=left][font=楷体][color=black]但工艺生产的差异,考虑工业用水的助剂成份不同,完全采用上述的关系折算部可靠,本文通过实验研究水质中总溶解固体与电导率的关系。[/color][/font][/align][b]2、总溶解固体与电导率介绍2.1 总溶解固体介绍[/b][font=楷体]总溶解性固体(TDS)是指溶解在水中的固体(如氯化物、硫酸盐、硝酸盐、重碳酸盐及硅酸盐等)的总量,TDS值越高,表示水中含有的溶解物越多。 总溶解固体指水中全部溶质的总量,包括[url=https://baike.baidu.com/item/%E6%97%A0%E6%9C%BA%E7%89%A9/781954?fromModule=lemma_inlink][color=windowtext]无机物[/color][/url]和[/font][url=https://baike.baidu.com/item/%E6%9C%89%E6%9C%BA%E7%89%A9/300787?fromModule=lemma_inlink][font=楷体][color=windowtext]有机物[/color][/font][/url][font=楷体]两者的含量。一般可用[/font][url=https://baike.baidu.com/item/%E7%94%B5%E5%AF%BC%E7%8E%87/1016751?fromModule=lemma_inlink][font=楷体][color=windowtext]电导率[/color][/font][/url][font=楷体]值大概了解溶液中的盐份, [/font][url=https://baike.baidu.com/item/%E7%94%B5%E5%AF%BC%E7%8E%87/1016751?fromModule=lemma_inlink][font=楷体][color=windowtext]电导率[/color][/font][/url][font=楷体]越高,盐份越高,TDS越高。在无机物中,除溶解成离子状的成分外,还可能有呈分子状的无机物。由于天然水中所含的有机物以及呈分子状的无机物一般可以不考虑,所以一般也把含盐量称为总溶解固体。[/font][font=楷体]总溶解性固体(TDS)的测定:将待测水样用慢速[/font][url=https://baike.baidu.com/item/%E5%AE%9A%E9%87%8F%E6%BB%A4%E7%BA%B8/6827825?fromModule=lemma_inlink][font=楷体][color=windowtext]定量滤纸[/color][/font][/url][font=楷体]或滤板孔径为2~5μm的玻璃砂芯漏斗过滤。用移液管移取100mL过滤后的水样,置于已于105~110℃干燥至恒重的蒸发皿中。将蒸发皿置于沸水浴上蒸发至干,再将蒸发皿于105~110℃下干燥至恒重。[/font][font=楷体][color=black]溶解性固体总量的计算公式,通常情况下:[/color][/font][align=center][font=楷体][color=black]C=(W[sub]2[/sub]-W[sub]1[/sub])*10[sup]6[/sup]/V[/color][/font][/align][font=楷体][color=black]式中:[/color][/font][font=楷体][color=black]——C为溶解性固体的含量(mg/L)[/color][/font][font=楷体][color=black]——W[sub]2[/sub]为蒸发皿和溶解性固体总质量(g)[/color][/font][font=楷体][color=black]——W[sub]1[/sub]为蒸发皿的总质量(g)[/color][/font][font=楷体][color=black]——V为水的体积(mL)[/color][/font][b]2.2 电导率介绍[/b][font=楷体] [/font][font=楷体]电导率(conductivity)是用来描述物质中[/font][url=https://baike.baidu.com/item/%E7%94%B5%E8%8D%B7?fromModule=lemma_inlink][font=楷体][color=windowtext]电荷[/color][/font][/url][font=楷体]流动难易程度的参数。由于水中含有各种溶解盐类,并以离子的形式存在。当水中插入一对电极时,通电之后,在电场的作用下,带电的离子就产生一定方向的移动。水中阴离子移向阳极,使水溶液起导电作用,水的导电能力的强弱程度,就称为电导(或电导度),用G表示。电导反映了水中含盐量的多少,是水的纯净程度的一个重要指标,水越纯净,含盐量越少,电阻越大,电导越小,超纯水几乎不能导电。通常,当电压保持不变时,这种直流电电路中的电流与电导成比例关系。如果电导加倍,则电流也加倍;如果电导减少到它初始值的1/10,电流也会变为原来的1/10。电导与电导率之间存在一定的关系,称作为电导池常数,为K[sub]cell[/sub]=l/A,单位为m[sup]-1[/sup],因电极间距离l 和电极面积A不能精确地测量,实际测量时常用比较法测定电导池常数,即测定已知电导率的标准溶液(通常为KCl溶液)的K[sub]cell[/sub]。电导(G)与电导率([/font][font=等线]κ[/font][font=楷体])[/font][font=楷体]关系如下:G=[/font][font=等线]κ*A/l=κ/K[sub]cell[/sub]。[/font][b][font=黑体]3[/font][font=黑体]、探究水质中总溶解固体与电导率关系[/font][/b] [font=楷体]为[/font][font=楷体]了探究水质中总溶解固体与电导率关系,结合实验室现有的盐类试剂进行如下实验探究[/font][font=楷体]。[/font][b][font=黑体]3.1 [/font][font=黑体]探究单一盐类与电导率关系[/font][/b] [font=楷体]采用氯化钠、氯化钾、硫酸钠、乙酸钠、硫酸铜、磷酸氢二钾和氯化钙等试剂配制一定溶度的溶液,探究总溶解固体与电导率之间的关系。[/font][align=left][b][font=黑体]3.1.1 [/font][font=黑体]氯化钠溶液实验[/font][/b][/align][align=left][font=楷体]配制一定梯度的氯化钠溶液,分别测定梯度溶液对应的电导率,形成如下表格:[/font][/align][table][tr][td=4,1] [align=center][font=楷体]氯化钠溶液实验数据统计[/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]样品[/font][/align] [/td][td] [align=center][font=楷体]质量浓度/mg/L[/font][/align] [/td][td] [align=center][font=楷体]理论电荷的物质的量浓度/mol/L[/font][/align] [/td][td] [align=center][font=楷体]电导率/[/font]μ[font=楷体]S/cm[/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度1[/font][/align] [/td][td] [align=center][font=等线][color=black]32.035[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.0010964[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]55.7[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度2[/font][/align] [/td][td] [align=center][font=等线][color=black]64.07[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.002192[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]109.4[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度3[/font][/align] [/td][td] [align=center][font=等线][color=black]160.175[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.004386[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]217.8[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度4[/font][/align] [/td][td] [align=center][font=等线][color=black]320.35[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.010964[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]522.5[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度5[/font][/align] [/td][td] [align=center][font=等线][color=black]640.7[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.02192[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]975.1[/color][/font][/align] [/td][/tr][/table][align=center][font=楷体]表1:氯化钠溶液实验数据统计[/font][/align][font=宋体] [/font][font=楷体]结合上述数据,绘制电导率与质量浓度和理论电荷的物质的量浓度的关系图,如下:[/font][align=center][img=,481,]https://ng1.17img.cn/bbsfiles/images/2023/08/202308031340334240_8094_3989257_3.png!w690x420.jpg[/img][/align][align=center][font=楷体]图1:氯化钠溶[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]量浓度与电导率关系图[/font][/align][align=center][img=,481,]https://ng1.17img.cn/bbsfiles/images/2023/08/202308031340451095_7818_3989257_3.png!w690x419.jpg[/img][/align][align=center][font=楷体]图2:氯化钠溶液理论电荷的物质的量浓度与电导率关系图[/font][/align][align=left][b][font=黑体]3.1.2[/font][font=黑体]氯化钾溶液实验[/font][/b][/align][align=left][font=楷体]配制一定梯度的氯化钾溶液,分别测定梯度溶液对应的电导率,形成如下表格:[/font][/align][align=left][font=楷体] [/font][/align] [table][tr][td=4,1] [align=center][font=楷体]氯化钾溶液实验数据统计[/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]样品[/font][/align] [/td][td] [align=center][font=楷体]质量浓度/mg/L[/font][/align] [/td][td] [align=center][font=楷体]理论电荷的物质的量浓度/mol/L[/font][/align] [/td][td] [align=center][font=楷体]电导率/[/font]μ[font=楷体]S/cm[/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度1[/font][/align] [/td][td] [align=center][font=等线][color=black]37.08[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.0009948[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]52.0[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度2[/font][/align] [/td][td] [align=center][font=等线][color=black]74.16[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.0019896[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]116.6[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度3[/font][/align] [/td][td] [align=center][font=等线][color=black]148.32[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.00398[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]233.6[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度4[/font][/align] [/td][td] [align=center][font=等线][color=black]370.8[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.009948[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]569.2[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度5[/font][/align] [/td][td] [align=center][font=等线][color=black]741.6[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.019896[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]1180.0[/color][/font][/align] [/td][/tr][/table][align=center][font=楷体]表2:氯化钾溶液实验数据统计[/font][/align][font=楷体]结合上述数据,绘制电导率与质量浓度和理论电荷的物质的量浓度的关系图,如下:[/font][align=center][img=,481,]https://ng1.17img.cn/bbsfiles/images/2023/08/202308031340555571_1576_3989257_3.png!w690x418.jpg[/img][/align][align=center][font=楷体]图3:氯化钾溶[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]量浓度与电导率关系图[/font][/align][align=center][img=,481,]https://ng1.17img.cn/bbsfiles/images/2023/08/202308031341053998_3826_3989257_3.png!w690x418.jpg[/img][/align][align=center][font=楷体]图4:氯化钾溶液理论电荷的物质的量浓度与电导率关系图[/font][/align][align=left][b][font=黑体]3.1.3[/font][font=黑体]硫酸钠溶液实验[/font][/b][/align][align=left][font=楷体]配制一定梯度的硫酸钠溶液,分别测定梯度溶液对应的电导率,形成如下表格:[/font][/align] [table][tr][td=4,1] [align=center][font=楷体]硫酸钠溶液实验数据统计[/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]样品[/font][/align] [/td][td] [align=center][font=楷体]质量浓度/mg/L[/font][/align] [/td][td] [align=center][font=楷体]理论电荷的物质的量浓度/mol/L[/font][/align] [/td][td] [align=center][font=楷体]电导率/[/font]μ[font=楷体]S/cm[/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度1[/font][/align] [/td][td] [align=center][font=等线][color=black]71.205[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.0020052[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]88.9[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度2[/font][/align] [/td][td] [align=center][font=等线][color=black]142.41[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.004012[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]199.1[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度3[/font][/align] [/td][td] [align=center][font=等线][color=black]284.82[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.00802[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]403.2[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度4[/font][/align] [/td][td] [align=center][font=等线][color=black]712.05[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.020052[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]942.6[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度5[/font][/align] [/td][td] [align=center][font=等线][color=black]1424.1[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.04012[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]1823.0[/color][/font][/align] [/td][/tr][/table][align=center][font=楷体]表3:硫酸钠溶液实验数据统计[/font][/align][font=楷体]结合上述数据,绘制电导率与质量浓度和理论电荷的物质的量浓度的关系图,如下:[/font][align=center][img=,444,]https://ng1.17img.cn/bbsfiles/images/2023/08/202308031341148663_4966_3989257_3.png!w673x415.jpg[/img][/align][align=center][font=楷体]图5:硫酸钠溶[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]量浓度与电导率关系图[/font][/align][align=center][img=,445,]https://ng1.17img.cn/bbsfiles/images/2023/08/202308031341235789_463_3989257_3.png!w679x413.jpg[/img][/align][align=center][font=楷体]图6:硫酸钠溶液理论电荷的物质的量浓度与电导率关系图[/font][/align][align=left][b][font=黑体]3.1.4[/font][font=黑体]乙酸钠溶液实验[/font][/b][/align][align=left][font=楷体]配制一定梯度的乙酸钠溶液,分别测定梯度溶液对应的电导率,形成如下表格:[/font][/align] [table][tr][td=4,1] [align=center][font=楷体]乙酸钠溶液实验数据统计[/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]样品[/font][/align] [/td][td] [align=center][font=楷体]质量浓度/mg/L[/font][/align] [/td][td] [align=center][font=楷体]理论电荷的物质的量浓度/mol/L[/font][/align] [/td][td] [align=center][font=楷体]电导率/[/font]μ[font=楷体]S/cm[/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度1[/font][/align] [/td][td] [align=center][font=等线][color=black]42.83[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.0010442[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]29.7[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度2[/font][/align] [/td][td] [align=center][font=等线][color=black]85.66[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.002088[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]69.6[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度3[/font][/align] [/td][td] [align=center][font=等线][color=black]171.32[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.004176[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]139.6[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度4[/font][/align] [/td][td] [align=center][font=等线][color=black]428.3[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.010442[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]371.4[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度5[/font][/align] [/td][td] [align=center][font=等线][color=black]856.6[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.02088[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]716.5[/color][/font][/align] [/td][/tr][/table][align=center][font=楷体]表4:乙酸钠溶液实验数据统计[/font][/align][font=楷体]结合上述数据,绘制电导率与质量浓度和理论电荷的物质的量浓度的关系图,如下:[/font][align=center][img=,450,]https://ng1.17img.cn/bbsfiles/images/2023/08/202308031341329070_1238_3989257_3.png!w682x406.jpg[/img][/align][align=center][font=楷体]图7:乙酸钠溶[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]量浓度与电导率关系图[/font][/align][align=center][img=,453,]https://ng1.17img.cn/bbsfiles/images/2023/08/202308031341422100_8193_3989257_3.png!w688x394.jpg[/img][/align][align=center][font=楷体]图8:乙酸钠溶液理论电荷的物质的量浓度与电导率关系图[/font][/align][align=left][b][font=黑体]3.1.5[/font][font=黑体]硫酸铜溶液实验[/font][/b][/align][align=left][font=楷体]配制一定梯度的硫酸铜溶液,分别测定梯度溶液对应的电导率,形成如下表格:[/font][/align] [table][tr][td=4,1] [align=center][font=楷体]硫酸铜溶液实验数据统计[/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]样品[/font][/align] [/td][td] [align=center][font=楷体]质量浓度/mg/L[/font][/align] [/td][td] [align=center][font=楷体]理论电荷的物质的量浓度/mol/L[/font][/align] [/td][td] [align=center][font=楷体]电导率/[/font]μ[font=楷体]S/cm[/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度1[/font][/align] [/td][td] [align=center][font=等线][color=black]79.575[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.0019944[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]79.1[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度2[/font][/align] [/td][td] [align=center][font=等线][color=black]159.15[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.0039884[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]178.8[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度3[/font][/align] [/td][td] [align=center][font=等线][color=black]318.3[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.007976[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]333.4[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度4[/font][/align] [/td][td] [align=center][font=等线][color=black]795.75[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.019944[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]722.7[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度5[/font][/align] [/td][td] [align=center][font=等线][color=black]1591.5[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.039884[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]1250.1[/color][/font][/align] [/td][/tr][/table][align=center][font=楷体]表5:硫酸铜溶液实验数据统计[/font][/align][font=楷体]结合上述数据,绘制电导率与质量浓度和理论电荷的物质的量浓度的关系图,如下:[/font][align=center][img=,449,]https://ng1.17img.cn/bbsfiles/images/2023/08/202308031341522903_3268_3989257_3.png!w679x411.jpg[/img][/align][align=center][font=楷体]图9:硫酸铜溶[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]量浓度与电导率关系图[/font][/align][align=center][img=,454,]https://ng1.17img.cn/bbsfiles/images/2023/08/202308031341598896_2218_3989257_3.png!w684x413.jpg[/img][/align][align=center][font=楷体]图10:硫酸铜溶液理论电荷的物质的量浓度与电导率关系图[/font][/align][align=left][b][font=黑体]3.1.6[/font][font=黑体]磷酸氢二钾溶液实验[/font][/b][/align][align=left][font=楷体]配制一定梯度的磷酸氢二钾溶液,分别测定梯度溶液对应的电导率,形成如下表格:[/font][/align] [table][tr][td=4,1] [align=center][font=楷体]磷酸氢二钾溶液实验数据统计[/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]样品[/font][/align] [/td][td] [align=center][font=楷体]质量浓度/mg/L[/font][/align] [/td][td] [align=center][font=楷体]理论电荷的物质的量浓度/mol/L[/font][/align] [/td][td] [align=center][font=楷体]电导率/[/font]μ[font=楷体]S/cm[/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度1[/font][/align] [/td][td] [align=center][font=等线][color=black]68.12[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.0020024[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]47.4[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度2[/font][/align] [/td][td] [align=center][font=等线][color=black]136.24[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.004004[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]84.3[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度3[/font][/align] [/td][td] [align=center][font=等线][color=black]272.48[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.008008[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]173.6[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度4[/font][/align] [/td][td] [align=center][font=等线][color=black]681.2[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.020024[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]432.9[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度5[/font][/align] [/td][td] [align=center][font=等线][color=black]1362.4[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.04004[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]862.8[/color][/font][/align] [/td][/tr][/table][align=center][font=楷体]表6:磷酸氢二钾溶液实验数据统计[/font][/align][font=楷体]结合上述数据,绘制电导率与质量浓度和理论电荷的物质的量浓度的关系图,如下:[/font][align=center][img=,456,]https://ng1.17img.cn/bbsfiles/images/2023/08/202308031342097154_1569_3989257_3.png!w689x415.jpg[/img][/align][align=center][font=楷体]图11:磷酸氢二钾溶[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]量浓度与电导率关系图[/font][/align][align=center][img=,457,]https://ng1.17img.cn/bbsfiles/images/2023/08/202308031342183743_1641_3989257_3.png!w690x412.jpg[/img][/align][align=center][font=楷体]图12:磷酸氢二钾溶液理论电荷的物质的量浓度与电导率关系图[/font][/align][align=left][b][font=黑体]3.1.7 [/font][font=黑体]氯化钙溶液实验[/font][/b][/align][align=left][font=楷体]配制一定梯度的氯化钙溶液,分别测定梯度溶液对应的电导率,形成如下表格:[/font][/align] [table][tr][td=4,1] [align=center][font=楷体]氯化钙溶液实验数据统计[/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]样品[/font][/align] [/td][td] [align=center][font=楷体]质量浓度/mg/L[/font][/align] [/td][td] [align=center][font=楷体]理论电荷的物质的量浓度/mol/L[/font][/align] [/td][td] [align=center][font=楷体]电导率/[/font]μ[font=楷体]S/cm[/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度1[/font][/align] [/td][td] [align=center][font=等线][color=black]55.5[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.0019896[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]97.1[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度2[/font][/align] [/td][td] [align=center][font=等线][color=black]110.4[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.0039792[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]194.2[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度3[/font][/align] [/td][td] [align=center][font=等线][color=black]220.8[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.00796[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]376.8[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度4[/font][/align] [/td][td] [align=center][font=等线][color=black]552.0[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.019896[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]911.0[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]梯度5[/font][/align] [/td][td] [align=center][font=等线][color=black]1104.0[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]0.039792[/color][/font][/align] [/td][td] [align=center][font=等线][color=black]1853.9[/color][/font][/align] [/td][/tr][/table][align=center][font=楷体]表7:氯化钙溶液实验数据统计[/font][/align][font=楷体]结合上述数据,绘制电导率与质量浓度和理论电荷的物质的量浓度的关系图,如下:[/font][align=center][img=,465,]https://ng1.17img.cn/bbsfiles/images/2023/08/202308031342273895_5727_3989257_3.png!w690x417.jpg[/img][/align][align=center][font=楷体]图13:氯化钙溶[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]量浓度与电导率关系图[/font][/align][align=center][img=,458,]https://ng1.17img.cn/bbsfiles/images/2023/08/202308031342351706_9837_3989257_3.png!w690x376.jpg[/img][/align][align=center][font=楷体]图14:氯化钙溶液理论电荷的物质的量浓度与电导率关系图[/font][/align][align=left][b][font=黑体]3.1.8 [/font][font=黑体]单一溶液实验总结[/font][/b][/align][font=楷体]结合上述实验数据,对相关数据进行汇总统计如下:[/font] [table][tr][td] [align=center][font=楷体]溶液名称[/font][/align] [/td][td] [align=center][font=楷体]质量浓度/电导率[/font][/align] [align=center][font=楷体](mg/L/[/font]μ[font=楷体]S/cm[/font][font=楷体])[/font][/align] [/td][td] [align=center][font=楷体]电导率/电荷物质的量浓度[/font][/align] [align=center][font=楷体]([/font]μ[font=楷体]S/cm/mol/L[/font][font=楷体])[/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]氯化钠溶液[/font][/align] [/td][td] [align=center][font=楷体]0.6527[/font][/align] [/td][td] [align=center][font=楷体]44133[/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]氯化钾溶液[/font][/align] [/td][td] [align=center][font=楷体]0.628[/font][/align] [/td][td] [align=center][font=楷体]59335[/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]硫酸钠[/font][/align] [/td][td] [align=center][font=楷体]0.7851[/font][/align] [/td][td] [align=center][font=楷体]45183[/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]乙酸钠[/font][/align] [/td][td] [align=center][font=楷体]1.1819[/font][/align] [/td][td] [align=center][font=楷体]34691[/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]硫酸铜[/font][/align] [/td][td] [align=center][font=楷体]1.3003[/font][/align] [/td][td] [align=center][font=楷体]30478[/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]磷酸氢二钾[/font][/align] [/td][td] [align=center][font=楷体]1.5814[/font][/align] [/td][td] [align=center][font=楷体]21515[/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]氯化钙[/font][/align] [/td][td] [align=center][font=楷体]0.5989[/font][/align] [/td][td] [align=center][font=楷体]46310[/font][/align] [/td][/tr][/table][align=center][font=楷体]表8:单一溶液实验汇总数据[/font][/align][font=楷体]从上述数据进行讨论得出如下结论:[/font][font='微软雅黑',sans-serif]①[/font][font=楷体]单一溶[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]量浓度/电导率值为变值,且与在用理论值0.5偏差大,因此实际操作中选用0.5倍的电导率值为TDS含量的结果是不准确的,结果偏低;[/font][font=楷体]②单一电导率值/电荷物质的量浓度值也为为变值,因此相同电荷数条件下,不同物质对电导率影响也不相同;[/font][font='微软雅黑',sans-serif]③[/font][font=楷体]通过查阅资料发现,不同物质对电导率影响主要体现在以下3个因素:水化离子半径、离子价数和特殊迁移方式,一般情况下,半径r越大,则运动速度v越小,电导率越小;离子价数越大,则运动速度v越大,电导率越大;H[sup]+[/sup]、OH[sup]-[/sup]是一般离子导电能力5-8倍。 [/font][align=left][b][font=黑体]3.2[/font][font=黑体]多组分盐类与电导率关系[/font][/b][/align][align=left][b][font='Times New Roman',serif] [/font][/b][font=楷体]从上述单一组分盐类的实验可以看出不同种类的盐类对于电导率的影响不同,因此需要通过实验进行探究不同离子浓度与电导率之间的关系。[/font][/align][align=left][b][font=黑体]3.2.1[/font][font=黑体]多组分盐类实验探究[/font][/b][/align][align=left][font=楷体]目前我们装置上使用的助剂主要有磷酸盐类,同时我们的工业用水的体系中存在钠、钾、钙、氯和硫酸根等离子组分,通过采用上述离子配制相应浓度的溶液,并测定对应的电导率值,测定数据汇总如下:[/font][/align] [table][tr][td] [align=center][font=楷体]样品[/font][/align] [/td][td] [align=center][font=楷体][color=black]1[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]2[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]3[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]4[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]5[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]6[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体][color=black]Na[sup]+[/sup]/mg/L[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]46.12[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]92.24[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]60.85[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]94.37[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]81.78[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]140.49[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体][color=black]K[sup]+[/sup]/mg/L[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]78.04[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]97.61[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]19.57[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]39.14[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]97.61[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]39.02[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体][color=black]Ca[sup]2+[/sup]/mg/L[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]39.87[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]79.74[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]59.81[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]119.61[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]19.94[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]39.87[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体][color=black]Cl[sup]-[/sup]/mg/L[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]105.95[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]176.58[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]164.31[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]250.80[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]90.08[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]127.20[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体][color=black]SO[sub]4[/sub][sup]2-[/sup]/mg/L[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]96.35[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]192.70[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]48.17[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]289.04[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]144.52[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]240.87[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体][color=black]PO[sub]4[/sub][sup]3-[/sup]/mg/L[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]95.08[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]142.63[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]47.54[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]95.08[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]142.63[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]47.54[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体]电导率/[/font]μ[font=楷体]S/cm[/font][/align] [/td][td] [align=center][font=楷体]561.4[/font][/align] [/td][td] [align=center][font=楷体]994.0[/font][/align] [/td][td] [align=center][font=楷体]581.0[/font][/align] [/td][td] [align=center][font=楷体]1055.7[/font][/align] [/td][td] [align=center][font=楷体]673.6[/font][/align] [/td][td] [align=center][font=楷体]876.7[/font][/align] [/td][/tr][/table][align=center][font=楷体]表8:多组分溶液实验数据统计[/font][/align][font=楷体] [/font][font=楷体]结合上述数据以多组分物质质量浓度为自变量,结合数学模型,计算出各组分与电导率之间的关系,如下:[/font][align=center][font=等线]κ[/font][font=楷体]=4.285C(Na[sup]+[/sup])+2.079C(K[sup]+[/sup])+4.6988C(Ca[sup]2+[/sup])-0.07697C(Cl[sup]-[/sup])+0.02512C(SO[sub]4[/sub][sup]2-[/sup])+0.2096C(PO[sub]4[/sub][sup]3-[/sup])[/font][/align][align=left][b][font=楷体]3.2.2[/font][font=楷体]实验论证数学模型的可行性[/font][/b][/align][font=黑体] [/font][font=楷体]同上述实验操作,配制4个验证样品,数据如下:[/font] [table][tr][td] [align=center][font=楷体]样品[/font][/align] [/td][td] [align=center][font=楷体][color=black]1[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]2[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]3[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]4[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体][color=black]Na[sup]+[/sup]/mg/L[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]92.24[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]0.00[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]115.29[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]46.12[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体][color=black]K[sup]+[/sup]/mg/L[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]78.28[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]156.56[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]0.00[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]97.85[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体][color=black]Ca[sup]2+[/sup]/mg/L[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]0.00[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]79.74[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]99.68[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]39.87[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体][color=black]Cl[sup]-[/sup]/mg/L[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]0.00[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]141.26[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]176.58[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]70.63[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体][color=black]SO[sub]4[/sub][sup]2-[/sup]/mg/L[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]192.70[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]0.00[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]240.87[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]96.35[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体][color=black]PO[sub]4[/sub][sup]3-[/sup]/mg/L[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]190.17[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]380.34[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]0.00[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]237.71[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体][color=black]理论值[/color][/font][font=楷体]/[/font]μ[font=楷体]S/cm[/font][/align] [/td][td] [align=center][font=楷体][color=black]602.67[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]769.02[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]954.87[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]635.20[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体][color=black]实测值[/color][/font][font=楷体]/[/font]μ[font=楷体]S/cm[/font][/align] [/td][td] [align=center][font=楷体][color=black]632.60[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]831.10[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]985.20[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]592.40[/color][/font][/align] [/td][/tr][tr][td] [align=center][font=楷体][color=black]相对偏差/%[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]-2.42[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]-3.88[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]-1.56[/color][/font][/align] [/td][td] [align=center][font=楷体][color=black]3.49[/color][/font][/align] [/td][/tr][/table][font=楷体] [/font][font=楷体]从上述4组验证数据来看,实验所得的数学模型是可靠的,在相同体系条件下可以用于电导率与TDS之间的转化。[/font][align=left][b][font=黑体]4.[/font][font=黑体]实验[/font][font=黑体]总结[/font][/b][/align][align=left][font=楷体][color=#333333]⑴[/color][/font][font=楷体]单一溶[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]量浓度/电导率值为变值,且与在用理论值0.5偏差大,因此实际操作中选用0.5倍的电导率值为TDS含量的结果是不准确的,结果偏低[/font][font=楷体][color=#333333]。[/color][/font][/align][align=left][font=楷体][color=#333333]⑵[/color][/font][font=楷体]单一电导率值/电荷物质的量浓度值也为为变值,因此相同电荷数条件下,不同物质对电导率影响也不相同,不同物质对电导率影响主要体现在以下3个因素:水化离子半径、离子价数和特殊迁移方式,一般情况下,半径r越大,则运动速度v越小,电导率越小;离子价数越大,则运动速度v越大,电导率越大;H[sup]+[/sup]、OH[sup]-[/sup]是一般离子导电能力5-8倍[/font][font=楷体][color=#333333][back=white]。[/back][/color][/font][/align][align=left][font=楷体][color=#333333]⑶[/color][/font][font=楷体]实验所得的数学模型是可靠的,在相同体系条件下可以用于电导率与TDS之间的转化[/font][font=楷体][color=#333333]。[/color][/font][/align][align=left][b][font=黑体] [/font][/b][/align][align=left][b][font=黑体]5.[/font][font=黑体]参考文献[/font][/b][/align][align=left][font=楷体][color=#333333][1][/color][/font][font=楷体]方志刚,杨岳平,周德佳.海水淡化与舰船淡水保障.国防工业出版社.2016.03.第18页.[/font][/align]
[b]1、原理[/b] 上海誉琰科技有限公司( 网址:yuyantech.com.cn ) HD1000手持式溶解氧分析仪溶解氧的测量是基于克拉克(Clark)电极原理(其他用于电厂的溶氧仪多数采用此原理),传感器由阴极和阳极构成,电极浸在电极腔内的电解液中,由透气膜和电解液薄层将电极与所测介质分开,并允许溶解氧透过。当对传感器两电极施加稳定极化电压时,水中溶解氧透过薄膜,产生稳定的扩散电流,扩散电流的大小与水中溶解氧的浓度呈线性关系。探头输出的电流信号与氧浓度呈线性关系,根据输出的电流信号,即可算出水中溶解氧的浓度。在一定温度t下,探头电流与氧浓度有如下关系:[align=center]I= R * C + I[sub]0 [/sub][/align]I:电流I[sub]0[/sub]:氧浓度为零时的电流,即残余电流(零点校准时得到)C:氧浓度。对溶解氧,单位为mg/L;R:探头系数(与电极面积、膜及温度相关)-即其他仪器的斜率[b]2、氧浓度计算[/b] 仪器出厂前或使用中用户会进行零点校准,取得残余电流I[sub]0[/sub]。使用时,待仪器稳定后,以空气为标样进行校准,由I= R * C + I[sub]0[/sub]可算出当前温度的探头系数R(此即为其他仪器的空气校准),此时的浓度C为校准气温下的饱和溶解氧浓度(25℃时为8.25mg/L),电流I为空气中探头的电流,I[sub]0[/sub]为仪器零点校准得到的残余电流。 测量样品,先得到当前探头输出的电流I。由氧电流I、残余电流I[sub]0[/sub]及探头系数R由下式计算氧浓度: C=(I-I[sub]0[/sub])/R=I/R- I[sub]0[/sub]/R 一般情况下,HD1000仪器所用探头在空气中的电流约为600nA(25℃),探头系数R(探头的灵敏度系数,即信号除以浓度)约75pA/(μg/L),残余电流I[sub]0[/sub]小于50pA(25℃),残余电流相当于的氧浓度(即I[sub]0[/sub]/R)小于1μg/L,也就是如果不扣除残余电流(扣除零点)的话,引起的误差小于1μg/L。对上海誉琰科技有限公司的手持式溶解氧分析仪HD1000-S,探头残余电流I[sub]0[/sub]约为20pA(25℃),残余电流相当于的氧浓度(即I[sub]0[/sub]/R)约0.3-0.4μg/L。 大多数溶解氧分析仪,探头在空气中的电流约为50-60nA(25℃),残余电流小于50pA,以空气中的电流为60nA,残余电流20pA计算,探头系数R(探头的灵敏度系数,即信号除以浓度)小于10pA/(μg/L),其零点为3μg/L。 另外溶氧仪在使用过程中,随着电解液及阳极的消耗,探头的零点及探头系数均会发生变化。因为多数仪器的零点较大,且在变化,所以需要经常校准。在零点为数μg/L的基础上,如果进行低浓度样品(比如1-2μg/L)的测量,显然会带来较大的误差,况且零点还在不断变化。HD1000在零点为零点几μg/L的基础上,进行样品(比如1-2μg/L)的测量,误差会较小。 在实际使用中,由于多数仪器的反应速度较慢,零点校准需要很长时间(探头放于无氧水中电流不断下降,要很长时间后才能达到稳定,这个过程至少要数小时),用户等不及电流稳定或者在电流未下降到稳定值前(比如说半小时,或者1小时)就进行了零点校准,此时得到的零点比真实的零点要高,测量时由于过高的零点扣除,会导致测量结果偏低(偏低的数据更符合标准,显得更好看些)。我们在现场测量中多次见到在线表显示为0.0μg/L的数据,从侧面印证了这一点,因为不正确的零点校准,导致0.0μg/L这种错误的结果。
大家有谁知道,水的电导率和溶解性总固体之间的关系是固定的常数关系吗?
[url=http://www.hach.com.cn/product/ldo][color=#000000]溶氧仪[/color][/url]一般由主机和溶解氧探头组成,目前使用较多的极谱式溶解氧电极探头是由阳极和阴极组成。在使用前需要在探头末端的溶解氧膜中注满电解液,反应时会在两个电极中间产生一股电流差,仪器会根据电流差得出溶液中离子浓度。大气压对溶解氧测试有较大的影响,需要根据现场环境情况手动调节气压补偿功能,可以保证准确度。电极内部的电解液中不能有气泡,否则会影响反应速度和精密度。
如题:1、地表水中电导率没有相关标准,为何还要监测?2、上述的关系是什么?
前两天开会时有同事就问,溶解氧浓度报的是实际值还是标准条件下(25度,标准大气压)的浓度值,目前便携式仪器上给出的读数是校正值,实际值是要通过换算获得的,想知道大家的原始记录和报告上是如何体现这些值的呢?
请教大家一个关于溶解氧的问题:对于密封的水样,温度改变后,溶解氧浓度会改变吗?我做了一个小实验,用做BOD的溶解氧瓶装了三份纯水,使用溶解氧测定仪测初始溶解氧(初始值在7.0附近),然后把瓶子密封好,放入冰箱4小时后取出再测,三份溶解氧都增加了。仪器有温度补偿功能,为什么测出来的结果会增加?
老师你好!有没有国产的水质快速检测仪器,可以同时监测气温、水温 、PH、电导、浊度、溶解氧、气压及部分离子的仪器,进口的也行,但价格低一点的。
我遇到一个问题想问问大家,这个问题是[b]哈希[/b]的SC1000型号的在线溶解氧测量原理是四极式电导池法吗?谢谢亲们解答~
无需稀释的水样,在培养前试样中溶解氧浓度有啥要求么,标准上说试样中溶解氧浓度低则需要曝气15min,那怎么确定这浓度是否低,那这个范围怎么确定
电解质溶液的电导率与电介质的本性、溶剂的性质、温度、以及溶液的浓度有关。在测量的过程中,会对测量结果产生影响的因素有以下几点: 一、温度 电导率与温度具有很大相关性。金属的电导率随着温度的增高而降低。半导体的电导率随着温度的增高而增高。在一段温度值域内,电导率可以被近似为与温度成正比。为了要比较物质在不同温度状况的电导率,必须设定一个共同的参考温度。电导率与温度的相关性,时常可以表达为,电导率对上温度线图的斜率。在精密测量中,为避免温度影响,最好在恒温条件下测量。 二、掺杂程度 固态半导体的掺杂程度会造成电导率很大的变化。增加掺杂程度会造成高电导率。水溶液的电导率高低相依于其内含溶质盐的浓度,或其它会分解为电解质的化学杂质。水样本的电导率是测量水的含盐成分、含离子成分、含杂质成分等等的重要指标。水越纯净,电导率越低(电阻率越高)。水的电导率时常以电导系数来记录 电导系数是水在25°C温度的电导率。 三、各向异性 有些物质会有各向异性(的电导率,必需用3×3矩阵来表达(使用数学术语,第二阶张量,通常是对称的。 四、水的纯度 电导率测定中一般都用水为溶剂,普通的蒸馏水含有CO2、NH3和微量Na+等杂质以及玻璃器皿等的器壁溶解物。当测定电导率较小的稀溶液的电导率值时,必须用更纯的水。25 ℃时,与空气中的CO2相平衡的电导水的电导率为0.8-1.0 mS/cm,这种水可用普通蒸馏水加入少量碱性高锰酸等试剂,经二次蒸馏后得到。也可用离子交换树脂来进一步纯化蒸馏水或电渗析水,使其电导率达0.03-0.06 mS/cm,用于更高精度的电导的测量。 非水溶剂也应经蒸馏纯化,以防止杂质或痕量水影响测量结果。有时,也可用扣除空白(本底)的方法来求得精密电导率值。 五、电极极化 在交流法电导测量中,电极极化问题一般可忽略不计。但当频率太低且被测介质电导较大(大于10-3 S)时,由于电流较大或电流中含有一定的直流分量,仍可产生极化。可通过提高测量电源频率和增大电极面积的方法来消除。直流电导法中电极极化带来的影响不容忽略,但可用四电极法来减小。

降水中电导率的测定 降水,包括降雨,降雪,还有雹,雾,霜等,并不是指的是单独的雨。我们单位降水的监测项目有pH、电导率、钾、钠、钙、镁、铵、硫酸根 、硝酸根、氟、氯和降水量,其中降水量的数据我们采用的是气象部门的。有些地方可以根据所在地情况增测甲酸和乙酸等。其中降水我们使用降水自动采样器采集,我们的型号为SCJ-320型。以前的原创中有此仪器的照片。从每次降雨(雪)开始,要采集全过程(开始到结束)雨(雪)样。如遇连续降雨(雪),当日9时开始至次日9时,连续采集24 h为一次样。 降水采集后先检测电导率和PH,然后经0.45um有机微孔滤膜过滤后检测其它离子。电导率的测定非常简单,但是要注意尽量减小误差。降水一般用聚乙烯烧杯采集。电导率的测定我们用DDS-IIA型电导率仪进行检测,电导率检测需要记录下温度,最后换算成25度下的电导率上报的。具体换算如下:Ks = Kt ,其中Ks 为 25 摄氏度时的电导率,t 为测定电导率时的温度,Kt 为温度为 t 时的电导率,a 为各种离子电导率的平均温度系数,定为0.022。 我一般是检测PH的时候记录下当时的温度,然后检测电导率最后换算。不过我们单位还有一台哈希的HQ30d仪器,可以检测溶解氧,电导率和PH。而且电导率不用换算,非常方便。所以有时我会拿这个仪器进行检测,省去了自己换算。 11月下月我们这降水,我就是用的HQ30d进行检测的,数据正常,一般我们这降水的电导率在10us/cm左右。 http://ng1.17img.cn/bbsfiles/images/2013/12/201312031304_480476_2595817_3.jpg
水质——溶解氧的测定——电化学探头法 ( 水质 溶解氧的测定电化学探头法GB11913—89Water quality-Determination of dissolvedoxygen—Electrochemical probe method本标准等同采用国际标准ISO 5814—1984《水质——溶解氧的测定——电化学探头法》。1 主题内容与适用范围1.1 主题内容本标准规定了采用一种用透气薄膜将水样与电化学电池隔开的电极来测定水中溶解氧的方法。根据所采用探头的不同类型,可测定氧的浓度(mg/L),或氧的饱和百分率(%溶解氧),或者二者皆可测定。本方法可测定水中饱和百分率为0%至100%的溶解氧。可是,大多数仪器能测定高于100%的过饱和值。本方法不但可以用于实验室内的测定,还可用于现场测定和溶解氧的连续监测。本方法适于测定色度高及混浊的水,还适于测定含铁及能与碘作用的物质的水,所有上述物质会干扰用碘量法的测定。一些气体和蒸气象氯。二氧化硫、硫化氢、胺、氨、二氧化碳、溴和碘能扩散并通过薄膜,如果上述物质存在,会影响被测电流而产生干扰。样品中存在其他物质,会因引起薄膜阻塞、薄膜损坏或电极被腐蚀而干扰被测电流。这些物质包括溶剂、油类、硫化物、碳酸盐和藻类。1.2 适用范围本方法适用于天然水、污水和盐水,如果用于测定海水或港湾水这类盐水,应对含盐量进行校对。2 原理本方法所采用的探头由一小室构成,室内有两个金属电极并充有电解质,用选择性薄膜将小室封闭住。实际上水和可溶解物质离子不能透过这层膜,但氧和一定数量的其他气体及亲水性物质可透过这层薄膜。将这种探头浸入水中进行溶解氧测定。因原电池作用或外加电压使电极间产生电位差。由于这种电位差,使金属离子在阳极进入溶液,而透过膜的氧在阴极还原。由此所产生的电流直接与通过膜与电解质液层的氧的传递速度成正比,因而该电流与给定温度下水样中氧的分压成正比。因为膜的渗透性明显地随温度而变化,所以必须进行温度补偿。可采用数学方法(使用计算图表、计算机程序);也可使用调节装置;或者利用在电极回路中安装热敏元件加以补偿。某些仪器还可对不同温度下氧的溶解度的变化进行补偿。3 试剂在分析过程中,仅使用公认的分析纯试剂和蒸馏水或纯度相当的水。3.1 无水亚硫酸钠(Na2SO3)或七水合亚硫酸钠(Na2SO37H2O)。3.2 二价钴盐,例如六水合氯化钴(Ⅱ)(CoCl26H2O)。4 仪器4.1 测量仪器。由以下部件组成4.1.1 测量探头。原电池型(例如铅/银)或极谱型(例如银、金),如果需要,探头上附有温度灵敏补偿装置。4.1.2 仪表,刻度直接显示溶解氧的浓度,和(或)氧的饱和百分率或电流的微安数。4.2 温度计,刻度分度为0.5℃。4.3 气压表刻度分度为10Pa。5 步骤使用测量仪器时,应遵照制造厂的说明书。5.1 测量技术和注意事项5.1.1 不得用手接触摸膜的活性表面。5.1.2 在更换电解质和膜之后,或当膜干燥时,都要使膜湿润,只有在读数稳定后,才能进行校准。需要的时间取决于电解质中溶解氧消耗所需要的时间。5.1.3 当将探头浸入作品中时,应保证没有空气泡截留在膜上。5.1.4 作品接触探头的膜时,应保持一定的流速,以防止与膜接触的瞬间将该部位样品中的溶解氧耗尽,而出现虚假的读数。应保证样品的流速不至使读数发生波动,在这方面要参照仪器制造厂家的说明。5.1.5 对于分散样品,测定容器应能密封以隔绝空气并带有搅拌器(例如电磁搅拌棒)。将样品充满容器至溢流,密闭后进行测量。调整搅拌速度使读数达到平衡后保持稳定,并不得夹带空气。对流动样品,例如河道,要检验是否可保证有足够的流速。如不够,则需在水样中往复移动探头,或者取出分散样品按上段叙述的方法测定。5.2 校准核准步骤在5.2.1至5.2.3中叙述,但必须参照仪器制造厂家的说明书。5.2.1 调节调整仪器的电零点,有些仪器有补偿零点,则不必调整。5.2.2 检验零点检验零点(必要时尚需调整零点)时,可将探头浸入每升已加入1g亚硫酸钠(3.1)和约1mg钴盐(Ⅱ)(3.2)的蒸馏水中。10min内应得到稳定读数。注:新式仪器只需2~3min。5.2.3 接近饱和值的校准在一定温度下,向水中曝气,使水中的氧的含量达到饱和或接近饱和。在这个温度下保持15min再测定溶解氧的浓度,例如用碘量法测定。5.2.4 调整仪器将探头浸没在瓶内,瓶中完全充满按上述步骤制备并标定好的样品。让探头在搅拌的溶液中稳定10min以后。如果必要,调节仪器读数至样品已知的氧浓度。当仪器不能再校准,或仪器响应变得不稳定或较低时(见厂家说明书),应更换电解质或(和)膜。注:①如过去的经验已给出空气饱和样品需要的曝气时间和空气流速,则可查表A1和表A3来代替碘量法测定。②许多仪器可在空气中校准。5.3 测定按照厂家说明书对待测水进行测定。在探头浸入样品后,使探头停留足够的时间,使探头与待测水温一致并使读数稳定。由于所用仪器型号不同及对结果的要求不同,必要时要检验水温和大气压力。6 结果的表示6.1 溶解氧的浓度(mg/L)溶解氧的浓度以每升中氧的毫克数表示,取值到小数点后第一位。在测量样品时的温度不同于校准仪器时的温度,应对仪器读数给予相应校正。有些仪器可以自动进行补偿。该校正考虑到了在两种不同温度下,氧溶解度的差值。例:校准温度 25℃25℃溶解度 8.3mg/L测量时的温度 10℃仪器读数 7mg/L10℃时溶解度 11.3mg/L注:上例中以mg/L表示的Cm和Cc值可根据对应的温度由表A1中“Cs”栏中查得。6.2 作为温度和压力函数的溶解氧浓度表互和表2给出了溶解氧浓度的理论值。表1给出了在标准大气压力下做为温度函数的值。表2则给出作为温度和压力两项函数的值。6.3 盐水样品经过校正的溶解氧浓度氧在水中溶解度随盐含量的增加而减少,在实际应用中,当含盐量(以总盐表示)在35g/L以下时可合理地认为上述关系呈线性。表1给出每1g/L含盐量在校正时减去校正值。即△Cs。所以,当水中含盐量为ng/L时,水中氧的溶解度等于纯水中相应的溶解度减去n△Cs。6.4 以饱和百分率表示的溶解浓度这是以mg/L表示的实际溶解氧浓度,必要时需经过温度校正,除以表A1和表A3给出的理论值而得出的百分率:Cs(测定值)------------×100%Cs(理论值)7 试验报告试验报告包括下列资料:a.参考本国家标准;b.测定结果及其表示方法;c.采样和检测时的水温;d.采样和检测时的大气压力;e.水中含盐量;f. 所用仪器的型号;g.测定期间可能注意到的特殊细节;h.本国家标准中没有规定的或考虑可任选的操作细节。
碘量法测溶解氧的实验中,先在碱性条件下用二价锰将溶解氧以四价锰的碱性氧化物形式固定,然后加酸溶解,四价锰氧化碘离子为碘分子,用淀粉为指示剂滴定。我的问题是:加酸溶解以后,四价锰被碘离子还原成二价,那如果水样中重新溶解了空气中的氧(因为水中浓度很低,溶解扩散应该较快),溶解的氧会不会在酸性条件下把二价锰氧化成四价,而造成误差?感谢先!
电导率是电解质溶液的一个固有特性,它直接反映溶液中相应离子的浓度。同时,水质的电导率值也是表现水质纯净浓度的一个重要指标。溶液的电导率与溶液的性质和其温度密切相关,温度升高电导率值增加,反之,电导率值降低。而电导率的温度系数即温度每变化1℃,电导率的变化量就溶液的性质而有所不同,对大多数离子电导率的温度系数值为+2%℃-1~+3%℃-1。对于H+和OH-离子,电导率温度系数分别为+1.5%℃-1和+1.8%℃-1。对于电导率测量的准确度的仪器要求(一般为±1%或优于±1%)是不容忽视的。因此,要准确地测量溶液的电导率值必须要考虑该溶液的温度系数和进行可靠的温度补偿,或必须在恒温条件下进行。通常情况下约定,所指溶液的电导率是指该液体在25℃时的电导率,当溶液温度不在25℃时其电导率会有一个变量,温度补偿的作用就是为了消除这个变量,将任何温度下溶液的电导率值转换为25℃时的电导率值。其温度补偿原理遵循以下公式:K=K25℃[1+α(t-25)]K25℃=Kt/1+α(t-25)式中Kt:溶液在实际温度下的电导率K25℃:溶液在25℃时的电导率α:溶液电导率的温度系数,不同溶液温度系数不同t:溶液的实际温度从公式中可以看出,对于所有电解质溶液而言,存在着两个变量,一个是α,一个是t。因此为了适应所有性质溶液电导率的准确测量,即要有温度补偿,又要符合被测液电导率的温度系数,即温度系数可按需要设置和调整。国产早期生产的电导率仪既无温度补偿也无温度系数的调节,很难保证测试的准确。后期生产的电导率普通增加了温度补偿的功能,但大多温度系数调节。设计时,以为适应大多普通电解质溶液的温度系数的范围而固定设计为2%。严格地说,它只适于测定电导率温度系数为2%的溶液,而测量电导率温度系数不为2%的溶液时必然会产生误差。温度系数偏离2%越多测试误差越大。
水质中电导率与温度等的关系 在水质检测标准中经常可以看到电导率,TDS,盐度等标准,不少人对他们的定义不是很了解,甚至有认为三者是同一个概念。今天我们就来了解下电导率,TDS,盐度的定义及相关关系。一、电导率:生态学中,电导率是以数字表示的溶液传导电流的能力,电导率的物理意义是表示物质导电的性能。电导率越大则导电性能越强,反之越小。单位以西门子每米(S/m)表示。影响因素:1)温度:电导率与温度具有很大相关性。在一段温度值域内,电导率可以被近似为与温度成正比。为了要比较物质在不同温度状况的电导率,必须设定一个共同的参考温度。2)掺杂程度: 增加掺杂程度会造成高电导率。水溶液的电导率高低相依于其内含溶质盐的浓度,或其它会分解为电解质的化学杂质。水样本的电导率是测量水的含盐成分、含离子成分、含杂质成分等等的重要指标。水越纯净,电导率越低(电阻率越高)。水的电导率时常以电导系数来纪录;电导系数是水在 25°C 温度的电导率。 3)各向异性:有些物质会有异向性(anisotropic) 的电导率,必需用 3 X 3 矩阵来表达(使用数学术语,第二阶张量,通常是对称的) 二、TDS:总溶解固体(英文:Total dissolved solids),又称溶解性固体总量,测量单位为毫克/升(mg/L),它表明1升水中溶有多少毫克溶解性固 体。TDS值越高,表示水中含有的杂质越多。 总溶解固体指水中全部溶质的总量,包括无机物和有机物两者的含量。一般可用电导率值大概了解溶液中的盐份,一般情况下,电导率越高,盐份越高,TDS越 高。在无机物中,除开溶解成离子状的成分外,还可能有呈分子状的无机物。由于天然水中所含的有机物以及呈分子状的无机物一般可以不考虑,所以一般也把含盐量称为总溶解固体。 但是在特定水中TDS并不能有效反映水质的情况。比如电解水,由于电解过的水中HO-等带电离子显著增多,相应的导电量就异常加大。它和电导率往往存在一种相通的关系,有时候TDS也可以用来表示电导率,两者的关系:1TDS=2μS其中μS为电导率的单位。国家标准GB5749-2006《生活饮用水卫生标准》中对饮用自来水的溶解性总固体(TDS)有限量要求:溶解性总固体≤1000mg/L 三、盐度:盐度的定义经历了几个阶段,1)克纽森盐度公式在本世纪初,克纽森(Knudsen)等人建立了盐度定义,当时的盐度定义是指在 1000g海水中,当碳酸盐全部变为氧化物、溴和碘以氯代替,所有的有机物质全部氧化之后所含固体物质的总数。其测量方法是取一定量的海水,加盐酸和氯水,蒸发至干,然后在380℃和480℃的恒温下干燥48h,最后称所剩余固体物质的重量。用上述的称量方法测量海水盐度,操作十分复杂,测一个样品要花费几天的时间,不适用于海洋调查,因此,在实践中都是测定海水的氯度,根据海水的组成恒定性规律,来间接计算盐度,氯度与盐度的关系式(克纽森盐度公式)如下:S‰=0.030+1.8050Cl‰克纽森的盐度公式使用时,用统一的硝酸银滴定法和海洋常用表,在实际工作中显示了极大的优越性,一直使用了70年之久。但是,在长期使用中也发现,克纽森的盐度公式只是一种近似的关系,而且代表性较差;滴定法在船上操作也不方便。于是人们寻求更精确更快速的方法。2)重新定义 盐度与氯度的上述关系式,建立在海水组成恒比规律的基础上,这是不严格的;况且当时所取的水样,多数为波罗的海表层水,难以代表整个大洋水的规律。实际上,关系式中的常数项 0.030,不符合大洋海水盐度变化的实际情况。根据海水的电导率取决于其温度和盐度的性质,通过测定其电导率和温度就可以求得海水的盐度。1950年以后,电导盐度计的研究和发展,使盐度的测定方法得到简化,精密度也提高,比测定氯度后计算盐度的方法,更加准确和方便。因此,联合国教科文组织(UNESCO)、国际海洋考察理事会(ICES)、 海洋研究科学委员会(SCOR)和国际海洋物理科学学会(IAPSO)4个国际组织联合发起,于1962年 5月召开会议,成立了海水状态方程式联合小组。此小组于1963年第二次会议上改名为“海洋用表与标准联合专家小组(JPOTS)”。经过多次讨论和研究,为了保持历史资料的统一性,将盐度公式改为S‰=1.80655Cl‰R.A.考克斯等对采自各大洋和海区的135个水样(深度在100米以内)的氯度值进行了准确的测定,按上述公式换算成盐度,并测定了电导比R15,得到S‰与R15关系的多项式S‰=-0.08996+28.2970R15+12.80832R215-10.67869R315+5.98624R415-1.32311R515式中R15 为一个标准大气压和 15°C条件下海水样品与S=35.000的标准海水电导率的比值。1966年,JPOTS推荐这多项式为海水盐度定义。同年,联合国教科文组织和英国国立海洋研究所出版的《国际海洋用表》,其中的盐度数据,就是采用上述测定电导率后换算成盐度的方法。3) 实用盐度标度 20世纪70年代以后,现场仪器如电导-温度-深度仪(CTD)等的应用,越来越多,而国际海洋用表(1966)中没有包括10°C以下的盐度数据,致使低于10°C的现场测定结果,无法统一。此外,测定了1967~1969年制备的标准海水,还发现用电导法测得的盐度,和从氯度换算得到的不一致,而出现了标准海水作为电导率标准的可靠性问题。因此 JPOTS决定使用标准氯化钾溶液标定标准海水,并推荐1978年实用盐度标度。本来,绝对盐度(SA)为海水中溶质质量和海水质量的比值,但它实际上不能直接测定,故用K15定义海水的实用盐度(S)来表达海洋观测的结果。S=a0+a1K1/215+a2K15+a3K3/215+a4K215+a5K5/215a0=0.0080 a1=-0.1692a2=25.3851 a3=14.0941a4=-7.0261 a5=2.7081Σai=35.0000 2≤S≤42式中K15是在15°C和一个标准大气压的条件下,海水样品电导率和质量比为 32.4356×10-3的氯化钾溶液电导率的比值。当K15准确为1时,S 恰好等于35。实用盐度值为过去盐度值的1000倍,例如,过去盐度值为0.03512(即35.12‰),实用盐度值则为35.12。从定义的实用盐度公式可以看出,氯度被看作是和实用盐度无关的一个独立变量。实用盐度的通用标准仍为标准海水,后者除标有氯度值外,尚标有K15值。 所以从上述文章的描述可以发现,电导率,TDS,盐度不是同一个概念,但是三者之间是有密切的关系的。应用广泛应用于火电、化工化肥、反渗透、养殖、制药、环保、食品和自来水等溶液中电导率值/TDS的连续监测。
1.电导的定义电导(conductance)是物体传导电流的能力。电导率测量仪的测量原理是将两块平行的极板,放到被测溶液中,在极板的两端加上一定的电势(通常为正弦波电压),然后测量极板间流过的电流。根据欧姆定律,电导(G)--电阻(R)的倒数,是由电压和电流表征的。 1 I (amps) G =── =───── R E (volts) 因为溶液中离子的电荷会加速电流的导通,所以溶液的电导与溶液中的离子浓度成比例。但是,某些溶液的电导与离子浓度没有直接的关系。一些高浓度溶液离子的相互作用会改变这种线性关系。2.测量单位电导的基本单位是西门子(S),原来被称为欧姆-1次方。因为电导池的几何形状影响电导值,标准的测量中用单位电导即电导率conductivity(S/cm)来表示,以补偿各种电极尺寸造成的差别。单位电导率(s)简单的说是所测电导率(G)与电导池常数(L/A)的乘积.这里的L为两块极板之间的液柱长度,A为极板的面积。(见右图)C = G x (L/A)如果电导池常数为1 cm-1 ,单位电导率与所测溶液的电导相同。尽管电极的形状各异,每一个电极都可以用相应的理论电导池表示。尽管因为空间的限制我们把电导率具体为:μS或 mS,这一系列的单位应被理解为相应的单位电导率单位:μS/cm 或 mS/cm。1μS/cm = 0.001 mS/cm = 0.000001 S/cm = 1μmho/cm下表列出了三种不同电导池常数的最佳电导率范围:电导池常数 最佳电导率(us/cm) 0.1 0.5 to 400 1.0 10 to 2000 10.0 1000 to 200,0003. 电导仪的校正和电导池的维护 电导仪和电导池在使用前用标准溶液校对。选择一种最接近所测溶液电导率的标准溶液。已经极化的和弄脏的电极应重新镀铂或清洗,以恢复电导池的活性表面。大多数情况下,热水加一些温和的液体清洁剂是一种非常有效的清洁剂。大多数有机物可以很容易的用丙酮清洁,亚氯酸溶液可以去除藻类、细菌或霉菌。不要用研磨剂清理电极。下表列出了一些常用溶液的电导率。溶液 电导率 (电阻率) 纯水 0.055 us/cm 18.2MΩ.cm电厂锅炉水 1.0 us/cm 1 MΩ.cm城市用水 50us/cm 0.02 Ω.cm海水 53 mS/cm 20Ω.cm31.0% HNO3 31.0% 硝酸 865 mS/cm 1Ω.cm4. 电导率的温度补偿 电导率测量是与温度相关的。温度对电导率的影响程度依溶液的不同而不同,可以用下面的公式求得。Gt = Gtcal{1 + α(t-tcal)}其中:Gt = 某一温度(°C)下的电导率Gtcal = 标准温度(°C)下的电导率α = 标准温度(°C)下溶液的温度系数下表列出了常用溶液的α值。要得到其他溶液的α值,只要测量某个温度范围内的电导率,并以温度为纵轴绘出相应的电导率的变化曲线,与标准温度相对应的曲线点为该溶液的α值。溶液(25°C) 浓度 Alpha (α) 盐酸 10 wt% 1.56 氯化钾溶液 10 wt% 1.88 硫酸 50 wt% 1.93 氯化钠溶液 10 wt% 2.14 氢氟酸 1.5 wt% 7.20 硝酸 31 wt% 31.0目前市场上所销售的所有电导仪都可以参照标准温度(通常为25°C)进行调节的或自动温度补偿。大多数固定温度补偿的电导仪的α调节为2%/°C(近似25°C时氯化钠溶液的α)。可调节温度补偿的电导仪可以把α调节到更加接近所测溶液的α。
溶解氧测定仪测定的是氧浓度还是氧分压? 有仪器生产商告诉我,溶氧仪直接测定的是水溶液中氧气的分压,而溶解氧溶度是通过C=H*P换算得到的(H为Henry系数,受溶液性质影响很大)。 又因为“平衡时,氧气在空气和在水中的分压相等,即脱离和进入溶液的氧气分子数相同”,藉此可以理解溶氧仪利用饱和水蒸气法标定时,输入的标准值却是对应温度下水溶液的饱和溶氧值(如20度)。实际上,此时空气中氧气溶度和溶液中氧气溶度差30倍左右。 也就是说,在某一温度下达到平衡时,水中和空气中氧气分压都是相同的,即使是含盐水或污水也一样。而不同条件下产生溶解氧浓度不同的取决于H系数。对于已知盐浓度的,可以进行盐度补偿,通过H的修正准确测量溶解氧溶度。但是对于污水等成分特别复杂的水溶液,H很难修正得到,那么此时是不是就无法准确测量污水的溶解氧值?如果是这样的话,溶氧仪在环保局大量使用的意义又是什么呢?如果知道H值了,自己就能理论计算出溶解氧浓度了,还需要溶氧仪干什么呢? 所以从这点上,我更偏信溶氧仪直接测量的是水中溶解氧的浓度,可是这个观点却一直无法解释溶氧仪的校准方法。被溶氧仪的原理给绕晕了,百思不得其解,只能请各位大侠帮忙了:)
电导率仪是适用于精密测量各种液体介质的仪器设备,主要用来精密测量液体介质的电导率值。电导仪配以相应常数的电极可以精确测量高纯水电导率,广泛应用各领域的科研和生产。 电导率仪的测量原理是将两块平行的极板,放到被测溶液中,在极板的两端加上一定的电势,通常为正弦波电压,然后测量极板间流过的电流。利用电导率仪或总固体溶解量计可以间接得到水的总硬度值。测量电导大小的方法,可用两个电极插入溶液中,以测出两个极间的电阻。电极常数常选用已知电导率的标准氯化钾溶液测定。不同浓度氯化钾溶液的电导率(25℃)列于下表。溶液的电导率与其温度、电极上的极化现象、电极分布电容等因素有关,电导率仪一般都采用了补偿或消除措施。 电导率仪是实验室电导率测量仪表,它除能测定一般液体的电导率外,且能满足测量高纯水的电导率的需要。电导率仪可接自动电子电位差计进行连续记录,是食品厂、饮用水厂办理QS、HACCP认证的必备检验设备。
哪些因素影响了溶解氧仪测量的误差不准? 制约溶解氧仪测量溶解氧不准的因素:有温度、压力和水中溶解的盐,流速。【安徽赛科环保科技有限公司】提供以下资料。原文参考:http://www.saikehb.cn/article-1502.html1. 温度对溶解氧仪测量的影响 由于温度变化,膜的扩散系数和氧的溶解度都将发生变化,直接影响到溶氧电极电流输出,常采用热敏电阻来消除温度的影响。温度上升,扩散系数增加,溶解度反而减小。温度对溶解度系数a 的影响可以根据Henry 定律来估算,温度对膜扩散系数β可以通过阿仑尼乌斯定律来估算。(1)氧的溶解度系数:由于溶解度系数a 不仅受温度的影响,而且受溶液的成分的影响。在相同氧分压下,不同组分的实际氧浓度也可能不同。根据亨利定律可知氧浓度与其分压成正比,对于稀溶液,温度变化溶解度系数a 的变化约为2%/℃。(2)膜的扩散系数:根据阿仑尼乌斯定律,溶解度系数β与温度T 的关系为:C=KPo2·exp(-β/T),其中假定K、Po2 为常数,则可以计算出β在25℃时为2.3%/℃。当溶解度系数a 计算出来后,可通过仪表指示和化验分析值对比计算出膜的扩散系数(这里略去计算过程),膜的扩散系数在25℃时为1.5%/℃。2. 大气压的影响 根据Henry 定律,气体的溶解度与其分压成正比。氧分压与该地区的海拔高度有关,高原地区和平原地区的差可达20%,使用前必须根据当地大气压进行补偿。有些溶解氧仪仪表内部配有气压表,在标定时可自动进行校正;有些溶解氧测定仪仪表未配置气压表,在标定时要根据当地气象站提供的数据进行设置,如果数据有误,将导致较大的测量误差。3. 溶液中含盐量 盐水中的溶解氧明显低于自来水中的溶解氧,为了准确测量,必须考虑含盐量对溶解氧的影响。在温度不变的情况下,盐含量每增加100mg/L,溶解氧降低约1%。如果仪表在标定时使用的溶液的含盐量低,而实际测量的溶液的含盐量高,也会导致误差。在实际使用中必须对测量介质的含盐量进行分析,以便准确测量及正确补偿。4. 样品的流速 氧通过膜扩散比通过样品进行扩散要慢,必须保证电极膜与溶液完全接触。对于流通式检测方式,溶液中的氧会向流通池内扩散,使靠近膜的溶液中的氧损失,产生扩散干扰,影响测量。为了溶解氧仪测量准确,应增加流过膜的溶液的流量来补偿扩散失去的氧,样品的最小流速为0.3m/s。 总结: 由于温度变化对溶解氧仪电极膜的扩散和氧溶解度有较大影响,标定时需较长时间(约10min),以使温补电阻达到平衡;氧分压与该地区的海拔高度有关,仪表在使用前必须根据当地大气压进行补偿;测量溶液的含盐量高时,溶解氧测量仪仪表标定时应使用含盐量相当的溶液;对于流通式测量方式,要求流过电极的最小流速为0.3m/s。 赛科环保提醒注意:由于溶解氧电极信号阻抗较高(约20MΩ),溶解氧电极与转换器之间距离最大为50m;溶解氧电极不用时也应处于工作状态,可接在溶解氧转换器上。久置或重新再生(更换电解液或膜)的电极,在使用前应置于无氧环境极化1~2h。推荐好用的溶氧仪产品:便携式溶氧仪 DOS-118-S, DOG-3128-S型 工业溶解氧仪
电导率EC和总固体溶解量TDS定义:电导率是物质传送电流的能力。它和电阻值相对。测量单位为Siemens/cm(S/cm),此单位的10[sup]-6[/sup]以μS/cm表示,10[sup]-3[/sup]时,以mS/cm表示。水的电导率表 超纯水..... 0.055μS/cm 蒸馏水..... 0.5μS/cm 山泉水..... 1μS/cm 自来水..... 50-800μS/cm 饮用水..... 1055μS/cm 海水..... 56mS/cm 盐水..... 100mS/cm 水溶液的电导率直接和溶解固体量浓度成正比,而且固体量浓度越高,电导率越大。电导率和溶解固体量浓度的关系近似表示为:1.4μS/cm=1ppm或2μS/cm=1ppm(每百万单位CaCO3)其中,1ppm等于1mg/l,为总固体溶量的量测单位。电导率仪以外,TDS仪器将电导率值自动换算成ppm值,并提供总固体溶解浓度的直接测量值溶液的电导率大小决定分子的运动,因为温度影响分子的运动,所以要做准确的测量,必须考虑温度。因此,一般为比较测量结果,标准温度定为20℃或25℃。为了修正温度的影响使用温度补偿系数β表示。单位是%/℃,它随测量溶液的不同而改变,一般为β=2%/℃
空气中的分子态氧溶解在水中称为溶解氧。水中的溶解氧的含量与空气中氧的分压、水的温度都有密切关系。在自然情况下,空气中的含氧量变动不大,故水温是主要的因素,水温愈低,水中溶解氧的含量愈高。溶解于水中的分子态氧称为溶解氧,通常记作DO,用每升水里氧气的毫克数表示。水中溶解氧的多少是衡量水体自净能力的一个指标。溶解氧测定的方法有碘量法和膜电极法两种:1、碘量法。碘量法是氧化还原滴定法中,应用比较广泛的一种方法。这是因为电对I2-I-的标准电位既不高,也不低,碘可做为氧化剂而被中强的还原剂(如Sn2+,H2S)等所还原;碘离子也可做为还原剂而被中强的或强的氧化剂(如H2SO4,IO3-,Cr2O72-,MnO4-等)所氧化。2、溶解氧分析仪测量原理氧在水中的溶解度取决于温度、压力和水中溶解的盐。溶解氧分析仪传感部分是由金电极(阴极)和银电极(阳极)及氯化钾或氢氧化钾电解液组成,氧通过膜扩散进入电解液与金电极和银电极构成测量回路。当给溶解氧分析仪电极加上0.6~ 0.8V 的极化电压时,氧通过膜扩散,阴极释放电子,阳极接受电子,产生电流,整个反应过程为:阳极 Ag+Cl→AgCl+2e- 阴极 O2+2H2O+4e→4OH- 根据法拉第定律:流过溶解氧分析仪电极的电流和氧分压成正比,在温度不变的情况下电流和氧浓度之间呈线性关系。1、溶解氧测定仪各位如何维护http://bbs.instrument.com.cn/shtml/20150701/5857289/2、溶解氧测定仪探头应该放多深?http://bbs.instrument.com.cn/shtml/20150701/5857275/3、溶解氧测定仪影响的因素有哪些?http://bbs.instrument.com.cn/shtml/20150701/5857269/4、溶解氧测定仪准确吗?http://bbs.instrument.com.cn/shtml/20150701/5857248/5、昨天去采样测溶解氧的问题http://bbs.instrument.com.cn/shtml/20150708/5866974/目前我接触到的是两种探头的电极法一种是膜电极 比如YSI550A一种是荧光法 比如哈希HQ30D如果说的不对请批评指正。其他现场溶解氧测定还有什么问题还请大家畅所欲言。
在污水处理过程中,通过增加污水中的氧含量使污染物通过活化泥浆被分解出来,达到污水净化的目的,在线测量氧含量有助于确定最佳的净化方法和最经济的曝气池配置。在生物发酵过程中氧含量的测量数据可对工艺过程进行指导,如判断发酵过程的临界氧浓度、发酵罐的供氧能力以及菌体的活性和菌体的生长量等,并根据发酵时的供氧和需氧变化来指导补料操作。 一 溶解氧分析仪测量原理氧在水中的溶解度取决于温度、压力和水中溶解的盐。溶解氧分析仪传感部分是由金电极(阴极)和银电极(阳极)及氯化钾或氢氧化钾电解液组成,氧通过膜扩散进入电解液与金电极和银电极构成测量回路。当给溶解氧分析仪电极加上0.6~0.8V 的极化电压时,氧通过膜扩散,阴极释放电子,阳极接受电子,产生电流,整个反应过程为:阳极 Ag+Cl→AgCl+2e-阴极 O2+2H2O+4e→4OH-根据法拉第定律:流过溶解氧分析仪电极的电流和氧分压成正比,在温度不变的情况下电流和氧浓度之间呈线性关系。二 溶解氧含量的表示方法溶解氧含量有3 种不同的表示方法:氧分压(mmHg);百分饱和度(%);氧浓度(mg/L 或10-6),这3 种方法本质上没什么不同。(1)分压表示法:氧分压表示法是最基本和最本质的表示法。根据Henry 定律可得,P=(Po2+P H2O )×0.209,其中,P 为总压;Po2 为氧分压(mmHg);P H2O为水蒸气分压;0.209 为空气中氧的含量。(2)百分饱和度表示法:由于曝气发酵十分复杂,氧分压不能计算得到,在此情况下用百分饱和度的表示法是最合适的。例如将标定时溶解氧定为100%,零氧时为0%,则反应过程中的溶解氧含量即为标定时的百分数。(3)氧浓度表示法:根据Henry 定律可知氧浓度与其分压成正比,即:C=Po2×a,其中C 为氧浓度(mg/L);Po2 为氧分压(mmHg);a 为溶解度系数(mg/mmHgL)。溶解度系数a 不仅与温度有关,还与溶液的成分有关。对于温度恒定的水溶液,a为常数,则可测量氧的浓度。氧浓度表示法在发酵工业中不常用,但在污水处理、生活饮用水等过程中都用氧浓度来表示。三 影响溶解氧测量的因素氧的溶解度取决于温度、压力和水中溶解的盐,另外氧通过溶液扩散比通过膜扩散快,如流速太慢会产生干扰。1. 温度的影响由于温度变化,膜的扩散系数和氧的溶解度都将发生变化,直接影响到溶氧电极电流输出,常采用热敏电阻来消除温度的影响。温度上升,扩散系数增加,溶解度反而减小。温度对溶解度系数a 的影响可以根据Henry 定律来估算,温度对膜扩散系数β可以通过阿仑尼乌斯定律来估算。(1)氧的溶解度系数:由于溶解度系数a 不仅受温度的影响,而且受溶液的成分的影响。在相同氧分压下,不同组分的实际氧浓度也可能不同。根据亨利定律可知氧浓度与其分压成正比,对于稀溶液,温度变化溶解度系数a 的变化约为2%/℃。(2)膜的扩散系数:根据阿仑尼乌斯定律,溶解度系数β与温度T 的关系为:C=KPo2exp(-β/T),其中假定K、Po2 为常数,则可以计算出β在25℃时为2.3%/℃。当溶解度系数a 计算出来后,可通过仪表指示和化验分析值对比计算出膜的扩散系数(这里略去计算过程),膜的扩散系数在25℃时为1.5%/℃。2. 大气压的影响根据Henry 定律,气体的溶解度与其分压成正比。氧分压与该地区的海拔高度有关,高原地区和平原地区的差可达20%,使用前必须根据当地大气压进行补偿。有些仪表内部配有气压表,在标定时可自动进行校正;有些仪表未配置气压表,在标定时要根据当地气象站提供的数据进行设置,如果数据有误,将导致较大的测量误差。3. 溶液中含盐量盐水中的溶解氧明显低于自来水中的溶解氧,为了准确测量,必须考虑含盐量对溶解氧的影响。在温度不变的情况下,盐含量每增加100mg/L,溶解氧降低约1%。如果仪表在标定时使用的溶液的含盐量低,而实际测量的溶液的含盐量高,也会导致误差。在实际使用中必须对测量介质的含盐量进行分析,以便准确测量及正确补偿。4. 样品的流速氧通过膜扩散比通过样品进行扩散要慢,必须保证电极膜与溶液完全接触。对于流通式检测方式,溶液中的氧会向流通池内扩散,使靠近膜的溶液中的氧损失,产生扩散干扰,影响测量。为了测量准确,应增加流过膜的溶液的流量来补偿扩散失去的氧,样品的最小流速为0.3m/s。四 注意的问题对溶解氧分析仪来说,只要选型、设置、维护得当,一般均能满足工艺的测量要求。溶解氧分析仪的使用不好的主要问题出在:使用维护不正确;电极内部泄露造成温度补偿不正常;电极输入阻抗降低等。1. 日常维护仪表的日常维护主要包括定期对电极进行清洗、校验、再生。(1)1~2 周应清洗一次电极,如果膜片上有污染物,会引起测量误差。清洗时应小心,注意不要损坏膜片。将电极放入清水中涮洗,如污物不能洗去,用软布或棉布小心擦洗。(2)2~3 月应重新校验一次零点和量程。(3)电极的再生大约1 年左右进行一次。当测量范围调整不过来,就需要对溶解氧电极再生。电极再生包括更换内部电解液、更换膜片、清洗银电极。如果观察银电极有氧化现象,可用细砂纸抛光。(4)在使用中如发现电极泄露,就必须更换电解液。2. 仪表标定仪表的标定方法一般可采用标准液标定或现场取样标定。(1)标准溶液标定法:标准溶液标定一般采用两点标定,即零点标定和量程标定。零点标定溶液可采用2%的Na2SO3 溶液。量程标定溶液可根据仪表测量量程选择4M 的KCl 溶液(2mg/L);50%的甲醇溶液(21.9mg/L)。(2)现场取样标定法(Winkler 法):在实际使用中,多采用Winkler 方法对溶解氧分析仪进行现场标定。使用该方法时存在两种情况:取样时仪表读数为M1,化验分析值为A,对仪表进行标定时仪表读数仍为M1,这时只须调整仪表读数等于A 即可;取样时仪表读数为M1,化验分析值为A,对仪表进行标定时仪表读数改变为M2,这时就不能将调整仪表读数等于A,而应将仪表读数调整为1 MA ×M2。3. 使用中应注意的问题使用中应注意以下问题:由于溶解氧电极信号阻抗较高(约20MΩ),溶解氧电极与转换器之间距离最大为50m;溶解氧电极不用时也应处于工作状态,可接在溶解氧转换器上。久置或重新再生(更换电解液或膜)的电极,在使用前应置于无氧环境极化1~2h;由于温度变化对电极膜的扩散和氧溶解度有较大影响,标定时需较长时间(约10min),以使温补电阻达到平衡;氧分压与该地区的海拔高度有关,仪表在使用前必须根据当地大气压进行补偿;测量溶液的含盐量高时,仪表标定时应使用含盐量相当的溶液;对于流通式测量方式,要求流过电极的最小流速为0.3m/s。此文章由 http://www.3017.com.cn 转发文章连接: http://www.31517.cn/jishuwenzhang/wenzhang.asp?wenzhang_id=150&ta=3&tb=4 我站诚邀友情连接:QQ 84424693
核心提示: 在污水处理过程中,通过增加污水中的氧含量使污染物通过活化泥浆被分解出来,达到污水净化的目的,在线测量氧含量有助于确定 在污水处理过程中,通过增加污水中的氧含量使污染物通过活化泥浆被分解出来,达到污水净化的目的,在线测量氧含量有助于确定最佳的净化方法和最经济的曝气池配置。在生物发酵过程中氧含量的测量数据可对工艺过程进行指导,如判断发酵过程的临界氧浓度、发酵罐的供氧能力以及菌体的活性和菌体的生长量等,并根据发酵时的供氧和需氧变化来指导补料操作。一、溶解氧分析仪测量原理氧在水中的溶解度取决于温度、压力和水中溶解的盐。溶解氧分析仪传感部分是由金电极(阴极)和银电极(阳极)及氯化钾或氢氧化钾电解液组成,氧通过膜扩散进入电解液与金电极和银电极构成测量回路。当给溶解氧分析仪电极加上0.6~0.8V的极化电压时,氧通过膜扩散,阴极释放电子,阳极接受电子,产生电流,整个反应过程为:阳极Ag Cl→AgCl 2e-阴极O2 2H2O 4e→4OH-根据法拉第定律:流过溶解氧分析仪电极的电流和氧分压成正比,在温度不变的情况下电流和氧浓度之间呈线性关系。二、溶解氧含量的表示方法溶解氧含量有3种不同的表示方法:氧分压(mmHg);百分饱和度(%);氧浓度(mg/L或10-6),这3种方法本质上没什么不同。(1)分压表示法:氧分压表示法是最基本和最本质的表示法。根据Henry定律可得,P=(Po2 PH2O)×0.209,其中,P为总压;Po2为氧分压(mmHg);PH2O为水蒸气分压;0.209为空气中氧的含量。(2)百分饱和度表示法:由于曝气发酵十分复杂,氧分压不能计算得到,在此情况下用百分饱和度的表示法是最合适的。例如将标定时溶解氧定为100%,零氧时为0%,则反应过程中的溶解氧含量即为标定时的百分数。(3)氧浓度表示法:根据Henry定律可知氧浓度与其分压成正比,即:C=Po2×a,其中C为氧浓度(mg/L);Po2为氧分压(mmHg);a为溶解度系数(mg/mmHg·L)。溶解度系数a不仅与温度有关,还与溶液的成分有关。对于温度恒定的水溶液,a为常数,则可测量氧的浓度。氧浓度表示法在发酵工业中不常用,但在污水处理、生活饮用水等过程中都用氧浓度来表示。三、影响溶解氧测量的因素氧的溶解度取决于温度、压力和水中溶解的盐,另外氧通过溶液扩散比通过膜扩散快,如流速太慢会产生干扰。1.温度的影响由于温度变化,膜的扩散系数和氧的溶解度都将发生变化,直接影响到溶氧电极电流输出,常采用热敏电阻来消除温度的影响。温度上升,扩散系数增加,溶解度反而减小。温度对溶解度系数a的影响可以根据Henry定律来估算,温度对膜扩散系数β可以通过阿仑尼乌斯定律来估算。(1)氧的溶解度系数:由于溶解度系数a不仅受温度的影响,而且受溶液的成分的影响。在相同氧分压下,不同组分的实际氧浓度也可能不同。根据亨利定律可知氧浓度与其分压成正比,对于稀溶液,温度变化溶解度系数a的变化约为2%/℃。(2)膜的扩散系数:根据阿仑尼乌斯定律,溶解度系数β与温度T的关系为:C=KPo2·exp(-β/T),其中假定K、Po2为常数,则可以计算出β在25℃时为2.3%/℃。当溶解度系数a计算出来后,可通过仪表指示和化验分析值对比计算出膜的扩散系数(这里略去计算过程),膜的扩散系数在25℃时为1.5%/℃。2.大气压的影响根据Henry定律,气体的溶解度与其分压成正比。氧分压与该地区的海拔高度有关,高原地区和平原地区的差可达20%,使用前必须根据当地大气压进行补偿。有些仪表内部配有气压表,在标定时可自动进行校正;有些仪表未配置气压表,在标定时要根据当地气象站提供的数据进行设置,如果数据有误,将导致较大的测量误差。3.溶液中含盐量盐水中的溶解氧明显低于自来水中的溶解氧,为了准确测量,必须考虑含盐量对溶解氧的影响。在温度不变的情况下,盐含量每增加100mg/L,溶解氧降低约1%。如果仪表在标定时使用的溶液的含盐量低,而实际测量的溶液的含盐量高,也会导致误差。在实际使用中必须对测量介质的含盐量进行分析,以便准确测量及正确补偿。4.样品的流速氧通过膜扩散比通过样品进行扩散要慢,必须保证电极膜与溶液完全接触。对于流通式检测方式,溶液中的氧会向流通池内扩散,使靠近膜的溶液中的氧损失,产生扩散干扰,影响测量。为了测量准确,应增加流过膜的溶液的流量来补偿扩散失去的氧,样品的最小流速为0.3m/s。四注意的问题对溶解氧分析仪来说,只要选型、设置、维护得当,一般均能满足工艺的测量要求。溶解氧分析仪的使用不好的主要问题出在:使用维护不正确;电极内部泄露造成温度补偿不正常;电极输入阻抗降低等。1.日常维护仪表的日常维护主要包括定期对电极进行清洗、校验、再生。(1)1~2周应清洗一次电极,如果膜片上有污染物,会引起测量误差。清洗时应小心,注意不要损坏膜片。将电极放入清水中涮洗,如污物不能洗去,用软布或棉布小心擦洗。(2)2~3月应重新校验一次零点和量程。(3)电极的再生大约1年左右进行一次。当测量范围调整不过来,就需要对溶解氧电极再生。电极再生包括更换内部电解液、更换膜片、清洗银电极。如果观察银电极有氧化现象,可用细砂纸抛光。(4)在使用中如发现电极泄露,就必须更换电解液。2.仪表标定仪表的标定方法一般可采用标准液标定或现场取样标定。(1)标准溶液标定法:标准溶液标定一般采用两点标定,即零点标定和量程标定。零点标定溶液可采用2%的Na2SO3溶液。量程标定溶液可根据仪表测量量程选择4M的KCl溶液(2mg/L);50%的甲醇溶液(21.9mg/L)。(2)现场取样标定法(Winkler法):在实际使用中,多采用Winkler方法对溶解氧分析仪进行现场标定。使用该方法时存在两种情况:取样时仪表读数为M1,化验分析值为A,对仪表进行标定时仪表读数仍为M1,这时只须调整仪表读数等于A即可;取样时仪表读数为M1,化验分析值为A,对仪表进行标定时仪表读数改变为M2,这时就不能将调整仪表读数等于A,而应将仪表读数调整为1MA×M2。3.使用中应注意的问题使用中应注意以下问题:由于溶解氧电极信号阻抗较高(约20MΩ),溶解氧电极与转换器之间距离最大为50m;溶解氧电极不用时也应处于工作状态,可接在溶解氧转换器上。久置或重新再生(更换电解液或膜)的电极,在使用前应置于无氧环境极化1~2h;由于温度变化对电极膜的扩散和氧溶解度有较大影响,标定时需较长时间(约10min),以使温补电阻达到平衡;氧分压与该地区的海拔高度有关,仪表在使用前必须根据当地大气压进行补偿;测量溶液的含盐量高时,仪表标定时应使用含盐量相当的溶液;对于流通式测量方式,要求流过电极的最小流速为0.3m/s。