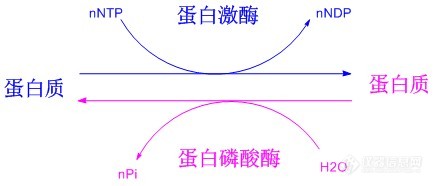
生命活动与蛋白质的动态变化密切相关, 很多情况下某些蛋白质是通过各种翻译后修饰来完成或改变其功能。在数量众多的蛋白质翻译后修饰中,蛋白质磷酸化修饰无疑是最重要的一类,它是指通过蛋白激酶(Protein kinase,PK)介导的酶促反应把磷酸基团从一个化合物转移到另一个化合物上的过程(Figure 1所示),是生物体内存在的一种普遍的调节方式。现今发现的所有人类蛋白质中超过30%可被磷酸化修饰,这一修饰在细胞信号的传递过程中占有极其重要的地位,与生命活动的许多过程都密切相关,对此的研究已经成为蛋白质科学的热点之一。 http://img.dxycdn.com/trademd/upload/userfiles/image/2012/09/1346918444_small.jpg磷酸化多肽(主要指肽链中的酪氨酸、丝氨酸和苏氨酸残基的侧链羟基被磷酸化生成酸式磷酸酯的修饰多肽)是研究蛋白质磷酸化过程的必不可少的工具,它可作为磷酸酶模型底物,或作为可产生抗磷酸化蛋白抗体的抗原,也可以在确定磷酸化蛋白的物理参数时作为参考化合物等。因此磷酸化多肽的合成在过去的几年中吸引了相当大的兴趣,目前已确定了较为成熟的合成路线,使磷酸化多肽的合成趋于常规。目前磷酸化多肽的合成主要有两个策略:后磷酸化法(Global phosphorylation)和单体法(Building block approach),如Figure 2所示。前者是在多肽序列合成结束后再在固相载体上对丝氨酸、苏氨酸或酪氨酸的侧链羟基进行磷酸化,可以在同一次合成中同时得到带有和不带有磷酸化位点的多肽;而后者则将适当保护的磷酸化氨基酸直接引入到多肽序列中,操作较前者更为简单,现已成为磷酸化多肽合成的首选策略。在采用单体法构建磷酸化多肽时,目前广泛采用的原料为侧链单苄基保护的氨基酸:Fmoc-AA(PO(OBzl)OH)-OH (AA = Ser, Thr or Tyr)。这类保护的磷酸化位点由于侧链磷酸化基团的离子化而产生较大的位阻效应,并且磷酸化位点的引入往往能促进肽链二级结构的形成,故而磷酸化位点及其后的氨基酸的引入会比较困难。这些问题在合成含有多个磷酸化位点的多肽时将会变得尤为严重,往往会使最终产物的组成非常复杂,难以进行纯化,甚至直接导致合成的失败。http://img.dxycdn.com/trademd/upload/userfiles/image/2012/09/1346918477_small.jpg一般来讲,增加投料量和延长反应时间都能促使连接反应趋于完全,但增加投料量无疑会提高合成成本,对于较昂贵的带有保护的磷酸化氨基酸更是这样,而延长反应时间则可能增加其它副反应发生的风险,故而在合成磷酸化多肽时,需要对氨基酸投料量、反应方法以及反应时长等进行优化调整以期达到更理想、更经济的合成效果。我们有针对性地对磷酸化多肽合成条件进行了探索和调整,采用最终的优化条件成功合成了含有多达六个磷酸化丝氨酸残基的多肽:FAM-Ahx-X(pS)XX(pS)X(pS)X(pS)XX(pS)X(pS)-NH2(客户肽,详细序列未给出;其氨基端标记FAM以进行荧光检测),经过RP-HPLC纯化后最终纯品的纯度高达95%(见Figure 3)。http://img.dxycdn.com/trademd/upload/userfiles/image/2012/09/1346918493_small.jpg参考文献:1. P. Cohen, “The Role of Protein Phosphorylation in Neural and Hormonal Control of Cellular Activity”, Nature, 1982, 296 (5858): 613-620.2. From: http://en.wikipedia.org/wiki/Protein_kinase.3. L. A. Pinna, A. Donella-Deana, “Phosphorylated Synthetic Peptides as Tools for Studying Protein Phosphatases”, Biochim. Biophys. Acta., 1994, 1222 (3): 415-431.4. W. C. Chan, P. D. White, “Fmoc Solid Phase Peptide Synthesis-A Practical Approach” (2000), Oxford University Press.
磷酸化的Ser、Tyr和Thr修饰的多肽:我们国肽生物提供单磷酸化和多磷酸化多肽服务,目前我们已经能够提供四个磷酸化位点修饰的多肽。[img=,434,186]https://ng1.17img.cn/bbsfiles/images/2019/04/201904191649355554_2764_3531468_3.jpg!w434x186.jpg[/img][img=,486,498]https://ng1.17img.cn/bbsfiles/images/2019/04/201904191649358877_2957_3531468_3.jpg!w486x498.jpg[/img]我们主要提供:多肽定制、磷酸肽、生物素标记肽、荧光标记肽、同位素标记肽、人工胰岛素、药物肽、多肽合成、目录肽、偶联蛋白、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、RGD环肽等。合肥国肽生物官网:http://www.bankpeptide.com欢迎咨询服务热线:17718122172;17718122684;17730030476;17718122397
磷酸化蛋白质及多肽相关研究的技术进展 摘要磷酸化修饰是一种重要的蛋白质化学修饰,对蛋白质功能的完成或改变起到重要作用。该领域的研究存在很多技术难点,对该领域研究形成了挑战。近年来相关技术有了很多突破,磷酸化研究也取得了很多新的成就。文章将从磷酸化蛋白的检出、磷酸化蛋白质和肽段的富集、生物质谱技术的改进以及磷酸化蛋白和多肽的定量与比较几个方面介绍该研究领域的技术进展。关键词磷酸化蛋白磷酸化肽生物质谱定量分析生命活动与蛋白质的动态变化密切 摘要 磷酸化修饰是一种重要的蛋白质化学修饰, 对蛋白质功能的完成或改变起到重要作用。该领域的研究存在很多技术难点, 对该领域研究形成了挑战。近年来相关技术有了很多突破, 磷酸化研究也取得了很多新的成就。文章将从磷酸化蛋白的检出、磷酸化蛋白质和肽段的富集、生物质谱技术的改进以及磷酸化蛋白和多肽的定量与比较几个方面介绍该研究领域的技术进展。 关键词 磷酸化蛋白 磷酸化肽 生物质谱 定量分析
[font=宋体]磷酸化抗体是一种特殊的抗体,能够识别并结合到已经被磷酸化的蛋白质。磷酸化是一种重要的蛋白质修饰方式,通过将磷酸基团结合到特定的氨基酸残基上,可以改变蛋白质的结构和功能。在许多生物学过程中,磷酸化都扮演着重要的角色,因此磷酸化抗体成为了研究生物学和生物化学的重要工具。[/font][font=宋体] [/font][font=宋体]蛋白质磷酸化是指蛋白在激酶作用下在特定氨基酸位点(最常见的是丝氨酸、苏氨酸、酪氨酸残基)发生磷酸化的过程。蛋白磷酸化是极其重要的翻译后修饰,其动态调控是信号转导中不可或缺的一环,调控着细胞生长、分化、代谢、凋亡等等过程。[/font][font=宋体] [/font][font=宋体]磷酸化抗体主要是针对磷酸化位点制备的,可以特异性识别磷酸化氨基酸位点,对磷酸化蛋白进行定性、定量分析,检测蛋白受刺激后磷酸化水平变化情况。[/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州可以为客户提供一系列具有高特异性(经内源性、磷酸化特异性等多方面验证)、高灵敏度([/font][font=Calibri]1:200000[/font][font=宋体]稀释度)特点的磷酸化抗体,满足[/font][font=Calibri]WB[/font][font=宋体]、[/font][font=Calibri]IHC[/font][font=宋体]等应用。同时我们还可以为客户提供定制化的磷酸化抗体定制服务。[/font][/font][font=宋体] [/font][font=宋体][b]义翘神州磷酸化抗体服务优势:[/b][/font][font=宋体] [/font][font=宋体][font=宋体]①专业高效的多肽设计软件及高效偶联方法,保证多肽免疫成功率[/font][font=Calibri]95%[/font][font=宋体]以上。[/font][/font][font=宋体]②多种纯化策略,正负筛选平台,确保得到高特异识别指定磷酸化位点的抗体。[/font][font=宋体]③竞争性的价格[/font][font=宋体] [/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供多种生物的制备服务,包括磷酸化兔多克隆抗体制备服务、磷酸化鼠单克隆抗体制备服务、磷酸化兔单克隆抗体制备服务[/font][font=宋体]……详情可以关注[/font][font=Calibri]https://cn.sinobiological.com/services/phospho-specific-antibody-service[/font][/font][font=宋体] [/font][font=宋体]总之,义翘神州[url=https://cn.sinobiological.com/services/phospho-specific-antibody-service][b]磷酸化抗体定制服务[/b][/url]能够满足您的个性化需求,帮助您在研究领域获得更多的突破。我们致力于为您提供高质量、高效率的抗体定制服务,助力您的科研事业更上一层楼。[/font]
合肥国肽生物科技有限公司(简称:国肽生物TM)成立于2014年,是一家专业从事多肽产品的研发、生产和销售以及多肽技术转让的高新技术企业。BP公司成立之初,便成功收购了国内几家多肽、抗体公司,是目前国内的专业多肽合成、抗体制备、蛋白表达的规模型生产企业。国肽生物专长于荧光标记肽、同位素标记肽、人工胰岛素、药物肽、化妆品肽、长肽困难肽等产品的合成与研发,致力于学术水平的科研提升,搭建学术交流平台,促进前沿、专业的学术知识推广,推动多肽在生物医学材料等领域的研究与应用。公司产品广泛应用于药物研发,抗体的制备(包括单抗与双抗),荧光分子探针的构建以及细胞透膜研究、活体成像、新型材料研发和质谱分析等研究领域国肽生物按照客户定制要求供应高品质普通多肽。我们拥有成熟的多肽合成纯化方法,利用SPPS方法和液相合成方法为客户提供高品质多肽。我们的服务特点是:1. 纯度:我们提供粗品肽和纯度纯度为70%,75%,80%,85%,90%,95%,98%,99%的纯品多肽。2.脱盐和转盐:根据客户要求,我们可以对多肽进行脱TFA盐处理,也可以转为醋酸盐。3.交货期限:30个氨基酸之内,一般2-3周,最快1-2周。4.质量控制:每条多肽都免费提供合格的HPLC,MS和COA文件。5.售后服务:1-2周内可以提出异议,我们免费复测,不合格免费退货,1-3个月内使用不合格可以免费提供复测,样品免费保存3个月。国肽生物根据客户要求,供应各种修饰型多肽。1.磷酸化的Ser、Tyr和Thr修饰的多肽:我们提供单磷酸化和多磷酸化多肽服务,目前我们已经能够提供四个磷酸化位点修饰的多肽。2.5(6)-FAM,FITC,CY5,RhodamineB,PNA,EDNAS/dabcyl等荧光标记修饰的多肽:荧光标记修饰多肽技术是我们国肽生物的代表性多肽合成技术,我们的这项技术已经相当成熟。3.生物素Biotin,Lys(Biotin)修饰的多肽:生物素是维生素B2的组成部分,Biotin,Lys(Biotin)修饰的多肽也是客户经常定制的多肽。我们提供生物素修饰的多肽已经有将近100%的成功率。4.含有一对或多对二硫键修饰的多肽:二硫键在蛋白质的结构稳定中起到重要作用,目前我们已经能够为客户提供四对二硫键修饰的多肽。5.含有同位素C13,N15修饰的多肽:同位素标记的多肽主要应用于医学和生物学领域,通常价格较高,为了满足客户需要,我们接受微克级的同位素多肽定制。6.含有特殊氨基酸修饰的多肽:例如,D型氨基酸,氨基酸衍生物,脂肪族羧酸等等,都在我们接受的定制范围内。国肽生物提供150个氨基酸以内的长肽合成服务。多肽合成过程中,肽链过长时,经常会出现缺残基,氨基酸缩合困难等情况,基于这些现象,我们开发了三种有效提高反应成功率的方案:1. 微波合成法:对于合成过程中出现的一些难以缩合的氨基酸,我们采用微波法进行合成,该方法效果显著,并且大大缩短了反应时间。2. 片段合成法:当某些多肽用常规合成方法合成困难,我们也会采用将多肽中某一段的某几个氨基酸缩合之后作为一个整体缩合到肽链上去,这种方法也能够解决许多合成中存在的问题。3.酰肼合成法:酰肼法合成多肽的方法是将固相合成的 N末端Cys 多肽和 C末端多肽酰肼之间的化学选择性反应形成酰胺键而实现多肽的连接,该方法根据肽链中Cys的位置,将整条肽链分成多条序列分别合成,最终经过液相缩合反应得到目标肽,显著地提高了最终产物纯度,广泛适用于含有Cys的长链多肽的合成。国肽生物拥有成熟的长肽合成工艺,能够根据客户定制的多肽序列,快速有效地设计合成方案并迅速开始合成,更快更好的为客户提供所需的服务是我们不变的坚持。详情请咨询合肥国肽生物www.bankpeptide.com
请问从sigma购买货号为C6780 的α-casein(α-酪蛋白)中,磷酸化的比例是多少?希望大家可以提供帮助,谢谢
请问从sigma购买货号为C6780 的α-casein(α-酪蛋白)中,磷酸化的比例是多少?希望大家可以提供帮助,谢谢
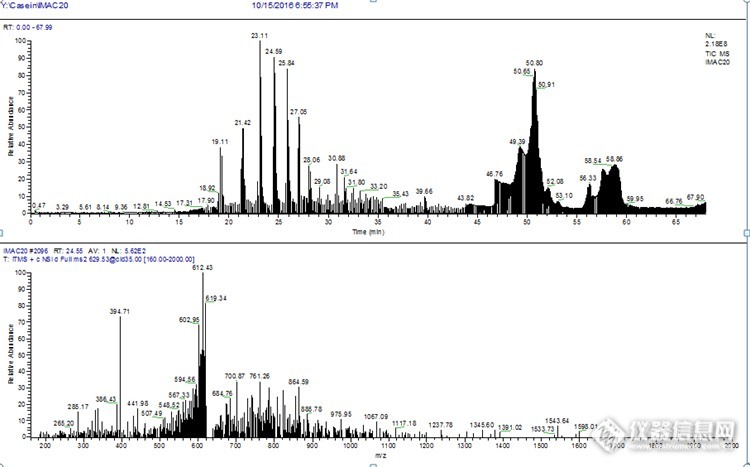
各位老师:求助哪位老师有IMAC富集磷酸化肽段的经验?磷酸化肽段采用IMAC富集后,nano-LC-orbitrap检测后出现奇怪峰,从19.11到28.06分钟出现的峰都不是蛋白及肽段。哪位老师有经验知道这些峰有可能是什么,并且经数据库检测后只获得了7个磷酸化肽段。图见附件谢谢各位老师,上图是IMAC以后的图,下图是IMAC以前,in-gel digesition之后的

【专家讲座】:第三讲:蛋白质磷酸化研究(Antibody base protein phosphorylatoion)【讲座时间】:2016年1月14日 10:00【主讲人】:胡克平:目前为中国医学科学院/北京协和医学院药用植物研究所研究员,博士生导师, 药理毒理研究中心主任。主要研究方向:从事Rett syndrome及MeCP2,并开展了与能量代谢直接关联的三羧酸循环(TCA)复合物研究。【会议简介】以DNA甲基化结合蛋白MeCP2磷酸化发现及功能研究为故事展现如何确定一个蛋白的磷酸化以及磷酸化位点的确定及后继的功能研究。-------------------------------------------------------------------------------1、报名条件:只要您是仪器网注册用户均可报名参加。2、报名截止时间:2016年1月14日9:303、报名参会:http://www.instrument.com.cn/webinar/meeting/meetingInsidePage/17704、报名及参会咨询:QQ群—171692483http://ng1.17img.cn/bbsfiles/images/2017/10/2015042911235201_01_2507958_3.jpg
生物质谱技术在细胞生物学中的应用桑志红 王红霞 综述 概 论 蛋白分离与显色 蛋白质鉴定 数据库查寻 灵敏度 具体示例 展望未来(相关文献)摘 要 基因组计划的飞速发展使我们提早进入"后基因组时代",而质谱技术的重要进展使得通过酶解、质量分析、序列分析及其数据库检索对蛋白质进行高通量快速鉴定的技术方法应运而生,并成为"后基因组时代"的关键核心技术。这种技术的应用范围已经从细胞,组织以及整个有机体中蛋白质的表达到蛋白质翻译后修饰等等方面。本文简要综述生物质谱技术在细胞生物学等学科中的应用。 过去的十年经历并见证了生命科学革命性的变化. 大规模基因组测序技术的问世使人类基因组计划最终目标的实现比预期一再提前。与此同时,近几年间已有10余种模式生物的基因组序列测定告罄,3年内还将有40种左右生物的基因组全序列问世。因此大多数人同意我们现在已经提早进入"后基因组时代"(post-genome era), 目前我们所面临的挑战是如何破解基因组计划已获得的大量序列信息并加以应用。这个问题的关键是基因的生物学功能不能只通过对核酸一级结构(序列)的检测来确定。研判一个未知基因的功能、与其他基因产物及其亚细胞结构之间的功能联系, 最终都必须通过在蛋白水平对基因产物的研究才能确定。蛋白质组这个名词是近几年才提出来的,它用来描述一个细胞的全部蛋白质,而在蛋白水平上进行大规模的研究引出了新的术语蛋白质组学。蛋白质表达图谱是依靠蛋白质显示技术和精确定量技术对细胞或组织中蛋白质表达总况进行比较(2), 这个领域最近已有综述(11)。细胞图谱蛋白质组学是指应用生物质谱技术鉴定蛋白质及其相互作用并确定在亚细胞中的定位。本文的目的是 简要综述生物质谱技术在细胞生物学领域中越来越多的应用,并为该领域正考虑应用这种技术的研究者提供一些的有用的信息。 作为一个新的研究领域,蛋白质组学发展的关键是近年来质谱技术的革新。这种革新极大地促进了质谱技术在生命科学研究中的应用。质谱现在可以作为将各种蛋白质与序列数据库联系起来的桥梁。生物质谱根据质量数和所载电荷数不同的多肽片断在磁场中产生不同轨道而以质荷比(m/z)方式来分离它们。80年代末,随着两种崭新的尤其适合蛋白质研究的软电离方式ESI(电喷雾电离)和MALDI(基质辅助激光解吸附电离)的出现,质谱成为现代蛋白质科学中最重要和不可缺少的组成部分。 生物质谱最强大的应用功能之一是能够鉴定蛋白质复合物的组成成分(19)。细胞中一些最重要的生命过程都是通过多蛋白质复合体来执行和调节的,但由于蛋白质鉴定的困难,大多数上述蛋白复合体都是未知的。生物质谱灵敏度的不断提高显著地促进了对具有生物学功能和治疗潜力的蛋白复合体的鉴定,例如,NF-k B信号通路,CD95(FAS/APO-1)介导的细胞死亡途径,和核受体介导的转录信号传导过程中形成的蛋白复合体。在某些情况下,复合物可通过常规蛋白纯化的方法进行纯化,如剪接体复合(25),酵母纺锤体复合物(29)及VHL肿瘤抑制复合物(18)。然而,更常见的是,复合物中的组成成分通过一步免疫沉淀或免疫亲和步骤后就可纯化,这种方法甚至可以用于鉴定那些用常规蛋白纯化和鉴定技术所不及的一些过渡态或不稳定的复合物。因为生物质谱技术的介入,现在已经不再需要通过抗体进行免疫印迹实验,而是通过生物质谱技术对免疫沉淀获得的蛋白复合体组分直接进行蛋白序列分析。以酵母P24复合物鉴定为例,应用上游表位标签策略有可能不需制备抗目标蛋白的抗体就能对蛋白质复合物进行鉴定(13)。这种方法(36)对于基因组序列已完全清楚和遗传稳定的生物(如芽殖酵母,啤酒酵母)尤为简便, 例如对RENT复合物和促有丝分裂后期复合物(49)。因为这种方法的成功应用,使人们对上游表位标签策略-蛋白纯化-生物质谱分析的方法兴趣倍增。值得一提的是,将能被特殊蛋白酶切除的连接子(接头)掺入表位标签是尤为有利的(如下所述)。 上述方法是通过识别蛋白复合物中相互作用和配对的各组分而达到对蛋白鉴定的目的,另一种策略则是通过对分离纯化的细胞器蛋白组成进行鉴定而在亚细胞水平对蛋白质定位. 用这种方法确定蛋白质位置, 对评价蛋白质潜在的功能将是大有帮助的. 应用这种方法,我们称为细胞器蛋白质组学, 已经发现正常工作状态下的细胞器含有比我们以前所知道的数量多得多的蛋白种类。然而实际上,由于质谱极高的分辨率和灵敏度,纯化后的细胞器组分即使只有微量的混杂,也能被质谱分辨并误认为是细胞器的组成部分。因此,如何充分的纯化以保证至少绝大多数被鉴定的蛋白质都来自同一种细胞器,成为制约上述工作的瓶颈。 蛋白质翻译后修饰也是蛋白鉴定工作中的一个重要方面。根据DNA序列信息并不能可靠预测或推导出蛋白质翻译后的修饰。而质谱技术已经被证明对研究蛋白质翻译后的修饰(例如磷酸化和糖基化)是极为有用的,特别是对序列已知的蛋白的鉴定。例如:Betts等人(1a)用这种方法成功地鉴定了从小鼠大脑中分离的神经纤维蛋白体内磷酸化位点。同样方法, Wong等人(45)确定了钙联蛋白质(calnexin)C未端的磷酸化位点。在糖基化的例子中, Carr等人(5)采用液相色谱与质谱联用技术选择性地鉴定了糖蛋白中N- 和O-联接的寡糖. 稍后, 本文将会通过对E-选择素中糖基化位点的鉴定来进一步说明这种方法.
6 质谱仪的最新进展用质谱检测蛋白,首先考虑到用PMF与 MALDI-TOF联用,如果无法检测,下一步就用ESI-MS/MS创建序列标签。在PMF分析中,MALDI的平板中只需一小部分样本就足以检测,剩下的样本就可以用来创建序列标签。并且,在MALDI-TOF仪器上,用一种叫做“源后延迟”的方法可以对只有部分序列的肽段进行检测。然而,用这个方法产生的质谱图比较难说明,精确性也很差。最近,用MALDI联合四级杆-时间质谱分析器[30,31]以及原始的MALDI-TOF/TOF[32]方法产生了。因此同一份标本可以首先考虑用PMF检测蛋白[33],如果有必要的话,再用MS/MS创建序列标签。MALDI联合四级杆-TOF检测高通量蛋白是有希望的[31]。7 蛋白质组研究中的转录后修饰分析蛋白组分析很重要的一点就是能对蛋白表达水平以及转录后修饰,如磷酸化和糖基化进行研究。蛋白质的磷酸化是很有趣的,因为在信号转导途径中它扮演了重要的角色。最早检测蛋白质表达水平的方法是进行2-DE之前用35S-Met对样本进行代谢性标记,再在2-DE上进行放射自显影[34-36]。在凝胶中,不同蛋白的磷酸化和糖基化位点通常在凝胶中显示一连串蛋白质点,但是还需要做更详细的分析来确定修饰类型。蛋白质磷酸化的改变既可以用32P标记细胞,也可以用特异性磷酸化抗体做western blotting进行研究。如果用32P标记的方法,仍然需要做2-DE。经过凝胶比较后,把感兴趣的点从胶上切下来,然后用质谱鉴定[36]。Soskic使用的是印迹法,两个2-DE同时进行,一个用于做特异的磷酸化抗体实验,另一个做常规染色。蛋白质磷酸化和糖基化更为详细的特性可以用质谱来检测,但是需要更多的起始材料而不仅仅是二维凝胶上的一个点。另外这些分析不能产生直接的序列信息,技术上也比用质谱检测蛋白要难的多。在蛋白上查找磷酸化位点有很多种方法。为了检测消化后的混和肽中哪一个是磷酸化的,可以用MALDI-MS在磷酸化前后对混合肽做PMF分析:经过磷酸酯酶处理后,磷酸化的肽将会失去一个磷酸基团,分子量将比处理前小80Da.糖基化研究中,多聚糖从蛋白中释放出来,对多聚糖结构的检测就是从这些游离的多聚糖中得到的。一般把MALDI仪和外源性糖苷酶[37-40]联合使用进行检测。如果需要更为详细的信息,可以用ESI-MS联合使用前体离子扫描仪[41-44]。到目前为止,能够用电泳分离后的蛋白进行糖蛋白结构检测的报道很少。其中有一项研究是N端糖蛋白酶切以后用一维SDS-PAGE分离,然后用MALDI-MS以及外源性的糖苷酶进行结构分析[45]。8 用质谱研究蛋白-蛋白之间的作用经典的蛋白组学着重于研究蛋白质在何时何处表达。因为大部分的细胞功能都是由蛋白质复合体而不是由单个蛋白来执行的,所以鉴定蛋白质的成分和相互作用是非常重要的。这个过程可以用生物化学方法纯化蛋白质后用质谱来鉴定不同的成分,如人类剪接体的成分,酵母的核孔复合体[46]以及核蛋白体等都可以用此策略检测出来。一般的蛋白复合体是用亲和层析的方法纯化和分离,如免疫沉淀反应[47,48]。 DNA结合蛋白可以用同它们有特异性亲和力的核酸来分离,然后用质谱来鉴定[49]。Rigaut等人在串联层析的基础上,建立了一种通用的蛋白质复合体纯化方法[50]。在这个方法中,一种TAP标签和靶蛋白融合在一起,然后把蛋白转移到宿主细胞或者组织中,融合蛋白在宿主细胞和组织中能持续表达。TAP标签包括一种A蛋白和一种钙调蛋白,在标签之间有一个TEV蛋白酶切位点。用串联亲和层析法能将融合蛋白及与它相互作用的蛋白成分从细胞提取物中有效的分离,纯化出来。Rappsiber等人分别用亲和层析,交叉耦合以及质谱等方法[51]对酵母的核孔复合物Nup85p的亲和性进行研究。经过层析以后,用一维SDS-PAGE方法就可以分离蛋白复合体中的各个成分,因此二维电泳的不足之处就可以避免。同样也有可能直接用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]方法分析大分子量蛋白质复合体[52]。蛋白组分析的优越之处主要是用于蛋白和蛋白之间的相互作用以及蛋白的转录后修饰的研究,同时也可以用于基因表达水平的研究。质谱对于蛋白组分析来说是一项非常重要的技术,近年来仪器以及数据库软件的发展使得质谱成为能力更强大的工具。参考文献[1] O’Farrell PH. J Biol Chem,1975,250:4007–4021.[2] Karas M, Bachmann D, Bahr U, et al. Int J MassSpecrom Ion Process,1987,78:53–68.[3] Meng CK, Mann M, Fenn JB. et al. Atoms, Mol Clusters,1988,10:361–368.[4] Fenn JB, Mann M, Meng CK, et al.Science,1989,6(246):64–71.[5] Corthals GL, Wasinger VC, Hochstrasser DF, et al.Electrophoresis,2000,21:1104–1115.[6] Celis JE, Kruhoffer M, Gromova I, et al. FEBS Lett,2000,480:2–16.[7] Anderson L, Seilhamer J. Electrophoresis,1997,18:533–537.[8] Gygi SP, Rochon Y, Franza BR, et al. Mol Cell Biol,1999,19:1720–1730.[9] Henzel WJ, Stults JT, Wong SC, et al. ProcNatl Acad Sci USA,1993,90:5011–5015.[10] Mann M, Hojrup P, Roeppstorff P. Biol Mass Spectrom,1993,22:338–345.[11] Pappin DJ, Hojrup P, Bleasby AJ. Curr Biol,1993,3:327–332.[12] James P, Quadroni M, Carafoli E, et al. Biochem BiophysRes Commun,1993,195:58–64.[13] Yates JRD, Speicher S, Griffin PR, et al. AnalBiochem,1993,214:397–408.[14] Mann M, Wilm M. Anal Chem,1994,66:4390–4399.[15] Eng JK, McCormack AL, Yates JR. J Am Soc Mass Spectrom,1994,5:976–989.[16] Wilm M, Mann M. Int J Mass Spectrom Ion Process,1994,136:167–180.[17] Wilm M, Shevchenko A, Houthaeve T, et al. Nature 1996 379:466–469.[18] Wilm M, Mann M. Anal Chem,1996,68:1–8.[19] Morris HR, Paxton T, Panico M, et al. JProtein Chem,1997,16:469–479.[20] Rosenfeld J, Capedeville J, Guillemot JC, et al. AnalBiochem,1992,203:173–179.[21] Shevchenko A, Wilm M, Mann M. Anal Chem,1996,68:850–858.[22] Pandey A, Andersen JS, Mann M. Science’s STKE: www.stke.org/cgi/content/full/OC–sigtrans 2000/37/pl1.[23] Kussmann M, Nordhoff E, Rahbek-Nielsen H, et al. J Mass Spectrom,1997,32:593–601.[24] Gobom J, Nordhoff E, Mirgorodskaya E, et al. J Mass Spectrom,1999,34:105–116.[25] Clauser KR, Baker P, Burlingame AL. Anal Chem,1999,71:2871–2882.[26] Binz PA, Muller M, Walther D, et al. Anal Chem,1999,71:4981–4988.[27] Bienvenut WV, Sanchez JC, Karmime A, et al. Anal Chem,1999,71:4800–4807.[28] Neubauer G, King A, Rappsilber J, et al. Nat Genet,1998,20:46–50.[29] Yates III JR, Carmack E, Hays L, et al. MethodsMol Biol,1999,112:553–569.[30] Loboda AV, Krutchinsky AN, Bromirski M, et al. Rapid Commun Mass Spectrom,2000,14:1047–1057.[31] Shevchenko A, Loboda A, Schevchenko A, et al. Anal Chem,2000,72:2132–2141.[32] Medzihradszky KF, Campbell JM, Baldwin MA, et al. Anal Chem 2000,72:552–558.[33] Krutchinsky AN, Zhang W, Chait BT. J Am Soc Mass Spectrom,2000,11:493–504.[34] Nyman TA, Matikainen S, Sareneva T, et al. Eur J Biochem 2000 267:4011–4019.[35] Celis JE, editor. Cell Biology: A Laboratory Handbook, vol. 4,2nd. Academic Press, 1998,375–385.[36] Gerner C, Frohwein U, Gotzmann J, et al. J Biol Chem,2000,Sep 7 [epubahead of print].[37] Colangelo J, Orlando R. Anal Chem,1999,71:1479–1482.[38] Geyer H, Schmitt S, Wuhrer M, et al. Anal Chem1999 71:476–482.[39] Harvey DJ. Mass Spectrom Rev,1999,18:349–450.[40] Nyman TA, Kalkkinen N, et al. Eur J Biochem,1998,253:485–493.[41] Sheeley DM, Reinhold VN. Anal Chem,1998,70:3053–3059.[42] Reinhold VN, Reinhold BB, Costello CE. Anal Chem,1995,67:1772–1784.[43] Kuster B, Hunter AP, Wheeler SF, et al. Electrophoresis,1998,19:1950–1959.[44] Rout MP, Aitchison JD, Suprapto A, et al. J Cell Biol,2000,148:635–651.[45] Yamaguchi K, Subramanian AR. J Biol Chem ,2000,275:28 466–28 482.[46] Yamaguchi K, von Knoblauch K, Subramanian AR. J BiolChem,2000,275:28 455–28 465.[47] Rotheneder H, Geymayer S, Haidweger E. J Mol Biol,1999,293:1005–1015.[48] Boehning D, Joseph SK. EMBO J,2000,19:5450–5459.[49] Nordhoff E, Krogsdam AM, Jorgensen HF, et al. Nat Biotechnol,1999,17:884–888.[50] Rigaut G, Shevchenko A, Rutz B, et al. Nat Biotechnol,1999,17:1030–1032.[51] Rappsilber J, Siniossoglou S, Hurt EC, et al. Anal Chem2000 72:267–275.[52] Link AJ, Eng J, Schieltz DM, et al. Nat Biotechnol,1999,17:676–682.T.A. Nyman /Biomolecular Engineering, 2001:18 .221–227.
[color=#444444]样品是磷酸化多肽,我们的仪器是[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]的ESI质谱,老师说拿测出来的质谱图和MALDI质谱测出来的图对照,如果找到相应的峰(去卷积后的数值和maldi的数值减去1相同),就说明测到了磷酸化多肽,我一直想不明白,有没有大神替我解释一下这是为什么?[/color]
请问Q-TOF和MALDI-TOF的区别?这两种质谱的特点,能不能检测出蛋白的磷酸化位点,谢谢!!!
一、 前言基因工程已令人难以置信的扩展了我们关于有机体DNA序列的认识。但是仍有许多新识别的基因的功能还不知道,也不知道基因产物是如何相互作用从而产生活的有机体的。功能基因组试图通过大规模实验方法来回答这些问题。但由于仅从DNA序列尚不能回答某基因的表达时间、表达量、蛋白质翻译后加工和修饰的情况、以及它们的亚细胞分布等等,因此在整体水平上研究蛋白质表达及其功能变得日益显得重要。这些在基因组中不能解决的问题可望在蛋白质组研究中找到答案。蛋白质组研究的数据与基因组数据的整合,将会在后基因组研究中发挥重要作用。目前蛋白质组研究采用的主要技术是双向凝胶电泳和质谱方法。双向凝胶电泳的基本原理是蛋白质首先根据其等电点,第一向在pH梯度胶内等电聚焦,然后转90度按他们的分子量大小进行第二向的SDS-PAGE分离。质谱在90年代得到了长足的发展,生物质谱当上了主角,蛋白质组学又为生物质谱提供了一个大舞台。他们中首选的是MALDI-TOF,其分析容量大,单电荷为主的测定分子量高达30万,干扰因素少,适合蛋白质组的大规模分析。其次ESI为主的LC-MS联机适于精细的研究。本文将简介几种常用的生物质谱技术,并着重介绍生物质谱技术在蛋白质组学各领域的应用。二、 生物质谱技术1.电喷雾质谱技术(ESI)电喷雾质谱技术( Electrospray Ionization Mass Spectrometry , ESI - MS) 是在毛细管的出口处施加一高电压,所产生的高电场使从毛细管流出的液体雾化成细小的带电液滴,随着溶剂蒸发,液滴表面的电荷强度逐渐增大,最后液滴崩解为大量带一个或多个电荷的离子,致使分析物以单电荷或多电荷离子的形式进入气相。电喷雾离子化的特点是产生高电荷离子而不是碎片离子, 使质量电荷比(m/ z) 降低到多数质量分析仪器都可以检测的范围,因而大大扩展了分子量的分析范围,离子的真实分子质量也可以根据质荷比及电荷数算出。2.基质辅助激光解吸附质谱技术(MOLDI)基质辅助激光解析电离(MOLDI)是由德国科学家Karas和Hillenkamp发现的。将微量蛋白质与过量的小分子基体的混合液体点到样品靶上,经加热或风吹烘干形成共结晶,放入离子源内。当激光照射到靶点上时,基体吸收了激光的能力跃迁到激发态,导致蛋白质电离和汽化,电离的结果通常是基体的质子转移到蛋白质上。然后由高电压将电离的蛋白质从离子源转送到质量分析器内,再经离子检测器和数据处理得到质谱图。TOF质量分析器被认为是与MALDI的最佳搭配,因为二者都是脉冲工作方式,在质量分析过程中离子损失很少,可以获得很高的灵敏度。TOF质量分析器结果简单,容易换算,蛋白质离子在飞行管内的飞行速度仅与他的(m/z)-1/2成正比,因此容易通过计算蛋白质离子在飞行管内的飞行时间推算出蛋白质离子的m/z值。与传统质量分析器相比,更易得到高分辨率和高测量精度;速度快,离子飞行时间仅为几个μs和约100μs之间;质量范围宽,可以直接检测到几十万道尔顿的单电荷离子。飞行时间质量分析器被认为是21世纪最有应用前景的质量分析器。3.傅立叶变换-离子回旋共振质谱(FT-ICR MS)傅立叶变换-离子回旋共振质谱法(FT-ICR MS)是离子回旋共振波谱法与现代计算机技术相结合的产物。傅立叶变换-离子回旋共振质谱法是基于离子在均匀磁场中的回旋运动, 离子的回旋频率、半径、速度和能量是离子质量和离子电荷及磁场强度的函数, 当对离子施加与其回旋频率相同的射频场作用时, 离子将同相位加速到一较大的半径回旋, 从而产生可被接受的类似电流的信号。傅立叶变换-离子回旋共振质谱法所采用的射频范围覆盖了欲测定的质量范围,所有离子同时被激发, 所检测的信号经过傅立叶变换, 转换为质谱图。其主要优点有:容易获得高分辨;便于实现串极质谱分析;便于使用外电离源并与色谱仪器联用。此外,他还有灵敏度高,质量范围宽,速度快,性能可靠等优点。4.快原子轰击质谱技术(FABMS)快原子轰击质谱技术( Fast Atom Bomebardment Mass Spectrometry , FABMS) 是一种软电离技术,是用快速惰性原子射击存在于底物中的样品,使样品离子溅出进入分析器,这种软电离技术适于极性强、热不稳定的化合物的分析,特别适用于多肽和蛋白质等的分析研究。FABMS能提供有关离子的精确质量,从而可以确定样品的元素组成和分子式。而FABMS -MS 串联技术的应用可以提供样品较为详细的分子结构信息,从而使其在生物医学分析中迅速发展起来。三、蛋白质的分析鉴定随着质谱技术的发展,分子量的测定已从传统的有机小分子扩展到了生物大分子。MALDI-MS技术以其极高的灵敏度、精确度在蛋白质分析中得到了广泛的应用。该技术不仅可测定各种疏水性、亲水性和糖蛋白的分子量,还可直接测定蛋白质混合物的分子量。这可认为是蛋白质分析领域的一项重大突破。蛋白质组的研究是从整体水平上研究细胞或有机体内蛋白质的组成及其活动规律。质谱技术作为蛋白质组研究的三大支撑技术之一,除了用于多肽,蛋白质的分子量测定外,还广泛的应用于肽指纹图谱测定及氨基酸序列测定。肽指纹图谱(Peptide Mass Fingerprinting, PMF)测定是对蛋白酶解或降解后所得多肽混合物进行质谱分析的方法。质谱分析所得肽断与多肽蛋白数据库中蛋白质的理论肽断进行比较,判断出所测蛋白是已知还是未知。由于不同的蛋白质具有不同的氨基酸序列,不同蛋白质所得肽断具有指纹特征。采用肽指纹谱的方法已对酵母、大肠杆菌、人心肌等多种蛋白质组进行了研究。对肽序列的测定往往要应用串连质谱技术,采用不同的技术选择特定质核比的离子,并对其进行碰撞诱导解离,通过分析肽段的断裂情况推导出肽序列。四、后转录修饰的蛋白质的检测和识别在蛋白质组的研究中,蛋白质和多肽的序列分析已不局限于阐明蛋白质的一级结构,对翻译后的修饰的进一步分析也是蛋白质化学的一项重要任务。这种修饰对于蛋白质的功能非常重要,如:细胞识别中的蛋白质相互作用,信号传导和蛋白质定位。1. 蛋白质的糖基化糖蛋白在细胞内部,细胞膜和细胞外均有发现,实际上大部分蛋白质是糖蛋白。对糖蛋白的检测和分析发现,糖蛋白中糖组分的结构和功能具有多样性。糖蛋白中的糖通常是不同种类的,而且是由一些可控数量的单糖组成。糖基化的多样性与细胞周期,细胞分化和发展的状态有关。在蛋白组时代中,蛋白质的修饰会引起其理化性质的改变,因此是不容忽视的。从1D或2D凝胶得到的糖基化蛋白的识别,一般是进行MALDI-MS指纹分析, 或是对MALDI-PAD或ESI-MS/MS得到的碎片谱进行分析。对完整的糖蛋白的研究是非常困难的,所有已知的离子化技术都有其局限性。目前,人们主要研究糖肽,其好处之一就是质量减小了,这就会得到更好的分辨率,而且糖肽仍保留了糖基化位点。将分离的糖蛋白用不同的蛋白酶消化后就可进行糖肽的研究。一旦糖肽被识别出,就可以用串连质谱(ESI-MS/MS)来阐明肽序列。当蛋白的序列已知时,计算质量差就可推出其上附着的寡糖的质量。要将糖部分从糖蛋白中释放出来,可用化学切割或酶切割(流程图见图1)。目前,连有结构专一性糖苷酶的质谱在提供序列,分支和链接数据方面是最有力的技术。对于N糖基化常用的糖苷内切酶有PNGase-F, PNGase-A, EndoF和EndoH。化学切割也可以用来释放O-连接和N-连接的多糖,但经常出现的缺点是他会完全破坏所有的肽键,因而丢失了关于糖附着位点的信息。而且这些切割不能从糖肽中连续释放单糖。用肼的化学切割可以除去两种类型的糖基化。在60℃可专一性的释放O-连接的糖,而在95℃能释放N-连接的糖。释放O-原子更常用的方法是用碱进行β消除。通常,糖基中加入金属离子在MALDI和ESI中离子化。用MALDI-MS分析糖类的一个好的选择是将之与其他一些化合物混合,这样可以进一步提高灵敏度和分辨率。不同的质谱方法可以产生多糖的源后裂解(PSD)和碰撞诱导解离 (CID)谱,这可以给出有关糖的序列,分支及糖间的连接等信息。2. 蛋白质的磷酸化蛋白质中氨基酸的磷酸化在生命系统中起重要的作用。磷酸化经常作为分子开关控制不同过程蛋白质的活性,如新陈代谢,信号传导,细胞分裂等过程。因此,蛋白质中磷酰氨基酸的识别在蛋白质分析中是一项重要的工作。已知的磷酰氨基酸的类型有四种:1.O-磷酸盐,通过羟氨酸的磷酸化形成的,如丝氨酸,苏氨酸,酪氨酸。2.N-磷酸盐,通过精氨酸,赖氨酸或组氨酸中的氨基的磷酸化形成的。3.乙酰磷酸盐,通过天冬氨酸或谷氨酸的磷酸化形成的。4.S-磷酸酯,通过半胱氨酸的磷酸化形成的。
欢迎大家讨论一下自己做质谱的经验心得,在医疗领域和其他众多领域质谱无疑是以后发展的科研和临床应用的主流方向,其配套仪器业发展的很快,如气象色谱、液相色谱、毛细管电泳等等。因为应用领域广,讨论的范围肯定很大,大家可以各抒己见啊。我是做蛋白磷酸化修饰的,也是刚跟质谱打交道,所以很想听听各位高手的高见啊,欢迎,O(∩_∩)O谢谢。
PS1利用基质辅助激光解吸电离-飞行时间(MALDI-TOF)技术来表征生物分子。样品溶于固定的底物中形成晶体,用激光脉冲使其离子化,离子被加速后通过飞行管时分离,所有离子均可被检测。系统包括三个组成部件:样品点样制备工作站(SymBiot 1)、生物质谱工作站(Voyager-DE PRO)和自动化分析软件(AutoMS-Fit)。SymBiot1 是一个自动样品处理系统,支持亚微升级微量点样,具有快速省时、重现性好的特点;Voyager-DE PRO是为蛋白质组研究专门设计的自动飞行时间质谱分析系统,配有AB公司之专利—延迟检测技术,具有高分辨率、质荷比宽等特点;AutoMS软件可以批处理方式或实时动态方式检索Protein Prospector蛋白数据库或您指定的蛋白数据库,查询参数可以任意设定,检索结果以Microsoft Access格式分类编号及储存。 PS 1技术平台建立伊始便受到了许多蛋白质课题研究组的关注。中国科学院上海生物化学研究所戚正武院士课题组从猪肝中提取某一活性蛋白组分,该组分理化性质不清楚,天然含量十分低,并无相关文献报道。用HPLC分离以后对活性组分的成分不能确定。上海基康生物技术有限公司运用PS 1系统对HPLC分离后的活性组分作了质谱分析,仅在一个工作日内就精确确定该组分由分子量极为相近的几种蛋白质构成,分子量精确度达到10 ppm。后经HPLC再次细分(洗脱梯度增加了2.5倍),证实了质谱的结论。此活性组分曾滤过1kD分子筛,基康的质谱数据纠正了研究人员过去对该活性组分分子量的误判,为研究人员明确实验方向、优化实验步骤提供了强有力的依据。 PS1除了可以进行生物大分子的精确分子量测定,还可用于蛋白的肽指纹图谱分析(peptide mass fingerprint,PMF),提供相关生物信息学服务,并且还可以利用源后衰变(Post Source Decay,PSD)技术来获得样品的MS/MS数据,以得到一级结构信息。PSD方法通常增加了激发激光的功率,使其超过产生一般肽指纹谱图所需功率的阈值,过剩的能量使前体离子在源内离子化之后发生裂解,产生一系列碎片离子,在反射器的作用下,最终可以得到一张连续的碎片离子图谱。经特定的软件分析后,即可在数据库中检索到肽段的氨基酸序列。利用PSD分析技术,还可以对磷酸化,糖基化等翻译后修饰进行定位分析,同样也可以鉴定产生翻译后修饰肽段的蛋白质。Neville et al.(1997)将这一方法成功的用于磷酸肽的序列分析。作为重要的蛋白质鉴定手段之一,PS1的精确度可以达到10 ppm,灵敏度为fmol,分子量检测范围可达到500 kDa,每天可自动分析40-100个样品,适用于大规模“蛋白质组学”研究。
转从:中国分析网,很不错的一网站。[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=16097]YYSWXS0296 蛋白质 糖蛋白重组人白介素 4受体 N-糖基化位点测定 基质辅助激光解吸附电离飞行时间质谱法[/url][img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=16098]YYSWXS0281 蛋白质 β-casein的磷酸化分析 电喷雾质谱法[/url][img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=16099]YYSWDB0131 蛋白质细胞色素C 分子量的测定电喷雾质谱法[/url]
[b]什么是磷酸化蛋白质[/b]蛋白质磷酸化是指在激酶催化作用下把ATP或者GTP的磷酸基团(P04)转移到不同种类的氨基酸上(主要包括丝氨酸S、苏氨酸T、酪氨酸Y),从而使蛋白质发生翻译后修饰的过程。该修饰是蛋白质翻译后修饰(PTM)中最为重要的形式,具有显著的生物学功能,细胞增殖和凋亡,良性发育,信号转导,新陈代谢,肿瘤发生等过程都有磷酸化蛋白质的插足,研究磷酸化蛋白质对探究生物学病变机理有着非常重要的意义。[b]富集磷酸化蛋白质重要性[/b]磷酸化蛋白质具有低丰度和高动态性的特点,因此对磷酸化蛋白质组学研究首先需要对磷酸化蛋白样品进行富集,降低样品复杂程度和提高磷酸化位点鉴定数目。固相金属离子亲和色谱法(IMAC)是磷酸化蛋白质组学研究中最常用的磷酸化蛋白质富集技术之一。[b]Welchrom Ti Poss (phosphate ester)固相金属离子亲和填料[/b]Welchrom Ti Poss (phosphate ester) 是月旭科技推出的的新一代固相金属离子亲和填料,金属离子Ti??鳌合在磷酸酯 (phosphate ester) 为配基的多级孔杂化整体材料上形成的亲和填料,利用磷酸化基团与固相化的Ti??的高亲和力来富集磷酸化蛋白质。磷酸化蛋白质上的磷酸基团中的三个氧原子分别与富集材料上的三个不同Ti??螯合以形成稳定的八面体形的配位结构,这种配位方式提供了良好的结合能力。该填料具有吸附量大、选择性好、成本低、适用范围广、操作简单特点。[b]规格参数[/b][table=521][tr][td=1,1,156]基架名称[/td][td=1,1,365]多面体低聚倍硅氧烷(POSS)作为单体所制备的多级孔杂化整体材料[/td][/tr][tr][td=1,1,156]粒径范围[/td][td=1,1,365]几十微米至几百微米[/td][/tr][tr][td=1,1,156]结合载量[/td][td=1,1,365]63.6 mg/g[/td][/tr][tr][td=1,1,156]适用样品范围[/td][td=1,1,365]所有含有磷酸基团的蛋白质和肽段[/td][/tr][tr][td=1,1,156]磷酸化肽段富集特异性[/td][td=1,1,365]97%[/td][/tr][tr][td=1,1,156]pH稳定性[/td][td=1,1,365]强酸、强碱下均可使用[/td][/tr][tr][td=1,1,156]化学稳定性[/td][td=1,1,365]常见有机溶剂下均可使用[/td][/tr][tr][td=1,1,156]保存条件[/td][td=1,1,365]干燥状态下室温保存[/td][/tr][tr][td=1,1,156]通用性操作步骤[/td][td=1,1,365]采用80% ACN/6% TFA水溶液作为富集溶液,这样可以在富集过程中,很大程度上避免疏水性非磷酸化肽段的吸附。去除上清溶液后,依次用洗涤溶液A(50% ACN/6% TFA/200 mMNaCl)和溶液B(30%ACN/0.1%TFA)进行洗涤,这样可以最da程度上洗去非特异性肽段。最后采用100 μL 10%(wt%)的氨水洗脱吸附在材料上的磷酸化肽段。[/td][/tr][/table][b]应用案例[/b][align=center][img]https://img1.17img.cn/17img/images/201910/uepic/556dc556-79d8-4012-81ef-a8a16364ff16.jpg[/img][/align](a)β-酪蛋白酶解液直接进行分析的 MALDI TOF-MS谱图和(b)Welchrom Ti Poss材料富集后分析的MADLI TOF-MS谱图[b]实验条件:[/b]0.1μg β-酪蛋白酶解液;采用80% ACN/6% TFA水溶液作为富集溶液,去除上清溶液后,依次用洗涤溶液A(50% ACN/6% TFA/200 mM NaCl)和溶液B(30%ACN/0.1%TFA)进行洗涤,最后采用100 μL 10%(wt%)的氨水洗脱吸附在材料上的磷酸化肽段。图a中,未经过富集的β-酪蛋白酶解液样品MALDI谱图中,非磷酸化肽段的质谱信号峰非常强,严重影响了对磷酸化肽段的辨别。而经过Ti??-IMAC富集,从MADLI谱图中(图b)可以清晰的看到磷酸化肽段以及其去磷酸化肽段的信号峰,而且几乎没有出现任何非磷酸化肽段的信号峰。证实了Welchrom Ti Poss富集对磷酸化肽段具有良好的富集能力。[table=562][tr][td][align=center][b]产品名称[/b][/align][/td][td][align=center][b]规格[/b][/align][/td][td][align=center][b]货号[/b][/align][/td][/tr][tr][td][align=center][b]Welchrom Ti Poss (phosphate ester)[/b][/align][/td][td][align=center][b]250mg[/b][/align][/td][td][align=center][b]ATI001[/b][/align][b][/b][/td][/tr][/table]
ABSCIEX 生物质谱新技术培训4月/25日9:00-9:15am ABSCIEX 介绍9:15-10:15am 复旦杨芃原:生物质谱QTOF的仪器技术10:15-10:30am Break10:30-11:15am 实验室考察: 复杂生物样本的蛋白质鉴定11:15-12:00pm AB SCIEX 专家: 蛋白质鉴定和定量的实验设计--5600 QTOF的应用12:00-1:00pm 午餐1:00-2:30pm ABSCIEX 专家(Wenhai): SWATH 技术的实验设计2:30-3:15pm 实验室考察: 建立SWATH 技术的实验流程3:15-3:30pm Break3:30-5:00pm ABSCIEX 专家:SWATH 技术的数据处理4月/26日9:00-9:45am 复旦刘晓慧/陈晨/张磊:疾病生物标志物的鉴定和确认技术9:45-10:15am AB SCIEX 专家:MIDAS 实验设计10:15-10:30am Break10:30-12:00pm 实验室考察: MIDAS 实验流程的建立和数据处理12:00-1:00pm 午餐1:00-2:30pm ABSCIEX 专家: 应用iTRAQ 技术筛选分子标志物2:30-3:30pm 热电公司专家:待定”生命科学中的化学基础协同创新中心”生物质谱培训和讨论班4月/27日9:00-9:50am 复旦杨芃原: 生物质谱的仪器技术概况10:00-10:50am 复旦金红: 组蛋白修饰分析的质谱技术10:50-11:10am Break11:10-12:00 am 诺华/复旦廖日晶: 组蛋白修饰(甲基化)分析的质谱技术12:00-1:00pm 午餐2:00-2:50pm 复旦陆豪杰:磷酸化蛋白的质谱分析3:00-3:50pm 复旦杨芃原/曹玮倩/刘铭琪: 糖修饰蛋白的质谱分析3:50-4:10pm Break4:10-5:00pm 热电公司张伟:Orbitrap质谱的蛋白质组学方法开发与应用进展5:00-5:50pm康昱盛信息科技有限公司: 非标记定量方法的介绍和前期数据质量控制4月/28日9:00-9:50am 复旦申华莉/刘晓慧:蛋白质组测序的深度覆盖技术10:00-10:50am 北京蛋白质组研究中心应万涛:蛋白质谱分析的绝对定量技术10:50-11:10am Break11:10-12:00 am 康昱盛信息科技有限公司:蛋白质组学的IPA生物通路分析方法12:00-1:00pm 午餐2:00-2:30pm 热电公司讲座(欢迎参加)地址:上海市徐汇区东安路130号 复旦大学上海医学院 生物医学研究院 明道楼2楼
质谱技术是抗体药物分析最重要的技术手段之一。本文简述了抗体药物的发展和质谱技术的原理。对于质谱技术在抗体药物的分析中应用进行了归类整理,主要分为在一级结构和高级结构分析中的应用。抗体类药物是指含有抗体片段的蛋白类药物,所以在恶性肿瘤、自身免疫性疾病、心血管疾病、感染和器官移植排斥等重大疾病上得到了快速的发展,是当前生物药物领域增长最快的一类药物.1.抗体药物发展新趋势在生物药物领域,抗体药物占据着越来越重要的地位,全球销售排名前10位的药物中有6个为抗体药物,抗体药物按来源分类可以分为:鼠源单克隆抗体、人鼠嵌合抗体、人源化抗体和全人源抗体。目前,批准的单克隆抗体药物中,人源化单抗和全人源单抗数量已占据大多数。1.1 抗体药物偶联物(ADC)抗体药物偶联物(ADC)由单克隆抗体和小分子化合物两部分组成。通过抗体的靶向作用,ADC 的抗体部分和肿瘤细胞表面抗原特异性识别并结合,通过细胞内吞作用,将抗体和小分子化合物一起带进肿瘤细胞内部,释放出小分子化合物。这样既可以降低小分子药物的毒性,同时具有靶向结合的作用。已经上市的两个ADC 是Kadyla 和Adcetris。1.2 双特异性抗体(BsAb)双特异性抗体(BsAb)是含有两种特异性抗原结合位点的人工抗体,能在靶细胞和功能分子(细胞)之间架起桥梁,由于基因工程的发展,目前双特异性抗体已经研发出多种类型,主要类型有三功能双特异性抗体、IgG-scFv、三价双特异性分子、串联单链抗体(串联scFv)、DVD-Ig 等多种形式。2.质谱技术近年来质谱仪性能的显著改进主要基于开发出的两种离子化技术:一种是介质辅助的激光解吸/离子化技术。另一种是电喷雾离子化技术。由于这两种电离技术的出现,使原本只能检测小分子的质谱技术,可以运用于检测生物大分子。在过去质谱技术主要运用于对一级结构和序列的表征,而现在质谱技术越来越多地运用于高级结构的分析,而高级结构对于抗体药物的生物活性至关重要。3.质谱技术在抗体药物一级结构分析中的应用3.1 完整抗体药物精确分子量测定当得到抗体药物时,可以直接通过高分辨率的MALDI-TOF或者ESI-MS进行分子量的检测。通过对于脱糖后分子量的检测,可以对于抗体药物进行初步定性分析,并将可以作为药物常规放行的分析方法。对于脱糖前的抗体药物进行分析,可以得到抗体药物的糖基化类型的信息及糖基化水平的分布,对于快速了解生产工艺与药物质量的关系具有十分重要的意义。3.2 药物抗体偶联比(DAR)对于赖氨酸链接的抗体偶联药物,采用C4色谱柱及联用的质谱对去糖基化样品进行分析,根据偶联不同数目药物分子的质量数增加判断偶联数目。对于质谱测定的结果,不仅可以给出确切的药物抗体偶联比值,更能够给出链接不同个小分子药物的分布情况,及反应过程副产物空链接头的分布情况。3.3 肽图谱分析蛋白被特异酶切后的蛋白酶水解后得到的肽片段质量图谱。由于不同的抗体药物具有不同的氨基酸序列,蛋白质被酶水解后,产生的肽片段也各不相同,肽混合物的质量数具有唯一特征。可以通过LC-ESI-MS进行肽片段的一级质量数的鉴定,也可以通过LC-ESI-MS/MS对于每个肽片段进行进一步确证,提高肽图谱的准确性。3.4 翻译后修饰研究蛋白质的翻译后修饰(PTM)对于抗体药物的生物学功能十分重要。常见的翻译后修饰有:磷酸化、脱酰胺、甲硫氨酸氧化、糖基化修饰、N端焦谷氨酸环化,C端赖氨酸切除等。质谱分析仪检测蛋白和肽片段的分子量偏差,可以实现高灵敏、高通量和高精确地鉴别蛋白质的翻译后修饰的种类。3.5 N端氨基酸序列检测常规N端氨基酸检测用Edman降解法进行检测,但是抗体药物有时候会出现N 端环化的现象,在这种情况下用Edman降解法需要先对抗体进行去封闭处理,而直接使用质谱可以直接测出N端的氨基酸序列,同时可以检测出N端环化的相对比例。4.质谱技术在抗体药物高级结构分析中的应用4.1 氢/氘交换质谱(HDX-MS)常规的质谱只能获得蛋白的一级结构信息。氢/氘交换质谱(HDX-MS)可以进行蛋白质构象,溶液动力学和表位映射进行分析。在能够调查的蛋白质的高阶结构和动态结构技术中,HDX-MS已经证明适合单克隆抗体和单克隆抗体-抗原复合物的构象分析。4.2 离子淌度质谱法(IM-MS)离子淌度是根据蛋白的电荷和形状选择性分离的方法,可以区分相同分子量的蛋白和肽段,可用于检测蛋白的简单高级结构。4.3 高分辨率傅立叶变换离子回旋共振质谱(FTICR-MS)高分辨率傅立叶变换离子回旋共振质谱(FTICR-MS)能够检测最高质量数的质谱仪器,并且有着很高的分辨率。FTICR-MS 是目前被公认为是蛋白质组学研究的有力工具,特别是和完整的蛋白质鉴定和上/下调翻译后修饰(PTM)蛋白质的鉴定。
高分辨质谱 用低分辨质谱测定时,分子的质量数都是整数表示,如CO、N2、C2H4和CH2N的质量都是28。如果用高分辨质谱测定就能得到如C2H4=28.031299,CH2N=28.018723,因此,根据高分辨质谱所测得的精密质量就可以对结构加以剖析和区别 小分子化合物确定结构式有多种方法,NMR,高分辨质谱(由于每个元素的原子量实际都是小数的,通过高分辨质谱可以直接获得化学式! 其中高分辨质谱我们强烈推荐THERMO LTQ ORBITRAP Orbitrap具有高分辨率[最高可达45万半峰全宽(FWHM)],高质量精度(0.1×10-6~1×10-6),质量范围宽,动态范围广的优点,可提供大范围的定性和定量分析,并且克服了其他高分辨质谱如傅里叶变换离子回旋共振(FTICR)质谱、飞行时间(TOF)质谱的尺寸大,维护与操作复杂的缺点。 在药物分析的应用 此段摘取贺美莲 郭常川 石峰 姜玮 所著的《Orbitrap高分辨质谱技术在药物分析领域中的应用进展》 在药物代谢方面的应用 Orbitrap高分辨质谱可以在很宽的质量范围内生成全扫描数据,同时提供组分的定性和定量分析[21]。此外,在各种生物基质(如血浆、血清,尿液等)中的药物代谢物分析需要复杂的前处理过程,而Orbitrap质谱对于复杂生物基质中的痕量分析物也可进行准确的分析,从而简化了样品前处理过程。基于这些优势,Orbitrap质谱已成为药物代谢研究中强有力的分析工具 在中药组分分析方面的应用 Orbitrap串联超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url]实现单针进样即可高通量获取中药中的成百上千化合物的定性和定量信息,能够显著提高中药复杂体系中化学成分的快速分析鉴定能力。 中药由于成分复杂,对于其真正起治疗作用的化学成分往往不够清晰。应用二维[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]串联LTQ-Orbitrap质谱对丹参中的酚酸和双萜类成分进行定性和定量分析。根据裂解机制和高分辨MSn数据,共鉴定或初步表征了102个化合物,同时检测到丹参样品中的14个生物活性化合物,其中10个酚酸类和4个双萜类,这些成分是丹参发挥心血管疾病治疗作用的主要成分。 从中药中探索新的化学实体是筛选候选药物的重要来源。采用Orbitrap高分辨质谱鉴定蛇麻花中具有潜在抗菌活性的化合物,对钩藤中的92个吲哚生物碱进行系统表征并发现56个新的潜在生物活性分子,进一步明确了钩藤治疗作用的物质基础。 在药品杂质检查方面的应用 杂质检查是药品质量安全评价的重要环节。得益于其强大的定性和定量分析性能,Orbitrap技术可为原料药中杂质和药物降解产物研究提供强有力的支持。采用超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]串联紫外检测器和高分辨质谱检测器(UPLC-UV-LTQ-Orbitrap)对左旋甲状腺素的氧化降解杂质进行鉴定,利用时间分辨的高分辨质谱数据和自动数据处理的结合能够推断出单个化合物基础上杂质形成的动力学及其形成机制;通过比较降解曲线,总共识别了4个主要类型的甲状腺素降解杂质的产生路径。 采用超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]串联Orbitrap质谱仪对伊潘立酮降解杂质进行分离和鉴定,通过[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS分析共鉴定了7种降解杂质,并发现在水解和氧化条件下,伊潘立酮是不稳定的。 在中成药非法添加筛查方面的应用 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]串联高分辨质谱技术不仅可以用来筛查已知的非法添加成分,还可以发现并鉴定复杂基质中的未知成分,先后对中成药中非法添加的磷酸二酯酶-5抑制剂、降糖药和糖皮质激素的筛查和鉴定进行了研究。在63批次中成药和34批次保健品样本的检测中,共有7批保健品检测到降糖药,涉及二甲双胍、苯乙双胍和格列本脲等在非法添加糖皮质激素的检测中,分析物响应与质量浓度(1.0~1 000 ngmL-1)呈良好的线性关系,回归系数(r2)大于0.999 0,所有分析物检测下限(LODs)为1.0 ngmL-1,在42批中成药中共有22批样品检测到醋酸泼尼松,其中1批样品同时检测到了泼尼松和醋酸氢化可的松。 在蛋白质组学的应用 目前广泛使用的用于蛋白质鉴定的质谱分析主要使用两种类型质谱:一种是MALDI-TOF直接对分子量进行测量;另一种是使用ESI-MS高分辨率质谱分析电喷雾得到的多电荷信号,然后对信号进行去卷积分析,获得精确分子量数值。这两种方法各有其优点及适用的领域 采用直接MALDI-TOF进行分子量测定的主要问题是,MALDI-TOF质谱仪在不同质量区域内分辨率差别很大,分子量越大,分辨率越低。因此当样品为大分子蛋白质样品(比如抗体类药物)时,MALDI-TOF无法测得精确分子量,更不用说对蛋白质的糖基化等修饰形式进行分析。 (1) 抗体类蛋白质药物的精确分子量测定 抗体类蛋白质药物是生物医药界非常重要的一类样品,这些蛋白质分子的分子量非常大,一般情况下150KDa左右。因此在没有高分辨率质谱仪的情况下,要对这类蛋白质进行精确分子量测定是困难的。 在高分辨率质谱仪,特别是orbitrap原理的质谱仪出现以后,抗体类蛋白质的去卷积分子量测定变得容易实现。 (2) 还原后抗体类样品的不同亚基精确分子量测定 抗体类蛋白质样品通过还原,可以将轻链和重链分开,然后通过HPLC分离,在线进行MS分析得到亚基的精确分子量。 (3) 小分子量(25KDa)蛋白质样品的精确分子量测定 常用蛋白质样品包括抗体类蛋白质(150 KDa),同时也包括一些相对较小的蛋白质分子。对着这些相对较小的蛋白质,进行[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]分析,并去卷积分析得到精确分子量,不需要太高的分辨率即可实现(早期的离子阱,如LTQ就可以实现对小分子量蛋白质的分子量测定)。 高分辨率质谱可以对蛋白质样品(约10-150KDa)进行精确分子量测定,精度达到1Da左右,可以满足分析蛋白质的修饰状态(比如糖基化、磷酸化、氧化、C末端K缺失情况等),并可以对这些修饰情况进行定量分析
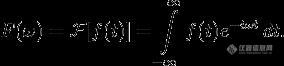
在介绍Orbitrap之前需要先简单介绍傅里叶变化的数据采集模式和傅立叶变换离子回旋共振质谱(FTICR)。 傅里叶变换是是一种线性的积分变换。连续傅里叶变换将平方可积的函数f(t)表示成复指数函数的积分或级数形式。http://ng1.17img.cn/bbsfiles/images/2011/10/201110301957_327268_2265735_3.gif这是将频率域的函数F(ω)表示为时间域的函数f(t)的积分形式。连续傅里叶变换的逆变换 (inverse Fourier transform)为http://ng1.17img.cn/bbsfiles/images/2011/10/201110301957_327269_2265735_3.gif 这种数据采集方式最成功的应用是核磁共振仪(NMR),恩斯特因为在傅里叶变换NMR的贡献获得诺贝尔奖。简短的说就是在核磁中用一个短而强的脉冲瞬时激发所有核,取代连续波照射(原连续波NMR),收集这些信号,把时间谱变换为频谱(这些激发和数据采集的过程设计到傅里叶变换,我也不懂,感兴趣的版友可以自己阅读文献,鼓励与大家共享),利用快速傅里叶变换缩短了采样时间和检测灵敏度。生物质谱需要高的灵敏度和快速扫描速度来满足高通量分析要求,傅里叶变换离子回旋共振质谱(FTICR)和Orbitrap的神奇之处在于他们采用傅里叶变化模式采集数据,检测分子质量,拥有高的分辨率和质量精度。 傅里叶变换离子回旋共振质谱(FTICR)拥有超高的分辨率和精确的质量准确度,同时它也可以完全兼用CID,ECD,ETD等多种模式产生的多级质谱,所以傅立叶变换离子回旋共振质谱(FTICR)是从头开始(top-down)蛋白组学的理想检测工具。但是傅立叶变换离子回旋共振质谱(FTICR)是昂贵的质谱,体积庞大和巨额的运行维护费用让FTICR一直为少数科学家和大型实验所应用。2000年出现的新质谱——静电轨道阱质谱(Orbitrap)在一些实验中几乎可以达到傅立叶变换离子回旋共振质谱(FTICR)一样的高分辨率和质量准确度。 Orbitrap质量分析器工作时,两个电极之间形成静电场。当高速运动带电离子进入Orbitrap内,在静电作用下围绕中心电极做圆周轨道运动,不同的离子在z方向形成不同频率ωz与(m/z)1/2 成正比。检测器检测离子运动形成的电势,经过信号放大和快速傅立叶变换后形成频谱,经过处理最后形成质谱。在2005年,Thermo公司推出商品化的静电轨道阱质谱——LTQ-Orbitrap线性Orbitrap价格相比傅立叶变换离子回旋共振质谱(FTICR)便宜很多,使用维护方便。Orbitrap质量分析器形状如同纺椎,纺椎内有一个内心电极,两个半纺锥体构成外套电极,质离子阱静电轨道阱串联质谱。(图1)线性离子阱和Orbitrap由双曲面四级杆C-trap连接,C-trap把线性离子阱快速扫描的离子或二级质谱产生的离子聚焦推入Orbitrap进行高分辨的质量分析。LTQ-Orbitrap在蛋白组学已经获得了比较成功的应用,在高通量蛋白样品鉴定和磷酸化蛋白组学有一定的优势。http://ng1.17img.cn/bbsfiles/images/2011/10/201110301959_327270_2265735_3.gif图1线性离子阱静电轨道阱联用质谱仪(LTQ-Orbitrap)。a质谱仪组合装置示意图。b静电场轨道阱示意图。(引自自Thermo宣传资料)
质谱技术在蛋白鉴定等实验中具有不可忽视的作用,应用前景十分广泛。那么,有问题了怎么解决呢?问题1. 一级质谱和二级质谱有什么区别?什么时候做一级,什么时候做二级?答:一级质谱鉴定的方式主要指胎指纹图谱(peptide-mass mapping, PMF),即利用质谱仪精确测量酶解片段的分子量并搜库比较实现蛋白质的鉴定,二级质谱是在一级质谱的基础上再选择部分肽段做进一步的破碎并对碎片进行深入分析和比较,鉴定出该肽段的序列并结合PMF的结果从而实现蛋白质的鉴定。二级质谱能够得到部分肽短的序列,具有更高的可靠性。随着现在杂志对数据的要求越来越严格,二级质谱鉴定是蛋白鉴定的大趋势,而且即使目前做一级质谱鉴定的结果,也需要挑选部分PMF结果做二级质谱验证。问题2. 研究的物种不是模式生物怎么办?答:可以参考亲缘关系最近的模式生物做比对而实现蛋白质的成功鉴定,如果质谱图很好而没有鉴定结果说明这是一个全新的蛋白,可以采用de-novo等技术做深入分析与鉴定。问题3. 该如何评价质谱效果的好坏?答:做PMF一般得分超过60分(P0.05)就算成功鉴定,而串联质谱,得分超过60分或者虽然没有超过60分,但是有最少一条肽段的得分超过30分就算成功鉴定。问题4. 一些特殊的质谱方法有什么用途?答:质谱的其它用途包括修饰位点分析、蛋白测序、混合蛋白鉴定以及分子量精确测定、二硫键位置分析等等。问题5. 用什么染色方法比较好?答:最好用考马斯亮蓝法进行染色,银染也可以,但鉴定成功率稍低,并且推荐用串联质谱对银染蛋白进行鉴定可以大大提高鉴定成功率。问题6 质谱鉴定取胶点有什么注意事项?答:离心管最好用进口离心管,以免塑料污染;水最好用去离子水或者双蒸水;取点的时候带好口罩与手套,以免角蛋白污染。问题7. 凝胶是否可以长期保存?该如何保存?如何运送?答:蛋白凝胶可以长期保存而不影响质谱鉴定效果,一般而言,如果在一两个星期以内,最好用保鲜膜包好,放到4度冰箱保存,如果保存时间超过一个月,可以把蛋白点取下后放入-20度或者-80度冰箱,不会影响后续质谱鉴定效果。运送胶点的时候采用常温运送即可,三五天内都不会有太大的影响。问题8. 质谱鉴定大致是什么流程?质谱鉴定主要包括蛋白酶解、质谱数据获取、对库检索三个步骤。问题9. 串联质谱鉴定和质谱测序有什么区别?质谱鉴定往往采用软件对已有数据库进行自动检索匹配得到结果,而质谱测序则需要根据质谱峰图中相邻或者相近峰的分子量差异直接推算出肽段的序列。问题10. 未知蛋白质是通过质谱还是蛋白质测序仪来测序的呢?现在比较简单的方法是质谱法。如果质谱法不能确定的话还可以结合N端测序,可测10几个氨基酸。两个数据结合分析基本可以确定目的蛋白了,现在的蛋白质组数据库相当强大了。不知道看完这10个FAQ,各位有没有些许受益,如果还有好的想法或者意见,欢迎给小编留言!(来源:互联网)
Methods 35 (2005) 256–264[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=88153]analysis of protein phosphorylation by mass spectrometry[/url]
[color=#333333]质谱鉴定样品对蛋白的染色方法要求是什么?[/color]
各位老师们好,我目前需要进行一个磷酸盐孵育实验,使用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]检测孵育产物的浓度。但是因为磷酸盐对质谱伤害较大,故前处理方法我想使用甲基叔丁基醚进行液液萃取,想请教一下各位老师磷酸盐会在萃取的时候进入 MTBE 中吗,该前处理方法是否会对仪器有影响呢,谢谢各位老师。
19世纪末“正电荷粒子束在磁场中发生偏转”被发现后,1912年世界上第一台质谱仪在英国面世,从此一种通过测量离子电荷质量比,而进行样品成分和结构分析的方法在生物学及医学上大放异彩。质谱以其灵敏度高、特异性强、分析速度快、多指标同时检测等特点跻身高端定量检测分析仪器行列。 分辨率、灵敏度、质量范围、质量测定准确性是衡量质谱的主要技术指标。分辨率R是指相邻两个峰被分离的程度,是质谱仪区别两个峰的能力指标。灵敏度的指标实际上是仪器综合性能的反映,因为它与样品、分辨率、扫描速度、进样方式以及电离方式密切相关。磁质谱仪器的质量范围与加速电压有关,在仪器最高加速电压下可测的最高值为范围指标,加速电压降低,范围加大,但灵敏度下降。 质谱工作原理,是将样品分子经过离子化后,利用其不同质荷比(m/z)的离子在静电场或磁场中受到的作用力不同而改变运动方向,使其在空间上分离,最后通过收集和检测这些离子得到质谱图谱,实现成分和结构分析。 [b]质谱仪虽种类繁多, 但每种仪器结构可概括为以下6部分:[/b] 1.进样口:直接进样或接其他仪器,用于样品的引入。 2.真空系统:用于维持质量分析器至检测器部分的高真空状态,使离子能够在电磁场作用下自由飞翔,避免离子在运动途中发生碰撞,导致信号丢失或产生虚假信号。 3.离子源:用于将样品离子化。 4.质量分析器:用于将不同质荷比的离子分离开,让他们逐个进入检测器,或只筛选特定质荷比的离子进入检测器。 5.检测器:通常是电子倍增管或其他,将离子的数量转化为电信号的大小。 6.数据处理系统:处理检测器捕获到的电信号,获得质谱图,并进一步处理得到所需信息。 质谱种类多,应用广。从用途(分析对象)可分为:无机质谱、有机质谱、同位素质谱及气体质谱等。从单机或组合可分为:单(一)质谱、串联质谱,单一质谱两个及以上的组合即为串联质谱。广泛应用于化合物结构的定性测定或混合物组成的定量测定。飞行时间质谱仪(MADLI-TOFMS)归类于有机质谱,可应用于临床微生物(包括细菌和真菌)的高通量快速鉴定、疾控中心的微生物传染病原的鉴定与监测、海关进出口商品的检验检疫、食品生产中的微生物检测和工业、农业和环境中的细菌监测等领域。 目前,服务于临床诊疗的质谱检测项目已达400余项,主要涉及临床化学、临床免疫学以及临床微生物鉴定等领域,也被用于建立临床化学检测项目的参考测量程序和研制参考物质。欧美发达国家从1961开始将质谱技术用于新生儿筛查,目前实现使用串联质谱技术对多个代谢产物进行联合检测,可筛查新生儿遗传代谢病等30种新生儿遗传代谢疾病。国内质谱的临床检测主要用于新生儿遗传筛查、维生素D检测、微生物诊断、药品检测等检测领域。 相比国外100多年的质谱发展历史,受限于国际离子源与质量分析器的核心专利知识产权保护,国产质谱设备发展备受制约,直到2000年后国内企业才逐步开始质谱技术的积累。从2006年第一台国产商业化质谱——四级杆[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质联用仪[/color][/url]问世,到17年7月国家质量监督检验检疫总局和中国国家标准化管理委员会发布,18年2月份开始实施的推荐性国标——质谱仪通用规范。短短十年时间,以安图生物为代表的6家国产IVD生产企业陆续推出MALDI-TOF 质谱仪,逐步打破以进口品牌垄断为主的中国质谱格局,努力弥补当前国产质谱仪占有率相对较低,2016年抽样调查中[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]及[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GC-MS[/color][/url]国产化率均不到2%的差距,全力推进MALDI-TOF MS质谱在临床微生物检测领域的发展。[align=center][img=1.jpg]https://i4.antpedia.com/attachments/att/image/20200602/1591081536537269.jpg[/img][/align] 众所周知,微生物诊断指的是通过病原学和药物敏感性分析为临床传染性疾病的预防、诊断、治疗与疗效观察提供依据。传统微生物快速诊断包括三种方法: 1.样品的直接检测,例如[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]检测; 2.菌体富集后检测; 3.分离培养后检测。 传统的生物化学、分子生物学和形态学等方法基于单菌落的生化特征需要菌种的筛选、培养、鉴定等过程,实验时间需要数天不等,耗时耗力,且实验操作较为繁琐,并不能满足临床对检测结果时效性的要求;分子生物学方法进行微生物鉴定大大地提高了灵敏度和时效性,但对工作人员技术要求高,检测成本高,仅针对某些特定细茵,难以满足临床常规要求。因而,样本流转(TAT)时间长仍然是当前制约临床微生物检验发展的主要因素之一。MALDI-TOF MS质谱仪可实现临床对部分微生物传统检测方法的技术替代,通过对未知化合物(菌)所得谱图的分析,进而解析出化合物结构。MALDI-TOF MS快速鉴定经固(液)体培养基短时培养的阳性血培养物中的病原菌,且一次实验可同时多个样本检测,准确率与检测通量均有大幅的提升,一定程度上节省了人力和财力,可适用于微生物室日常工作的血培养阳性标本快速鉴定的方法。从而助力临床微生物检验在感染性疾病诊断、临床用药指导、抗菌药物管理、院内感染控制等多方面均衡发展,将彻底改变微生物实验室的面貌。[align=center][img=1.jpg]https://i4.antpedia.com/attachments/att/image/20200602/1591081550562115.jpg[/img][/align][align=center][font=黑体, SimHei]图.全自动微生物质谱检测系统[/font][/align][align=center][font=黑体, SimHei](Automated Mass Spectrometry Microbial Identification System)[/font][/align] 飞行时间质谱仪的质量分析器是一个离子漂移管。由离子源产生的离子加速后进入无场漂移管,并以恒定速度飞向离子接收器。离子质量越大,到达接收器所用时间越长,离子质量越小,到达接收器所用时间越短,根据这一原理,可以把不同质量的离子按m/z值大小进行分离。质谱图,横轴表示单位电荷质量(m/z);纵轴表示离子流强度,通常以相对强度(相对丰度)来表示。相对丰度以最强的离子流强度定义为100%,其他离子流以其百分比显示。 进样系统、基质辅助激光解吸电离离子源、飞行时间质量分析器、传感器和电脑是临床微生物鉴定的 MALDI—TOFMS主要组成部分。MALDI—TOFMS鉴定微生物的标志物主要是特异性保守核糖体蛋白。MALDI—TOFMS基于微生物蛋白指纹图谱的特异性峰谱进行鉴定,只需将细菌涂布于靶板,加入基质溶液裂解,室温干燥后即上机检测,获取的质量图谱与数据库中的标准图谱进行自动对比分析,即可获得鉴定结果。鉴定结果全程自动判读、自动分析、自动报告、标本自动卸载,20分钟内可完成96个菌株的鉴定,且检测成本低,仪器使用耗材只需样品板和质谱专用基质,无须其他任何附加试剂,对工作人员的技术要求不高。 有研究证实,在重症监护室(ICU)临床治疗中,抗生素如果晚一小时准确治疗,病人存活率下降8%。而运用质谱检测技术则可缩短至少1.5天的鉴定时间,为临床救治危急重症患者赢得更多时间。除单一质谱外,串联质谱在美国及欧盟国家商业化应用相对成熟的主要是药物浓度监测、小分子标志物检测、新生儿筛查和维生素检测等。国内除目前已实现商业化的微生物鉴定、新生儿筛查、维生素等临床检测领域外,应拓展质谱在血药浓度监测领域的绝对优势;紧抓质谱在小分子生物标志物在心脑血管和代谢病方面的发展趋势,质谱仪因能敏锐地分析其他设备仪器难以分析的肿瘤生长分泌的微量外泌体,在癌症的液体活检领域,质谱检测也有望跟基因检测分一杯羹。 质谱作为一个能同时检测大量的化合物的分析器,有望开启IVD检测发展的新篇章。从1953年飞行时间质谱仪原型被设计出,到1955年世界上第一台飞行时间质谱仪诞生,再到国产飞行时间质谱迅猛发展,随着临床对个体化和精准化医疗需求的增加,基于质谱技术的基因组学、蛋白组学、代谢组学等很多研究成果正不断转化至临床实践,值得我们翘首以盼。 中国质谱仪过去面临着4大挑战,技术发展水平的挑战、进口产品替代的挑战、知识产权保护的挑战以及做强、做大与做大、做强之间的挑战。未来希望国内的质谱仪企业抓住全球市场需求增长率超过10%,以及中国市场远超10%的需求增长,结合市场需求和实际情况,通过自身的努力,将更多精良的产品投入到市场中,从而推动中国质谱行业的快速发展。 参考文献: [1]中国临床微生物质谱共识专家组.中国临床微生物质谱应用专家共识[J]. 中华医院感染学杂志,2016,26(10) [2]李永军,Sihe Wang.[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-质谱联用技术临床应用[M].上海科学技术出版社 [3]中国质量检测设备摸底调研.分析测试百科网.中金公司研究部
[b]仪器信息网讯[/b] 2010年全国质谱大会曁第三届世界华人质谱研讨会将于7月30日在长春国际会展中心正式拉开序幕。在开幕的前一天,大会主办单位邀了中科院化学所的王光辉研究员、中国医科院基础医学研究所的李智立研究员、复旦大学的陆豪杰教授、北京协和医院的胡蓓教授以及沃特世公司和安捷伦公司的工程师分别进行了内容新颖的质谱技术培训讲座,使广大参会人员在其相关领域的质谱技术上得到了启迪和可借鉴的经验。培训讲座由中科院长春应化所的刘淑莹研究员主持。[align=center][img]http://bimg.instrument.com.cn/lib/editor/UploadFile/20107/201073051322457.jpg[/img][/align][align=center]质谱技术培训讲座现场[/align][align=center][img]http://bimg.instrument.com.cn/lib/editor/UploadFile/20107/201073074547744.jpg[/img][/align][align=center]王光辉研究员就小分子的激光电离研究进展进行讲解[/align] 来自中科院化学所的王光辉研究员给大家进行了题为《小分子的激光电离研究进展》的讲座。王光辉研究员具体介绍了MALDI中利用不同表面物理形态的靶(如多空硅及硅纳米丝)及不同基质(如铅笔芯及质子海面)检测小分子物质的方法和实例,并根据其导电性影响,给大家介绍了多种不同材质的样品靶,如聚四氟乙烯、胶带、陶瓷等。王老师的试验方法及结果很好的证明了MALDI进行小分子检测的能力,拓宽了MALDI检测的分子量范围,给大家在进行小分子检测时增加了新的思路和适用方法。[align=center][img]http://bimg.instrument.com.cn/lib/editor/UploadFile/20107/201073074622988.jpg[/img][/align][align=center]李智立研究员介绍傅里叶离子回旋共振质谱仪(FTICR-MS)在生物医学中的应用[/align] 接着,来自中国医科院基础医学研究所的李智立研究员就傅里叶离子回旋共振质谱仪(FTICR-MS)在生物医学中的应用给大家进行了详细的讲解。李老师具体介绍了FTICR-MS的原理及其主要功能,以及它在生物大分子、有机小分子及代谢产物和组织成像等领域中的主要应用和当前存在的问题。[align=center][img]http://bimg.instrument.com.cn/lib/editor/UploadFile/20107/2010730581960.jpg[/img][/align][align=center]陆豪杰教授介绍质谱大规模研究肿瘤蛋白质标志物的新技术新方法[/align] 复旦大学化学系的陆豪杰教授给参会人员介绍了质谱大规模研究肿瘤蛋白质标志物的新技术新方法。陆博士肯定了蛋白质组学在转化医学中所处的核心地位,蛋白质是肿瘤最主要的标志物,目前基于质谱的分析方法是目前大规模筛选肿瘤标志物的最有效手段。陆博士继而介绍了他们建立的复合材料富集低含量蛋白质、痕量蛋白质酶解、复合纳米材料富集糖蛋白、化学修饰磷酸化蛋白质这四种质谱分析新方法。[align=center][img]http://bimg.instrument.com.cn/lib/editor/UploadFile/20107/20107305823579.jpg[/img][/align][align=center]胡蓓教授介绍质谱技术在临床药理研究中的应用[/align] 来自协和医院的胡蓓教授给参会人员介绍了质谱技术在临床药理研究中的应用。胡教授主要介绍了他们正在进行的PK和PD/PK研究及其延伸性研究进展,以及药物的生物转化研究等内容。在定量分析方法学问题上,胡教授介绍了在临床研究中为保证生物标本定量分析的安全性和可靠性所需要符合的各项规范及其相关考核内容。[align=center][img]http://bimg.instrument.com.cn/lib/editor/UploadFile/20107/20107305949266.jpg[/img][/align][align=center]沃特世公司丁雁灵博士介绍SYNAPT G2 HDMS的离子淌度 高清质谱技术及应[/align][align=center][img]http://bimg.instrument.com.cn/lib/editor/UploadFile/20107/201073051010884.jpg[/img][/align][align=center]Agilent的王颖博士介绍安捷伦超高解析度质谱技术在药物代谢中的应用[/align] 除了以上4专家以外,来自沃特世公司丁雁灵博士和来自安捷伦公司的王颖博士也分别就SYNAPT G2 HDMS的离子淌度高清质谱技术及应用和安捷伦超高解析度质谱技术在药物代谢中的应用这两个主题进行了仪器介绍及相关实例讲解。SYNAPT G2 HDMS显示出了其优秀的分离及检测能力,而安捷伦超高解析度质谱的代谢产物鉴定软件可根据数据进行评分,并进行分子特征提取,大大提高了代谢产物选择的准确性。[url]http://www.instrument.com.cn/news/20100730/045713.shtml[/url]
简述[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质联用[/color][/url]分析时质谱仪漏气部位的鉴定方法?通常采用什么方法检测离子源室的真空状态?为什么?我们的测试题,请大家不要给我讲现在市面上用什么仪器,谢谢大家了!
19世纪末“正电荷粒子束在磁场中发生偏转”被发现后,1912年世界上第一台质谱仪在英国面世,从此一种通过测量离子电荷质量比,而进行样品成分和结构分析的方法在生物学及医学上大放异彩。质谱以其灵敏度高、特异性强、分析速度快、多指标同时检测等特点跻身高端定量检测分析仪器行列。 分辨率、灵敏度、质量范围、质量测定准确性是衡量质谱的主要技术指标。分辨率R是指相邻两个峰被分离的程度,是质谱仪区别两个峰的能力指标。灵敏度的指标实际上是仪器综合性能的反映,因为它与样品、分辨率、扫描速度、进样方式以及电离方式密切相关。磁质谱仪器的质量范围与加速电压有关,在仪器最高加速电压下可测的最高值为范围指标,加速电压降低,范围加大,但灵敏度下降。 质谱工作原理,是将样品分子经过离子化后,利用其不同质荷比(m/z)的离子在静电场或磁场中受到的作用力不同而改变运动方向,使其在空间上分离,最后通过收集和检测这些离子得到质谱图谱,实现成分和结构分析。 质谱仪虽种类繁多, 但每种仪器结构可概括为以下6部分: 1.进样口:直接进样或接其他仪器,用于样品的引入。 2.真空系统:用于维持质量分析器至检测器部分的高真空状态,使离子能够在电磁场作用下自由飞翔,避免离子在运动途中发生碰撞,导致信号丢失或产生虚假信号。 3.离子源:用于将样品离子化。 4.质量分析器:用于将不同质荷比的离子分离开,让他们逐个进入检测器,或只筛选特定质荷比的离子进入检测器。 5.检测器:通常是电子倍增管或其他,将离子的数量转化为电信号的大小。 6.数据处理系统:处理检测器捕获到的电信号,获得质谱图,并进一步处理得到所需信息。 质谱种类多,应用广。从用途(分析对象)可分为:无机质谱、有机质谱、同位素质谱及气体质谱等。从单机或组合可分为:单(一)质谱、串联质谱,单一质谱两个及以上的组合即为串联质谱。广泛应用于化合物结构的定性测定或混合物组成的定量测定。飞行时间质谱仪(MADLI-TOFMS)归类于有机质谱,可应用于临床微生物(包括细菌和真菌)的高通量快速鉴定、疾控中心的微生物传染病原的鉴定与监测、海关进出口商品的检验检疫、食品生产中的微生物检测和工业、农业和环境中的细菌监测等领域。 目前,服务于临床诊疗的质谱检测项目已达400余项,主要涉及临床化学、临床免疫学以及临床微生物鉴定等领域,也被用于建立临床化学检测项目的参考测量程序和研制参考物质。欧美发达国家从1961开始将质谱技术用于新生儿筛查,目前实现使用串联质谱技术对多个代谢产物进行联合检测,可筛查新生儿遗传代谢病等30种新生儿遗传代谢疾病。国内质谱的临床检测主要用于新生儿遗传筛查、维生素D检测、微生物诊断、药品检测等检测领域。 相比国外100多年的质谱发展历史,受限于国际离子源与质量分析器的核心专利知识产权保护,国产质谱设备发展备受制约,直到2000年后国内企业才逐步开始质谱技术的积累。从2006年第一台国产商业化质谱——四级杆[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质联用仪[/color][/url]问世,到17年7月国家质量监督检验检疫总局和中国国家标准化管理委员会发布,18年2月份开始实施的推荐性国标——质谱仪通用规范。短短十年时间,以安图生物为代表的6家国产IVD生产企业陆续推出MALDI-TOF 质谱仪,逐步打破以进口品牌垄断为主的中国质谱格局,努力弥补当前国产质谱仪占有率相对较低,2016年抽样调查中[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]及[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GC-MS[/color][/url]国产化率均不到2%的差距,全力推进MALDI-TOF MS质谱在临床微生物检测领域的发展。 众所周知,微生物诊断指的是通过病原学和药物敏感性分析为临床传染性疾病的预防、诊断、治疗与疗效观察提供依据。传统微生物快速诊断包括三种方法: 1.样品的直接检测,例如[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]检测; 2.菌体富集后检测; 3.分离培养后检测。 传统的生物化学、分子生物学和形态学等方法基于单菌落的生化特征需要菌种的筛选、培养、鉴定等过程,实验时间需要数天不等,耗时耗力,且实验操作较为繁琐,并不能满足临床对检测结果时效性的要求;分子生物学方法进行微生物鉴定大大地提高了灵敏度和时效性,但对工作人员技术要求高,检测成本高,仅针对某些特定细茵,难以满足临床常规要求。因而,样本流转(TAT)时间长仍然是当前制约临床微生物检验发展的主要因素之一。MALDI-TOF MS质谱仪可实现临床对部分微生物传统检测方法的技术替代,通过对未知化合物(菌)所得谱图的分析,进而解析出化合物结构。MALDI-TOF MS快速鉴定经固(液)体培养基短时培养的阳性血培养物中的病原菌,且一次实验可同时多个样本检测,准确率与检测通量均有大幅的提升,一定程度上节省了人力和财力,可适用于微生物室日常工作的血培养阳性标本快速鉴定的方法。从而助力临床微生物检验在感染性疾病诊断、临床用药指导、抗菌药物管理、院内感染控制等多方面均衡发展,将彻底改变微生物实验室的面貌。 飞行时间质谱仪的质量分析器是一个离子漂移管。由离子源产生的离子加速后进入无场漂移管,并以恒定速度飞向离子接收器。离子质量越大,到达接收器所用时间越长,离子质量越小,到达接收器所用时间越短,根据这一原理,可以把不同质量的离子按m/z值大小进行分离。质谱图,横轴表示单位电荷质量(m/z);纵轴表示离子流强度,通常以相对强度(相对丰度)来表示。相对丰度以最强的离子流强度定义为100%,其他离子流以其百分比显示。 进样系统、基质辅助激光解吸电离离子源、飞行时间质量分析器、传感器和电脑是临床微生物鉴定的 MALDI—TOFMS主要组成部分。MALDI—TOFMS鉴定微生物的标志物主要是特异性保守核糖体蛋白。MALDI—TOFMS基于微生物蛋白指纹图谱的特异性峰谱进行鉴定,只需将细菌涂布于靶板,加入基质溶液裂解,室温干燥后即上机检测,获取的质量图谱与数据库中的标准图谱进行自动对比分析,即可获得鉴定结果。鉴定结果全程自动判读、自动分析、自动报告、标本自动卸载,20分钟内可完成96个菌株的鉴定,且检测成本低,仪器使用耗材只需样品板和质谱专用基质,无须其他任何附加试剂,对工作人员的技术要求不高。 有研究证实,在重症监护室(ICU)临床治疗中,抗生素如果晚一小时准确治疗,病人存活率下降8%。而运用质谱检测技术则可缩短至少1.5天的鉴定时间,为临床救治危急重症患者赢得更多时间。除单一质谱外,串联质谱在美国及欧盟国家商业化应用相对成熟的主要是药物浓度监测、小分子标志物检测、新生儿筛查和维生素检测等。国内除目前已实现商业化的微生物鉴定、新生儿筛查、维生素等临床检测领域外,应拓展质谱在血药浓度监测领域的绝对优势;紧抓质谱在小分子生物标志物在心脑血管和代谢病方面的发展趋势,质谱仪因能敏锐地分析其他设备仪器难以分析的肿瘤生长分泌的微量外泌体,在癌症的液体活检领域,质谱检测也有望跟基因检测分一杯羹。 质谱作为一个能同时检测大量的化合物的分析器,有望开启IVD检测发展的新篇章。从1953年飞行时间质谱仪原型被设计出,到1955年世界上第一台飞行时间质谱仪诞生,再到国产飞行时间质谱迅猛发展,随着临床对个体化和精准化医疗需求的增加,基于质谱技术的基因组学、蛋白组学、代谢组学等很多研究成果正不断转化至临床实践,值得我们翘首以盼。 中国质谱仪过去面临着4大挑战,技术发展水平的挑战、进口产品替代的挑战、知识产权保护的挑战以及做强、做大与做大、做强之间的挑战。未来希望国内的质谱仪企业抓住全球市场需求增长率超过10%,以及中国市场远超10%的需求增长,结合市场需求和实际情况,通过自身的努力,将更多精良的产品投入到市场中,从而推动中国质谱行业的快速发展