
来源:药品质量研究对于色谱的分离,相信绝大多数的色谱工作者都能信手拈来各种分离的方式。但是对于色谱的基础理论,相信很多小伙伴都跟小编一样,在毕业的那一刻就还给老师了。那么今天,请大家跟着小编一起,重新梳理回忆一下当年校园的那些“你侬我侬”外的学习基础。 塔板理论作为色谱学中的一个重要理论,至今延用不衰,为广大色谱工作者所承认。塔板理论是1941年马丁(Martin)和辛格(Synge)建立的,它是一个半经验理论,并初步揭示了色谱分离过程。塔板理论将色谱分离过程比作蒸馏过程,将连续的色谱分离过程分割成多次平衡过程的重复(类似于蒸馏塔塔板上的平衡过程);假想色谱柱由许多块塔板组成,在每个理论塔板内的空间由流动相和固定相两部分占据。[align=center][img=,232,323]http://ng1.17img.cn/bbsfiles/images/2018/02/201802111354557128_5738_1610895_3.jpg!w232x323.jpg[/img][/align]为简化起见,塔板理论有如下假设:(a)在每一个平衡过程间隔内,平衡可以迅速达到;(b)流动相进入色谱柱是脉动(间歇)过程,每次进入柱中的体积为一个塔板体积;(c)所有组分开始都集中在第零号塔板上,且组分沿色谱柱方向的纵向扩散可忽略;(d)分配系数在所有塔板上都为常数,与组分在塔板中浓度无关。[align=center][img=,84,281]http://ng1.17img.cn/bbsfiles/images/2018/02/201802111355387985_2923_1610895_3.jpg!w84x281.jpg[/img][/align]根据上述假定,在色谱分离过程中,该组分的分布可计算如下:开始时,若有单位质量,即m=1(例1mg或1μg)的该组分加到第0号塔板上,分配平衡后,由于k=1,即n[sub]s[/sub]=n[sub]m[/sub]故n[sub]m[/sub]=n[sub]s[/sub]=0.5。当一个板体积(lΔV)的流动相以脉动形式进入0号板时,就将流动相中含有n[sub]m[/sub]部分组分的流动相顶到1号板上,此时0号板固定相中n[sub]s[/sub]部分组分及1号板[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]中的n[sub]m[/sub]部分组分,将各自在两相间重新分配。故0号板上所含组分总量为0.5,其中液固两相各为0.25而1号板上所含总量同样为0.5。液固相亦各为0.25。以后每当一个新的板体积流动相以脉动式进入色谱柱时,上述过程就重复一次(详细的分配过程见下表)。[align=center][img=,500,345]http://ng1.17img.cn/bbsfiles/images/2018/02/201802111355564313_9465_1610895_3.jpg!w690x477.jpg[/img][/align]按上述分配过程,对于n=5,k=1,m=1的体系,随着脉动进入柱中板体积流动相的增加,组分分布在柱内任一板上的总量(液固两相中的总质量)见下表:[align=center][img=,690,464]http://ng1.17img.cn/bbsfiles/images/2018/02/201802111356266653_4218_1610895_3.jpg!w690x464.jpg[/img][/align][align=center][img=,464,680]http://ng1.17img.cn/bbsfiles/images/2018/02/201802111356437610_3828_1610895_3.jpg!w464x680.jpg[/img][/align]由塔板理论可建流出曲线方程:[align=center][img=,690,147]http://ng1.17img.cn/bbsfiles/images/2018/02/201802111357002942_7014_1610895_3.jpg!w690x147.jpg[/img][/align]m为组分质量,Vr为保留体积,n为理论塔板数。 当V=Vr 时,C值最大,即:[align=center][img=,412,156]http://ng1.17img.cn/bbsfiles/images/2018/02/201802111357126069_3254_1610895_3.jpg!w412x156.jpg[/img][/align]由流出曲线方程可推出:[align=center][img=,276,78]http://ng1.17img.cn/bbsfiles/images/2018/02/201802111357243282_3260_1610895_3.jpg!w276x78.jpg[/img][/align]而理论塔板高度(H)即:[align=center][img=,260,156]http://ng1.17img.cn/bbsfiles/images/2018/02/201802111357374972_2248_1610895_3.jpg!w260x156.jpg[/img][/align]从上两式可以看出,色谱峰W越小,n就越大,而H就越小,柱效能越高。因此,n和H是描述柱效能的指标。由于死时t0包括在t[sub]r[/sub]中,而实际的t[sub]0[/sub]不参与柱内分配,所计算的n值较大,H很小,但与实际柱效能相差甚远。所以,提出把t0扣除,采用有效理论塔板数n[sub]eff[/sub]和有效塔板高H[sub]eff[/sub]评价柱效能。[align=center][img=,432,214]http://ng1.17img.cn/bbsfiles/images/2018/02/201802111357524259_7355_1610895_3.jpg!w432x214.jpg[/img][/align]塔板理论用热力学观点形象地描述了溶质在色谱柱中的分配平衡和分离过程,导出流出曲线的数学模型,并成功地解释了流出曲线的形状及浓度极大值的位置,还提出了计算和评价柱效的参数。但由于它的某些基本假设并不完全符合柱内实际发生的分离过程,例如,纵向扩能解释造成谱带扩张的原因和影响板高的各种因素,也不能说明为什么在不同流速下可以测得不同的理论塔板数,这就限制了它的应用。 [b]塔板理论的特点和不足:[/b](a)当色谱柱长度一定时,塔板数 [i]n [/i]越大(塔板高度 [i]H [/i]越小),被测组分在柱内被分配的次数越多,柱效能则越高,所得色谱峰越窄。(b)不同物质在同一色谱柱上的分配系数不同,用有效塔板数和有效塔板高度作为衡量柱效能的指标时,应指明测定物质。(c)柱效不能表示被分离组分的实际分离效果,当两组分的分配系数[i]K[/i]相同时,无论该色谱柱的塔板数多大,都无法分离。(d)塔板理论无法解释同一色谱柱在不同的载气流速下柱效不同的实验结果,也无法指出影响柱效的因素及提高柱效的途径。
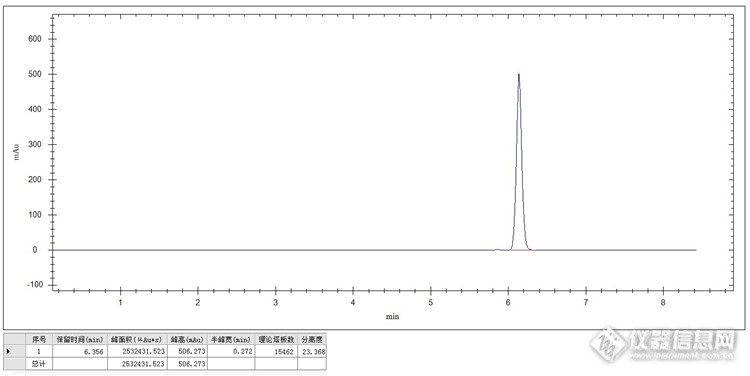
液相色谱分析重要指标之一——理论塔板数 理论塔板数是色谱分析中的一个重要参数,它来源于塔板理论。塔板理论是色谱学的基础理论,它是将色谱柱(色谱的核心部件)看作成一个分馏塔,将分离组分(被分离的样品)在分馏塔的塔板间移动,在每一个塔板内组分分子在固定相和流动相之间形成某种平衡,随着流动相的流动,组分分子不断从一个塔板移动到下一个塔板,同时形成新的平衡,直至完全被洗脱(移动)出去。 理论塔板数是反应色谱柱性能的主要参数,是表示色谱柱对样品的分离能力或是分离效率(简称柱效),常用“N”表示。通常N值越大,柱效越高,分离能力越强,分离效果就越好。 N取决于色谱柱固定相(填料)的种类、性质(粒度、粒径分布等)、填充状况、柱长、柱内径、流动相的种类和流速及测定柱效所用物质的性质。如果色谱峰形对称并符合正态分布,N可近似表示为: 理论塔板数=5.54(保留时间/半高峰宽)2,也就是N=5.54(t/w1/2)2。柱效率用理论塔板数定量的表示:N=16(t/w)2。其中,t是样品保留时间(样品从进样到峰形最高点的时间),单位秒(s),w为峰宽(该样品峰在基线处的宽度),单位厘米(cm)。 不同的色谱柱在同一色谱条件下,理论塔板数大的色谱柱柱效高。N的大小和色谱柱的柱长关系密切,色谱柱越长(塔板数越多),N值越大。 N的大小主要和色谱峰中的两个因数有关,一是保留时间,二是色谱峰宽,保留时间越长N越大,色谱峰宽越窄N越大。要想提高色谱峰的分离效果,增加N值,我们只要从这两个方面做起就足够。一是尽量延长保留时间,二是尽量减小色谱峰宽。延长保留时间方法很多,比如选择更长的色谱柱,降低色谱柱温度,减小流速(这个最好不要变,因为流速减小,色谱峰宽也会变宽,检测灵敏度也会降低,这样可能会得不偿失),适当降低流动相中有机相的含量(主要针对反相色谱)等等。减小色谱峰宽的方法也有很多,比如减小进样量,减小进样器到检测池之间管路的死体积,尤其是缩短连接管路,采用超高效液相色谱,当然采用缩短(和延长保留时间的方法正好相反)保留时间的方法也能减小色谱峰宽,但这样可能对增加N并无帮助。有些方法在改变这两个因数时相互矛盾,我们在具体操作时,可以取利避弊,争取达到最佳效果。 通常我们增加N最常采用的办法就是一是选择更长的色谱柱,二是减小进样量,实际中这两种方法是非常常见的也是非常实用的。 下面我们就用几个具体的实列,简单的说明下。 这是150mm长色谱柱色谱图效果:http://ng1.17img.cn/bbsfiles/images/2014/07/201407272352_508091_2369266_3.jpg 这是250mm长色谱柱色谱图效果:http://ng1.17img.cn/bbsfiles/images/2014/07/201407272352_508092_2369266_3.jpg 这是20ul进样量色谱图效果:http://ng1.17img.cn/bbsfiles/images/2014/07/201407272352_508094_2369266_3.jpg 这是10ul进样量色谱图效果:http://ng1.17img.cn/bbsfiles/images/2014/07/201407272352_508093_2369266_3.jpg 增加色谱柱长度和减小进样量对于增加理论塔板数效果还是不错的。对于调节其它色谱条件来改变理论塔板数过程比较复杂,结果可能存在很多不确定性,做起来难度较大,在这我暂不做比较。 另外如果色谱柱的柱效下降了,N值降低到了很低时,我们一般会选择换一根柱效高一些的能满足实验要求的色谱柱。这也是最简单,最实用的方法。但为了减少实验成本,我们不妨试试对色谱柱采用一些再生的方法,如果还不行,那也没遗憾了。 反相色谱柱分别用甲醇:水=10:90,纯甲醇(色谱纯),异丙醇(色谱纯),二氯甲烷(色谱纯)等溶剂作为流动相,依次冲洗,每种流动相流经色谱柱不少于30倍色谱柱体积。然后再以相反的次序以不少于30倍色谱柱体积冲洗。 正相色谱柱分别用正己烷(色谱纯),异丙醇(色谱纯),二氯甲烷(色谱纯),甲醇(色谱
其他讲座资料看[url=http://www.instrument.com.cn/bbs/detail.asp/threadid/1679222/forumid/25/year/2009/query/search] 学习[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]跟yuen72老师入门[/url]10个人跑步,4个人8m/s,6个人不动。平均速度是3.2,这个大家知道。但是这样跑下去,人会分成两批。为什么进入色谱柱的组分,分成固定相中的部分和流动相中的部分后,却同时流出色谱柱,成为一个色谱峰呢?这是因为组分在固定相和流动相中的平衡,是一种动态平衡。为什么进样的时候是一个浓度相等的体积,出来的时候就成了高斯分布的扣钟形呢?为了解释这个原因,1942年英国科学家Martin和Synge发表了著名的有关塔板理论的论文,解释了其中的原因,并因此获得了1952年诺贝尔化学奖。什么是塔板理论?塔板理论是由以下四个假设构成的。1、在柱内一小段长度H内,组分可以在两相间迅速达到平衡。这一小段柱长称为理论塔板高度H。2、流动相(如载气)进入色谱柱不是连续进行的,而是脉动式,每次进气为一个塔板体积(ΔVm)。3、所有组分开始时存在于第0号塔板上,而且试样沿轴(纵)向扩散可忽略。4、分配系数在所有塔板上是常数,与组分在某一塔板上的量无关。这四条假设严格讲都是不成立的。但我们知道科学需要适当进行抽象和简化,因此这样略有偏差的简化是可以接受的。偏差带来了误差,为了消除这些误差,1956年荷兰人Van Deemter提出了速率理论,对塔板理论做出了修正。塔板理论不仅仅是一个抽象的理论,它是分析色谱问题的主要出发点之一。这四条假设必须牢记在心,并在色谱出现问题的时候用来解释这些问题出现的原因。当你做到这些,你就可以自豪的说:我,色谱已经入门了。
药典通常都是规定一个目标峰的理论塔板数不得低于多少,我们在实际应用当中,柱效低了理论塔板数也会变低,不换色谱柱的情况下,你有什么办法提高峰的理论塔板数?开动你的脑筋,扒扒你的经验,说说你的可行手段吧!!!
甲烷怎么用百分数表示呀?色谱做出来的甲烷是1.36mg/m3,现在想用百分数表示,是把1.36 mg/m3换算成umol/mol,再除以10-6*100%吗?还是用1.36÷空气密度*100%呀?谢谢各位老师
GB4789.10-2016金黄色葡萄球菌检验第二法中,如果都是未检出,该如何表示呢?国标上说“如T=0,则以小于1乘以最低稀释倍数表示”。如果我最低稀释10倍,未检出,最后的表示是不是<1x10?非微生物专业,临时顶替,望各位大神路过帮忙解答一下,谢谢
柱效一般用理论塔板数来判断,理论塔板数需要用一个单分散物质进样并计算,我们可以认为溶剂峰是吸收了大气中单分散杂质而出的峰,所以可以用溶剂峰积分来计算理论塔板数,PL软件具有计算理论塔板数的功能,具体步骤如下:在GPC offline软件中打开file:///C:/Users/wen/AppData/Roaming/Foxmail/FoxmailTemp(527)/Catch(04-09-18-32-32).jpgreciewer选择最近做的一个样品在工具栏用file:///C:/Users/wen/AppData/Roaming/Foxmail/FoxmailTemp(527)/Catch8A69(04-09-18-32-32).jpg积分工具积分一个峰型对称、峰宽相对较窄并且基线无其他峰干扰的溶剂峰:选择peak summary选项卡在column length中填入相应的柱长(PL色谱柱一般是预柱50+主柱300*n,n为主柱数量),plates per Metre 50%就是理论塔板数了(PL色谱柱说明书上会有写新色谱柱的理论塔板数)file:///C:/Users/wen/AppData/Roaming/Foxmail/FoxmailTemp(527)/CatchC485(04-09-18-32-32).jpg另外,可以选择一个稳定的样品或者单标作为质控样品,测试结果与以前的结果对比看是否有较大差异,这样来判断仪器、色谱柱、标准曲线是否稳定,根据情况来判断是否需要重新标定标准曲线,如果重新标定曲线结果也不好,可以根据理论塔板数来分析是否需要更换色谱柱
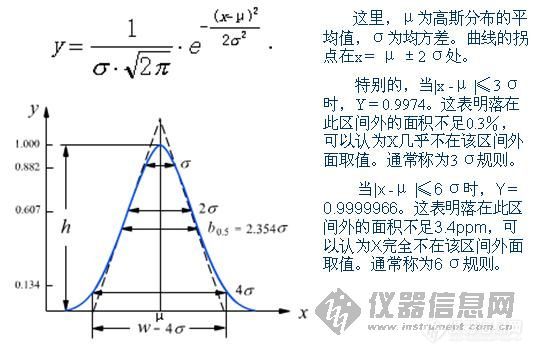
其他讲座资料看[url=http://www.instrument.com.cn/bbs/detail.asp/threadid/1679222/forumid/25/year/2009/query/search] 学习[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]跟yuen72老师入门[/url]还记得高斯分布和塔板理论的流出曲线方程么?让我们温习一下:[img]http://ng1.17img.cn/bbsfiles/images/2009/03/200903220834_139943_1641581_3.jpg[/img][img]http://ng1.17img.cn/bbsfiles/images/2009/03/200903220834_139944_1641581_3.jpg[/img]很明显,他们是同一类函数。因此他们的指数应该是统一的。我们把流出曲线方程变化到标准方程,来看看有什么结果。首先统一指数部分:[img]http://ng1.17img.cn/bbsfiles/images/2009/03/200903220850_139945_1641581_3.jpg[/img]第一:让分子部分参数统一,即:平均值u = 保留体积(时间)Vr 。也就是说,色谱流出曲线最大值的横坐标等于保留体积(时间)。第二:让分母部分参数统一,即:[img]http://ng1.17img.cn/bbsfiles/images/2009/03/200903220855_139946_1641581_3.jpg[/img],由于高斯曲线宽度W为4σ,因此色谱峰宽W与理论塔板数之间存在关系:[img]http://ng1.17img.cn/bbsfiles/images/2009/03/200903220858_139947_1641581_3.jpg[/img]其次,让我们来看看系数部分,显然系数应该是色谱流出曲线的最大值,也就是色谱峰高h。它和进样量m成正比,和保留体积Vr成反比,和理论塔板数n成正比。这个叙述正确么?从表面看是正确的,但需要深入分析。
直读光谱仪为什么可以用质量分数表示?昨天遇到一客户提出,可以接收碳硫分析仪、ICP用%表示,由于他们用天平称取了重量,但是直读光谱仪不能理解为什么是质量分数表示?这客户外行啊!
新买了一根色谱柱,按照出厂检验报告对柱子进行测试,其理论塔板数比报告中高出一倍,检测样品时,出峰时间稳定,但峰面积、峰高、峰面积所占百分数都不稳定,峰面积、峰高相差将近3-4倍,请问理论塔板数对这些有影响吗?
一、基本概念和术语1.色谱图和峰参数Ø 色谱图(chromatogram)——样品流经色谱柱和检测器,所得到的信号-时间曲线,又称色谱流出曲线(elution profile)。Ø 基线(base line)——经流动相冲洗,柱与流动相达到平衡后,检测器测出一段时间的流出曲线。一般应平行于时间轴。Ø 噪音(noise)——基线信号的波动。通常因电源接触不良或瞬时过载、检测器不稳定、流动相含有气泡或色谱柱被污染所致。Ø 漂移(drift)——基线随时间的缓缓变化。主要由于操作条件如电压、温度、流动相及流量的不稳定所引起,柱内的污染物或固定相不断被洗脱下来也会产生漂移。Ø 色谱峰(peak)——组分流经检测器时响应的连续信号产生的曲线。流出曲线上的突起部分。正常色谱峰近似于对称形正态分布曲线(高斯Gauss曲线)。不对称色谱峰有两种:前延峰(leading peak)和拖尾峰(tailing peak)。前者少见。Ø 拖尾因子(tailing factor,T)——T=,用以衡量色谱峰的对称性。也称为对称因子(symmetry factor)或不对称因子(asymmetry factor)。《中国药典》规定T应为0.95~1.05。T<0.95为前延峰,T>1.05为拖尾峰。Ø 峰底——基线上峰的起点至终点的距离。Ø 峰高(peak height,h)——峰的最高点至峰底的距离。Ø 峰宽(peak width,W)——峰两侧拐点处所作两条切线与基线的两个交点间的距离。W=4σØ 半峰宽(peak width at half-height,Wh/2)——峰高一半处的峰宽。Wh/2=2.355σØ 标准偏差(standard deviation,σ)——正态分布曲线x=±1时(拐点)的峰宽之半。正常峰的拐点在峰高的0.607倍处。标准偏差的大小说明组分在流出色谱柱过程中的分散程度。σ小,分散程度小、极点浓度高、峰形瘦、柱效高;反之,σ大,峰形胖、柱效低。Ø 峰面积(peak area,A)——峰与峰底所包围的面积。A=×σ×h=2.507 σ h=1.064 Wh/2 h2.定性参数(保留值)Ø 死时间(dead time,t0)——不保留组分的保留时间。即流动相(溶剂)通过色谱柱的时间。在反相HPLC中可用苯磺酸钠来测定死时间。Ø 死体积(dead volume,V0)——由进样器进样口到检测器流动池未被固定相所占据的空间。它包括4部分:进样器至色谱柱管路体积、柱内固定相颗粒间隙(被流动相占据,Vm)、柱出口管路体积、检测器流动池体积。其中只有Vm参与色谱平衡过程,其它3部分只起峰扩展作用。为防止峰扩展,这3部分体积应尽量减小。V0=F×t0(F为流速)Ø 保留时间(retention time,tR)——从进样开始到某个组分在柱后出现浓度极大值的时间。Ø 保留体积(retention volume,VR)——从进样开始到某组分在柱后出现浓度极大值时流出溶剂的体积。又称洗脱体积。VR=F×tRØ 调整保留时间(adjusted retention time,t'R)——扣除死时间后的保留时间。也称折合保留时间(reduced retention time)。在实验条件(温度、固定相等)一定时,t'R只决定于组分的性质,因此,t'R(或tR)可用于定性。t'R=tR-t0Ø 调整保留体积(adjusted retention volume,V'R)——扣除死体积后的保留体积。V'R=VR-V0或V'R=F×t'R3.柱效参数Ø 理论塔板数(theoretical plate number,N)——用于定量表示色谱柱的分离效率(简称柱效)。N取决于固定相的种类、性质(粒度、粒径分布等)、填充状况、柱长、流动相的种类和流速及测定柱效所用物质的性质。如果峰形对称并符合正态分布,N可近似表示为:N=()2=16()2=5.54()2N为常量时,W随tR成正比例变化。在一张多组分色谱图上,如果各组分含量相当,则后洗脱的峰比前面的峰要逐渐加宽,峰高则逐渐降低。用半峰宽计算理论塔数比用峰宽计算更为方便和常用,因为半峰宽更易准确测定,尤其是对稍有拖尾的峰。N与柱长成正比,柱越长,N越大。用N表示柱效时应注明柱长,如果未注明,则表示柱长为1米时的理论塔板数。(一般HPLC柱的N在1000以上。)若用调整保留时间(t'R)计算理论塔板数,所得值称为有效理论塔板数(N有效或Neff)。Ø 理论塔板高度(theoretical plate height,H)——每单位柱长的方差。H=。实际应用时往往用柱长L和理论塔板数计算:H=,H有效=。4.相平衡参数Ø 分配系数(distribution coefficient,K)——在一定温度下,化合物在两相间达到分配平衡时,在固定相与流动相中的浓度之比。K=。分配系数与组分、流动相和固定相的热力学性质有关,也与温度、压力有关。在不同的色谱分离机制中,K有不同的概念:吸附色谱法为吸附系数,离子交换色谱法为选择性系数 (或称交换系数),凝胶色谱法为渗透参数。但一般情况可用分配系数来表示。在条件(流动相、固定相、温度和压力等)一定,样品浓度很低时(Cs、Cm很小)时,K只取决于组分的性质,而与浓度无关。这只是理想状态下的色谱条件,在这种条件下,得到的色谱峰为正常峰;在许多情况下,随着浓度的增大,K减小,这时色谱峰为拖尾峰;而有时随着溶质浓度增大,K也增大,这时色谱峰为前延峰。因此,只有尽可能减少进样量,使组分在柱内浓度降低,K恒定时,才能获得正常峰。在同一色谱条件下,样品中K值大的组分在固定相中滞留时间长,后流出色谱柱;K值小的组分则滞留时间短,先流出色谱柱。混合物中各组分的分配系数相差越大,越容易分离,因此混合物中各组分的分配系数不同是色谱分离的前提。在HPLC中,固定相确定后,K主要受流动相的性质影响。实践中主要靠调整流动相的组成配比及pH值,以获得组分间的分配系数差异及适宜的保留时间,达到分离的目的。Ø 容量因子(capacity factor,k)——化合物在两相间达到分配平衡时,在固定相与流动相中的量之比。k=。因此容量因子也称质量分配系数。分配系数、容量因子与保留时间之间有如下关系:k===K=,t'R=k t0。上式说明容量因子的物理意义:表示一个组分在固定相中停留的时间(t'R)是不保留组分保留时间(t0)的几倍。k=0时,化合物全部存在于流动相中,在固定相中不保留,t'R=0;k越大,说明固定相对此组分的容量越大,出柱慢,保留时间越长。容量因子与分配系数的不同点是:K取决于组分、流动相、固定相的性质及温度,而与体积Vs、Vm无关;k除了与性质及温度有关外,还与Vs、Vm有关。由于t'R、t0较Vs、Vm易于测定,所以容量因子比分配系数应用更广泛。Ø 选择性因子(selectivity factor,α)——相邻两组分的分配系数或容量因子之比。α== (设k2>k1)。因k=t'R/t0,则α=,所以α又称为相对保留时间(《美国药典》)。要使两组分得到分离,必须使α≠1。α与化合物在固定相和流动相中的分配性质、柱温有关,与柱尺寸、流速、填充情况无关。从本质上来说,α的大小表示两组分在两相间的平衡分配热力学性质的差异,即分子间相互作用力的差异。5.分离参数Ø 分离度(resolution,R)——相邻两峰的保留时间之差与平均峰宽的比值。也叫分辨率,表示相邻两峰的分离程度。R=。当W1=W2时,R=。当R=1时,称为4σ分离,两峰基本分离,裸露峰面积为95.4%,内侧峰基重叠约2%。R=1.5时,称为6σ分离,裸露峰面积为99.7%。R≥1.5称为完全分离。《中国药典》规定R应大于1.5。Ø 基本分离方程——分离度与三个色谱基本参数有如下关系:R=××其中称为柱效项,为柱选择性项,为柱容量项。柱效项与色谱过程动力学特性有关,后两项与色谱过程热力学因素有关。从基本分离方程可看出,提高分离度有三种途径:①增加塔板数。方法之一是增加柱长,但这样会延长保留时间、增加柱压。更好的方法是降低塔板高度,提高柱效。②增加选择性。当α=1时,R=0,无论柱效有多高,组分也不可能分离。一般可以采取以下措施来改变选择性:a. 改变流动相的组成及pH值;b. 改变柱温;c. 改变固定相。③改变容量因子。这常常是提高分离度的最容易方法,可以通过调节流动相的组成来实现。k2趋于0时,R也趋于0;k2增大,R也增大。但k2不能太大,否则不但分离时间延长,而且峰形变宽,会影响分离度和检测灵敏度。一般k2在1~10范围内,最好为2~5,窄径柱可更小些。
[b][font=宋体]问题描述:药典中色谱法测定中药成分的方法都规定了理论塔板数,这个参数重要吗?理论塔板数与分离度哪个更重要?[/font][font=宋体]解答:[/font][/b][font=宋体]([/font]1[font=宋体])药典分析中理论塔板数这个参数非常重要,在保证理论塔板数的前提下,才能保证色谱峰的对称性,才能保证不同组分之间的分离度。[/font][font=宋体]([/font]2[font=宋体])理论塔板数达不到要求,说明色谱柱的柱效下降,满足不了药典要求。理论塔板数达不到要求,分离度下降,同一个色谱峰中可能还有其他组分。[/font][font=宋体]([/font]3[font=宋体])理论塔板数越高,色谱峰的对称性越好,不同组分间的分离度越高。[/font][font=宋体]([/font]4[font=宋体])对于色谱分析而言,分离度和重复性也非常重要。分离度又称分辨率,表示相邻两峰的分离程度,分离度越大,表明相邻两组分分离越好。药典中规定分离度应大于[/font]1.5[font=宋体]。药典中规定了许多的色谱数据,其目的是为了保证结果的重现性。[/font][font='微软雅黑','sans-serif'][color=black][back=white]领取更多《实战宝典》请进:[url]http://instrument-vip.mikecrm.com/2bbmrpI[/url][/back][/color][/font][font='微软雅黑','sans-serif'][color=black][back=white] [/back][/color][/font]
已知A、B二组分在某一根柱子上的保留时间分别为13.5min和13.8min,理论塔板数对二组分均为4100,试问:(1)A、B两组分能分离到何种程度?(2)假设A、B两组分保留时间不变,分离度要达到1以上时(按峰宽度计算),理论塔板数为多少?(3)什么样的色谱柱才适合?[color=#DC143C]大家写出计算过程,版主有加积分的奖励 by水中月[/color]
我是液相新手,在做液相时发现理论塔板数达不到5000,只有三千多,但是分离度达到1.5以上,峰形也较好,这样的结果有效么?这种情况为什么会发生啊?怎么解决这个问题啊?另外,当做平行测定时,发现峰宽不稳定,导致五个点的RSD大于2%,这是什么原因啊?如何解决类似的问题?这些问题和流动相有很大的关系么?液相型号:岛津LC-20AT;色谱柱型号:shim-pack vp-ODS请各位大师们帮忙指导一下,万分感激!谢谢!
同一台气相色谱仪,同样的实验条件,同一个样品,同一个人操作,前一针理论塔板数为9000多,后一针理论塔板数只有2000多,理论塔板数一直这样时高时低,请问是什么原因,如何解决啊?
请问论坛的大神,色谱分析仪的理论塔板数应该在什么范围内比较合适?针对不同的被测物质,理论塔板数范围不同吗?谢谢!
“2012年,有关部门出台了一项新政策,专门针对农民合作社的。在食品生产许可证《发证细则》里,要求生产蜂蜜的企业必须配备液相色谱仪。”甜蜜的事业不甜蜜。眼下正是蜂蜜上市旺季,往年这个时候,蜂农纷纷把新酿的蜂蜜卖给合作社,而今年,越来越多蜂农无奈上马路摆地摊。近日,记者去养蜂基地延庆县大庄科乡采访,才知道,这些养蜂合作社,因为买不起50多万元的检测仪器,办不了食品生产许可证。过去进超市能卖18元一斤的蜂蜜,如今马路边只能卖10元。很多蜂农都表示,明年不再养蜂了。生产蜂蜜属食品行业,要有食品生产许可证,办证要有化验室。2008年,合作社投入资金购买设备。 “培养箱3000多元,干燥箱也差不多,这都是大头,还有试管、天平、恒温水浴锅什么的,就花不了多少钱了。”合作社会计付全省告诉记者,合作社一共花了3万元建起5平方米的无菌操作室。1、现在要求生产蜂蜜的企业必须配备液相色谱仪,一台液相色谱都要几十万,蜂农表示伤不起啊。生产蜂蜜企业有必要配液相色谱吗?2、你都用液相色谱测过蜂蜜的什么项目?
k1)。因k=tR’/t0,则α=k2/k1,所以α又称为相对保留时间(《美国药典》)。要使两组分得到分离,必须使α≠1。α与化合物在固定相和流动相中的分配性质、柱温有关,与柱尺寸、流速、填充情况无关。从本质上来说,α的大小表示两组份在两相间的平衡分配热力学性质的差异,即分子间相互作用力的差异。5.分离参数⊕分离度(resolution,R)--相邻两峰的保留时间之差与平均峰宽的比值。也叫分辨率,表示相邻两峰的分离程度。R=(tR2-tR1)/,当W1=W2时,R=。当R=1时,称为4σ分离,两峰基本分离,裸露锋面积为95.4%,内测峰基重叠约2%。R=1.5时,称为6σ分离,裸露锋面积为99.7%。R≥1.5称为完全分离。《中国药典》规定R应大于1.5。⊕基本分离方程――分离度与三个色谱基本参数有如下关系:R=1/4(а-1)×N0.5×其中N称为柱效项,α为柱选择项,k’为柱容量项。柱效项与色谱过程动力学特性有关,后两项与色谱过程热力学因素有关。从基本分离方常可看出,提高分离度有三种途径:①增加塔板数。方法之一是增加柱长,但这样会延长保留时间、增加柱压。更好的方法是降低塔板高度,提高柱效。②增加选择性。当α=1时,R=0,无论柱效有多高,组分也不可能分离。一般可以采取以下措施来改变选择性:a.改变流动相的组成及PH值;b.改变柱温;c.改变固定相。③改变容量因子。这常常是提高分离度的最容易方法,可以通过调节流动相的组成来实现。k2趋于0时,R也趋于0;k2增大,R也增大。但k2 不能太大,否则不但分离时间延长,而且峰形变宽,会影响分离度和检测灵敏度。一般k2 在1~10范围内,最好为2~5,窄径柱可更小些。二、塔板理论1.塔板理论的基本假设塔板理论是Martin和Synger首先提出的色谱热力学平衡理论。它把色谱柱看作分馏塔,把
仪器:Waters的e2695色谱柱:Thermo ods HYPERSIL在检测葛根素时,理论塔板数特别低,只有几百,平时能达到9000,换了一根新的色谱柱(Thermo),还是很小,对照品和样品均出现这个问题,已经排除甲醇,水有问题的可能,仪器是厂家工程师刚做过维护保养的,最关键的是,同样的仪器,同样的柱子,用同样的流动相(比例不同)检测别的项目,就不会出现这个问题。请问有没有老师能给出建议,可能是哪里有问题。关于甲醇:上次出现同样问题是半年前,当时换了一个甲醇的厂家,图谱就正常了,之后就一直用新厂家的甲醇,现在又出现同样问题,然后,换回原来的甲醇,还是不行。
各位亲,甲烷结果是mg/m3,怎么换算成用体积百分数表示呢

以前没有接触过类似的工作。现在用微流芯片通过电泳分离了不同长度的DNA片段,通过芯片检测仪得到了分离的图谱,横坐标是时间,纵坐标是信号的强度,总共有9个峰。现在怎么计算这个图谱的理论塔板数呢?色谱工作站是不是可以直接导入TXT文档,然后得到理论塔板数?如果可以的话,具体怎么操作?小白求解http://ng1.17img.cn/bbsfiles/images/2013/12/201312172037_482707_2840306_3.jpg
新买的pss的凝胶色谱柱,需要测试理论塔板数。厂家测试条件上是用BTH,是2,6-二叔丁基-4甲基苯酚吗?具体是怎么操作的?样品直接进样测试,还是需要用流动性稀释之后再测?求各位老师帮助,谢谢!
凝胶色谱法的基本理论简介:凝胶色谱技术是六十年代初发展起来的一种快速而又简单的分离分技术,由于设备简单、操作方便,不需要有机溶剂,对高分子物质有很高的分离效果。内容: 目前已经被生物化学、分子生物学、生物工程学、分子免疫学以及医学等有关领域广泛采用,不但应用于科学实验研究,而且已经大规模地用于工业生产。基本理论(一) 分子筛效益 一个含有各种分子的样品溶液缓慢地流经凝胶色谱柱时,各分子在柱内同时进行着两种不同的运动:垂直向下的移动和无定向的扩散运动。大分子物质由于直径较大,不易进入凝胶颗粒的微孔,而只能分布颗粒之间,所以在洗脱时向下移动的速度较快。小分子物质除了可在凝胶颗粒间隙中扩散外,还可以进入凝胶颗粒的微孔中,即进入凝胶相内,在向下移动的过程中,从一个凝胶内扩散到颗粒间隙后再进入另一凝胶颗粒,如此不断地进入和扩散,小分子物质的下移速度落后于大分子物质,从而使样品中分子大的先流出色谱柱,中等分子的后流出,分子最小的最后流出,这种现象叫分子筛效应。 具有多孔的凝胶就是分子筛。各种分子筛的孔隙大小分布有一定范围,有最大极限和最小极限。分子直径比凝胶最大孔隙直径大的,就会全部被排阻在凝胶颗粒之外,这种情况叫全排阻。两种全排阻的分子即使大小不同,也不能有分离效果。直径比凝胶最小孔直径小的分子能进入凝胶的全部孔隙。如果两种分子都能全部进入凝胶孔隙,即使它们的大小有差别,也不会有好的分离效果。因此,一定的分子筛有它一定的使用范围。综上所述,在凝胶色谱中会有三种情况,一是分子很小,能进入分子筛全部的内孔隙;二是分子很大,完全不能进入凝胶的任何内孔隙;三是分子大小适中,能进入凝胶的内孔隙中孔径大小相应的部分。大、中、小三类分子彼此间较易分开,但每种凝胶分离范围之外的分子,在不改变凝胶种类的情况下是很难分离的。 对于分子大小不同,但同属于凝胶分离范围内各种分子,在凝胶床中的分布情况是不同的:分子较大的只能进入孔径较大的那一部分凝胶孔隙内,而分子的可进入较多的凝胶颗粒内,这样分子较大的在凝胶床内移动距离较短,分子较小的移动距离较长。于是分子较大的先通过凝胶床而分子较小的后通过凝胶床,这样就利用分子筛可将分子量不同的物质分离。另外,凝胶本身具有三维网状结构,大的分子在通过这种网状结构上的孔隙时阻力较大,小分子通过时阻力较小。分子量大小不同的多种成份在通过凝胶床时,按照分子量大小“排队,凝胶表现分子筛效应。(二) 色谱柱的重要参数⑴柱体积:柱体积是指凝胶装柱后,从柱的底板到凝胶沉积表面的体积。在色谱柱中充满凝胶的部分称为凝胶床,因引柱体积又称“床”体积,常用Vt 表示。⑵外水体积:色谱柱内凝胶颗粒间隙,这部分体积称外水体积,亦称间隙体积,常用Vo表示。⑶内水体积:因为凝胶为三维网状结构,颗粒内部仍有空间,液体可进入颗粒内部,这就分间隙的总和为内水体积,又称定相体积,常用Vi表示。 不包括固体支持物的体积(Vg)。⑷峰洗脱体积:是指被分离物质通过凝胶柱所需洗脱液有体积,常用Ve 表示。当使用样品的体积很少时,(与洗脱体积比较可以忽略不计),在洗脱图中,从加样到峰顶位置所用洗脱液体积为Ve。 当样品体积与洗脱体积比较不能忽略时,洗脱体积计算可以从样品体积的一半到峰顶位置。当样品很大时,洗脱体积计算可以从应用样品开始到洗脱峰升高的弯曲点(或半高处)。
速率理论是1956年由荷兰学者VanDeemter提出,后经美国人Giddings修改完善,英国人Golay推广应用到毛细管柱上,该理论表述了分离过程中影响柱效的因素及提高柱效的多种途径,其核心是速率方程(也称范·弟姆特方程式或范式方程)H=A+B/u+Cu 式中,H为理论塔板高度,u为载气的线性流速,A为涡流扩散项,B/u为分子扩散项,Cu为传质阻力项。下面将分别从速率方程中的三个因子分别进行分析:1. 涡流扩散A 当色谱柱内的组分随流动相经过固定相颗粒流出色谱柱时,如果固定相颗粒不均匀,则组分在穿过固定相空隙时必然会碰到大小不一的颗粒而不断改变方向,由于流经途径不同使得同一时间进入色谱柱的样品流出时间不同,这种现象称为涡流扩散。涡流扩散的大小可用下式表示: A=2λdP式中,λ为填充不均匀因子,dP为固定相平均颗粒直径。 涡流扩散的存在,造成色谱峰展宽。在填充柱中,固定相颗粒大小是影响涡流扩散的重要原因。一般来说,颗粒细,有利于填充均匀,但是过细时可能造成流动相通过色谱柱时压力增加,不便操作。一般减小涡流扩散的方法是选择细而均匀的颗粒,采用良好的填充技术和尽可能使用短柱。目前气质联用所使用的色谱柱为开管毛细管柱,由于这种色谱柱是空心柱,不存在固定相颗粒对于流动相的影响,因此使用开管毛细管色谱柱的涡流扩散项为0。2. 分子扩散B/u 分子扩散又称纵向扩散,是由于组分在柱的轴向(即流动相前进方向)上形成浓度梯度,样品,沿轴向进行扩散。分子扩散项造成的谱带展宽程度可以表示为:B/u=2γDm/u式中,γ为弯曲因子,反映固定相对分子扩散的阻碍;Dm为样品在流动相中的扩散系数,填充柱的弯曲因子一般在0.6~0.8左右,开管毛细管柱为1。 样品的扩散程度主要与样品的扩散系数、载气的种类和流速大小、温度、柱长等有关。样品分子在流动相中的扩散系数越小,扩散越小;载气的流速越大,样品分子在柱子内部滞留的时间就越短,扩散越小;温度越高,扩散越严重。欲使纵向分子扩散减小,应该选择球状颗粒、适当增加载气流速、选择分子质量较大载气作为流动相(扩散系数小),同时采用短柱和较低柱温。3. 传质阻力Cu 由于溶质分子在流动相和固定相中的扩散、分配、转移的过程并不是瞬间达到平衡,这使得某些组分与固定相作用被保留,某些组分不被保留或保留较小,保留小的组分很快被流动相带走,由于传质过程造成的峰展宽称为传质阻力。气相色谱的传质阻力项分为固定相传质阻力和流动相传质阻力。 一般采用薄的液膜厚度、小的载体颗粒、低黏度的固定液、较高的柱温和较低的载气流速有利于减小传质阻力。 速率理论为柱型的研究和发展提供了理论依据,在速率理论的指导下,围绕如何降低涡流扩散、分子扩散和传质阻力从而降低理论塔板高度,有大量研究和应用。为操作条件的选择,流速的选择,柱温的选择,为色谱柱的填充提供理论指导。 由于目前GC-MS使用的是开管毛细管色谱柱,因此速率理论可以简化为H=2Dm/u+Cu。从式中可以看到流速过小分子扩散项会增大,传质阻力项减小,而流速过大分子扩散项减小,传质阻力项增大,对最后的理论塔板高度都会有影响,因此需要选择合理的流速值,过大或过小都打不到最好的分离效率。而从上面的表述可以看出较低的柱温,较厚的膜厚都是有利于降低理论塔板高度,提高分离效率。而在理论塔板高度一定的情况下,较长的色谱柱会增加理论塔板数,提高分离度。
气相中色谱柱理论塔板数受什么影响
改错题:(要求写出理由)1、GC法分离时,选择固定液分离试样时,如果选择的固定液极性越大,则分离的效果就越好。2、采用HPLC法分离时,洗脱时间与流动相的洗脱程度成反比。一般来说,当洗脱液的极性变大时,可缩短分析时间。3、对于难分离组分来说,运用程序升温的效果一般来说会比恒温色谱要好。4、程序升温主要是用于沸点范围大的样品分离,但其分离时的峰容量则与恒温色谱基本相同。5、评价色谱分离效果时,分离度只是表示理论上的分离效果,实际分离效果要用真实分离度来表示。[color=#DC143C]大家答题,版主给加积分奖励 by水中月[/color]
速率理论是1956年由荷兰学者VanDeemter提出,后经美国人Giddings修改完善,英国人的Golay推广应用到气相色谱仪毛细管柱上,该理论表述了分离过程中影响柱效的因素及提高柱效的多种途径,其核心是速率方程(也称范·弟姆特方程式或范式方程)H=A+B/u+Cu 式中,H为理论塔板高度,u为载气的线性流速,A为涡流扩散项,B/u为分子扩散项,Cu为传质阻力项。 下面将分别从速率方程中的三个因子分别进行分析:1. 涡流扩散A 当色谱柱内的组分随流动相经过固定相颗粒流出色谱柱时,如果固定相颗粒不均匀,则组分在穿过固定相空隙时必然会碰到大小不一的颗粒而不断改变方向,由于流经途径不同使得同一时间进入色谱柱的样品流出时间不同,这种现象称为涡流扩散。涡流扩散的大小可用下式表示:A=2λdP 式中,λ为填充不均匀因子,dP为固定相平均颗粒直径。 涡流扩散的存在,造成色谱峰展宽。在填充柱中,固定相颗粒大小是影响涡流扩散的重要原因。一般来说,颗粒细,有利于填充均匀,但是过细时可能造成流动相通过色谱柱时压力增加,不便操作。一般减小涡流扩散的方法是选择细而均匀的颗粒,采用良好的填充技术和尽可能使用短柱。目前气相色谱仪-质谱仪联用所使用的色谱柱为开管毛细管柱,由于这种色谱柱是空心柱,不存在固定相颗粒对于流动相的影响,因此使用开管毛细管色谱柱的涡流扩散项为0。2. 分子扩散B/u 分子扩散又称纵向扩散,是由于组分在柱的轴向(即流动相前进方向)上形成浓度梯度,样品,沿轴向进行扩散。分子扩散项造成的谱带展宽程度可以表示为:B/u=2γDm/u 式中,γ为弯曲因子,反映固定相对分子扩散的阻碍;Dm为样品在流动相中的扩散系数,填充柱的弯曲因子一般在0.6~0.8左右,开管毛细管柱为1。 样品的扩散程度主要与样品的扩散系数、载气的种类和流速大小、温度、柱长等有关。样品分子在流动相中的扩散系数越小,扩散越小;载气的流速越大,样品分子在柱子内部滞留的时间就越短,扩散越小;温度越高,扩散越严重。欲使纵向分子扩散减小,应该选择球状颗粒、适当增加载气流速、选择分子质量较大载气作为流动相(扩散系数小),同时采用短柱和较低柱温。3. 传质阻力Cu 由于溶质分子在流动相和固定相中的扩散、分配、转移的过程并不是瞬间达到平衡,这使得某些组分与固定相作用被保留,某些组分不被保留或保留较小,保留小的组分很快被流动相带走,由于传质过程造成的峰展宽称为传质阻力。气相色谱仪的传质阻力项分为固定相传质阻力和流动相传质阻力。 一般采用薄的液膜厚度、小的载体颗粒、低黏度的固定液、较高的柱温和较低的载气流速有利于减小传质阻力。 速率理论为柱型的研究和发展提供了理论依据,在速率理论的指导下,围绕如何降低涡流扩散、分子扩散和传质阻力从而降低理论塔板高度,有大量研究和应用。为操作条件的选择,流速的选择,柱温的选择,为色谱柱的填充提供理论指导。
色谱过程动力学研究物质在色谱过程中的运动规律,如解释色谱流出曲线的形状、谱带展宽的机理,从而为选择色谱分离条件提供理论指导。用严格的数学公式表述色谱理论需要根据溶质在柱内的迁移过程及影响这一过程的各种因素,列出相应的偏微分方程组,求出描述色谱谱带运动的方程式。其数学处理相当复杂,方程组的求解也非常困难。在实际研究中,通常要进行适当的条件假设并作简化的数学处理。在此仅作简单介绍。 1. 塔板理论 塔板理论把气液色谱柱当作一个精馏塔,沿用精馏塔中塔板的概念描述溶质在两相间的分配行为,并引入理论塔板数(the number of theoretical plates)N和理论塔板高度(theoretical plate height)H作为衡量柱效的指标。 根据塔板理论,溶质进入柱入口后,即在两相间进行分配。对于正常的色谱柱,溶质在两相间达到分配平衡的次数在数千次以上,最后,"挥发度"最大(保留最弱)的溶质最先从"塔顶"(色谱柱出口)逸出(流出),从而使不同"挥发度"(保留值)的溶质实现相互分离。 理论塔板数N可以从色谱图中溶质色谱峰的有关参数计算,常用的计算公式有以下两式:分式中:b1/2为半峰宽;w为峰底宽(经过色谱峰的拐点所作三角形的底边宽)。理论塔高度H与理论塔板数N和柱长的关系如下: H=l/N[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=8620]相关附件[/url]
请问各位大侠,我们都知道用nm表示的分辨率很好理解,如某仪器分辨率是2nm,很直观。但是用波数表示的分辨率究竟该怎么理解呢?比如有些仪器标称分辨率是4cm-1,折合成nm表示具体应该是多少呢?谢谢了[em0810]
微生物结果以对数表示是什么意思[img]https://ng1.17img.cn/bbsfiles/images/2022/11/202211102222343702_7446_4176878_3.png[/img]