[b][url=http://www.f-lab.cn/vivo-imaging/nexus128.html]三维光声超声成像系统Nexus128[/url][/b]是全球首款成熟商用的[b]3D光声成像系统[/b]和[b]3D光声CT系统[/b]和[b]3D光声断层扫描成像系统[/b],具有更高灵敏度和各向同性分辨率,提高光声图像质量,具有更快的扫描时间和更高光声成像处理能力。三维光声超声成像系统利用内源性或外源性对比产生层析吸收的断层图像,适用于近红外吸收染料或荧光探针进行对比度增强和分子成像应用。三维光声超声成像系统应用分子探针的吸收和分布肿瘤血管-血红蛋白浓度肿瘤缺氧-二氧化硫[img=三维光声超声成像系统]http://www.f-lab.cn/Upload/photo-acoustic-CT-Nexus128.png[/img]三维光声超声成像系统Nexus128特点预定义的肿瘤生物学和探头吸收协议先进灵活的研究模式的扫描参数先进的重建算法易于使用的图形用户界面紧凑,方便的现场系统强大的查看和分析软件易于使用的图形用户界面数据可视化与分析三维光声数据从三维光声超声成像系统传输到工作站进行观察和分析。工作站上的数据具有与三维光声超声成像系统相同的结构/组织。独立的工作站允许调查员分析数据,而另一个操作员正在获取数据。前置像头具有强大的内置工具Endra 可以为特殊定量数据应用提供OsiriX 插件三维光声超声成像系统Nexus128:[url]http://www.f-lab.cn/vivo-imaging/nexus128.html[/url]
[b][url=http://www.f-lab.cn/vivo-imaging/lois-3d.html]三维光声层析成像系统[/url][/b]是全球首个[b]体积光声层析成像仪[/b]器,提供[b]三维的组织模拟幻影[/b],包括小动物以及其他在成像模块中的组织图像。三维光声层析成像系统lois-3d是最早根据[b]体积光声层析成像技[/b]术描绘吸收的光能生产综合信息(血液分布及其氧)的系统,提供极其丰富的互补解剖和功能的三维光声图像。[img=三维光声层析成像系统]http://www.f-lab.cn/Upload/LOIS-3D-optoacoustic-tomography.JPG[/img]该三维光声层析成像系统的成像模块被设计成三度扫描,通过研究对象(在临床前研究系统)或模块本身(在临床乳房成像系统)的360度旋转。视频在左边绘制显示成像模块设计的基础激光光声成像系统,lois-3d。它无探针准线快速扫描最佳,而且提供了一个用于小动物活动的灵活的小控制台。三维光声层析成像系统:[url]http://www.f-lab.cn/vivo-imaging/lois-3d.html[/url]
共焦显微镜因其高分辨率和能三维立体成像的优点被广泛应用在生物、医疗、半导体等方面。文章首先分析了影响共焦显微镜分辨率的因素,主要有光源、探测器孔径和杂散光等;并结合这些因素介绍了双光子共焦碌微镜、彩色共焦显微镜、荧光共焦显微镜、光纤共焦显微镜;然后从提高系统成像速度的方面介绍了波分复用共焦显微镜和频分复用共焦显微镜;最后分析了共焦显微镜的发展趋势。一、引言随着人们对于生物医学的研究,传统的光学显微镜已经无法满足研究的需要,人们需要可以实现三维成像的显微镜。1957年Marvin Minsky提出了共焦扫描显微镜的原理。1969年,耶鲁大学的Paul Davidovits和M.David Egger设计了第一台共焦显微镜,1987年第一台商业化共焦显微镜的问世,真正实现了三维立体成像。与普通光学显微镜相比,共焦显微镜具有极其明显的优点:能对物体的不同层面进行逐层扫描,从而获得大量的物体断层图像;可以利用计算机进行图像处理;具有较高的横向分辨率和纵向分辨率;对于透明和半透明物体,可以得到其内部的结构图像;还可以对活体细胞进行观察,获取活细胞内的信息,并对获得的信息进行定量分析。自共焦显微原理被提出以来,引起了研究者的广泛关注,提高显微系统的分辨率和改善系统的性能是研究者开发新型显微镜时考虑的主要因素。近几十年,国内外学者通过对共焦显微成像系统的三维点扩散函数、光学传递函数等方面的分析,得出影响显微系统分辨率的因素,主要包括系统的激励光源、探测器孔径、杂散光等。此外,共焦显微镜的成像速度也是决定系统性能的一个重要因素,专家们也一直在进行提高系统成像速度的研究。本文主要从提高显微系统分辨率和系统成像速度这两个方面来介绍共焦显微镜的发展情况。二、共焦扫描显微镜分辨率的提高光源、探测器孔径和杂散光等是影响共焦显微镜分辨率的几个主要因素,因此可以通过改善这些方面来提高显微系统的分辨率。1.光源显微镜的成像性质在很大程度上取决于所采用光源的相干性,有关研究表明,光源相干性好的系统其分辨率要比相干性差的系统要好,并且照明光源对分辨率的改变范围达到了26.4%。因此,选取适合的照明光源对提高显微系统的分辨率有很大帮助。常规的共焦扫描显微镜主要使用普通单色激光作为光源,随着技术的进步,目前已经出现了使用飞秒激光、超白激光、高斯光束作为光源的共焦显微镜,以提高系统性能,获得更高的分辨率。①飞秒激光为光源的双先子扫描共焦显微镜双光子扫描共焦显微镜通常使用近红外的飞秒激光作为激发光源,由于红外光具有较强的穿透性,它能探测到生物样品表面下更深层的荧光图像,并且生物组织对红外光吸收少,随着探测深度的增加衰减会变小,另一方面红外光的衍射低,光束的形状保持性好。2005年,Wild等人利用双光子扫描共焦显微技术实时观察和定量分析了PAHs在植物叶片表面和内部的光降解过程。后来又进一步研究了菲从空气到叶片的迁移过程、菲在叶片内部的运动及其分布情况等,该技术可观测PAHs在叶片内部的最大深度约为200μm。②白激光( supercontinuum laser)为光源的彩色共焦显微镜彩色共焦显微镜是利用光学系统的彩色像差,光源的不同光谱成分会聚焦到样品的不同深度,通过分析由样品反射的光谱能有效地获得样品的扫描深度。2004年,美国宾夕法尼亚州立大学的Zhiwen Liu课题小组使用光子晶体光纤产生的超连续谱白光作为彩色共焦显微镜的光源,这种超连续谱白光具有大的带宽,能够提高系统的扫描范围,能达到7μm扫描深度。另外超白激光有较高的空间相干性,无斑点噪声,能提高系统的信噪比和扫描速度。③使用高斯光束的荧光共焦显微镜荧光共焦显微镜是通过激光照射样品激发样品发出荧光,再通过探测器接受荧光对样品进行观察的共焦显微镜。华南农业大学的杨初平等人研究了不同光源孔径和束斑尺寸的高斯光束对荧光共焦显微镜分辨率的影响表明:与一定孔径尺寸的平行光束相比,采用高斯光束系统可以获得更好的分辨率。 2. 探测器孔径和杂散光共焦显微镜中探测器孔径能滤除部分杂散光,提高系统的分辨率和信噪比。根据相关文献对共焦扫描显微镜的三维光学传递函数与探测器孔径之间的依赖关系的研究,可以得到探测小孔直径为:d=β*1.22λ/NA,式中,β为物镜的放大率,λ为光的波长,NA为物镜的数值孔径。由该公式确定探测器小孔的直径,一方面满足了共焦扫描系统对探测器小孔直径的要求,从而保证高的横向和纵向分辨率,另一方面,又最大限度地使由试样中发射的荧光能量被探测器接收。为了更进一步提高系统分辨率,许多研究者对共焦显微镜中探测孔径进行了改进,例如使用单模光纤代替普通针孔孔径,还有双D型孔径等。① 使用单模光纤的光纤共焦显微镜在光纤共焦显微镜中用光纤分路器代替传统共焦显微镜中的光束分路器,并以单模光纤来代替光源和探测器的微米尺寸针孔孔径。使用单模光纤的优点在于:首先,在采用寻常针孔制作的共焦显微镜中,光源、针孔、探测器等有可能不在一条直线上从而会引起像差;但是在光纤作为针孔的共焦显微镜中,即使有的部件偏离直线时也不会引入像差。其次,使用单模光纤代替微型针孔,容易清除针孔的污染,而且不易受污染。第三,在使用光纤的系统中,可以自由移动显微镜部分而不必挪动探测器。2006年德克萨斯大学使用光纤共焦显微镜进行口腔病变检测,测得的系统横向和轴向分辨率分别为2. 1µm和10µm,成像速度为15帧/s,可观测范围为200µm×200µm。② 具有D型孔径的共焦显微镜近几年,具有对称D型光瞳的共焦显微成像技术引起广泛的关注,图1所示是该系统示意图。2006年美国东北大学的Peter J.Dwyer等人使用这种共焦显微镜进行了人体皮肤内部成像的实验,测得横向分辨率为1.7士0.1µm。2009年新加坡国立大学的Wei Gong等人采用傍轴近似方法理论分析了在共焦显微镜中使用双D型孔径对轴向分辨率的影响。分析表明在图1中的d值给定时,进入瞳孔的光信号强度l会随着探测器尺寸的增加而增加;但是在探测器尺寸给定时,光信号强度I会随着d的增加而单调递减。在使用有限大小的探测器时,改变d的大小,轴向分辨率可以得到改善。 http://www.biomart.cn//upload/userfiles/image/2011/11/1321512815.png 图1 双D型孔径共焦成像系统示意图在共焦成像光学系统中,到达像面的杂散光会在像面上产生附加的强度分布,从而进一步降低了像面的对比度,限制了系统分辨率的提高,因此在显微系统设计时,杂散光的影响也是不容忽视的。一般除了使用探测小孔来抑制杂散光,其他的一些设备例如可变瞳滤波器等对杂散光也有很好的过滤作用。最近以色列魏茨曼科学研究所的O.sipSchwartz and Dan Oron等人提出在系统中使用可变瞳滤波器,这个滤波器能够使多光子荧光共焦显微镜达到分辨率阿贝极限的非线性模拟,从而改善系统的分辨率。三、共焦扫描显微成像速度的提高共焦显微镜快速的成像速度为研究者观察生物细胞中快速动态反应提供了良好的条件。在共焦扫描显微成像系统中,传统的方法是通过改善扫描探测技术来提高成像速度。现有的扫描探测技术主要有Nipkow转盘法、狭缝共焦检测法、多光束的微光学器件检测法。这些方法可以改善扫描速度,但是与系统分辨率,视场之间都存在矛盾,因此又诞生了两种提高成像速度的新型显微镜:波分复用共焦显微镜和频分复用共焦显微镜。
[b][font=宋体][color=black]【序号】:1[/color][/font][font='微软雅黑',sans-serif][color=black][/color][/font]【作者】:[b][b]杨欣[/b][/b][/b][font=&]【题名】:[b][b][b]基于共振扫描的显微成像技术及系统研究[/b][/b][/b][/font][font=&]【期刊】:cnki[/font][b][color=#545454]【链接]: [url=https://kns.cnki.net/kcms/detail/detail.aspx?dbcode=CDFD&dbname=CDFDLAST2016&filename=1015712320.nh&uniplatform=NZKPT&v=g8fPyqfSNBIZFLi6JV5IjwK9gKCSBCEvUuN3dTxvKpYlXKEQlXfSHL3OoehSZY07]基于共振扫描的显微成像技术及系统研究 - 中国知网 (cnki.net)[/url][/color][/b]
一、前沿2009年10月6日,瑞典皇家科学院宣布,将2009年诺贝尔物理学奖的一半授予美国科学家威拉德• 博伊尔和乔治• 史密斯,因为他们于1969年发明了半导体集成电路成像技术,CCD感应器。经过四十年的发展,CCD技术由实验室逐步走向了市场,具有越来越广阔的应用。CCD数码成像对摄影产生了革命性的影响。在感光胶片之外,人们可以通过电子电路捕捉图像,这些以数字形式存在的图像更加易于处理和分发。数字图像已经成为许多研究领域中不可替代的重要工具。数码成像技术应用到显微镜上,以替代以往的胶卷拍摄,现在已经广泛应用了。以前我们用胶卷来进行显微拍摄,要等一卷拍完,冲洗出来才能确定拍摄的图像是否清晰,如果拍摄的图像不理想,而显微观察的样品又失效了,就需要重新制作样品,给研究工作带来很大的不便,而现在使用显微数码相机来拍摄显微图像,所见即所得,当时就是保存处理,甚至统计分析,极大的提高了工作效率。二、显微数码成像系统的组成显微数码成像系统包括CCD/CMOS专业相机,图像采集处理软件,显微镜接口,数据传输线等,其中最核心的设备是CCD和CMOS图像传感器,前者由光电耦合器件构成,后者由金属氧化物器件构成。两者都是光电二极管结构感受入射光并转换为电信号,主要区别在于读出信号所用的方法。CCD(Charge Coupled Device ,感光耦合组件)上感光组件的表面具有储存电荷的能力,并以矩阵的方式排列。当其表面感受到光线时,会将电荷反应在组件上,整个CCD上的所有感光组件所产生的信号,就构成了一个完整的画面。CCD的结构分三层 ,第一层“微型镜头”“ON-CHIP MICRO LENS”,这是为了有效提升CCD的总像素,又要确保单一像素持续缩小以维持CCD的标准面积,在每一感光二极管上(单一像素)装置微小镜片。CCD的第二层是“分色滤色片”,目前有两种分色方式,一是RGB原色分色法,另一个则是CMYG补色分色法。原色CCD的优势在于画质锐利,色彩真实,但缺点则是噪声问题。第三层:感光层,这层主要是负责将穿过滤色层的光源转换成电子信号,并将信号传送到影像处理芯片,将影像还原。数码成像的核心器件除CCD,现在越来越多的使用CMOS(Complementary Metal-Oxide Semiconductor,互补性氧化金属半导体,CMOS和CCD一样同在数码相机中可记录光线变化的半导体。CMOS传感器中每一个感光元件都直接整合了放大器和模数转换逻辑,当感光二极管接受光照、产生模拟的电信号之后,电信号首先被该感光元件中的放大器放大,然后直接转换成对应的数字信号。CMOS的优势在于成本低,耗电需求少,便于制造, 可以与影像处理电路同处于一个芯片上,缺点是较容易出现杂点。三 显微镜成像系统相关参数对CCD/CMOS数码成像系统的结构和原理有了一个基本了解后,我们再对成像系统的一些基本参数作一个说明。在实际应用中,很多用户对像素多少很敏感,一上来就提到我要多少万像素的成像系统,其实在专业成像应用中,像素多少只是影响成像的一个因素,还有其他很多指标,包括分辨率,感光器件大小,动态范围,灵敏度,量子效率,信噪比等。感光器件的面积大小是衡量显微成像系统质量的一个重要指标,感光器件的面积越大,捕获的光子越多,感光性能越好,信噪比越低。当前数码成像系统中较常应用的感光器件规格如下:1英寸(靶面尺寸为宽12.7mm*高9.6mm,对角线16mm),2/3英寸, 1/2英寸,1/3英寸,另外有时也用到1/1.8英寸,1/2.5英寸的CCD/CMOS感光器件。 像素是CCD/CMOS能分辨的最小的感光元件,显微数码成像系统的像素由低到高有:45万左右,140万左右,200万左右,300万左右,500万左右,900万像素,甚至还有更高的达到2000万像素以上。一般来说,像素越高,图像分辨率越高,成像也就越清晰,但有时候图像分辨率达到一定程度后,就不是影响成像质量的主要指标了。比如图像分辨率高,噪声也很高时,成像质量也不会很好。暗电流是导致CCD噪音的很重要的因素。暗电流指在没有曝光的情况下,在一定的时间内,CCD传感器中像素产生的电荷。我们在做荧光拍摄的时候,需要的曝光的时候比较长,这样导致CCD产生较多的暗电流,对图像的质量影响非常大。通常情况下通过降低CCD的温度来最大限度的减少暗电流对成像的影响。Peltier制冷技术一般可将CCD温度降低5-30°C,在长时间拍摄或一次曝光超过5-10秒,CCD芯片会发热,没有致冷设备的芯片,“热”或者白的像素点就会遮盖图像,图像会出向明显的雪花点。CCD结构设计、数字化的方法等都会影响噪音的产生。当然通过改善结构、优化方法,同样能减少噪音的产生。显微荧光或其他弱光的拍摄对CCD噪音的降低要求很高,应选用高分辨率数字冷却CCD成像系统,使其能够捕获到信号极其微弱的荧光样品图像,并且能够最大程度的降低噪音,减少背景,提供出色的图像清晰度。所以一般在荧光及弱光观察时需要选择制冷CCD。在显微数码成像过程中,对于荧光及弱光的拍摄,除了制冷降低热噪声外,还可使用 BINNING技术提高图像的灵敏度,BINNING像素合并是一种非常有用的功能,它可被用来提高像素的大小和灵敏度,比如摄像头像素大小为5u,当经过2x2合并后,像素大小为10u,3X3合并后,像素大小为15u, 这是图像的整体像素变少了,但成像的灵敏度可提高9倍。动态范围表示在一个图像中最亮与最暗的比值。12bit表示从最暗到最亮等分为212=4096个级别,16bit即分为216个级别,可见bit值越高能分出的细微差别越大,一般CMOS成像系统动态范围具有8-10bit, CCD以10-12bit为主,少部分可达16bit。对动态范围进行量化需要一个运算公式,即动态范围值 = 20 log (well depth/read noise),动态范围的值越高成像系统的性能就越好。量子效率也称像素灵敏度,指在一定的曝光量下,像素势阱中所积累的电荷数与入射到像素表面上的光子数之比。不同结构的CCD其量子效率差异很大。比如100光子中积累到像素势阱中的电荷数是50个,则量子效率为50%(100 photons = 50 electrons means 50% efficiency)。值得注意的是CCD 的量子效率与入射光的波长有关。对显微数码成像系统的参数有了整体认识后,在实际应用中选择合适型号的产品就比较容易了。高分辨率显微数码成像技术在国外已有二十来年的发展历史,产品目前已比较成熟。国外的专业数码产品有多个品牌,比较著名的有德国的ProgRes,美国Roper Scientific的系列产品,另外OLYMPUS、NIKON、LEICA、ZEISS等显微镜厂家也有一些配套的专业数码成像系统 。其中CCD成像系统主要采用SONY及KODRA公司的芯片,因此相关产品性能差别不是很大。国内专业数码成像产品的设计制造时间还不长,但随着配套技术的成熟,100万像素以上的CCD/CMOS专业数码成像产品开始陆续推出,主要的专业厂家有北京的大恒、微视、杭州欧普林,广州明美等企业。北京大恒早期主要研发生产图像采集卡,目前可以量产140万像素的CCD摄像头,130万/200万/320万/500万像素CMOS摄像头,主要用到工业领域。
这款[url=http://www.f-lab.cn/microscopes-system/pam.html][b]光声显微镜PAM[/b][/url]是全球首款覆盖光学分辨率到声学分辨率级别的[b]光声显微镜系统[/b]和[b]光声成像显微镜[/b],是全球[b]光声显微镜品牌[/b]中[b]光声显微镜价格[/b]合理的仪器.在光学分辨率的系统(OR-PAM)和声学分辨率(ar-pam)领域MPA提供商业光声显微镜(PAM)。发展快速扫描光学分辨率的光声显微镜(OR-PAM),能够通过无荧光、荧光吸光剂标记而成像。• 结合OR-PAM系统与明场声学分辨率的光声显微镜(ar-pam),能够获得具有高分辨率和深度组织信息的图像。• 通过提供前沿光声显微镜设备,促进生物和临床研究的创新。[img=光声显微镜]http://www.f-lab.cn/Upload/PAM-Microscope.JPG[/img][b][url=http://www.f-lab.cn/microscopes-system/pam.html]光声显微镜PAM[/url]参数OR-PAM Systems:[/b]Signal penetration depths up to 1 mmLateral resolution down to 5 μmAxial resolution down to 30 μmIntegrated, KHz tunable laser[b]AR-PAM Systems:[/b]Signal penetration depths up to 3 mmLateral resolution down to 45 μmAxial resolution down to 30 μmIntegrated, KHz tunable laser[img=光声显微镜]http://www.f-lab.cn/Upload/microphotoacustics.png[/img]光声显微镜:[url]http://www.f-lab.cn/microscopes-system/pam.html[/url]
[b][font='Microsoft YaHei', 宋体, sans-serif]【序号】:1[/font]【作者】:[/b][font=&][size=12px][color=#1c1d1e][b][b]魏通达[/b][/b][/color][/size][/font][font='Microsoft YaHei', 宋体, sans-serif][b][b][/b][/b][/font][font=&]【题名】:[/font][b][b][color=#333333][b][font=&][color=#032d2c][b]共聚焦激光扫描光学显微成像关键技术研究[/b][/color][/font][/b][/color][/b][/b][font=&]【期刊】:[/font][font=Arial][font=&][size=12px]CNKI[/size][/font][/font][font='Microsoft YaHei', 宋体, sans-serif][color=#545454][b]【链接】:[url=https://link.springer.com/book/10.1007/978-0-387-45524-2]共聚焦激光扫描光学显微成像关键技术研究 - 中国知网 (cnki.net)[/url][/b][/color][/font]
[b][url=http://www.f-lab.cn/vivo-imaging/msot.html]小动物光声成像系统[/url][/b]MSOT是全球唯一能够提供[b][url=http://www.f-lab.cn/vivo-imaging/msot.html]小动物全身光声成像[/url][/b]能力的小动物实时光声成像系统,用于临床前小动物成像和临床前研究。小动物光声成像系统能够可帮助生物过程和药理物质作用在体内,在深部组织中高分辨率下实时观察。小动物光声成像系统是全球唯一混合光声超声成像技术,OPUS成像技术的同类仪器,也是世界上第一个交叉断层成像系统,提供非平行的用户独立的图像质量,并且具有实时性,可以获得整个动物的横截面影像。这套小动物光声成像系统包含组织形态基于血红蛋白信息产生的光声层析成像,反射式超声成像的集成(r-uct)能力添加互补的解剖信息,特别是低灌注结构。小动物光声成像系统可以调谐激发激光波长,采集光声信号,执行多个波长的光谱分解,这样内源性色基团以及外在探针可有效被区分。小动物光声成像系统工作MSOT探测器小动物置台可以利用各种手持探测器实现小动物的二维和三维自动成像。动物置台可作为内部图像和EIP MSOT成像系统的附件。主要特点包括:自动数据采集三维阶段控制加热的动物垫激光安全联锁装置动物监控摄像机接入导管或生命体征监测[img=小动物光声成像系统]http://www.f-lab.cn/Upload/MOST-invision-imaging.JPG[/img]小动物光声成像系统混合光声超声成像技术(OPUS成像)小动物光声成像系统是全球唯一混合光声超声成像技术,OPUS成像技术的同类仪器,也是世界上第一个交叉操作断层成像系统,提供非平行的用户独立的图像质量,并且具有实时性,可以获得整个动物的横截面影像。这套小动物光声成像系统包含组织形态基于血红蛋白信息产生的光声层析成像,反射式超声成像的集成(r-uct)能力添加互补的解剖信息,特别是低灌注结构。[img=小动物光声成像系统]http://www.f-lab.cn/Upload/Hybrid-OPUS-IMAGING.jpg[/img]初步实验表明,小动物光声成像系统t的升级版将应用在以下需要可视化的任何结构:肿瘤边缘转移胰腺膀胱小动物光声成像系统技术信息单波长的光声成像在10 Hz帧频高达5赫兹帧频的实时频谱分量可视化公司注册的反射式超声计算机断层扫描(r-uct)MSOT IN VISION 512-ECHO成像穿透深度2-4厘米,适合全身小动物成像。横截面的空间平面分辨率:150μM高功率/快速可调谐激光系统(100兆焦耳/ 10毫秒)具有64/128/256/512元件的断层超声探测器阵列全自动图像采集用于光谱和时间分析的数据后处理套件[b][/b]
显微镜成像系统,是能够连接显微镜和电脑,方便教学与及研究,不知道有多少人选择了便用显微镜成像系统
激光共聚焦显微镜系统的原理和应用激光扫描共聚焦显微镜是二十世纪80年代发展起来的一项具有划时代的高科技产品,它是在荧光显微镜成像基础上加装了激光扫描装置,利用计算机进行图像处理,把光学成像的分辨率提高了30%--40%,使用紫外或可见光激发荧光探针,从而得到细胞或组织内部微细结构的荧光图像,在亚细胞水平上观察诸如Ca2+ 、PH值,膜电位等生理信号及细胞形态的变化,成为形态学,分子生物学,神经科学,药理学,遗传学等领域中新一代强有力的研究工具。激光共聚焦成像系统能够用于观察各种染色、非染色和荧光标记的组织和细胞等,观察研究组织切片,细胞活体的生长发育特征,研究测定细胞内物质运输和能量转换。能够进行活体细胞中离子和PH值变化研究(RATIO),神经递质研究,微分干涉及荧光的断层扫描,多重荧光的断层扫描及重叠,荧光光谱分析荧光各项指标定量分析荧光样品的时间延迟扫描及动态构件组织与细胞的三维动态结构构件,荧光共振能量的转移的分析,荧光原位杂交研究(FISH),细胞骨架研究,基因定位研究,原位实时PCR产物分析,荧光漂白恢复研究(FRAP),胞间通讯研究,蛋白质间研究,膜电位与膜流动性等研究,完成图像分析和三维重建等分析。一.激光共聚焦显微镜系统应用领域:涉及医学、动植物科研、生物化学、细菌学、细胞生物学、组织胚胎、食品科学、遗传、药理、生理、光学、病理、植物学、神经科学、海洋生物学、材料学、电子科学、力学、石油地质学、矿产学。二.基本原理传统的光学显微镜使用的是场光源,标本上每一点的图像都会受到邻近点的衍射或散射光的干扰;激光扫描共聚焦显微镜利用激光束经照明针孔形成点光源对标本内焦平面的每一点扫描,标本上的被照射点,在探测针孔处成像,由探测针孔后的光点倍增管(PMT)或冷电耦器件(cCCD)逐点或逐线接收,迅速在计算机监视器屏幕上形成荧光图像。照明针孔与探测针孔相对于物镜焦平面是共轭的,焦平面上的点同时聚焦于照明针孔和发射针孔,焦平面以外的点不会在探测针孔处成像,这样得到的共聚焦图像是标本的光学横断面,克服了普通显微镜图像模糊的缺点。三.应用范围:细胞形态学分析(观察细胞或组织内部微细结构,如:细胞内线粒体、内质网、高尔基体、微管、微丝、细胞桥、染色体等亚细胞结构的形态特征;半定量免疫荧光分析);荧光原位杂交研究;基因定位研究及三维重建分析。1.细胞生物学:细胞结构、细胞骨架、细胞膜结构、流动性、受体、细胞器结构和分布变化2.生物化学:酶、核酸、FISH(荧光原位杂交)、受体分析3.药理学:药物对细胞的作用及其动力学4.生理学:膜受体、离子通道、细胞内离子含量、分布、动态5.神经生物学:神经细胞结构、神经递质的成分、运输和传递、递质受体、离子内外流、神经组织结构、细胞分布6.微生物学和寄生虫学:细菌、寄生虫形态结构7.病理学及临床应用:活检标本诊断、肿瘤诊断、自身免疫性疾病诊断、HIV等8.遗传学和组胚学:细胞生长、分化、成熟变化、细胞的三维结构、染色体分析、基因表达、基因诊断四.激光共聚焦显微镜在医学领域中的应用A.在细胞及分子生物学中的应用1. 细胞、组织的三维观察和定量测量2. 活细胞生理信号的动态监测3. 粘附细胞的分选4. 细胞激光显微外科和光陷阱功能5. 光漂白后的荧光恢复6. 在细胞凋亡研究中的应用B.在神经科学中的应用1. 定量荧光测定2. 细胞内离子的测定3. 神经细胞的形态观察C.在耳鼻喉科学中的应用1. 在内耳毛细胞亚细胞结构研究上的应用2. 激光扫描共聚焦显微镜的荧光测钙技术在内耳毛细胞研究中的应用3. 激光扫描共聚焦显微镜在内耳毛细胞离子通道研究上的应用4. 激光扫描共聚焦显微镜在嗅觉研究中的应用D.在肿瘤研究中的应用1. 定量免疫荧光测定2. 细胞内离子分析3. 图像分析:肿瘤细胞的二维图像分析4. 三维重建 E.激光扫描共聚焦显微镜在内分泌领域的应用1. 细胞内钙离子的测定2. 免疫荧光定位及免疫细胞化学研究3. 细胞形态学研究:利用激光扫描共聚焦显微镜 F.在血液病研究中的应用1. 在血细胞形态及功能研究方面的应用2. 在细胞凋亡研究中的应用 G.在眼科研究中的应用1. 利用激光扫描共聚焦显微镜观察组织、细胞结构2. 集合特殊的荧光染色在活体上观察角膜外伤修复中细胞移行及成纤维细胞的出现3. 利用激光扫描共聚焦显微镜观察视网膜中视神经细胞的分布以及神经原的树枝状形态4. 三维重建H. 激光扫描共聚焦显微镜在肾脏病中的应用可以系统观察正常人肾小球系膜细胞的断层扫描影像及三维立体影像水平,使图像更加清晰,从计算机分析系统可从外观到内在结构,从平面到立体,从静态到动态,从形态到功能几个方面对系膜细胞的认识得到提高。北京中科研域科技有限公司(蔡司显微镜代理商)地址:北京市朝阳区建国路15号院甲1号北岸1292,一号楼406室联系人:张辉13911188977 邮编:100024电话:010-57126588 传真:010-85376588E-mail:[email=zhs_8000@126.com][color=#0365bf]zhs_8000@126.com[/color][/email]
激光共聚焦显微镜系统的原理和应用激光扫描共聚焦显微镜是二十世纪80年代发展起来的一项具有划时代的高科技产品,它是在荧光显微镜成像基础上加装了激光扫描装置,利用计算机进行图像处理,把光学成像的分辨率提高了30%--40%,使用紫外或可见光激发荧光探针,从而得到细胞或组织内部微细结构的荧光图像,在亚细胞水平上观察诸如Ca2+ 、PH值,膜电位等生理信号及细胞形态的变化,成为形态学,分子生物学,神经科学,药理学,遗传学等领域中新一代强有力的研究工具。激光共聚焦成像系统能够用于观察各种染色、非染色和荧光标记的组织和细胞等,观察研究组织切片,细胞活体的生长发育特征,研究测定细胞内物质运输和能量转换。能够进行活体细胞中离子和PH值变化研究(RATIO),神经递质研究,微分干涉及荧光的断层扫描,多重荧光的断层扫描及重叠,荧光光谱分析荧光各项指标定量分析荧光样品的时间延迟扫描及动态构件组织与细胞的三维动态结构构件,荧光共振能量的转移的分析,荧光原位杂交研究(FISH),细胞骨架研究,基因定位研究,原位实时PCR产物分析,荧光漂白恢复研究(FRAP),胞间通讯研究,蛋白质间研究,膜电位与膜流动性等研究,完成图像分析和三维重建等分析。一.激光共聚焦显微镜系统应用领域:涉及医学、动植物科研、生物化学、细菌学、细胞生物学、组织胚胎、食品科学、遗传、药理、生理、光学、病理、植物学、神经科学、海洋生物学、材料学、电子科学、力学、石油地质学、矿产学。二.基本原理传统的光学显微镜使用的是场光源,标本上每一点的图像都会受到邻近点的衍射或散射光的干扰;激光扫描共聚焦显微镜利用激光束经照明针孔形成点光源对标本内焦平面的每一点扫描,标本上的被照射点,在探测针孔处成像,由探测针孔后的光点倍增管(PMT)或冷电耦器件(cCCD)逐点或逐线接收,迅速在计算机监视器屏幕上形成荧光图像。照明针孔与探测针孔相对于物镜焦平面是共轭的,焦平面上的点同时聚焦于照明针孔和发射针孔,焦平面以外的点不会在探测针孔处成像,这样得到的共聚焦图像是标本的光学横断面,克服了普通显微镜图像模糊的缺点。三.应用范围:细胞形态学分析(观察细胞或组织内部微细结构,如:细胞内线粒体、内质网、高尔基体、微管、微丝、细胞桥、染色体等亚细胞结构的形态特征;半定量免疫荧光分析);荧光原位杂交研究;基因定位研究及三维重建分析。1.细胞生物学:细胞结构、细胞骨架、细胞膜结构、流动性、受体、细胞器结构和分布变化2.生物化学:酶、核酸、FISH(荧光原位杂交)、受体分析3.药理学:药物对细胞的作用及其动力学4.生理学:膜受体、离子通道、细胞内离子含量、分布、动态5.神经生物学:神经细胞结构、神经递质的成分、运输和传递、递质受体、离子内外流、神经组织结构、细胞分布6.微生物学和寄生虫学:细菌、寄生虫形态结构7.病理学及临床应用:活检标本诊断、肿瘤诊断、自身免疫性疾病诊断、HIV等8.遗传学和组胚学:细胞生长、分化、成熟变化、细胞的三维结构、染色体分析、基因表达、基因诊断四.激光共聚焦显微镜在医学领域中的应用A.在细胞及分子生物学中的应用1.细胞、组织的三维观察和定量测量2.活细胞生理信号的动态监测3.粘附细胞的分选4.细胞激光显微外科和光陷阱功能5.光漂白后的荧光恢复6.在细胞凋亡研究中的应用B.在神经科学中的应用1.定量荧光测定2.细胞内离子的测定3.神经细胞的形态观察C.在耳鼻喉科学中的应用1.在内耳毛细胞亚细胞结构研究上的应用2.激光扫描共聚焦显微镜的荧光测钙技术在内耳毛细胞研究中的应用3.激光扫描共聚焦显微镜在内耳毛细胞离子通道研究上的应用4.激光扫描共聚焦显微镜在嗅觉研究中的应用D.在肿瘤研究中的应用1. 定量免疫荧光测定2. 细胞内离子分析3. 图像分析:肿瘤细胞的二维图像分析4. 三维重建 E.激光扫描共聚焦显微镜在内分泌领域的应用1. 细胞内钙离子的测定2. 免疫荧光定位及免疫细胞化学研究3. 细胞形态学研究:利用激光扫描共聚焦显微镜 F.在血液病研究中的应用1. 在血细胞形态及功能研究方面的应用2. 在细胞凋亡研究中的应用 G.在眼科研究中的应用1. 利用激光扫描共聚焦显微镜观察组织、细胞结构2. 集合特殊的荧光染色在活体上观察角膜外伤修复中细胞移行及成纤维细胞的出现3. 利用激光扫描共聚焦显微镜观察视网膜中视神经细胞的分布以及神经原的树枝状形态4. 三维重建H. 激光扫描共聚焦显微镜在肾脏病中的应用可以系统观察正常人肾小球系膜细胞的断层扫描影像及三维立体影像水平,使图像更加清晰,从计算机分析系统可从外观到内在结构,从平面到立体,从静态到动态,从形态到功能几个方面对系膜细胞的认识得到提高。
要采购低温冰箱,荧光PCR仪,高压灭菌锅,凝胶成像仪,显微成像系统等,哪几家公司(国外)的性价比高且结实耐用啊,求高手指点。
[url=http://www.f-lab.cn/microscopes-system/storm.html][b]实时超分辨率显微成像系统[/b][/url]突破了光学显微镜的半波长分辨率极限,提供了比宽视场,共聚焦显微镜更好分辨率。实时超分辨率显微成像系统采用尼康或奥林巴斯显微镜,Chroma 滤波片,Andor公司EMCCD相机以及独特的照明系统,为客户提供全球同步的超分辨率成像系统。[img=实时超分辨率显微成像系统]http://www.f-lab.cn/Upload/storm-2.JPG[/img][b]实时超分辨率显微成像系统特点[/b]横向分辨率可达20nm,轴向分辨率可达40nm实时和线下图像重建GPU加速处理图像先进的自动聚焦硬件高分辨率X-Y-Z工作台灵活的配置[img=实时超分辨率显微成像系统]http://www.f-lab.cn/Upload/storm-1.JPG[/img]实时超分辨率显微成像系统:[url]http://www.f-lab.cn/microscopes-system/storm.html[/url]
[font=宋体]传统的[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]技术测量的是平均光谱,反映样本的平均组成,而近红外显微成像技术增加了光谱的空间分布信息,可以使样品的异质性得到进一步[/font][font=宋体]确定。近红外显微成像系统是将[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱仪[/color][/url]与光学显微镜联用的系统,主要由近红外主机、近红外显微镜系统和计算机组成。近红外主机多采用干涉分光原理,主要部件包括迈克尔逊干涉仪、显微镜光学系统、检测器等。显微镜把光束聚焦到测量样品的微区上,可移动镜头从而对样品进行点、线、面的分子水平的扫描,可以快速获得大量的[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]图,并把测量点的坐标与对应的红外光谱同时存入计算机,得到不同化合物在微区分布的平面图或立体图。[/font][font='Times New Roman']1. [/font][font=宋体]近红外显微成像技术的特点[/font][font=宋体][font=宋体]([/font][font=Times New Roman]1[/font][font=宋体])样品不需预处理。[/font][/font][font=宋体][font=宋体]([/font][font=Times New Roman]2[/font][font=宋体])穿透能力强。[/font][/font][font=宋体][font=宋体]([/font][font=Times New Roman]3[/font][font=宋体])水的干扰小,可以对鲜活组织和溶液中的细胞样品直接测定。[/font][/font][font=宋体][font=宋体]([/font][font=Times New Roman]4[/font][font=宋体])测定的区域可达到[/font][/font][font='Times New Roman']lcm[/font][sup][font='Times New Roman']2[/font][/sup][font=宋体]以上,并且可以检测粗糙表面的样品。[/font][font=宋体][font=宋体]([/font][font=Times New Roman]5[/font][font=宋体])非接触性、非破坏性、无环境污染。[/font][/font][font=宋体][font=宋体]([/font][font=Times New Roman]6[/font][font=宋体])二维光谱可以增强分辨率,展示更多的细节。[/font][/font][font=宋体][font=宋体]([/font][font=Times New Roman]7[/font][font=宋体])可分析多种物态的样品。[/font][/font][b][font='Times New Roman']2. [/font][font=宋体]成像方式[/font][/b][font=宋体][font=宋体]([/font][font=Times New Roman]1[/font][font=宋体])总吸收图像,以每一个的数据点的[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]图为基础,宏观显示图像分析区域内的近红外吸收强度。[/font][/font][font=宋体][font=宋体]([/font][font=Times New Roman]2[/font][font=宋体])单波长成像,以特定波长的近红外吸收强度为特征,显示对应化学官能团在图像分析区域内的分布信息。[/font][/font][font=宋体][font=宋体]([/font][font=Times New Roman]3[/font][font=宋体])化学成像,也叫峰面积图像,是以特定吸收峰的峰面积为特征,显示对应化学官能团在图像分析区域内的分布信息。[/font][/font][font=宋体]([/font][font='Times New Roman']4[/font][font=宋体])相关谱成像,以某一张[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]为标准,计算出整个图像上的像素点光谱与它的相关性,再以相似度为度量成像。特别适于鉴别纯物质中的零星污染物。[/font][font=宋体]([/font][font='Times New Roman']5[/font][font=宋体])峰比率成像,以[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]图不同吸收峰的峰比率为特征,显示对应化学官能团在图像分析区域内的分布信息。[/font][font=宋体]近红外显微成像技术在材料、食品、医药等行业已经发挥了较大的作用,利用其进行化学成分测定及微区分析,快速、简单、直观。与扫描电镜、透射电镜、电子探针、[/font][font='Times New Roman']X[/font][font=宋体]射线衍射等其他微区分析技术相比,近红外显微成像技术具有制样简单、操作方便、快速定量、无损分析的优点。因此,作为现代分析技术,近红外显微成像技术必将得到越来越广泛的应用。如何建立适用性、稳定性更好的数学模型,实现不同仪器之间、同一仪器不同条件下的定标模型的转移,以及与其他分析技术的联用将是近红外显微成像技术的发展趋势。[/font]
[b]摘要[/b]在神经科学和神经外科中对活体大脑组织中神经元的成像能力是一项基本要求。尤其是需求一种具有测微计尺分辨率的大脑形态学的非侵入探针的开发,因为它可以在临床诊断上提供一种非侵入式光学活体组织检查的手段。在这一领域,双光子激光扫描显微镜(2PLSM)是一个强大工具,并已成为活体生物样品最小侵入性损害的高分辨率成像的标准方法。但是,(2PLSM)基于光学方法提供足够分辨率的同时,对荧光染料的需求妨碍了图像对比度的提高。本文中,我们提供了一种活体大脑组织以细胞分辨率的高对比度成像方法,无需荧光探针,使用光学三次谐波发生进行成像。我们利用细胞水平的特殊几何学和大脑组织的液体内容物来获取THG的部分相匹配,提供了一种荧光对比度机制的替代方法。我们发现THG大脑图像允许快速、无侵入性标记的神经元、白质结构、血管同时成像。而且,我们利用THG成像来引导微吸管指向活体组织中指定的神经元。这个工作是一个无标记活体大脑成像的主要步骤,并开启了活体大脑中激光引导的微注射技术发展的可能性。[b]材料与方法[/b]THG成像对于THG成像实验,我们使用了一台商业化双光子激光扫描显微镜([color=#ff0000]TrimScope, Lavision BioTec[/color])。光源是一个光学参量震荡器(Mira-OPO,APE),810nm泵浦光来自一个Ti:Sa锁模激光器(Coherent Chameleon Ultra II)。使用一个20X,0.95N.A水浸物镜(Olympus XLUMPFL-IR)将光聚焦到样品上。使用epidetection几何学描述THG实验。使用分光镜(Chroma T800lpxrxt)将背景散射THG光子从入射激光束中分离出来,用一个THG波段的带通滤波器(Chroma HQ390-70X)过滤。检测器是GaAsP高灵敏度光电倍增管(Hamamatsu H7422-40),400nm处量子效率为25%。最高分辨率成像(1024×1024像素)的典型获取时间为1.6s,我们用于目标定向实验的512 X 512像素成像时间为0.6s。 为与前向端口比较,使用了一个定制的投射端口。这个端口使用了一个1.4N.A油浸物镜,一个长波分光镜(UQG optics)和一个400nm的相干窄带滤波器。对于THG与SR-101联合实验我们用1200nm的OPO来同时产生两种信号。使用一个594nm带通和561nm隔断的分光镜将SR-101荧光从THG信号中分离。SR-101信号使用一个PMT检测(Hamamatsu H6780-20)。Nile Red和THG成像也是由1200nm的OPO同步激发。在这个案例中THG信号由投射端口测量,Nile Red荧光通过一个593∕40 nm的带宽滤波器检测。对于THG和GFP联合成像,用来泵浦OPO的Ti:Sa激光被调谐到970nm并耦合到显微镜中。组织块的GFP和THG信号使用同一个检测器连续测量。但使用一个不同的(561∕40 nm)带通滤波器检测GFP。使用显微镜软件(Imspector Pro)获取图像并以16bit 的tiff格式存储,图像分析使用Image J(MacBioPhotonics)进行。[b]主要结果[/b] [img=,575,768]http://qd-china.com/uploads/bio-product/21.jpg[/img]Fig. 1.无标记活体大脑的三次谐波显微成像(A)脑组织THG成像的epidetection几何学图示。插图:THG原理。注意基质中没有光学激发发生。(B) 树突处的聚焦激光束。通过将激光聚焦体积设定到树突直径的几倍大小,可以获得部分相匹配,显著的THG信号将会产生。(C)细胞体内的聚焦激光束。由于不好的结构相匹配状态,没有THG信号产生。(D) 小鼠大脑组织的活神经元成像。体细胞以暗影存在。 [img=,466,500]http://qd-china.com/uploads/bio-product/22.jpg[/img]Fig. 2.活体大脑组织的THG成像(A)小鼠皮质的THG图像 (B) 与A同位置的Nile Red染色的双光子荧光图像 (C) 大鼠凹陷的脑回THG图像(水平切面) (D)小鼠脑胼胝体THG图像,轴突纤维束被清晰得分辨。Movie S1是这个结构的一个3D投影 (E)小鼠大脑纹状体的THG图像(冠状面)。白质和神经元细胞清晰可见。明亮的粒状结构是垂直穿行图像平面的轴突纤维。Movie S2是这个区域的3D投影。(F)麻醉活小鼠的脑皮质上层的血管THG图像(z栈平均投影密度是50um) [img=,510,767]http://qd-china.com/uploads/bio-product/23.jpg[/img]Fig. 3. THG与双光子成像的叠加 (A)小鼠额前叶脑皮质的THG图像 (B)SR-101标记的星细胞双光子图像 (C) A、B的叠加提供了神经网络中星细胞的分布信息 (D) 小鼠额前叶皮质的THG图像 (E) GFP标记的生长抑素神经元的双光子荧光图像 (F)D、E的叠加显示了生长抑素神经元在脑前叶皮质结构中的分布 [img=,461,768]http://qd-china.com/uploads/bio-product/24.jpg[/img]Fig. 4.THG成像深度与自动化细胞检测 (A-C) 小鼠额前叶皮质的THG图像,成像深度分别为100, 200, and 300 μm 。每幅图像都是3个以2微米深度间隔独立图像的最大密度投影(D) 110 μm深度处神经元细胞的自动检测THG图像。细胞检测的运算法则定义为以红色显示的神经元 (E)红色标记:来自A-C的图像栈的细胞可见性对比。黑色标记:作为一个深度功能的平均检测到的THG密度。 [img=,531,768]http://qd-china.com/uploads/bio-product/25.jpg[/img]Fig. 5. 无标记目标定向和细胞活性(A)小鼠新大脑皮层的THG图像 (B) 在对一个神经元进行THG引导膜片钳之后同一位置的THG图像 (C)一个200um深处钳住神经元的大视野THG图像(5幅深度间隔2um的图像平均) (D)记录以100pA电流脉冲刺激B中被钳住的神经元的动力势训练 (E) 测量在THG扫描期间静止膜电位的改变。即使以最高的能量,也只观察到4%的电压变化,保持了完全的可逆性。0.8秒的周期相应于图像扫描时间。(F)最大观察到的静止膜电位Vs扫描时的激光能量。没有非线性效应出现。
激光共聚焦扫描显微镜简介一、 激光共聚焦显微镜的基本组成激光扫描共聚焦显微镜(laser scanning confocal microscope LSCM)是20世纪80年代发展起来的一项具有划时代意义的高科技新产品,是当今世界最先进的细胞生物学分析仪器。激光共聚焦显微镜利用激光作为光源,在传统光学显微镜基础上采用共轭聚焦的原理和装置,以及通过针孔的选择和PMT的收集,并带有一套对其所观察到的对象进行数字图像分析处理的系统软件。与传统光学显微镜相比,它具有更高的分辨率,实现多重荧光的同时观察并可形成清晰的三维图象等优点。所以它问世以来在生物学的研究领域中得到了广泛应用。激光共聚焦显微镜主要有四部分组成:1、显微镜光学系统。2、扫描装置。3、激光光源。4、检测系统。整套仪器由计算机控制,各部件之间的操作切换都可在计算机操作平台界面中方便灵活地进行。1.1 显微镜光学系统 显微镜是LSCM的主要组件,它关系到系统的成象质量。显微镜光路以无限远光学系统可方便地在其中插人光学选件而不影响成象质量和测量精度。物镜应选取大数值孔径平场复消色 差物镜,有利于荧光的采集和成象的清晰。物镜组的转换,滤色片组的选取,载物台的移动调节,焦平面的记忆锁定都应由计算机自动控制。1.2 扫描装置 LSCM使用的扫描装置在生物领域一般为镜扫描。由于转镜只需偏转很小角度就能涉及很大的扫描范围,图象采集速度大大提高,512×512画面每秒可达4帧以上,有利于那些寿命短的离子作荧光测定。扫描系统的工作程序由计算机自动控制。1.3 激光光源 LSCM使用的激光光源有单激光和多激光系统。多激光器系统在可见光范围使用多谱线氩离子激光器,发射波长为457nm、488nm和514nm的蓝绿光,氦氖绿激光器提供发射波长为543nm的绿光,氦氖红激光器发射波长为633nm的红光,新的405nm半导体激光器的出现可以提供近紫外谱线,但是小巧便宜而且维护简单。1.4 检测系统 LSCM为多通道荧光采集系统,一般有三个荧光通道和一个透射光通道,能升级到四个荧光通道,可对物体进行多谱线激光激发,样品发射荧光的探测器为感光灵敏度高的光电倍增管PMT,配有高速12位A/D转换器,可以做光子计数。PMT前设置针孔,由计算机软件调节针孔大小,光路中设有能自动切换的滤色片组,满足不同测量的需要,也有通过光栅或棱镜分光后进行光谱扫描功能的设置。二、激光共聚焦显微镜的特点以及在生物领域的应用传统光学显微镜相比,激光共聚焦显微镜具有更高的分辨率,实现多重荧光的同时观察并可形成清晰的三维图象等优点,在对生物样品的观察中,激光共聚焦显微镜有如下优越性:1、对活细胞和组织或细胞切片进行连续扫描,可获得精细的细胞骨架、染色体、细胞器和细胞膜系统的三维图像。2、 可以得到比普通荧光显微镜更高对比度、高解析度图象、同时具有高灵敏度、杰出样品保护。3、***图象的获得,如7 维图象(XYZaλIt): xyt 、xzt 和xt 扫描,时间序列扫描旋转扫描、区域扫描、光谱扫描、同时方便进行图像处理。 4、细胞内离子荧光标记,单标记或多标记,检测细胞内如PH和钠、钙、镁等离子浓度的比率测定及动态变化。5、荧光标记探头标记的活细胞或切片标本的活细胞生物物质,膜标记、免疫物质、免疫反应、受体或配体,核酸等观察;可以在同一张样品上进行同时多重物质标记,同时观察; 6、对细胞检测无损伤、精确、准确、可靠和优良重复性;数据图像可及时输出或长期储存。 由于共聚焦显微镜的以上优点,激光共聚焦显微镜在以下研究领域中应用较为广泛:1、细胞生物学:如:细胞结构、细胞骨架、细胞膜结构、流动性、受体、细胞器结构和分布变化、细胞凋亡机制;各种细胞器、结构性蛋白、DNA、RNA、酶和受体分子等细胞特异性结构的含量、组分及分布进行定量分析;DNA、RNA含量、利用特定的抗体对紫外线引起的DNA损伤进行观察和定量;分析正常细胞和癌细胞细胞骨架与核改变之间的关系;细胞黏附行为等 2、生物化学:如:酶、核酸、受体分析、荧光原位杂交、杂色体基因定位等,利用共聚焦技术可以取代传统的核酸印迹染交等技术,进行基因的表达检测,使基因的转录、翻译等检测变的更加简单、准确。3、药理学:如:药物对细胞的作用及其动力学;药物进入细胞的动态过程、定位分布及定量 4、生理学、发育生物学:如:膜受体、离子通道、离子含量、分布、动态;动物发育以及胚胎的形成,骨髓干细胞的分化行为;细胞膜电位的测量.荧光漂白恢复(FRAP)、荧光漂白丢失(FLIP)的测量等。 5、遗传学和组胚学:如:细胞生长、分化、成熟变化、细胞的三维结构、染色体分析、基因表达、基因诊断; 6、神经生物学:如:神经细胞结构、神经递质的成分、运输和传递; 7、微生物学和寄生虫学:如:细菌、寄生虫形态结构; 8、病理学及病理学临床应用:如:活检标本的快速诊断、肿瘤诊断、自身免疫性疾病的诊断; 9、免疫学、环境医学和营养学。如:免疫荧光标记(单标、双标或三标)的定位,细胞膜受体或抗原的分布,微丝、微管的分布、两种或三种蛋白的共存与共定位、蛋白与细胞器的共定位;对活细胞中的蛋白质进行准确定位及动态观察可实时原位跟踪特定蛋白在细胞生长、分裂、分化过程中的时空表达,荧光能量共转移(FRET)。

http://ng1.17img.cn/bbsfiles/images/2017/10/2016082816541190_01_3092793_3.jpg YEESPEC智能细胞成像系统已全面升级:强大的配置与功能,高品质成像质量,更方便的显微操作,绝对能带给您眼前一亮的全新体验。 作为新一代的智能细胞成像系统,它比传统显微镜操作要方便许多,所有的操作工程都可以通过前面的触摸控制屏完成。只要轻轻地点几下屏幕,就可以轻松地完成整个细胞成像过程,包括:镜头切换、荧光切换、聚焦。 同时,因为设计的小巧,我们也可以把它放在培养箱或者安全柜里使用,可以边做实验室边观察。 YEESPEC智能细胞成像系统,更是科研的得力助手。与传统活细胞工作站相比,它具有更强大的功能特点。 1、 操作方便,即开即用: 采用全触控屏操作,也可以通过手机端平板端进行操作;荧光光源采用高亮度LED光源,不需要预热。 2、 成像质量好,光路的主要元器件均采用原装进口: 采用顶级CCD芯片、原装进口长工作距离荧光物镜、Omega荧光滤光片、K9光学玻璃载物台,透过率非常高。 3、 没有耗材,使用成本低: 采用高亮度白色LED,荧光光源采用高亮度单色LED。LED的寿命是5万个小时以上,基本上仪器买回去10年都不用更换。 4、保证实验安全: 内部装有两块10000mAh,12V的电池,短时间观察使用时可以不需要接电源,即使停电也可以完成实验,保证了实验安全。
BX51显微成像系统有些什么技术要求?采购注意事项?如有报价可联系QQ:809585384.
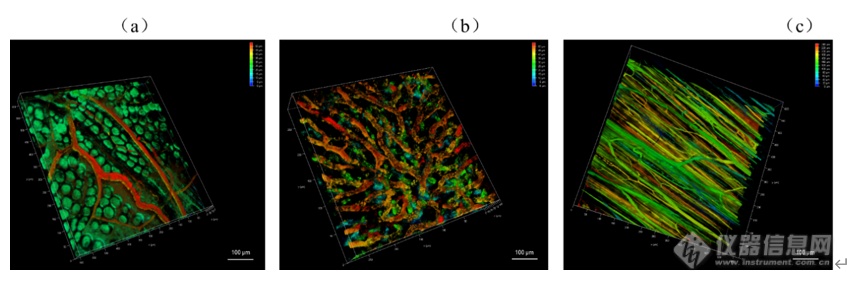
[align=center][b]双光子激光扫描显微镜的检测模式及其在生物医学领域的应用[/b][/align][align=center][font=宋体]刘皎[/font][sup]1[/sup],吴晶[sup]1[/sup][/align][align=center]1. [font=宋体]北京大学医药卫生分析中心,北京,[/font]100191[/align][b][font=黑体][[/font]摘要] [/b]双光子激光扫描显微镜(two-photon laser scan microscope, TPLSM[font=宋体])具有低光毒性、高时空分辨率、高信噪比等优点,结合了激光扫描共聚焦显微镜和双光子激发技术,广泛应用于脑科学、免疫学、肿瘤、胚胎发育等生物医学相关研究领域。本文结合作者所在的北京大学医药卫生分析中心共聚焦平台的工作经验,概述了[/font]TPLSM适用的样本、检测模式以及在生物医学领域的应用,以期为相关科研技术人员提供参考。[b][font=&][Abstract][/font] [/b]Two-photon laser scan microscopy (TPLSM) has the advantages of low phototoxicity, high spatial and temporal resolution, and high signal-to-noise ratio.TPLSM combines laser scanning confocal microscopy with two-photon excitationtechnology and it is widely used in brain science, immunology, tumor, embryodevelopment and other biomedical related research fields. Based on the author'swork experience in the confocal center of Peking University Medical and HealthAnalysis Center, this paper summarizes the applicable samples, detection modesand applications of TPLSM in the biomedical field, in order to provide referencefor related scientific researchers and technicians.[b][font=黑体][[/font]关键词] [/b]显微镜双光子,检测模式,应用[b]1 引言[/b]双光子激发技术的基本原理是在高光子密度情况下,荧光分子可同时吸收2个长波长光子,产生一个一半波长光子去激发荧光分子的相同效果。双光子激光扫描显微镜(two-photon laser scan microscope, TPLSM[font=宋体])在激光扫描共聚焦显微镜的基础上,以红外飞秒激光作为光源,长波长的近红外激光受散射影响小,易穿透标本,可深入组织内部非线性激发荧光,对细胞毒性小且具有高空间分辨率,适合生物样品的深层成像及活体样品的长时间观察成像[/font][1]。使用高能量锁模脉冲激光器,物镜焦点处的光子密度最高,在焦点平面上才有光漂白及光毒性,焦点外不损伤细胞。双光子效应只发生在焦点处,所以双光子显微镜无需共聚焦针孔,也能做到点激发点探测,提高了荧光检测效率[2]。[b][/b]双光子激光扫描显微镜显微镜可以通过XYZ,XYT,XYλ,XYZT,XYλT等多种模式实现多维成像,亦可进行更复杂实验的拍摄,比如二次谐波成像(Second Harmonic Generation Imaging,SHG[font=宋体])、双光子荧光寿命成像([/font]Two-photon Fluorescence Lifetime Imaging Microscopy, TP-FLIM[font=宋体])、荧光寿命[/font]-[font=宋体]荧光共振能量转移成像([/font]FluorescenceLifetime - Fluorescence Resonance Energy Transfer Imaging, FLIM-FRET[font=宋体])等实验以满足对样品的定性、定量、定位、共定位等多维度多功能的研究。[/font]TPLSM已成为生命科学各领域重要的研究工具,可在细胞及亚细胞水平对活体动物的神经细胞形态结构、离子浓度、细胞运动、分子相互作用等生理现象进行直接的长时间成像监测,还能进行光激活染及光损伤等光学操纵,广泛应用于脑科学、免疫学、肿瘤、胚胎发育等生物医学相关研究[3-5]。本文拟通过按TPLSM常见的检测模式分别阐述其在生物医学领域的应用,以其为相关科研技术人员提供参考。[b]2. TPLSM适用的样本[/b]TPLSM适用的样本非常广泛,从液体、固体等形式的材料或制剂、细菌、细胞、细胞团、类器官、组织切片、到各种模式动物(如线虫、果蝇、斑马鱼、小鼠、大鼠、兔、猴等)及其[font=宋体]脑、脊髓、肝脏、肺、皮肤等器官[/font],都可以通过搭载不同载物台进行测试。相对于传统激光扫描共聚焦显微镜200μm的成像深度极限,双光子显微镜成像深度可达800μm,如果是透明化样品可更厚。TPLSM尤其适合活体动物成像,且比小动物荧光成像有更高的分辨率和信噪比,一般TPLSM的XY轴分辨率为200 nm左右,Z轴分辨率为300 nm左右。[b]3. TPLSM的检测模式[/b]3.1 二维成像模式TPLSM可以实现点扫描、点探测,得到生物样品高反差、高分辨率、高灵敏度的二维图像,从而获得细胞/组织等光学切片的物理、生物化学特性及变化。也可以对所感兴趣的区域进行准确的定性、定量及定位分析。激光扫描显微镜的zoom功能,可以用来调节扫描区域的放大倍数。但受物镜分辨率的限制,一味的增大zoom值,不能得到相应的高清图像,需根据实际情况参考piexl size进行设定。TPLSM可以实现XY、XZ或XT的二维成像模式,XT线扫会在后文与XYT时间序列成像一起进行举例说明(图2b)。3.2 三维成像模式3.2.1 Z轴序列三维成像(XYZ)[align=left]TPLSM可沿Z轴方向通过电动载物台的连续扫描对样品进行无损伤的光学切片(XYZ),获得三维立体图像。同理,通过沿Y轴方向连续扫描,可获得连续的XZY图像。如图1所示TPLSM[font=宋体]可以顺利观察到可以观察到血管清晰形态结构:单个胚胎的胎盘微血管(图[/font]1a)、肝脏血窦微血管(图1b)和后肢微血管(图1c)[6]。[/align][align=center][img=,690,230]https://ng1.17img.cn/bbsfiles/images/2022/12/202212151626576232_4807_3237657_3.png!w690x230.jpg[/img][/align][align=center]图1(a)胚胎胎盘微(b)肝脏血窦和(c)后肢的微血管三维成像[/align]3.2.2 时间序列扫描模式(XYT)[align=left]按照一定的时间间隔重复采集,则可实现对该样品的实时监测(XYT)。此类实验可观察组织区域内特异荧光探针标记的单个细胞或细胞内不同部位接受刺激后的整个变化过程。[font=宋体]如图[/font]2[font=宋体]([/font]a[font=宋体]),可以根据微血管[/font]XYT[font=宋体]序列扫描的成像结果中某一血细胞在前后两张图的位置移动和这两帧图的扫描时间间隔计算血流速度。若血流速度很快,[/font]XYT扫描不足以捕捉实际流速,可以使用XT线扫计算。如图2(b),微血管XT扫描图像中绿色荧光背景里的黑色线条代表单个血细胞的流动轨迹,每条线条的横坐标代表血细胞移动的距离(distance / μm[font=宋体]),纵坐标代表此段时间([/font]time/ ms[font=宋体]),根据这两个数据可以计算出单位时间内血细胞的流动速度([/font]μm / ms)[6]。[/align][align=center][img=,690,262]https://ng1.17img.cn/bbsfiles/images/2022/12/202212151627102569_8367_3237657_3.png!w690x262.jpg[/img] [/align][align=center]图2 微血管(a)XYT扫描结果和(b)XT一维扫描结果图像计算血流说明示意图[/align]3.2.3 光谱扫描模式(XYλ/XYΛ)通常配置有可调节接受范围的检测器的TPLSM,可以实现从400nm-800nm的发射波谱扫描。通过配置具有连续可调波长的双光子激光器,还可以实现750nm-1300nm激发波谱扫描。这对于开发研制特殊染料探针的课题来说是很方便、全面的检测功能。3.3四维成像模式(XYZT/XYλT/XYΛT)基于上述三维成像模式,结合时间序列扫描,可以实现TPLSM的四维成像。3.4二次谐波成像(SHG)SHG是一个二阶非线性过程,且一般为非共振过程,适合富含胶原纤维的样本成像,如角膜、鼠尾肌腱、皮肤等。生物组织产生的二次谐波最主要的转换源自胶原,不同生物组织中的二次谐波信号强弱与组织中的胶原含量密切相关,含胶原丰富的组织包括结缔组织和肌肉组织等二次谐波信号也比较强,另外还有一些能产生强二次谐波的生物结构是微管,如细胞分裂中纺锤体。对于具有中心对称性的生物结构,如果局部中心对称性的破坏也会产生二次谐波:在两中心对称介质的界面,不同物态分子的相互作用使局部微观场特性在交界面(如细胞膜)发生突变,从而产生界面二次谐波[7]。除了动物组织外,一些含有特殊分子结构的植物组织也能产生二次谐波。二次谐波显微成像具有高空间分辨率、深成像深度、低损伤、以及对结构对称性的高度敏感性的特点,如果能与其他成像技术结合,将成为生物样品研究的有力工具[8]。3.5双光子荧光寿命成像(TP-FLIM)[9]FLIM技术是研究细胞内生命活动状态的一种非常可靠的方法。荧光寿命是荧光团在返回基态之前处于激发态的平均时间,是荧光团的固有性质,因此其不受探针浓度、激发光强度和光漂白效应等因素影响,且能区分荧光光谱非常接近的不同荧光团,故具有非常好的特异性和很高的灵敏度。此外,由于荧光分子的荧光寿命能十分灵敏地反映激发态分子与周围微环境的相互作用及能量转移,因此FLIM技术常被用来实现对微环境中许多生化参数的定量测量,如细胞中折射率、黏度、温度、pH值的分布和动力学变化等,这在生物医学研究中具有非常重要的意义。目前FLIM技术在细胞生物学中一些重要科学问题的研究、临床医学上一些重大疾病的诊断与治疗研究以及纳米材料的生物医学应用研究等方面均有广泛应用,并取得了许多利用传统的研究手段无法获取的数据。FLIM检测需要脉冲激光,TPLSM带有的高能量锁模脉冲激光器可以满足激发要求。3.6荧光寿命-荧光共振能量转移成像(FLIM-FRET)[10]传统的FRET过程分析通常是基于荧光强度成像来实现,分析的结果容易受光谱串扰的影响。而将FLIM技术应用于FRET过程分析,利用FLIM技术可定量测量这一优势,可非常灵敏地反映供体荧光分子与受体荧光分子之间的能量转移过程。当受体分子与供体之间的距离10nm时,供体的能量转移到受体,受体从基态发生能量跃迁,从而影响供体的荧光寿命。与没有受体分子的时候相比,发生FRET的供体分子的荧光寿命降低。因此,FRET-FLIM联合能够实时监测生物细胞中蛋白质的动态变化,如蛋白质折叠、分子间(蛋白-蛋白,蛋白-核酸)相互作用和细胞间信号分子传递、分子运输以及病理学研究等。[b]4 结论和展望[/b]综上,TPLSM应用灵活,具备多种检测模式,适用于多种样本,亦可实现多种实验目的,如荧光的定量、定性、定位、共定位,动态荧光的测定等。一些特殊的实验模式,将TPLSM在生物医学领域的应用进一步扩大。通过结合其他技术(多手段联合拓展,如膜片钳、原子力显微镜、光电联用等),TPLSM必将成为助力生物医学领域研究的有力工具。双光子荧光成像由于具有天生的三维层析能力以及深穿透能力,在活体生物组织成像上广受欢迎。双光子显微镜镜下空间增大后,可广泛应用于猴、大小鼠、兔等较大的模式动物的活体成像。且可结合电生理技术、光遗传技术,广泛应用于麻醉、清醒或运行行为等生理状态下的动物脑科学神经相关研究,在单细胞、单树突精度上对神经元群体活动进行监控。如结合膜片钳技术,对活体脑组组急性切片神经元进行双光子深层成像[11];结合光遗传技术,实现视觉皮层同一神经元和神经元群体的稳定操控和长期多次重复记录[12];对在健身球上移动的头部固定小鼠小脑进行成像,探讨觉醒状态和运动行为对胶质网络中钙离子的激发的影响[13];结合多种疾病模型,探讨大脑皮层神经元及胶质细胞活性的改变及作用等[14]。随着多种双光子显微镜系统的出现,双光子显微镜成像技术将以其实时、无损地探测、诊断及检测能力,在生物医药及临床医学应用中发挥更大作用。[b]参考文献[/b][1] [font=宋体]李娟[/font],[font=宋体]张岚岚[/font],[font=宋体]吴珏珩[/font].[font=宋体]双光子显微镜的应用优势与维护要素[/font][J].[font=宋体]中国医学装备[/font],2021,18(12):158-163.[2] HendelT,Mank M, Schnell B,et al.Fluorescence changes of genetic calcium indicatorsand OGB1correlated with neural ac tivity and calcium in vivo and in vitro[J].JNeurosci, 2008,28(29):7399-7411.[3] DolginE.What leva lamps and vinaigrette can teach us about cellbiology[J].Nature,2018,555(7696):300-302.[4] Noguchi J,Nagaoka A, Watanabe S,et al.in vivo two-photon uncaging of glutamate revealingthe structure-function relatio nships of dendritic spines in the neocortex ofadult mice[J]. J Physiol,2011,589(Pt 10):2447-2457.[5] BishopD,Nikiél, Brinkoetter M,et al.Nearinfrared branding efficiently correlateslight and electron microscopy[J]. Nat Methods,2011,8(7):568-570.[6] [font=宋体]刘皎[/font],[font=宋体]丛馨[/font],[font=宋体]何其华[/font].[font=宋体]活体小鼠微血管血流倒置双光子激光扫描显微镜检测方法的建立[/font][J].解剖学报,2022,53(02):261-265.[7] [font=宋体]屈军乐[/font],[font=宋体]陈丹妮[/font],[font=宋体]杨建军[/font],[font=宋体]许改霞[/font],[font=宋体]林子扬[/font],[font=宋体]刘立新[/font],[font=宋体]牛憨笨[/font].[font=宋体]二次谐波成像及其在生物医学中的应用[/font][J].[font=宋体]深圳大学学报[/font],2006,(01):1-9.[8] [font=宋体]孙娅楠[/font],[font=宋体]赵静[/font],[font=宋体]李超华[/font],[font=宋体]等[/font].[font=宋体]二次谐波结合双光子荧光成像方法观察人源胶原蛋白透皮吸收情况[/font][J].激光生物学报,2017,26(1):24-29.[9] [font=宋体]刘雄波,林丹樱,吴茜茜,严伟,罗腾,杨志刚,屈军乐,荧光寿命显微成像技术及应用的最新研究进展。物理学报,[/font]2018,67(17):178701-1-178701-14[10] [font=宋体]罗淋淋,牛敬敬,莫蓓莘,林丹樱,刘琳,荧光共振能量转移[/font]-荧光寿命显微成像(FRET-FLIM[font=宋体])技术在生命科学研究中的应用进展。光谱学与光谱分析,[/font]2021,41(4):1023-1031[11] Isom-BatzG,Zimmem PE.Collagen injection for female urinary incontinence after urethralor periurethral surgery[J].J Unol,2009,181(2):701-704.[12] JuN,Jiang R,Mrcknik SL,et al.Long-term all-optical interrogation of corticalneurons in awake-behaving nonhuman prim ates[J].LOSBiology,2018,16(8):e2005839.[13]Nimmerjahn A,Mukamel EA, Schnitzer MJ.Motor behavior activates Bergmann glialnetworks[J].Neuron,2009,62(3):400-412.[23] Huang L, Lafaille JJ, YangG.LearningDependent dendritic spine plasticity is impaired in spontaneousautoimmune encep halomyelitis[J].Dev Neurobiol,2021,81(5):736-745.[14] Huang L,Lafaille JJ,Yang G.LearningDependent dendritic spine plasticity is impaired inspontaneous autoimmune encep halomyelitis[J].Dev Neurobiol, 2021,81(5):736-745.
[url=http://www.f-lab.cn/vivo-imaging/msot.html][b]小动物光声成像系统MSOT[/b][/url]是全球唯一能够提供[b]小动物全身光声成像[/b]能力的小动物[b]实时光声成像系统[/b],用于临床前小动物成像和临床前研究。小动物光声成像系统能够可帮助生物过程和药理物质作用在体内,在深部组织中高分辨率下实时观察。小动物光声成像系统是全球唯一[b]混合光声超声成像技术,OPUS成像[/b]技术的同类仪器,也是世界上第一个[b]交叉断层成像系统[/b],提供非平行的用户独立的图像质量,并且具有实时性,可以获得整个动物的横截面影像。[img=小动物光声成像系统]http://www.f-lab.cn/Upload/MOST-invision-imaging.JPG[/img][img=小动物光声成像系统]http://www.f-lab.cn/Upload/Hybrid-OPUS-IMAGING.jpg[/img]小动物光声成像系统:[url]http://www.f-lab.cn/vivo-imaging/msot.html[/url]
(一)阿贝成像原理 为了理解相差尼康显微镜的原理,不得不回顾普通显微镜的成像原理。德国光学家阿贝(E. Abbe)从1874年以后创立了成像原理.在现代波动光学的发展基础上兴起的变换光学中的空间信息滤波和信息处理概念,就是奠基于阿贝成像原理。 据阿贝的看法,尼康显微镜的透镜或透镜组不只是反映物平面和像平面的共扼关系,而且也反映透镜前后的无数个对应平面的共扼关系。当然,显微镜的成像光路中最为重要的共扼面还是物平面和像平面(图10-18,0--0').显微镜成像光路中同样具有重要的共扼面是发光平面((KY1000显微镜)和光源的像平面(L')。 但是如果在显徽镜结构中在聚光镜的前焦面上放置孔径光栏时,那么光源和光源像两平面的共辘关系,代之以聚光镜前焦面的光栏平面和物镜后焦面的L"平面的共扼关系。 阿贝认为发光平面的共扼面即L’平面,是显微镜的初级成像平面,而物平面是次级成像平面。若通俗一点来讲,L‘烛光是L烛光的像,而O‘空间是L'烛光的像。 如果我们在尼康显微镜的初级成像光路上在聚光镜和物镜之间,擂入一张不同光密度的标本O(图10-20上是光栅)时,立即破坏了初级成像光路.这是因为标本细节的光密结构(栅)和光疏结构(间隙)的折射率不同,而产生光的衍射。其结果如图10-20所示,L烛光在它的像平面上出现了数支烛光。与此同时,在像平面上出现标本0的干涉像.这些干涉纹是由次波源。,一1,+1发射的衍射光的重叠所造的。这样由于标本的干涉次级成像过程,已由CM100的共扼面改变成CM300FL的共扼面。也就是说像平面上不是L,的像,而是标本0的像了。 总之,相干成像过程的第一步是形成衍射斑,而第二步是相干干涉.当然未染色生物标本细节的折射率有很小的差异,在像平面上的对比度非常小。为了提高物像的对比度(反差),荷兰物理学家(F. Zernike(1935)设计了相差显微镜的基本部件如环状光栏和位相板。 从阿贝成像原理已经知道尼康显微镜的聚光镜前焦面上放置孔径光栏时,这个平面就成为物镜后焦面的共扼面。F. Zernike在这个平面上放置了环状光栏,按空间滤波概念,称带通滤波器。 环状光栏给物镜后焦面提供的是照射在环形甲像平面上的相干光束。照射在环形像平面上的相图10-20显徽镜的成像光路干光束,不同于线形窄缝所提供的相干光束.前者不能造成带有方向性衍射斑.在共扼面上的光分布强度也不像窄缝衍射那种零级强度。它所造成的衍射光是均匀的无方向性的. F. Zernike在相差尼康显微镜的物镜后焦面上放置了位相板。恰巧位相板的吸收环变成环状光栏的成像平面。其结果就像F. Zernike指出的,如果人工地改变照射到不吸光物体而形成初级成像光束的光波,以此来改变衍射光和直射光的位相和振幅,使之近似乎吸光物体的初级成像光束时,那么其结果就造成完全像吸光物体的次级成像,也就是加强了物体细节的反衬度。巧妙地使用位相板,就能够使物像平面上的光强度分布与物体细节的位相信息成为线性关系.也就是人工地用物体细节的位相分布调整像平面的光强分布。甚至巧妙地选配不同类型的位相板,使之适合于物体细节的折射率时,可以强使物像平面上的反衬度出现逆转,即由明反差改变为暗反差,或者反之。
[align=left][font=宋体][color=#374151]摘要:光学显微成像技术在神经科学研究中发挥着不可或缺的作用。文章将深入探讨两种主要的光学显微成像技术,即荧光显微镜和多光子显微镜,在神经科学领域的应用案例。我们首先介绍了这些技术的基本原理和发展历程,然后详细描述了它们在神经细胞成像、突触可塑性研究和脑功能成像中的应用。通过这些案例,我们展示了光学显微成像技术在神经科学研究中的重要性,以及它们对我们深入理解神经系统的贡献。[/color][/font][/align][font=宋体][color=#374151]关键词:神经科学、荧光显微镜、多光子显微镜、神经细胞成像[/color][/font][font=宋体][color=#374151]光学显微成像技术自17世纪以来一直在科学研究中扮演着重要的角色。随着技术的不断发展,光学显微镜已经成为许多科学领域的核心工具之一,尤其在生命科学和神经科学领域。文章将深入探讨光学显微成像技术在神经科学研究中的应用案例,重点介绍荧光显微镜和多光子显微镜这两种主要技术的原理和应用。[/color][/font][font=宋体][color=#374151]一、光学显微成像技术应用[/color][/font][font=宋体][color=#374151]1.荧光显微镜的应用[/color][/font][font=宋体][color=#374151]荧光显微镜是一种广泛应用于神经科学研究的工具,它使用荧光染料或标记物来可视化和研究神经系统的结构和功能。以下是荧光显微镜在神经科学研究中的应用案例,包括神经细胞成像、突触可塑性研究、脑疾病研究等方面。[/color][/font][font=宋体][color=#374151](1)神经细胞成像[/color][/font][font=宋体][color=#374151]荧光显微镜在观察和研究神经细胞的结构和功能方面发挥了关键作用。通过使用荧光标记的抗体或分子探针,研究人员可以可视化神经元的不同结构,包括轴突、树突、细胞核等。这有助于研究神经细胞的形态特征以及它们在不同生理条件下的变化。[/color][/font][font=宋体][color=#374151](2)突触可塑性研究[/color][/font][font=宋体][color=#374151]荧光显微镜在突触可塑性研究中也具有重要应用。突触可塑性是指突触的结构和功能如何受到刺激和学习的影响。通过标记突触相关的蛋白质或分子,研究人员可以实时观察突触的变化,如突触增强或突触抑制,以深入理解学习和记忆的神经机制。[/color][/font][font=宋体][color=#374151](3)脑功能成像[/color][/font][font=宋体][color=#374151]荧光显微镜在脑功能成像方面也具有潜力。通过将钙指示剂或光遗传学标记物引入神经元,研究人员可以实时监测神经元的活动。这种技术使我们能够理解大脑不同区域的活动模式,以及不同刺激下神经元的响应。这对于研究认知过程、行为和神经疾病有着重要意义。[/color][/font][font=宋体][color=#374151](4)神经干细胞研究[/color][/font][font=宋体][color=#374151]荧光显微镜也被广泛用于研究神经干细胞。通过标记和追踪神经干细胞的命运和分化过程,研究人员可以理解神经系统的发育和再生机制。这对于神经系统修复和治疗神经系统疾病具有潜在应用。[/color][/font][font=宋体][color=#374151](5)荧光标记的蛋白表达[/color][/font][font=宋体][color=#374151]荧光显微镜也可用于研究不同蛋白质在神经系统中的表达和定位。通过使用荧光标记的蛋白表达技术,研究人员可以观察不同蛋白质的分布和相互作用,从而深入理解神经系统中的信号传导和调控。[/color][/font][font=宋体][color=#374151](6)脑疾病研究[/color][/font][font=宋体][color=#374151]荧光显微镜在研究脑疾病方面也发挥着关键作用。研究人员可以使用荧光显微镜来研究神经系统疾病的病理机制,如帕金森病、阿尔茨海默病和精神分裂症。这有助于发现潜在的治疗方法和药物筛选。[/color][/font][font=宋体][color=#374151]荧光显微镜在神经科学研究中的应用是多方面的,涵盖了神经细胞成像、突触可塑性研究、脑功能成像、神经干细胞研究、蛋白质表达和脑疾病研究等多个领域。这一技术为神经科学家提供了非常强大的工具,帮助他们深入理解神经系统的结构和功能,以及与神经相关的疾病的机制。未来,随着技术的不断发展,荧光显微镜将继续在神经科学领域中发挥关键作用,为我们揭示神经系统的奥秘提供更多的洞察力。[/color][/font][font=宋体][color=#374151]2.多光子显微镜的应用[/color][/font][font=宋体][color=#374151]多光子显微镜(Multi-Photon Microscopy)是一种先进的成像技术,它利用非线性光学效应,如多光子吸收,为神经科学家提供了强大的工具,用于研究神经系统的结构和功能。相比传统的荧光显微镜,多光子显微镜具有许多显著的优势,包括更深的成像深度、较少的光损伤、更少的荧光标记物和更高的空间分辨率。以下是多光子显微镜在神经科学研究中的应用领域:[/color][/font][font=宋体][color=#374151](1)脑功能成像[/color][/font][font=宋体][color=#374151]脑功能成像是多光子显微镜的一个主要应用领域。这种技术允许研究人员实时观察活体动物的脑活动,包括神经元的兴奋与抑制、突触传递和脑区之间的相互作用。多光子显微镜能够提供高分辨率的三维图像,而无需使用荧光标记物。这对于研究大脑的基本功能、学习和记忆等过程至关重要。[/color][/font][font=宋体][color=#374151](2)钙离子成像[/color][/font][font=宋体][color=#374151]钙离子在神经元内起着关键的信号传导作用。多光子显微镜可以用于监测神经元内的钙离子浓度变化,这对于理解神经元的兴奋性和突触传递至关重要。通过使用荧光钙染料,研究人员可以实时观察神经元内钙离子浓度的动态变化,以及不同神经元之间的协同作用。[/color][/font][font=宋体][color=#374151](3)神经元形态学研究[/color][/font][font=宋体][color=#374151]多光子显微镜在研究神经元的形态学和结构上也具有独特的优势。它可以提供高分辨率的三维成像,允许研究人员详细观察神经元的分支结构、突触连接和细胞器的分布。这对于理解神经元的连接方式、发展和退行性疾病的机制至关重要。[/color][/font][font=宋体][color=#374151](4)活体动物模型研究[/color][/font][font=宋体][color=#374151]多光子显微镜也在活体动物模型研究中发挥着关键作用。研究人员可以使用这种技术观察小鼠、果蝇等模型动物的脑活动,从而研究不同物种的神经系统功能和行为。这对于神经药理学、疾病建模和药物筛选具有重要意义。[/color][/font][font=宋体][color=#374151](5)细胞内成像[/color][/font][font=宋体][color=#374151]多光子显微镜也可用于单个神经元或突触的细胞内成像。这允许研究人员观察细胞内的亚细胞结构、蛋白质运输和突触形成等过程。这对于研究神经元的分子机制和突触可塑性非常有帮助。[/color][/font][font=宋体][color=#374151]多光子显微镜的应用领域不仅局限于神经科学,还扩展到其他生命科学领域,如细胞生物学、免疫学和生物医学研究。其高分辨率和深层成像能力使其成为许多领域中不可或缺的工具。[/color][/font][font=宋体][color=#374151]尽管多光子显微镜在神经科学研究中具有巨大的潜力,但它也面临着一些挑战。其中之一是成像速度,尤其在观察大脑活动时,需要高速成像以捕捉快速的神经事件。另一个挑战是数据处理和分析,因为高分辨率、三维和四维成像产生了大量的数据,需要强大的计算资源和分析工具。[/color][/font][font=宋体][color=#374151]未来,我们可以期待多光子显微镜技术的不断改进和发展,以应对这些挑战。新的激光技术、荧光标记物和成像算法将继续推动这一领域的进展,为我们深入理解神经系统的复杂性提供更多的洞察力。多光子显微镜将继续在神经科学领域中发挥关键作用,有望帮助我们解决一些最具挑战性的神经科学问题。[/color][/font][font=宋体][color=#374151]二、光学显微成像技术在神经科学研究中的应用存在问题[/color][/font][font=宋体][color=#374151]光学显微成像技术在神经科学研究中的应用虽然具有众多优势,但也存在一些问题和挑战,这些问题需要科研人员不断努力来解决。以下是一些存在问题:[/color][/font][font=宋体][color=#374151]1.有限的成像深度[/color][/font][font=宋体][color=#374151]传统的光学显微成像技术受到光的折射和吸收的限制,导致成像深度受到限制。这在研究深层脑区时成为问题,因为光无法有效透过多层组织,导致深层神经元无法清晰成像。多光子显微镜已经在这一方面取得了进展,但仍然存在深度限制。[/color][/font][font=宋体][color=#374151]2.光损伤和毒性[/color][/font][font=宋体][color=#374151]荧光标记物和强光源在成像过程中可能对生物样本产生光损伤和毒性作用。这对于活体成像和长时间观察是一个挑战,因为它可能导致样本的退化和死亡。科研人员需要努力寻找更温和的成像方法和标记物,以减轻这些问题。[/color][/font][font=宋体][color=#374151]3.数据量庞大[/color][/font][font=宋体][color=#374151]高分辨率和多维成像技术产生大量的数据,需要强大的计算资源和复杂的数据分析工具。处理和管理这些数据可能是一个挑战,尤其是在长期实验和大规模成像项目中。[/color][/font][font=宋体][color=#374151]4.标记物的选择[/color][/font][font=宋体][color=#374151]合适的荧光标记物对于获得高质量的成像数据至关重要。然而,选择适当的标记物可能会受到限制,因为一些标记物可能会干扰样本的正常生理活动,或者不适合特定的实验条件。因此,需要不断开发新的标记物和成像方法。[/color][/font][font=宋体][color=#374151]5.解析度限制[/color][/font][font=宋体][color=#374151]光学显微成像的分辨率受到光的波长限制,通常受到绕射极限的限制。虽然一些超分辨率成像技术已经出现,但它们仍然无法突破光学分辨率极限。这可能会限制对神经系统微观结构的精确观察。[/color][/font][font=宋体][color=#374151]6.活体成像的挑战[/color][/font][font=宋体][color=#374151]对于活体成像,尤其是在大脑中,样本的运动和呼吸等因素可能导致成像失真。稳定和精确定位样本是一个技术挑战。[/color][/font][font=宋体][color=#374151]尽管存在这些问题,光学显微成像技术仍然是神经科学研究的不可或缺的工具,因为它们提供了独特的实时、高分辨率和非侵入性的成像能力。科研人员不断努力解决这些问题,通过技术创新和改进,光学显微成像技术有望继续为神经科学领域的研究提供更多洞察力。[/color][/font][font=宋体][color=#374151]三、下一步研究方向[/color][/font][font=宋体][color=#374151]基于上述问题,光学显微成像技术在神经科学研究中的应用仍然需要不断改进和发展。下面是可能的下一步研究方向,以解决这些问题:[/color][/font][font=宋体][color=#374151]1.改进成像深度[/color][/font][font=宋体][color=#374151]研究人员可以探索新的成像方法,如双光子显微镜和光学波前调制成像,以增加成像深度。此外,开发新的光学透明样本制备技术,如透明大脑样本技术,可以帮助克服深度限制问题。[/color][/font][font=宋体][color=#374151]2.减少光损伤和毒性[/color][/font][font=宋体][color=#374151]研究人员可以寻找更温和的成像条件,减少光损伤和荧光标记物的毒性。此外,使用先进的成像系统,如自适应光学成像,可以减小激光功率,同时保持高分辨率。[/color][/font][font=宋体][color=#374151]3.数据管理和分析工具[/color][/font][font=宋体][color=#374151]开发更强大的数据管理和分析工具,以处理庞大的成像数据。机器学习和深度学习方法可以帮助提高数据分析的效率,并自动检测和量化细胞和结构。[/color][/font][font=宋体][color=#374151]4.标记物的改进:寻找更多、更具选择性的标记物,以减少对样本的干扰。这可以包括荧光标记物的改进、发展新的基因表达标记和探测技术。[/color][/font][font=宋体][color=#374151]5.突破分辨率极限[/color][/font][font=宋体][color=#374151]进一步发展超分辨率成像技术,以突破传统光学分辨率极限,获得更高的细节分辨率。例如,结构光显微镜和单分子成像技术可以帮助提高分辨率。[/color][/font][font=宋体][color=#374151]6.活体成像技术改进:研究人员可以探索新的样本固定和稳定技术,以减小样本运动对成像的影响。另外,开发新的活体成像方法,如头部悬置成像和小型显微成像技术,可以帮助在动态活体条件下进行成像。[/color][/font][font=宋体][color=#374151]7.多模态成像[/color][/font][font=宋体][color=#374151]结合不同的成像技术,如光学显微镜与电生理记录、光学显微镜与功能磁共振成像(fMRI)等,以获得更全面的神经科学数据。[/color][/font][font=宋体][color=#374151]8.多尺度成像[/color][/font][font=宋体][color=#374151]开发多尺度成像方法,能够在微观和宏观水平上同时观察神经系统的活动,从神经元到整个脑区。[/color][/font][font=宋体][color=#374151]这些研究方向代表了改进和扩展光学显微成像技术在神经科学研究中的应用的可能途径。通过不断的技术创新和跨学科合作,神经科学家和工程师有望克服这些问题,提高光学显微成像技术的效能和应用广度,以更深入地理解神经系统的复杂性。[/color][/font][font=宋体][color=#374151]四、结论[/color][/font][font=宋体][color=#374151]光学显微成像技术在神经科学研究中的应用案例清楚地表明,这些技术在揭示神经系统的复杂性和功能中起到了关键作用。然而,这仅仅是一个开始,未来仍有许多挑战和机遇等待我们探索。例如,新的成像技术和荧光标记方法的不断发展将进一步扩展我们的研究领域。此外,将光学显微成像技术与其他分子生物学和生物化学技术相结合,可以更全面地理解神经系统的功能。[/color][/font][font=宋体][color=#374151]在未来,我们可以期待更高分辨率、更深层次的成像以及更多三维和四维成像的发展。这将有助于解决神经科学中的一些最具挑战性的问题,如神经网络的复杂性和神经退行性疾病的机制。光学显微成像技术将继续为神经科学研究提供有力的工具,推动我们对大脑和神经系统的理解不断深入。[/color][/font][font=宋体][color=#374151]参考文献:[/color][/font][font=宋体][color=#374151][1]高宇婷,潘安,姚保利等.二维高通量光学显微成像技术研究进展[J].液晶与显示,2023,38(06):691-711.[/color][/font][font=宋体][color=#374151][2]王义强,林方睿,胡睿等.大视场光学显微成像技术[J].中国光学(中英文),2022,15(06):1194-1210.[/color][/font][font=宋体][color=#374151][3]章辰,高玉峰,叶世蔚等.自适应光学在双光子显微成像技术中的应用[J].中国激光,2023,50(03):37-54.[/color][/font][font=宋体][color=#374151][4]曹怡涛,王雪,路鑫超等.无标记光学显微成像技术及其在生物医学的应用[J].激光与光电子学进展,2022,59(06):197-212.[/color][/font][font=宋体][color=#374151][5]关苑君,马显才.光学显微成像技术在液-[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]分离研究中的应用[J].中山大学学报(医学科学版),2022,43(03):504-510.DOI:10.13471/j.cnki.j.sun.yat-sen.Univ (med.sci).2022.0319.[/color][/font][font=宋体][color=#374151][6]陈廷爱,陈龙超,李慧等.结构光照明超分辨光学显微成像技术与展望[J].中国光学,2018,11(03):307-328.[/color][/font][font=宋体][color=#374151][7]安莎. 轴平面光学显微成像技术及其应用研究[D].中国科学院大学(中国科学院西安光学精密机械研究所),2021.DOI:10.27605/d.cnki.gkxgs.2021.000055.[/color][/font][font=宋体][color=#374151][8]杜艳丽,马凤英,弓巧侠等.基于空间光调制器的光学显微成像技术[J].激光与光电子学进展,2014,51(02):13-22.[/color][/font][font=宋体][color=#374151][9]莫驰,陈诗源,翟慕岳等.脑神经活动光学显微成像技术[J].科学通报,2018,63(36):3945-3960.[/color][/font][font=宋体][color=#374151][10]张财华,赵志伟,陈良怡等.自适应光学在生物荧光显微成像技术中的应用[J].中国科学:物理学 力学 天文学,2017,47(08):26-39.[/color][/font]

[size=24px]报告:高速大视场彩色三维显微成像技术及应用 [url=https://www.instrument.com.cn/webinar/meetings/swxw2021][b]精彩回放[/b][/url][/size]【摘要】 生物体表面色彩的不同色相、饱和度和明度在很大程度上反映了其微观结构和光学性质的不同。以激光共聚焦扫描显微镜为代表的点扫描显微成像技术具有三维层析成像能力,然点扫描显微成像技术的颜色通道十分有限,通常仅有三至四个,不能反映样品的全部色彩信息。研究团队开发了三维多视场成像技术,该技术是目前唯一的将高分辨、三维、大视场、彩色、定量和快速六大成像要素集为一体的光学显微成像技术。最大三维光切片速度100fps@1024×1024pixels。[size=18px][color=#ff0000][b][url=https://www.instrument.com.cn/webinar/meetings/swxw2021/]精彩回放:https://www.instrument.com.cn/webinar/meetings/swxw2021/[/url][/b][/color][/size][size=18px][color=#ff0000][/color][/size][size=18px][color=#ff0000][b]====[/b][/color][/size][img=,690,1227]https://ng1.17img.cn/bbsfiles/images/2021/08/202108061826440679_4529_2507958_3.jpg!w690x1227.jpg[/img]
显微镜(microscope)简称光镜,是一种将肉眼无法看清楚的微生物体进行光学放大成像的常用仪器。在生命科学、材料科学、基础科学及众多的微观领域中都离不开显微镜。1590年.荷兰的Han,父子始创放大10倍显微镜。175.8年,Dollond制成消色差透镜,提高了显微镜放大倍数。1873年,德国科学家Abbe设计成近代显微镜。1953年.上海江南光学仪器厂国产显微镜诞生,并陆续生产了荧光、相衬、偏光等专用显微镜。生物及医用显微镜可分为光学放大及电子放大两大类。前者按用途可分为普通型、特种型、高级型显微镜和手术显微镜。普通型生物显微镜仅供一般用途使用,通常的农用与医用显微镜、倒税显微镜均属这一类。特种型生物显微镜可作某些专用的观察和研究。暗场生物显微镜、荧光显微镜、偏光显微镜、相衬和干涉相衬显微镜等均属于这一类。高级型生物显微镜系指大型多用途的生物显微镜.研究用生物显微镜和万能研究用生物显微镜等属于这一类。一、显微镜放大成像系统显微镜光学系统由物镜和目镜两部分组成。因为被观测的物体本身不发光,而要借助于外界照明,故显微镜需要有一个照明系统,这些部分都是由较复杂的透镜组成,尤其物镜更为复杂。下图是显微镜成像的光路原理图,图中的物镜和目镜均用薄透镜表示。http://www.yi7.com/file/upload/201201/07/14-00-33-93-1.jpg显微镜成像原理显微镜的物体AB处于物镜的2倍焦距之内一倍焦距之外,它首先通过物镜成一放大的倒立实像A'B',且使之位于目镜的物方焦平面上或焦平面以内很靠近的地方,然后目镜将这一实像再次成一个正立虚像A"B"于无限远或人眼明视距离之外,以供眼睛观察。显微镜对物体进行2次放大,因此与放大镜相比,具有更高的放大倍率,能观察到肉眼所不能直接观察的微小物体,分辨更细小的细节。在这里目镜相当于放大镜,只不过这时放大镜的物是物镜所成的像而已。由于物镜所成的像是实像.因而可在实像处(即目镜的物方焦平面处)安放各种用途分划板.供对准或测量用。二、显徽镜的放大率与分辨本领1.显微镜的分辨本领 分辨本领主要指接物镜分辨被检查物体细微结构的能力,也就是说在显微镜下判别的最小微粒的大小或两点之间最短距离及某物点最小直径的限度,便叫做显微镜的分辨本领.或称为鉴别率。通常用d表示:http://www.yi7.com/file/upload/201201/07/14-00-33-14-1.jpg式中.A表示波长;n sins (NA)表示数值孔径。 从式中可知,显微镜的分辨率主要取决于光的波长和数值孔径这两个因素。d值越小,分辨本领也就越强,越能看清物体的细微结构。鉴别率计算单位是Um. 显微镜的鉴别率的提高只有两个办法: (1)增大物镜的数值孔径(镜口率)。从图可以看出,影响数值孔径(n sina)的因素有两个:其一为物体上某点射人物镜光锥角(镜口角)的一半(sina);其二为检品与物镜间媒质的折射率n。即数值孔径为NA = n sine镜口角半数最大能到900,故si na的最大值为1.00,这时物镜的焦距最短而曲度也很大,制造上是极为困难的。即使能办到,在干燥系中的镜口率只有1 x sin90“(控气n二1)。若再增大镜口率便只有从媒质着手,所以便有水、甘油,石蜡油和香柏油等浸润均匀媒质的应用,确实改进了镜口率不少.它最高可到1.40。如果用澳萘液可达1.67左右,更接近盖片和透镜的折射率。http://www.yi7.com/file/upload/201201/07/14-00-33-51-1.jpghttp://www.yi7.com/file/upload/201201/07/14-00-33-44-1.jpg (2)缩短光源的波长:采用紫外线作光源,波长可到0.1Um,这样放大倍数比自然光放大的倍数大3-4倍,普通紫外线光波在0.2 Um左右,即使能产生出0.1 Um波长的紫外线.一般透镜也将把它吸收干净.无法利用。显微镜的最大数位孔径可达1.5 Um左右,在这种情形下: http://www.yi7.com/file/upload/201201/07/14-00-33-33-1.jpg即在这种显微镜里,仍可分辨的两点间最短距离差不多等于所用光波波长的1/30假定绿光的光波的波长http://www.yi7.com/file/upload/201201/07/14-00-33-23-1.jpg那么显微镜能分辨的最短距离为:http://www.yi7.com/file/upload/201201/07/14-00-33-89-1.jpg 则这台显微镜的最高分辨距离也超不过。.182 Um。肉眼在明视距离(250 mm)能分辨的两点之间最短距离为0.1 mm,约为上述d值的560倍.因此I台光学显徽镜的放大率有100()倍也就足够了。这是因为光的本性及光的绕射现象就限制了显徽镜的放大极限。凡是光波超过微粒直径的2倍时,光线就很方便地绕过微粒而继续前进,所以普通干燥系显微镜的最大鉴别率只能达到光源波长的1/2,直径小到0.2 5m的微粒就无法被光学显微镜发觉。虽然后来应用浸润系方法,如油镜,提高了折射率,其鉴别率也只不过能提高到光源波长的1/3而已。而且还要用最好的透镜才能达到。

讲座名称:共聚焦光片成像技术——让荧光成像速度更快,光毒性更低,光操作更容易 主讲老师:易海英 徕卡显微系统生命科学产品应用专家,2014年毕业于华中科技大学生命科学与技术学院,研究生期间的主要研究方向为力学微环境对肿瘤干细胞及其转移的影响,以及力学信号对胚胎干细胞分化及发育的影响,在激光共聚焦和超高分辨率成像领域积累了丰富经验,参与的文章发表在Nature Communications等杂志期刊上。 主要内容:2014年,光片荧光显微技术(light-sheet fluorescence microscopy)被《Nature Methods》评选为年度技术(Method of the Year 2014)。光片(light sheet)技术简单来说即使用一薄层光束从侧面激发荧光样品,随后从样本的上部或下部检测所产生的荧光信号,即检测方向与照射方向相垂直。该技术能够以很高的三维分辨率对不同大小的固定样品或活样品进行三维成像,快速地捕捉细胞或亚细胞水平上的动态变化。其高速、低毒性、低漂白等优势使得光片技术在生命科学领域开始流行起来。光片荧光显微技术的概念其实早在一百多年前就已经被提出来了,但此后很长时间都没有什么进展,直到近年来才活跃起来,其中徕卡创造性地以其成熟的激光扫描共聚焦系统为平台,直接搭载上光片系统,得到既可以实现光片成像,又可以进行常规单光子成像,还可以将光片与单光子、多光子联合使用以实现和开创更为丰富多样的可能性的系统——Leica TCS SP8 DLS!光片荧光显微技术在细胞生物学、发育生物学、微生物学、植物学等多个领域都有广泛的应用,本次Webinar将着重介绍徕卡共聚焦光片系统DLS在生物学研究领域的应用。 举行时间:2016-11-17 14:00 报名链接:http://www.instrument.com.cn/webinar/meeting/meetingInsidePage/2178http://ng1.17img.cn/bbsfiles/images/2017/01/201701191701_669464_2507958_3.jpg手机扫描二维码,报名参会http://exmail.qq.com/cgi-bin/viewfile?type=signature&picid=ZX0717-9QlCeoL%7EVb5UZDdhPeiRO6f&uin=1407973628

讲座名称:共聚焦光片成像技术——让荧光成像速度更快,光毒性更低,光操作更容易 主讲老师:易海英 徕卡显微系统生命科学产品应用专家,2014年毕业于华中科技大学生命科学与技术学院,研究生期间的主要研究方向为力学微环境对肿瘤干细胞及其转移的影响,以及力学信号对胚胎干细胞分化及发育的影响,在激光共聚焦和超高分辨率成像领域积累了丰富经验,参与的文章发表在Nature Communications等杂志期刊上。 主要内容:2014年,光片荧光显微技术(light-sheet fluorescence microscopy)被《Nature Methods》评选为年度技术(Method of the Year 2014)。光片(light sheet)技术简单来说即使用一薄层光束从侧面激发荧光样品,随后从样本的上部或下部检测所产生的荧光信号,即检测方向与照射方向相垂直。该技术能够以很高的三维分辨率对不同大小的固定样品或活样品进行三维成像,快速地捕捉细胞或亚细胞水平上的动态变化。其高速、低毒性、低漂白等优势使得光片技术在生命科学领域开始流行起来。光片荧光显微技术的概念其实早在一百多年前就已经被提出来了,但此后很长时间都没有什么进展,直到近年来才活跃起来,其中徕卡创造性地以其成熟的激光扫描共聚焦系统为平台,直接搭载上光片系统,得到既可以实现光片成像,又可以进行常规单光子成像,还可以将光片与单光子、多光子联合使用以实现和开创更为丰富多样的可能性的系统——Leica TCS SP8 DLS!光片荧光显微技术在细胞生物学、发育生物学、微生物学、植物学等多个领域都有广泛的应用,本次Webinar将着重介绍徕卡共聚焦光片系统DLS在生物学研究领域的应用。 举行时间:2016-11-17 14:00 报名链接:http://www.instrument.com.cn/webinar/meeting/meetingInsidePage/2178http://ng1.17img.cn/bbsfiles/images/2017/01/201701191701_669468_2507958_3.jpg手机扫描二维码,报名参会http://exmail.qq.com/cgi-bin/viewfile?type=signature&picid=ZX0717-9QlCeoL%7EVb5UZDdhPeiRO6f&uin=1407973628
[url=http://www.f-lab.cn/microarray-manufacturing/ombroscopic-imaging.html]ombroscopic成像系统[/url]是基于测雨成像原理, ombroscopic imaging,而设计的胚胎成像系统,在几平方毫米区域面积提供了高对比度流速图像,广泛用于胚胎成像和细胞生物打印。ombroscopic成像系统采用脉冲在20ns的[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]的照明系统,采用高质量图像软件的列车速度运动的液滴的速度计算的方式,能够计算出微小区域的液滴流体速度。ombroscopic成像系统还包括一个微距镜头和一个与我们的EG灯同步照明的相机。ombroscopic成像系统成功用于细胞微流图像的生物打印和胚胎成像技术的细胞打印,人体生物组织使用激光辅助生物打印技术在三维微米精度的细胞位置。这项创新技术基于激光脉冲细胞微流,该过程的精度依赖于流特性的控制。ombroscopic成像系统:[url]http://www.f-lab.cn/microarray-manufacturing/ombroscopic-imaging.html[/url]

讲座名称:共聚焦光片成像技术——让荧光成像速度更快,光毒性更低,光操作更容易 主讲老师:易海英 徕卡显微系统生命科学产品应用专家,2014年毕业于华中科技大学生命科学与技术学院,研究生期间的主要研究方向为力学微环境对肿瘤干细胞及其转移的影响,以及力学信号对胚胎干细胞分化及发育的影响,在激光共聚焦和超高分辨率成像领域积累了丰富经验,参与的文章发表在Nature Communications等杂志期刊上。 主要内容:2014年,光片荧光显微技术(light-sheet fluorescence microscopy)被《Nature Methods》评选为年度技术(Method of the Year 2014)。光片(light sheet)技术简单来说即使用一薄层光束从侧面激发荧光样品,随后从样本的上部或下部检测所产生的荧光信号,即检测方向与照射方向相垂直。该技术能够以很高的三维分辨率对不同大小的固定样品或活样品进行三维成像,快速地捕捉细胞或亚细胞水平上的动态变化。其高速、低毒性、低漂白等优势使得光片技术在生命科学领域开始流行起来。光片荧光显微技术的概念其实早在一百多年前就已经被提出来了,但此后很长时间都没有什么进展,直到近年来才活跃起来,其中徕卡创造性地以其成熟的激光扫描共聚焦系统为平台,直接搭载上光片系统,得到既可以实现光片成像,又可以进行常规单光子成像,还可以将光片与单光子、多光子联合使用以实现和开创更为丰富多样的可能性的系统——Leica TCS SP8 DLS!光片荧光显微技术在细胞生物学、发育生物学、微生物学、植物学等多个领域都有广泛的应用,本次Webinar将着重介绍徕卡共聚焦光片系统DLS在生物学研究领域的应用。 举行时间:2016-11-17 14:00 报名链接:http://www.instrument.com.cn/webinar/meeting/meetingInsidePage/2178http://ng1.17img.cn/bbsfiles/images/2016/10/201610281713_615330_0_3.jpg手机扫描二维码,报名参会http://exmail.qq.com/cgi-bin/viewfile?type=signature&picid=ZX0717-9QlCeoL%7EVb5UZDdhPeiRO6f&uin=1407973628

讲座名称:共聚焦光片成像技术——让荧光成像速度更快,光毒性更低,光操作更容易 主讲老师:易海英 徕卡显微系统生命科学产品应用专家,2014年毕业于华中科技大学生命科学与技术学院,研究生期间的主要研究方向为力学微环境对肿瘤干细胞及其转移的影响,以及力学信号对胚胎干细胞分化及发育的影响,在激光共聚焦和超高分辨率成像领域积累了丰富经验,参与的文章发表在Nature Communications等杂志期刊上。 主要内容:2014年,光片荧光显微技术(light-sheet fluorescence microscopy)被《Nature Methods》评选为年度技术(Method of the Year 2014)。光片(light sheet)技术简单来说即使用一薄层光束从侧面激发荧光样品,随后从样本的上部或下部检测所产生的荧光信号,即检测方向与照射方向相垂直。该技术能够以很高的三维分辨率对不同大小的固定样品或活样品进行三维成像,快速地捕捉细胞或亚细胞水平上的动态变化。其高速、低毒性、低漂白等优势使得光片技术在生命科学领域开始流行起来。光片荧光显微技术的概念其实早在一百多年前就已经被提出来了,但此后很长时间都没有什么进展,直到近年来才活跃起来,其中徕卡创造性地以其成熟的激光扫描共聚焦系统为平台,直接搭载上光片系统,得到既可以实现光片成像,又可以进行常规单光子成像,还可以将光片与单光子、多光子联合使用以实现和开创更为丰富多样的可能性的系统——Leica TCS SP8 DLS!光片荧光显微技术在细胞生物学、发育生物学、微生物学、植物学等多个领域都有广泛的应用,本次Webinar将着重介绍徕卡共聚焦光片系统DLS在生物学研究领域的应用。 举行时间:2016-11-17 14:00 报名链接:http://www.instrument.com.cn/webinar/meeting/meetingInsidePage/2178http://ng1.17img.cn/bbsfiles/images/2017/01/201701191701_669462_2507958_3.jpg手机扫描二维码,报名参会http://exmail.qq.com/cgi-bin/viewfile?type=signature&picid=ZX0717-9QlCeoL%7EVb5UZDdhPeiRO6f&uin=1407973628
[center]真实色共焦显微镜与激光扫描共焦显微镜主要特点对比[/center]真实色共焦显微镜与激光扫描共焦显微镜,二者在成像原理上基本是一样的,最大不同之处是照明光源不同。1、激光扫描共焦显微镜激光扫描共焦显微镜的照明光源是激光,即单色光。其实际成像过程是根据被观察物体对该单色激光的反射光的强弱来成像的。由于是单色光照明,不能分辨颜色,对于在同一试样的同一视场内,颜色不同,但对该单色激光反射光强度相同的不同组织或成分不能分辨。容易产生同相异色,同色异相的现象,不利于对微观组织和成分的正确分辨。2、真实色共焦显微镜真实色共焦显微镜的光源是氙光源,即白光。其实际成像过程是在白光照明的条件下,对物体形貌(包括颜色)进行综合的成像。 由于是多色光照明和成像,真实色共焦显微镜能够更真实的反应物体的颜色和形貌,避免了激光扫描共焦显微镜产生的同相异色,同色异相的现象发生,观察者可以通过颜色,分辨和判断试样的成分和组织。在这方面,其分辨率远强于激光扫描共焦显微镜 综合分析:在有颜色差异的试样的观察条件下,真实色共焦显微镜避免了激光扫描共焦显微镜产生的同相异色,同色异相的现象发生,观察者可以通过颜色,分辨和判断试样的成分和组织。在这种条件下,真实色共焦显微镜的分辨率高于激光扫描共焦显微镜。在单色试样的观察条件下,分辨率才接近各自的技术指标。然而,在实际观察的试样中,绝大多数不同的组织和成分都是有颜色差异的。对应于没有颜色差异或颜色差异小的试样,可以通过人为的染色(例如腐蚀处理),提高图像的分辨能力。在这一方面,激光扫描共焦显微镜是无能为力的。 另外,分辨率是在特定条件下所能达到的一项技术指标,当在实际使用中,不满足该技术条件时(实际是常常不能满足),其分辨率是达不到所给出的数值。