针织产品成分分析中,棉氨拆分法有没有什么比较快的拆分方法?我们半天才能拆一个样品?
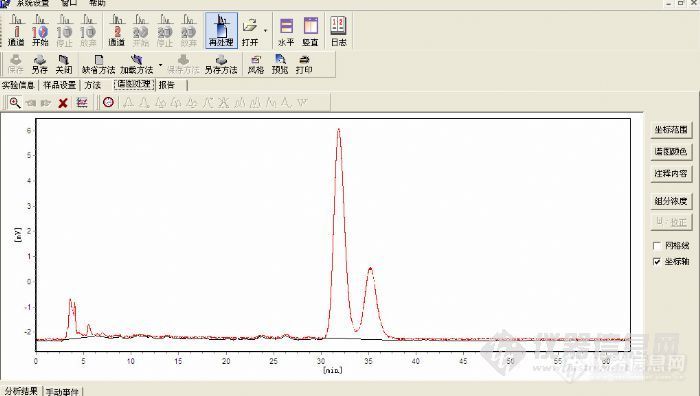
手性色谱柱在手性异构体拆分中的应用实例 手性是自然界的一种普遍现象,构成生物体的基本物质如氨基酸、糖类等都是手性分子。手性分子的重要性不仅表现在与生物相关的领域,在功能材料领域,如液晶、非线性光学材料、导电高分子方面也显示出诱人前景。随着对手性分子认识的不断深入,人们对单一手性物质的需求量越来越大,对其纯度的要求也越来越高。单一手性物质的获得方法大致有以下三种:①手性源合成法。②不对称合成法。③外消旋体拆分法。那么外消旋体的拆分方法主要有1 机械拆分法 2 化学拆分法3 生物化学拆分法4 色谱拆分法5 萃取拆分法6 膜拆分法,等。这里介绍的是色谱拆分法,各种色谱技术均可用于手性拆分。可以将外消旋体与手性试剂作用生成非对映异构体,用普通的色谱技术拆分;也可以使用手性流动相或手性固定相进行拆分,而以后者最为简便、廉价,下面介绍的实例也是后者。 仪器 高效液相色谱仪(安捷伦1200型),Waters600. 试剂 甲醇(色谱级),重蒸水,乙腈(色谱级) 手性柱为CHIRALPAKR AD-RH Column Size 150×4.6mmhttp://ng1.17img.cn/bbsfiles/images/2010/11/201011282059_262536_2165260_3.jpg C18柱为依利特分析柱, Column Size 250×4.6mm 下图为样品1的分析图谱, 分析条件:C18柱为依利特分析柱,Column Size 250×4.6mm,甲醇:水 50:50,柱温25度。 http://ng1.17img.cn/bbsfiles/images/2010/11/201011282101_262537_2165260_3.jpg 显而易见,为一单一化合物,即而测试核磁共振谱,经解析为一含手性中心的化合物,其为R型还是S型,亦或是R型和S型共同存在,无从得知。 于是我们决定用手性色谱柱进行分析,旨在判断是否为混合物。 分析条件 手性柱为CHIRALPAKR AD-RHColumn Size 150×4.6mm ,已腈:水 30:70,柱温 25度(波长280) 分析图谱如下http://ng1.17img.cn/bbsfiles/images/2010/11/201011282120_262538_2165260_3.jpg 结果显而易见,为两种异构体的混合物,其量比大约3:2。 经过对样品1进行分析的结果,我们对样品2也进行了同样分析。其分析图谱如下: 分析条件:C18柱为依利特分析柱,Column Size 250×4.6mm,甲醇:水 50:50,柱温25度。 http://ng1.17img.cn/bbsfiles/images/2010/11/201011282127_262539_2165260_3.jpg 经核磁图谱解析仍为一手性化合物,于是进行了手性柱色谱分析。 分析条件 手性柱为CHIRALPAKR AD-RHColumn Size 150×4.6mm ,已腈:水 40:60,柱温 25度(波长280) 图谱如下:http://ng1.17img.cn/bbsfiles/images/2010/11/201011282132_262540_2165260_3.jpg 分析结果显示样品2为一混合物,其量比约为3:1 结论:我们在得知样品为一手性化合物时,为确定其是否为一异构体混合物,对其进行了手性柱色谱分析,结果显示为混合物,我们进而对其进行了累计制备,分别得到了R型和S型单体,也是实验室对手性拆分的成功实例。 最后,补充一句,次此实验所用手性柱在保养方面与一般的色谱柱还是有些差别的,其最后保存在40%的已腈水中,避免以高浓度的有机溶剂冲洗洗柱子。
自然 界存在各种各样的手性现象,比如蛋白质、氨基酸、多糖、核酸、酶等生命活动重要基础物质,都是手性的。据,在研发的1200种新药中,有820种是手性的,占世界新药开发的68%以上。美国 FDA 在1992年发布了手性药物指导原则,该原则要求各医药 企业 今后在新药研发上,必须明确量化每一对映异构体的药效作用和毒理作用,并且当两种异构体有明显不同作用时,必须以光学纯的药品形式上市。随后欧共体和日本也采取了相应的措施。此项措施大大促进了手性药物拆分技术的 ,手性药物的研究与开发,已经成为当今世界新药发展的重要方向和领域。当前大多数药物是以外消旋体的形式出现,即药物里含有等量的左右两种对映体。但是近年来单一对映体药物市场每年以20%以上的速度增长。1993年全球100个热销药中,光学纯的药物仅仅占20%;然而到了1997年,100个中就有50个是以单一对映体形式存在,手性药物已占到世界医药市场的半壁江山。在1993年,手性药物的全球销售额只有330亿美元;到了1996年,手性药物世界市场已经增长到730亿美元;2002年总销售额更是达到1720亿美元,2010年可望超过2500亿美元。广阔的应用前景和巨大的市场需求触发了更多的医药企业和学者探索更新更高效地获得单一手性化合物的方法。 目前获得单一手性化合物的方法有3种:①手性源合成法:以手性物质为原料合成其他手性化合物。②不对称催化合成法:是在催化剂或酶的作用下合成得到单一对映体化合物的方法。③外消旋体拆分法:是在拆分剂的作用下,利用物理化学或生物方法将外消旋体拆分成两个对映体。外消旋体拆分法作为一种经典的分离方法,在此显示出其 省时的优势,在工业生产上得到广泛的应用。目前,外消旋体拆分法可分为结晶拆分、化学拆分、生物拆分、色谱拆分、膜拆分和手性萃取拆分等方法。本文作者根据国内外相关 文献 报道,对外消旋体的几种拆分方法进行了综述。 1 经典结晶法 用结晶的方式进行外消旋体的分离,是手性化合物拆分中最常用也是最主要的方法。传统的拆分法过于繁琐,而结晶法实际上是机械分离法的改进。经典的接种结晶法是在一个热的外消旋体混合物的饱和溶液中,加入适量的某一对映体的晶种进行诱晶,适当冷却,这一对映体由于过饱和从外消旋混合物中析出,分别加入两种对映体晶种,就可以得到两种对映异构体。如 L-甲基多巴的生产即采用此法。对于不生成外消旋混合物的化合物,可通过手性酸、碱等拆分试剂将其转化成非对映异构体盐后,再进行反复结晶。如 D-苯基甘氨酸的 Amdeno 制备法即是用樟脑磺酸盐作拆分剂进行结晶,年产量上千吨。接种结晶法工艺简单,经济又方便,但通常只能间歇生产,一次收率较低。 2 化学拆分法 化学拆分法是广泛使用的一种方法。根据手性试剂与外消旋体反应所得生成物不同可分为以下几种。 2.1 经典拆分法 如果外消旋体分子含有如羧基、氨基、羟基或者双键等活性基团,可让其与某一光学活性试剂(拆分剂)进行反应,生成两种非对映异构体的盐或其它复合物,再利用它们物理性质(如溶解度)和化学性质的不同将两者分开,最后把拆分剂从中分离出去,便可得到单一对映体。拆分成功的关键是选择合适的拆分剂。适用于这类光学拆分方法的外消旋体有酸、碱、醇、酚、醛、酮、酰胺及氨基酸等。其过程如下式(1)所示: (DL)-A+(D)-B→(D)-A·(D)-B+(L)-A·(D)-B(1) 这种经典的方法运用广泛,但其也有明显的局限性,比如拆分剂和溶剂的选择较为盲目;拆分剂价格昂贵;收率和e.e.值不高等。近年来,随着主-客体化学的深入研究,开发出了包结拆分和组合拆分等新型手性拆分技术,在一定程度上弥补了经典成盐拆分法的不足。 2.2 组合拆分 组合拆分(combinatorial resolution) 是近年来报道的一种新方法,它的原理是采用一组同一结构类型的手性衍生物拆分剂家族(resolving agent family) 代替单一的手性拆分剂进行外消旋化合物的拆分。这些拆分剂家族往往是以常用的手性拆分剂为原料,经结构修饰得到的衍生物。也可以是含有不同取代基的某一类结构类型的化合物。Wynberg 设计了一系列芳香环取代的衍生物组成不同的拆分剂家族,首次将该方法应用于化学拆分中。经过实验验证,酒石酸类衍生物的拆分剂家族 T 和TA(1),可用于碱性化合物的拆分,α-苯乙胺类拆分剂家族PE-I,PE-II 和PE-III(图2),通常用于酸性化合物的拆分。 实际操作时将拆分底物与拆分剂家族以 1∶1 的形式,于同一溶剂中进行拆分。这种组合拆分方法和前述的经典拆分方法比较,具有结晶速度快,收率高,纯度高等特点。 2.3 包结拆分 包结拆分是由日本化学家 Toda 教授发明的,其原理是利用非共价键体系,如氢键和分子间的次级作用,使外消旋体的一个对映异构体与手性拆分剂发生包结,形成稳定的超分子配合物,再通过结晶方法将两个对映体分开。由于主体和客体分子不发生化学反应,只存在分子间作用力,所以很容易通过柱层析、溶剂交换和逐级蒸馏等与客体分离,然后再循环利用。因此,包结拆分具有操作简单、成本低廉、易于规模生产,具有很高的工业价值。Toda 等还采用氯化 N-苄基辛可尼定作为包结主体,在甲醇中首次成功地拆分了外消旋的联二萘酚,光学纯度(e.e.值)达到100%。邓金根等用光学纯联二萘酚类化合物和酒石酸衍生物等手性化合物作为包结主体,选择性地与某种构型的奥美拉唑形成包结络合物,并以结晶形式出现,而另一种对映体则留在溶剂中,然后用层析的方法将包结主体和奥美拉唑分离,可制得两种对映体。其中具有药效作用的 S-奥美拉唑总收率可达88%,e.e.值为100%。过程如图3所示。 2.4 动力学拆 分经典动力学拆分的原理在于两个对映体与某一手性试剂的作用, 中间体是一对非对映异构体,反应速度一般存在差异。利用它们反应的动力学差异,从而达到拆分的目的。通过经典动力学得到的光学纯产物的最大产率为50%,多数情况下,有一个异构体是没用的,这将浪费一半的原料。因此,为了克服以上缺点,人们开始采用动态动力学拆分方法,就是在拆分过程中伴随着底物的现场消旋化,从而使那一半没用的对映体转化为消旋体继续拆分。理论上产率可达到100%,这在工业应用上将具有重大的意义。 3 生物拆分法 酶的活性中心是一个不对称结构,这种结构有利于识别消旋体。在一定条件下,酶只能催化消旋体中的一个对映体发生反应而成为不同的化合物,从而使两个对映体分开。反应产物的e.e.值可达100%。随着酶固定化、多相反应器等新技术的日趋成熟,越来越多的酶已用于外消旋体的拆分。徐刚等通过对不同来源酶的筛选,找到了 Novozym 435和 Alcaligenes sp两种选择性较好的酶,有效拆分制备了(S)-2-氯-1-(2-噻吩)-乙醇,产率为48.6%,e.e.值为98.5%。酶催化立体选择性强、反应条件温和、操作简便、副反应少、产率高、成本低,且不会造成污染,这些都使得用酶拆分外消旋体成为理想的选择。酶法拆分外消旋体在实验室制备和工业生产中都已取得长足的进步,但是仍然有其局限性。比如菌种筛选困难、酶制剂不易保存、产物后处理量大,以及通常只能得到一种对映体等缺点。尽管如此,利用微生物进行手性药物的合成及对映体的拆分仍是当前研究热点。 4 色谱拆分法 色谱法是目前手性药物分析和分离中应用最广最有效的方法之一。主要应用分为两类:分析级水平和制备级水平。用于分析领域的色谱拆分法包括气相色谱(GC)、高效液相色谱(HPLC)、超临界流体色谱(supercritical fluid chromatography,SFC)、毛细管电泳(CE)等。在制备领域中,高效液相色谱的应用较为广泛。另外,在工业化生产中比较成熟、比较前沿的是模拟移动床(simulated moving bed,SMB)技术。 4.1 高效液相色谱 高效液相色谱法在手性药物拆分中的应用是最广泛的,是药物质量控制、立体选择性的药 和毒理学研究的重要手段。 HPLC 分离药物对映体的方法可分为间接法和直接法。前者又称为手性试剂衍生化法,后者又可分为手性固定相法(CSP)和手性流动相添加剂法(CMPA)。间接法是利用手性药物对映体混合物在预处理中进行柱前衍生化,形成一对非对映异构体,根据其理化性质上的差异,使用非手性柱得以分离。该法分离效果好,分离条件简便,一般的非手性柱可满足要求,但需要高纯度的衍生试剂,操作比较麻烦。直接拆分法中的 CMPA 法是在流动相中加入手性添加剂,利用非手性固定相 HPLC 进行拆分;而 CSP法发展异常迅速,目前已开发的商品化手性固定相有多糖类、蛋白类、环湖精类、冠醚类等,其中多糖类衍生物手性识别能力强,方法也较成熟。直接法可用 Dalglsh 于1952年提出的着名的“三点作用原理”来解释:药物一个对映体先与手性固定相或流动相的添加剂间发生分子间的三点作用,同时另一对映体则发生二点作用,前者形成的分子复合物较后者稳定,用 HPLC 法依次使其对映体分离。郭娜等采用羟丙基-β-环糊精为手性流动相添加剂,拆分了奥昔布宁对映体,分离度为 1.54,检测限为 1.0 ng。HPLC 法用于对映体药物的拆分,具有多种途径,各具特色,可
因为随着论坛的发展壮大,色谱版块下面的子项太多了,建议拆分,这样还有利于两个版块的进一步细分,大家认为如何?

这种纤维就是二烯类弹性纤维吗?除了拆分法,能用溶解法定量吗?[img=,690,1226]http://ng1.17img.cn/bbsfiles/images/2018/06/201806111031172360_6499_2154459_3.jpg!w690x1226.jpg[/img]
手性是自然界的一种普遍现象,构成生物体的基本物质如氨基酸、糖类等都是手性分子。手性异构体(对映体)在药物中占有很大的比例,据统计,已知药物中约有30%~40%是手性的。经由化学合成得到的药物往往是对映体,不是单一的光学异构体。虽然其物理化学性质基本相同,但是由于药物分子所作用的受体或靶位是氨基酸、核苷、膜等组成的手性蛋白质和核酸大分子等,它们对与其结合的药物分子的空间立体构型有一定的要求,因此,对映体药物在体内往往呈现很大的药效学、药动学等方面的差异(图1)。鉴于此,美国食品医药管理局(FAD)规定,今后研制具有不对称中心的药物,必须给出手性拆分结果,欧共体也采取了相应措施,因此手性拆分已成为药理学研究和制药工业日益迫切的课题。 利用化学拆分法、超临界流体色谱法、膜法、酶法以及模拟流动床法分离药物对映体,已成为新药研究和分析化学的领域之一。本文综述了近几年来利用上述方法拆分手性异构体研究的新进展。 1 化学法 化学拆分法是广泛使用的一种方法,经典的化学拆分是利用手性试剂与外消旋体反应,生成两个非对映异构体,再利用其物理性质的差异将其拆分。但此类方法存在收率较低、拆分剂消耗大及在拆分的化合物类型上受到限制等缺点。近几年来,随着主客体化学的深入研究而发展起来的包结拆分(inclusion resolution)由于其拆分效率高、操作简单及适用条件广泛等优点而受到重视。 包结拆分的基本原理是:手性主体化合物通过氢键及分子间的次级作用,选择地与客体分子中一个对映体形成稳定的包结络合物析出来,从而实现对映体的分离,如图2所示。 由于包结拆分中主体分子与客体分子间不发生任何化学反应,只是通过分子间作用力来实现拆分,因而很容易地通过如柱、溶剂交换以及逐级蒸馏等手段与客体分离和可循环使用。甾类化合物是最优良的包结主体之一,因为其化学结构中富含多种功能基且刚性很强,其中胆汁酸类衍生物(图3)广泛地应用于手性醇、酮及手性亚砜类化合物的拆分。 Hisakazu等利用一种酒石酸衍生物nonane](图4)作为包结主体拆分了外消旋的甲基取代环丙烯等一系列化合物,经蒸馏后,得到光学纯度为28%~75%的包结络合物。 2 超临界流体色谱法(SFC) 超临界流体色谱具有简单、高效、易于变换操作条件等优点,已成为和高效液相色谱(HPLC)和气相色谱(GC)互为补充的拆分方法,因其具有独特的优越性,应用前景极为广阔。Petersson对1993年以前SFC在手性化合物分离上的应用作了综述[5],李桦等总结了SFC在手性药物拆分中的优越性[6]。 根据手性选择剂种类不同,SFC分离方式主要包括[7]氨基酸和酰胺类手性固定相、Prikle型手性固定相、环糊精型键合固定相、多糖型的手性固定相以及其他手性固定相如聚甲基异丁烯酯等。但是SFC正处于迅速发展阶段,各种参数(如温度、压力、流动相的组成和密度等)对分离度的影响机制还未完全清楚。人们可借鉴HPLC、GC、HPCE手性分离的经验和成果,研制出各种类型的适合SFC分析的手性固定相及操作条件。 最近,Nozal[7]等用Chiralpak AD柱和Chiralcel OD柱在SFC条件下拆分了驱肠蠕虫药阿苯哒唑亚砜化合物(图5),并研究了甲醇、乙醇、2丙醇及乙腈等有机溶剂对立体选择型的影响。结果表明,在以Chiralpak AD柱为固定相时,用2丙醇可以获得最好的拆分效果;而在Chiralcel OD柱上用甲醇效果最好。 3 膜分离法 氨基酸的生物转移通常是由埋在生物膜中的载体蛋白来传递的,这种转移的对映体选择性是非常高的。很久以来,人们就希望将这种对映体转移体系用于分离技术中,通过膜分离进行旋光异构体的拆分正是这种生物过程的模拟。 3.1 液膜分离法 1979年D.J.cram等首先报道了一种膜分析方法。在这种液膜体系中,手性分子(主体)与外消旋(客体)结合,通过氯仿载其从一水溶液至另一水溶液再释放出来。这种装置能够同时连续地将外消旋体拆分为两个对映体,得到旋光纯度为70%~90%。另外,一种氨基酸光学拆分液体膜在光学活性冠醚中浸入聚合薄膜的形式而得以制备[8]。手性冠醚(图6A)通过液体膜可作为氨基酸及胺类对映体选择性的中间媒介,几乎所有的氨基酸都可通过它们的对映体形式分离,其中大空间位阻基团的氨基酸会有较高的光学拆分率。 3.2 手性固定膜 近年来,对映体膜分离的另一个新发展是手性固体膜的发展[9]。Maruryama等认为,物质通过膜的渗透是由被拆分物质早膜中的分配行为和他们在膜中的扩散速度来决定的。为了提高膜的对映体选择性,需要优化这两个因素。据此他们制备了有两亲性侧链的α螺旋链聚氨基酸衍生物,作为手性膜材料,成功拆分了酪氨酸和色氨酸,D,L对映体的渗透比率大于8.0,经过500 h的渗透,选择性没有下降。纤维素衍生物固体膜在手性拆分中的应用也较多。尤其是纤维素三(3.5二甲基苯基氨甲酸酯,CTPC)(图6B)膜表现出极好的手性选择性。Jang[10]等最近用海藻酸钠(SA,图6C)和脱乙酰壳多糖(CS,图6D)分别与戊二醛所生成的交联复合物作为膜材料,对外消旋的色氨酸进行了拆分,光学纯度达98%以上。 4 模拟流动床色谱(SMB)法 模拟流动床色谱(simulated moving bed chromatography)技术是由D.B.Broughton在1961年的一个专利中提出来的。最初这种技术用于正己烷和环己烷的分离,后来又用于间二甲苯和对二甲苯的大规模制备。模拟流动床手性拆分系统在运行过程中,旋转阀间歇性地开关,控制在不同时间外消旋体的进样、新溶剂的注入和两个旋光异构体的提取位置。SMB的流程简图如图7所示[11]。 装置是由12根色谱柱串联,由一循环泵将最后一根柱子中的溶液泵回到第一根形成环路。将外消旋混合物在两根柱子之间加入,经一段时间后,保留时间小的组分在前面,保留时间长的组分在后面,在预定的时间和位置,分别将其取出小部分。因为流动相的运动和固定相是相对反向的,因此这种逆流色谱性质使得传质驱动力达到最大,这样就减小了洗脱剂的消耗量。 Nagamatsu[12]等用中等规模的SMB成功的拆分了奎尼丁甲羟戊酸酯(DOLE,图8),所采用的是分析型Chiralcel OF柱,流动相为ψ(正己烷∶2丙醇)=8∶2,流速为1.0 mL/min。试验还通过计算机软件寻求最佳的操作条件,结果表明,较高的流速和较短的间歇时间可以提高对映体的拆分,其无论是从产率和溶剂消耗量上都优于液相色谱法。 5 酶法 应用酶和微生物在底物上引进手性中心的方法有很久的历史了,如氢化可的松及维生素C的生产等。因为酶的活性中心是一个不对称环境,有利于识别消旋体,在一定条件下,酶只能催化消旋体中的一个对映体发生反应而成为不同的化合物,从而使两个对映体分开,反应产物的对映过剩百分率可达100%。另外,酶催化的反应大多在温和的条件下进行,温度通常不超过0~50 ℃,pH值接近中性;而且酶无毒,易降解不会造成环境污染,适于大规模生产。因此,用催化效率高、专一性强的酶拆分消旋体是获取对映体纯化合物的捷径。随着酶固定化技术、多相反应器等新技术日趋成熟,大大促进了酶拆分技术的发展,脂肪酶、酯酶、蛋白酶、转氨酶等诸多酶类已用于外消旋体的拆分[13]。 脂肪酶(Lipase)是研究最早的一类酶,是一类特殊的酯键水解酶。脂肪酶具有高度的选择性和立体专一性,且反应条件温和,副反应少,适用于催化非水相介质中的化学反应。Michimasa[14]等分别用Pseudomonas sp脂肪酶和猪胰脂肪酶(PPL)对2苯1丙醇进行了拆分,反应是通过两种酶分别催化酯交换反应而进行,使得对映体拆分率分别提高到了39%和41%。 另外,酯酶具有很高的工业价值,其应用前景也极为广阔。最近,Jianxin[15]等利用Pseudomaonas cepacia脂肪酶拆分了一类酰基取代的1环己烯衍生物。因为在抗体或抗肿瘤的天然活性物质中常含有此基团,是一类极有药用前途的母核。该方法通过酶催化酯交换反应,而得到了产率较高的光学纯化合物,且提供了反应过程监测方法,因此可有效的推广到该类化合物的一系列衍生物的合成与拆分,其主要反应如图9所示。图9 1-环己烯衍生物的拆分Fig.9 The resolution of derivates of 1-hexene 随着科技的进步,酶法在实现手性药物的拆分和生物转化方面发挥着越来越大的作用,各种新的方法与技术正层出不穷,抗体酶、交联酶晶体、固定化酶及非水相酶学等都成为当今酶学研究的活跃领域,这些技术的发展与完善必将推进拆分技术的发展。 6 小结 目前在药物对映体拆分中,采用的主要手段是气相色谱法和高效液相色谱法[18],但因其手性柱费用高,易污染且手性衍生化常带进副产物等缺点仍需进一步研究。而SFC正处于发展阶段,虽各种参数的影响尚未完全清楚,但随其理论和技术的日臻完善,SFC在手性物质分析的应用上将得到进一步发展。模拟流动
当拆分手性胺类化合物的时候,应该选择怎样的液相色谱拆分条件啊?可以使用C18柱么?如果使用缓冲溶液做流动相,会对仪器和柱子都产生影响的吧。
乳酸异构体的拆分,有什么色谱柱可以选择?
[color=#444444]在用高效液相色谱进行拆分时,得到的谱图一般有两个手性对映体的峰,也有四个等。两个峰是哪个是R型哪个是S型?是前一个固定称为R型还是有其他命名的规则?当两个以上时又怎么命名,总不至于就标个1,2,3,4吧?求教了![/color]
【序号】:1【作者】:罗积杏 唐世平 齐楠 杨立荣【题名】:菊酸的高效液相色谱法拆分与测定【期刊】:《农药》 【年、卷、期、起止页码】:2005年09期 【全文链接】:http://www.cnki.com.cn/Article/CJFDTotal-NYZZ200509010.htm【序号】:2【作者】:杜曦 周锡兰 余录 唐斌 刘可【题名】:葡萄及葡萄酒中有机酸测定的衍生化[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法【期刊】:酿酒 【年、卷、期、起止页码】: 2008年3期【全文链接】:http://d.wanfangdata.com.cn/Periodical_nj200803030.aspx
[em0808] 在论坛出入的高手们,我想请问下图谱要达到完全分离(基线分离)的条件是什么,比如说流动相,流速等条件。还有就是那些操作条件会引起拆分图谱在基线的下面?对了是在正相拆分的条件下!麻烦各位了~~~~[em0808]
摘 要:综述了高效液相色谱配体交换色谱手性固定相的发展、制备及其在手性拆分中的应用,讨论了洗速、进样量、中心金属离子及其浓度、流动相pH 值、柱温、有机改性剂等对对映体分离的影响,阐述了对手性识别机理的认识.[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=23983]高效液相色谱手性拆分中的配体交换色谱手性固定相[/url]
国内哪家手性色谱柱比较好?大赛璐以外的,SFC拆分手性化合物
[size=4]想要在一根手性色谱柱子上拆分一些外消旋化合物,来考察手性色谱柱的拆分性能!但仅仅知道该柱子是手性柱!不知道哪些外消旋化合物合适该手性色谱柱!也不知道流动相的条件是什么!请教各位具体的操作步骤是什么?很感谢!!![/size]
对典型性手性农药的液相色谱拆分方法有哪些?特别是要用到哪些色谱柱?
衍生 手性物质 实现反相拆分新技术一种用液相色谱法分离测定奈必洛尔杂质的方法 在药物分析中色谱技术和光谱技术已基本普及,近年来色谱法和光谱法的联用技术在药物分析中被日益广泛应用.本文拟对用于药物分析的现代分析技术作简单介绍,以便有关研究工作者作参考. 1 现代色谱法 1.1 手性药物的液相色谱分析法上世纪80 年代初,随着大量商品化HPLC 用手性固定相的问世以及对手性识别机理的较深入的认识,HPLC法已迅速成为广泛应用于分离和测定药物对映体的方法. 手性HPLC拆分法分类: 由于D-型和L-型对映体的物理性质完全相同,难以在普通固定相上分离,只能在手性固定相上才能获得拆分;如果利用对映体分子中的反应基团与某一光学纯试剂反应形成了非对映光学异构体混合物,其物理性质就有较大的差异,因而在普通固定相上实现分离.因此,手性HPLC 拆分法通常分为直接法和间接法两大类.对映体混合物以手性试剂作柱前衍生,形成非对映体异构体对,然后以常规固定相分离,称为间接法,也称手性衍生试剂法;未作上述处理,使用手性流动相或手性固定相拆分者即是直接法.其共同特点是,均以现代HPLC 技术为基础,并引入不对称中心;不同的是间接法是将其引入分子内,而手性固定相和手性流动相则引入分子间.引入手性环境使对映异构体间呈现物理特征的差异是手性HPLC进行光学异构体拆分的基础.本发明公开了一种用液相色谱法分离测定奈必洛尔杂质的方法,以纤维素三(3,5-二甲苯基氨基甲酸酯)即OD-H柱为填料的手性色谱柱,以缓冲盐溶液与有机相按一定配比组成的混合溶液为流动相,该方法能快速准确地分离和测定这两种光学异构体。建立了在碱性条件下从水相中用乙酸乙酯提取阿替洛尔,用GITC进行柱前手性衍生化,以及用流动相NaH2PO4缓冲液-CH3OH-CH3CN(50∶20∶30)在ODS柱上拆分的分析方法,254 nm波长处检测。 前言:本文用乙酰葡萄糖异硫氰酸酯(GITC)作柱前手性衍生化试剂,反相高效液相色谱法拆分氨基酸立体异构体。研究了不同构型氨基酸与GITC反应后所生成的衍生物的紫外吸收响应特点。探讨了16种氨基酸GITC衍生物的色谱分离情况。采用ZORBAX-C8(150 mm×4.6 mm,5μm)色谱柱,在流动相为甲醇-0.05 mol.L-1磷酸二氢钾溶液(40:60,pH6.0)、紫外检测波长为254 nm、流速为1.5 m.lmin-1、柱温35℃的色谱条件下,巴氯芬对映体衍生物获得了基线分离,分离度为1.93,并确认了R(+)-衍生物的色谱峰摘要 目的:建立阿替洛尔两对映体在鼠肝微粒体中的RP-HPLC测定方法。方法:从鼠肝微粒体中提取阿替洛尔消旋体,采用手性衍生化试剂2,3,4,6-四-O-乙酰基-β-D-吡喃葡萄糖异硫氰酸酯(GITC)对阿替洛尔消旋体进行柱前手性衍生化再以RP-HPLC拆分,测定鼠肝微粒体中阿替洛尔各对映体含量。结果:建立了在碱性条件下从水相中用乙酸乙酯提取阿替洛尔,用GITC进行柱前手性衍生化,以及用流动相NaH2PO4缓冲液-CH3OH-CH3CN(50∶20∶30)在ODS柱上拆分的分析方法,254 nm波长处检测。阿替洛尔对映体在1~20 μg.mL-1范围内呈良好线性关系,S(-)-阿替洛尔:Y=840 076.5X+141 742.8,r=0.999 8;R(+)-阿替洛尔:Y=873 157.2X+192 187.5,r=0.999 8),LOD为55 ng.mL-1,LOQ为145 ng.mL-1(RSD7%),相对回收率在95%~105%(RSD5%)。用此方法试验了阿替洛尔在鼠肝微粒体中的代谢测定。结论:结果表明此方法可用于研究阿替洛尔消旋体在鼠肝微粒体中代谢和酶动力学研究。关键词 阿替洛尔 2,3,4,6-四-O-乙酰基-β-D-吡喃葡萄糖异硫氰酸酯(GITC) 鼠肝微粒体 高效液相色谱法 手性衍生化 阿替洛尔(atenolol,(+)-4- propoxy] benzeneacetamide,图1-A)作为一种β-受体阻断药,能与去甲肾上腺素能神经递质或肾上腺素受体激动剂竞争β-受体,从而拮抗其β型拟肾上腺素作用,临床上常用于治疗心绞痛和高血压,通常以消旋体给药,但阿替洛尔S(-)-对映体的β-受体阻断作用比R(+)-对映体强[1]。所以R(+),S(-)-阿替洛尔的手性拆分在药效学和药动学的研究中都具有重要意义。关于阿替洛尔的测定,文献报道多为阿替洛尔消旋体的测定方法,如薄层色谱法[2]、气相色谱法[3]以及用紫外和荧光检测器的HPLC法[4~7]。在手性衍生化法拆分方面Chin SK、Rosseel MT等建立了以S-(-)-β-甲苄基异氰酸酯、(+)-1-(9-芴基)乙基氯甲酸酯为手性衍生化试剂的RP-HPLC法[8~10],测定阿替洛尔在血和尿中的对映体含量。图1 结构式A.阿替洛尔 B.GITC 为研究手性药物的代谢机制,需要运用手性分离手段[11~13]。本文应用2,3,4,6-四-O-乙酰基-β-D-吡喃葡萄糖异硫氰酸酯(2,3,4,6-tetra-O-acetyl-β-D-glucopyranosyl isothiocynate,GITC,图1-B)为手性衍生化试剂与阿替洛尔消旋体反应生成非对映衍生物,用RP-HPLC法实现了分离,并建立了阿替洛尔消旋体在鼠肝微粒体中的对映体测定方法。用此方法观察了阿替洛尔在鼠肝微粒体中的代谢情况。1 仪器与试剂 日本Shimadzu LC-10ATvp泵、SPD10Avp紫外检测器。 还原型辅酶Ⅱ(NADPH)、GITC、6-磷酸葡萄糖(G-6-P)、6-磷酸葡萄糖脱氢酶(G-6-PDH)均购自美国Sigma公司,阿替洛尔购自中国药品生物制品检定所。 实验中所用试剂均为分析纯试剂。 NaH2PO4缓冲液:精密称取NaH2PO4.2 H2O 0.780 1 g,精确加入水500.0 mL,混匀后用5 μm孔径的滤膜过滤,即得(10 mmol.L-1,pH=4.64)。2 手性衍生化方法 在0.5 mL含阿替洛尔的微粒体孵育液(由“9”项获得)中,加氯化钠0.2 g及浓氨水50 μL,旋涡振荡30 s,加乙酸乙酯3.00 mL,再旋涡振荡2 min,3 000 r.min-1 5 min,精密移取有机层2.80 mL至另一试管,加无水硫酸钠约70 mg脱水后,再精密移取有机层2.60 mL至另一试管中,在室温下用空气吹干,加入与药物摩尔比约为1∶2量的GITC乙腈液(称取GITC 2.0 mg,用1.0 mL乙腈溶解,实验中根据需要用乙腈进一步稀释后使用。),35 ℃恒温反应30 min,吹干后用NaH2PO4缓冲液-CH3CN混合液(50∶30)300 μL溶解后,色谱进样20 μL。3 色谱条件 色谱柱:Shim-pack CLC-ODS(25 cm×4.6 mm, 10 μm);保护柱:ODS(10 mm×5 mm,10 μm);检测波长:254 nm;灵敏度:0.005AUFS;流速:0.5 mL.min-1;流动相:NaH2PO4缓冲液-CH3OH-CH3CN(50∶20∶30)。 此条件下阿替洛尔的微粒体孵育液经手性衍生化后的典型色谱图见图2。图2 阿替洛尔的微粒体孵育液经手性衍生化后的典型色谱图A.空白鼠肝微粒体孵育液 B.加样鼠肝微粒体孵育液1.S(-)-阿替洛尔(13.64 min)2.R(+)-阿替洛尔(16.35 min)4 鼠肝微粒体的制备 大鼠(Sprague-Dawley雄性大鼠,体重160~230 g,浙江医科大学实验动物中心提供)用地塞米松磷酸钠(Dex)诱导处理(Dex溶于生理盐水,po 100 mg.kg-1,3 d;末次给药后,于处死前16 h断食,仅给水),然后断头处死,按文献方法[14]制备大鼠肝微粒体备用,置-20 ℃冰冻保存。按Lowry[15]法测定所制得的鼠肝微粒体中的蛋白质浓度。5 色谱条件的选择5.1 检测波长的选择 阿替洛尔衍生物峰在228 nm、254 nm吸收值接近,而在280 nm时吸收值很小。在228 nm时有溶剂峰的干扰,而波长增加则杂质吸收减少,基线易走平。故选择波长为254 nm。5.2 流动相的选择 用甲醇、乙腈、水、2%冰醋酸与NaH2PO4缓冲液(10 mmol.L-1,pH 4.64)分别组成流动相进行试验,结果表明,用水和2%冰醋酸与甲醇配制流动相,分离度较好但峰形较差;流动相改用NaH2PO4缓冲液可改善峰形。在缓冲液中加甲醇作流动相时峰形较好,但一降解产物峰与R(+)-阿替洛尔峰重叠,加乙腈时该降解产物峰与R(+)-阿替洛尔峰已分开但对映体间分离度较差。根据以上结果我们采用混合溶剂(NaH2PO4缓冲液-CH3OH-CH3CN(50∶20∶30)作为流动相(图3),得到较好的分离度(R=1.56)和峰形。图3 阿替洛尔色谱图1. S(-)-阿替洛尔 2. R(+)-阿替洛尔3. 降解产物6 提取条件试验6.1 碱化试剂的选择 阿替洛尔为弱碱性药物,应在碱性条件下提取。分别用浓氨水和氢氧化钠溶液作碱化试剂对水溶液中的阿替洛尔进行提取,
最近想做苯乙胺的手性拆分实验,用液相色谱进行检测,有机相中进行酶法拆分,有没有大神做过这方面的实验啊,,请指点迷津啊,感觉这方面的文献不是很多
[size=3][b]如何对红外光谱3D图进行拆分[/b][/size]有哪位大侠知道,如何对红外光谱3D图进行拆分的?谢谢大家了
因为我下不到,求GC,HPLC,CE用于手性拆分的书,好人上传啊
因公司要求料件拆分均质数必须和历史拆分均质数一致,不然就算不符合,而样品拆分为均质比想象中的要困难,拆分手法、工具、经验等都直接影响到最终的拆分均质数,不管如何规范操作,都会出现漏拆均质的情况,有没有大神提供下建议,是否可以在拆分均质报告中备注免责声明![img]https://ng1.17img.cn/bbsfiles/images/2020/04/202004162048042714_5884_3979656_3.png[/img]
因公司要求料件拆分均质数必须和历史拆分均质数一致,不然就算不符合,而样品拆分为均质比想象中的要困难,拆分手法、工具、经验等都直接影响到最终的拆分均质数,不管如何规范操作,都会出现漏拆均质的情况,有没有大神提供下建议,是否可以在拆分均质报告中备注免责声明![img]https://ng1.17img.cn/bbsfiles/images/2020/04/202004162033552090_5950_3979656_3.png[/img]
如题,要开展这方面的工作,买了根柱子,瓦的,型号:CP-Chirasil-Dex CB(25m,0.32mm,0.25um)。说明书上写的最高柱温200°(恒温),程序升温225°。有没有用过这个型号柱子的版友?老化柱子的时候是否有什么注意事项?手性拆分对载气是否有要求?还有这个型号的固定液组成是什么?
各位老师,在拆分时要求拆分工具不含限用元素,大家有没有推荐的拆分工具呢,我们测试了一下,发现买的工具都含Cr啊,也很难直接找到有RoHS认证的工具,大家用的工具都是什么材质呢?
小弟正在做一个菊酯类拆分,由于没有液相,只能采用:菊酯先水解,再衍生化后,会生成4个异体(资料上说的)。现在用DB-210进行GC分析,很难确定那个峰是属于4个异构体的峰,并且对应的峰是什么?请教各位大哥,是否有什么好的方法确定,(或有哪位大哥做过这类的分析),小弟资源有限,gc-MS就不考虑了!
各位同学,请问一下电池样品测试RoHS该如何拆分呀,是要拆到均质材料吗?如拆成外壳,电极,电芯,电解液,包裹层等吗?请拆过的同学介绍一下经验,谢谢!
我们知道,在测试之前,样品拆分很重要,不知大家公司都有哪些样品拆分工具呢?http://simg.instrument.com.cn/bbs/images/default/em09511.gif我先说下我司目前有的几种简单工具:1. 剪刀 2. 尖嘴钳 3.斜口钳4.老虎钳 5.剥线钳 6.刀片7.砂轮机
在SJ/T 11363-2006中:"电子信息产品中现有条件不能进一步拆分的小型零部件或材料,一般指规格小于或等于4mm3的产品"列为EIP-C类.在 GB/Z 20288-2006《电子电气产品中有害物质检测样品拆分通用要求》 中"3.5当拆分对象难以进一步拆分且质量≤10mg时,不必拆分,作为非均质检测单元,直接提交检测." "3.6 当拆分对象难以进一步拆分且体积≤1.2mm3时,不必拆分,可以整体制样作为非均质检测单元,直接提交检测."关于上面拆分准则,在两个标准中提到的原则是不一样的.我们在实际检测时对产品的拆分到底是以哪个为标准?谢谢!
有没有关于整机拆分的相关资料~~相关方面的知识相当缺乏.谢谢
毛细管气相色谱法:高分辨率,柱效高,开管型→挥发油1.开管柱 (1)特点:固定液量很少(2)类型:①壁涂层开管柱→容量低,不适于痕量分析和室温下分析低分子量成分及永久气体。②载体涂层开管柱(SCOT):应用广,可作痕量组分分析。常用柱:交联弹性石英开管柱(3000多)③大内径厚液膜开管柱:柱容量大,痕量和低分子分析④微内径开管柱:高分离效能。开管柱内径↓,μopt↑,更适用于快速分析。 (3)柱内径:柱内径要兼顾柱效,分析速度和柱容量,0.25~0.53mm。 (4)液膜厚度:df=0.1μm~5μm;df↑,柱容量↑。 (5)柱温:Tc↓,tR↑,毛细管柱常用于程序升温GC。 (6)进样量:n↓10%是最大允许进样量,与柱长、k正比,与n成反比 2.选择毛细管柱: (1)填充柱不能达到分离度(α≥1.015),t长。 (2)b.p≥2℃,选非极性柱;b.p≤2℃,选极性较大柱。 (3)高沸点:选耐热、高温 (4)常用柱(OV—10、OV—210、PEG—20M) 3.进样方式 (1)直接进样:分流(30~50:1)和不分流进样(大内径厚液膜开管柱) (2)顶空进样:在非气态和气态达到平衡后,→吸空气进样 N2吹尾:提高灵敏度;顶空GC:液上气相色谱法或顶空分析法; 优点:含量低;不能直接进样的;最低LOD减小。 基本原理:Ai=fi·pi=fi·γi·pi0·xi →组分 ↓ 组分蒸汽压 γi=1时理想,但其不等于1 当T一定时,气液平衡,若Vs不变,则Cg=C0/(K+ρ)。其中Cg为气相中被测组分浓度,Cs为液相中被测组分浓度,C0为样品中被测组分原始浓度,K=Cs/Cg,为气—液相中被测组分平衡常数。 静态顶空GC装置:?二、手性药物HPLC:纯度检查,分离 三点相互作用:对映体与CSP相互作用的部位,吸引,排斥等。 拆分:直接法(CMP法)和间接法(衍生试剂法) (1)柱前手性衍生化法(GDR法):高光学温度,速率有时不同,非手性柱,提高检测灵敏度,生物样品分析。 (2)手性流动相拆分法(CMP法): 手性添加剂:①配基交换型手性添加剂(CLEC) ②CD环糊精:分子大小形成CD化合物 常用:β—CD、γ—CD或改性CD ③手性离子对络合剂(CIPC)。 (3)手性固定相拆分法(CSP): 蛋白质 π—碱型 三种常用 环糊精 → π—酸型 电荷转移型手性固定相 铜绿 氨基酸型 蛋白质:牛血清蛋白(BSA) CD:疏水性,每个glu有5个手性碳 CDR法:条件简易,普通柱,预分离,光学纬度高。 CMP法:范围的有限,添加剂不稳定,干扰,条件简易,不必柱前衍生化。 CSP法:各类化合物,分析可靠,常规及生物样品,某些需柱前衍生化。三、超高速(UPLC):速度、灵敏度及分离度为HPLC的9、3、和1.7倍;压力大(140pa)。 1.dp↓,更宽优化线速度 2.dp↓,分离速度↑ 条件:dp2μm;超高压溶剂泵;泵片死体积小;快速自动进样;高速检测系统;更适合LC—MS。四、超临界(SFC)色谱SF为流动相,硅胶或化学键合相为“S”对象:热敏性,低挥发性化合物,比GC广;特点:比HPLC分离制备快,更易于MS、FT—IR和MNR连用。五、高速逆流色谱(HSCCC)high-speed counter-current chronati 1.特点: (1)固定相为液体; (2)不出现,峰畸形,拖尾; (3)回收率↑; (4)制备量大,重现性好; (5)体系更换,平衡方便快捷。 2.基本原理:离心力→混合 梯度洗脱 3.装置:进液部;分离部分;输出部分
做了不同区域的地表水项目,原合同委托出在同一份报告里,现在报告已发放。客户又要求拆分报告,按照一个区域出一份报告。是要客户写原因说明,并且敲章?还是补充协议?拆分报告后,原报告还要收回吗?怎样一个流程?