FT-ICR高分辨质谱才是蛋白质天然结构研究的 Mr.Right
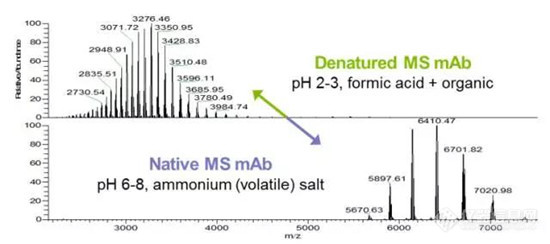
p G 蛋白偶联受体 (G-Protein-coupled reptors, GPCRs) 类的膜蛋白贡献了大约50%的药物靶点,因此对膜蛋白的结构表征意义重大。质谱做为蛋白研究最主要的工具之一已经发展的非常成熟,但由于膜蛋白一旦脱离了稳定的天然膜环境,天然结构就会遭到破坏,因此常规的质谱分析方法难以对膜蛋白等非共价连接的蛋白复合物进行研究。Native Mass 方法 (天然质谱法) 的出现则使对膜蛋白或共价连接的蛋白复合物质谱研究成为可能,Native Mass 可以在消耗少量样品的情况下同时提供分子量、化学计量、纯度等信息,更关键的是在这种方法下蛋白质能保持天然的状态,因此,Native Mass已经成为膜蛋白等非共价连接的蛋白复合物天然结构表征的利器。/pp Native Mass 最早被应用在四级杆-飞行时间质谱 (Q-TOF) 上用于膜蛋白分析,近来年在傅立叶变换质谱 (FT-ICR) 或质量范围扩展的轨道离子阱质谱 (Orbitrap-EMR) 上,采用 Native Mass 方法研究蛋白天然结构的报道越来越多。/pp 2016年,加州大学洛杉矶分校 (UCLA) 的 Loo 教授团队[1]用 Bacteriorhodopsin?OGMicelle (细菌视紫红质-辛烷基葡糖苷胶束) 和 MSP1D1-Nd (膜骨架蛋白-纳米磷脂盘复合物) 作为膜蛋白复合物的模型,比较了 Q-TOF (Waters Synapt G2)、FT-ICR (Bruker Solarix 15T FT-ICR) 和 Orbitrap-EMR (Thermo Orbitrap Exactive-Plus EMR) 三种质谱仪器在 Native MS 时的表现。/pp 分析结果表明 FT-ICR 和 Orbitrap-EMR 相对于 Q-TOF 能得到更高质量的数据,Orbitrap-EMR (图1b) 和 FT-ICR (图1c) Native Mass 质谱图显然比 Q-TOF (图1a) 具有更高的信噪比 (S/N),并且 FT-ICR 和 Orbitrap-EMR 均可以基本做到基线分离,而 Q-TOF 无法做到。另外,由于 FT-ICR 独特的离子传输设计,能更好地保持蛋白 Native 状态,因此,比 Orbitrap-EMR 更容易得到更窄的电荷价态分布,从而使质谱图更简单。/pp style="text-align: center "img src="http://img1.17img.cn/17img/images/201802/noimg/c791e6bd-562c-438b-9808-4781f1ab5d1b.jpg" title="001.png"//pp style="text-align: center "span style="color: rgb(0, 112, 192) "strong ▲ 图1: MSP1D1-Nd 在 Q-TOF (1a)、Orbitrap-EMR (1b) 和 FT-ICR (1c) 上获得的 Native Mass 质谱图。质谱图的右上角为去卷积后的质量分布和电荷数分布热图。/strong/span/pp 不同的解离技术对离子活化效率比较结果显示,相对 Q-TOF 采用的 CID (碰撞诱导解离),FT-ICR 采用的 IRMPD (红外多光子解离) 更容易将 DMPC 从 MSP1D1-Nd 剥离,因此,经过解离后 MSP1D1-Nd 颗粒结合的 DMPC 数目更少,从而使MSP1D1-Nd 的谱图更简单 (图2a, 2b)。/pp style="text-align: center "img src="http://img1.17img.cn/17img/images/201802/noimg/63195da6-1a75-42b7-a342-79db15d7835a.jpg" title="002.png"//pp style="text-align: center "span style="color: rgb(0, 112, 192) " strong ▲ 图2: 在 Q-TOF 平台采用 CID 离子解离时 MSP1D1-Nd 的质谱图 (2a) 在 FT-ICR 采用 IRMPD 离子活化时 MSP1D1-Nd 的质谱图 (2b)。/strong/span/pp FT-ICR 在分析中的独特优势,使其成为 Loo 教授团队 Native Mass 研究首选质谱平台,并在近期完成了多项开创性研究,包括利用 FT-ICR 在 Native Mass 条件下进行 Top-down 分析,研究蛋白和蛋白复合物的结构[2],并将 Native Mass 与 Top-down 技术相结合,用于研究蛋白序列与高级结构和功能的关系[3],还利用 Native Mass 分析方法,精确测定了 ADC (Antibody Drug Conjugates) 的 DAR (Drug Antibody Ratio)[4]。/pp [1] Iain D.G. Campuzano, et al., Anal. Chem., 2016, 88(24), 12427-12436/pp [2] Huilin Li, et al., Anal.Chem., 2017, 89(5), 2731-2738/pp [3] HuilinLi, et al., Nat. Chem.,2018, 10, 139-148/pp [4] Iain D. G. Campuzano,et al., Anal. Chem., 2018, 90(1), 745-751/ppbr//p