[color=#444444]为什么我用离子阱质谱,[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url],测定蛋白质分子量时,得到的蛋白质分子簇不是特别明显,想问一下用什么方法可使得到的蛋白质分子簇更明显些?[/color]
我这个东西可能是重油,碳链应该比较长,沸点在250-300摄氏度之间不知道能不能用质谱测定一下其大概分子量?清高手指教
[color=#444444]想用质谱测定一个小分子的分子量,该物质在水、甲醇中不溶解,而在乙腈中溶解度不是太大。。。。想问一下像这种在溶剂中溶解性不太好的物质,测分子量时有没有影响???或者说质谱测定分子量时,对被测物在溶剂中的溶解度有没有要求?[/color]
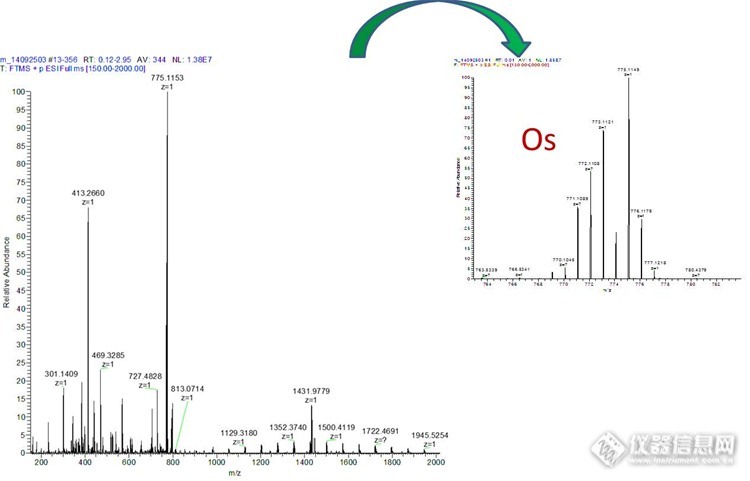
质谱应用之分子量测量 最近10年质谱技术的飞速发展,耐用的离子源,高性能的质量分析器和多种有效的扫描方式推动了质谱仪器走进各个单位,质谱成为功能强大的生物化学分析平台。目前基于质谱的物质定量定性实验应用广泛,从普通色谱-质谱(GC-LC&LC-MS)连用技术的定量分析实验(药理药代、农残筛查、环境污染物分析……),到大规模发现鉴定的组学实验(蛋白质组学和代谢组学)。抛开这些酷炫的方法和技术,我们今天讨论一下质谱的基本应用——测定分子量,通过一些测定分子量的实验我们可以看到分子量代表的更多意义。 质谱分析是一种测量离子质荷比(质量-电荷比)的分析方法,质谱法(Mass Spectrometry, MS)即用电场和磁场将运动的离子(带电荷的原子、分子或分子碎片,有分子离子、同位素离子、碎片离子、重排离子、多电荷离子、亚稳离子、负离子和离子-分子相互作用产生的离子)按它们的质荷比分离后进行检测的方法。测出离子准确质量即可确定离子的化合物组成。这是由于核素的准确质量是一多位小数,决不会有两个核素的质量是一样的,而且决不会有一种核素的质量恰好是另一核素质量的整数倍。分析这些离子可获得化合物的分子量、化学结构、裂解规律和由单分子分解形成的某些离子间存在的某种相互关系等信息(以上内容来自百度百科和高中教科书)。从定义我们看出,测定分子量是质谱的基本技能,一台质谱仪我们首先问的是它测量的分子量范围是多少,测量的准确度怎么样。1小分子的测定 质谱的首先发展是测定元素的相对分子量,比如我们一般说到元素C的分子量是12,其实说的是C在自然界的最高丰度12C的相对原子量,考虑自然界只有12C相对含量1.082%的13C,C准确平均分子量是12.011。化合物一般有C、H、O……多种元素组成,这些元素的同位素互相组合,如果我们的质谱可以区分相邻的同位素的相对分子量,质谱图上会显示的一簇峰,每个质谱峰对应相同的分子式下不同的同位素组成的化合物响应。因为化合物组形成元素的不同,他们的质谱簇峰分子量(momoisotopic mass)组成独特的质谱峰模式(pattern),如果质谱区分不了相邻的同位素峰,这一簇峰变成一个质谱峰所对应的是平均分子量(average mass)。 如果我们测定一个化合物分子量,如果通过质谱可以得到精细的元素分子量(momoisotopicmass)及其相对丰强度(在质谱上表现为簇峰的强度)的信息,可以通过谱图推测化合物的组成写出分子式。图1 A是测的城市污水提取物的分子量,三个主要质谱峰为同一个化合物的同位素质谱峰,推测分子式为C2HO2Br2,采用软件(很多软件都可以进行,最简单的是chem office)模拟此分子式的精确分子量,图2 B即为模拟所得的质谱图。可以看出所测得的质量偏差很小,最高元素峰216.8331-216.8328=0.0003Da,质谱峰分布模式(分子量和相对强度)实际测量图和模拟图几乎一致,可以确定该化合物的分子式是C2HO2Br2。http://ng1.17img.cn/bbsfiles/images/2014/12/201412131121_526995_2265735_3.jpg图1 污水提取物质谱图。A测量图,B模拟图。质谱Thermo LTQ-orbit,HESI源。 对于有特殊的元素的化合物,测量准确的分子量及其同位素质谱模式可以准确的判定特殊元素的存在,图2是测得某配位化合物的质谱图,通过其特殊的质谱图可以确定此化合物为Os金属配合物。http://ng1.17img.cn/bbsfiles/images/2014/12/201412131125_526996_2265735_3.jpg图2 Os配合物质谱图。质谱Thermo LTQ-orbit,HESI源。 上述测量过程简单实用,但是这个实验要求质谱有足够的质量准确度,所测的分子量与实际值最好在小数点最后一位有波动,不然预测分子式会有很大的偏差。2更高分子量的测量 对于同位素峰的测量,需要质谱区分相邻的同位素峰。在图1中两个同位素峰相差越2个道尔顿,在测量217分子量时候,只要质谱可以区分2个道尔顿的质谱峰就可以了,在图2中,同位素峰相差1道尔顿,区分度只有1个道尔顿。当分子量达到5K以上的时候,如果化合物仅仅由CHON等简单同位素组成,因为组成原子个数的增多,同位素峰越来越复杂,两个同位素峰之间的区分度越来越小,当质谱区分不开这些同位素峰的时候,测得是平均分子量(average mass)。图3 A测量的是一个分子量为10380Da的多肽,B和C是带10个电荷和11电荷同位素峰的局部方法图。在B中,同位素质谱峰间距(区分度)为0.1001Da。随着分子量的增加,需要质谱对相近同位素峰区分能力更强。评价质谱这种能力的指标是分辨率,我们一般用单位分辨率R=m/Δm来表示(该论述与严格定义有区别),图1需要的分辨率217/2=108,图2的分辨率780/1=780,而图三需要的分辨率1100/0.1=11000。所以说准确测分子量尤其是大分子量需要质谱具有高的分辨率。http://ng1.17img.cn/bbsfiles/images/2014/12/201412051959_526030_2265735_3.jpg图3多肽质谱测定。 A,质谱图B,,+10电荷质谱放大图C,+11电荷质谱放大图。Thermo LTQ-orbit,HESI源。3不同离子源的测定大分子的策略 目前测定大分子的主要离子源有基质辅助激光解吸(MALDI)和电喷雾(ESI)。图4是采用不同离子源测定聚乙二醇修饰药物分子量,A是MALDI质谱测得,几乎为所有分子的都带一个电荷,质谱间距为聚乙二醇重复单元-CH2-CH2-O-44Da;B为ESI质谱所测谱图,Z为分子所带电荷数,z=4质谱间距为44/4=11,z=3质谱间距为44/3=14.67。http://ng1.17img.cn/bbsfiles/images/2014/12/201412052001_526031_2265735_3.jpg图4聚乙二醇化药物质谱图。A AB MALDI-TOF谱图,基质DHB反射模式;B Thermo ESI-LTQ-Orbit谱图。 MALDI电离的离子一般带一个电荷(随着分子量增加,会出现带多个电荷的情况),图5是测得8478和11675多肽质谱图,5737为11675多肽带双电荷所得。采用MALDI测量分子量谱图测量结果直观方便,图6是测量分子
高分子的平均分子量(包括重均分子量)一般实验室采用体积排阻色谱(ses)来表征,有没有那位大牛用质谱测高分子的分子量?文献上好像有质谱测定的方法
想做核酸检测,但因为是新手,所以N多问题都不是很懂,还望各位大神不吝赐教!1、用质谱对核酸进行定性分析,这样的方法可行吗?2、如果可行,那是不是就是将我做出的质谱图拿来与质谱数据库中的该核酸标准质谱图进行对比,以确定我所得出的就是我想检测的核酸呢?这个不知道思路是不是这样的,如果不是,还望帮我指条明路http://assets.dxycdn.com/gitrepo/bbs/emotions/default/078.gif 如果是这样思路的话,那标准质谱图/质谱数据库我该去哪儿找呢?
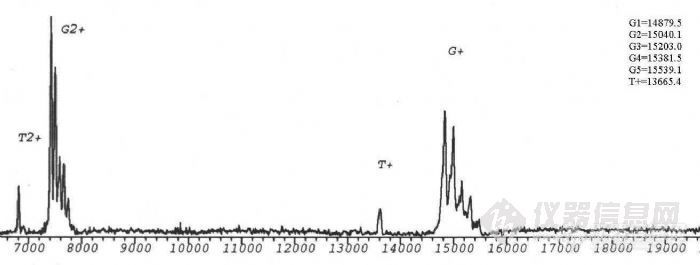
生物质谱在糖蛋白结构分析中的应用项目完成人:桑志红 蔡 耘项目完成单位:国家生物医学分析中心 随着人们对糖蛋白参与生命活动机理的日益深入了解,对天然糖蛋白及重组糖蛋白类药物的分析越来越受到重视。重组糖蛋白类药物的质量控制更是直接关系到药物的疗效及至人类的健康。九十年代以来,随着带有反射功能的基质辅助激光解吸附电离飞行时间质谱(MALDI-TOF-MS)和纳升电喷雾串联质谱(nano-ESI-Q-TOF)等具有软电离方式的现代质谱 技术的发展,质谱以其高灵敏度和强有力的分析混合物的能力,提供了生物大分子的分子量、序列、一级结构信息以及结构转换、修饰等方面的信息,使糖基化分析有了重要的进展。 通常研究糖蛋白的方法是把蛋白链上的寡糖切下来,分别研究蛋白部分和寡糖部分的结构,因此无法研究与两部分共同相关的结构问题,也不能区分不同糖基化位点上切下来的寡糖。自90年代初,国外有人开始用质谱法研究糖蛋白的结构,同时描述了各个位点的不均一性。我们用建立的现代生物质谱技术研究糖蛋白一级结构的方法,将其应用与基因重组糖蛋白的结构分析。为糖蛋白结构分析及基因重组糖蛋白类药物的质量控制提供新的手段。一、 生物质谱研究糖蛋白结构方法的建立实验所用仪器为:1.德国BRUKER 公司的REFLEXIII型基质辅助激光解吸附电离飞行时间质谱仪,N2激光器,波长337nm,线性飞行距离150cm,加速电压2kv。2.英国Micromass 公司Q-TOF型电喷雾串联质谱仪。源温80°C,气体流速40L/h,枪头电压650V,检测频率2.4S,氩气碰撞池压力6*10-5mbar。1. 基质的选择,在MALDI-TOF-MS分析中,基质起着相当重要的作用。不同的基质对不同类的物质响应不同,a-氰基-4-羟基肉桂酸用于测定糖蛋白核糖核酸酶B效果相对较好。2. 糖蛋白分子量的测定,糖蛋白核糖核酸酶B由124个氨基酸组成,在34位Asn处连有一个高甘露糖型N-糖链。由于糖链的微不均一性,与普通蛋白质及核酸不同,其分子离子峰在MALDI-TOF-MS 质谱图上表现为一簇峰,各峰之间约相差一个糖基。正是由于这种微不均一性,使得其分子离子峰变宽,灵敏度降低。糖链分子量越大,峰越宽,灵敏度越低,所以一般只有糖链较短,蛋白的质量不太大的糖蛋白才能测定其平均分子量。用MALDI-TOF可直接测定糖蛋白核糖核酸酶B的平均分子量为 15208.6Da。http://ng1.17img.cn/bbsfiles/images/2011/03/201103211511_284179_1604317_3.jpg3. 糖含量的测定,采用O聚糖酶及内糖苷键酶F分别作用于核糖核酸酶 B,只有内糖苷键酶F能够是其分子量发生变化,表明核糖核酸酶B分子中不存在O-连接糖链存在着N-连接糖链。内糖苷键酶F切断N-糖链五糖核心最内侧的GlcNAc-GlcNAc糖苷键,得到含一个GlcNAc的肽链,减去GlcNAc,可以计算出准确的肽链分子量T=13695.6,与糖蛋白平均分子量之差为糖链的平均分子量G=1513.4,平均糖含量为:(糖链大小/糖蛋白分子量)×100%=9.95%。4. 糖基化位点的确定,研究糖基化类型及糖基化位点的策略:采用蛋白酶酶解与糖苷内切酶酶解相结合的方法,通过酶切前后含糖肽片的位移,结合网上数据库检索,可以确定糖基化类型和糖基化位点。以不同类型的糖苷内切酶作用于糖蛋白(N-糖苷键酶或O-糖苷键酶),在MALDITOF-MS 上观察其质量的变化,可以直接确定糖蛋白中是否含有响应类型的糖链,这是我们确定糖蛋白中糖苷键类型的基础。我们采用先将核糖核酸酶B还原烷基化,加Glu-C酶切,产物再用内糖苷肩酶F酶切,可观察到含糖肽段出现位移,将核糖核酸酶B的肽质量指纹图进行数据库检索,证实发生位移的肽段中含有N-糖链特异连接位点,由此确定34位Asn为糖基化位点。另外我们采用内糖苷键酶F及肽-N-聚糖酶F两种酶进行差位酶切法对含糖肽段进行验证,两种酶酶切后分子离子峰的差值除以GlcNAc的质量,结果就是N-糖基化位点的个数5. 质谱测定氨基酸序列, 我们对核糖核酸酶B肽质量指纹谱中的含糖肽段进行了串联质谱测定,首先在一级质谱图中选择离子4972.23,在串联质谱的碰撞活化室以氩气与其碰撞产生碎片,从碎片的质荷比推算出此肽片中的一段氨基酸序列,检索结果为核糖核酸酶B,从而判断其理论序列是否一致。6. 糖链结构的研究,凝集素对糖肽的亲和提取,进一步分析糖肽序列及糖链结构的关键是含糖肽段的提取。核糖核酸酶B中糖链为高甘露糖型,我们选用对其有特异性吸附的伴刀豆球蛋白对其进行提取利用这种简捷的亲和质谱的方法,对糖肽段进行了分析。建立了亲和质谱分析糖肽类物质的方法,为今后糖肽序列分析及糖链结构分析奠定了基础。二、基因重组糖蛋白人促红细胞生成素(rhEPO)的结构分析。 利用以上建立的方法,我们对样品重组人促红细胞生成素进行了分析,断定此样品为非完全糖基化,样品中只存在N-连接的糖链,无O-糖链。应用酶切法用肽-N-聚糖酶处理后,得到两个含糖肽段,进行数据库检索,测得38位及83位为N-糖基化位点,与文献报道相符,结果可靠。因此,该项课
[color=#444444]为什么分子量多24?[/color][color=#444444]我做了三个化合物,组成原子为C、H、O、N,进行分子量鉴定,质谱数据比理论上的分子量每个化合物都多24!我怀疑是质谱测试的系统误差,可是我不知道这个误差是怎么来的。请专家帮助我!谢谢[/color]
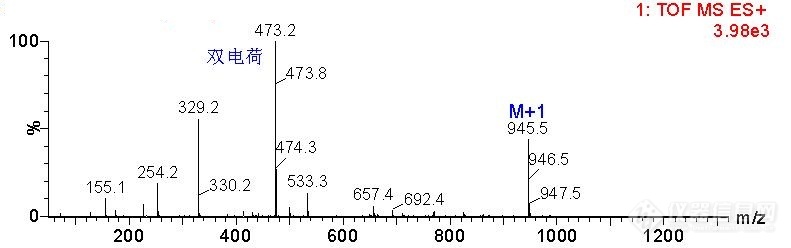
[color=#444444]求大家帮忙看看这张ESI质谱图[/color][color=#444444]以下是我打的质谱图,样品为多肽。[/color][color=#444444]我的目的是想看分子量。[/color][color=#444444]我是用UPLC-QTOF-MS做的,ESI源,仪牌子是Waters MALDI SYNAPT QTOF MS液相色谱串联四级杆飞行时间质谱。[/color][color=#444444]那请问大家,从这张图上如何分析我样品的分子量?[/color][color=#444444]其次,图右上角的3.98e3是什么意思?代表样品的能量信号吗?样品含量越高,这个值也就越大吗?[/color][color=#444444]不甚感激!!![/color][color=#444444][img=,690,216]https://ng1.17img.cn/bbsfiles/images/2019/08/201908281609380409_3981_1806906_3.jpg!w690x216.jpg[/img][/color]
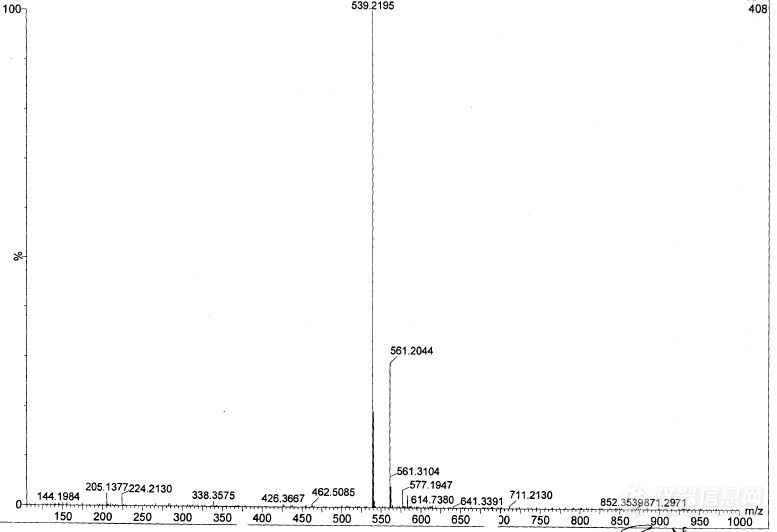
[color=#444444]化合物的真实分子量应该是512,但是在它的质谱图的峰对应的分子量却是539,我想不明白是怎么回事。下面分别是分子结构以及质谱图。[/color][color=#444444]请大家帮忙,看看这张质谱图是不是正确的。[/color][color=#444444][img=,690,472]https://ng1.17img.cn/bbsfiles/images/2019/08/201908301112390150_900_1827556_3.jpg!w690x472.jpg[/img][img=,287,202]https://ng1.17img.cn/bbsfiles/images/2019/08/201908301112398496_2516_1827556_3.jpg!w287x202.jpg[/img][/color]
基于质谱的DNA序列测定进展 许崇峰 杨芃原 岳贵花 卞利萍 摘 要 对质谱DNA序列测定的各种技术的原理、进展、面临的困难以及发展的前景作了评述。 关键词 质谱 DNA序列测定 评述 Abstract This article gives a review on DNA sequencing by mass spectrometry,including the principles of MS techniques,and their progress,difficulties and perspective. Key words Mass spectrometry;DNA sequencing;Review 1 引言 DNA序列分析在生物基因学以及遗传病和病毒性疾病的诊断和治疗上具有重要的作用。用质谱化学方法进行DNA序列分析是一种新兴的技术。Sanger双脱氧链终止序列测定方法是常规的DNA序列分析方法,Sanger产物需要通过凝胶分离和显色来得到DNA的序列信息。而当采用质谱(MS)时,Sanger产物可不需分离而直接测定,因而质谱方法具有快速性的优点。80年代中后期相继出现的质谱离子化新技术电喷雾(ESI)和基体辅助激光解析电离(MALDI)使得用质谱进行DNA序列测定成为可能。但是由于技术尚不成熟,目前使用质谱方法仅能测定含几十个碱基的寡聚核苷酸。要使质谱在人类基因工程(HGP)和临床分析中得到广泛的应用,质谱技术和质谱方法必须得到显著改善。2 生物质谱方法 生物质谱,有别于传统质谱,测定的对象是分子量可高达几万至几十万的生物分子,这使得传统的电子轰击(EI)、化学电离(CI)等电离技术的应用受到了极大的限制。随着快原子轰击(FAB)、MALDI、ESI、离喷雾(IS)、大气压下碰撞电离(APCI)等电离技术的出现,大大提高了质谱的测定范围。特别是ESI-MS和MALDI-MS显示了在生物大分子分析(如蛋白质和核酸)上的巨大潜力。 2.1 ESI-MS 电喷雾是一种软电离方法。通常认为电喷雾可以用两种机制来解释:1)离子蒸发机制,在喷针针头与施加电压的电极之间形成了强电场,该电场使液体带电,带电的溶液在电场的作用下向带相反电荷的电极运动,并形成带电的液珠(液滴)。由于小雾滴的分散,比表面增大,在电场中迅速蒸发,结果使带电雾滴表面单位面积的场强高达108V/cm2,从而产生液滴的“爆裂”。重复此过程,最终产生分子离子;2)带电残基(分子)机制,首先也是电场使溶液形成带电雾滴,带电雾滴在电场作用下运动并迅速溶去,溶液中分子所带电荷在去溶时被保留在分子上,结果形成离子化的分子。一般来讲,电喷雾方法适合使溶液中的分子带电而离子化。离子蒸发机制是主要的电喷雾过程,但对质量数大的分子化合物,带电残基的机制也会起相当重要的作用。 电喷雾所形成的离子是多电荷离子,由于质谱测定的是质荷比,这就拓宽了它所能测定的质量范围,使得它适合于生物大分子的测定。 2.2 MALDI-MS MALDI也是一种软电离方法,它利用激光束照射分散于基体(又称基质、底物)中的样品,由于样品被包裹在基体中,因而大部分激光能量被基体所吸收,从而保护了样品分子。MALDI中的基体起到了多种重要的作用:从脉冲激光中吸收足够的能量;隔离样品分子;提供光激发的酸或碱基团,以及在离子-分子碰撞中电离样品分子。目前MALDI比较公认的机理是:激光光束的能量首先被发色团的基本吸收,接着这些基体迅速蒸发为气相,被包含的分析物的分子从而被带入气相。而离子化的产生是由于受激的基体分子将质子转移给分析物分子。 MALDI可以由不同类型的质谱来实现,特别是飞行时间质谱(TOF)。理论上,飞行时间质谱的质量上限是无限的,这决定了它特别适合于生物大分子分子量的测定。

[color=#444444]如题,为啥?理论值305.05,实测305.49?分子式有二茂铁和酚羟基,我是用Chemdraw计算的分子量[/color][color=#444444][color=#444444]核磁打了没问题,很纯。是不是质谱机器问题?[/color][color=#444444]各位大侠帮忙。[/color][/color][color=#444444][color=#444444][img=,576,330]https://ng1.17img.cn/bbsfiles/images/2019/09/201909101101275508_2448_1827556_3.png!w576x330.jpg[/img][/color][/color]
一些基础的问题请大佬帮忙解答一下:1、在相关查阅学习中,都提到了原子量和分子量是没有单位的,但是为什么质谱中又用Da(D)来作为原子量(分子量)的单位?2、“质谱中不能用平均分子量计算离子的化学组成,例如:不能用氯的平均分子量35.5,而是用35和37”,这里35.5不应该是氯的相对原子质量吗?所以这些基础的东西搞的傻傻分不清楚了,希望有老师帮忙解惑
核酸及蛋白质常用数据1.核苷三磷酸的物理常数化合物分子量λmax(pH7.0)1摩尔溶液(pH7.0)中λmax时的最大吸收值OD280/OD260ATP507259154000.15CTP48327190000.97GTP523253137000.66UTP484262100000.38dATP494259152000.15dCTP46727193000.98dGTP507253137000.66dTTP48226796000.712.常用核酸的长度与分子量核酸核苷酸数分子量λDNA48502(双链环状)3.0×107pBR3224363(双链)2.8×10628SrRNA48001.6×10623SrRNA37001.2×10618SrRNA19006.1×10519SrRNA[/td
[color=#444444]最近用同样方法做了一系列的化合物。就是苯环的官能团变一下。其中有一个化合物我做质谱时发现100%峰比我的分子量少了1,氢谱能对上挺纯的,其他的化合物的分子量都能对上,就差这一个化合物。不知道怎么回事儿,请教一下大家。谢谢了![/color][color=#444444]MS:GC-EI,[/color]
[color=#444444]利用液相色谱-质谱做的酯类润滑油,检测出分子量都在七八百,实际情况应该在四百左右。请问什么因素会导致检测结果大这么多呢?[/color]
21世纪的最前沿科学之一,随着人类第一张基因序列草图的完成和发展,生命科学的研究也将进入一个崭新的后基因组学,即蛋白质组学时代。正如基因草图的提前绘制得益于大规模全自动毛细管测序技术一样,后基因组研究也将会借助于现代生物质谱技术等得到迅猛发展。本文拟简述生物质谱技术及其在生命科学领域研究中的应用。1 质谱技术质谱( Mass SPectrometry)是带电原子、分子或分子碎片按质荷比(或质量)的大小顺序排列的图谱。质谱仪是一类能使物质粒子高化成离子并通过适当的电场、磁场将它们按空间位置、时间先后或者轨道稳定与否实现质荷比分离,并检测强度后进行物质分析的仪器。质谱仪主要由分析系统、电学系统和真空系统组成。质谱分析的基本原理用于分析的样品分子(或原子)在离子源中离化成具有不同质量的单电行分子离子和碎片离子,这些单电荷离子在加速电场中获得相同的动能并形成一束离子,进入由电场和磁场组成的分析器,离子束中速度较慢的离子通过电场后编转大,速度快的偏转小;在磁场中离子发生角速度矢量相反的偏转,即速度慢的离子依然偏转大,速度快的偏转小;当两个场的偏转作用彼此补偿时,它们的轨道便相交于一点。与此同时,在磁场中还能发生质量的分离,这样就使具有同一质荷比而速度不同的离子聚焦在同一点上,不同质荷比的离子聚焦在不同的点上,其焦面接近于平面,在此处用检测系统进行检测即可得到不同质荷比的谱线,即质谱。通过质谱分析,我们可以获得分析样品的分子量、分子式、分子中同位素构成和分子结构等多方面的信息。质谱技术的发展质谱的开发历史要追溯到20世纪初J.J.Thomson创制的抛物线质谱装置,1919年Aston制成了第一台速度聚焦型质谱仪,成为了质谱发展史上的里程碑。最初的质谱仪主要用来测定元素或同位素的原子量,随着离子光学理论的发展,质谱仪不断改进,其应用范围也在不断扩大,到20世纪50年代后期已广泛地应用于无机化合物和有机化合物的测定。现今,质谱分析的足迹已遍布各个学科的技术领域,在固体物理、冶金、电子、航天、原子能、地球和宇宙化学、生物化学及生命科学等领域均有着广阔的应用。质谱技术在生命科学领域的应用,更为质谱的发展注入了新的活力,形成了独特的生物质谱技术。 2 生物质谱技术电喷雾质谱技术和基质辅助激光解吸附质谱技术是诞生于80年代末期的两项轨电离技术。这两项技术的出现使传统的主要用于小分子物质研究的质谱技术发生了革命性的变革。它们具有高灵敏度和高质量检测范围,使得在pmol(10-12甚至fmol(10-15的水平上准确地分析分子量高达几万到几十万的生物大分子成为可能,从而使质谱技术真正走入了生命科学的研究领域,并得到迅速的发展。以下主要介绍与生物医学有关的几项质谱技术。电喷雾质谱技术电喷雾质谱技术(Electrospray Ionizsation MassSpectrometry,ESI-MS)是在毛细管的出口处施加一高电压,所产生的高电场使从毛细管流出的液体雾化成细小的带电液滴,随着溶剂蒸发,液滴表面的电荷强度逐渐增大,最后液滴崩解为大量带一个或多个电荷的离子,致使分析物以单电荷或多电荷离子的形式进入[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]。电喷雾离子化的特点是产生高电荷离子而不是碎片离子,使质量电荷比(m/z)降低到多数质量分析仪器都可以检测的范围,因而大大扩展了分子量的分析范围,离子的真实分子质量也可以根据质荷比及电行数算出。电喷雾质谱的优势就是它可以方便地与多种分离技术联合使用,如液一质联用([url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url])是将液相色谱与质谱联合而达到检测大分子物质的目的。基质辅助激光解吸附质谱技术基质辅助激光解吸附质谱技术(MatriX AssistedLaser Desorption /Ionization,MALDI)的基本原理是将分析物分散在基质分子中并形成晶体,当用激光照射晶体时,由于基质分子经辐射所吸收的能量,导致能量蓄积并迅速产热,从而使基质晶体升华,致使基质和分析物膨胀并进入[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]。MALDAI所产生的质谱图多为单电荷离子,因而质谱图中的离子与多肽和蛋白质的质量有—一对应关系。MALDI产生的离子常用飞行时间(Time-of-Flight,TOF)检测器来检测,理论上讲,只要飞行管的长度足够,TOF检测器可检测分子的质量数是没有上限的,因此MALDI-TOF质谱很适合对蛋白质、多肽、核酸和多糖等生物大分子的研究。快原子轰击质谱技术快原子轰击质谱技术是一种软电离技术,是用快速惰性原子射击存在于底物中的样品,使样品离子溅出进入分析器,这种软电离技术适于极性强、热不稳定的化合物的分析,特加适用于多肽和蛋白质等的分析研究。只能提供有关离子的精确质量,从而可以确定样品的元素组成和分子式。而FABMS-MS串联技术的应用可以提供样品较为详细的分子结构信息,从而使其在生物医学分析中迅速发展起来。同位素质谱是一种开发和应用比较早的技术,被广泛地应用于各个领域,但它在医学领域的应用只是近几年的事。由于某些病原菌具有分解特定化合物的能力,该化合物又易于用同位素标示,人们就想到用同位素质谱的方法检测其代谢物中同位素的含量以达到检测该病原菌的目的,同时也为同位素质谱在医学领域的应用开辟了一条思路。3 生物质谱技术的应用随着质谱技术的不断改进和完善,质谱的应用范围已扩展到生命科学研究的许多领域,特别是质谱在蛋白质、医学检测、药物成分分析及核酸等领域的应用,不仅为生命科学研究提供了新方法,同时也促进了质谱技术的发展。质谱与蛋白质分析蛋白质分子量的测定 蛋白质类生物大分子分子量的测定有着十分重要的意义,如对均一蛋白质一级结构的测定,既要测定蛋白质的分子量,又要测定亚基和寡聚体的分子量及水解、酶解碎片的分子量。常规的分子量测定主要有渗透压法、光散射法、超速高心法、凝胶层析及聚丙烯酸胺凝胶电泳等。这些方法存在样品消耗量大,精确度低易受蛋白质的形状影响等缺点。MALI-MS技术以其极高的灵敏度、精确度很快在生物医学领域得到了广泛的应用,特别是在蛋白质分析中的应用,至今已被分析的蛋白质已有数百种之多,不仅可测定各种亲水性、疏水性及糖蛋白等的分子量,还可直接用来测定蛋白质混合物的分子量,也能被用来测定经酶等降解后的混合物,以确定多肽的氨基酸序列。可以认为这是蛋白质分析领域的一项重大突破。蛋白质组研究 蛋白质组是指一个基因组、一个细胞或组织所表达的全部蛋白质成分。蛋白质组的研究是从整体水平上研究细胞或有机体内蛋白质的组成及其活动规律,包括细胞内所有蛋白质的分离、蛋白质表达模式的识别、蛋白质的鉴定、蛋白质翻译后修饰的分析及蛋白质组数据库的构建。质谱技术作为蛋白质组研究的三大支撑技术之一,除了用于多肽、蛋白质的质量测定外,还广泛地应用于肽指纹图谱测定以及氨基酸序列恻定等。肽指纹图谱( PePtide Mass Fingerprinting,PMF)测定是对蛋白酶解或降解后所得多肽混合物进行质谱分析的方法,对质谱分析所得肽片与多肽蛋白数据库中蛋白质的理论肽片进行比较,从而判别所测蛋白是已知还是未知。由于不同的蛋白质具有不同的氨基酸序列,因而不同蛋白质所得肽片具有指纹的特征。采用肽指纹谱的方法已对酵母、大肠杆菌、人心肌等多种蛋白质组进行了研究。对大肠杆菌经PVDF膜转印的蛋白质的研究表明,三个肽片即可达到对蛋白质的正确识别。而采用原位酶解的方法对酵母蛋白质组研究的结果显示,约90%的蛋白质被识别,其中三十多种新蛋白质被发现,而这些蛋白质是酵母基因组研究中未能识别的开放阅读框架。研究显示,肽指纹谱的方法比氨基酸组成分析更为可靠,这是因为MALDI测定肽质量的准确度为99.9%,而氨基酸组成分析的准确度仅为90%。另外MALDI可以耐受少量杂质的存在,对于纯度不是很高的样品也能得到理想的结果。对肽序列的测定往往要通过串联质谱技术才能达到分析目的,它采用不同的质谱技术选择具有特定质荷比的离子,并对其进行碰撞诱导解高,通过推断肽片的断裂,即可导出肽序列。质谱与核酸研究现代质谱技术自诞生以来在多肽及蛋白质的研究中获得了极大的成功,于是人们开始偿试着特质谱技术用于核酸的研究工作,近年来合成寡核苷酸及其类似物作为反义治疗剂在病毒感染和一些癌症的治疗方面有着良好的前景,寡核苷酸作为药物其结构特征必须进行确证。常规的色谱或电泳技术只能对其浓度和纯度进行分析,而对其碱基组成、序列等结构信息却无能为力。ESI和MALDI质谱技术的出现为寡核苷酸及其类似物的结构和序列分析提供了强有力的方法,它是将被测寡核苷酸样品先用外切酶从3’或5’端进行部分降解,在不同时间内分别取样进行质谱分析,获得寡核苷酸部分降解的分子离子峰信号,通过对相邻两个碎片分子质量进行比较,可以计算出被切割的核苷酸单体分子质量,将其与四个脱氧苷酸的标准分子量进行对照,就可以读出寡核苷酸的序列。由于MALDI技术分辨率的问题,使得其更适合于减基数较少的短链核酸的分析。如何获得高分辨率的DNA质谱图一
请问MALDI-TOF测定未知多糖的分子量,时采用什么样的测定条件?谢谢
有机质谱原理及应用 陈耀祖,涂亚平主编 有机质谱是有机结构分析和有机成分分析不可缺少的工具,目前发展的三个热点是:软电离技术、联用技术和生物大分子质谱分析。本书是根据作者在实际教学与有机质谱研究工作中的实际经验编写而成的,在介绍有机质谱的常用技术及原理的基础上,结合生物活性分子的分析着重介绍这些热点技术的研究,具有鲜明的实用性。另外,本书还结合作者在分子一离子反应机理方面进行的开拓性研究,介绍反应质谱在立体化学分析中的应用,更富启发性。 本书可供大专院校化学、生物、医药学专业高年级学生及研究生和科研、生产、环保监测单位的分析工作人员参考阅读。 本书目录 目录 前言 第一章 绪论 1.1有机质谱的发展历史 1.2我国有机质谱概况 1.3有机质谱的进展 参考文献 第二章 有机质谱仪器 2.1进样系统 2.1.1储罐进样 2.1.2探头进样 2.1.3色谱进样 2.2电离方式和离子源 2.2.1电子轰击电离 2.2.2化学电离 2.2.3大气压化学电离 2.2.4二次离子质谱 2.2.5等离子体解吸质谱 2.2.6激光解吸/电离 2.2.7电喷雾电离 2.3质量分析器 2.3.1扇形磁场和静电场 2.3.2四极分析器与离子 2.3.3飞行时间质谱 2.3.4傅里叶变换离子回旋共振 参考文献 第三章 电子轰击质谱 3.1电离过程 3.1.1分子的电离与FranckCondon原理 3.1.2电离能和出现能 3.2离子的单分子反应动力学 3.2.1离子的飞行时间及寿命 3.2.2分子离子的能量分布和能量转换 3.2.3离子的热力学能和反应速率 3.3分子离子的单分子碎裂反应 3.3.1离子的碎裂反应中心 3.3.2分子离子的单分子碎裂反应 参考文献 第四章 化学电离质谱 4.1分子和离子的热化学性质 4.1.1质子亲和势与[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]碱度 4.1.2氢负离子亲和势 4.1.3电子亲和势 4.1.4[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]酸度 4.1.5结构对热化学性质的影响 4.2化学电离中的离子分子反应 4.2.1质子转移反应 4.2.2电荷交换反应 4.2.3氢负离子转移反应 4.2.4加合与缔合反应 4.2.5特殊反应 4.3化学电离试剂体系 4.3.1质子转移试剂 4.3.2电荷交换试剂 4.4分子的质子化位置 4.4.1脂肪族化合物 4.4.2芳香族化合物 参考文献 第五章 质谱/质谱 5.1质谱/质谱基础 5.1.1质谱/质谱基本概念 5.1.2质谱/质谱仪器 5.1.3碎裂与重排反应热力学 5.2质谱/质谱研究方法 5.2.1亚稳离子与动能释放 5.2.2碰撞诱导解离 5.2.3中性化再电离和碰撞诱导解离电离 5.3质谱/质谱的应用 5.3.1离子结构的确定 5.3.2反应机理的推测 参考文献 第六章 反应质谱 6.1概述 6.2反应质谱在立体化学分析及苯环位置异构体区分中的应用 6.2.1糖的立体化学分析 6.2.2直链邻二羟基物的立体化学分析 6.2.3取代烯的立体化学分析 6.2.4甾体化合物的立体化学分析 6.2.5氨基酸的手性检测 6.2.6有机化合物绝对构型测定 6.2.7二元取代苯异构体的区分 6.2.8双键位置的测定 6.3自碰撞室引入试剂的反应质谱 6.3.1[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]离子/分子反应机理研究 6.3.2离子结构测定和异构体区分 6.3.3有机物结构测定 6.3.4金属离子反应 6.3.5检测[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]中H/D交换反应 参考文献 第七章 质谱法测定分子结构(I)原理 7.1概述 7.1.1分子量的测定 7.1.2元素组成的确定 7.1.3测定官能团和碳骨架 7.2质谱裂解机理 7.2.1游离基中心引发的裂解 7.2.2电荷中心引发的裂解 7.2.3游离基中心引发的重排 7.2.4电荷中心引发的重排 7.2.5其他裂解反应 7.2.6影响离子丰度的因素 7.3各类化合物的裂解特征 7.3.1烃 7.3.2羟基化合物 7.3.3卤化物 7.3.4醚 7.3.5醛、酮 7.3.6羧酸 7.3.7羧酸酯 7.3.8胺 7.3.9酰胺 7.3.10腈 7.3.11硝基物 参考文献 第八章 质谱法测定分子结构(II)示例 例1溴苯 例2戊酮 例3亮氨酸 例4二十九碳醇 例5氨基3氯吩嗪 例6皂苷loganin的苷元 例7Mo(CO)3与异丙苯复合物 例84腈基4羟基二苯甲烷 例9新当归内酯 例10BrefeldinA 例11生物碱 例12木脂素 例13糖苷 例14混合糖苷 例15紫乌定及类似二萜生物碱 例16鬼桕毒素类 参考文献 第九章 生物大分子的质谱分析 9.1概述 9.1.1电喷雾电离质谱(ESIMS) 9.1.2基质辅助激光解吸离子化质谱 9.1.3快原子轰击质谱(FABMS) 9.2多肽和蛋白质的质谱分析 9.2.1多肽和蛋白质的一级结构 9.2.2多肽和蛋白质的分子量测定 9.2.3多肽和蛋白质的序列分析 9.3核酸的质谱分析 9.3.1核酸的一级结构 9.3.2核酸分子量的测定 9.3.3核酸的序列分析 9.4糖类的质谱分析 9.4.1概述 9.4.2寡糖的质谱分析 9.4.3糖复合物的质谱分析 参考文献 附录Ⅰ 分子的质子亲和度(PA)和[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]碱度(GB) 附录〖WTHZ〗Ⅱ 离子和中性物种的热化学数据 [em09511]在资料中心的下载地址为:[url=http://www.instrument.com.cn/download/shtml/088332.shtml]http://www.instrument.com.cn/download/shtml/088332.shtml[/url]
chemdraw中的分子量哪个和质谱数据对应?如下面分子式会给出两个分子量,二者有什么区别?到底哪个是和质谱对应的?谢谢!Chemical Formula: C18H21NO5Exact Mass: 331.1420Molecular Weight: 331.3630
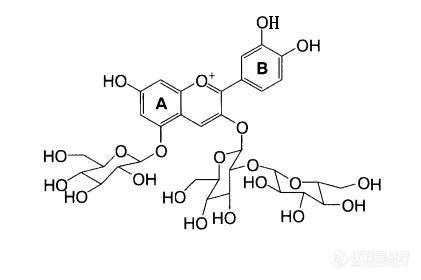
[color=#444444]因为要做高分辨质谱,所以要知道化合物的分子式。看了很多文献,写花色苷的结构式时,那个氧原子上都有个加号,这个是正离子吧,如下图。它的中文名称是矢车菊-3-二葡萄糖苷-5-葡萄糖苷,按这个正离子数出来,应该是C(33)H(41)O(21),那么它的分子量计算时是不是要减去一个氢原子,为C(33)H(40)O(21)啊?做质谱时筛选母离子是用C(33)H(41)O(21) 还是C(33)H(40)O(21)来设置加氢加钠啊?应该按照请大家帮帮忙!谢谢!算分子量是不是要按照中性分子来计算啊?[/color][color=#444444][img=,421,280]https://ng1.17img.cn/bbsfiles/images/2019/09/201909060957079190_8147_1843534_3.jpg!w421x280.jpg[/img][/color]
质谱可测的分子量的大小,是由什么决定的呢?本人质谱小白一枚,还望前辈指点
求助,请问测试胶原蛋白一级分子量的质谱图是这个样子是因为什么呀[img=,690,400]https://ng1.17img.cn/bbsfiles/images/2023/11/202311161504437870_2134_5879980_3.png[/img]
请教一下各位:分子量测定用哪种质谱比较合适呢?
质谱分析分子量减少17是为什么
求大家帮忙看看这张ESI质谱图以下是我打的质谱图,样品为多肽。我的目的是想看分子量。我是用UPLC-QTOF-MS做的,ESI源,仪牌子是Waters MALDI SYNAPT QTOF MS液相色谱串联四级杆飞行时间质谱。那请问大家,从这张图上如何分析我样品的分子量?其次,图右上角的3.98e3是什么意思?代表样品的能量信号吗?样品含量越高,这个值也就越大吗?不甚感激!!!http://edu.emuch.net/attachment/0b/cd/1217637_1301900306_879.jpg

1.问题描述在化合物检测中,质谱检测由于其高精密和宽检测范围,是化合物定性和定量分析的必要手段 其检测的离子峰基于精确分子量(ExcatMass),12C为12,1H为1.007825,16O为15.994915,而一般数据库或计算所得均为相对分子量,在实际检测过程中不能满足及时、快速的计算要求。利用[b]小程序-分子量计算器[/b]可以快速、准确解决这一问题。2.搜索小程序-分子量计算器[img=搜索小程序,627,377]https://ng1.17img.cn/bbsfiles/images/2019/07/201907231138351812_3608_3963607_3.png!w627x377.jpg[/img][align=left]3.分子量计算器主界面[/align][align=left]点击进入小程序后,主界面如下所示:[/align][img=,375,648]https://ng1.17img.cn/bbsfiles/images/2019/08/201908141636090567_9413_3963607_3.png!w375x648.jpg[/img][align=left]4.小程序计算相对分子量通过键盘输入分子式,如乙酸乙酯分子式为C4H8O2,依次点击’C’-’4’-’H’-’8’-’O’-’2’,然后点击‘≈’(即约等号),即可得到该化合物的相对分子量,结果为88.106。[/align][img=,372,649]https://ng1.17img.cn/bbsfiles/images/2019/08/201908141636370065_6838_3963607_3.png!w372x649.jpg[/img][align=left]5.小程序计算精确分子量[/align][align=left]同上操作,按‘=‘(即等号),即可得到该化合物的精确分子量,结果为88.05243。[/align][img=,374,644]https://ng1.17img.cn/bbsfiles/images/2019/08/201908141636560395_842_3963607_3.png!w374x644.jpg[/img]6.结束语简单快捷的操作,准确的计算结果,希望能够成为质谱检测工作者的手边利器。[img=,258,258]https://ng1.17img.cn/bbsfiles/images/2019/07/201907271601233013_7936_3963607_3.jpg!w258x258.jpg[/img]----------------------------------------[align=left]版本更新,界面稍有变化,功能有所加强。如乙酸乙酯C4H8O2,亦可输入CH3COOC2H5,小程序会自动简化分子式,并计算相对分子量/精确分子量,最大支持原子个数99。如无法使用,请更新至微信最新版本。[/align]
带羟基和羧酸的二萜,二级质谱中碎片离子质量与分子量差62,这是掉落了什么呀
刚入手单四级杆质谱,发现分子量误差比较大,分子量大比如1000左右的误差0.5,分子量小的大概300误差0.2,不知道是不是正常,还有厂家让进样浓度很低,紫外都快观察不到,一般正常紫外吸收多高分析合适,进样浓度太低,主峰都很矮,杂质峰就看不到,怎么提取分子量,还忘各位大师指点
新合成了一种富勒烯的氨基高分子衍生物,可完全溶于水,分子量约在17000-20000之间,但去做过质谱无法离子化做不出来。请问各位大虾还有其他什么方法能够测定其分子量的么?北京有哪些测试中心可以做?给个联系方式就行,非常感谢!