
选择离子流动管质谱是一种新的实时分析技术。它采用软化学电离方法,使用H3O+、NO+和O2+作为初始离子,与目标分析物在流动管中反应,通过四级杆虑质器进行全扫描或者SIM,无需色谱分析,即可同时定性和定量全空气样品中的多种VOCs化合物至ppb甚至ppt水平。历史选择离子流动管质谱作为分析技术在1996年由Spanel 和 Smith教授第一次提出,但它的起源应追溯到20世纪60年代。1963年,Prof. H.P. Broid实验室研究中性分子在氦气流动余辉(亚稳态氦)中的光谱性质时发现,中性分子在氦气流速100m/s下在1m处发生电离。在1969年,美国ESSA(美国海洋大气局前身)实验室采用流后余辉质谱仪第一次定量了离子-分子反应速率常数(Ferguson and co-workers)。此技术被用于大气电离层和星际间气体反应研究。但是流后余辉技术有两大缺陷:1.不纯物造成不必要的化学反应;2.流动管中出现电子。为了克服这些问题,Smith 和 Adams发明了SIFT(selected ion flow tube)技术:通过引进第二个四级杆虑质器分离离子产生区域和离子-分子反应区域。此后,SIFT被广泛用于气态分子-离子反应动力学研究:测量反应速率常数和产物离子分布。1996年,Spanel 和 Smith教授提出了一个概念:如果反应速率常数和产物离子分布已知,那么分析物的浓度能够被测量。一个简单的过程倒置,却创造了一个强大的分析工具。原理:Figure 1 SIFT-MShttp://ng1.17img.cn/bbsfiles/images/2012/10/201210301354_400319_1738834_3.jpgSIFT-MS工作的五个步骤:1. 水/空气混合气通过微波放电或者射频放电离子化,真空度大约在0.3~0.5Torr左右;2. 通过四级杆虑质器选择H3O+、NO+和O2+作为初始离子(无缝切换 10ms左右);3. 在精确控制反应条件的流动管中与分析物反应;4. 通过第二个四级杆进行全扫描或者选择离子监控;5. 粒子倍增管计数(响应时间 100ms);理论数学模型:以反应 http://ng1.17img.cn/bbsfiles/images/2012/10/201210301706_400359_1738834_3.jpg为例:反应速率方程:http://ng1.17img.cn/bbsfiles/images/2012/10/201210301707_400360_1738834_3.jpg求解得:http://ng1.17img.cn/bbsfiles/images/2012/10/201210302120_400421_1738834_3.jpg (1)其中:http://ng1.17img.cn/bbsfiles/images/2012/10/201210301723_400361_1738834_3.jpg: 0时刻离子浓度 http://ng1.17img.cn/bbsfiles/images/2012/10/201210301723_400363_1738834_3.jpg:t时刻离子浓度 http://ng1.17img.cn/bbsfiles/images/2012/10/201210301723_400364_1738834_3.jpg :反应速率常数 http://ng1.17img.cn/bbsfiles/images/2012/10/201210301726_400368_1738834_3.jpg:分析物浓度 http://ng1.17img.cn/bbsfiles/images/2012/10/201210301724_400366_1738834_3.jpg :反应时间产物离子计数P可表示为:http://ng1.17img.cn/bbsfiles/images/2012/10/201210301727_400372_1738834_3.jpg (2)除以方程(1)得:http://ng1.17img.cn/bbsfiles/images/2012/10/201210301728_400374_1738834_3.jpg (3)考虑到http://ng1.17img.cn/bbsfiles/images/2012/10/201210301726_400369_1738834_3.jpg(痕量气体分析),方程(3)简化为http://ng1.17img.cn/bbsfiles/images/2012/10/201210301728_400375_1738834_3.jpg (4)重排(4),并且考虑多种初始离子(在高湿空气中初始离子形成簇合物像H3O+•H20、H3O+•(H20)2等)和多种产物离子,及不同初始离子和产品离子对的扩散系数http://ng1.17img.cn/bbsfiles/images/2012/10/201210301732_400382_1738834_3.jpg,分析物的浓度为:http://ng1.17img.cn/bbsfiles/images/2012/10/201210301728_400376_1738834_3.jpg (5)其中http://ng1.17img.cn/bbsfiles/images/2012/10/201210301730_400377_1738834_3.jpg:分析物浓度(个分子/cm3)http://ng1.17img.cn/bbsfiles/images/2012/10/201210301731_400378_1738834_3.jpg=http://ng1.17img.cn/bbsfiles/images/2012/10/201210301746_400397_1738834_3.jpg =反应时间http://ng1.17img.cn/bbsfiles/images/2012/10/201210301731_400379_1738834_3.jpg= 初始离子计数(cps)http:/
二级质谱如何选择母离子?
[color=#444444]我想请教下各位大侠,离子液体(相当于盐类化合物)要打质谱的话,模式是如何选择的?。。。ESI源的话,正负离子模式是不是都要做的?其中正离子模式下,ESI+会出现+峰,而负离子模式下,ESI-会出现-峰,且两者互不干扰?。。。这只是我的猜测,请问是不是这样的呢,ESI+和ESI-都要打的呢?[/color]
现在正在做多肽的离子交换分离(SCX),请教大家,怎样选择流动相的PH值,以及盐的浓度怎么选择?还有推荐下离子交换色谱的相关书籍',谢谢!
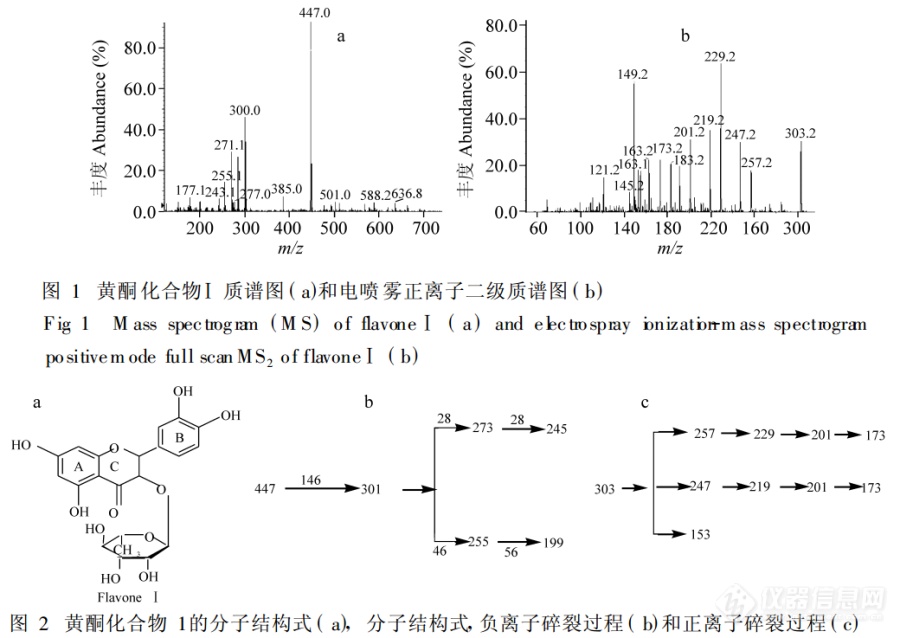
作者用的是AB公司的QTRAP质谱,esi负离子模式,一级质谱中=447,且一级质谱中的碎片并未显示303碎片强度高,但是二级质谱却选择的303作为母离子,这是为什么呢?谢谢大家![img=,690,489]https://ng1.17img.cn/bbsfiles/images/2019/10/201910181431235619_2340_1618372_3.png!w690x489.jpg[/img]
请问各位专家,用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱分析农药残留做定性定量分析时,怎么选择定性和定量离子?依据是什么?谁能分享一下相关的资料!谢谢!
摘自《色谱联用技术》,汪正范等编著,化学工业出版社,2001。 包括接口的选择(ESI与APCI的比较)、正、负离子模式的选择、流动相和流量的选择、温度的选择、系统背景的消除、柱后补偿技术等。 文件在二楼。 觉得此书不错,列了他的目录,如有需要我可以拷贝后贴上来。(列出大半本书的目录,还有和[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LCMS[/color][/url]联系不大,就不贴了,识别效果差,懒得再修改了)第一章 绪论 第一节 色谱联用技术概况 —、色谱联用的目的 二、色沿联用中的“接口 三、常用色谱联甩技术 第二节 质谱简介 一、质谱仪器 (一)真空系统 (二)进佯系统 (三)离子源 (四)质量分析器 (五)检测器 (六)计算机系统 二、质谱潜图解析第三节 傅里叶变换红外光谱简介 一、博里昨变换红外光谱仪器 二、红外光谱诺图解析 (一)红外光谱的产生(二)红外光谱中的几种振动形式及其表示符号(三)红外光浴谙图解析的—般程序第四节 原子光谱简介 一、原子光谱的产生及应用 二、原于吸收光谱仪 (一)基本结构和工作原理 (二)主要部件 三、原子发射光谱仪 (一)基本结构祁工作原理 (二)主要部件 四、原子荧光光谱仪 (一)基本结构与工作原理 (二)主要部件参考文献第五章 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]质诺联用 第一节 [url=https://insevent.instrument.com.cn/t/Mp]气相[/url]色洛—质谱联用仪器系统 一、[url=https://insevent.instrument.com.cn/t/Mp]gc[/url]—MS系统的组成 二、[url=https://insevent.instrument.com.cn/t/Mp]gc[/url]-Ms联用中主要的技术问题 三、CC—MS联用仪和[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]的主要区别 四、[url=https://insevent.instrument.com.cn/t/Mp]gc[/url]—Ms联用仪器的分类 五、一些主要的国外[url=https://insevent.instrument.com.cn/t/Mp]gc[/url]—Ms联用仪产品简介第二节 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱联用的接口技术 一、[url=https://insevent.instrument.com.cn/t/Mp]gc[/url]—Ms联用接口技术评介 二、目前常用的[url=https://insevent.instrument.com.cn/t/Mp]gc[/url]—Ms接口 第三节 [url=https://insevent.instrument.com.cn/t/Mp]气相[/url]色诺质谙联用中常用的衍生方法 —、一般介绍 二、硅烷化衍生化 (一)衍生比试剂 (二)硅烷化衍生比方法 三、酰化衍生化 四、烷基化衍生化第四节 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]—质谱联用质谱图库和计算机检索 一、常用的质谱谱库 二、NIST/EPA/NIH库及其检索简介 三、使用语库检索时应注意的问题 四、互联网上有关[url=https://insevent.instrument.com.cn/t/Mp]gc[/url]—MS和MS的信息资源第五节 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]质诺联用技术的应用 一、况Ms检测环境样品中的::曙英 二、[url=https://insevent.instrument.com.cn/t/Mp]gc[/url]—Ms在兴奋剂检测中的应用 三、[url=https://insevent.instrument.com.cn/t/Mp]gc[/url]“Ms—M5区分空间异构体 四、常用于[url=https://insevent.instrument.com.cn/t/Mp]gc[/url]Ms检测提高信噪比的方法 五、[url=https://insevent.instrument.com.cn/t/Mp]gc[/url] Ms(ToF)的应用 参考文献 第三章 液相色谱—质谱联用 第一节 液相色谱质谱联用的接口 一、直接液体导入接口 二、移动带技术 三、热喷雾接口 四、粒子束接口 五、快原子轰击 六、激光解吸离子化相墓质辅助激光解吸高于化 七、电喷雾电离 八.多种电喷雾接口技术及相应的术语 九、LL—MS商品仪器简介 第二节 电喷雾电离和大气压化学电离接口与质谱联机 一、电喷雾电离接口的结构与工作原理 二、接口的碰撞诱导解离(cID)功能 三、多电衍离子的产生与大分子分子量计算 四、AKl接口的结构及工作原理 五、样品导入方式 六、流动相化学 七、联机的流量匹配和参数优化 第三节 ESI相APCI的离子化机制 一、E5I的离子化机制 二、APCIN离子化机制 第四节 碰撞诱导解离质谱及其解释 一、电子轰击碎片化与碰撞诱导解离的区别 二、(M十H)+和其他分子加成物的CID碎片 三、碰撞诱导解离的效率 四.碰撞诱导解离质谱的解释 第五节 LC—Ms分析条件的选择与优化 一、接口的选择 二、正、负离子模式的选择 三、流动相和流量的选择 四、湿度的选择五、系统背景的消除 六、校后补偿技术第六节 样品制备第七节 LC—Ms技术的应用 一、小分子化合物 (一)药物及其代谢物的分析 (二)首草活性成分甘草酸的 (三)胃波中外甲基亚硝基腮的团二、大分子化古物(一)利用多置电荷离子洲定肪类t蛋白质大分子的分(二)多电荷离于用于蛋白质醒诱导构象变化的观察 (三)蛋白质的一级结构测定 (四)分子生物学与Lc—Ms 三、比—Ms定量分析的评价 (一)置现性和线性范围 (二)分析实例:辛伐他汀的定量第八节 毛细管电泳—质谱联用技术及应用 一、毛纫管电泳和质潜联用的接口 二、毛细管电泳和质潜联用时应注意的问题 三、毛纲管电泳和质谱联用技术的应用 参考文献
[color=#444444]仪器:岛津液相连接ABSCIEX的三重四极杆质谱[/color][color=#444444]柱子:CarboPac PA1阴离子交换柱[/color][color=#444444]待测物质:levoglucosan 左旋葡聚糖[/color][color=#444444]该物质在HPAEC-PAD上能顺利测出,用NaOH做淋洗液 (pH在10.5至12之间都可以)[/color][color=#444444]现在用MS/MS,因NaOH的盐效应对离子化有很大影响,且容易结晶析出污染MS端[/color][color=#444444]请问流动相可以换成氨水吗?氨水对离子化的抑制作用如何消除?[/color]
Q:在做[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]测定生物样品时,若选择M+H峰可在流动相中加入一些添加剂提供H离子,如甲酸等,一般准分子离子峰较稳定。有人认为用M+Na峰时离子不稳定,大家认为选M+Na峰时是不是也应该在流动相中添加一些钠离子,如甲酸钠,醋酸钠等来增加稳定性?战友们有没有选用过M+Na来测定某种药物在组织或血浆中的浓度,大家讨论一下吧!A1:绝对不能用在做[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]的流动相系统中加甲酸钠或醋酸钠。因为无论你使用ESI还是APCI源,这样的盐类都不能挥发,结果很可能是堵住离子源后方的加热毛细管,这时问题就很严重了。 我不大清AB,Agilent的公司的质谱仪对于不挥发性的盐的耐受能力如何,但是就我们实验室的几台Finnigan公司的质谱仪情况来看,无论是离子阱质谱仪还是三重四极杆的质谱仪,都不能在流动相系统中加入不挥发性的盐类。如果实在是必须在流动相中加缓冲盐以调节峰形,我使用的唯一的缓冲盐就是可以挥发的醋酸铵,而且浓度也严格控制在10 mM以下。即便这样,晚上作完实验打开仪器的离子源也还是发现在离子源里有层白色的膜。 总之,对于[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url],能不用盐就尽量不要用缓冲盐了。若做的药物对于正离子响应好,一般采用甲醇-水-甲酸系统或乙腈-水-甲酸系统就完全可以搞定;若做的药物对于负离子响应好,一般采用甲醇-水-氨水系统或乙腈-水-氨水系统也完全可以搞定。 从我的经验来看,M+Na峰离子确实不稳定,对M+Na峰进行二级全扫描质谱分析,几乎不可能得到稳定的二级碎片离子。M+Na峰和M+NH4峰的情况是类似的。我做过大约30个药物的体内样品[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]-MS定量分析,约有10%的药物出现M+Na峰或M+NH4峰,我从来不用它们做定量分析的离子。我认为很难做好。 关于药物产生M+Na峰和M+NH4峰的情况,我曾咨询过一些高手,包括我的老板,他们的观点是:药物产生M+Na峰或M+NH4峰,属药物本身的性质所决定,主要与该药物的碱性有关,一般情况下,碱性稍弱的药物易于产生M+Na峰或M+NH4峰。 据我所知,醋酸钠是不挥发性的 做酰胺药物,正负离子都会有质谱响应,我建议你试一试负离子 在流动相中加一点氨水吧,比例是0.1-0.5%的5%的氨水。不要用太高了,否则废柱子。 不过一般还是正离子好做,至少对于Finnigan的质谱是这样。 不知道你是否试过在离子源内加上一点源内CID电压,有时可能会收到异想不到的效果。A2:一般认为,由于化合物中O、S、N原子还有未配对的孤对电子,而Na离子有没有电子的空轨道,所以O、S、N特别容易捕获Na离子而形成带电粒子,而但样品还有多个O、S、N的时候,形成+Na峰的几率增加,+H峰的比例逐渐减少甚至消失;在[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]分析中,由于基质中含有钠、钾、铵等,可以加成到药物分子中,也可以不加成到药物分子中而占据液滴表面,从而抑制分析物离子的信号,这就使其信号出现很大的波动;因此不建议使用这种加成的监测离子。
在建立药物残留方法的时候,我们都是要用标准品溶液首先优化药物的质谱条件的,那这个时候流动相是如何选择的,Thermo的操作规程是要求使用50%甲醇50%水作为带动流动相,将蠕动泵注入的标准溶液带入质谱内,但我想也不至于是硬性规定吧,也不知道是否有依据。我做试验药物响应还可以,也是运气好啊,可是其他人做的药物按照这样做响应却很低,即使浓度配的很高,但是怎么调正离子模式响应也达不到e7,那遇到这样的问题应该如何去解决呢,按照这样优化,系统的压力不能高于多少。我想是不能太高的,不然药物很难被带入,是不是有硬性规定呢。其他厂家进行质谱优化的时候是不是也用的三通呢,AB的好像不是的,直接用蠕动泵打进去的,那还有其他的呢,比如Agilent,Waters,岛津的等等。有没有版友用过这些的,有什么体会,具体的操作是怎样的,能否详加列入。
理论上[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]禁止使用任何不挥发性的缓冲盐,如果需要尽量使用诸如乙酸氨等挥发性盐,浓度不要超过20mmol/l。对于不挥发性的缓冲盐,如果你的仪器有吹扫捕集的话也可使用,但一定要小心。万不得已也不要用,首先有不挥发盐是得不到好的离子流的,其次盐留在质谱中很难除掉,除非停机清洗,不然一直会影响其他样品的分析。可以找质谱友好的条件来做[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]联机,例如色谱条件为20mM磷酸盐的水/乙腈流动相,做[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]联机的时候就可以用醋酸铵代替,然后用醋酸调节pH值与磷酸盐的一致即可。除了难挥发的盐,三乙胺、表面活性剂、还有高浓度(0.5%)的TFA,都对质谱不好,[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]的流动相中应该避免。质谱的基线其实跟液相的紫外检测器和荧光检测器一样,基线高的原因不外乎内部和外部的原因。你选择的流动相在质谱的响应比较高,比如水相比较多的时候,噪音比较大些;还有如果盐含量比较大的时候,噪音更大些。检测器的灵敏度越高的时候,噪音应该越高。如果质谱的污染比较严重时,基线肯定比较高。比如离子阱检测器,用得久了,阱中的离子就会增多,一方面降低了质谱的灵敏度,另一方面增加了基线噪音。质谱的基线很多时候还跟你选择的离子宽度有关。比如你作选择离子扫描的时候,基线就低些。你作选择反应扫描的时候,离子宽度不要选得太宽,太宽噪音就高些。多级质谱一般做二级或三级质谱,基线噪音就低很多。
今天清洗离子源时,把离子传输管也拿出清洗了,这个传输管区别于ab家质谱仪的Qjet传输管,不太明白为什么赛默飞的离子传输管不需要卸真空就可以取出来清洗,麻烦各位老师指点
[b]用液相色谱质谱仪检测葡萄糖是用正离子模式还是负离子模式?[/b]这个选择有什么讲究?对流动相有什么要求?
最近做质谱发现流动相对质谱的结果有影响。比如之前用乙腈水做流动相,有一个化合物的分子离子峰就出不来,出的是一半分子量,但把乙腈换成甲醇就可以出。还有另一个化合物,同样用乙腈水体系,用20%乙腈起步的梯度,分子离子峰就出不来,出的都是碎片,但是换成60%乙腈起步的梯度,分子离子峰就出。都是同一样品前后进样,质谱条件参数都没变,为什么会这样?有没有高手能解释一下,谢谢。我猜测是不是质子性溶剂和非质子性溶剂的原因?
关于质谱图中的定量离子与定性离子的确定方法:定量离子是不是以质谱图中最高的相对离子强度为定量离子,定性离子的选择则以特征离子的丰度比为选择依据啊,我是初学者,多谢指教
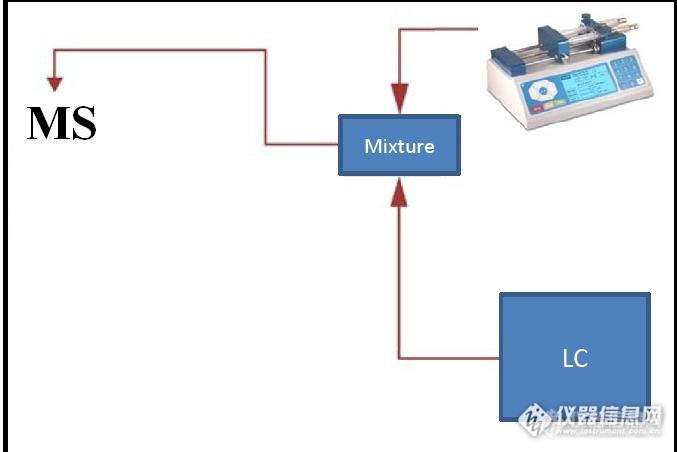
近期在摸索黄曲霉毒素的液质分析条件,纯溶剂(水:乙腈=90:10)条件下,4种毒素B1/B2/G1/G2的定量限只能做到0.1-0.2ppb和另一家的TQ相比,灵敏度差了至少1个数量级以上,于是怀疑参数没有优化到最好,开始重新优化参数。质谱参数如锥孔电压、碰撞能量等重新优化后和原先差不多,雾化气、去溶剂气和反吹气参数也大致相同,主要调节了离子源的三维位置,如图所示。http://ng1.17img.cn/bbsfiles/images/2013/09/201309032005_462039_1970765_3.jpg我是用T通流动注射方式来优化的,如下图所示。http://ng1.17img.cn/bbsfiles/images/2013/09/201309032005_462041_1970765_3.jpg注射泵进的是黄曲霉毒素单标(10uL/min),LC进的是流动相(水:甲醇+乙腈(1:1)=45:55,流速0.29mL/min),这样来模拟一个真实进样环境,监控分析物的定量离子对的MRM响应,从而优化得到最佳的离子源位置。从Orifice孔的轴线方向看,当把探头(Probe)越往里移动时,质谱响应越高,直到探头移不动为止,响应比最开始增加了3倍以上然后又调节了Probe出口的喷雾针伸出长度,刚开始固定在伸出套管2mm左右,后来尝试着增大伸出长度,发现响应越来越高,在最佳灵敏度时目测了下大概伸出长度有7-8mm。通过优化离子源位置,发现质谱响应比没优化前高了5倍左右,于是非常开心的拿了配好的混标(10ppb)进样,结果一进样发现基线噪音有1.0e4cps,四种毒素都没有出峰,难不成离子源位置太靠里,造成分析物响应升高的同时,基线噪音也随之增加,可是用T通流动注射优化时,也分辨不出来啊。各位,你们对这个情况是怎么看的呢?顺便问下论坛里做过黄曲霉毒素的筒子,你们仪器的定量限大概在什么范围?
问下质谱sim选择离子扫描模式怎么设置时间,驻留时间这些,需要对辅助定量离子绘图吗我这样设置后好像只出了最后一组的峰,图中三个大峰都是最后一组的[img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107241622009775_4336_5293607_3.png[/img][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107241622011381_1955_5293607_3.png[/img][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107241622012648_1084_5293607_3.png[/img][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107241622015842_7348_5293607_3.png[/img]
想问一下各位大神 总离子流图怎么看呢 这边是SRM模式 看离子的话只有选定的两个子离子 是全扫描看吗 但是全扫描得到的图是质荷比排列的质谱图 想看保留时间的质谱图 是在质谱方法中不选择SRM模式吗 那应该选择哪个模式呢
大家好,我们公司需要购进一台质谱,主要是用于定性,推测药物未知杂质的结构,以及推测是不是我们想要的杂质或结构。定量要求不高。分子量基本在1000以下。请问:(1)选择哪种质量分析器的质谱比较好,适用于我们的要求。(2)离子肼质谱和飞行时间质谱的主要区别在哪,用于推测未知杂质结构,哪种更合适一点(3)飞行时间质谱是不是只能得到一个母离子峰,而没有碎片离子峰,虽然能得到精确的分子式,但对于推测结构是不是信息量少了点。(4)如果定性,单四极杆能不能满足我们的要求。希望得到各位专家和同仁的指点,谢谢,不胜感激。
我之前定量没有用同位素内标,保留时间也能分开。最近看到关于质谱定量内标选择的内容,认为同位素内标好,能校正基质效应,色谱行为和响应特征接近,即便没有合适的同位素内标,也要选择结构类似的,色谱行为接近的。但是如果液相分不开一起进质谱的话,会不会产生离子抑制?
[color=#444444]我用的是thermo LCQ DECA xp plus (ion trap), 最近刚重启仪器,进 表样调谐时发现,有之前用过的人的目标物离子,而且很高。所以就清理了下离子源, 之后问题依旧。[/color][color=#444444]于是全面诊断了下,在最后的API source那里说 failed.[/color][color=#444444]当把ion transfer capillary 堵上,做scan,没有质谱图;[/color][color=#444444]把ion transfer capillary 打开但不进任何流动相或表样时,做scan也没有质谱图;[/color][color=#444444]只有当用注射器打甲醇或者通流动相时,做scan才会显示质谱,base peak 还是以前人的目标离子峰。[/color][color=#444444]请问高手们,这是怎么回事啊?[/color][color=#444444]是哪里出了问题?[/color]
以ESI正离子为例,通常产生的M+H正离子的H源是流动相中带来的吗,如果是的话,那么以非质子性纯有机相做流动相是否无法让待测样品离子化,质谱也就没有信号。恳请大佬解惑。
如题,用选择性离子扫描时,质谱的定性和定量峰是如何选择的?分子离子峰可用做什么?谢谢,新手求助!
兄弟姐妹们,求助一篇文献:利用液相色谱/三重串联四极杆质谱多反应监测优化离子选择评估油橄榄类保健品
[size=18px]目前在用AB的[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]测三苯基氯甲烷,Q1 MI模式扫243.1的离子[font=-apple-system, BlinkMacSystemFont, &](应该是三苯甲基碳正离子)[/font],发现基线非常高(30万-50万之间),且不稳定,时高时低,导致峰面积也 不稳定,打电话问客服,几个人几种说法,“液相部分污染了”“这个是正常现象,多走走就稳定了”,尝试用MRM模式去做,打出一个165.2的碎片,基线不到1000,做了线性和回收也都挺好,但是,这个碎片离子是怎么打出来的比较困惑,就怕以后再做的时候重现不出来……[/size][size=18px]流动相是90%甲醇,溶剂是正丁醇:乙腈(80:20)[/size][size=18px]请教一下各位大神,AB的仪器用SIM模式选择Q1 MI还是Q3 MI好呢?基线高且时高时低,除了污染还有什么原因呢?[font=-apple-system, BlinkMacSystemFont, &]三苯甲基碳正离子在质谱里能被打碎吗?会裂解成什么碎片离子?[/font][/size][size=18px][font=-apple-system, BlinkMacSystemFont, &][/font][/size]
是这样的,质谱例如乙苯的定量离子是91/106,那么我看质谱图的时候发现它的碎片是91.1/106.1,再进一针发现它的碎片是91/106,在做线的时候选择的定量离子是91.1/106.1,这样是对于91/106是可以正常定量的吗,会对结果有什么影响吗,例如定不了量之类的,感谢老师??
质谱分析的前提就是离子,而样品的离子体形成,就决定了仪器离子源的构造,本期主题:质谱的离子体形成讨论内容:1、ICPMS离子体的形成过程2、GCMS离子体的形成过程3、LCMS离子体的形成过程4、3种质谱离子体的形成有啥主要区别?还是过程有区别,最终目的一致?5、各种仪器对离子体形成都有哪些构造呢?筒子们,赶快参与吧,让新手也好对质谱有个全面了解~~~==========质=谱=比=较=帖=子=汇总==========1、无机质谱与有机质谱的离子体形成区别http://bbs.instrument.com.cn/shtml/20120503/4012287/2、气质与液质的离子源区别http://bbs.instrument.com.cn/shtml/20120505/4016562/3、ICPMS、GCMS、LCMS气体的选择与使用http://bbs.instrument.com.cn/shtml/20120507/4019049/4、质谱的进样方式与进样接口的区别http://bbs.instrument.com.cn/shtml/20120510/4025193/5、质谱质量分析器的类型、区别及特点http://bbs.instrument.com.cn/shtml/20120519/4042099/6、高分辨质谱与低分辨质谱的区别http://bbs.instrument.com.cn/shtml/20120525/4053208/
请问大家做用离子阱电雾质谱做二级裂解的时候,isolation width都设置为多少啊,这个有什么影响?我的化合物做一级质谱的时候强度还可以,但是选择做二级质谱的时候就不怎么稳定了,这是怎么回事哦,谢谢帮忙
今天做液质时,某个项目采用甲酸胺(pH5.0)和乙腈作为流动相,结果质谱离子图中,众多峰中均有一个307的峰,而且在很多的峰中响应是最强的!看了下,基线中其它的噪音峰的质谱图,也发现均有307这个峰,响应也基本上是最强的,而且与其它噪音峰差很大。个人将这个分子量与常见的背景离子峰对比了一下,没有发现有这个,可有人遇到过或知道否?谢谢
质谱图中碎片离子为何表观是棒图,而实际是峰形,比如在计算分辨率的时候,谢谢