关键词:单细胞凝胶电泳目的:为便于各室单细胞凝胶电泳试验结果的可比性背景知识:略原理:在细胞核中,DNA是环状附着在核基质上,细胞裂解过程中,核基质被溶解、抽提,DNA的结构则未发生变化。如果DNA链上存在缺口,则使DNA超螺旋变的松弛,DNA环向外展,同时由于暴露了阴电荷,在电场力的作用下,松动的DNA环向阳极迁移,但是由于这种松动的DNA环一端仍附着于核DNA,其迁移距离受到限制,因此尾长并不总是真实反映链缺口的多少。实际应当依靠尾长与尾部的荧光强度同时来进行分析。主体内容:操作步骤见下文主要参考文献:略操作步骤:1. 分离制备单细胞悬液:(1) 体外培养的细胞株:用胰酶消化,吹打成单细胞悬液(2) 体内脏器细胞:处死动物,取出脏器,于Hanks’液中制备成单个细胞悬液。2. 胶板制备:(1) 取20~50μl于56℃水浴中保温的0.5%普通熔点琼脂糖,铺于磨沙载玻片上,形成底胶。(2) 取100~150μl 0.5%普通熔点琼脂糖加在底胶上,再于其上加盖玻片,4℃冷凝10分钟。(3) 取下盖片,取50~100μl于37℃水浴中保温的1.0%的低熔点琼脂糖与50~100μl细胞悬液(105个细胞/ml)混匀,立即铺片,加上盖玻片,4℃冷凝10分钟。(4) 去掉盖玻片,取70~100μl于37℃水浴中保温的0.5%的低熔点琼脂糖铺片,加盖玻片,4℃冷凝。3. 细胞裂解与电泳:(1) 将制备好的胶板去掉盖玻片后,浸于4℃预冷的细胞裂解液中,4℃裂解1小时。(2) 取出胶板,放入电泳槽中,浸泡在电泳液中解旋20分钟。(3) 4℃电泳20分钟(25V,300mA)。4. 中和与染色:(1) 电泳结束,将胶板浸泡于中和液中,每次15分钟,共中和两次,注意更换中和液。(2) 取出胶板,置于染色架上,滴加5μg/ml的PI,暗处染色20分钟。(3) 蒸馏水脱色15分钟。5. 镜检和分析:(1) 在荧光显微镜下观察,绿光激发吸收滤片590nm。必要时照相记录。(2) 记数观察的细胞,记录彗星细胞出现的频率,用目镜测微尺测头长与全长,计算核DNA迁移距离。* * * * *使用两层凝胶法,经裂解、DNA解旋、电泳和中和得到湿琼脂糖凝胶片。将湿琼脂糖凝胶片置于冰冷无水乙醇中脱水10分钟,后置于空气中自发干燥。每人制备2张琼脂糖凝胶片。全部操作在采血后8小时内完成,操作过程中注意避光。脱水干燥的琼脂糖凝胶片装于含有干燥剂的载片盒中运回实验室。使用50μl 30μM的溴乙锭溶液染色、照相。使用单细胞凝胶电泳软件分析所有照片,每人随机测量100个以上细胞的尾长和olive尾矩,以尾长和olive尾矩的算术均数代表个体DNA损伤情况。
凝胶电泳(英语:Gel electrophoresis)或称胶体电泳 是一大类技术,被科学工作者用于分离不同物理性质(如大小、形状、等电点等)的分子。凝胶电泳通常用于分析用途,但也可以作为制备技术,在采用某些方法(如质谱(MS)、聚合酶链式反应(PCR)、克隆技术、DNA测序或者免疫印迹)检测之前部分提纯分子。凝胶电泳仪 - 使用方法凝胶电泳被广泛用于分子生物学、遗传学和生物化学:1.大的DNA或者RNA分子通常利用琼脂糖凝胶电泳(agarose gel electrophoresis)分离,也可以使用聚丙烯酰胺凝胶电泳(PAGE)。2.蛋白质的凝胶电泳通常在加入十二烷基硫酸钠的聚丙烯酰胺凝胶中进行(SDS-PAGE),或者非变性凝胶电泳,或二维电泳。 SDS-PAGE 蛋白质凝胶电泳图。 3.毛细管电泳 4.酶谱法(zymography) 5.变性梯度胶凝电泳(Denaturing Gradient Gel Electrophoresis,DGGE) 琼脂糖和聚丙烯酰胺可以制成各种形状、大小和孔隙度。琼脂糖凝胶分离DNA片度大小范围较广,不同浓度琼脂糖凝胶可分离长度从200bp至近50kb的DNA片段。琼脂糖通常用水平装置在强度和方向恒定的电场下电泳。聚丙烯酰胺分离小片段DNA(5-500bp)效果较好,其分辩力极高,甚至相差1bp的DNA片段就能分开。聚丙烯酰胺凝胶电泳很快,可容纳相对大量的DNA,但制备和操作比琼脂糖凝胶困难。聚丙烯酰胺凝胶采用垂直装置进行电泳。目前,一般实验室多用琼脂糖水平平板凝胶电泳装置进行DNA电泳。 琼脂糖主要在DNA制备电泳中作为一种固体支持基质,其密度取决于琼脂糖的浓度。在电场中,在中性pH值下带负电荷的DNA向阳极迁移,其迁移速率由下列多种因素决定:1、 DNA的分子大小。度琼脂糖凝胶中的迁移速率与DNA分子量对数成反比,分子越大则所受阻力越大,也越难于在凝胶孔隙中蠕行,因而迁移得越慢。 2、 琼脂糖浓度 一个给定大小的线状DNA分子,其迁移速度在不同浓度的琼脂糖凝胶中各不相同。DNA电泳迁移率的对数与凝胶浓度成线性关系。凝胶浓度的选择取决于DNA分子的大小。分离小于0.5kb的DNA片段所需胶浓度是1.2-1.5%,分离大于10kb的DNA分子所需胶浓度为0.3-0.7%, DNA片段大小间于两者之间则所需胶浓度为0.8-1.0%。 3、 DNA分子的构象DNA分子处于不同构象时,它在电场中移动距离不仅和分子量有关,还和它本身构象有关。相同分子量的线状、开环和超螺旋DNA在琼脂糖凝胶中移动速度是不一样的,超螺旋DNA移动最快,而开环双链DNA移动最慢。如在电泳鉴定质粒纯度时发现凝胶上有数条DNA带难以确定是质粒DNA不同构象引起还是因为含有其他DNA引起时,可从琼脂糖凝胶上将DNA带逐个回收,用同一种限制性内切酶分别水解,然后电泳,如在凝胶上出现相同的DNA图谱,则为同一种DNA。
[b]凝胶水平电泳仪[/b]和[b]进口水平电泳仪[/b]非常经济的低缓冲量,非常适合超大规模样品检测或高分辨率分离实验的[b]水平电泳仪,[url=http://www.f-lab.cn/electrophoresis/me-10.html]水平凝胶电泳仪[/url][/b][url=http://www.f-lab.cn/electrophoresis/me-10.html]FP-ME-10-20[/url]专业为克隆或PCR实验而设计,适合大规模的凝胶电泳实验和超高分辨率的分离,也适合样品转移到膜层上进行进一步分析。[b]水平凝胶电泳仪[/b]特色具有三种凝胶盘尺寸:200x200mm,200x250mm和200x100mm兼容多通道[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液器[/color][/url][/color][/url]的凝胶卡可一次性使用40个样品,单个凝胶可加载440个样品电泳液冲洗消耗少兼容多道[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液器[/color][/url][/color][/url]单个铸造电泳槽安全可靠方便样品加载电泳指示功能凝胶灌胶无需夹具,弹簧[b]水平凝胶电泳仪参数[/b]体积:W395xL230xH90mm凝胶卡尺寸: W200xL200mm, W200xL100mm 最大样品:200@W200xL200mm, 450@W200xL100mm 缓冲液容积:1200ml建造:注塑铸造,耐用防漏电极:99.99%铂金电极,可更换而抗腐蚀更多凝胶电泳仪请浏览官网:[url]http://www.f-lab.cn/electrophoresis.html[/url]
凝胶电泳仪器的发展 电泳系统虽然只是作为生化分离分析所必需的常规仪器,但它的进展与其他大型仪器设备一样,同样是非常迅速的。从1809年的第一次电泳实验所用的雏型装置到1946年第一台商品自由移界电泳系统问世经历了一个多世纪。但此后的50多年电泳仪器的发展却极其迅猛,特别是电泳介质由流动相改为凝胶后,各种各样的凝胶电泳装置便层出不穷以适应各种研究工作和生产实践的需要。
第一节 概 述一. DNA的限制性内切酶酶切分析限制性内切酶能特异地结合于一段被称为限制性酶识别序列的DNA序列之内或其附近的特异位点上,并切割双链DNA。它可分为三类:Ⅰ类和Ⅲ类酶在同一蛋白质分子中兼有切割和修饰(甲基化)作用且依赖于ATP的存在。Ⅰ类酶结合于识别位点并随机的切割识别位点不远处的DNA,而Ⅲ类酶在识别位点上切割DNA分子,然后从底物上解离。Ⅱ类由两种酶组成: 一种为限制性内切核酸酶(限制酶),它切割某一特异的核苷酸序列; 另一种为独立的甲基化酶,它修饰同一识别序列。Ⅱ类中的限制性内切酶在分子克隆中得到了广泛应用,它们是重组DNA的基础。绝大多数Ⅱ类限制酶识别长度为4至6个核苷酸的回文对称特异核苷酸序列(如EcoRⅠ识别六个核苷酸序列:5'- G↓AATTC-3'),有少数酶识别更长的序列或简并序列。Ⅱ类酶切割位点在识别序列中,有的在对称轴处切割,产生平末端的DNA片段(如SmaⅠ:5'-CCC↓GGG-3');有的切割位点在对称轴一侧,产生带有单链突出末端的DNA片段称粘性未端, 如EcoRⅠ切割识别序列后产生两个互补的粘性末端。5'…G↓AATTC…3' →5'… G AATTC…3'3'…CTTAA↑G …5' →3'… CTTAA G…5'DNA纯度、缓冲液、温度条件及限制性内切酶本身都会影响限制性内切酶的活性。大部分限制性内切酶不受RNA或单链DNA的影响。当微量的污染物进入限制性内切酶贮存液中时,会影响其进一步使用,因此在吸取限制性内切酶时,每次都要用新的吸管头。如果采用两种限制性内切酶,必须要注意分别提供各自的最适盐浓度。若两者可用同一缓冲液,则可同时水解。若需要不同的盐浓度,则低盐浓度的限制性内切酶必须首先使用,随后调节盐浓度,再用高盐浓度的限制性内切酶水解。也可在第一个酶切反应完成后,用等体积酚/氯仿抽提,加0.1倍体积3mol/L NaAc和2倍体积无水乙醇,混匀后置-70℃低温冰箱30分钟,离心、干燥并重新溶于缓冲液后进行第二个酶切反应。DNA限制性内切酶酶切图谱又称DNA的物理图谱,它由一系列位置确定的多种限制性内切酶酶切位点组成,以直线或环状图式表示。在DNA序列分析、基因组的功能图谱绘制、DNA的无性繁殖、基因文库的构建等工作中,建立限制性内切酶图谱都是不可缺少的环节,近年来发展起来的RFLP(限制性片段长度多态性)技术更是建立在它的基础上。构建DNA限制性内切酶图谱有许多方法。通常结合使用多种限制性内切酶,通过综合分析多种酶单切及不同组合的多种酶同时切所得到的限制性片段大小来确定各种酶的酶切位点及其相对位置。酶切图谱的使用价值依赖于它的准确性和精确程度。在酶切图谱制作过程中,为了获得条带清晰的电泳图谱,一般DNA用量约为0.5-1μg。限制性内切酶的酶解反应最适条件各不相同,各种酶有其相应的酶切缓冲液和最适反应温度(大多数为37℃)。对质粒DNA酶切反应而言, 限制性内切酶用量可按标准体系1μg DNA加1单位酶,消化1-2小时。但要完全酶解则必须增加酶的用量,一般增加2-3倍,甚至更多,反应时间也要适当延长。二. 凝胶电泳琼脂糖或聚丙烯酰胺凝胶电泳是分离鉴定和纯化DNA片段的标准方法。该技术操作简便快速,可以分辨用其它方法(如密度梯度离心法)所无法分离的DNA片段。当用低浓度的荧光嵌入染料溴化乙啶(Ethidium bromide, EB)染色,在紫外光下至少可以检出1-10ng的DNA条带,从而可以确定DNA片段在凝胶中的位置。此外,还可以从电泳后的凝胶中回收特定的DNA条带,用于以后的克隆操作。琼脂糖和聚丙烯酰胺可以制成各种形状、大小和孔隙度。琼脂糖凝胶分离DNA片度大小范围较广,不同浓度琼脂糖凝胶可分离长度从200bp至近50kb的DNA片段。琼脂糖通常用水平装置在强度和方向恒定的电场下电泳。聚丙烯酰胺分离小片段DNA(5-500bp)效果较好,其分辩力极高,甚至相差1bp的DNA片段就能分开。聚丙烯酰胺凝胶电泳很快,可容纳相对大量的DNA,但制备和操作比琼脂糖凝胶困难。聚丙烯酰胺凝胶采用垂直装置进行电泳。目前,一般实验室多用琼脂糖水平平板凝胶电泳装置进行DNA电泳。琼脂糖主要在DNA制备电泳中作为一种固体支持基质,其密度取决于琼脂糖的浓度。在电场中,在中性pH值下带负电荷的DNA向阳极迁移,其迁移速率由下列多种因素决定:1、DNA的分子大小:线状双链DNA分子在一定浓度琼脂糖凝胶中的迁移速率与DNA分子量对数成反比,分子越大则所受阻力越大,也越难于在凝胶孔隙中蠕行,因而迁移得越慢。2、琼脂糖浓度一个给定大小的线状DNA分子,其迁移速度在不同浓度的琼脂糖凝胶中各不相同。DNA电泳迁移率的对数与凝胶浓度成线性关系。凝胶浓度的选择取决于DNA分子的大小。分离小于0.5kb的DNA片段所需胶浓度是1.2-1.5%,分离大于10kb的DNA分子所需胶浓度为0.3-0.7%, DNA片段大小间于两者之间则所需胶浓度为0.8-1.0%。
有做PFGE脉冲场凝胶电泳实验的没,提供些材料。尤其是和领导建设性建议方面的。
请问:国产和进口变性梯度凝胶电泳一般都在什么价位。比较好的品牌有那几个,谢谢!
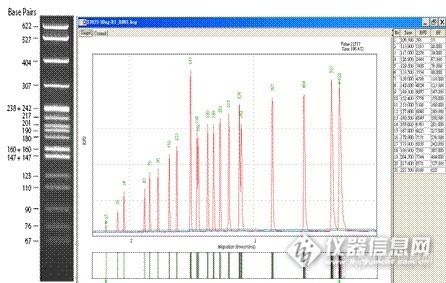
毛细管电泳技术(Capillary Electrophoresis, CE)又称高效毛细管电泳(HPCE)或毛细管分离法(CESM),是一类以毛细管为分离通道、以高压直流电场为驱动力,根据样品中各组分之间迁移速度和分配行为上的差异而实现分离的一类液相分离技术,迅速发展于80年代中后期,它实际上包含电泳技术和色谱技术及其交叉内容,是分析科学中继高效液相色谱之后的又一重大进展。http://ng1.17img.cn/bbsfiles/images/2013/08/201308081111_456810_2646159_3.jpg1987年,Cohen发表了毛细管凝胶电泳的工作。当电泳从凝胶板上移到毛细管中以后,发生了奇迹般的变化:分析灵敏度提高到能检测一个碱基的变化,分离效率达百万理论塔板数;分析片段能大能小,小到分辨单个核苷酸的序列,大到分离Mb的DNA;分析时间由原来的以小时计算缩减到以分、秒计算。CE可以说是经典电泳技术与现代微柱分离技术完美结合的产物。 一.毛细管凝胶电泳的原理 不同分子所带电荷性质、多少不同,形状、大小各异。一定电解质及PH的缓冲液或其它溶液内,受电场作用,样本中各组分按一定速度迁移,从而形成电泳。电泳迁移速度(v)可用下式表示:v=uE其中E为电场强度(E=V/L,V为电压,L为毛细管总长度)。u为电泳淌度。毛细管凝胶电泳是将板上的凝胶移到毛细管中作支持物进行的电泳。凝胶具有多孔性,起类似分子筛的作用, 溶质按分子大小逐一分离。凝胶粘度大, 能减少溶质的扩散, 所得峰形尖锐, 能达到CE中最高的柱效。电流通过导体时产生焦耳热。传统平板凝胶电泳的最大局限性在于其无法克服两端高电压带来的焦耳热所产生的负面影响。焦耳热可使筛分介质内部出现温度、粘度及分离速度的不均一,影响迁移、降低效率、使区带变宽。由于这种负面影响与电场强度成正比,所以极大地限制了高电压的引入。也难以提高电泳速度。毛细管电泳使样品在一根极细的柱子中进行分离。细柱可减小电流,使焦耳热的产生减少;同时又增大了散热面积,提高散热效率,大大降低了管中心与管壁间的温差,减少了柱子径向上的各种梯度差,保证了高效分离。因此可以加大电场强度,达到100~200V/cm,全面提高分离质量。在进行分析时将毛细管内充满了凝胶,毛细管两端通高压电,使凝胶内带电分子移到毛细管相反电荷的一端。因为不同分子的大小对电荷比不同,就以不同的速率在管中移动,达到毛细管终点也有快有慢。毛细管电泳即依此探测、分离不同分子。 二.毛细管凝胶电泳的特点 1.所需样品量少、仪器简单、操作简便。2.分析速度快,分离效率高,分辨率高,灵敏度高。3.无需核酸染料,安全无毒。4.无需制胶,省时省力。5.无需照胶,杜绝人工分析结果误差。6.自动出结果,包括片段大小和样品浓度,软件可输出电泳峰图、凝胶电泳图、DNA片段碱基差异分析、相对定量分析。http://ng1.17img.cn/bbsfiles/images/2013/08/201308081111_456811_2646159_3.jpg三.毛细管凝胶电泳的应用1.PCR条件的优化及多重PCR的检测2.高分辨率的检出,相差1-4bp的DNA片段的差异,及相同长度不同序列的差异3.动态检测酶切体系的进程4.评估基因组DNA质量高低5.HLA分型6.STR分析7.质粒的纯度分析8.DNA/DNA杂交9.DNA/蛋白互作
由于实验需要现准备购置一台二维凝胶电泳仪,价格适中最好,希望各位大侠帮忙推荐!先谢了![em23]
脉冲场凝胶电泳1)高分子量DNA琼脂糖凝胶块制备和加工1.收集10ml全血,加入30ml细胞裂解液。置冰浴中至少20min直至红细胞完全溶解。2.2000r/min离心10min,移去红色上清液,再次用细胞裂解液洗涤细胞,然后用PBS重悬细胞。3.稀释单细胞悬液并取一小份用Neubauer腔计数细胞。4.用PBS重悬细胞,以达到40μl PBS中含1百万个细胞比例(1百万个二倍体哺乳动物大约含有基因组DNA 10μg)5.用PBS配制2%浓度低熔点琼脂糖溶液并保持在50℃。6.将等体积(各1ml)细胞悬液与琼脂糖溶液于室温下混匀,立即倒入凝胶块模具中。7.静置20min让琼脂糖固化,用无菌塑料杯(通常用作划菌)将凝胶块自模具中取出并置入蛋白酶缓冲液中,加入2mg/ml的蛋白酶K。8.将带有凝胶块的蛋白酶K缓冲液于50℃保持2~3天。每个盛有50ml蛋白酶缓冲液的Falcon管可容纳多达100个凝胶块。9.蛋白酶K消化后,可将凝胶块保留在此缓冲液或0.5mol/L EDTA溶液中保存于4℃。10. 此外,继续将凝胶块用高压消毒过的TE缓冲液冲洗数遍的步骤。11. 将凝胶块放入装有TE及0.04mg/ml PMSF溶液的Falcon试管中,灭活残留的蛋白酶K。12. 室温下用TE溶液漂洗凝胶块数次,将凝胶块放入另一干净的试管,可直接用于酶切反应或用0.5mol/L EDTA,(pH8.0)4℃保存凝胶块。13. 若用EDTA保存凝胶块,取出后应用TE溶液室温下漂洗30 min×2次。2)大小标准物的制备 l λ多联体1.以TE缓冲液悬浮λ多联体(Boehringer MA宝灵曼公司产品),浓度为4μg/40μl。2.用等体积TE配制的2%低熔点琼脂糖(温度保持在45℃)混匀。3.移去混合液注入预冷的凝胶块模具中。4.室温下用TE及100 mmol/L NaCl溶液温育2天。l 酵母染色体1.从YPD(酵母提取物,蛋白胨和葡萄糖)培养基瓶皿中挑选单一克隆加入10ml YPD预培养的肉汤中,30℃下剧烈震荡生长24小时,然后加入200ml YPD肉汤,剧烈振荡24~48h(产量大约100块)。2.4000×g转速,离心10min,然后用50mmol/L EDTA/10 mmol/L Tris-HCl(pH7.5)溶液悬浮。3.仍以4000×g转速离心10min,再用SCE[1 mol/L 山梨醇,0.1mol/L枸椽酸钠,pH5.8及10 mmol/L EDTA (pH7.5)]溶液重悬。4.取稀释后的细胞悬液用Neubauer腔计数。5.溶液短暂离心后,再用SCE重悬细胞,使40μl SCE溶液中含5×107个细胞(相当于80μl体积的模块中含有5×107个细胞)。6.溶液与0.1mg/ml酵母扣糖酶100T和100mmol/Lβ-巯基乙醇混匀,37℃保温15~30min。7.细胞悬液与等体积的SCE配制的2%低熔点琼脂糖凝胶混匀,保持在50℃。8.将混合物移注入预冷的凝胶块模具中。9.凝胶块用含10 mmol/L二硫苏糖醇的SCE溶液37℃下振荡温育1~2小时。10. 将凝胶块移入蛋白酶缓冲液中,加入2mg/ml蛋白酶K,50℃温育48h。11. 用50 mmol/L EDTA/10 mmol/L Tris-HCl(pH7.5)溶液洗涤凝胶块3次,每次20min。12. 凝胶块可用此混合液于4℃保存或不用漂洗直接装载入凝胶中。3)琼脂糖凝胶块中DNA的限制性内切酶消化1.应使用消毒溶液及戴无菌手套以免DNA降解。2.在Falcon试管中用1×TE溶液漂洗凝胶块20min 3次,以去除EDTA。3.混合:酶反应缓冲液(高、中或低盐缓冲液),100 mmol/L亚精胺(只用于高盐缓冲液状态),10~20单位的内切酶。20单位的内切酶就足以过夜完全消化10μg DNA。4.设立一个除内切酶成分外含有混合物各组分的阴性对照,以检查是否有非特异性DNA降解。5.将琼脂糖凝胶块加入反应混合溶液中:通常用消毒过的手术刀或套环将凝胶块移入。6.若两种内切酶所需缓冲液条件一致,可以同时或先后用两种不同的酶进行消化(先用低盐缓冲液的酶消化,再调整盐浓度)。倘若首次消化的酶要求50℃条件,在第二个酶消化时要换缓冲液。7.若要进行部分消化,则首先在同一温度和反应时间用1:10稀释的酶进行尝试。4)凝胶电泳1.将0.8%的琼脂糖在0.25×TBE中熔化后冷却至50~60℃,立即注入凝胶框架中,并插入梳子。2.凝胶固化后小心地拔出齿梳,用2把无菌手术刀将DNA凝胶块上样。若用不同内切酶消化凝胶块,则取不同样品时应将手术刀片烧灼后冷却。将DNA大小标志物上样至凝胶的两旁。3.用1%液态低熔点琼脂糖凝胶(0.25×TBE配制)密封狭槽。4.若有气泡存在,用注射器驱赶气泡。5.一旦密封的低熔点琼脂糖已固化(大约10min),可将凝胶搁入腔室,并用电泳缓冲液覆盖过胶面。6.应设定合适的电压及转换时间(参考《分子医学技术》84页表8.1)并开始电泳。两个不同电泳方向的电流应相等。7.电泳结束后,凝胶用0.25×TBE配制成的EB(0.4μg/ml)染色。8.用泵自槽中排除缓冲液,续以双蒸水冲洗电泳槽。9.凝胶成像:DNA在曝光的过程中可能会形成缺口。10. 用0.25mol/L HCl漂洗凝胶30min,让DNA脱嘌呤,并有利于转移。11. 凝胶用碱(变性溶液中)变性20min,两次,续以中性溶液1~5min。12. 采用标准Southern印迹方案将DNA转印至尼龙膜上。一般来说,印迹PFGE凝胶的时间较普通凝胶印迹时间长(约48h)。
目前需要一批凝胶电泳的仪器设备,有资源的联系18366183623
求助于高手们: 我要用毛细管凝胶电泳检测乳制品中的蛋白质,请问我的样品和电泳缓冲溶液用什么啊?
有人做过毛细管凝胶电泳吗?凝胶毛细管柱是买的还是自己做的?能提供比较好的凝胶毛细管柱制备方法吗?
1.原理等电聚焦凝胶电泳是依据蛋白质分子的静电荷或等电点进行分离的技术,等电聚焦中,蛋白质分子在含有载体两性电解质形成的一个连续而稳定的线性pH梯度中电泳。载体两性电解质是脂肪族多氨基多羧酸,在电场中形成正极为酸性,负极为碱性的连续的pH梯度。蛋白质分子在偏离其等电点的pH条件下带有电荷,因此可以在电场中移动;当蛋白质迁移至其等电点位置时,其静电荷数为零,在电场中不再移动,据此将蛋白质分离。 等电聚焦中,只有在凝胶两端给以高电压时,才能获得较好的蛋白质条带分辨率,这就需要非常有效的凝胶冷却系统(否则会导致烧胶),即凝胶同期周围液体之间的热传递效率要高。由于平板胶热传递能力高,并可方便的同时比较多种蛋白质样品,所以平板胶用在等电聚焦上的居多。由于等电聚焦对蛋白质的电荷差异非常敏感,若要好的重复性,制备蛋白样品时一定要小心,要避免任何对蛋白质化学组成和结构的修饰。另外,蛋白质-脂类、蛋白质-蛋白质相互作用可引起电荷改变,进而导致等电点迁移或纹理现象。除非特殊需要研究蛋白质-蛋白质相互作用或者必须保持蛋白质的生物学功能,等电聚焦通常在含有尿素的变性凝胶系统中进行。使用非离子去垢剂也可以提高分辨率。 2.主要仪器、试剂仪器:微型电泳系统、电源、注射器、固定和染色用容器 试剂:丙稀酰胺、双-丙稀酰胺、载体两性电解质、尿素、过硫酸胺、TEMED、TritonX-100、2-巯基乙醇、溴酚蓝、磷酸、氢氧化钠、氯化钾、三氯乙酸、考马斯亮蓝、甲醇、乙酸。 储存液:1)30%(w/v)丙稀酰胺,1%(w/v)双-丙稀酰胺;2)20%Triton X100;3)10%三氯乙酸;4)1%三氯乙酸;5)1%溴酚蓝;6)考马斯亮蓝染色液;7)考马斯亮蓝脱色液;
脉冲场凝胶电泳以其重复性好、分辨力强而被誉为细菌分子分型技术的“金标准”。它可以用于的分子DNA的分离,其分辨范围可达10Mb。PFGE选用识别稀有酶切位点的限制性内切酶切割基因组DNA,获得的DNA大片段在外加脉冲电场的低浓度琼脂糖凝胶中分离,产生数量有限的DNA条带。其原理是DNA分子在脉冲电场中随着电泳方向的改变不断改变其分子构象,挤过凝胶间隙。小的DNA分子比大的分子重新定向快,在凝胶中移动快,从而使小分子DNA片段与大片段相分离,同时较大的DNA片段也能被有效分离,在凝胶上按染色体片段长度的不同而呈现出电泳带型。
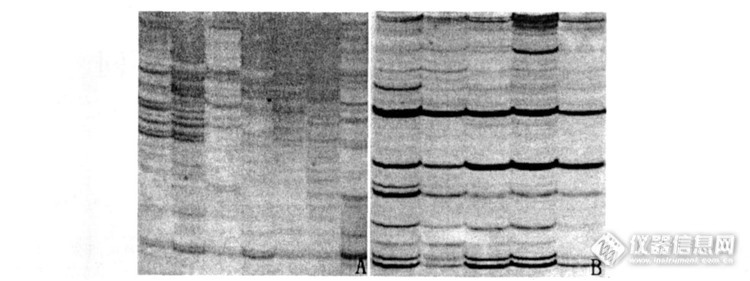
在基因克隆过程中,开发标记是一个重要过程,而在筛标记的时候,群体往往很大,聚丙烯酰胺凝胶电泳(polyacryamide gel electrophoresis,PAGE)能够适应这种大群体筛标记,帮助实验人员开发标记,因此多年来一直被广受各大实验室应用。http://simg.instrument.com.cn/bbs/images/default/em09503.gif 有关PAGE的简介已经可以从很多途径获得了,因此我把这方面的内容附在文后,主要想写的是有关PAGE的安全操作。 我曾经做过一个采访,当然不是正式的,范围仅限本实验室需进行PAGE实验操作的实验人员,问题是如果有其他选择,是否愿意来跑PAGE,为什么?98%都回答不想跑,所有女生都表示没得选择,只为毕业。听到这样的结果每个人估计会有不同的猜想了,为什么呢?http://simg.instrument.com.cn/bbs/images/default/emyc1010.gif请看下面分解。 首先,PAGE实验过程中用到的很多试剂对人体毒害很大,比如硅化剂和反硅化剂含有对呼吸道和批发有刺激作用的物质。其次,PAGE是一个长期的实验过程,长期处于一个毒性的环境中不可避免的人体会受到伤害。所以提高PAGE实验的安全意识很有必要。http://simg.instrument.com.cn/bbs/images/default/em09507.gifhttp://simg.instrument.com.cn/bbs/images/default/em09507.gifhttp://simg.instrument.com.cn/bbs/images/default/em09507.gif 1 佩戴手套,口罩。实验时用防护性好的手套,多戴几层,避免实验操作中有些不经意中划破了。普通口罩带两层,有条件的可以带防毒面具。 2 配置通风橱。进行有关有毒试剂操作时,尽量在通风橱内进行。 3 室内通风透气。实验室内空气要和外界流通,避免吸入过多有害气体。 4 及时清理垃圾,保持环境清洁。泡胶的池子要及时清理,防止有害物质滋生蔓延。 5 有毒试剂统一集中处理。类似银染液、显色液需集中收集,送至专门的有毒试剂处理处处理,不能随便倾倒,不应直接导入水池中。聚丙烯酰胺凝胶电泳给科学研究带来了不可估量的作用,既然不能避免不做实验,那我们应该提高实验安全意识,减少实验危害。附:PAGE相关知识介绍:1 原理PAGE是以聚丙烯酰胺凝胶作为支持介质,聚丙烯酰胺凝胶是丙烯酰胺单体在TEMED和过硫酸铵共同作用下聚合形成长链,长链在交联剂甲叉双丙烯酰胺在催化剂作用下形成的三维网状结构物质。2 适用范围不同大小的DNA的要配置不同浓度的胶,比如,3.5%的丙烯酰胺有效分离100-2000bp的DNA片段,这是由聚丙烯酰胺凝胶孔径大小决定的,而丙烯酰胺和交联剂的浓度和比例决定了聚丙烯酰胺凝胶孔径,因此,在制胶之前先要根据DNA片段大小选择试剂用量。PAGE分离效果强,电泳的分辨率高,适用于小DNA片段分离,是利用连续或不连续的pH梯度原理,在电泳时,样品被压缩成一条狭窄的条带,清晰可见,5-500bp的片段之间即使仅差1bp也能分开。3 步骤简介及改进聚丙烯酰胺凝胶电泳包括聚丙烯酰胺凝胶的制备、凝胶电泳、显色-银染三个大的部分,操作步骤较多,一套流程下来需要三个小时左右,比较费时费力,因此有些人在该方法做了一些改进,以求加快实验进度,提高实验效率。如利用电解质梯度变性聚丙烯酰胺凝胶电泳系统对稻纵卷叶螟取食的水稻叶片进行cDNA-AFLP分析,结果表明产生的cDNA条带比普通变性聚丙烯酰胺凝胶电泳系统大约增加30%,解决了传统的聚丙烯酰胺凝胶电泳在同一块胶板中大片段DNA条带堆积而小片段DNA条带间距过大,且读带数量有限的问题(曹蕾等,附件农林大学学报,2007)。http://ng1.17img.cn/bbsfiles/images/2015/09/201509171913_566486_3039681_3.jpgA.普通变性聚丙烯酰胺凝胶(质量分数为5%);B.电解质梯度变性聚丙烯酰胺凝胶(质量分数为5%).
有没有做过毛细管凝胶电泳的啊?怎么制备凝胶柱啊?第一次做,而且没人指导,文献里也没找到详细的方法,各位帮帮忙啊。急啊!
Difference Gel Electrophoresis (DIGE)即差异凝胶电泳是目前2D领域相当热门的一项技术,可以说它的出现消除了传统双向的一些弊端,使得好多实验室对双向重拾信心http://img.dxycdn.com/images_new/smiles/smile_tongue.gif 先简要介绍一下DIGE技术的历史和路线。DIGE技术最早在1997年由Jon Minden实验室提出,后来Amresham成为此项技术的主要推动者,其技术路线是将样品在电泳前标记Cy2、Cy3 和Cy5 这3 种荧光染料(其中Cy2 作为用Cy3、Cy5 标记的蛋白质内标, 用以比较数据库中各个胶之间的蛋白质的量的差异),然后将标记后的3 种样品混合, 同时在一块胶上进行电泳。所得到的2D 胶图像可使用3 种不同的激发P发射过滤器得到不同颜色荧光信号,根据这些信号的比例来判断样品之间蛋白质的差异,这样可避免在匹配时出现的误差,进行定量分析时也不依赖于胶与胶之间的重复性。用于标记的荧光基团在化学结构上相似,分子量也基本相同,都带有正电荷,所以在与赖氨酸残基反应时,保证了所有的样品可以移至相同的位置。该方法的灵敏度可与银染和SYPRO Ruby 相媲美,可以检测到100~200pg 的蛋白质,线形动态范围在5个数量级左右。该方法也提高了定量上的准确性。由于实验方法本身造成的蛋白质斑点强度的差异,比如样品在进入胶条时会有一些样品损失,但在同一块差异凝胶电泳胶上就不会出现这样的差异。DIGE 可在同一次检测中通过分析单一胶上的相互覆盖的信息来得到蛋白质的信息,可以同时在一块胶上在相同电泳条件下分离2~3 个样品,大大减少了一个实验需要的胶的总数。虽然从理论上来说,该方法非常诱人, 但DIGE 本身还有很多技术上的问题。主要的问题在于:1) 只有当约1 %~2 %的蛋白质的赖氨酸残基在荧光标记时修饰,才可以维持被标记的蛋白在电泳时的溶解性;2) 在DIGE 染色中丢失的蛋白质基本确定为样品中的低丰度蛋白; 3) 虽然经染色后在电荷上未发生变化,被染料标记的蛋白质比未标记的蛋白质点向大分子方向有轻微迁移,主要是由于荧光团的加入(500Da左右)使得在标记的和未标记蛋白之间产生95%的误差, 之后在质谱分析时产生更多的复杂问题。4) 另一个值得注意的影响灵敏度的问题是荧光物质在激发P发射过程中会出现信号的相互干扰,引发Cy3 的激发波长有时可引起Cy5 标记的蛋白发射。(以上内容部分摘自国外医学卫生学分册2004年第31卷第1期姜楠文章)
毛细管凝胶电泳缓冲液加入有机试剂如甲醇的作用原理是什么?
美国Alpha Innotech 的凝胶电泳成像系统的camera卡的驱动,使用的是Chemilmager TM IS 4400软件,仪器上写的是 Multilmage Light cabinet ,需要的驱动是仪器上那个卡的驱动,叫着 ITI Image capture device,请使用相同仪器的兄弟姐妹们给我发过来一个吧,愁死了,仪器没法用了
单细胞凝胶电泳步骤:1. 分离制备单细胞悬液:(1) 体外培养的细胞株:用胰酶消化,最后用PBS悬浮吹打成单细胞悬液,细胞要计数,具体的量我前边已经说过。(2) 体内脏器细胞:处死动物,取出脏器,于Hanks’液中制备成单个细胞悬液。2. 胶板制备:(1) 取100μl于45℃水浴中保温的0.5%NMA,铺于磨沙载玻片上,形成底胶。盖玻片推匀,不能有气泡,4度凝固5至8分钟。(2) 水平取下盖片,取100μl于37℃水浴中保温的0.5%LMA与20μl细胞悬液(约400个细胞)混匀,立即铺片,加上盖玻片,4度凝固5至8分钟。3. 细胞裂解与电泳:(1) 将制备好的胶板去掉盖玻片后,浸于4℃预冷的细胞裂解液中,在4℃下裂解2.5到3小时。(2) 取出胶板,用双蒸水浸没漂洗后放入电泳槽中,浸泡在4℃预冷的电泳液中解旋20分钟。(3) 玻片水平放置阳极端附近,4℃电泳20到25分钟(25V,300mA)。可在电泳槽周围加冰块以保持低温。4. 中和与染色:(1) 电泳结束,将胶板浸泡于中和液中,每次10分钟,共中和3次,每次要更换中和液。最后晾干。(2) 取出胶板,置于染色缸中,在2μg/ml的EB染色液中,暗处染色5到10分钟。(3) 蒸馏水漂洗2次,每次5分钟。稍晾干,滤纸吸去多余水分,尽快在荧光显微镜下观察。从胶板制备开始到最后都应该在暗光下操作。先讲这些,你们可以先开始摸索,真正做了才能发现具体的问题,到时我们再探讨。
[size=10px][b]一、琼脂糖凝胶电泳原理[/b] 琼脂糖凝胶电泳是一种重要的分子生物学研究方法,?它利用琼脂糖凝胶的网络结构,?通过电场作用使带电颗粒(?如DNA或RNA)?在凝胶中移动,?根据分子大小和电荷性质的不同实现分离。?这种技术不仅操作简单迅速,?而且具有高分辨率,?因此在基因操作中扮演着关键角色,[font='PingFang SC']其[b]原理主要基于DNA分子的两大特性:电荷效应和分子筛效应。[/b][/font] ?琼脂糖是一种天然的长链状聚合分子,它在沸水中溶解,当温度降至45℃时开始凝固并形成多孔刚性立体网状结构,其孔径的大小取决于琼脂糖的浓度。 [b]分子筛效应[/b]指的是琼脂糖凝胶由琼脂糖分子交联形成的网状结构,其孔径大小与琼脂糖浓度成反比。当DNA分子通过凝胶时,会受到凝胶孔径的阻碍。较小的DNA片段可以通过凝胶孔隙,而较大的DNA片段则会被阻挡,导致迁移速率降低。?? [/size][align=center][size=10px] [/size][/align][size=10px][b]电荷效应[/b]指的是DNA分子在碱性条件下(pH7)会电离,带负电荷。当DNA样品置于电场中时,在外加电场的作用下受到电场力的作用,向正极方向移动。DNA分子的迁移速率与其所带的电荷量成正比,而电荷量又与DNA片段的长度成正比。因此,在相同电场条件下,较长的DNA片段迁移速率较慢,而较短的DNA片段迁移速率较快。不同DNA的分子量大小及构型各不相同,因此它们在电泳中的迁移率也会有所不同,从而可分离出不同的区带。[b]为什么核酸条带显示荧光?[/b]主要便于观察,对核酸进行了染色。溴化乙锭EB是一种扁平状分子,在紫外光照射下能发射荧光。当EB与DNA分子形成EB-DNA复合物后,其发射的荧光强度比游离状态的EB提高10倍以上,且荧光强度与DNA的含量呈正比。 [b]二、?琼脂糖凝胶电泳的详细操作步骤(1%琼脂糖凝胶电泳为例) [font='Times New Roman', 'serif']1.安装制胶模具[/font][font='Times New Roman','serif']:[/font][/b]利用电泳托盘,安装制胶模具,水平放置于试验桌上。 [b][font='Times New Roman', 'serif']2.[/font]制备琼脂糖凝胶:[/b]将琼脂糖粉末溶解于缓冲液中,加热煮沸,冷却后凝固成凝胶。(根据电泳所需要的分辨率准备琼脂糖-电泳缓冲液凝胶溶液)[font='Times New Roman','serif'](1)[/font]称取[font='Times New Roman','serif']1g[/font]琼脂糖,放入盛有[font='Times New Roman','serif']100mL 0.5×TBE[/font]缓冲液的[font='Times New Roman','serif']500mL[/font]三角瓶中,摇匀用天平称量其重量,摇匀。在微波炉中,使琼脂糖完全溶解,放回天平上,加入蒸馏水补齐至初始重量。冷却至不烫手([font='Times New Roman','serif']55℃[/font]左右),加入[font='Times New Roman','serif']100μL[/font][font='Times New Roman','serif']0.5mg/mL EB[/font]溶液(终浓度为[font='Times New Roman','serif']0.5 μg/mL[/font]),或加入[font='Times New Roman','serif']5-10μL[/font][font='Times New Roman','serif']StarGreen DNA Dye(GenStar)[/font],摇匀。 [font='Times New Roman','serif'](2) [/font]将凝胶溶液倒入安装好的制胶模具中,凝胶厚度应在[font='Times New Roman','serif']3-5mm[/font]。 [font='Times New Roman','serif'](3) [/font]选择合适的梳子,梳子的插入深度应使齿的底部和板的表面距离在[font='Times New Roman','serif']0.5[/font]到[font='Times New Roman','serif']1.0mm[/font]。要检查梳子齿下方或之间是否有气泡,在室温下冷却凝固。 [font='Times New Roman','serif'](4) [/font]待凝胶充分凝固后,垂直向上小心拔出梳子,以保证点样孔完好。 [font='Times New Roman','serif'](5)[/font]将凝胶置入电泳槽中,加入[font='Times New Roman','serif']0.5×TBE[/font]缓冲液[font='Times New Roman','serif'],以浸没凝胶约1mm为合适。[/font] [/size] [size=10px][b][font='Times New Roman','serif']3[/font][font='Times New Roman','serif'].[/font]制备DNA样品:[/b]将DNA样品与上样缓冲液混合。[/size] [size=10px]把DNA样品和上样缓冲液混合,利用[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url]把电泳样品加到没入缓冲液中凝胶槽中,在凝胶的两侧样品槽内加入合适的分子量标准品。[/size] [size=10px]上样量的多少根据样品中DNA片断的多少和大小而定,已知浓度的DNA用于估测样品质粒DNA的浓度。 [b][font='Times New Roman','serif']4.[/font]电泳:[/b]将DNA样品加载到凝胶上的样品孔中,在电场的作用下进行电泳。[/size] [size=10px]盖上电泳槽的盖子,正确连结电泳槽上的导线。电泳电压以正负电极的距离的一到五倍为合适(1到5V/cm)。如果电泳线连接正确,那么在进行电泳时可以看到有气泡从电泳槽内电极导线处产生,同时,在几分钟后,可见溴酚蓝条带从负极向正极移动,从上样槽内移入胶体。[/size] [size=10px][b]5.观察:[/b]当核酸样品移动到距离胶板下沿约1cm处时,停止电泳。电泳结束后,利用紫外灯观察DNA片段的迁移情况。当DNA样品在凝胶内移动到合适的距离时,关闭电源,去除电泳导线和电泳槽盖子。在室温下,用电泳缓冲液或水配制的EB溶液(0.5 μg/ml)对凝胶进行染色[b][font=-apple-system, helvetica, sans-serif]。[/font] 三、琼脂糖凝胶电泳的主要应用[/b] [/size] [size=10px][b]1.DNA片段的鉴定:[/b]通过比较DNA片段的迁移距离,与标准品进行对照,可以判断DNA片段的大小。[/size] [size=10px][b]2.DNA片段的分离:[/b]利用不同大小DNA片段的迁移速率差异,可以将DNA片段进行分离。[/size] [size=10px][b]3.DNA的纯化:[/b]通过电泳将目的DNA片段与其他杂质分离,得到纯化的DNA片段。(割胶回收)[/size] [size=10px][b]四、操作技巧和注意事项[/b][/size] [b][font='Times New Roman','serif'][size=10px]1.EB毒性[/size][/font][/b] [size=10px]EB是一种很强的诱变剂。在接触含有EB溶液时,应该全程戴手套和口罩。[/size] [size=10px]电泳中使用的溴化乙锭(EB)为中度毒性、强致癌性物质,务必小心,勿沾染于衣物、皮肤、眼睛、口鼻等。所有操作均只能在专门电泳区域操作,戴一次性手套,并及时更换。[/size] [b][font='Times New Roman','serif'][size=10px]2. 加热熔化琼脂糖[/size][/font][/b] [size=10px]用微波炉加热熔化琼脂糖时,溶液体积不能超过三角瓶容量的1/3,以免煮沸时溶液溢出。同时,琼脂糖必须完全熔化,否则可能导致电泳图像模糊不清。[/size] [b][font='Times New Roman','serif'][size=10px]3.凝胶厚度[/size][/font][/b] [size=10px]凝胶的厚度一般为4-6nm,若太厚可能会影响检测的灵敏度。待凝胶充分凝固后才能拔出梳子,以保证点样孔形状完好,防止漏样。[b][font='Times New Roman','serif']4.上样[/font][/b][/size] [size=10px]上样时,须先除去点样孔中的气泡,并且加样操作需小心谨慎,以免漏样或损坏胶孔。[/size] [b][font='Times New Roman','serif'][size=10px]5.电泳电压[/size][/font][/b] [size=10px]选择适当的电泳运行条件很重要,包括电压和距离。推荐的电压范围是4-6V/cm,电压太低会降低迁移率,电压太高会降低分辨率。[/size]
网上都是SDS-PAGE的配方表,可是我要做非变性的电泳,请问哪位大侠有 非变性 凝胶电泳的 分离胶 和 浓缩胶 配方表啊???请赐予 万分感谢
美国Alpha Innotech 的凝胶电泳成像系统的camera卡的驱动,使用的是Chemilmager TM IS 4400软件,仪器上写的是 Multilmage Light cabinet ,需要的驱动是仪器上那个卡的驱动,叫着 ITI Image capture device,请使用相同仪器的兄弟姐妹们给我发过来一个吧,愁死了,仪器没法用了
做了一小段时间的琼脂糖凝胶电泳, 有一些体会给新手们参考, 不当之处也请专家们指正.1. 加热时, 一定要煮沸, 以保证琼脂糖的完全溶解.2. 待溶液冷却至不烫手, 感觉温暖舒适时加EB. 一定要在通风柜里.3. 倒胶时, 可用干净的纸巾拭去气泡.4. 胶凝固后先倒入些电泳缓冲液以方便取梳子.5. 保证缓冲液淹过胶的边沿, 边沿部分常高出1-2mm.6. 有时需要大的上样孔, 可用胶带把几个相邻的梳齿粘在一起, 这种情况下, 尽量让胶液冷一些再倒胶.7. 如果只是为了看一下结果(不需要照相), 同一块胶可重复用1-3次. 有一次我跑了4遍, 条带很弱, 用加了EB的缓冲液(约10ul EB in 50ml 缓冲液)泡半小时后就如正常了.8. 要保存胶到第二天用, 可以保鲜膜包裹后放入4 度冰箱.9. TAE 电泳缓冲液也可重复使用, 至少10次没有问题.10. 为了防止电泳时两极缓冲液槽内pH和离子强度的改变,可在每次电泳后合并两极槽内 的缓冲液,混匀后再用。

同样是电泳,但是DNA聚丙烯酰胺凝胶电泳和琼脂糖电泳在操作上有很大的区别。相比之下,琼脂糖凝胶操作简单很多,只需要准备好制胶槽和梳子,融好胶后加一点核酸染料后,倒入制胶槽,然后点样,电泳,即可显示,时间大概在1个小时左右就可以了。而DNA聚丙烯酰胺凝胶电泳,先要洗板子,然后用乙醇擦板子,用硅化剂和反硅化剂擦,再制胶,然后预电泳,期间要插梳子,缓冲液热了后,点样电泳,电泳完后,下板子染色15分钟,最后显色。这一系列步骤听下来都有些复杂,所以有必要把该方法整理下来,标注好实验关键点。以下自己对聚丙烯酰胺凝胶电泳的实验总结,虽然步骤大体上和其他网上搜的一致,但是不同实验室甚至个人对于一个实验操作都会有不同,所以我把自己的拿出来和大家一起分享,重点在于一些小细节操作。一 聚丙烯酰胺凝胶的制备根据分离DNA片段的大小及需凝胶的容积,配制聚丙烯酰胺凝胶.1玻璃板清洗:NaOH溶液浸泡玻璃板一定时间,想要快的话可以用开水浸泡,将剥离板上的胶铲除,用去污剂(洗洁精也可)和清水清洗干净,最后用双蒸水冲洗两遍,垂直放置,晾干(清洗短长板的工具要分开)。2 用滤纸蘸取95%乙醇擦拭长短板,5分钟待乙醇挥发后。分别用脱脂棉蘸取硅化剂和反硅化剂均匀擦拭长短板。2.固定玻璃板:5分钟之后,把两个封条分别置于长板处理面两侧,短板处理面向下盖到长板上,两侧用夹子固定,准备好梳子,调整板子的平衡,使板子和台面保持水平。3配制胶溶液(5%): 原胶: 8.34ml;尿素: 45ml; 5xTBE:15ml;双蒸水:6.66ml; 尿素在室温难溶解,这一部分胶先配好在55℃水浴中预热,溶解完后过滤,制胶时再加入TEMED: 30ul;过硫酸铵: 200ul4灌胶:缓缓地使胶溶液倒入两板间,等胶溶液布满整个板子时,倒插梳子,用夹子夹紧使梳子和玻璃博间没有缝隙从而防止点样时串样,整个过程不要产生气泡。5.凝固:灌完胶后,放于室温让其自然凝固,观察胶边沿出现折射线就表明胶以凝固。二 聚丙烯酰胺凝胶电泳1.固定玻璃板于电泳仪:取掉玻璃板上的夹子,拔下梳子,除去长板点样处的胶,用清水冲洗干净玻璃板,短板向里固定于电泳仪支架上,即凹口板面向电泳液。2.插梳子:取5xTBE200ml稀释到1000ml制成1xTBE。向电泳仪下端槽内倒1xTBE约500ml,向上槽倒1xTBE,使液面高于短板上沿。用10ml的枪吸打缓冲液吹除插梳子除的废胶,插好梳子,点3ul 上样缓冲液,观察点样孔是否串样,如串样再调试梳子。3 预电泳:打开变压器,调节电压为1800V,功率100W,电流100A,预电泳大约40min至玻璃板热。4 样品变性:12ul体积的样品中加入6ulLoading Buffer,沸水浴5min,迅速放于冰上冷却。5电泳: 吸取3-4ul 变性后的样品,按顺序点样。调节电压为1800V,功率100W,电流80A,电泳大约1h。6 卸玻璃板。电泳完毕,关掉电泳仪,放出缓冲液,取下玻璃板,卸下短板、梳子、封条,只留下长板和上面的胶。http://ng1.17img.cn/bbsfiles/images/2015/08/201508042043_559121_3030491_3.jpg三 聚丙烯酰胺凝胶电泳的显色----银染1.洗胶:把长板置于双蒸水中清洗一次。2.染色: 染色液 硝酸银: 1.5g(0.1%);37%甲醇:2.25ml;加双蒸水至1.5L。把长板放在染色液中15分钟。3 洗胶:从染色液中拿出长板后,于双蒸水中清洗一次,该步骤动作要迅速。4.显色:显色液 碳酸钠: 45g(0.03g/ml); 37%甲醛: 2.25ml(0.15%);硫代硫酸钠:300ul(10mg/ml);加双蒸水至1.5L。把清洗干净的胶板置于盛有显色液的塑料盘中显色。显色时间根据条带和背景颜色深浅调整,达到DNA条带清晰的目的。5.终止显色:在水龙头下冲洗板子,防止胶被烧而无法读带。7.干胶:胶板置于室温自然干燥。http://ng1.17img.cn/bbsfiles/images/2015/08/201508042043_559120_3030491_3.jpg上图是自己按操作跑的板子,所有的实验操作都需带好手套,口罩,注意实验安全。板子读完后拍照保存,及时泡于NaOH溶液中。对于同一个实验每个实验室在有些步骤上会不同,所以本文也仅限拿出来分享而已。
我平时配制胶的浓度都为1%,但是我的导师告诉我其实在在凝胶电泳检测病毒和做胶回收提质粒时胶是有分别两个浓度的,不过她忘了应该是多少浓度了,所以我想问一下当目的不同时(一次跑胶为了验证有没有病毒,另一次跑胶为了胶回收),胶的浓度分别为多少比较合适呢?谢谢大家
各位大哥,电泳仪怎么样维护比较好(主要做琼脂糖凝胶电泳的),还有一些注意事项的?比如……
讲解聚丙烯酰胺凝胶电泳的三种效应: 1、浓缩效应。 2、电荷效应。 3、分子筛效应。
1.体系配制时候最关键的几个试剂一定要确定它们还有效、或者还没被污染:引物,酶,超纯水。这些东西最好自己收好,写上个人的名字放好,冰盒上记得带上橡皮筋,这样就不会因为别人翻冰箱时候把你的冰盒碰散了,试剂都碰掉。否则,你的试剂被污染了,到时候阴性对照狂出条带,再去找污染源很麻烦。而且配置体系时候要注意保持实验区的干净,事先可用小喷壶进行酒精喷雾,固定空气中的DNA,而且全程要戴手套,避免污染体系。2.pcr体系要摸准,最好用人家都做得很多的老体系来上手。3.要想得到漂亮的电泳图,可以在PCR开始时候就把胶倒上(前提是你的PCR总时间在1.5小时左右,并且1.5小时候之后你还在实验室.),让凝胶凉着,这样凝胶的上样孔会比较规则,胶体里面的其本身的孔径也会较规则。如果你要第二天再跑胶,千万记得把PCR完毕的样本放入4℃保存。第二天做时候建议把胶凉上25分钟左右。4.电泳上样时候建议使用排枪上样,不仅快速而且样本加到胶孔里的速度一致。当然,排枪上样最好选用进口枪头,国产枪头就不要想了。5.不管电泳室使用的频率高还是低,我都建议每次电泳时候更换电泳液,避免出现“︿”形条带。