推荐厂家
暂无
暂无
 银牌3年
银牌3年
 400-860-5168转4826
400-860-5168转4826
 留言咨询
留言咨询
 铜牌2年
铜牌2年
 400-860-5168转4221
400-860-5168转4221
 留言咨询
留言咨询
 留言咨询
留言咨询

 400-860-5168转4826
400-860-5168转4826
 留言咨询
留言咨询

 400-825-5669
400-825-5669
 留言咨询
留言咨询

 400-825-5669
400-825-5669
 留言咨询
留言咨询




你们的蒸馏(加热)冷凝管装置所用的冷却水是自来水还是制冷机的冷冻水?

结构生物学是用物理学方法在原子水平阐明生物大分子的三维结构,进而诠释生物大分子的生物学功能及其分子机制的科学。近几年,冷冻电镜在生物物理,特别是结构生物学领域掀起了一轮新的革命。冷冻电镜技术包括单颗粒技术和原位冷冻电镜技术,2017年单颗粒技术已获得诺贝尔奖,放眼未来,冷冻电镜更多的是要应用于获取细胞和组织样品的原位信息,尤其是利用冷冻电镜电子断层扫描成像技术(Cryo-ET)获得三维图像,将细胞内的生命过程可视化,在原位对生物大分子的结构进行解析,并进一步分析其与所处周围环境之间的相互作用关系,进而阐明其发挥功能的分子机制。蛋白质聚集是许多神经退行性疾病的典型症状,包括帕金森病(Parkinson’sdisease)、亨廷顿病(Huntington’sdisease)、以及肌萎缩侧索硬化症(amyotrophiclateral sclerosis)等,至今为止还没有针对这类疾病的有效治疗方案,因此了解这类疾病的致病机理尤为重要。在细胞内表达这些疾病相关的蛋白会导致细胞毒性以及形成大的胞内包涵体,然而这些包涵体的具体致病机理还不清楚,而且这些包涵体的组成以及其精细的细胞原位结构信息也无人知晓。为了回答这一科学问题,德国马克斯普朗克生物化学研究所Baumeister教授组的研究人员利用先进的冷冻电镜光电关联技术(Cryo-CLEM)、冷冻聚焦离子束切割技术(Cryo-FIB)、以及冷冻电子断层扫描三维重构技术(Cryo-ET),在小鼠原代神经细胞原位解析了亨廷顿基因1号外显子中衍生的多聚谷氨酰胺(polyQ)所形成的包涵体及其微环境的原位精细结构,相关结果发表在2017年9月的Cell杂志。他们发现polyQ包涵体是由淀粉样肽的纤维构成,与细胞的内膜系统特别是内质网相互作用,使内质网膜发生形变并扰乱其组成,还改变了包涵体周围的内质网膜的动态性。该研究结果暗示淀粉样肽的纤维和内质网的异常相互作用导致了蛋白质聚集物所产生的细胞毒性。[align=center][img=,690,424]https://ng1.17img.cn/bbsfiles/images/2018/11/201811271518599236_8463_3224499_3.jpg!w690x424.jpg[/img][/align]2018年3月,该研究组在PNAS杂志发表在酵母系统内的polyQ原位分子的结构解析,他们发现在酵母细胞内polyQ蛋白聚集体形成了无定形的包涵体以及少量的纤维丝,并使线粒体和脂滴的形态发生变形。对比这两种不同的机体系统下的差异,我们可以看到同样的polyQ蛋白聚集体在不同的环境中采用了不同的构像并利用特定的机制来靶向不同的细胞结构,从而产生细胞毒性。[align=center][img=,690,770]https://ng1.17img.cn/bbsfiles/images/2018/11/201811271519325828_4209_3224499_3.jpg!w690x770.jpg[/img][/align]另外,2018年2月的Cell杂志报道了该研究组在大鼠神经细胞原位解析了一种重复短肽(poly-GA)蛋白聚集体及其微环境的结构,不同于polyQ形成的纤维状结构,poly-GA聚集体是由平面扭曲的长短不一的丝带状结构组成。poly-GA聚集体大量募集了26S蛋白酶体复合物,而其他生物大分子如核糖体或分子伴侣却被排除在聚集体外部。与poly-GA的直接相互作用使蛋白酶体处于失活状态,虽然在整体水平上细胞内的蛋白酶体表达量没有变化,但有功能的蛋白酶体的数量大幅减少,揭示了蛋白质聚集物所产生细胞毒性的另一原因。[align=center][img=,690,378]https://ng1.17img.cn/bbsfiles/images/2018/11/201811271519469883_8555_3224499_3.jpg!w690x378.jpg[/img][/align]Baumeister教授组是Cryo-CLEM、Cryo-FIB以及Cryo-ET等关键技术方法发展的开拓者和领航者。Cryo-CLEM-FIB-ET即是在整个细胞内定位荧光标记的特定目标分子,观察其动态变化并在感兴趣的时刻进行快速冷冻,然后转移到冷冻扫描电镜利用冷冻聚焦离子束进行光电关联匹配,精确定位目标分子位置并进行聚焦离子束切割产生一层100-200nm厚的切片,最后利用冷冻电子断层扫描成像从原子分辨率上解析其未被破坏的天然原位结构信息。目前冷冻光电关联的一大瓶颈是光镜的分辨率较低,虽然超分辨光电关联技术在飞速发展,但是其缺点如高强度激光照射可能使样品升温,成像速度慢等还需要一一克服。超分辨光电关联令人振奋的一大潜在应用是来精确指导冷冻聚焦离子束切割,使得大的细胞样品中的任何感兴趣目标分子都能被精确定位切割,进而进行高分辨率数据收集。另外,随着技术进一步发展,用高电子密度标签来标记目标分子并在电镜下直接成像也将会成为可能。结构生物学的终极目标是了解细胞生命过程中每一个分子的结构、功能以及它们之间的相互作用,Cryo-CLEM-FIB-ET则是在结构生物学与细胞生物学之间架起的一座桥梁,让细胞内的微观生命动态过程可视化![b]参考文献[/b]1. Bauerlein,F. J. B., et al. 2017. In Situ Architecture and Cellular Interactions of PolyQInclusions. Cell 171(1): 179-187.2. Guo, Q., etal. 2018. In Situ Structure of Neuronal C9orf72 Poly-GA Aggregates RevealsProteasome Recruitment. Cell 172(4): 696-705.3. Gruber, A.,et al. 2018. Molecular and structural architecture of polyQ aggregates inyeast. Proc Natl Acad Sci U S A. .4. Wolff, G.,et al. 2016. Towards correlative super-resolution fluorescence and electroncryo-microscopy. Biol Cell 108(9): 245-258.Oikonomou, C. M. 2017. Cellular ElectronCryotomography: Toward Structural Biology In Situ. Annu Rev Biochem 20(86):873-896.来源:【生物成像中心】
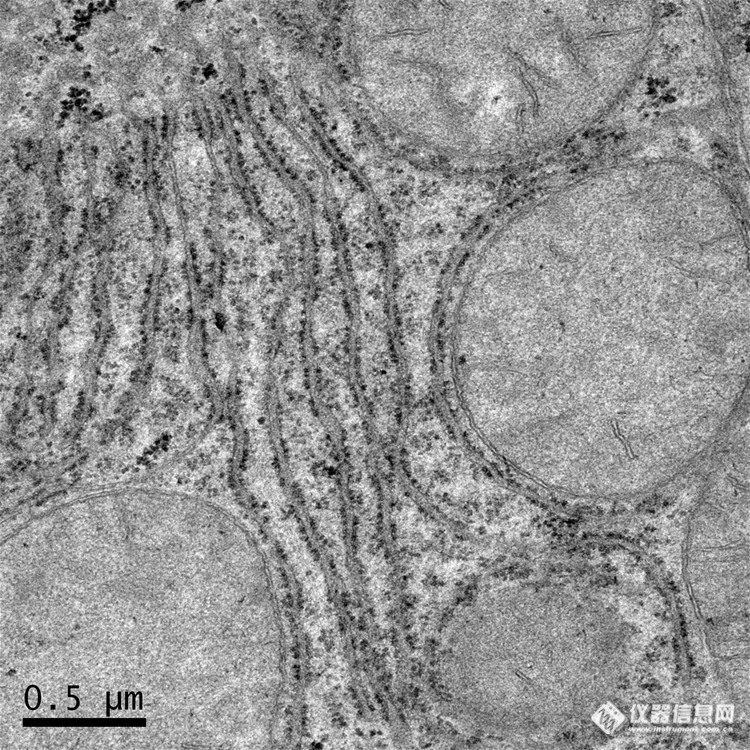
最近一直在摸索着用高压冷冻和冷冻替代样品制备技术,刚开始做的时候冰晶特别严重,如下图Hela细胞。冰晶已经把细胞超微结构破坏的不行了。http://ng1.17img.cn/bbsfiles/images/2016/09/201609231539_611900_2423894_3.jpg经过很长时间的摸索,得到以下制样方法:1 取样1.1 培养细胞:取适量的细胞悬浮液,低速离心成细胞团,去上清,细胞团呈米糊状,用移液枪取适量细胞,填满Carrier,加入适量冷冻保护液1-Hexadecene,滤纸吸取多余水分,使冷冻保护液液面略高于Carrier(Carrier用丙酮清洗,然后在空气中晾干,用1-Hexadecene浸泡备用)。1.2 小鼠肝脏:从活体上取出的组织,先用锋利的刀片在低温下切成尽可能薄片状,从中挑选合适的部分切下来,然后装入Carrier,加入适量冷冻保护液1-Hexadecene,滤纸吸取多余水分,使冷冻保护液液面略高于Carrier。2高压冷冻高压冷冻仪在使用前,要先做一些准备工作:要先加入足够的液氮,并加入压力液甲基环己烷,然后用空载的carrier高压冷冻三次,保证高压冷冻仪在最佳工作状态。2.1 将上述装有样品的carrier快速安置到高压冷冻仪,准备高压冷冻。2.2 高压冷冻样品,迅速把样品冷冻下来,并做好记录。通过高压冷冻仪冷冻样品后产生的冷冻速度和压力变化曲线,可以选择冷冻效果较好的样品继续下面实验。2.3 转移样品,首先把现配的替代液1%锇酸(0.5g锇酸溶于50mL丙酮)分装到2mL冻存管中,迅速放入液氮冷冻备用,冷冻过程中保持冷冻管直立。与此同时,冷冻替代仪加满液氮,将自制的冻存管架放入样品腔,预冷至-100℃。用预冷的镊子,在液氮下将Carrier分别装入冻存管,冻存管盖不宜拧的过紧,然后迅速转移到冷冻替代仪样品腔室的冻存管架里。3 冷冻替代 步骤 温度 时间 1 -100℃ -90℃ 4h 2 -90℃ 72h 3 -90℃ -60℃ 8h 4 -60℃ 8h 5 -60℃ -30℃ 4h 6 -30℃ 8h 7 -30℃ -20℃ 2h 8 -20℃ 8h 9 -20℃ 4℃ 2h 10 4℃ 1h 温度达到4℃后,用4℃的丙酮浸洗样品3次,每次15分钟。此过程中,会有部分样品与Carrier分离,若还有没分离的可以用解剖针将样品从Carrier中剥离。4 渗透包埋分别用以下渗透液渗透。 步骤 渗透液 浓度 时间 1 Epon812/丙酮 1:1 1.5-2h 2 Epon812/丙酮 3:1 6-12h 3 Epon812 100% 1h 4 Epon812 100% 8h 5 Epon812 100% 1h然后将样品转移至包埋槽,60℃烘箱聚合48h。5 超薄切片把两种生物样品对应的每一个包埋块分别超薄切片,各捞两个铜网,并染色。6 电镜观察观察细胞内超微结构保存情况,对感兴趣区域拍照。终于有所改善,如下图的小鼠肝脏细胞,轮廓十分清楚,结构保存完好。http://ng1.17img.cn/bbsfiles/images/2016/09/201609231516_611895_2423894_3.jpg局部放大后观察,能看见核孔,双层核膜,甚至是膜的磷脂双分子层结构(这是在常规化学固定制样中很难看到的),看到这些让人激动不已。http://ng1.17img.cn/bbsfiles/images/2016/09/201609231516_611894_2423894_3.jpg碰巧看见一个正在分裂的线粒体。线粒体脊很清楚,双层膜紧挨着,不像常规制样间隙那么大。另外,线粒体基质保存完好,所以线粒体整体较细胞基质反差大。http://ng1.17img.cn/bbsfiles/images/2016/09/201609231516_611893_2423894_3.jpg以下是常规化学固定制样的结果,可与上面高压冷冻及冷冻替代制样技术结果对比:http://ng1.17img.cn/bbsfiles/images/2016/09/201609231644_611928_2423894_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/09/201609


