又称恒电流库仑滴定法,是建立在控制电流电解过程基础上的[url=http://www.hudong.com/wiki/%E5%BA%93%E4%BB%91%E5%88%86%E6%9E%90%E6%B3%95][color=#0268cd]库仑分析法[/color][/url]。 [b]原理 [/b] 用强度一定的恒电流通过电解池,同时用电钟记录时间。由于电极反应,在工作电极附近不断产生一种物质,它与溶液中被测物质发生反应。当被测定物质被“滴定”(反应)完了以后,由指示反应终点的仪器发出讯号,立即停止电解,关掉电钟。
我们实验室一直是用的老式的燃烧法加碘量法测硫。因为我们是地质实验室,所以绝大多数样品是矿石样而非煤样。现在要换新仪器,想知道现在的库仑滴定法测硫仪是否适用于矿石样品?谢谢。
向广大同仁求助sh/t1551-2018 工业芳烃溴指数的测定库仑滴定法标准,请大神帮忙!!
HC211型库伦滴定法COD测定仪说明书,有版友可以分享一下吗?
【序号】:5【作者】: 谷雪贤【题名】:库仑滴定法测定羧甲基壳聚糖的含量【期刊】:理化检验(化学分册). 【年、卷、期、起止页码】:2019,55(09)【全文链接】:https://kns.cnki.net/kcms2/article/abstract?v=3uoqIhG8C44YLTlOAiTRKibYlV5Vjs7iLik5jEcCI09uHa3oBxtWoIaI05yc0UOpzxra7LwzF96-sTRMLls1-oVXPYAHrnRo&uniplatform=NZKPT
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=98395]浅析库仑滴定法测定全硫准确度的影响因素[/url]
标准号:GB/T 11133-2015标准名称:石油产品、润滑油和添加剂中水含量的测定 卡尔费休库仑滴定法英文名称:Standard test method for determination of water in petroleum products,lubricating oils,and additives—Coulometric Karl Fischer titration method标准状态:现行首发日期:1989-03-31发布日期:2015-12-31实施日期:2016-06-01出版语种:中文简体
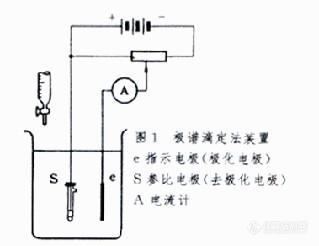
利用电解池中电流的变化指示滴定终点的电滴定分析方法。分为一个极化电极的安培滴定法和两个极化电极的安培滴定法。用滴汞电极为极化电极的一个极化电极的安培滴定法称为极谱滴定法。两个极化电极的安培滴定法称为死停终点法或双安培滴定法。 极谱滴定法是基于极谱法的原理在一定外加电压下滴加标准溶液,藉观察滴定过程中扩散电流的改变以确定滴定终点的容量滴定法。极谱滴定法装置就是一台简易极谱仪加一支滴定管( 图1 )。溶液中被测离子于一定的外加电压下在滴汞电极上还原(或氧化),此时由于浓差极化产生扩散电流。随着被测离子与滴定剂反应浓度越来越低,在滴汞电极上还原(或氧化)而产生的扩散电流越来越小,达到滴定终点时,扩散电流降至零。若将滴定剂体积与每加一次滴定剂后相应的电流读数作图,可得一直线。过滴定终点之后再将滴定剂体积与加滴定剂后的相应电流作图,又得一直线。将所得两条直线延长相交,交点所对应的滴定剂体积即为滴定终点。此法的优点是:①适用范围广,可用于沉淀反应、络合反应和氧化还原反应 ;② 适用浓度范围宽 , 测量范围为0.1~10-4摩尔/升(mol/L)。缺点是 :① 选择性差,易受其他物质干扰;②操作麻烦。 双安培滴定法的装置和图1相似, 两个电极都是铂电极,串联一个电流计指示电流。外加电压一般为几十毫伏。当滴定至电流发生突变时,表示滴定终点到达。滴定曲线的形状取决于滴定体系的可逆性程度( 图2 )。双安培滴定法可用于沉淀反应、络合反应和氧化还原反应。在双安培滴定法中,应用较广的是碘滴定法 ,此外 ,在铈量法测定As3+和Sb3+离子 ,银量法测定卤素离子和CN- 离子也常用此法指示终点 , 此外,也常用来指示库仑滴定法的终点。双安培滴定法的特点是装置简单,准确快速。[img]http://ng1.17img.cn/bbsfiles/images/2010/04/201004221500_213989_1604460_3.jpg[/img]
现求购库仑滴定仪一套,可做恒电流库仑滴定
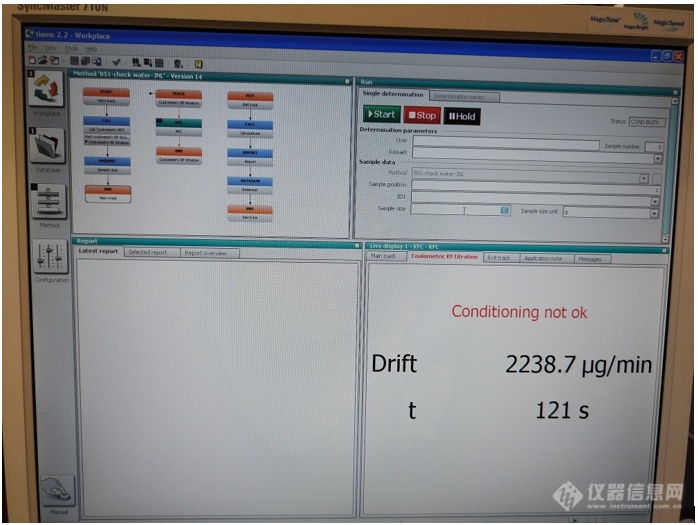
[align=center][size=18px]水分测定之库伦滴定仪使用心得[/size][/align][size=16px]水分测定通常有两种方法,一种是滴定法,一种是库伦法,滴定法常常用于水分含量较高的样品,而库伦法则适用于水分含量比较低的样品。单位有一台瑞士万通水分测定仪,用的是是库伦法测定水分。[/size][size=16px]1.使用前检查:检查内容包括电源是否连接,信号传输是否正常,因为水分测定仪不止一个模块,每个模块有自己的电源线与信号连接线,有时候不小心碰了电源或者连接线,结果打开软件发现某个模块未连接,所以从一开始使用前就进行检查。[/size][size=16px]2.检查阳极液是否需要更换,器皿中装有100ml左右库伦法阳极液,样品测试次数多了以后,阳极液中含有的水量达到饱和后就会影响测试,我们可以从图中draft值进行判断,如果平衡过程中居高不下,那就是需要更换了。还有阳极液[/size][align=center][size=16px][img]https://ng1.17img.cn/bbsfiles/images/2023/10/202310170957352467_5494_3141805_3.png[/img][/size][/align][size=16px]3.正常颜色为淡黄色,随着样品测试越来越多,其颜色也会越来越深,此时我们也可以进行更换。[/size][size=16px]4.干燥硅胶更换,每次分析样品前检查仪器上的干燥硅胶是否变色,若果颜色都变了,那需要及时进行更换。否则会出现测试过程中系统一直难以稳定的情况。[/size][align=center][size=16px][img]https://ng1.17img.cn/bbsfiles/images/2023/10/202310170957354549_2389_3141805_3.png[/img][/size][/align][size=16px]4.仪器平衡,刚开启仪器draft值会很高,我们需要等待较长时间让仪器平衡稳定,待仪器平衡完成后,仪器会显示状态OK的提示,代表此时可以开始加样测试。[/size][align=center][size=16px][img]https://ng1.17img.cn/bbsfiles/images/2023/10/202310170957358259_4368_3141805_3.jpeg[/img][/size][/align][size=16px]5.样品准备,对于分析的样品固体和液体均可,但要保证加入的样品能够在阳极液中完全溶解。如果出现不能完全溶解的情况,一来仪器很难稳定下来,二来即使仪器稳定下来了,那测试结果实际是偏小的,因为有水分会包夹在未溶解的样品里面。[/size][size=16px]6.样品称量可以采用减量法,样品加样前归零,然后取完样加入仪器加样口后再次称量,天平显示的差值即为加入样品的质量,这一步要注意用来取样的称量勺或者其它器皿要和装有样品的样品瓶一起称重,否则称量结果是错误的。[/size][size=16px]7.加入样品的时候要注意不要粘在加样口,对于液体样品还好一点,可以用滴管吸取样品,然后深入加样口,在器皿内液面上方进行滴加。对于固体样品,特别是粉末样品,由于加样口比较小,很容易在加样的时候粘在加样口,因此要特别小心。如果粘上了样品,需要快速将其掸入,否则会造成样品损失,导致最终测试结果偏低。[/size][size=16px]8.加样速度是影响测试结果准确性的一个重要因素,加样的时候需要打开加样口磨口塞,此时外部空气会进入,然后溶解在阳极液里面,而空气中又含有水分,因而会造成结果偏高。加样时打开磨口塞的时间越久,那么溶解在阳极液里面的水分就越多,最后的结果就会越偏大。[/size][size=16px]总结:库伦法水分测定虽然是一个很成熟的测试方法,其稳定性好,应用广泛,准确度高,但上述这些前提均需要操作人员严格执行操作步骤,清楚测试过程中的注意事项,这样测试才会又快又准。[/size]
我们有一上海安亭的ZSD-2水分测定仪,现需要测定羟苯丙酯钠水分,要求按照费休氏-库伦滴定法滴定,不知上海安亭的ZSD-2水分测定仪可否能用?
谁了解微库仑滴定仪,介绍介绍。销售说能测到0.1ppm硫,靠谱吗?
我在做一个库仑滴定仪,我发现一下几个问题1、在电解的时候和没有电解的时和没有电解时指示电极的输出信号变化很大2、在电解过程中,指示电极输出的信号变化波动没有规律3、当电解液已经变色后,开始电解时指示电极输出的信号没有明显的变化这些问题在以前的课本上没有学过,也不知道去什么地方找了,来这里问问了
卡尔-费休法,它是利用碘氧化二氧化硫时需要定量的水的原理测定液体、固体和气体样法中的含水量。被许多国家定为标准分析方法, 用来校正其它分析方法和测量仪器。(一).应用范围 Karl-Fisher滴定法可适用于多种有机和无机物中含水的测定。由于各种化合物性质的差异, 可分为能直接进行测定和不能直接进行测定两类。可以直接测定的主要有机和无机化合物如表1所示。 表1 无干扰的有机和无机化合物 化合物种类 举 例 无机化合物 (1).有机酸盐 Na(CH3 )SO4 ,Ba(OOCCH3 )2 ,K2 C2 O4 ,VO2 (OOCCH3 )2 , Na2 C2 H4 O6 (2).无机酸盐 NH4 PO4 ,CaCl2 ,NaHSO4 ,Na2 SO4 ,KF,NH4 NO3 ,MgSO4 , Na2 SO4 ,KSCN,FeSO4 ,Al2 (SO4 )3 KSO4 ,CaHPO4 , NaI,CaCO3 ,FeF3 ,VO2 (NO3 )2 (3).酸式氧化物 SiO2 ,Al2 O3 (4).无机酸和酸酐 SO2 ,HI,HF,HNO3 ,HCN,H2 SO4 ,HSO3 ,NH2
用途:用电解产生的二价铁离子滴定毫克级重铬酸钾即六价铬。要求:精密度高,可达万分之几以下。目前,有很多卡氏水分库仑测定仪,可否用于这个用途?谢谢
用途:用电解产生的二价铁离子滴定毫克级重铬酸钾即六价铬。要求:精密度高,可达万分之几以下。目前,有很多卡氏水分库仑测定仪,可否用于这个用途?谢谢
有没有坛友知道上海什么地方有库伦法水分滴定仪维修的,我们实验室的库伦法 水分滴定仪好久不用了,今天加新鲜的阳极液和阴极液后, 无法平衡,离子交换膜从来没更换过,有没有人知道哪里有库伦法 水分滴定仪上用的离子交换膜卖?
目前一般实验室滴定分析采用的是人工滴定法,它是根据指示剂的颜色变化指示滴定终点,然后目测标准溶液消耗体积,计算分析结果。自动电位滴定法是通过电位的变化,由仪器自动判断终点。为了比较仪器和人工滴定方法的测定结果,我们选用了酸价和过氧化值两个指标,分别用自动电位滴定法和人工滴定法进行样品分析。 1 实验部分 1.1 自动电位滴定法的实验仪器 瑞士万通(METROHM)751GPD自动电位滴定仪 727磁力搅拌滴定台 10ml交换单元 6.0431.100Pt电极 6.0133.100pH玻璃电极 6.0729.100Ag/AgCl参比电极 6.0331.0Pt辅助电极 1.2 人工滴定法 按照GB/T5009.37—1996的方法测定样品中的酸价和过氧化值。 2 实验结果与讨论 2.1 两种滴定方法的测定结果对照 自动电位滴定法和人工滴定法测定植物油的酸价和过氧化值结果无显著性差异,表明自动电位滴定仪测定植物油酸价和过氧化值,与现行的国家卫生标准滴定方法结果相近。 2.2 两种滴定方法的精密度比较 选用酸价值较高的样品,分别用自动电位滴定法和人工滴定法平行测定5次,自动电位滴定法测定的相对标准偏差1.1%,人工滴定法为1.6% 平行测定酸价值较低的样品5次,自动电位滴定法测定的相对偏差为2.1%,而人工滴定法的相对标准偏差高达11.4%,表明自动电位滴定法的精密度优于人工滴定法。综上所述,自动电位滴定法测定结果与国标法无异,精密度达到检验要求。由于自动电位滴定法是根据滴定曲线的一阶导数确定终点,等当点与终点的误差非常小,准确度高,避免了人工滴定法由于要加指示剂可能因加入量、指示终点与等当量间、操作者对颜色判断等的误差 电动定位滴定法无须使用指示剂,故对有色溶液、浑浊度以及没有适合指示剂的溶液均可测定 Metrohm自动电位滴定仪可判断多达9个等当点,可以连续滴定溶液中的多个成分,如连续滴定水样中Ca2+、Mg2+,滴定混合酸。自动电位滴定仪还能对滴定分析的各种测定参数,例如测定日期、仪器型号、滴定用标准溶液的消耗量、滴定曲线作自动记录,并自动计算打印出测定结果作为原始记录保存,减少了分析者原始记录数据处理的工作量和运算差错,提高了实验室间分析结果的可比性,有利于实验室管理,因此适于理化分析实验室用作代替人工操作的分析仪器。
[em39] 库仑滴定的当发现到了电解终点就停止滴定还是怎么着呢?
在做库仑滴定分析滴定终点如何确定呢! 做试验就没有做准过,发现不了指示信号的变化规律? 那位大侠可以给指条路呢? 谢谢了
库仑滴定仪可以测定低含量的VAC吗?该选择什么仪器,怎样测?
用RPA-200微库仑滴定仪测定的氯含量是总氯吗?为什么拿石科院的盐含水量标准样到RPA-200微库仑滴定仪测定其氯含量,其结果不符合?
什么是滴定法,滴定法准确度高不高? 滴定法是将已知浓度的标准溶液均匀缓慢地滴入试祥溶液中,使标准液与试样溶液中的被测组分进行化学反应。用指示剂或其他电测手段判断反应的终点。根据滴定的标准溶液数量,计算出试样溶液中待测组分的含量。在环境监测中,COD、各种形态的氮、卤素离子、亚硫酸离子、氰基离子等许多项目,都用滴定法测定。有时判断仪器分析值是否准确也常用滴定法校验。滴定法使用的计量器具有容量瓶、移液管、滴定管、量筒等。 滴定法与其他方法相比具有方法简单、器具较少、准确可靠等优点。当试样溶液中被测组分浓度较高时,其准确度较[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]法、分光光度法、[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法等高得多。所以,尽管仪器分析方法比较普遍,仍不能完全取代滴定法。但是,滴定法不适用于微量分析。当被溯组分浓度很低时,许多仪器分析比滴定法灵敏度高。而且,滴定法容易受分析者的操作经验和熟练程度所左右。经验多、较熟练的分析人员所得到的分析结果比经验少、不熟练者准确可靠。因此,在滴定法操作中,一方面要求配制的标准溶液准确无误,另一方面要求滴定时观察的液面与眼睛高度严格保持一致。同时还要注意以下事项: (1)不要加热带有刻度的计量容器; (2)各类计量容器必须充分洗净方可使用; (3)取20mL的溶液时,应当用20mL的移液管取一次,一般不用10mL移液管取两次; (4)不要用嘴把溶液吸入移液管,要用吸耳球。
电位滴定法和永停滴定法有何联系和区别?两者的使用范围有何不同呢?哪种方法更为实用呢?
电位滴定法与永停滴定法电位滴定法与永停滴定法是容量分析中用以确定终点或选择核对指示剂变色域的方法。选用适当的电极系统可以作氧化还原法、中和法(水溶液或非水溶液)、沉淀法、重氮化法或水分测定法等的终点指示。 电位滴定法选用2支不同的电极。1支为指示电极,其电极电势随溶液中被分析成分的离子浓度的变化而变化;另1支为参比电极,其电极电势固定不变。在到达滴定终点时,因被分析成分的离子浓度急剧变化而引起指示电极的电势突减或突增,此转折点称为突跃点。 永停滴定法采用2支相同的铂电极,当在电极间加一低电压(例如50mV)时,若电极在溶液中极化,则在未到滴定终点前,仅有很小或无电流通过;但当到达终点时,滴定液略有过剩,使电极去极化,溶液中即有电流通过,电流计指针突然偏转,不再回复。反之,若电极由去极化变为极化,则电流计指针从有偏转回到零点,也不再变动。仪器装置 电位滴定可用电位滴定仪、酸度计或电位差计,永停滴定可用永停滴定仪或按图示装置。 电流计的灵敏度除另有规定外,测定水分时用10A/格,重氮化法用10A/格。所用电极可按下表选择。 ────────┬──────────┬────────────── 方 法 │ 电 极 系 统 │ 说 明 ────────┼──────────┼────────────── 水溶液氧化还原法│ 铂-饱和甘汞 │铂电极用加有少量三氯化铁的硝 │ │酸或用铬酸清洁液浸洗 ────────┼──────────┼────────────── 水溶液中和法 │玻璃-饱和甘汞 │ ────────┼──────────┼────────────── 非水溶液中和法 │玻璃-饱和甘汞 │饱和甘汞电极套管内装氯化钾的 │ │饱和无水甲醇溶液。玻璃电极用 │ │过后应即清洗并浸在水中保存 ────────┼──────────┼────────────── 水溶液银量法 │ 银-玻璃 │银电极可用稀硝酸迅速浸洗 ├──────────┼────────────── │银-硝酸钾盐桥-饱和甘│ │汞 │ ────────┼──────────┼────────────── -C≡CH中氢置换法│玻璃-硝酸钾盐桥-饱和│ │甘汞 │ ────────┼──────────┼────────────── 硝酸汞电位滴定法│铂-汞-硫酸亚汞 │铂电极可用10%(g/ml)硫代硫酸 │ │钠溶液浸泡后用水清洗。汞-硫 │ │酸亚汞电极可用稀硝酸浸泡后用 │ │水清洗。────────┼──────────┼──────────────永停法 │铂-铂 │铂电极用加有少量三氯化铁的硝 │ │酸或用铬酸清洁液浸洗 ────────┴──────────┴──────────────滴定法 (1)电位滴定法 将盛有供试品溶液的烧杯置电磁搅拌器上,浸入电极,搅拌,并自滴定管中分次滴加滴定液;开始时可每次加入较多的量,搅拌,记录电位;至将近终点前,则应每次加入少量,搅拌,记录电位;至突跃点已过,仍应继续滴加几次滴定液,并记录电位。 滴定终点的确定 用坐标纸以电位(E)为纵坐标,以滴定液体积(V)为横坐标,绘制E-V曲线,以此曲线的陡然上升或下降部分的中心为滴定终点。或以△E/△V(即相邻两次的电位差和加入滴定液的体积差之比)为纵坐标,以滴定液体积(V)为横坐标,绘制(△E/△V)-V曲线,与△E/△V的极大值对应的体积即为滴定终点。也可采用二阶导数确定终点。根据求得的△E/△V值,计算相邻数值间的差值,即为△E/△V,绘制(△E/△V)-V曲线,曲线过零时的体积即为滴定终点。 如系供指示剂变色域的选择核对,滴定前加入指示剂,观察终点前至终点后的颜色变化,以选定该品种终点时的指示剂颜色。 (2)永停滴定法 用作重氮化法的终点指示时,调节R使加于电极上的电压约为50mV。取供试品适量,精密称定,置烧杯中,除另有规定外,可加水40ml与盐酸溶液(1→2)15ml,而后置电磁搅拌器上,搅拌使溶解,再加溴化钾2g,插入铂-铂电极后,将滴定管的尖端插入液面下约2/3处,用亚硝酸钠滴定液(0.1mol/L或0.05mol/L)迅速滴定,随滴随搅拌,至近终点时,将滴定管的尖端提出液面,用少量水淋洗尖端,洗液并入溶液中,继续缓缓滴定,至电流计指针突然偏转,并不再回复,即为滴定终点。用作水分测定的终点指示时,可调节R使电流计的初始电流为5~10μA,待滴定到电流突增至50~150μA,并持续数分钟不退回,即为滴定终点。
本章教学目的:1、掌握氧化还原滴定法分类及各种方法的反应实质。2、了解氧化还原滴定法和酸碱滴定法的异同点。从而明确严格控制反应测定结果的关键。3、熟练掌握碘量法的分析原理、指示剂变色原理及误差来源。教学重点与难点:氧化还原滴定法中各种不同方法的反应实质。教学内容: 一、方法简介1、氧化还原滴定法的分类:氧化还原滴定法:以氧化还原反应为基础的滴定分析方法。标准溶液:氧化剂——测定还原性物质含量。 还原剂——测定氧化性物质含量。氧化还原滴定法: 高锰酸钾法 重铬酸钾法 碘量法 溴酸钾法氧化还原滴定法的特点及与酸碱滴定法的比较:①酸碱滴定法是离子互换反应,反应历程简单、快速。②氧化还原滴定法是电子转移反应,反应复杂、反应速度快慢不一、受外界条件影响较大。比较结果:氧化还原滴定法需要控制反应条件,使其符合滴定分析的要求2、氧化还原滴定法滴定终点的确定①标准溶液自身做指示剂2MnO4- + 5C2O42-ˉ + 16H+ == 2Mn2+ + 10CO2↑ + 8H2O高锰酸钾为紫色,极稀溶液中呈无色。过量的半滴KMnO4,溶液变粉色。②专属指示剂I2 + 2Na2S2O3 == 2NaI + Na2S4O6稍过量的碘标准溶液与溶液中的淀粉指示剂形成浅蓝色。
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=94642]电位滴定法与手工滴定法比较[/url]
滴定法是最常用的化学分析方法。在滴定中,只要被测组分、滴定剂或反应生成物中的任何一个在紫外光区有特征吸收,并遵守朗伯-比尔定律,就可通过滴定体系的吸光度的变化来指示滴定过程和滴定终点,这就是紫外分光光度滴定法。分光光度滴定法不仅适用紫外光区,也适用可见光区和红外光区。在滴定后,以滴定剂的用量为横坐标,以滴定体系的吸光度为纵坐标,绘制分光光度滴定曲线。滴定曲线中两条直线的交点就是滴定终点。由滴点终点所示的滴定剂体积和浓度,就可计算样品溶液中待测组分的含量或浓度。 分光光度滴定法准确、灵敏和精密度高(相对误差可0.1%),且有适用范围广和可实现自动滴定等特点。有人用这个做过吗
沉淀滴定法 : 是 以沉淀反应为基础的一种滴定分析方法。 沉淀滴定法必须满足的条件: 1. S 小,且能定量完成; 2. 反应速度大; 3. 有适当指示剂指示终点; 4. 吸附现象不影响终点观察。 目前,应用较广泛的是: 生成难溶性银盐的沉淀滴定法 银量法 沉淀反应: Ag + +沉淀滴定法:是 以沉淀反应为基础的一种滴定分析方法。 沉淀滴定法必须满足的条件: 1. S 小,且能定量完成; 2. 反应速度大; 3. 有适当指示剂指示终点; 4. 吸附现象不影响终点观察。 目前,应用较广泛的是:生成难溶性银盐的沉淀滴定法——银量法 沉淀反应: Ag+ +X- ⇌ AgX↓ Ag+ + SCN- ⇌ AgSCN ↓应用:Cl-、Br-、I-、Ag+、SCN-以及能定量地产生这些离子的有机化合物。
水分测定仪容量滴定和库仑滴定有什么区别,ZKF-1型是属于哪一种的有知道的指点下,谢谢了!