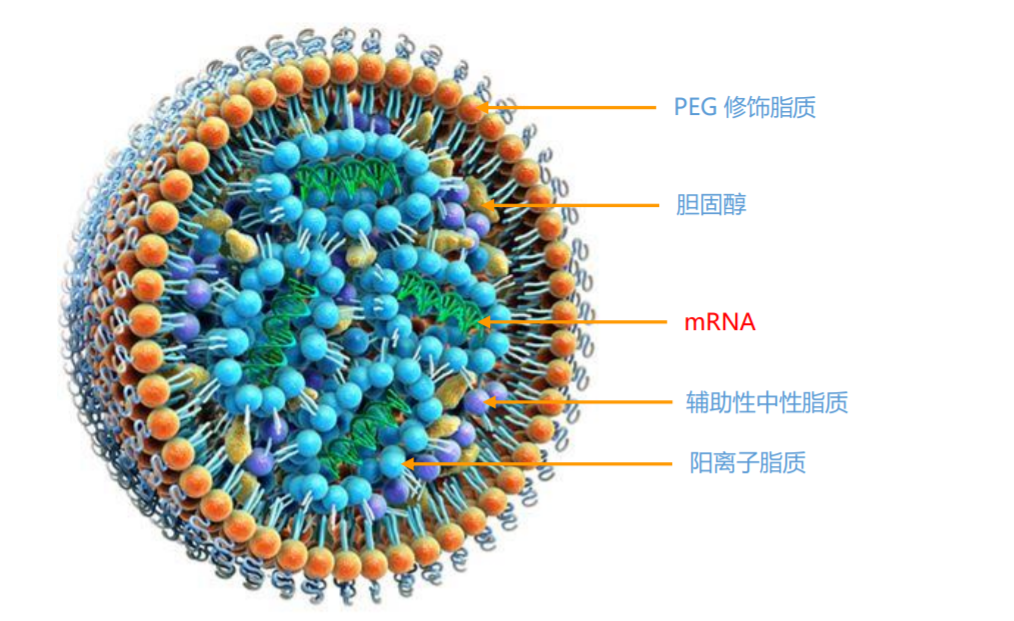
以三大mRNA制药公司分析mRNA药物前景
p 随着mRNA修饰和制剂等技术的不断突破,mRNA制药行业日渐成熟。Moderna、BioNTech和CureVac等公司都已拥有丰富的mRNA药物产品线,布局在肿瘤疫苗和抗感染疫苗等领域。本文将以这三家公司的技术平台和产品线为切入点,讲述mRNA药物的发展现状、核心技术及行业前景。/pp strongmRNA药物简介/strong/pp mRNA药物一直被寄予厚望,从上世纪90年代初步证实mRNA的药效开始,大量的精力投入到了mRNA药物的研发中。mRNA可以快速地在细胞内翻译,表达所需蛋白,适用于制作抗感染疫苗和肿瘤疫苗。然而,mRNA非常不稳定,进入体内后很快会被降解,成为困扰行业多年的症结,mRNA药物的研发一直在艰难中前行。/pp 随着技术不断发展与成熟,多种技术被用于产生更稳定的mRNA。首先,是用人工合成的非天然核糖核酸替换天然核糖核酸来合成mRNA,这样可以逃避免疫系统的清除。其次,加上5’帽子、3’ poly(A)n尾和UTR序列等也能稳定mRNA,并增加翻译效率。再者,特殊的新型制剂技术可以有效地保护mRNA,并且促进免疫反应的产生。/pp style="text-align: center "img width="554" height="216" title="微信图片_20180807094631.jpg" style="width: 451px height: 180px " src="http://img1.17img.cn/17img/images/201808/insimg/96973997-f88d-4807-806e-3426ba5592ba.jpg"//pp style="text-align: center " span style="font-size: 14px "mRNA常用的结构修饰技术/span/pp mRNA药物技术的进步使行业进入了快速发展期,近几年,BioNTech、Moderna、CureVac和Arcturus等mRNA制药企业获得了大量的投融资,多个项目进入临床阶段,产品主要布局在肿瘤疫苗和抗感染疫苗等领域。/pp 肿瘤疫苗是技术难度最大,需求最迫切的疫苗,其开发过程也非常曲折坎坷,最初的肿瘤疫苗通常使用肿瘤相关抗原,即正常组织中低表达,肿瘤组织中高表达的抗原,如MUC家族蛋白、PSA和NY-ESO-1等,然而,这些疫苗在上世纪90年代至2010年间几乎都在临床试验中失败。新一代的肿瘤疫苗使用肿瘤新抗原(neoantigen),即肿瘤的突变分子,如KRAS突变等,它们只存在于肿瘤细胞中,正常组织中没有表达,能够提高对肿瘤细胞的特异性。而最新的个性化疫苗通过对病人肿瘤样本测序后获得肿瘤新抗原信息,并针对最有价值的新抗原制定个性化治疗方案,实现精准医疗。目前,mRNA、多肽和DNA都可用于制备肿瘤疫苗,后文将讲述mRNA疫苗的优势。/pp 这里,我们对mRNA疫苗领域最大的三家公司——Moderna、BioNTech和CureVac进行比较介绍,并着重讲述在肿瘤疫苗方面的进展,由此展开对整个行业的展望。/pp strongModerna/strong/ppstrong 1.公司简介/strong/pp Moderna Therapeutics成立于2010年,总部位于美国马塞诸塞州剑桥市,公司雇员500余人。公司首席执行官Sté phane Bancel 2011年加盟,寻求了大量融资,为公司迅猛发展功不可没。/pp 2010年,Moderna的创始人之一Rossi发明了一种利用修饰的mRNA制作干细胞的方法。基于这项技术的巨大潜能,Rossi等人创立了Moderna。但使用非天然核糖核酸合成RNA的方法已有专利限制, Moderna的首要任务就是尝试新的RNA合成方法,避开专利限制。经过大量的尝试之后,Moderna开发了用1-甲基假尿嘧啶合成mRNA的方法。此后,Moderna又陆续开发了一系列新的mRNA合成修饰技术。/pp Moderna公司是RNA领域炙手可热的新星,该公司自2013与阿斯利康签订2.4亿美元的技术合作之后,又与Alexion Pharmaceuticals(亚力兄制药)、默克等制药公司签订技术合作,以及风险投资等融资方式,获得近20亿美元资金用于技术开发与临床研究,span style="color: rgb(255, 0, 0) "创下3年内融资14.25亿美金的全球生物医药领域私募股权融资的最高纪录。/span而这些在相当程度上得益于Moderna的CEO Sté phane Bancel,他在融资和资本运作上有相当出色的能力。/ppstrong 2. 产品线/strong/pp 该公司成立之后的相当长一段时间内都保持神秘,直到2017年1月才首次公布其产品线。该公司有四个不同研究方向的子公司: strongValera /strong(感染性疾病), strongOnkaido/strong (肿瘤免疫治疗), strongCaperna/strong (个体化肿瘤疫苗),及strong Elpidera/strong (罕见病),各子公司均以mRNA技术平台作为药物开发的基础。/pp Moderna已有包括肿瘤免疫、心血管疾病、肝病、治疗传染病和传染病疫苗的丰富的产品线。/pp style="text-align: center "img width="555" height="246" title="微信图片_20180807094627.jpg" style="width: 461px height: 147px float: none " src="http://img1.17img.cn/17img/images/201808/insimg/4ce7799f-6304-43e8-9d77-33936167c0e0.jpg"//pp style="text-align: center "img width="553" height="297" title="微信图片_20180807094622.jpg" style="width: 463px height: 173px float: none " src="http://img1.17img.cn/17img/images/201808/insimg/4982c9a8-bdcb-400a-9e6e-ad2a2d782ee7.jpg"//pp style="text-align: center "img width="556" height="96" title="微信图片_20180807094613.jpg" style="width: 465px height: 67px float: none " src="http://img1.17img.cn/17img/images/201808/insimg/7462e2f3-3de5-4a39-8d53-1dcd6e42f0e6.jpg"//ppbr//pp style="text-align: center "img width="556" height="392" title="微信图片_20180807094610.jpg" style="width: 464px height: 185px float: none " src="http://img1.17img.cn/17img/images/201808/insimg/58e651d6-5e63-4c5f-b8d0-f1e498cd4dc3.jpg"//pp style="text-align: center " span style="font-size: 14px "Moderna公司产品线/span/pp span style="color: rgb(255, 0, 0) "mRNA-4157是个性化肿瘤疫苗,/span于2017年11月开始I期临床试验。mRNA-5671是靶向Ras突变的肿瘤疫苗,该项目是目前唯一公布的KRAS RNA疫苗,span style="color: rgb(255, 0, 0) "2018年5月3日,该项目获得Merck 1.25亿美元的投资。/span/pp strong 3. 递送技术与专利/strong/pp Moderna采用脂质体纳米粒(LNP)递送技术,可以较好地维持RNA的稳定性。Moderna在Ras突变体序列、RNA结构元件和制剂等方面都有专利布局。/pp strongBioNTech/strong/ppstrong 1. 公司简介/strong/pp BioNTech是一家德国生物技术公司,成立于2008年,员工650人。其创始人Ugur Sahin是德国美因茨大学的教授,也是Ganymed的创始人和Claudin 18.2抗体的研究发起者。/pp strong 2. 技术平台与产品线/strong/pp BioNTech主要研发mRNA肿瘤治疗性疫苗,也有 CAR-T细胞治疗、双特异抗体及小分子药物项目。BioNTech于2017年在《Nature》上发表的个性化肿瘤疫苗的良好疗效引起一时轰动span style="color: rgb(255, 192, 0) "[1]span style="color: rgb(0, 0, 0) "。/span/span/pp style="text-align: center "img width="555" height="259" title="微信图片_20180807094606.jpg" style="width: 478px height: 195px " src="http://img1.17img.cn/17img/images/201808/insimg/39834cc4-b86b-4b6f-af62-eb60e3ac6ca5.jpg"//pp style="text-align: center " span style="font-size: 14px "BioNTech公司产品线/span/pp BioNTech在肿瘤疫苗方面有3种mRNA药物平台:①FixVAC® 是多种肿瘤相关抗原混合的肿瘤疫苗,不具有个性化 ②RNA-Warehouse是制作好包含多种抗原的疫苗库,鉴定病人的肿瘤特异性抗原后,选取对应抗原的疫苗治疗,有一定的个性化性质 ③IVAC® -Mutanome是通过测序得到病人所有的肿瘤特异性抗原,然后以此制定个性化的疫苗方案,再合成表达相应蛋白的mRNA作为疫苗,是个性化程度最高的疫苗,该类疫苗去年在临床试验中取得非常好的结果span style="color: rgb(255, 192, 0) "[1]span style="color: rgb(0, 0, 0) "。/span/spanspan style="color: rgb(255, 0, 0) "这3个平台产品的个性化程度越来越高。/span/pp style="text-align: center "img width="419" height="282" title="微信图片_20180807094601.jpg" style="width: 473px height: 253px " src="http://img1.17img.cn/17img/images/201808/insimg/c0bdd319-0890-43ff-a5c2-0e7178d6ea5f.jpg"//pp style="text-align: center " span style="font-size: 14px "BioNTech的3个mRNA疫苗平台,个性化程度依次增加/span/pp BioNTech还有通过RNA编码双特异抗体的技术平台DuoBody® ,该类RNA采用静脉注射给药,在体内表达双特异性抗体分子,目前处于临床前研究阶段。动物体内实验数据表明RNA分子能够在体内有效表达双特异抗体分子,并且有效抑制肿瘤的活性,结果于2017年发表在《Nature》上[span style="color: rgb(255, 192, 0) "2]span style="color: rgb(0, 0, 0) "。/span/span该平台选择了CD3× CLDN6,CLDN18.2× CD3,EpCAM× CD3等分子组合作为靶点。/pp BioNTech还有CAR-T细胞治疗和小分子药物的技术平台,但具体技术和靶点没有公布。/pp strong 3. 制剂与专利/strong/pp span style="color: rgb(255, 0, 0) "BioNTech采用的脂质体运载Lipoplexes(LPX)技术很先进,可以很好地稳定mRNA。/spanBioNTech在RNA结构元件和制剂等方面布局了一系列专利。/pp strongCureVac/strong/ppstrong 1. 公司简介/strong/pp CureVac由Ingmar Hoerr博士于2000年创立,专注于RNA药物的研发与产业化。CureVac总部位于德国T?bingen,有将近400名员工,已成为RNA制药行业的领军企业,是全球首家建立符合GMP标准的RNA生产线的公司。/pp strong 2. 技术平台与产品线/strong/pp CureVac有4种RNA技术平台:RNActive、RNArt、RNAntibody和RNAdjuvant。/pp 1)RNActive是编码抗原的mRNA疫苗。在肿瘤治疗领域,通过mRNA编码多种常见的肿瘤相关抗原,激活免疫系统攻击肿瘤细胞。在研项目有肿瘤治疗性疫苗CV9202。该平台还有用于预防病毒感染的疫苗,如预防狂犬病、流感和HIV感染的疫苗。/pp 2)RNArt是编码蛋白的RNA,可以补充或替换原来细胞中的蛋白,目前有一个用于治疗浅表肿瘤的项目处于临床前研究阶段。/pp 3)RNAtibody是编码抗体的RNA,与BioNTech的技术类似,但CureVac的在研项目应是编码单抗而不是双抗。span style="color: rgb(255, 0, 0) "细胞内表达的抗体可以靶向胞内的蛋白,阻断蛋白之间的相互作用,这是目前的抗体药物无法做到的。/spanRNA在细胞内编码的蛋白有人体的翻译后修饰,更易于制备多种抗体的混合物,有更好的药代动力学,可以保持高AUC,能持续、稳定地产生抗体。再者,用RNA生产抗体更简单、快速,CMC工艺稳定性更好。/pp 4)RNAdjuvant是促进免疫反应的Long non-coding RNA。用于激活免疫反应。/pp 基于以上四大技术平台,CureVac有丰富的产品线,主要分为3个大类,包括肿瘤治疗,预防病毒感染和基于RNA的分子治疗。/pp style="text-align: center "img width="555" height="593" title="微信图片_20180807094555.jpg" style="width: 494px height: 359px " src="http://img1.17img.cn/17img/images/201808/insimg/8fc7be8c-a29a-4f36-8270-331582db0f97.jpg"//pp style="text-align: center " span style="font-size: 14px "CureVac公司产品线/span/pp CureVac肿瘤方面的在研产品进展最快的是肿瘤疫苗CV9202和免疫佐剂CV8102。/pp CV9202是编码NY-ESO-1,MAGE-C2,MAGE-C1,Survivin,5T4,MUC1等常见肿瘤相关抗原的RNA混合物,通过激活免疫反应治疗肿瘤。值得注意的是CureVac之前有类似的编码PSA,PSMA,PSCA,STEAP,ACPP,MUC1等肿瘤相关抗原的肿瘤疫苗项目CV9104,已由于临床II期试验疗效不佳而终止研发。/pp CV8102是由长非编码RNA制成的免疫佐剂。该药物通过瘤内注射给药,刺激TLR 7,8和RIG-I等先天免疫信号通路,激活免疫反应。与免疫检查点抑制剂如PD-1抗体联用有协同效应。/pp strong 3. 制剂和专利/strong/pp CureVac最初使用鱼精蛋白制剂技术,这种制剂对RNA的保护较弱,不是理想的制剂。后来CureVac与Acuitas Therapeutics合作,使用其LNP制剂技术代替原来的鱼精蛋白制剂技术,可以使疫苗激活的免疫反应提高约10倍。/pp span style="color: rgb(255, 192, 0) "三大公司比较/span/pp strong1. 产品线比较/strong/pp 在肿瘤疫苗方面,span style="color: rgb(255, 0, 0) "BioNTech的产品最全面/span,覆盖肿瘤相关抗原疫苗(FixVAC® )、半个性化疫苗(RNA-Warehouse)和个性化疫苗(IVAC® -Mutanome),span style="color: rgb(255, 0, 0) "且其个性化疫苗进展最快/span。Moderna的疫苗包括个性化疫苗和肿瘤新抗原KRAS突变疫苗。CureVac的肿瘤疫苗都是肿瘤相关抗原疫苗,相对更为保守。/pp strong 2. 制剂技术比较/strong/pp 制剂技术是mRNA制药的核心技术与门槛之一。BioNTech采用的LPX技术可以很好地稳定RNA,并且制剂自身应有免疫佐剂的作用,是很好的制剂技术。Moderna和CureVac现在使用的LNP制剂技术也能稳定RNA。值得一提的是CureVac此前采用的鱼精蛋白制剂并不能很好地保护RNA,因此他们与Acuitas Therapeutics合作获得了LNP技术,并更换了以前许多产品的制剂。/pp strong 3. 专利布局比较/strong/pp 专利方面,BioNTech对UTR序列和3’ poly(A)n尾等RNA结构元件进行了专利保护,Moderna则有一系列专利保护RNA核苷酸的修饰方式。BioNTech和Moderna都有一系列制剂专利,包括纳米脂质体和阳离子试剂等。/pp strong4. 生产工艺/strong/pp RNA的生产比较简单,核酸药物虽然归属于生物制品,但其通过合成制备,因此在生产上兼具大分子和小分子药物的特性。通常治疗所需mRNA的量很低,通过高通量合成可以轻松制备,但纯度检测是一大挑战,常见的杂质包括模板DNA和合成不完全的RNA等。目前FDA和ICH还没有专门对于核酸药物质量的期望和标准,在国内外都是暂行参照基因治疗的相关规定进行申报。/pp 三家公司作为专业的mRNA制药公司,在生产上都有成熟的体系,建立了符合GMP标准的mRNA生产线。CureVac更是于2006年就建立了全球首个GMPmRNA生产线。最近,这几大公司都在扩建mRNA生产规模,以满足更大的临床需求。/pp span style="color: rgb(255, 192, 0) "mRNA药物发展前景/span/pp mRNA作为新技术药物,具有一些原有药物种类不具备的优势。mRNA翻译快速,会在体内自动降解,并且本身也有激活免疫反应的作用,再者,其易于改造插入基因片段。同时,mRNA还生产简单,合成快速,成本较低。mRNA相较于DNA的优势在于不局限于分裂细胞,没有整合宿主基因组的风险,且起效更快。多肽也是制作疫苗的一种选择,但其抗原呈递受到MHC单倍型的限制,且半衰期较短。对于制作个性化疫苗,mRNA的快速合成的特性使其成为节约时间非常合适的选择。除了用作疫苗,mRNA药物也可作为蛋白补充或替代疗法,治疗其他多种疾病。在解决mRNA的稳定性和递送问题后,它已成为一种非常理想的药物形式,表现出其独特的优势。/pp 个性化疫苗技术的日趋成熟也使mRNA药物炙手可热。个性化疫苗是一种高度定制的精准医疗方法,特别适用于癌症这种异质性极高的疾病。个性化疫苗涉及多个领域,需要整合不同的资源,诸如测序、分析、药物快速合成和医院的资源。随着近年来测序和分析技术的快速发展与成本降低,个性化疫苗的研发也迅速兴起。去年发表的个性化疫苗临床试验的良好疗效使mRNA疫苗形势大好。/pp 然而,该领域的技术门槛较高,有经验者极少,不仅要解决mRNA的稳定性和递送问题,还要建立一套完整的检测分析、质控和验证方案,并与CDE充分沟通。目前国内只有屈指可数的如上海斯微和江苏健安等企业在进行mRNA药物的研发,较高的风险与较低的成熟度使大多数企业望而却步。/pp span style="color: rgb(255, 192, 0) "总体而言,mRNA药物已进入发展的黄金时期,具有广阔的前景,是一个值得投入期望的领域。/span/ppspan style="color: rgb(255, 192, 0) " 参考文献:/span/pp 1. Sahin, U. et al. Personalized RNA mutanome vaccines mobilize poly-specifictherapeutic immunity against cancer. Nature547, 222-226 (2017)./pp 2. Stadler,C.R. et al. Elimination of largetumors in mice by mRNA-encoded bispecific antibodies. Nat Med 23, 815-817(2017)./pp style="text-align: right "span style="font-size: 12px "作者 l 悟行 编辑 l 细胞房间/span/ppspan style="font-size: 14px " /span/p