食品中苯甲酸山梨酸糖精钠检测加甲酸使峰分开是什么原理?望老师不吝赐教
在做国标 GB5009. 28 — 2016 食品安全国家标准食品中苯甲酸、山梨酸和糖精钠的测定对照品配制疑惑 标准溶液配制:苯甲酸、山梨酸和糖精钠(以糖精计)标准储备溶液( 1000mg / L ):分别准确称取苯甲酸钠、山梨酸钾和糖精钠 0.118g 、 0. 134g 和 0.117g (精确到 0.0001g ),用水溶解并分别定容至 100mL 。于 4℃贮存,保存期为 6 个月。当使用苯甲酸和山梨酸标准品时,需要用甲醇溶解并定容。红色这句话的意思是想用适量的甲醇溶解,然后在用水定容,还是用甲醇定容,感觉怪怪的?有那位老师可以指导一下, 共享一下经验,谢谢。
苯甲酸、山梨酸、糖精钠是最常见的食品添加剂,在液相色谱柱的标准出峰顺序是苯甲酸、山梨酸、糖精钠,通过改变流动相的比例可不可以对出峰顺序及分离度造成影响?
苯甲酸、山梨酸、糖精钠是衡量食品卫生质量的重要指标,苯甲酸、山梨酸的检测参照GB/T5009.29-1996,糖精钠的检测参照GB/T 5009.28-1996,即可开展实验。苯甲酸、山梨酸、糖精钠虽是较常见的检测项目,但是要得到一个准确可靠的结果,也存在一定的难度,许多新手常出现因对方法理解发生偏差而检测出错的事故。笔者根据自己多年该方面工作的实际经验出发,以苯甲酸、山梨酸为着重点,从样品前处理、检测仪器的选择、超标时的判断等几个易出问题的方面,进行了详细的阐述。2 样品前处理的注意事项 GB/T5009.28-1996和GB/T5009.29-1996 在文字结构上有缺陷,在涉及用仪器法测定苯甲酸、山梨酸、糖精钠时,只讲述了液体样品的前处理方法,没有涉及对固体样品的前处理。食品样品往往含有大量的油脂、蛋白质,对提取极为不利;如处理不干净也会污染色谱柱,影响检测工作。这类样品处理的关键在于如何找到一种较理想的沉淀剂,尽量排除待测样品中的油脂、蛋白质,且不影响待测物组分的回收率。GB/T5009.29-1996使用5%硫酸铜溶液沉淀蛋白,对于蛋白质含量较低的食品尚可,对于豆粉、奶粉、月饼等高油脂、高蛋白样品则沉淀效果不理想。如用10%钨酸钠溶液作为沉淀剂,效果好些;如用10%亚铁氰化钾溶液和20%醋酸锌溶液则效果更理想(这是笔者目前用过最理想的沉淀剂)。具体操作步骤如下:取一定量样品,捣碎,利用四分法原理称取样品5.0 克于50ml比色管中,加水20ml,浸泡、振荡均匀,加入氢氧化钠溶液(1mol/L)1.0 ml,加入9.5mL10%亚铁氰化钾溶液, 9.50mL 20%乙酸锌溶液,定容,振荡使其充分混匀后,用滤纸初滤除去沉淀物, 初滤液过0.45μm微孔滤膜,收集滤液于样品瓶中,样品处理液和标准有溶液各进样5uL测定。用这种方法简单易行,接触有机试剂少,重复性和回收率都令人满意;缺点是一定要用液相色谱法检测,有一定局限。3 检测仪器的选择虽然液相色谱仪操作起来比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]要复杂,但笔者建议如条件许可仍尽量用液相色谱法检测。原因如下:3.1 液相色谱法所用的样品处理方法远比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法简单,且不需使用有机试剂。尤其对于高油脂样品(如月饼)若采用碱化-排油-酸化-提取-挥干-溶解等步骤,再上[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]检测,工作量大,试剂毒性也大,且结果由于处理步骤太多而难以保证准确。3.2 用液相色谱法还可同时完成糖精钠项目的检测,而[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法只能做苯甲酸、山梨酸的检测。3.3 液相色谱仪所用的紫外检测器比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]的氢火焰检测器灵敏,可进行更低含量的检测。如用二极管阵列检测器,还可辅助定性,这更是[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]氢火焰检测器不可比拟的。4 选用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]时的注意事项 GB/T5009.29-1996所用的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]柱为 5%DEGS+1%磷酸固定液的60-80目 Chromosorb W AW,。这种柱有性能稳定、重复性好、保留时间稳定的优点,但同时也有稳定时间较长的缺点。该柱的适用的样品提取溶剂为石油醚或乙醚,如果用甲醇或乙醇,则溶剂峰拖尾效应较大,对山梨酸的测定有影响。如用毛细管柱,能取得更好的峰形和灵敏度,但其稳定性及特异性不如填充柱。一般可用非极性毛细管柱,0.530mm内径,10-15m长度。色谱条件可能需用程序升温。在[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]上的出峰次序为先出山梨酸,后出苯甲酸。糖精钠不能直接用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]进行检测,必须衍生化后才能汽化进样。5 选用液相色谱仪的注意事项 按照GB/T5009.29-1996,流动相应为5:95的甲醇:0.02M醋酸铵溶液,但是这个比例仅是个参考值,我们在工作中应根据实际情况进行调节。 为什么用甲醇溶液?甲醇有两个作用,(1)防腐,液相色谱柱最怕流动相长菌,尤其霉菌。甲醇可使蛋白质变性,有杀菌作用。(2)调节流动相极性,这是最重要的一点。甲醇在溶液中比例的较小变化都会使苯甲酸、山梨酸、糖精钠的保留时间发生明显的改变,因此可以通过改变流动相中甲醇含量,以调节这几个组分的出峰和分离,以得到较理想的色谱图。5:95是一个通用的比例,如减少甲醇含量,苯甲酸、山梨酸、糖精钠的出峰时间变慢,扩散效应增大,峰形较差,但这三组分的分离情况较好。如增加甲醇含量,苯甲酸、山梨酸、糖精钠的出峰时间提前,扩散效应较小,峰形尖锐,但这三组分的分离情况可能受影响,产生重叠。在选择条件时,只能通过实验手段,如配制3:97,4:96,5:95,6:96,7:93的流动相,综合考虑分离效果和分离时间选择最佳比例。不同柱的最适比例不同,举例来说,色谱科公司的液相柱最适比例为4:96,而岛津公司液相柱的最佳比例为7:93。就是同一根柱,一年前和一年后的极性也会有变化,需调节溶液配比。为什么使用0.02M醋酸铵溶液?加入醋酸铵是为了调节离子强度,使待测物的峰形不致于变坏。如果单独检测苯甲酸和糖精钠,加不加醋酸铵没有什么关系,都可以得到较好的峰形;但是检测山梨酸时流动相一定要加醋酸铵,否则得不到一个完整的色谱峰,峰形呈破裂状。醋酸铵溶液浓度不需严格控制,0.01M、0.02M、0.04M均可。苯甲酸、山梨酸、糖精钠在液相上的出峰次序很有特点。在流动相5:95及以下比例时,次序是苯甲酸、山梨酸、糖精钠(注意一下[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]的出峰次序),逐步增大甲醇含量,苯甲酸、山梨酸的出峰时间逐步提前,而糖精钠是出峰时间迅速提前,随着甲醇比例的逐步增大(15%-30%),原先在最后出峰的糖精钠集次和前面的山梨酸、山梨酸重叠,并位于最前面,其次序变为糖精钠、苯甲酸、山梨酸。再提高甲醇浓度,次序不变。用高甲醇比例条件(甲醇15%以上)做出的三种标准物质色谱图峰形较好,出峰时间也较快,但做实际样品时干扰较大;因此建议尽量使用低甲醇比例条件(甲醇5%左右)。6 苯甲酸、山梨酸超标时的判断苯甲酸、山梨酸超标的样品较多,由于它们往往牵涉到一批货物是否合格,因此责任重大。由于该方法定量较准确,因此遇到超标样品时应将精力集中于定性方面。如同时有[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]和液相色谱仪,建议用这两种性质相差较大的仪器进行对照,如定量结果差不多,即可确认。如只有[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url],应利用其在填充柱保留时间稳定的特性,同时进五针标准液和五针样品液(注:峰面积应差不多,否则需对一方按比例稀释),如标准和样品液的保留时间相差时间超过1 秒,可认为不是。(如进针的技术不过关,请不要做此实验)如用液相色谱仪,当检测器为二极管阵列检测器时,根据保留时间和紫外吸收图结合定性,当只有紫外检测器时,改检测波长为220nm,230nm,250nm,重复进标准和样品液,由标准和样品在不同波长的峰高比值看是否吻合。如有微生物检测手段,可加样品于有菌培养基中,观察有无抑菌现象,如无抑菌现象则无防腐剂。不是很推荐用双柱法,因为有时柱极性相差不大,反而会影响最终判断。7 糖精钠超标时的判断当检测糖精钠超标时,除了采用二极管阵列检测器或波长验证,还可以利用糖精钠的荧光特性,用荧光检测器进行验证。荧光条件是激发波长为277nm,荧光波长为410nm。只有当用荧光检测器和用紫外检测器做出的定量结果相差不多,才可以判断为是。还有一个简单粗糙、却也行之有效的验证方法,即感官法。糖精钠是一种甜味剂,用舌头可以感觉到它的甜味,如果含量超标,一定能尝出来。8 标准溶液的配制贮存问题苯甲酸、山梨酸、糖精钠的标准溶液如用水、乙醇作基体,一般几个月后会严重降解,。如用甲醇溶解再放于冰箱冷冻层,可保持稳定一两年。因此推荐用甲醇作溶剂。在配制标准溶液时,初学者常犯的错误多为用甲醇溶解苯甲酸钠,用水溶解苯甲酸,晃了半天才发现怎么也不没溶解。应该用弱碱性水溶解苯甲酸钠、山梨酸钾,用甲醇溶解苯甲酸、山梨酸。9 苯甲酸、山梨酸的应用范围首先应注意到,并不是所有食品都需要加入防腐剂,只有那些富含营养物质,且需要长时间暴露于空气的才有这样的需要,否则对厂家来说会增加不必要的成本。酱油、酱料、咸菜、浓缩果汁等由于开封后不可能短期内吃完,月饼等需在货架上摆放,如不加防腐剂很快会发霉变质,有添加防腐剂的必要。而利乐装或易拉罐装的饮料由于很快可以食用完毕,即在细菌大量繁殖前己被消化了,因而没有添加的必要。苯甲酸、山梨酸如果要起到防腐的作用,含量就不能太低。如果我们检测样品时只有几个ppm的浓度,有可能是从原料中带来的或由其它添加剂转化来的,而不是厂家出于防腐目的加入的。苯甲酸、山梨酸也只是防腐剂中的两种。并不是所有需要加入防腐剂的食品都会添加苯甲酸、山梨酸,有可能使用防霉剂或其它种类的防腐剂,或自行规定需冷藏(如某些月饼)。因此有些食品检测不出也属正常。另外,我们应该比较清楚地理解苯甲酸与苯甲酸钠、山梨酸与山梨酸钾之间的关系。在食品中添加防腐剂通常以苯甲酸钠、山梨酸钾形式加入,它们不易汽化,易溶于水,但不溶于甲醇等有机试剂;而苯甲酸、山梨酸易汽化,易溶于有机试剂,但
大家做苯甲酸山梨酸糖精钠检测时超声频率和功率怎么选择的呢?
苯甲酸、山梨酸、糖精钠是衡量食品卫生质量的重要指标,苯甲酸、山梨酸的检测参照GB/T5009.29-1996,糖精钠的检测参照GB/T 5009.28-1996,即可开展实验。苯甲酸、山梨酸、糖精钠虽是较常见的检测项目,但是要得到一个准确可靠的结果,也存在一定的难度,许多新手常出现因对方法理解发生偏差而检测出错的事故。笔者根据自己多年该方面工作的实际经验出发,以苯甲酸、山梨酸为着重点,从样品前处理、检测仪器的选择、超标时的判断等几个易出问题的方面,进行了详细的阐述。2 样品前处理的注意事项 GB/T5009.28-1996和GB/T5009.29-1996 在文字结构上有缺陷,在涉及用仪器法测定苯甲酸、山梨酸、糖精钠时,只讲述了液体样品的前处理方法,没有涉及对固体样品的前处理。食品样品往往含有大量的油脂、蛋白质,对提取极为不利;如处理不干净也会污染色谱柱,影响检测工作。这类样品处理的关键在于如何找到一种较理想的沉淀剂,尽量排除待测样品中的油脂、蛋白质,且不影响待测物组分的回收率。GB/T5009.29-1996使用5%硫酸铜溶液沉淀蛋白,对于蛋白质含量较低的食品尚可,对于豆粉、奶粉、月饼等高油脂、高蛋白样品则沉淀效果不理想。如用10%钨酸钠溶液作为沉淀剂,效果好些;如用10%亚铁氰化钾溶液和20%醋酸锌溶液则效果更理想(这是笔者目前用过最理想的沉淀剂)。具体操作步骤如下:取一定量样品,捣碎,利用四分法原理称取样品5.0 克于50ml比色管中,加水20ml,浸泡、振荡均匀,加入氢氧化钠溶液(1mol/L)1.0 ml,加入9.5mL10%亚铁氰化钾溶液, 9.50mL 20%乙酸锌溶液,定容,振荡使其充分混匀后,用滤纸初滤除去沉淀物, 初滤液过0.45μm微孔滤膜,收集滤液于样品瓶中,样品处理液和标准有溶液各进样5uL测定。用这种方法简单易行,接触有机试剂少,重复性和回收率都令人满意;缺点是一定要用液相色谱法检测,有一定局限。3 检测仪器的选择虽然液相色谱仪操作起来比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]要复杂,但笔者建议如条件许可仍尽量用液相色谱法检测。原因如下:3.1 液相色谱法所用的样品处理方法远比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法简单,且不需使用有机试剂。尤其对于高油脂样品(如月饼)若采用碱化-排油-酸化-提取-挥干-溶解等步骤,再上[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]检测,工作量大,试剂毒性也大,且结果由于处理步骤太多而难以保证准确。3.2 用液相色谱法还可同时完成糖精钠项目的检测,而[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法只能做苯甲酸、山梨酸的检测。3.3 液相色谱仪所用的紫外检测器比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]的氢火焰检测器灵敏,可进行更低含量的检测。如用二极管阵列检测器,还可辅助定性,这更是[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]氢火焰检测器不可比拟的。4 选用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]时的注意事项 GB/T5009.29-1996所用的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]柱为 5%DEGS+1%磷酸固定液的60-80目 Chromosorb W AW,。这种柱有性能稳定、重复性好、保留时间稳定的优点,但同时也有稳定时间较长的缺点。该柱的适用的样品提取溶剂为石油醚或乙醚,如果用甲醇或乙醇,则溶剂峰拖尾效应较大,对山梨酸的测定有影响。如用毛细管柱,能取得更好的峰形和灵敏度,但其稳定性及特异性不如填充柱。一般可用非极性毛细管柱,0.530mm内径,10-15m长度。色谱条件可能需用程序升温。在[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]上的出峰次序为先出山梨酸,后出苯甲酸。糖精钠不能直接用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]进行检测,必须衍生化后才能汽化进样。5 选用液相色谱仪的注意事项 按照GB/T5009.29-1996,流动相应为5:95的甲醇:0.02M醋酸铵溶液,但是这个比例仅是个参考值,我们在工作中应根据实际情况进行调节。 为什么用甲醇溶液?甲醇有两个作用,(1)防腐,液相色谱柱最怕流动相长菌,尤其霉菌。甲醇可使蛋白质变性,有杀菌作用。(2)调节流动相极性,这是最重要的一点。甲醇在溶液中比例的较小变化都会使苯甲酸、山梨酸、糖精钠的保留时间发生明显的改变,因此可以通过改变流动相中甲醇含量,以调节这几个组分的出峰和分离,以得到较理想的色谱图。5:95是一个通用的比例,如减少甲醇含量,苯甲酸、山梨酸、糖精钠的出峰时间变慢,扩散效应增大,峰形较差,但这三组分的分离情况较好。如增加甲醇含量,苯甲酸、山梨酸、糖精钠的出峰时间提前,扩散效应较小,峰形尖锐,但这三组分的分离情况可能受影响,产生重叠。在选择条件时,只能通过实验手段,如配制3:97,4:96,5:95,6:96,7:93的流动相,综合考虑分离效果和分离时间选择最佳比例。不同柱的最适比例不同,举例来说,色谱科公司的液相柱最适比例为4:96,而岛津公司液相柱的最佳比例为7:93。就是同一根柱,一年前和一年后的极性也会有变化,需调节溶液配比。为什么使用0.02M醋酸铵溶液?加入醋酸铵是为了调节离子强度,使待测物的峰形不致于变坏。如果单独检测苯甲酸和糖精钠,加不加醋酸铵没有什么关系,都可以得到较好的峰形;但是检测山梨酸时流动相一定要加醋酸铵,否则得不到一个完整的色谱峰,峰形呈破裂状。醋酸铵溶液浓度不需严格控制,0.01M、0.02M、0.04M均可。苯甲酸、山梨酸、糖精钠在液相上的出峰次序很有特点。在流动相5:95及以下比例时,次序是苯甲酸、山梨酸、糖精钠(注意一下[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]的出峰次序),逐步增大甲醇含量,苯甲酸、山梨酸的出峰时间逐步提前,而糖精钠是出峰时间迅速提前,随着甲醇比例的逐步增大(15%-30%),原先在最后出峰的糖精钠集次和前面的山梨酸、山梨酸重叠,并位于最前面,其次序变为糖精钠、苯甲酸、山梨酸。再提高甲醇浓度,次序不变。用高甲醇比例条件(甲醇15%以上)做出的三种标准物质色谱图峰形较好,出峰时间也较快,但做实际样品时干扰较大;因此建议尽量使用低甲醇比例条件(甲醇5%左右)。6 苯甲酸、山梨酸超标时的判断苯甲酸、山梨酸超标的样品较多,由于它们往往牵涉到一批货物是否合格,因此责任重大。由于该方法定量较准确,因此遇到超标样品时应将精力集中于定性方面。如同时有[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]和液相色谱仪,建议用这两种性质相差较大的仪器进行对照,如定量结果差不多,即可确认。如只有[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url],应利用其在填充柱保留时间稳定的特性,同时进五针标准液和五针样品液(注:峰面积应差不多,否则需对一方按比例稀释),如标准和样品液的保留时间相差时间超过1 秒,可认为不是。(如进针的技术不过关,请不要做此实验)如用液相色谱仪,当检测器为二极管阵列检测器时,根据保留时间和紫外吸收图结合定性,当只有紫外检测器时,改检测波长为220nm,230nm,250nm,重复进标准和样品液,由标准和样品在不同波长的峰高比值看是否吻合。如有微生物检测手段,可加样品于有菌培养基中,观察有无抑菌现象,如无抑菌现象则无防腐剂。不是很推荐用双柱法,因为有时柱极性相差不大,反而会影响最终判断。7 糖精钠超标时的判断当检测糖精钠超标时,除了采用二极管阵列检测器或波长验证,还可以利用糖精钠的荧光特性,用荧光检测器进行验证。荧光条件是激发波长为277nm,荧光波长为410nm。只有当用荧光检测器和用紫外检测器做出的定量结果相差不多,才可以判断为是。还有一个简单粗糙、却也行之有效的验证方法,即感官法。糖精钠是一种甜味剂,用舌头可以感觉到它的甜味,如果含量超标,一定能尝出来。8 标准溶液的配制贮存问题苯甲酸、山梨酸、糖精钠的标准溶液如用水、乙醇作基体,一般几个月后会严重降解,。如用甲醇溶解再放于冰箱冷冻层,可保持稳定一两年。因此推荐用甲醇作溶剂。在配制标准溶液时,初学者常犯的错误多为用甲醇溶解苯甲酸钠,用水溶解苯甲酸,晃了半天才发现怎么也不没溶解。应该用弱碱性水溶解苯甲酸钠、山梨酸钾,用甲醇溶解苯甲酸、山梨酸。9 苯甲酸、山梨酸的应用范围首先应注意到,并不是所有食品都需要加入防腐剂,只有那些富含营养物质,且需要长时间暴露于空气的才有这样的需要,否则对厂家来说会增加不必要的成本。酱油、酱料、咸菜、浓缩果汁等由于开封后不可能短期内吃完,月饼等需在货架上摆放,如不加防腐剂很快会发霉变质,有添加防腐剂的必要。而利乐装或易拉罐装的饮料由于很快可以食用完毕,即在细菌大量繁殖前己被消化了,因而没有添加的必要。苯甲酸、山梨酸如果要起到防腐的作用,含量就不能太低。如果我们检测样品时只有几个ppm的浓度,有可能是从原料中带来的或由其它添加剂转化来的,而不是厂家出于防腐目的加入的。苯甲酸、山梨酸也只是防腐剂中的两种。并不是所有需要加入防腐剂的食品都会添加苯甲酸、山梨酸,有可能使用防霉剂或其它种类的防腐剂,或自行规定需冷藏(如某些月饼)。因此有些食品检测不出也属正常。另外,我们应

防腐剂是一类重要的食品添加剂,它延长了食品的贮存期和货架期,防止了有毒微生物的危害,对食品工业的发展发挥了巨大的作用。但是它在促进食品工业发展的同时,也在食品安全方面产生了巨大的隐患,影响了人们的身体健康。这就需要我们能够准确地测量食品中添加剂的含量。本文采用高效液相色谱发来测定,具有方法简单,灵敏度高的特点。关键词:高效液相 防腐剂1 仪器与药品伍丰LC-100等度系统。包括泵LC-100P,柱温箱LC-100 CO,检测器UV-100Arcus 5 自动进样器等。超声波清洗机,PH计,电子天平。苯甲酸、山梨酸、糖精钠对照品(中国药品生物制品检定所)市售雪碧甲醇为HPLC级,醋酸铵为分析纯2 分析条件仪器: LC-100高效液相色谱仪色谱柱: Athena C18, 4.6*250mm, 5um流动相: A:B=5:95A: 甲醇 B: 醋酸铵水溶液(称量1.54g乙酸铵溶于1L水中)流速: 1mL/min检测波长:230nm进样量: 10uL柱温: 28℃ 3 样品处理对照品溶液:分别将苯甲酸,山梨酸,糖精钠标准品配成1mg/mL的溶液。然后分别用甲醇将苯甲酸钠,山梨酸钾溶液稀释成0.32mg/mL,0.16mg/mL,0.08mg/mL,0.04mg/mL,0.02mg/mL的溶液。糖精钠溶液用水稀释成0.32mg/mL,0.16mg/mL,0.08mg/mL,0.04mg/mL,0.02mg/mL的溶液。样品制备:称取雪碧10.003g,用水稀释至25mL,用1:1的氨水调PH至中性。用0.45um滤膜过滤后待用。4 实验步骤4.1 线性关系考察吸取上述对照品溶液各10 μL注入液相色谱仪,记录色谱图以及苯甲酸、山梨酸、糖精钠的峰面积。以三种物质的质量浓度对峰面积进行线性回归。结果表明,三种物质质量浓度0.02mg/mL-0.32 mg/mL范围内有良好的线性,线性相关系数r均大于0.999。 http://ng1.17img.cn/bbsfiles/images/2015/06/201506110937_549809_1635904_3.png 图1:苯甲酸校准曲线http://ng1.17img.cn/bbsfiles/images/2015/06/201506110937_549809_1635904_3.png 图2:山梨酸校准曲线http://ng1.17img.cn/bbsfiles/images/2015/06/201506110937_549810_1635904_3.png 图3:糖精钠校准曲线4.2 实际样品分析将上述配好的雪碧溶液吸取10 μL注入液相色谱仪记录色谱峰面积,使用外标法计算含量。测得市售雪碧中苯甲酸的含量为0.14g/kg。小于国家规定的0.2g/kg的标准。 http://ng1.17img.cn/bbsfiles/images/2015/06/201506110939_549811_1635904_3.png 图4:对照品谱图 http://ng1.17img.cn/bbsfiles/images/2015/06/201506110939_549812_1635904_3.png 图5:雪碧样品 5讨论与建议本方法对于市售雪碧中防腐剂做了相关实验,选取相关浓度的标准品对三种添加剂做标准曲线,线性范围良好,线性相关系数r大于0.999。根据标准曲线得出市售雪碧的苯甲酸含量,重复性好。数据表明,LC-100适合对食品中苯甲酸,山梨酸,糖精钠进行检测。该方法操作简单简单,分析时间短,专属性强。可以满足饮料中防腐剂测定。

防腐剂是一类重要的食品添加剂,它延长了食品的贮存期和货架期,防止了有毒微生物的危害,对食品工业的发展发挥了巨大的作用。但是它在促进食品工业发展的同时,也在食品安全方面产生了巨大的隐患,影响了人们的身体健康。这就需要我们能够准确地测量食品中添加剂的含量。本文采用高效液相色谱发来测定,具有方法简单,灵敏度高的特点。关键词:高效液相 防腐剂1 仪器与药品伍丰LC-100等度系统。包括泵LC-100P,柱温箱LC-100 CO,检测器UV-100Arcus 5 自动进样器等。超声波清洗机,PH计,电子天平。苯甲酸、山梨酸、糖精钠对照品(中国药品生物制品检定所)市售雪碧甲醇为HPLC级,醋酸铵为分析纯2 分析条件仪器: LC-100高效液相色谱仪色谱柱: Athena C18, 4.6*250mm, 5um流动相: A:B=5:95A: 甲醇 B: 醋酸铵水溶液(称量1.54g乙酸铵溶于1L水中)流速: 1mL/min检测波长:230nm进样量: 10uL柱温: 28℃ 3 样品处理对照品溶液:分别将苯甲酸,山梨酸,糖精钠标准品配成1mg/mL的溶液。然后分别用甲醇将苯甲酸钠,山梨酸钾溶液稀释成0.32mg/mL,0.16mg/mL,0.08mg/mL,0.04mg/mL,0.02mg/mL的溶液。糖精钠溶液用水稀释成0.32mg/mL,0.16mg/mL,0.08mg/mL,0.04mg/mL,0.02mg/mL的溶液。样品制备:称取雪碧10.003g,用水稀释至25mL,用1:1的氨水调PH至中性。用0.45um滤膜过滤后待用。4 实验步骤4.1 线性关系考察吸取上述对照品溶液各10 μL注入液相色谱仪,记录色谱图以及苯甲酸、山梨酸、糖精钠的峰面积。以三种物质的质量浓度对峰面积进行线性回归。结果表明,三种物质质量浓度0.02mg/mL-0.32 mg/mL范围内有良好的线性,线性相关系数r均大于0.999。http://ng1.17img.cn/bbsfiles/images/2015/08/201508200902_561638_1635904_3.jpg 图1:苯甲酸校准曲线http://ng1.17img.cn/bbsfiles/images/2015/06/201506110937_549809_1635904_3.png 图2:山梨酸校准曲线http://ng1.17img.cn/bbsfiles/images/2015/06/201506110937_549810_1635904_3.png 图3:糖精钠校准曲线4.2 实际样品分析将上述配好的雪碧溶液吸取10 μL注入液相色谱仪记录色谱峰面积,使用外标法计算含量。测得市售雪碧中苯甲酸的含量为0.14g/kg。小于国家规定的0.2g/kg的标准。 http://ng1.17img.cn/bbsfiles/images/2015/06/201506110939_549811_1635904_3.png 图4:对照品谱图 http://ng1.17img.cn/bbsfiles/images/2015/06/201506110939_549812_1635904_3.png 图5:雪碧样品 5讨论与建议本方法对于市售雪碧中防腐剂做了相关实验,选取相关浓度的标准品对三种添加剂做标准曲线,线性范围良好,线性相关系数r大于0.999。根据标准曲线得出市售雪碧的苯甲酸含量,重复性好。数据表明,LC-100适合对食品中苯甲酸,山梨酸,糖精钠进行检测。该方法操作简单简单,分析时间短,专属性强。可以满足饮料中防腐剂测定。
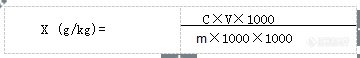
[align=center][b]食品中苯甲酸、山梨酸和糖精钠检测方法验证报告[/b][/align][align=center][b]GB 5009.28-2016(第一法)[/b][/align][align=center][b]李晓东[/b][/align]一、[b]方法概述1 范围[/b]本标准规定了食品中苯甲酸、山梨酸和糖精钠的测定方法。本标准适用于食品中苯甲酸、山梨酸和糖精钠的测定。[b]2 原理[/b]样品经水提取,高脂肪样品经正己烷脱脂、高蛋白样品经蛋白沉淀剂沉淀蛋白,采用液相色谱分离,紫外检测器检测,外标法定量。二、[b]仪器与试剂[/b]1.仪器1.1高效液相色谱仪:配有紫外检测器1.2分析天平:感量0.0001g和0.001g1.3匀浆机1.4恒温水浴锅1.5涡旋混合器1.6高速离心机:转速不低于8000r/min。1.7超声波发生器2. 试剂除非另有说明,本方法所有实际均为分析纯,水为GB/T 6682规定的一级水。2.1甲醇:色谱纯。2.2乙酸铵: 色谱纯。2.3甲酸:色谱级2.4氨水2.5亚铁氰化钾2.6无水乙醇2.7正己烷2.8氨水溶液:取1ml氨水加到99ml水中,混匀后备用。2.9亚铁氰化钾溶液(92g/L):称取106g亚铁氰化钾,加适量水溶解,用水定容至1L。2.9乙酸锌溶液(183g/L):称取220g乙酸锌溶于少量水中,加入30ml冰乙酸,用水定容至1L。2.10乙酸铵溶液(20mmol/L):称取1.54g乙酸铵,加入适量水溶解后用水定容至1L,经0.22μm水相微孔滤膜过滤后备用。2.11甲酸-乙酸铵溶液(2mmol/L甲酸+20mmol/L乙酸铵):称取1.54g乙酸铵,加入适量水溶解,再加入75.2μl甲酸,用水定容至1L,经0.22μm水相微孔滤膜过滤后备用。3. 材料3.1水相微孔滤膜3.2塑料离心管二、样品的制备与保存取多个预包装的饮料、液态奶等均匀样品直接混合;非均匀的液态、半固态样品用组织匀浆机匀浆;固体样品用研磨机充分粉碎并搅拌均匀;奶酪、黄油、巧克力等采用50℃~60℃加热熔融,并趁热充分搅拌均匀。取其中200g装入玻璃容器中,密封,液体试样于4℃保存,其他试样于-18℃保存。三、分析步骤3.1、标准曲线绘制3.1.1苯甲酸:纯度≥99.0%或经国家认证并授予标准物质证书的标准物质。3.1.2山梨酸:纯度≥99.0%或经国家认证并授予标准物质证书的标准物质。3.1.3糖精钠:纯度≥99%或经国家认证并授予标准物质证书的标准物质。3.1.4标准储备液:分别准确称取苯甲酸、山梨酸和糖精钠0.118g、0.134g和0.117g(精确到0.0001g),用水溶解并分别定容至100ml。此储备液各浓度为1000μg/ml。储备液于4℃贮存,保存期为6个月。当使用苯甲酸和山梨酸标准品时,需用甲醇溶解并定容。3.1.5标准混合中间液:分别取苯甲酸、山梨酸和糖精钠标准储备液各10.0ml于50ml容量瓶中,用水定容。于4℃贮存,保质期为3个月。3.1.6标准工作液:量取标准混合中间液适量,用水稀释成浓度为0.1μg/mL、0.2μg/mL、0.5μg/mL、1.0μg/mL、5.0μg/mL、10.0μg/mL、25.0μg/mL、50.0μg/mL标准工作液。(临用现配)3.1.7微孔滤膜:孔径0.22μm,有机相。3.2 样品的处理3.2.1含有胶基的果冻糖果等样品:称取2g样品(精确到0.001g)于50ml具塞离心管中,加25mL水,置50℃水浴中加热溶解,取出后趁热超声20min, 冷却至室温,取出加入2ml亚铁氰化钾溶液,摇匀,再加2ml乙酸锌溶液,于8000r/min离心机中离心5min,[u] [/u]取上清液于50mL容量瓶中,再加水20mL混匀后再超声5min后于8000r/min离心机中离心5min后合并上清液后再定容至刻度,上清液经0.22μm滤膜过滤,待测。3.2.2奶油、油脂、巧克力、奶油、油炸食品类样品:称取2g样品(精确到0.001g)于50mL具塞离心管中,加入10mL正己烷,置60℃水浴加热约5min,并不时轻摇以溶解脂肪,然后加25mL氨水溶液(1+99)1mL乙醇,涡旋混匀,于50℃水浴超声20min,冷却至室温后,加2ml亚铁氰化钾溶液,摇匀,再加入2ml乙酸锌溶液,于8000r/min离心机中离心5min,弃去有机相,水相转移至50mL容量瓶中,再加水20mL混匀后再超声5min,[u] [/u]后于8000r/min离心机中离心5min后合并上清液后再定容至刻度,上清液经0.22μm滤膜过滤,待测。3.2.3一般试样:称取2g样品(精确到0.001g)于于50mL离心管中加水25mL,在 50℃超声振荡提取20min后冷却至室温,取出加入2ml亚铁氰化钾溶液,摇匀,再加入2ml乙酸锌溶液,于8000r/min离心机中离心5min取上清液于50mL容量瓶中,再加水20mL混匀后再超声5min后于8000r/min离心机中离心[u] [/u]后合并上清液后再定容至刻度,上清液经0.22μm滤膜过滤,待测。3.3仪器测定条件3.3.1色谱柱:C18柱, 250mm×4.6mm,5μm,或相当者。3.3.2流动相:甲醇+乙酸铵溶液=5+95。3.3.3流速:1.0ml/min3.3.4波长:230nm3.3.5进样量:10μl(注:当存在干扰峰或需要辅助定性时,可以采用加入甲酸的流动相来测定,甲醇+甲酸-乙酸铵=8+92)四、[b]结果处理[/b][align=center][img=,360,58]http://ng1.17img.cn/bbsfiles/images/2018/07/201807281443198332_5739_2904018_3.png!w360x58.jpg[/img][/align][b]结果表述: [/b]式中:X -试样中各组分的含量,(g/kg); m-样品的质量,(g);[i] C[/i]-标准品的浓度,(μg/mL); V-样品最终定容体积,(mL)。五、验证结果1.线性结果A.将标准系列工作溶液分别注入液相色谱仪中, 测定相应的峰面积,以混合标准系列工作溶液的质量浓度为横坐标,以峰面积为纵坐标,绘制标准曲线。[u]苯甲酸 Y=34718.4*X-2258.22 R^2=0.9999618[/u][align=center][img=,690,421]http://ng1.17img.cn/bbsfiles/images/2018/07/201807281443357931_814_2904018_3.png!w690x421.jpg[/img] [/align][align=center]表1 苯甲酸标准系列试验结果[/align][table][tr][td](μg/mL)[/td][td][align=center]0.1[/align][/td][td][align=center]0.2[/align][/td][td][align=center]0.5[/align][/td][td][align=center]1.0[/align][/td][td][align=center]5.0[/align][/td][td][align=center]10.0[/align][/td][td][align=center]25.0[/align][/td][td][align=center]50.0[/align][/td][/tr][tr][td][align=center]A[/align][/td][td][align=center]3192[/align][/td][td][align=center]6472[/align][/td][td][align=center]15547[/align][/td][td][align=center]30792[/align][/td][td][align=center]171991[/align][/td][td][align=center]346341[/align][/td][td][align=center]857154[/align][/td][td][align=center]1737605[/align][/td][/tr][/table] 以上结果表明苯甲酸在0.1μg/mL ~50.0μg/mL范围内,R=0.9999809,吸光值与浓度呈线性关系,线性良好,符合要求。B.将标准系列工作溶液分别注入液相色谱仪中, 测定相应的峰面积,以混合标准系列工作溶液的质量浓度为横坐标,以峰面积为纵坐标,绘制标准曲线。[u]山梨酸 Y=58106.6*X-2551.27 R^2=0.9998775[/u][align=center][img=,690,424]http://ng1.17img.cn/bbsfiles/images/2018/07/201807281443489464_9593_2904018_3.png!w690x424.jpg[/img] [/align][align=center]表1 山梨酸标准系列试验结果[/align][table][tr][td](μg/mL)[/td][td][align=center]0.1[/align][/td][td][align=center]0.2[/align][/td][td][align=center]0.5[/align][/td][td][align=center]1.0[/align][/td][td][align=center]5.0[/align][/td][td][align=center]10.0[/align][/td][td][align=center]25.0[/align][/td][td][align=center]50.0[/align][/td][/tr][tr][td][align=center]A[/align][/td][td][align=center]6078[/align][/td][td][align=center]11004[/align][/td][td][align=center]27220[/align][/td][td][align=center]53019[/align][/td][td][align=center]266472[/align][/td][td][align=center]599121[/align][/td][td][align=center]1449933[/align][/td][td][align=center]2900929[/align][/td][/tr][/table] 以上结果表明山梨酸在0.1μg/mL ~50.0μg/mL范围内,R=0.9999387,吸光值与浓度呈线性关系,线性良好,符合要求。C.将标准系列工作溶液分别注入液相色谱仪中, 测定相应的峰面积,以混合标准系列工作溶液的质量浓度为横坐标,以峰面积为纵坐标,绘制标准曲线。[u]糖精钠 Y=28974.4*X-9635.15 R^2=0.9993261[/u][align=center][img=,690,429]http://ng1.17img.cn/bbsfiles/images/2018/07/201807281444024342_969_2904018_3.png!w690x429.jpg[/img] [/align][align=center]表1 糖精钠标准系列试验结果[/align][table][tr][td](μg/mL)[/td][td][align=center]0.1[/align][/td][td][align=center]0.2[/align][/td][td][align=center]0.5[/align][/td][td][align=center]1.0[/align][/td][td][align=center]5.0[/align][/td][td][align=center]10.0[/align][/td][td][align=center]25.0[/align][/td][td][align=center]50.0[/align][/td][/tr][tr][td][align=center]A[/align][/td][td][align=center]1855[/align][/td][td][align=center]4407[/align][/td][td][align=center]12203[/align][/td][td][align=center]25090[/align][/td][td][align=center]130262[/align][/td][td][align=center]261748[/align][/td][td][align=center]693650[/align][/td][td][align=center]1453554[/align][/td][/tr][/table] 以上结果表明糖精钠在0.1μg/mL ~50.0μg/mL范围内,R=0.9996630,吸光值与浓度呈线性关系,线性良好,符合要求。2.检出限结果A.将0.2μg/mL苯甲酸标准溶液逐级稀释至S/N=3±1,得出苯甲酸的方法检出限为 0.005mg/kg[color=#ff0000],[/color]此检出限结果满足条件。B..将0.2μg/mL苯甲酸标准溶液逐级稀释至S/N=3±1,得出山梨酸的方法检出限为 0.005mg/kg[color=#ff0000],[/color]此检出限结果满足条件。C.将0.2μg/mL苯甲酸标准溶液逐级稀释至S/N=3±1,得出苯甲酸的方法检出限为 0.005mg/kg[color=#ff0000],[/color]此检出限结果满足条件。[b]七、重复性测定[/b]A.对样品F1807000281进行7次进样,其苯甲酸测试值如下表所示:[table][tr][td][align=center]编号[/align][/td][td][align=center]m(g)[/align][/td][td]C(μg/ml)[/td][td]V(ml)[/td][td][align=center]X(mg/kg)[/align][/td][td][align=center]X[sub]平[/sub](mg/kg)[/align][/td][td][align=center]RSD(%)[/align][/td][/tr][tr][td][align=center]1[/align][/td][td][align=center]2.0223[/align][/td][td][align=center]6.02[/align][/td][td]50[/td][td]0.149[/td][td=1,7][align=center]0.149[/align][/td][td=1,7][align=center]0.10[/align][/td][/tr][tr][td][align=center]2[/align][/td][td][align=center]2.0237[/align][/td][td][align=center]6.023[/align][/td][td]50[/td][td]0.149[/td][/tr][tr][td][align=center]3[/align][/td][td][align=center]2.0186[/align][/td][td][align=center]6.002[/align][/td][td]50[/td][td]0.149[/td][/tr][tr][td][align=center]4[/align][/td][td][align=center]2.0212[/align][/td][td][align=center]6.012[/align][/td][td]50[/td][td]0.149[/td][/tr][tr][td][align=center]5[/align][/td][td][align=center]2.03264[/align][/td][td][align=center]6.033[/align][/td][td]50[/td][td]0.148[/td][/tr][tr][td][align=center]6[/align][/td][td][align=center]2.0201[/align][/td][td][align=center]6.007[/align][/td][td]50[/td][td]0.149[/td][/tr][tr][td][align=center]7[/align][/td][td][align=center]2.0195[/align][/td][td][align=center]6.004[/align][/td][td]50[/td][td]0.149[/td][/tr][/table]本方法的精密度为 0.10% ,符合《食品中苯甲酸、山梨酸和糖精钠测定方法》GB 5009.28-2016中给出的精密度要求。因此,本次测定均符合要求。B.对样品F1807000281进行7次进样,其山梨酸测试值如下表所示:[table][tr][td][align=center]编号[/align][/td][td][align=center]m(g)[/align][/td][td]C(μg/ml)[/td][td]V(ml)[/td][td][align=center]X(mg/kg)[/align][/td][td][align=center]X[sub]平[/sub](mg/kg)[/align][/td][td][align=center]RSD(%)[/align][/td][/tr][tr][td][align=center]1[/align][/td][td][align=center]2.0223[/align][/td][td][align=center]5.748[/align][/td][td]50[/td][td]0.142[/td][td=1,7][align=center]0.142[/align][/td][td=1,7][align=center]1.44[/align][/td][/tr][tr][td][align=center]2[/align][/td][td][align=center]2.0237[/align][/td][td][align=center]5.727[/align][/td][td]50[/td][td]0.141[/td][/tr][tr][td][align=center]3[/align][/td][td][align=center]2.0186[/align][/td][td][align=center]5.722[/align][/td][td]50[/td][td]0.142[/td][/tr][tr][td][align=center]4[/align][/td][td][align=center]2.0212[/align][/td][td][align=center]5.702[/align][/td][td]50[/td][td]0.141[/td][/tr][tr][td][align=center]5[/align][/td][td][align=center]2.03264[/align][/td][td][align=center]5.882[/align][/td][td]50[/td][td]0.145[/td][/tr][tr][td][align=center]6[/align][/td][td][align=center]2.0201[/align][/td][td][align=center]5.657[/align][/td][td]50[/td][td]0.14[/td][/tr][tr][td][align=center]7[/align][/td][td][align=center]2.0195[/align][/td][td][align=center]5.887[/align][/td][td]50[/td][td]0.146[/td][/tr][/table]本方法的精密度为 1.44% ,符合《食品中苯甲酸、山梨酸和糖精钠测定方法》GB 5009.28-2016中给出的精密度要求。因此,本次测定均符合要求。C.对样品F1807000281进行7次进样,其糖精钠测试值如下表所示:[table][tr][td][align=center]编号[/align][/td][td][align=center]m(g)[/align][/td][td]C(μg/ml)[/td][td]V(ml)[/td][td][align=center]X(mg/kg)[/align][/td][td][align=center]X[sub]平[/sub](mg/kg)[/align][/td][td][align=center]RSD(%)[/align][/td][/tr][tr][td][align=center]1[/align][/td][td][align=center]2.0223[/align][/td][td][align=center]5.891[/align][/td][td]50[/td][td]0.146[/td][td=1,7][align=center]0.145[/align][/td][td=1,7][align=center]0.64[/align][/td][/tr][tr][td][align=center]2[/align][/td][td][align=center]2.0237[/align][/td][td][align=center]5.882[/align][/td][td]50[/td][td]0.145[/td][/tr][tr][td][align=center]3[/align][/td][td][align=center]2.0186[/align][/td][td][align=center]5.887[/align][/td][td]50[/td][td]0.146[/td][/tr][tr][td][align=center]4[/align][/td][td][align=center]2.0212[/align][/td][td][align=center]5.857[/align][/td][td]50[/td][td]0.145[/td][/tr][tr][td][align=center]5[/align][/td][td][align=center]2.03264[/align][/td][td][align=center]5.85[/align][/td][td]50[/td][td]0.144[/td][/tr][tr][td][align=center]6[/align][/td][td][align=center]2.0201[/align][/td][td][align=center]5.821[/align][/td][td]50[/td][td]0.144[/td][/tr][tr][td][align=center]7[/align][/td][td][align=center]2.0195[/align][/td][td][align=center]5.793[/align][/td][td]50[/td][td]0.143[/td][/tr][/table]本方法的精密度为 0.64% ,符合《食品中苯甲酸、山梨酸和糖精钠测定方法》GB 5009.28-2016中给出的精密度要求。因此,本次测定均符合要求。[b]六、准确度验证(加标回收)[/b]A.对样品F1807000281加标,取苯甲酸浓度100 .0 μg/mL的标液 0.01mL、0.04mL和0.1ml同样品同步处理后,结果见下表[table][tr][td=2,1][align=center]测定编号[/align][/td][td=6,1]苯甲酸[/td][/tr][tr][td][align=center]序号[/align][/td][td][align=center]m(g)[/align][/td][td][align=center]V(mL)[/align][/td][td][align=center]C(μg/mL)[/align][/td][td][align=center]X(mg/kg)[/align][/td][td][align=center]X[sub]平[/sub](mg/kg)[/align][/td][td][align=center]加标量(mg/kg)[/align][/td][td][align=center]回收率%[/align][/td][/tr][tr][td][align=center]1#[/align][/td][td][align=center]2.0225[/align][/td][td][align=center]50[/align][/td][td][align=center]N.D[/align][/td][td][align=center]N.D[/align][/td][td=1,2][align=center]N.D[/align][/td][td][align=center]/[/align][/td][td][align=center]/[/align][/td][/tr][tr][td][align=center]2#[/align][/td][td][align=center]2.0236[/align][/td][td][align=center]50[/align][/td][td][align=center]N.D[/align][/td][td][align=center]N.D[/align][/td][td][align=center]/[/align][/td][td][align=center]/[/align][/td][/tr][tr][td][align=center]加标1#[/align][/td][td][align=center]2.0216[/align][/td][td][align=center]50[/align][/td][td][align=center]0.984[/align][/td][td][align=center]0.024[/align][/td][td][align=center]/[/align][/td][td][align=center]0.0247[/align][/td][td][align=center]98.4[/align][/td][/tr][tr][td][align=center]加标2#[/align][/td][td][align=center]2.0222[/align][/td][td][align=center]50[/align][/td][td][align=center]4.167[/align][/td][td][align=center]0.103[/align][/td][td][align=center]/[/align][/td][td][align=center]0.099[/align][/td][td][align=center]104[/align][/td][/tr][tr][td][align=center]加标3#[/align][/td][td][align=center]2.0307[/align][/td][td][align=center]50[/align][/td][td][align=center]9.931[/align][/td][td][align=center]0.245[/align][/td][td][align=center]/[/align][/td][td][align=center]0.246[/align][/td][td]99.6[/td][/tr][/table]由上表可以看出苯甲酸的加标回收范围在98.4%-104.0% ,RSD值为2.93%符合规定要求。B.对样品F1807000281加标,取苯甲酸浓度100 .0 μg/mL的标液 0.01mL、0.04mL和0.1ml同样品同步处理后,结果见下表[table][tr][td=2,1][align=center]测定编号[/align][/td][td=6,1]山梨酸[/td][/tr][tr][td][align=center]序号[/align][/td][td][align=center]m(g)[/align][/td][td][align=center]V(mL)[/align][/td][td][align=center]C(μg/mL)[/align][/td][td][align=center]X(mg/kg)[/align][/td][td][align=center]X[sub]平[/sub](mg/kg)[/align][/td][td][align=center]加标量(mg/kg)[/align][/td][td][align=center]回收率%[/align][/td][/tr][tr][td][align=center]1#[/align][/td][td][align=center]2.0225[/align][/td][td][align=center]50[/align][/td][td][align=center]N.D[/align][/td][td][align=center]N.D[/align][/td][td=1,2][align=center]N.D[/align][/td][td][align=center]/[/align][/td][td][align=center]/[/align][/td][/tr][tr][td][align=center]2#[/align][/td][td][align=center]2.0236[/align][/td][td][align=center]50[/align][/td][td][align=center]N.D[/align][/td][td][align=center]N.D[/align][/td][td][align=center]/[/align][/td][td][align=center]/[/align][/td][/tr][tr][td][align=center]加标1#[/align][/td][td][align=center]2.0216[/align][/td][td][align=center]50[/align][/td][td][align=center]0.982[/align][/td][td][align=center]0.0242[/align][/td][td][align=center]/[/align][/td][td][align=center]0.0247[/align][/td][td][align=center]98[/align][/td][/tr][tr][td][align=center]加标2#[/align][/td][td][align=center]2.0222[/align][/td][td][align=center]50[/align][/td][td][align=center]3.986[/align][/td][td][align=center]0.099[/align][/td][td][align=center]/[/align][/td][td][align=center]0.099[/align][/td][td][align=center]100[/align][/td][/tr][tr][td][align=center]加标3#[/align][/td][td][align=center]2.0307[/align][/td][td][align=center]50[/align][/td][td][align=center]9.196[/align][/td][td][align=center]0.226[/align][/td][td][align=center]/[/align][/td][td][align=center]0.246[/align][/td][td]91.9[/td][/tr][/table]由上表可以看出苯甲酸的加标回收范围在91.9%-100.0% ,RSD值为4.37%符合规定要求。C.对样品F1807000281加标,取苯甲酸浓度100 .0 μg/mL的标液 0.01mL、0.04mL和0.1ml同样品同步处理后,结果见下表[table][tr][td=2,1][align=center]测定编号[/align][/td][td=6,1]糖精钠[/td][/tr][tr][td][align=center]序号[/align][/td][td][align=center]m(g)[/align][/td][td][align=center]V(mL)[/align][/td][td][align=center]C(μg/mL)[/align][/td][td][align=center]X(mg/kg)[/align][/td][td][align=center]X[sub]平[/sub](mg/kg)[/align][/td][td][align=center]加标量(mg/kg)[/align][/td][td][align=center]回收率%[/align][/td][/tr][tr][td][align=center]1#[/align][/td][td][align=center]2.0225[/align][/td][td][align=center]50[/align][/td][td][align=center]N.D[/align][/td][td][align=center]N.D[/align][/td][td=1,2][align=center]N.D[/align][/td][td][align=center]/[/align][/td][td][align=center]/[/align][/td][/tr][tr][td][align=center]2#[/align][/td][td][align=center]2.0236[/align][/td][td][align=center]50[/align][/td][td][align=center]N.D[/align][/td][td][align=center]N.D[/align][/td][td][align=center]/[/align][/td][td][align=center]/[/align][/td][/tr][tr][td][align=center]加标1#[/align][/td][td][align=center]2.0216[/align][/td][td][align=center]50[/align][/td][td][align=center]0.95[/align][/td][td][align=center]0.0235[/align][/td][td][align=center]/[/align][/td][td][align=center]0.0247[/align][/td][td][align=center]95.1[/align][/td][/tr][tr][td][align=center]加标2#[/align][/td][td][align=center]2.0222[/align][/td][td][align=center]50[/align][/td][td][align=center]4.063[/align][/td][td][align=center]0.1[/align][/td][td][align=center]/[/align][/td][td][align=center]0.099[/align][/td][td][align=center]101[/align][/td][/tr][tr][td][align=center]加标3#[/align][/td][td][align=center]2.0307[/align][/td][td][align=center]50[/align][/td][td][align=center]9.398[/align][/td][td][align=center]0.231[/align][/td][td][align=center]/[/align][/td][td][align=center]0.246[/align][/td][td]93.9[/td][/tr][/table]由上表可以看出苯甲酸的加标回收范围在93.9%-101.0% ,RSD值为3.93%符合规定要求。七、总结本方法的检出限为0.005mg/kg。等于GB 5009.28-2016中给出的最低检出浓度0.005mg/kg。本方法的精密度分别为2.93%、4.37%和3.93%。符合《食品中苯甲酸、山梨酸和糖精钠的测定方法》GB 5009.28-2016中给出的精密度要求.通过对食品中苯甲酸、山梨酸和糖精钠的测定方法的检出限、精密度和准确度的评价,本方法测定食品中苯甲酸、山梨酸和糖精钠数据准确,结果可信。此方法的准确性好,测定结果真实可靠,可用于食品中苯甲酸、山梨酸和糖精钠的测定。
第九届原创离子色谱法测定饮料中的山梨酸、苯甲酸和糖精钠黄选忠 杜宏山 邹大喜(湖北兴山县疾病预防控制中心,443711)摘要 建立了用国产SH-AC-1型阴离子交换柱为分离柱,以1.5 mmol/LNa2CO3为淋洗液,流量为1.5mL/min,采用等度洗脱的方式测定食品中山梨酸、苯甲酸和糖精钠的方法,山梨酸、苯甲酸的线性范围为0~30.0mg/L,糖精钠的线性范围为0~15.0mg/L,方法应用于饮料等样品中山梨酸、苯甲酸和糖精钠的测定,其结果与气相色谱法相吻合,加标回收率分别为:97.9%~104.5%、96.3~100.9%和100.3%~104.5%,5次平行测定的相对标准偏差分别为:1.68%~3.92%、2.32~4.08%和2.02%~3.95%(n=5),按样品稀释50倍计方法的检出限分别3.5、2.5和1.5 mg/L。关键词 离子色谱法,饮料,山梨酸,苯甲酸,糖精钠食品中山梨酸、苯甲酸和糖精钠的测定方法国家标准推荐的主要有气相色谱法和高效液相色谱法等,其中,气相色谱法样品前处理方法繁杂,而高效液相色谱法虽然样品前处理方法简单但仪器价格偏贵基层实验室少有配置,使其应用受到限制。离子色谱法以其灵敏、快速、试剂消耗少、无环境污染等优点而备受广大分析工作者的青睐,已应用于食品中山梨酸、苯甲酸和糖精钠等多种添加剂的分析,但这些方法大多使用的是进口色谱柱并采用KOH淋洗液梯度洗脱方式进行测定,而进口色谱柱特别是具有梯度洗脱功能的离子色谱仪的价格普遍偏贵,目前基层实验室装备较少难以应用,因此研究用国产普通色谱柱和普通色谱仪测定食品中山梨酸、苯甲酸和糖精钠是一项有意义的工作,本工作研究了用国产普通色谱柱和色谱仪测定食品中山梨酸、苯甲酸和糖精钠的各种条件和可行性,结果表明,以1.5 mmol/LNa2CO3溶液作淋洗液,流量为1.5ml/min,用SH-AC-1型阴离子交换柱为分离柱,采用等度洗脱的方式可使山梨酸、苯甲酸和糖精钠较好分离,各组分的峰面积与其浓度在一定的范围内具有良好的线性关系,且各组分的保留时间在14 min以内,具有分析应用价值。据此,建立了用国产SH-AC-1型阴离子交换柱为分离柱,以1.5 mmol/LNa2CO3为淋洗液等度洗脱的方式测定食品中山梨酸、苯甲酸和糖精钠的方法,山梨酸、苯甲酸的线性范围为0~30.0mg/L,糖精钠的线性范围为0~15.0mg/L,方法应用于饮料等样品中山梨酸、苯甲酸和糖精钠的测定,获得了满意的结果。1、实验部分1.1主要仪器CIC-200型离子色谱仪(青岛盛翰色谱公司),抑制器:检测器:电导检测器,定量环体积为25μL;分离柱,SH-AC-1型阴离子交换柱(250×4.0mm i.d,青岛盛翰色谱公司,批号:1404016);1.2 仪器工作条件 柱箱温度35℃,电流:50mA。1.3主要试剂山梨酸、苯甲酸和糖精钠标准溶液:1000 mg/L,按照文献方法配制。临用时用纯水将各种标准溶液稀释成含山梨酸、苯甲酸各250.0 mg/L、 糖精钠125.0mg/L的混合标准应用液;75 mmol/LNa2CO3淋洗液贮备液,临用时用纯水稀释50倍使用。实验所用试剂均为AR及以上级,实验用水为超纯水(18.25ΜΩ·cm)。1.4 实验方法1.4.1标准曲线的绘制 取0.10、0.20、0.60、1.00、2.00和3.00 mL混合标准液于25mL容量瓶中加纯水至刻度,混匀,配制成含山梨酸、苯甲酸1.0、2.0、6.0、10.0、20.0、 30.0mg/L和糖精钠0.5、1.0、3.0、5.0、10.0和15.0mg/L标准系列,各进样1 mL上机(测试条件为,柱箱温度:35℃,电流:50mA;淋洗液:1.5mmol/L Na2CO3溶液;淋洗液流量:1.5mL/min;量程:1档)测定各成份峰面积(S),以S对浓度绘制工作曲线。1.4.2样品测定 将样品稀释50倍经0.45μm滤头过滤后进样1 mL上机(条件同1.4.1)测定各成份峰面积(S),以标准曲线法定量。2、结果与讨论2.1 Na2CO3浓度的选择 在高效液相色谱法中选择适当的淋洗液是改善分离度(R)的有效方法,为保证山梨酸、苯甲酸和糖精钠的有效分离,同时当以Na2CO3作淋洗液时,NO3-的保留时间与苯甲酸的保留时间比较接近,考虑到样品中可能存在的NO3-对苯甲酸测定的影响,为此进行了Na2CO3淋洗液浓度的选择实验,结果见表1。从表1可见,当Na2CO3浓度在1.0~表1 Na2CO3浓度对分离度和保留时间的影响(流量1.0 ml/min) 组分/浓度(mg/L) 1.0mmol/L 1.5mmol/L 2.0mmol/L 保留时间(min) R 保留时间(min) R 保留时间(min) R 山梨酸(20) 11.487 2.68 9.630 2.66 8.438 2.29 苯甲酸(20) 19.09 1.46 15.598 1.16 13.463 1.03 NO3-(10) 22.509 1.78 17.870 1.63 15.212 1.60 糖精钠(10) 26.048 / 20.645 / 17.543 / [/td

食品、饮料中防腐剂苯甲酸、山梨酸、糖精钠高效液相色谱检测防腐剂是食品添加剂中的重要组成部分,在食品生产、储存等环节起着非常重要的作用,但添加多了也会带来很多负面影响,尤其是对人体的影响。所以对食品添加剂的限量规定和检测是非常关键的。下面我们就一起来看看常见的食品添加剂(防腐剂苯甲酸、山梨酸、糖精钠)高效液相色谱检测。1. 实验项目(参考GB/T23495-2009)饮料、食品中防腐剂苯甲酸、山梨酸、糖精钠测试2. 实验内容测试检出限、校正曲线、重复性(RSD)、饮料、酱油样品等检测3. 仪器高效液相色谱仪(紫外检测器+等度泵+柱温箱+在线脱气机等)4. 色谱条件检测器:紫外检测器色谱柱:月旭Welchrom-C18 (250 mm × 4.6 mm,5μm)Serial Number:W13212255检测波长:230nm流动相:甲醇:0.02mol乙酸铵溶液=5:95(V:V)流速:1.0ml/min柱温:室温进样量:20ul5. 色谱图20.0ug/ml谱图 http://ng1.17img.cn/bbsfiles/images/2015/01/201501311901_533698_2498430_3.bmphttp://ng1.17img.cn/bbsfiles/images/2015/01/201501311911_533707_2498430_3.png20.0ug/ml谱图比较 http://ng1.17img.cn/bbsfiles/images/2015/01/201501311903_533699_2498430_3.bmp苯甲酸校正曲线 http://ng1.17img.cn/bbsfiles/images/2015/01/201501311904_533700_2498430_3.bmp山梨酸校正曲线 http://ng1.17img.cn/bbsfiles/images/2015/01/201501311904_533701_2498430_3.bmp糖精钠校正曲线 http://ng1.17img.cn/bbsfiles/images/2015/01/201501311905_533702_2498430_3.bmp某饮料样品色谱图 http://ng1.17img.cn/bbsfiles/images/2015/01/201501311910_533704_2498430_3.png该饮料样品加标色谱图 http://ng1.17img.cn/bbsfiles/images/2015/01/201501311911_533705_2498430_3.png
离子色谱法测定饮料中的山梨酸、苯甲酸和糖精钠黄选忠 杜宏山 邹大喜(湖北兴山县疾病预防控制中心,443711)摘要 建立了以青岛盛翰色谱公司生产的SH-AC-1型阴离子交换柱为分离柱,以1.5 mmol/LNa2CO3为淋洗液,流量为1.5mL/min,采用等度洗脱的方式测定食品中山梨酸、苯甲酸和糖精钠的方法,山梨酸、苯甲酸的线性范围为0~30.0mg/L, 糖精钠的线性范围为0~15.0mg/L,方法应用于饮料等样品中山梨酸、苯甲酸和糖精钠的测定,其结果与气相色谱法相吻合,加标回收率分别为:97.9%~98.4%、96.5~96.8%和100.6%~104.4%,5次平行测定的相对标准偏差分别为:1.68%~3.92%、2.32~4.08%和2.02%~3.95%(n=5),按样品稀释50倍计方法的检出限分别3.5、2.5和1.5 mg/L。关键词 离子色谱法,饮料,山梨酸,苯甲酸,糖精钠食品中山梨酸、苯甲酸和糖精钠的测定方法国家标准推荐的主要有气相色谱法和高效液相色谱法等,其中,气相色谱法样品前处理方法繁杂,而高效液相色谱法虽然样品前处理方法简单但仪器价格偏贵基层实验室少有配置,使其应用受到限制。离子色谱法以其灵敏、快速、试剂消耗少、无环境污染等优点而备受广大分析工作者的青睐,已应用于食品中山梨酸、苯甲酸和糖精钠等多种添加剂的分析,但这些方法大多使用的是进口色谱柱并采用KOH淋洗液梯度洗脱方式进行测定,而进口色谱柱特别是具有梯度洗脱功能的离子色谱仪的价格普遍偏贵,目前基层实验室装备较少难以应用,因此研究用国产普通色谱柱和普通色谱仪测定食品中山梨酸、苯甲酸和糖精钠是一项有意义的工作,本工作研究了用国产普通色谱柱和色谱仪测定食品中山梨酸、苯甲酸和糖精钠的各种条件和可行性,结果表明,以1.5 mmol/LNa2CO3溶液作淋洗液,流量为1.5ml/min,用SH-AC-1型阴离子交换柱为分离柱,采用等度洗脱的方式可使山梨酸、苯甲酸和糖精钠较好分离,各组分的峰面积与其浓度在一定的范围内具有良好的线性关系,且各组分的保留时间在14 min以内,具有分析应用价值。据此,建立了以青岛盛翰色谱公司生产的SH-AC-1型阴离子交换柱为分离柱,以1.5 mmol/LNa2CO3为淋洗液等度洗脱的方式测定食品中山梨酸、苯甲酸和糖精钠的方法,山梨酸、苯甲酸的线性范围为0~30.0mg/L, 糖精钠的线性范围为0~15.0mg/L,方法应用于饮料等样品中山梨酸、苯甲酸和糖精钠的测定,获得了满意的结果。1、实验部分1.1主要仪器CIC-200型离子色谱仪(青岛盛翰色谱公司),抑制器:检测器:电导检测器,定量环体积为25μL;分离柱,SH-AC-1型阴离子交换柱(250×4.0mm i.d,青岛盛翰色谱公司,批号:1404016); 1.2 仪器工作条件 柱箱温度35℃,电流:50mA。1.3主要试剂山梨酸、苯甲酸和糖精钠标准溶液:1000 mg/L,按照文献方法配制。临用时用纯水将各种标准溶液稀释成含山梨酸、苯甲酸各250.0 mg/L、 糖精钠125.0mg/L的混合标准应用液; 75 mmol/LNa2CO3淋洗液贮备液,临用时用纯水稀释50倍使用。实验所用试剂均为AR及以上级,实验用水为超纯水(18.2ΜΩ·cm)。1.4 实验方法1.4.1 标准曲线的绘制 取0.10、0.20、0.60、1.00、2.00和3.00 mL混合标准液于25 mL容量瓶中加纯水至刻度,混匀,配制成含山梨酸、苯甲酸1.0、2.0、6.0、10.0、20.0、 30.0mg/L和糖精钠0.5、1.0、3.0、5.0、10.0和15.0mg/L标准系列,各进样1 mL上机(淋洗液:1.5mmol/L Na2CO3溶液;流量:1.5mL/min;量程:1档)测定各成份峰面积(S),以S对浓度绘制工作曲线。1.4.2 样品测定 将样品稀释50倍经0.45μm滤头过滤后进样1 mL上机(条件同1.4.1)测定各成份峰面积(S),以标准曲线法定量。2、结果与讨论2.1 Na2CO3浓度的选择 在高效液相色谱法中选择适当的淋洗液是改善分离度(R)的有效方法,为保证山梨酸、苯甲酸和糖精钠的有效分离,同时当以Na2CO3作淋洗液时,NO3-的保留时间与苯甲酸的保留时间比较接近,考虑到样品中可能存在的NO3-对苯甲酸测定的影响,为此进行了Na2CO3淋洗液浓度的选择实验,结果见表1。从表1可见,当Na2CO3浓度在1.0~表1 Na2CO3浓度对分离度和保留时间的影响(流量1.0 ml/min)组分/浓度(mg/L)1.0mmol/L1.5mmol/L2.0mmol/L保留时间(min)R保留时间(min)R保留时间(min)R山梨酸(20)11.4872.689.6302.668.4382.29苯甲酸(20)19.091.4615.5981.1613.4631.03NO3-(10)22.5091.7817.8701.6315.2121.60糖精钠(10)26.048/20.645/
单位要开展酱油中的苯甲酸、山梨酸及糖精钠的检测,我查了最新食品标准是5009.28-2016,标准里有液相法和[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]法两种,而且[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]法适用于酱油,水果汁、果酱的测定,我记得被替代的5009.28-2003的标准就是液相法,而且很好做啊,直接用水进行稀释定容检测就行,为啥新的标准要分为两种方法呢?[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]法比液相法处理步骤麻烦。而且不能同时测定糖精钠。大家有知道原因的么?
高效液相色谱法测定食品中苯甲酸、山梨酸和糖精钠
苯甲酸、山梨酸、糖精钠是衡量食品卫生质量的重要指标,苯甲酸、山梨酸的检测参照GB/T5009.29-2003,糖精钠的检测参照GB/T 5009.28-2003,即可开展实验。 苯甲酸、山梨酸、糖精钠虽是较常见的检测项目,但是要得到一个准确可靠的结果,也存在一定的难度,许多新手常出现因对方法理解发生偏差而检测出错的事故。笔者根据自己多年该方面工作的实际经验出发,以苯甲酸、山梨酸为着重点,从样品前处理、检测仪器的选择、超标时的判断等几个易出问题的方面,进行了详细的阐述。 2 样品前处理的注意事项 GB/T5009.28-2003和GB/T5009.29-2003 在文字结构上有缺陷,在涉及用仪器法测定苯甲酸、山梨酸、糖精钠时,只讲述了液体样品的前处理方法,没有涉及对固体样品的前处理。 食品样品往往含有大量的油脂、蛋白质,对提取极为不利;如处理不干净也会污染色谱柱,影响检测工作。这类样品处理的关键在于如何找到一种较理想的沉淀剂,尽量排除待测样品中的油脂、蛋白质,且不影响待测物组分的回收率。 GB/T5009.29-2003使用5%硫酸铜溶液沉淀蛋白,对于蛋白质含量较低的食品尚可,对于豆粉、奶粉、月饼等高油脂、高蛋白样品则沉淀效果不理想。如用10%钨酸钠溶液作为沉淀剂,效果好些;如用10%亚铁氰化钾溶液和20%醋酸锌溶液则效果更理想(这是笔者目前用过最理想的沉淀剂)。 具体操作步骤如下: 取一定量样品,捣碎,利用四分法原理称取样品5.0 克于50ml比色管中,加水20ml,浸泡、振荡均匀,加入氢氧化钠溶液(1mol/L)1.0 ml,加入9.5mL10%亚铁氰化钾溶液, 9.50mL 20%乙酸锌溶液,定容,振荡使其充分混匀后,用滤纸初滤除去沉淀物, 初滤液过0.45μm微孔滤膜,收集滤液于样品瓶中,样品处理液和标准有溶液各进样5uL测定。 用这种方法简单易行,接触有机试剂少,重复性和回收率都令人满意;缺点是一定要用液相色谱法检测,有一定局限。 3 检测仪器的选择 虽然液相色谱仪操作起来比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]要复杂,但笔者建议如条件许可仍尽量用液相色谱法检测。原因如下: 3.1 液相色谱法所用的样品处理方法远比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法简单,且不需使用有机试剂。尤其对于高油脂样品(如月饼)若采用碱化-排油-酸化-提取-挥干-溶解等步骤,再上[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]检测,工作量大,试剂毒性也大,且结果由于处理步骤太多而难以保证准确。 3.2 用液相色谱法还可同时完成糖精钠项目的检测,而[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法只能做苯甲酸、山梨酸的检测。 3.3 液相色谱仪所用的紫外检测器比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]的氢火焰检测器灵敏,可进行更低含量的检测。如用二极管阵列检测器,还可辅助定性,这更是[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]氢火焰检测器不可比拟的。 4 选用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]时的注意事项 GB/T5009.29所用的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]柱为 5%DEGS+1%磷酸固定液的60-80目 Chromosorb W AW,。这种柱有性能稳定、重复性好、保留时间稳定的优点,但同时也有稳定时间较长的缺点。 该柱的适用的样品提取溶剂为石油醚或乙醚,如果用甲醇或乙醇,则溶剂峰拖尾效应较大,对山梨酸的测定有影响。 如用毛细管柱,能取得更好的峰形和灵敏度,但其稳定性及特异性不如填充柱。一般可用非极性毛细管柱,0.530mm内径,10-15m长度。色谱条件可能需用程序升温。 在[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]上的出峰次序为先出山梨酸,后出苯甲酸。 糖精钠不能直接用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]进行检测,必须衍生化后才能汽化进样。 5 选用液相色谱仪的注意事项 按照GB/T5009.29,流动相应为5:95的甲醇:0.02M醋酸铵溶液,但是这个比例仅是个参考值,我们在工作中应根据实际情况进行调节。 为什么用甲醇溶液?甲醇有两个作用,(1)防腐,液相色谱柱最怕流动相长菌,尤其霉菌。甲醇可使蛋白质变性,有杀菌作用。(2)调节流动相极性,这是最重要的一点。甲醇在溶液中比例的较小变化都会使苯甲酸、山梨酸、糖精钠的保留时间发生明显的改变,因此可以通过改变流动相中甲醇含量,以调节这几个组分的出峰和分离,以得到较理想的色谱图。 5:95是一个通用的比例,如减少甲醇含量,苯甲酸、山梨酸、糖精钠的出峰时间变慢,扩散效应增大,峰形较差,但这三组分的分离情况较好。如增加甲醇含量,苯甲酸、山梨酸、糖精钠的出峰时间提前,扩散效应较小,峰形尖锐,但这三组分的分离情况可能受影响,产生重叠。在选择条件时,只能通过实验手段,如配制3:97,4:96,5:95,6:96,7:93的流动相,综合考虑分离效果和分离时间选择最佳比例。 不同柱的最适比例不同,举例来说,色谱科公司的液相柱最适比例为4:96,而岛津公司液相柱的最佳比例为7:93。就是同一根柱,一年前和一年后的极性也会有变化,需调节溶液配比。 为什么使用0.02M醋酸铵溶液?加入醋酸铵是为了调节离子强度,使待测物的峰形不致于变坏。如果单独检测苯甲酸和糖精钠,加不加醋酸铵没有什么关系,都可以得到较好的峰形;但是检测山梨酸时流动相一定要加醋酸铵,否则得不到一个完整的色谱峰,峰形呈破裂状。 醋酸铵溶液浓度不需严格控制,0.01M、0.02M、0.04M均可。
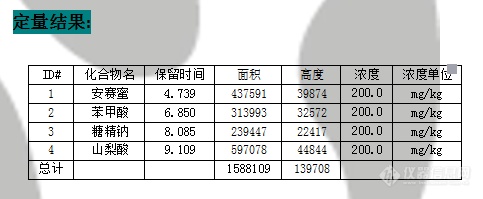
实验背景:食品中的防腐剂又称为抗微生物剂, 它是能防止由微生物引起的腐败变质、 延长[url=https://baike.sogou.com/v8882694.htm]食品保藏[/url]期的[url=https://baike.sogou.com/v254007.htm]食品添加[/url]剂。 目前我国规定使用的防腐剂有苯甲酸、 苯甲酸钠、[url=https://baike.sogou.com/v176790.htm]山梨酸[/url]、[url=https://baike.sogou.com/v1874186.htm]山梨酸钾[/url]、[url=https://baike.sogou.com/v6422150.htm]丙酸钙[/url]等25 种, 其作为重要的[url=https://baike.sogou.com/v254007.htm]食品添加剂[/url]之一, 在食品工业中被广泛使用。目前检 测 食 品 中 的 防 腐 剂 , 可 参 考 国 标 GB 5009 . 28 - 2016 , 该方法对苯甲酸、山梨酸、糖精钠三种物质进行了检测,以及国标GB 5009 . 140 -2016 法对安赛蜜物质进行了检测。本文采用Svea HPLC Column C 18 5 μm 110 Å 4. 6 * 250 mm 色谱柱对以上四种物质进行分析, 能够在较快的分析时间内得到良好的峰型, 并且使用寿命相对较长。色谱条件:色谱柱: Svea HPLC ColumnC18 5μm 110Å 4.6*250mm仪 器 :HPLC流动相: 甲醇:20mmol/L的乙酸铵=20:80(v:v) 流 速 :1.0 mL/min柱 温 :35 °C检测器: UV 230 nm提取剂: 超纯水进样体积: 5 μL分析物: 苯甲酸浓度0.01 mg/mL山梨酸浓度0.01 mg/mL糖精钠浓度0.01 mg/mL结 论:使用色谱柱Svea HPLC Column C 18 5 μm 110 Å 4. 6 * 250 mm 对以上三种物质进行分析, 有较好的保留, 并可以得到良好的峰型。[img=,483,199]https://ng1.17img.cn/bbsfiles/images/2018/12/201812251111384708_3045_1837999_3.png!w483x199.jpg[/img][img=,466,310]https://ng1.17img.cn/bbsfiles/images/2018/12/201812251111466670_3030_1837999_3.png!w466x310.jpg[/img][img=,424,344]https://ng1.17img.cn/bbsfiles/images/2018/12/201812251111497558_2167_1837999_3.png!w424x344.jpg[/img][img=,457,328]https://ng1.17img.cn/bbsfiles/images/2018/12/201812251111538258_9143_1837999_3.png!w457x328.jpg[/img]
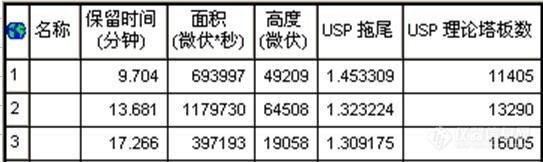
很多版友经常会发帖说苯甲酸、山梨酸、糖精钠的检测遇到问题,这次也有幸拿了月旭公司自主研发的新柱子Topsil C18柱试用,在对柱子评价的同时,也谈谈这3个项目的检测吧。色谱条件:流动相:甲醇+0.02mol/L乙酸铵溶液=5+95色谱柱:Topsil C18柱(4.6*250mm,5u)流速:1.0mL/min检测器:UV 230nm先看看国家标准的参考谱图吧,你可以跟我的图谱对照一下保留时间,峰行,峰位置等http://ng1.17img.cn/bbsfiles/images/2011/05/201105031108_291948_1608710_3.jpg这个是我用Topsil C18柱在这个色谱条件下测试的色谱图,附有理论塔板数的计算结果http://ng1.17img.cn/bbsfiles/images/2011/05/201105031111_291950_1608710_3.jpghttp://ng1.17img.cn/bbsfiles/images/2011/05/201105031111_291951_1608710_3.jpg下面这个图是用其他品牌的进口色谱柱的测试色谱图,已经不记得是不是全新的色谱柱测试的图了,供评价参考吧http://ng1.17img.cn/bbsfiles/images/2011/05/201105031113_291952_1608710_3.jpghttp://ng1.17img.cn/bbsfiles/images/2011/05/201105031113_291953_1608710_3.jpg柱子评价:1.很多版友都说,推荐一个好点的色谱柱做苯甲酸、山梨酸、糖精钠,那你的要求又是什么呢?分离度好、柱效高?其实这3个项目是很好做的,随便用一根C18柱就可以做,到是有一点,好的色谱柱寿命长啊,可是这点评试用是体现不出来的,而且跟你的样品基质也有很大关系。2.如果说分离度、柱效,这个Topsil C18柱子还是挺不错。苯甲酸、山梨酸、糖精钠检测的几点看法:1.有些人经常说山梨酸和糖精钠分不开,问题会出在哪里呢?几个可能的原因:一是你的柱子可以根据保留时间减少流动相甲醇的量,二是过滤流动相的过滤器尽量不要含甲醇,所以过滤前用水过滤下冲洗,三是柱温的设定,不要太高,温度对糖精钠的保留影响很大2.如果你走了2个泵,有些仪器泵精度不够高,5%的甲醇本身就很小,走仪器混合会出现重现不好。这个原因也是存在的,并不是不可能,尽量采用配置混合好的流动相。3.如果是3个混合在一起的标准溶液,苯甲酸很容易降解,放置时间不长
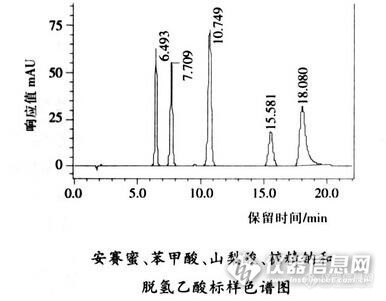
经常测食品中防腐剂的人,应该都很清楚,安赛蜜、苯甲酸、山梨酸、糖精钠、脱氢乙酸这几个项目,虽然国家标准方法不是同一个,都是流动相都大同小异。所谓大同小异,就是流动相都是甲醇+乙酸铵溶液,只是流动相中甲醇的量不同。而我们再做苯甲酸、山梨酸、糖精钠时,用的《GB/T 23495-2009 食品中苯甲酸、山梨酸和糖精钠的测定高效液相色谱法》标准,有的样品同时也会出现安赛蜜、脱氢乙酸的组分峰。我就遇到了,我就简单说说吧,希望对大家有帮助。这是一次测腌制菜中的苯甲酸、山梨酸、糖精钠,检测过程也基本是按照国家标准GB/T 23495-2009,如下:样品处理:称取粉碎样品1-2克于100毫升容量瓶中,加入约80毫升水,超声振荡提取30分钟,取出后加2毫升10.6%亚铁氰化钾溶液,摇匀,再加入2毫升22%乙酸锌溶液,摇匀,用水定容至刻度,摇匀后静置,然后过滤,上机分析。色谱条件:色谱柱:topsil C18柱(250mm*4.6mm,5μm)流动相:甲醇+乙酸铵溶液=6+94波长:230nm柱温:30流速:1.0mL/min 我走出来的样品,就是这样的图像,我采用的是DAD检测器,可以对比光谱图,发现糖精钠的光谱图根本就对不上,而是对应了脱氢乙酸的光谱吸收特征图。http://ng1.17img.cn/bbsfiles/images/2014/12/201412291112_529793_1608710_3.jpghttp://ng1.17img.cn/bbsfiles/images/2014/12/201412291112_529794_1608710_3.jpghttp://ng1.17img.cn/bbsfiles/images/2014/12/201412291112_529795_1608710_3.jpg给我的第一感觉就是脱氢乙酸和糖精钠峰重叠了,可是出的峰相当对称,光谱吸收图也很纯,难道样品中不含糖精钠吗?我清楚的记得,以前用这款柱子测,不会出现重叠的情况,而且分离的很好http://ng1.17img.cn/bbsfiles/images/2014/12/201412291115_529796_1608710_3.jpg这次出现这样的情况,是因为色谱柱是新买的,刚启用,第一次测,为了确保万一,还是换了根C8柱子重新测了一遍,发现样品中确实含有少量的糖精钠,因为脱氢乙酸含量高,重叠后完全掩盖了糖精钠的吸收。总结:1、测安赛蜜、苯甲酸、山梨酸、糖精钠、脱氢乙酸中任何一个项目,都要仔细对比光谱吸收或者进标准样品定位,以免出现重叠现象。2、很多人看脱氢乙酸的标准方法,觉得样品处理不一致,而且脱氢乙酸微溶于水,怎么还会出峰,却不知食品添加的其实大部分是脱氢乙酸钠,钠盐是易溶于水的。3、在遇到重叠的情况,改动柱子温度,糖精钠的出峰时间变化比较明显,我一般都是换一根不同品牌的柱子测试。
请问专家我们严格按照国标的方法同时做苯甲酸,山梨酸和糖精钠,可发现出峰顺序与标准不一样,标准是苯甲酸山梨酸,糖精钠,可我们是苯甲酸,糖精钠,山梨酸,怎么会这样?
请问做食品中山梨酸、苯甲酸和糖精钠的朋友,我前天刚开始做这三种物质的检测,走的标准样。如果按照国标流动相用甲醇:乙酸铵=5:95比列,流速1.0ml/min进标准混合样,柱温是40°。进样结果30分钟内无峰。如果把流动相改为甲醇:乙酸铵=50:50比列,则可以分出三个峰,但是国标上第三个峰是糖精钠,而我做的第一个峰是糖精钠。哪位大侠帮忙分析一下这是什么原因呢?我用的仪器是岛津LC-20AT。
请教一下各位高手关于苯甲酸、山梨酸、糖精钠的测定问题。灌注柱塞密封清洗泵的溶液应如何选用?洗针液应如何的选用?sunfire 色谱柱可否完成测定?
本人是测食品中的防腐剂。但是最近出峰异常,苯甲酸,山梨酸,糖精钠出鼓包峰。柱子是买了两周了。请问有知道是什么原因的吗?[img]https://ng1.17img.cn/bbsfiles/images/2019/08/201908241059191693_1922_3899930_3.png[/img][img]https://ng1.17img.cn/bbsfiles/images/2019/08/201908241059193273_6242_3899930_3.png[/img]
检测方法,请大家分享[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=135932]牛奶、奶粉中苯甲酸,山梨酸,糖精钠的检测方法[/url]
[font=宋体][size=15px]为了提高各实验室人员检测业务能力,保障监测数据准确性、真实性,推动检测行业健康发展由能力验证网主办,食品伙伴网协办“[/size][/font][b][font=微软雅黑][color=#333333]食品中山梨酸、苯甲酸、糖精钠检测实验室间比对[/color][/font][/b][font=宋体][size=15px]”活动。[/size][/font][font=Calibri][color=#333333][font=宋体]采取[/font] “[/color][/font][b][font=微软雅黑][color=#333333]线上培训讲解→分发样品→实验人员检测→数据分析→线上总结→通过发证[/color][/font][/b][font=Calibri][color=#333333]” [font=宋体]的模式[/font][/color][/font][font=宋体][color=#333333]。[/color][/font][font=宋体][size=15px]通过[/size][/font][font=宋体][size=15px]本次活动[/size][/font][font=宋体][size=15px]促进技能人才培养,推动检测技能培训,弘扬工匠精神,进一步推动我国经济高质量发展。[/size][/font][font=宋体] [/font][b][font=宋体][size=15px]一、主办单位:能力验证网[/size][/font][font=宋体][size=15px]二、协办单位:食品伙伴网[/size][/font][font=宋体][size=15px]三、活动时间:2022年07月25日 [/size][/font][font=宋体][size=15px]四、比对活动[/size][/font][font=宋体][size=15px](一)比对项目:[/size][/font][/b][font=宋体][size=15px]山梨酸、苯甲酸、糖精钠[/size][/font][b][font=宋体][size=15px](二)技术说明:[/size][/font][/b][font=宋体][size=15px]实验室(实验人员)按照日常检测程序和方法进行检测,检测方法可选用国标、行标等相关标准或非标方法。如采用非标方法,请将方法在结果报告单备注栏进行描述。[/size][/font][b][font=宋体][size=15px](三)活动流程:[/size][/font][/b][font=宋体][size=15px]过程按照T/FDSA 022—2021《食品检验检测实验室间比对 通用要求》进行样品发放、数据统计。对于结果满意的实验室,发放结果满意证书。为了满足实验人员的能力证明需求,证书会标识实验人员姓名(不超过三人)。[/size][/font][font=宋体][size=15px]在汇总完各实验室的检测数据后,老师会针对各室结果,针对性的给出意见,帮助实验人员找出实验过程存在的问题。[/size][/font][b][font=宋体][size=15px]六、参加对象:[/size][/font][/b][font=宋体][size=15px]生产企业、事业单位,第三方检验检测机构,学校及科研院所等。[/size][/font][b][font=宋体][size=15px]七、联系我们[/size][/font][/b][font=宋体][size=15px]联系人:[/size][/font][font=宋体][size=15px]杨老师[/size][/font][font=宋体][size=15px] [/size][/font][font=宋体][size=15px]18006456954[/size][/font][font=宋体][size=15px](微信同号) [/size][/font][font=宋体][size=15px] [/size][/font][font=宋体][size=15px]邮箱[/size][/font][font=宋体][size=15px]:[/size][/font][font=宋体][size=15px][color=#0563c1]pt[/color][/size][/font][font=宋体][size=15px][color=#0563c1]@foodmate.net[/color][/size][/font][font=宋体][size=15px][color=#0563c1][/color][/size][/font]
序号:01作者:胡梅; 王骏; 祝建华;期刊:粮食与食品工业题名:HPLC/MS测定食品中的苯甲酸、山梨酸、甜蜜素、糖精钠年号:2010年03期链接:http://202.119.208.220:8002/kns50/detail.aspx?dbname=CJFD2010&filename=LSSP201003027
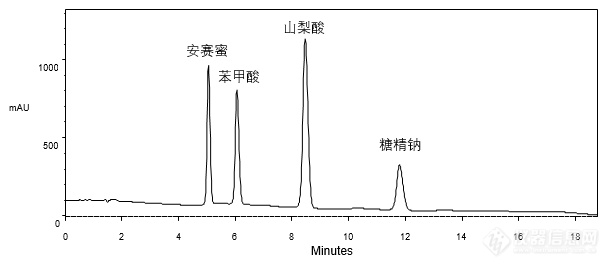
[align=center][b]GB 5009.28-2016食品安全国家标准 食品中苯甲酸、山梨酸和糖精钠的测定[/b][/align][align=center][b] ——标准品与乳品实际样品的分析[/b][/align][align=center][/align][align=left]本实验按照《GB5009.28-2016 食品安全国家标准食品中苯甲酸、山梨酸和糖精钠的测定》方法,分别对安赛蜜、苯甲酸、山梨酸、糖精钠的标准品混合溶液及加标乳品样品进行了分析。首先,使用CAPCELL PAK C[sub]18[/sub] MG S5 4.6 mm i.d. × 150mm色谱柱,对标准品混合溶液进行分析,如图1,安赛蜜、苯甲酸、山梨酸、糖精钠标准品均得到了良好的分析结果。[/align][align=left][/align][align=center][img=,611,268]http://ng1.17img.cn/bbsfiles/images/2018/03/201803221532276656_9890_2222981_3.png!w611x268.jpg[/img][/align][align=center]图1 标准品混合溶液分析色谱图[/align][img=,400,200]http://ng1.17img.cn/bbsfiles/images/2018/03/201803221532280132_6863_2222981_3.png!w400x200.jpg[/img][align=left][/align][align=left]其次,对乳品加标样品进行分析,如图2,糖精钠(Rt 12 min)与其后杂质峰之间未能取得基线分离,分离度仅为1.02。[/align][align=left][/align][align=center][img=,668,335]http://ng1.17img.cn/bbsfiles/images/2018/03/201803221533054905_2223_2222981_3.png!w668x335.jpg[/img][/align][align=center]图2 加标乳品样品分析色谱图[/align][align=left][img=,406,203]http://ng1.17img.cn/bbsfiles/images/2018/03/201803221533317202_2333_2222981_3.png!w406x203.jpg[/img][/align][align=left][/align][align=left]为改善糖精钠与杂质间的分离,在国标方法基础上,将流动相由[b]乙酸铵 / 甲醇 = 95 / 5[/b]调整为[b][b]乙酸铵 / 甲醇[/b][color=red]([/color][color=red]2 mmol/L [/color][color=red]甲酸)[/color]= 92 / 8[/b],再次对混合标准溶液和加标样品进行分析,结果如图3所示。[/align][align=left][/align][align=center][img=,690,545]http://ng1.17img.cn/bbsfiles/images/2018/03/201803221534141056_4073_2222981_3.png!w690x545.jpg[/img][/align][align=center]图3 混标与加标乳品样品分析色谱图[/align][align=left][img=,464,171]http://ng1.17img.cn/bbsfiles/images/2018/03/201803221535548985_7176_2222981_3.png!w464x171.jpg[/img][/align][align=left][/align][align=left]如图3,在酸性条件下,出峰顺序发生了变化,安赛蜜保留时间略有缩短,糖精钠保留时间明显缩短,由12 min缩短至8 min,苯甲酸和山梨酸保留时间分别延长至2 min和6 min;在分离度方面,糖精钠与苯甲酸之间分离度为2.79,苯甲酸与峰后杂质间分离度为2.04,所有色谱峰之间都达到了基线分离。[/align][align=left][/align][align=left]为使客户有更多选择,实验室又在国标原方法条件下继续筛选色谱柱,最终使用SUPERIOREX ODS S5 4.6 mm i.d. × 250 mm色谱柱时,仅微调有机相比例即可实现加标乳品样品的良好分析结果。如图4,杂质峰与糖精钠之间分离度达到2.48,达到基线分离要求。[/align][align=left][/align][align=center][img=,580,332]http://ng1.17img.cn/bbsfiles/images/2018/03/201803221537130173_1058_2222981_3.png!w580x332.jpg[/img][/align][align=center]图4 加标乳品样品分析色谱图[/align][align=left]*注:峰上标所示数字由下至上依次为分离度与不对称因子。[/align][align=left][img=,326,177]http://ng1.17img.cn/bbsfiles/images/2018/03/201803221537540634_9437_2222981_3.png!w326x177.jpg[/img][/align][align=left][/align][align=left]综上所述,按照国标《GB 5009.28-2016 食品安全国家标准食品中苯甲酸、山梨酸和糖精钠的测定》方法进行分析,使用CAPCELL PAK C[sub]18 [/sub]MG色谱柱对标准品混合溶液能得到良好分析结果,但在对加标乳品样品进行分析时,糖精钠与样品中的杂质未能实现基线分离,通过在流动相中添加甲酸可实现安赛蜜、糖精钠、苯甲酸、山梨酸及杂质的基线分离;另一方面,使用SUPERIOREX ODS色谱柱,在原条件基础上微调即可实现乳品中安赛蜜、苯甲酸、山梨酸、糖精钠及杂质间的良好分离。[/align]
苯甲酸、山梨酸、糖精钠是衡量食品卫生质量的重要指标,苯甲酸、山梨酸的检测参照GB/T5009.29-2003,糖精钠的检测参照GB/T 5009.28-2003,即可开展实验。 苯甲酸、山梨酸、糖精钠虽是较常见的检测项目,但是要得到一个准确可靠的结果,也存在一定的难度,许多新手常出现因对方法理解发生偏差而检测出错的事故。笔者根据自己多年该方面工作的实际经验出发,以苯甲酸、山梨酸为着重点,从样品前处理、检测仪器的选择、超标时的判断等几个易出问题的方面,进行了详细的阐述。 2 样品前处理的注意事项 GB/T5009.28-2003和GB/T5009.29-2003 在文字结构上有缺陷,在涉及用仪器法测定苯甲酸、山梨酸、糖精钠时,只讲述了液体样品的前处理方法,没有涉及对固体样品的前处理。 食品样品往往含有大量的油脂、蛋白质,对提取极为不利;如处理不干净也会污染色谱柱,影响检测工作。这类样品处理的关键在于如何找到一种较理想的沉淀剂,尽量排除待测样品中的油脂、蛋白质,且不影响待测物组分的回收率。 GB/T5009.29-2003使用5%硫酸铜溶液沉淀蛋白,对于蛋白质含量较低的食品尚可,对于豆粉、奶粉、月饼等高油脂、高蛋白样品则沉淀效果不理想。如用10%钨酸钠溶液作为沉淀剂,效果好些;如用10%亚铁氰化钾溶液和20%醋酸锌溶液则效果更理想(这是笔者目前用过最理想的沉淀剂)。 具体操作步骤如下: 取一定量样品,捣碎,利用四分法原理称取样品5.0 克于50ml比色管中,加水20ml,浸泡、振荡均匀,加入氢氧化钠溶液(1mol/L)1.0 ml,加入9.5mL10%亚铁氰化钾溶液, 9.50mL 20%乙酸锌溶液,定容,振荡使其充分混匀后,用滤纸初滤除去沉淀物, 初滤液过0.45μm微孔滤膜,收集滤液于样品瓶中,样品处理液和标准有溶液各进样5uL测定。 用这种方法简单易行,接触有机试剂少,重复性和回收率都令人满意;缺点是一定要用液相色谱法检测,有一定局限。 3 检测仪器的选择 虽然液相色谱仪操作起来比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]要复杂,但笔者建议如条件许可仍尽量用液相色谱法检测。原因如下: 3.1 液相色谱法所用的样品处理方法远比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法简单,且不需使用有机试剂。尤其对于高油脂样品(如月饼)若采用碱化-排油-酸化-提取-挥干-溶解等步骤,再上[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]检测,工作量大,试剂毒性也大,且结果由于处理步骤太多而难以保证准确。 3.2 用液相色谱法还可同时完成糖精钠项目的检测,而[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法只能做苯甲酸、山梨酸的检测。 3.3 液相色谱仪所用的紫外检测器比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]的氢火焰检测器灵敏,可进行更低含量的检测。如用二极管阵列检测器,还可辅助定性,这更是[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]氢火焰检测器不可比拟的。 4 选用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]时的注意事项 GB/T5009.29所用的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]柱为 5%DEGS+1%磷酸固定液的60-80目 Chromosorb W AW,。这种柱有性能稳定、重复性好、保留时间稳定的优点,但同时也有稳定时间较长的缺点。 该柱的适用的样品提取溶剂为石油醚或乙醚,如果用甲醇或乙醇,则溶剂峰拖尾效应较大,对山梨酸的测定有影响。 如用毛细管柱,能取得更好的峰形和灵敏度,但其稳定性及特异性不如填充柱。一般可用非极性毛细管柱,0.530mm内径,10-15m长度。色谱条件可能需用程序升温。 在[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]上的出峰次序为先出山梨酸,后出苯甲酸。 糖精钠不能直接用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]进行检测,必须衍生化后才能汽化进样。

【活动】【原创中秋测】我的中秋月饼中安赛蜜、苯甲酸、山梨酸、糖精钠、脱氢乙酸检测故事样品:各类月饼检测项目:山梨酸、苯甲酸、糖精钠、安赛蜜脱氢乙酸仪器条件:Waters e2695 ;色谱柱:Waters T3/250*4.6mm;检测器:PDA 230 nm 柱温:35 ℃;进样量:20 μL 流速:1.0 mL/min流动相:A:甲醇 D:0.02 mol/L醋酸铵水 Time(min) 0.0 10 10.1 15.0 15.1 20.0 A% 8 8 50 50 8 8样品处理:称2.0 g样品于50 mL离心管中,加入30 mL水均质提取1min,转移至50mL比色管中,含蛋白质样品加入5 mL 106 g/L亚铁氰化钾和5 mL 220 g/L乙酸锌沉淀剂(不含蛋白质不必加入沉淀剂)加入5mL甲醇,再加水定容到50 mL,摇匀,倒入50mL离心管,4000r/min离心5min(必要时取少量15000r/min高速离心),取上清液过0.45μm水系滤膜,上机检测[img=,690,423]https://ng1.17img.cn/bbsfiles/images/2018/09/201809251348054203_4797_2166779_3.png!w690x423.jpg[/img][img=,690,167]https://ng1.17img.cn/bbsfiles/images/2018/09/201809251351047260_5339_2166779_3.png!w690x167.jpg[/img]标准使用液配制记录:[img=,690,338]https://ng1.17img.cn/bbsfiles/images/2018/09/201809251353029794_3597_2166779_3.png!w690x338.jpg[/img]样品空白与混合标液2.0ug/mL堆栈色谱图:[img=,685,497]https://ng1.17img.cn/bbsfiles/images/2018/09/201809251403147035_9882_2166779_3.png!w685x497.jpg[/img]样品加标与样品堆栈色谱图:[img=,690,492]https://ng1.17img.cn/bbsfiles/images/2018/09/201809251355184880_1617_2166779_3.png!w690x492.jpg[/img]该样品的脱氢乙酸含量为:0.12g/kg(GB2760-2014规定为小于等于0.5g/kg),合格。回收率计算:(称取2.0g样品,加入混合标液100ug/mL1.0mL定容至50mL,加标浓度为0.050g/kg,理论上机浓度为2.0ug/mL)安赛蜜:102.5%、苯甲酸:76.0%、山梨酸:114.5%、糖精钠:96.5%、脱氢乙酸:95.5%;另一月饼的检测:混合标液光谱图:[img=,633,331]https://ng1.17img.cn/bbsfiles/images/2018/09/201809251413079635_2941_2166779_3.png!w633x331.jpg[/img]月饼检测的光谱图:[img=,690,341]https://ng1.17img.cn/bbsfiles/images/2018/09/201809251414182969_8069_2166779_3.png!w690x341.jpg[/img]该样品的山梨酸经光谱图验证后不是山梨酸,下面重点说下苯甲酸,该样品苯甲酸为0.03g/kg,依据GB2760-2014规定:月饼及月饼馅料中的苯甲酸均为不得使用,那是不是这个月饼样品就不合格呢?GB2760-2014中是这样规定带入原则的:[b]1.4 带入原则1.4.1在下列情况下食品添加剂可以通过食品配料(含食品添加剂)带入食品中:[/b][color=#1e1e1e]a) 根据本标准,食品配料中允许使用该食品添加剂;[/color][color=#1e1e1e]b) 食品配料中该添加剂的用量不应超过允许的最大使用量;[/color][color=#1e1e1e]c) 应在正常生产工艺条件下使用这些配料,并且食品中该添加剂的含量不应超过由配料带入的水平;[/color][color=#1e1e1e]d) 由配料带入食品中的该添加剂的含量应明显低于直接将其添加到该食品中通常所需要的水平。[/color][b]1.4.2当某食品配料作为特定终产品的原料时,批准用于上述特定终产品的添加剂允许添加到这些食品配料中,同时该添加剂在终产品中的量应符合本标准的要求。在所述特定食品配料的标签上应明确标示该食品配料用于上述特定食品的生产。2 食品添加剂的使用规定[/b][color=#1e1e1e]2.1表A.1列出的同一功能的食品添加剂(相同色泽着色剂、防腐剂、抗氧化剂)在混合使用时,各自用量占其最大使用量的比例之和不应超过1。[/color][color=#1e1e1e]2.2表A.3规定了表A.2所例外的食品类别,这些食品类别使用添加剂时应符合表A.1的规定。同时,这些食品类别不得使用表A.1规定的其上级食品类别中允许使用的食品添加剂。[/color][color=#1e1e1e]那会不会是什么月饼原料带入的呢?[/color][color=#1e1e1e][img=,690,213]https://ng1.17img.cn/bbsfiles/images/2018/09/201809251422240215_476_2166779_3.png!w690x213.jpg[/img][/color][color=#1e1e1e]那会不会是调味糖浆带入的呢?因为调味糖浆有允许使用的苯甲酸,限量为1.0g/kg,[/color][color=#1e1e1e]向生产企业要月饼生产的配料表:[/color][color=#1e1e1e][img=,489,244]https://ng1.17img.cn/bbsfiles/images/2018/09/201809251429529344_2683_2166779_3.png!w489x244.jpg[/img][/color][color=#1e1e1e]果然,这个月饼配料中有使用调味糖浆啊,这个GB2760的判定真的是有点防不胜防啊,不仅要会检测,而且还要会知道有哪些可能是由哪些原料带入的啊。[/color][color=#1e1e1e]结论:1、GB 5009.28-2016标准的液相方法样品经水提取,高脂肪样品经正己烷脱脂、高蛋白样品经蛋白沉淀剂沉淀蛋白,GB/T 5009.140-2003标准中对于汽水是先加热出去二氧化碳,然后取2.5mL稀释10倍上机检测,对于可乐、果茶、果汁类饮料是吸取2.5mL加20mL水稀释,离心,上清液过中性氧化铝柱,流动相洗脱、收集25mL作为上机检测液。GB 5009.28-2016液相色谱法采用GB/T 23377-2009法,标准中果蔬汁全部过柱;我们是如果有干扰才过柱。2、标准全部用超声波提取;我们是除去黄油类、果汁类,其他一般用均质提取,效率,回收率都能大大提高。3、过柱步骤,最后用水稀释上机,峰形好,标准方法峰形不好。 2、沉淀剂主要用于需除蛋白的样品,如肉酱,酱油,酱菜等;如上层有油层,则吸取中间清液; 3、四种混合标准中间溶液应用流动相配置(试验中发现用水配置,苯甲酸、山梨酸不稳定) 4、GB 5009.28-2016标准中提到当存在干扰峰或需要辅助定性时,可以采用加入甲酸的流动相来测定,如流动相:甲醇+甲酸-乙酸铵溶液(2mmo l / L甲酸+2 0mmo l / L乙酸铵)=8+92。 [/color][color=#1e1e1e]5、防腐剂在GB2760中的带入原则要慎重考虑,以免误判。[/color][color=#1e1e1e][/color][color=#1e1e1e][/color]
做苯甲酸,山梨酸和糖精钠很长时间了,一直分离的很好,峰形也很好,但最近一个月,几个峰开始拖尾严重,以致到现在山梨酸的保留时间延长和糖精钠根本分不开了,请问大家有碰到这种现象吗?我用的流动相是甲醇:乙酸铵=5.5:94.5。我最近换了针筒过滤器,它会带来这样的影响吗?请大家多给宝贵意见。谢谢!
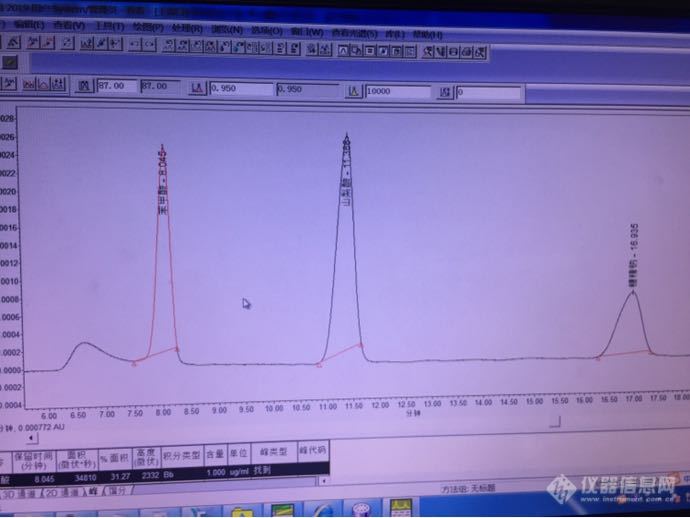
本人是刚接触液相色谱,在做苯甲酸山梨酸糖精钠的过程中,苯甲酸的峰前边有个类似峰的东西,为什么会出现这个情况呢,换过预柱了,大家能帮我分析一下什么原因吗?感谢![img=,690,517]https://ng1.17img.cn/bbsfiles/images/2019/08/201908081350406786_9043_2966618_3.png[/img]