核酸蛋白检测仪是层析分析的主要装置,核酸蛋白检测仪配上层析柱、恒流泵、部分收集器、层析谱分析系统(根据需要选配)和电脑打印设备即构成一套完整的核酸蛋白检测仪分离层析系统。它是当今从事生命科学研究、药物测定、化工、食品科学及医学研究等行业的现代分析实验仪器。核酸蛋白检测仪分析系统广泛用于工业、农业、科研和大专院校的科学研究和教学实验。其原理是根据物质(样品)对紫外光有明显吸收的特征,实现对样品成份含量比对分析,以便进行样品蛋白、核酸物质识别检测和含量测定。在生化分析、环保科学、食品研究、毒理研究、新药开发等领域中对核酸、蛋白检测、纯化和提取提供了一种独特的分析手段。
蛋白质测定仪是根据蛋白质中氮的含量恒定的原理,通过测定样品中氮的含量从而计算蛋白质含量的仪器但是实际中怎么操作呢?
求购一台粗蛋白快速测定仪,用于饲料厂检测原料,要求快速,结果准确(跟凯斯定氮仪结果比对)。
蛋白测定仪仪器厂商汇总,请跟贴说明。希望大家能提供图片。
海能公司的蛋白测定仪,好用吗?
如下FOSS(1026)蛋白测定仪的设置参数:蒸馏过程:碱2,蒸气3.6,吸收液30ml。我如何知道其蒸馏时间、加碱的体积、稀释液的体积、蒸汽量?
凯氏定氮仪与蛋白测定仪有什么区别?
求购核酸蛋白仪,
用核酸和蛋白样品测定NMR时,一般浓度多少比较合适?
ZHD型紫外蛋白核酸检测仪使用说明 一、系统简介 蛋白核酸检测仪是层析分析的主要装置,配上层析柱、恒流泵、部分收集器(根据需要选配)和电脑打印设备即构成一套完整的液相色谱分离系统。它是当今从事生命科学研究、药物测定、化工、食品科学及医学研究等行业的现代分析实验仪器。广泛用于工业、农业、科研和大专院校的科学研究和教学实验。其原理是根据物质(样品)对紫外光有明显吸收的特征,实现对样品成份含量比对分析,以便进行样品蛋白、核酸物质识别检测和含量测定。然而,目前国内生产的蛋白检测仪虽然种类繁多,但均采用记录仪描谱且预热时间较长。 ZHD型紫外蛋白核酸检测仪的研制成功,为科研和实验人员利用电脑系统实现核酸蛋白检测和分析提供了一种先进的手段,其特点是系统稳定、操作简便、电脑显示谱图、数据分析和打印谱图。 二、系统特点 本系列检测仪有别于其他检测仪,主要有以下特点: 1、预热时间短,一般做实验只要预热10分钟左右。 2、稳定性高,预热后每小时漂移一般小于0.001。 3、操作简洁,开机后仪器自动调整透光率(T)到100%,吸光度(A)调整到0.000。 4、透光率(T)和吸光度(A)对应准确,点两者误差小于1%。 5、双数据显示,仪器适时显示吸光度(A)和透光率(T)。 6、仪器带有电脑接口和记录仪接口(吸光度0—200mv)。 7、工作软件提供谱图采集、分析计算、保存、打印等功能,可将谱图插入文档(word)文件中。 8、一台电脑可配多台检测仪(由电脑有效端口数决定)。 三、 技术性能 1、通过测量选择菜单,在电脑屏幕上可描出吸光度(A)谱图,透过率(T%)谱图以及A-T%谱图。 2、通过图形平移、复读伸缩和压缩选择等菜单,可对谱图并进行幅度、宽度调整和谱图参数计算,预览满意后打印输出。 3、在描谱过程中,电脑会自动将图形左移(也可人工调整),电脑描谱最长时间为20小时。 4、采集数据自动保存。 四、主要参数: 1、波长:254nm,280nm(可根据用户需要调配)。 2、样品池100ul,光程3mm。 3、量程:吸光度(A):0--2.000 透光率(T):1%—100%。 4、分辩率:吸光度(A):0.001 透光率(T):0.1%。 5、电脑分析参数:峰高、峰宽、峰面积、峰面积比、保留时间、面积含量(归一化)、层析柱分辩率等。 6、电源220V±10%,50HZ。 7、主机重量:约3.5Kg。 五、系统安装与操作步骤 1、将仪器背板上的输出端通过一根串行口连接电缆与电脑主机的COM1或COM2串行口相连。 2、打开紫外蛋白核酸检测仪电源,仪器预热10分钟左右。 3、打开电脑后,将应用软件(ZHD.exe)复制到硬盘上。钦一下仪器面板上的复位按钮,待仪器显示0.000A和100%T后,双击ZHD.exe启动应用软件,系统进入采集(分析)状态。 4、在“测量选择”菜单下,用鼠标选择检测项目。 5、在“检测操作”菜单下点击“测量开始”,电脑开始采集。 6、要停止采集,点击“检测操作”下的“测量结束”菜单,然后关闭紫外蛋白酸检检测仪。 六、层析普工作站软件使用 1、 对硬件的基本要求: a、电脑在简体中文Windowsxp操作系统上运行; b、显示器分辩率为1024*768,小字体,256色配置; c、图形打印机; d、电脑系统必须正常工作,并保证串行口(COM2或COM1)有效; 2、系统连接无误后先让检测仪工作,再执行应用软件ZHD.exe; 3、 点击文件操作菜单下的“打开谱图”,出现文件操作对话框,打开随机盘上的数据文件(.ran),图形被打开,熟悉菜单操作。菜单介绍如下: a、“文件操作”菜单下有打开谱图、保存谱图、打印谱图、打印预览等; b、“检测操作”菜单下有测量开始、测量结束(测量结束后,系统在应用程序目录下生成“文件名.TXT”文件,此格式文件可在Excel软件中打开,并可转贴到Word文档中使用); c、“灵敏度选择”菜单下有A、T%、A-T%选项; d、“谱图平移”菜单后有向左慢移动 []和向右快移动[]; e、“谱图重绘”菜单:从起始点描谱;清理屏幕;释放压缩; f、“谱图全貌”菜单:在屏幕上观察全部谱图。 g、“参数选择”菜单:可对谱图进行参数分析计算。方法如下:在吸光度状态下,点击鼠标左键选取基线及时间范围(第一次点击选取第一点,第二次点击选取第二点),点击“选择参数”下拉菜单的峰高、标准差、半峰宽、峰底宽、峰面积、峰面积比、面积含量及保留时间等参数进行计算,还可间接计算出层析柱分辨率;双击鼠标左键,即可取消本次计算。 h、在吸光度(A)或透光率(T%)状态下,单击鼠标右键,屏幕显示该鼠标点的数值;双击鼠标右健,擦除屏幕显示数值。 七、注意事项: a、 更改波长方法:打开样品池挡板后,可见到滤光片的燕尾型支架和印字(245或280代表当前所使用的波长),用手将其轻轻抽出,换向后插入原位,再将样品池挡板装上,拧紧固定螺钉即可。 b、 在检测仪和电脑正常工作后才能运行应用软件; c、 应用软件执行后,十秒钟后不出现采集分析界面,说明电脑未收到数据,需检查系统连接是否正常; d、 在A—T%描谱过程中,开始1小时内,T%谱以实蓝线表示;1小时后(或点击“图形重绘” ),已描过的T%谱会以虚蓝线表示; e、 测量开始后(特别是出峰以后)不要按复位按钮。 f、 要停止采集,请点击“测量结束”后,先点击“EXIT”,再关闭检测仪。 g、 开始测量时,屏幕会弹出保存文件对话框,要求输入数据文件名及存放路径;之后,电脑自动保存数据。 I、基线选取要保证基线与所选峰必须要有两个焦点,并与其他峰无焦点。
食品中蛋白质测定仪是一种用于快速准确地测量食品中蛋白质含量的设备。以下是关于食品中蛋白质测定仪的一些详细信息: 一、工作原理 食品中蛋白质测定仪的工作原理通常基于蛋白质与某些化学试剂反应产生颜色变化,通过测定颜色的强度来计算蛋白质的含量。常用的化学试剂有比色法、尿素法、低丙酮酸法等。其中,比色法是一种常用的蛋白质测定方法,其原理是利用蛋白质与双糖试剂反应生成紫色化合物,通过比色法测定紫色化合物的吸光度来计算蛋白质的含量。 二、应用领域 1. 食品生产、加工、流通等环节:蛋白质测定仪可以用于检测食品的质量,确保食品符合国家食品安全标准。 2. 食品安全监管:蛋白质测定仪可以用于检测食品中的农药残留、重金属含量等食品安全指标,为食品安全监管提供准确的数据支持。 3. 科学研究:蛋白质是生命活动的基本物质,对生命科学的研究具有重要意义。蛋白质测定仪可以用于研究食品中的蛋白质结构、功能以及与其他物质的相互作用等,为生命科学研究提供重要的数据支持。 4. 教学实验:在高校和科研机构中,蛋白质测定仪可以用于教学实验和研究工作。 三、使用方法 使用蛋白质测定仪进行蛋白质含量的测定通常包括以下步骤: 1. 样品准备:取一定量的食品样品,按照仪器说明书的要求进行前处理,如稀释、过滤等。 2. 试剂添加:向样品中加入适量的化学试剂,使其与蛋白质发生反应。 3. 反应与测定:等待一定时间,使反应充分进行,然后使用蛋白质测定仪测定反应液的颜色强度。 4. 结果计算:根据仪器测定的颜色强度,结合标准曲线或公式,计算出样品中的蛋白质含量。 需要注意的是,不同的蛋白质测定仪可能具有不同的操作方法和要求,因此在使用前需要仔细阅读仪器说明书,并按照说明书的要求进行操作。 四、注意事项 1. 仪器应放置在干燥、通风、无尘的环境中,避免阳光直射和强烈震动。 2. 在使用前应对仪器进行预热和校准,确保仪器的准确性和稳定性。 3. 在操作过程中应注意安全,避免试剂溅出或吸入有害气体。 4. 定期对仪器进行维护和保养,如清洗、更换试剂等,以保证仪器的正常运行和延长使用寿命。
请教各位大家谁有FOSS2300蛋白测定仪 自校准方法?检定校准机器测定蛋白质含量的准确性怎么样,用什么方法做?
我们实验室用的是上海嘉鹏科技有限公司生产的的核算蛋白检测仪,型号为HD-2000,现在急需该仪器的说明书
欲购买凝胶成像系统、核酸蛋白仪全自动定氮仪,请各位使用者及代理商广泛给予建议,谢谢!
上海纤检仪器有限公司的蛋白测定仪与上海嘉定粮油仪器有限公司的,哪家更好些?
我现在在做蛋白和核酸的结合.我的蛋白和核酸可以结合. 蛋白是400多KDa的 核酸很小, 是30bp的dsDNA. 我现在的检测条件下只跑蛋白是可以跑出来的, 当我蛋白和核酸一起跑的时候, 也会在跟只跑蛋白在差不多的位置出峰. (我用的双波长检测,蛋白和核酸分别标记,所以都能看到.)问题就是,一起跑的时候, 出的所有峰, 都是既有蛋白又有核酸, 不管我加的比例是多少.我就很困惑. 如果我加的核酸量很小的话,不是应该有很多游离的蛋白吗,就是说应该有的蛋白峰对应的地方是没有核酸出峰才对的啊, 为什么没有这样的峰呢, 我什么地方理解错了吗?~ 请大家帮忙.谢谢~~~~!BTW, 我用的是bare fused silica capillary, 是CZE, 不是凝胶的 谢谢~~~
我想问一下,KDN-04蛋白质测定仪蒸馏时,打开电源后蒸炉自动进水是从自来水管道进的还是从蒸馏水管道进的?主要是我原理没弄清,资料上说是,自动进水后打开自来水管,意思是蒸炉内的水是从蒸馏水管道进的吗?有哪位前辈知道吗?急!谢谢了!
随着常规分子生物学研究的深入,越来越多的生物实验室日常需要测量的核酸、蛋白样品量也在不断地加大。传统的分光光度计虽然已经非常普及,但由于需要在测量后清洗比色杯,实际上消耗了不少宝贵的研究时间。同时,由于核酸样品的体积较小,即使使用昂贵的微量石英比色杯(容积数十ul左右),也往往需要对原始样品进行稀释,从而带来可能的操作偏差。对于一些稀有的样品来说,稀释即意味着测量后无法回收,同样也会对后续研究带来更高成本。因此,无需比色杯,仅需数ul即可测定样品浓度的超微量分光光度计现在受到很多实验室的关注和欢迎。NanoVue是GE Healthcare公司于2008年最新推出超微量分光光度计。GE Healthcare公司的分光光度计品牌Ultrospec和GeneQuant在市场上已经有了十多年的历史,在用户中有着很好的信誉和口碑。NanoVue在该系列仪器的基础上延续了出众的检测性能,同时大大改进了检测的光路设计,通过专利的检测技术使检测样品的体积最小仅需0.5ul, 190-1100nm的宽范围连续波长设计较市场上同类仪器宽了一倍左右,使得能够轻松检测核酸、蛋白样品和Cydye荧光染料标记物的浓度。仪器内置了RNA、DNA 和寡核苷酸浓度和纯度测定方法;寡核苷酸转换因子,分子量,理论Tm计算功能;包括一般紫外、Bradford、 Biuret、BCA、Lowry的蛋白定量法;以及波长扫描,动力学,标准曲线,多波长测定等扩展功能。除了强大的检测性能外,NanoVue还在许多操作性能上进行了精心的设计,能够给用户带来众多全新的体验,主要包括以下方面:1 唯一不需电脑就能在仪器面板上直接检测的超微量分光光度计。仪器配置了一块大面积高分辨率的背光液晶屏和操作面板。相对于点样后转去电脑控制,再回去仪器清洁的过程,NanoVue不仅节省了购买电脑的支出,同时点样,按键测量,擦拭一气呵成。可以通过整合的打印机直接打印分析数据。当然,如果需要在电脑上保存分析数据,NanoVue同样支持USB或蓝牙连接电脑,将珍贵的实验数据永久记录下来。2 通过特别设计的疏水点样表面,能够很容易回收稀有的样品,并且有效避免多个测量间的样品交叉污染,提高测量的准确性。NanoVue的点样表面具有专利设计,表面坚固而且光滑。不管是样品回收还是测量完直接擦去都非常简易,不会有任何样品粘附残留在点样面上。而且点样面耐用性也非常出众,保守估计可以至少测量20000个样品以上。3 最快的检测速度。NanoVue通过独特的光路设计,使得所有样品的检测都能够在5秒钟之内完成,把微量分光光度计的测量时间提升到了一个新的高度。而且NanoVue具备即开即用功能,避免了许多分光光度计开机需要预热的麻烦,真正做到省时省力。由此可见,NanoVue不仅性能出众,其易用性和灵活性也是目前超微量分光光度计中出类拔萃的。通过试用NanoVue的体验,使用者可以完全感受到,原来,核酸蛋白的测定可以这么简单,这么快速!目前,NanoVue已经正式在中国推出,欲了解更多的信息,请直接联系GE公司。
不知有谁使用过这个机器,是否能提供DU530核酸/蛋白分析仪使用说明书,谢谢!
食品中蛋白质含量测定仪是用于快速、准确地测量食品中蛋白质含量的专业仪器。这种仪器基于各种化学或物理方法,如凯氏定氮法、双缩脲法、考马斯亮蓝法(Bradford法)或紫外分光光度法等,来测定食品中蛋白质的含量。 以下是关于食品中蛋白质含量测定仪的一些详细信息: 工作原理 凯氏定氮法:这是一种经典的蛋白质测定方法。样品中的蛋白质在催化剂的作用下与硫酸共热消化,使蛋白质分解,分解的氨与硫酸结合生成硫酸铵。然后碱化蒸馏使氨游离,用硼酸吸收后再以硫酸或盐酸标准溶液滴定,根据酸的消耗量乘以换算系数,即可计算出样品的蛋白质含量。 双缩脲法:在碱性溶液中,双缩脲(尿素加热至180℃左右生成的二聚体)与铜离子形成紫色络合物,该络合物的颜色深浅与蛋白质含量成正比,而与蛋白质分子量及氨基酸成分无关,故可用来测定蛋白质含量。 考马斯亮蓝法(Bradford法):考马斯亮蓝G-250染料在酸性溶液中与蛋白质结合后,在595nm处有最大光吸收,其光吸收值与蛋白质含量成正比。因此,可用于蛋白质的定量测定。 紫外分光光度法:蛋白质中常含有酪氨酸、色氨酸等苯环结构,在280nm的紫外波段有较强的吸收峰,其吸光度与蛋白质含量成正比。这种方法操作简单、快速,但灵敏度较低,只适合测定蛋白质含量较高的样品。 应用领域 食品质量检测:蛋白质是食品中的重要营养成分,其含量是评价食品质量的重要指标之一。食品中蛋白质含量测定仪可用于检测各类食品(如肉类、奶类、蛋类、豆类、谷物等)中的蛋白质含量,为食品质量检测提供数据支持。 食品科学研究:在食品科学研究中,蛋白质含量测定仪可用于分析不同食品原料、加工工艺对蛋白质含量的影响,以及蛋白质在食品加工过程中的变化等。 注意事项 在使用蛋白质含量测定仪进行测试之前,需要仔细阅读产品说明书,了解仪器的使用方法、操作步骤及注意事项。 确保样品准备过程符合标准要求,避免样品污染或损坏导致检测结果不准确。 定期对仪器进行维护和校准,确保检测结果的准确性和可靠性。 在使用过程中注意安全防护措施,避免对人体造成伤害或对环境造成污染。 总之,食品中蛋白质含量测定仪是食品检测领域的重要工具之一,能够快速、准确地测定食品中的蛋白质含量,为食品质量控制和科学研究提供有力支持。[img=,690,690]https://ng1.17img.cn/bbsfiles/images/2024/05/202405151126410832_3840_4214615_3.jpg!w690x690.jpg[/img]
[font=宋体]蛋白质是包括人类在内的各种生物有机体的重要组成成分,是生命的物质基础之一。生物体的生长、发育、遗传和繁殖等一切生命活动都离不开蛋白质。[/font][font=宋体] [/font][font=宋体]随着分子生物学、结构生物学、基因组学等研究的不断深入,人们意识到仅仅依靠基因组的序列分析来试图阐明生命活动的现象和本质是远远不够的。只有从蛋白质组学的角度对所有蛋白质的总和进行研究,才能更科学地掌握生命现象和活动规律,更完善地揭示生命的本质。[/font][font=宋体] [/font][font=宋体]由此许多学者将生命科学领域的研究焦点从基因转向蛋白质,使蛋白质成为揭示生命活动现象和分子生物学机理的重要研究对象。研究蛋白质首要的步骤是将目的蛋白从复杂的大分子混合物中分离纯化出来,得到高纯度具有生物学活性的目的物。因此,高效的纯化技术和手段是蛋白质研究的重要基础和关键之一。[/font][font=宋体] [/font][font=宋体] [/font][b][font=宋体][font=宋体]蛋白纯化的目的[/font] [/font][/b][font=宋体][font=宋体]蛋白纯化的目的是将目标蛋白质从细胞裂解液的全部组分中分离出来,同时仍保留蛋白的生物学活性及化学完整性。蛋白质的分离和提纯工作是一项艰巨而繁重的任务,需根据蛋白的特性选择合适的纯化方法来提高获得的蛋白制品的纯度。[/font] [/font][font=宋体] [/font][b][font=宋体][font=宋体]蛋白纯化的原理[/font] [/font][/b][font=宋体][font=宋体]不同蛋白质的氨基酸序列及空间结构不同,导致其在物理、化学、生物学等性质上存在差异,利用待分离蛋白质与其它蛋白质性质上的差异,即可以设计出一套合理的蛋白纯化方案。蛋白的纯化大致分为粗分离阶段和精细纯化阶段两个阶段。粗分离阶段主要将目的蛋白和其他细胞成分如[/font] [font=Calibri]RNA[/font][font=宋体]、[/font][font=Calibri]DNA [/font][font=宋体]等分开,常用的方法为硫酸铵沉淀法。精细纯化阶段的目的是把目的蛋白与其他大小及理化性质接近的蛋白区分开来,[/font][/font][b][font=宋体][font=宋体]常用的方法有:凝胶过滤层析、离子交换层析、疏水层析、亲和层析等。[/font] [/font][/b][font=宋体] [/font][b][font=宋体]①[/font][font=宋体]凝胶过滤层析[/font][/b][font=宋体]凝胶过滤层析(又叫做分子筛)是根据样品的分子大小对样品进行分离的一种简单温和的层析技术。凝胶过滤层析也称分子筛层析、排阻层析,是利用具有网状结构的凝胶的分子筛作用,根据被分离物质的分子大小不同来进行分离。不同于离子交换层析和亲和层析,凝胶过滤的层析样品不与层析柱料结合,因此,缓冲液成分不直接影响分辨率。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体][font=宋体]原理:层析柱中的填料是球状颗粒的惰性的多孔网状结构的柱料,多是交联的聚糖[/font][font=Calibri]([/font][font=宋体]如葡聚糖或琼脂糖[/font][font=Calibri])[/font][font=宋体]类物质。在加入样品之后,样品中的小分子物质能进入球状填料内部,在柱子中停留时间较长;而大分子物质不能进入球状填料内部,停留时间较短。所以当样品经过凝胶过滤层析柱分离后,样品中的不同分子大小的物质就可以被分离开了。[/font][/font][font=宋体] [/font][font=宋体]特点:[/font][font=宋体] [/font][font=宋体]根据分子大小和形状进行分离[/font][font=宋体] [/font][font=宋体]是一种非吸附的分离方式[/font][font=宋体] [/font][font=宋体]缓冲液成分不直接影响分辨率,只需要一种缓冲液[/font][font=宋体] [/font][font=宋体]操作便捷[/font][font=宋体] [/font][font=宋体] [/font][b][font=宋体]②[/font][font=宋体]离子交换层析[/font][/b][font=宋体]离子交换层析是目前蛋白质分离纯化中应用最广泛的方法之一。[/font][font=宋体] [/font][font=宋体]原理:不同蛋白等电点差异,分子大小差异,在同一个流动相中电荷密度分布不同,电荷量不等,与具有相反电荷的离子交换介质结合强度不同,在流动相洗脱时保留时间不同,从而得以分离。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体]特点:[/font][font=宋体] [/font][font=宋体]根据分子大小和等电点差异进行分离[/font][font=宋体] [/font][font=宋体]灵敏度高,重复性,选择性好,分析速度快[/font][font=宋体] [/font][font=宋体] [/font][font=宋体] [/font][b][font=宋体]③[/font][font=宋体]疏水层析[/font][/b][font=宋体]原理:疏水层析是依据蛋白质疏水性差异分离的。即根据蛋白质和疏水介质表面的疏水基团的可逆相互作用进行分离。蛋白的疏水性在高离子强度下被增强,因此在高离子强度环境中结合,通常采用降低离子强度的方式进行洗脱。独特的吸附分离模式使得疏水层析成为硫酸铵盐析后或离子交换高盐洗脱后理想的纯化方式。[/font][font=宋体] [/font][font=宋体]特点:[/font][font=宋体] [/font][font=宋体]采用了盐的水溶液作为流动相,色谱条件温和,生物大分子的活性回收率很高。[/font][font=宋体] [/font][font=宋体][font=宋体]蛋白质在[/font][font=Calibri]HIC[/font][font=宋体]操作过程中是高盐上样,低盐洗脱(高盐浓度的样品不必作处理就可直接上样)。[/font][/font][font=宋体] [/font][font=宋体]在一次色谱中可同时实现出去盐酸胍、蛋白质复性和分离三个目的。[/font][font=宋体] [/font][font=宋体][font=宋体]温度升高,蛋白质天然折叠伸展,暴露出更多内部疏水集团,使蛋白质的[/font][font=Calibri]HIC[/font][font=宋体]保留发生变化。[/font][/font][font=宋体] [/font][font=宋体]色谱填料稳定性好,盐水体系作流动相无环境污染。[/font][font=宋体] [/font][b][font=宋体]④[/font][font=宋体]亲和层析[/font][/b][font=宋体][font=宋体]原理:[url=https://cn.sinobiological.com/resource/protein-review/protein-purification-by-ac][b]亲和层析[/b][/url]是应用生物高分子与配基可逆结合的原理,将配基通过共价键牢固结合于载体上而制得的层析系统。这种可逆结合的作用主要是靠生物高分子对它的配基的空间结构的识别。常用的生物亲和关系有酶[/font][font=Calibri]-[/font][font=宋体]底物、底物类似物、抑制剂、激活剂、辅因子,抗体[/font][font=Calibri]-[/font][font=宋体]抗原,激素[/font][font=Calibri]-[/font][font=宋体]受体蛋白、载体蛋白,外源凝集素[/font][font=Calibri]-[/font][font=宋体]多糖、糖蛋白、细胞表面受体,核酸[/font][font=Calibri]-[/font][font=宋体]互补核苷酸序列、组蛋白、核酸结合蛋白等,具有高效、简单、快速的优点,是当前最为理想的分离纯化蛋白的方法。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]更多详情可以参看蛋白纯化技术[/font][font=Calibri]/[/font][font=宋体]方法:[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/protein-purification-techniques[/font][/font][font=Calibri] [/font]
请教各位:有没有办法把植物中的一步把蛋白降为氨基酸,淀粉降为葡萄糖,核酸降为核苷酸,油脂降为脂肪酸?也不一定要一步,就是所有的组分要尽量少损失。有高手知道吗?
食品中蛋白质测定仪的优点主要取决于其技术类型、精度、使用便捷性等因素。以下是针对食品中蛋白质测定仪的一般性优点分析: 优点: 快速性:蛋白质测定仪能在短时间内完成大量样品的检测,大大提高了检测效率,适用于食品生产线上快速、连续的蛋白质含量测定。 准确性:采用先进的检测技术,如光谱技术、化学分析方法等,能够确保测量结果的准确性和可靠性。 操作简单:仪器操作简单易用,用户只需按照说明书进行操作即可完成检测,降低了操作难度和人工成本。 应用广泛:适用于各类食品中蛋白质含量的检测,如乳制品、肉制品、豆制品等,具有广泛的应用前景。 自动化程度高:部分蛋白质测定仪具有自动化功能,能够自动完成样品的处理、检测和数据分析,提高了工作效率和准确性。
国外的核酸蛋白检测仪比较起来哪个厂家的比较好,给推荐几个,价位
[font=宋体][font=宋体]蛋白质浓度测定的各种方法及原理是生物化学和分子生物学实验中的重要环节。蛋白质浓度的准确测定对于研究生物分子相互作用、蛋白质功能和动力学、以及生物样品的分析和鉴定等方面都具有重要的意义。本文将介绍几种常用的蛋白质浓度测定方法及其原理,包括紫外吸收法、微量凯氏定氮法、双缩尿法、[/font][font=Calibri]Lowry [/font][font=宋体]法和考马斯亮蓝法等。通过对这些方法的比较和分析,可以更好地了解它们的优缺点,以便根据实际实验需求选择合适的方法来测定蛋白质浓度。[/font][/font][font=宋体] [/font][font=宋体][b]①紫外吸收法[/b][/font][font=宋体] [/font][font=宋体]检测原理:[/font][font=宋体] [/font][font=宋体][font=宋体]蛋白质分子中,酪氨酸、苯丙氨酸和色氨酸残基的苯环含有共扼双键,使蛋白质具有吸收紫外光的性质。吸收高峰在[/font][font=Calibri]280nm[/font][font=宋体]处,其吸光度(即光密度值)与蛋白质含量成正比。此外,蛋白质溶液在[/font][font=Calibri]238nm[/font][font=宋体]的光吸收值与肽键含量成正比。利用一定波长下,蛋白质溶液的光吸收值与蛋白质浓度的正比关系,进行蛋白质含量的测定。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体]方法特点:[/font][font=宋体] [/font][font=宋体]优点:简便、灵敏、快速,不消耗样品,测定后仍能回收使用。[/font][font=宋体] [/font][font=宋体]缺点:测定蛋白质含量的准确度较差,干扰物质多。[/font][font=宋体] [/font][font=宋体]干扰物:含有嘌呤、嘧啶、核酸等吸收紫外光的物质。[/font][font=宋体] [/font][font=宋体][font=宋体]检出限:[/font][font=Calibri]50~100ug[/font][font=宋体]蛋白含量。[/font][/font][font=宋体] [/font][font=宋体]适用范围:适于用测定与标准蛋白质氨基酸组成相似的蛋白质。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体] [/font][font=宋体][b]②微量凯氏定氮法[/b][/font][font=宋体] [/font][font=宋体]凯氏定氮法被国内外视为蛋白质含量的标准检验方法,可作为衡量其他蛋白质含量检测方法准确性的标准。[/font][font=宋体] [/font][font=宋体]实验原理:[/font][font=宋体] [/font][font=宋体]样品与浓硫酸共热,含氮有机物即分解产生氨(消化),氨又与硫酸作用,变成硫酸氨。经强碱碱化使之分解放出氨,借蒸汽将氨蒸至酸液中,根据此酸液被中和的程度可计算得样品之氮含量。[/font][font=宋体] [/font][font=宋体]方法特点:[/font][font=宋体] [/font][font=宋体]优点:通用性强,测定费用低,易实现,仪器简单且测定结果的重复性和重现性好。[/font][font=宋体] [/font][font=宋体]缺点:实验耗时长、灵敏度低。[/font][font=宋体] [/font][font=宋体][font=宋体]检出限:[/font][font=Calibri]0.2~1mg[/font][font=宋体]蛋白含量。[/font][/font][font=宋体] [/font][font=宋体]适用范围:凯氏定氮法测的是总蛋白的量,一些非蛋白氮无法检测出。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体] [/font][font=宋体][b]③双缩尿法[/b][/font][font=宋体] [/font][font=宋体]实验原理:[/font][font=宋体] [/font][font=宋体][font=宋体]双缩尿([/font][font=Calibri]NH3CONHCONH3[/font][font=宋体])是两个分子经[/font][font=Calibri]180[/font][font=宋体]℃左右加热,放出一个分子氨后得到的产物。在强碱溶液中,双缩尿与[/font][font=Calibri]CuSO4[/font][font=宋体]形成紫色络合物,称为双缩尿反应。凡具有两个酰胺基或两个直接连接的肽链,或能过一个中间碳原子相连的肽键,这类化合物都有双缩尿反应。紫色络合物颜色的深浅与蛋白质浓度成正比,与蛋白质分子量及氨基酸成分无关。[/font][/font][font=宋体] [/font][font=宋体]方法特点:[/font][font=宋体] [/font][font=宋体]优点:适合检测总蛋白质的含量,操作简单、测量速度快。[/font][font=宋体] [/font][font=宋体]缺点:标准物质必须使用代表性很强的样品,需使用其他参考方法测出标准物质中的蛋白质总含量,故测定工作费力费时。不宜测定样品种类多、彼此差异大的样品。[/font][font=宋体] [/font][font=宋体][font=宋体]检出限:测定蛋白质含量测定范围为[/font][font=Calibri]1-20mg[/font][font=宋体]蛋白质。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]干扰物:硫酸铵、[/font][font=Calibri]Tris[/font][font=宋体]缓冲液和某些氨基酸等。[/font][/font][font=宋体] [/font][font=宋体]适用范围:常用于需要快速,但并不需要十分精确的蛋白质测定。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体] [/font][font=宋体][b][font=宋体]④[/font][font=Calibri]Lowry [/font][font=宋体]法[/font][/b][/font][font=宋体] [/font][font=宋体][font=Calibri]Lowry [/font][font=宋体]法是双缩脲法的发展,结合了双缩脲试剂和酚试剂与蛋白质的反应,是最灵敏的蛋白质测定方法之一,在生物化学领域得到广泛的应用,目前分为基本法和改良简易法,改良简易法可获得与基本法相近的结果。[/font][/font][font=宋体] [/font][font=宋体]基本法实验原理:[/font][font=宋体] [/font][font=宋体][font=宋体]显色原理与双缩尿法相同,但加入了[/font][font=Calibri]Folin-[/font][font=宋体]酚酞试剂,以增加显色量,从而提高检测蛋白质的灵敏度。这两种显色反应产生深兰色的原因是:①在碱性条件下,蛋白质中的肽键与铜结合生成复合物。②[/font][font=Calibri]Folin[/font][font=宋体]一酚试剂中的磷钼酸盐一磷钨酸盐被蛋白质中的酪氨酸和苯丙氨酸残基还原,产生深兰色(钼兰和钨兰的混合物)。在一定的条件下,兰色深度与蛋白的量成正比。[/font][/font][font=宋体] [/font][font=宋体]特点:[/font][font=宋体] [/font][font=宋体]优点:灵敏度高。[/font][font=宋体] [/font][font=宋体]缺点:耗费时间长,操作时间需精准控制,标准曲线绘制麻烦,专一性较差,干扰物质比较多。[/font][font=宋体] [/font][font=宋体][font=宋体]检出限:可检测的最低蛋白质量达[/font][font=Calibri]5ug[/font][font=宋体]。通常测定范围是[/font][font=Calibri]20~250ug[/font][font=宋体]。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]干扰物:酚类、柠檬酸、硫酸铵、[/font][font=Calibri]Tris[/font][font=宋体]缓冲液、甘氨酸、糖类、甘油等。[/font][/font][font=宋体] [/font][font=宋体]适用范围:除蛋白含量测定,也可用于酪氨酸和色氨酸的定量测定。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体] [/font][font=宋体][b]⑤考马斯亮蓝法[/b][/font][font=宋体] [/font][font=宋体]实验原理:[/font][font=宋体] [/font][font=宋体][font=宋体]考马斯亮蓝[/font][font=Calibri]G-250[/font][font=宋体]染料,在酸性溶液中与蛋白质结合,使染料的最大吸收峰的位置([/font][font=Calibri]max[/font][font=宋体]),由[/font][font=Calibri]465mm[/font][font=宋体]变为[/font][font=Calibri]595nm[/font][font=宋体],溶液的颜色也由棕黑色变为蓝色。经研究认为,染料主要是与蛋白质中的碱性氨基酸(特别是精氨酸)和芳香族氨基酸残基相结合。在[/font][font=Calibri]595mm[/font][font=宋体]下测定的吸光度值[/font][font=Calibri]A595[/font][font=宋体],与蛋白质浓度成正比。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体]方法特点:[/font][font=宋体] [/font][font=宋体][font=宋体]优点:灵敏度比[/font][font=Calibri]Lowry[/font][font=宋体]高约[/font][font=Calibri]4[/font][font=宋体]倍,高效率、检测过程简便、只需要一种试剂,抗干扰能力强。[/font][/font][font=宋体] [/font][font=宋体]缺点:测定误差大,不适用于不同蛋白的检测。[/font][font=宋体] [/font][font=宋体][font=宋体]检出限:其最低蛋白质检测量可达[/font][font=Calibri]1ug[/font][font=宋体]。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]干扰物:干扰物质少,但去污剂、[/font][font=Calibri]TritonX-100[/font][font=宋体]、十二烷基硫酸钠、[/font][font=Calibri]0.1N[/font][font=宋体]的[/font][font=Calibri]NaOH[/font][font=宋体]会干扰实验测定。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体] [/font][font=宋体][b]蛋白质含量测定方法选择[/b][/font][font=宋体] [/font][font=宋体]蛋白质含量测定时,考虑以下因素后选定适用的检测方法。[/font][font=宋体] [/font][font=宋体]①实验对测定所要求的灵敏度和精确度;[/font][font=宋体] [/font][font=宋体]②蛋白质的性质;[/font][font=宋体] [/font][font=宋体]③溶液中存在的干扰物质;[/font][font=宋体] [/font][font=宋体]④测定所要花费的时间。[/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供多种类型的[url=https://cn.sinobiological.com/resource/protein-review][b]蛋白资源[/b][/url],不仅有重组蛋白服务还有各种大咖讲座,详情可以关注[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review[/font][/font][font=Calibri] [/font]
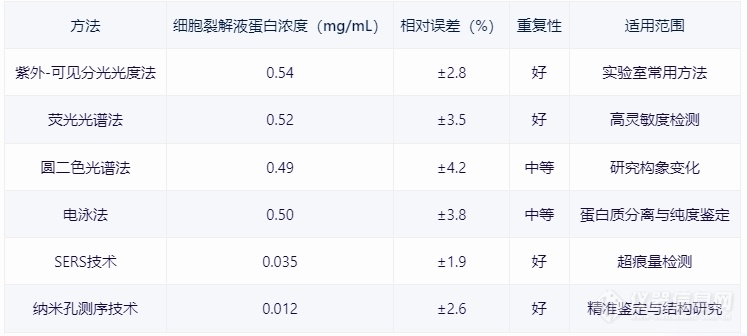
[b][font=宋体]一、引言[/font][/b][font=宋体] [/font][font=宋体]蛋白质浓度测定是生物化学实验中的一项基本操作,对于了解蛋白质的性质、评估实验效果以及开展生物学研究具有重要意义。本文将详细介绍蛋白浓度测定的方法、技术原理、最新进展及其在生物医学研究中的应用。[/font][font=宋体] [/font][b][font=宋体]二、蛋白浓度测定方法概述[/font][/b][font=宋体] [/font][font=宋体][font=宋体]①紫外[/font][font=Calibri]-[/font][font=宋体]可见分光光度法[/font][/font][font=宋体]原理:利用蛋白质中特定氨基酸(如酪氨酸、色氨酸)在紫外光区的吸收特性,通过测量吸光度值来计算蛋白质浓度。[/font][font=宋体] [/font][font=宋体]应用:适用于大多数蛋白质的测定,尤其在实验室中广泛使用。[/font][font=宋体] [/font][font=宋体]②荧光光谱法[/font][font=宋体]原理:利用荧光染料与蛋白质结合后产生的荧光光谱,通过测量荧光强度来计算蛋白质浓度。[/font][font=宋体] [/font][font=宋体]应用:适用于具有荧光特性的蛋白质,具有高灵敏度。[/font][font=宋体] [/font][font=宋体]③圆二色光谱法[/font][font=宋体]原理:利用圆二色光谱分析蛋白质的构象变化,从而推算蛋白质浓度。[/font][font=宋体] [/font][font=宋体]应用:常用于研究蛋白质的构象变化和稳定性。[/font][font=宋体] [/font][font=宋体]④电泳法[/font][font=宋体]原理:利用电泳技术将蛋白质分离,通过测量电泳带亮度或面积来计算蛋白质浓度。[/font][font=宋体] [/font][font=宋体]应用:常用于蛋白质分离和纯度鉴定。[/font][font=宋体] [/font][b][font=宋体]三、进展与技术优化[/font][/b][font=宋体] [/font][font=宋体][font=宋体]①表面增强拉曼散射([/font][font=Calibri]SERS[/font][font=宋体])技术[/font][/font][font=宋体]原理:利用金属表面增强拉曼散射效应,提高信号强度,从而提高检测灵敏度。[/font][font=宋体] [/font][font=宋体]应用:适用于痕量蛋白质的检测,具有高灵敏度和高分辨率。[/font][font=宋体] [/font][font=宋体]②纳米孔测序技术[/font][font=宋体]原理:利用纳米孔测序技术对蛋白质进行测序,通过电导变化检测蛋白质序列信息。[/font][font=宋体] [/font][font=宋体]应用:有助于蛋白质的精准鉴定和分子结构研究。[/font][font=宋体] [/font][font=宋体][b]四、[/b][/font][b][font=宋体]实际应用案例分析[/font][/b][font=宋体] [/font][align=center][img=蛋白浓度测定案例,690,310]https://ng1.17img.cn/bbsfiles/images/2024/01/202401231537106869_2656_5907840_3.png!w690x310.jpg[/img][font=宋体] [/font][/align][font=宋体][font=宋体]详情可以关注义翘神州更多[url=https://cn.sinobiological.com/resource/protein-review][b]蛋白资源[/b][/url]详情:[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review[/font][/font][b][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b]
食品中蛋白质含量测定仪的优点主要体现在以下几个方面: 检测速度快:能够在短时间内完成大量样品的检测,大大提高了检测效率,使食品生产厂家能够快速获取检测结果,及时调整生产策略。 操作简单:仪器操作简单易用,用户只需按照说明书进行操作即可完成检测,无需复杂的操作步骤和专业技能,降低了操作难度。 准确度高:采用先进的检测技术,如光谱技术、化学分析方法等,能够确保测量结果的准确性和可靠性,为食品生产厂家提供准确的数据支持。 应用广泛:适用于各类食品中蛋白质含量的检测,如乳制品、肉制品、豆制品等,满足了不同食品生产厂家的检测需求。 安全性高:使用食品中蛋白质含量测定仪可以避免直接接触样品,降低了交叉感染的风险,保障了检测人员的安全。 智能化程度高:一些先进的食品中蛋白质含量测定仪还采用了安卓智能操作系统,具有网线连接、Wi-Fi联网上传、GPRS无线远传等功能,可以快速上传数据,实现远程监控和管理。 稳定性强:仪器具有稳定的工作性能和较长的使用寿命,保证了长期使用的可靠性。 综上所述,食品中蛋白质含量测定仪具有检测速度快、操作简单、准确度高、应用广泛、安全性高、智能化程度高和稳定性强等优点,为食品生产和质量控制提供了有力的支持。[img=,690,690]https://ng1.17img.cn/bbsfiles/images/2024/05/202405151149314403_9648_4214615_3.jpg!w690x690.jpg[/img]
[font=宋体][url=https://cn.sinobiological.com/resource/protein-review/protein-purification-protocol][b]蛋白纯化[/b][/url]是生物实验室和制药工业中至关重要的技术。它涉及从复杂的混合物中分离出目标蛋白质,同时保持蛋白质的结构和功能。了解蛋白纯化的原理和步骤不仅有助于提高实验效率,还可以降低实验失败的风险。在本篇文章中,我们将详细介绍蛋白纯化的定义、原理和步骤。[/font][font=宋体] [/font][font=宋体][b]蛋白纯化定义及原理[/b][/font][font=宋体] [/font][font=宋体]蛋白纯化是生物研究常用的一种技术,是指从蛋白混合物中得到纯度较高的某种蛋白的过程。根据样本和杂质的特性选择适合的纯化方法,纯化技术的选择要简单化,并且要产生最佳的纯化效果。如果纯度的要求很高,再增加一个离子交换或疏水作用色谱的额外中间步骤。不过尽量尝试使用尽可能少的步骤,因为步骤增多会降低总蛋白产出量。亲和步骤常用重力柱,有时其他色谱步骤中会使用恒压泵,然而蛋白纯化系统将提供更多的控制,可获得更详细的目标蛋白和杂质信息,并为色谱柱提供更好的保护。[/font][font=宋体] [/font][font=宋体][b]可溶性蛋白纯化的步骤[/b][/font][font=宋体] [/font][font=宋体]用于分离可溶性重组或非重组蛋白的分离方法取决于蛋白的内在生理化学特性(被标记蛋白除外)。典型的纯化方案如下所示(使用离子交换色谱法)。[/font][font=宋体] [/font][font=宋体][font=Calibri]1[/font][font=宋体]、细胞裂解液[/font][/font][font=宋体]澄清裂解液[/font][font=宋体][font=宋体]离心([/font][font=Calibri]60000[/font][font=宋体]×[/font][font=Calibri]g[/font][font=宋体],[/font][font=Calibri]90 [/font][font=宋体]分钟)过滤或脱盐和交换缓冲液[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2[/font][font=宋体]、澄清裂解液[/font][/font][font=宋体]①用亲和法[/font][font=宋体][font=宋体]([/font][font=Calibri]1[/font][font=宋体])进行[/font][font=Calibri]DEAE-Sepharose[/font][font=宋体]离子交换[/font][/font][font=宋体]交换缓冲液[/font][font=宋体] [/font][font=宋体][font=宋体]([/font][font=Calibri]2[/font][font=宋体])进行离子交换[/font][/font][font=宋体][font=宋体]? 弱阳离子[/font][font=Calibri]-[/font][font=宋体]羧甲基[/font][/font][font=宋体][font=宋体]? 强阳离子[/font][font=Calibri]-[/font][font=宋体]甲基磺酸盐[/font][/font][font=宋体][font=宋体]? 强阴离子[/font][font=Calibri]-[/font][font=宋体]季铵盐[/font][/font][font=宋体][font=宋体]? 弱阴离子[/font][font=Calibri]-[/font][font=宋体]二乙氨基乙基[/font][/font][font=宋体]? 磷酸纤维素[/font][font=宋体] [/font][font=宋体][font=宋体]([/font][font=Calibri]3[/font][font=宋体])用其他色谱方法[/font][/font][font=宋体]? 染料基质[/font][font=宋体]? 疏水[/font][font=宋体]? 羟磷灰石[/font][font=宋体]? 层析聚焦[/font][font=宋体] [/font][font=宋体]②浓缩[/font][font=宋体] [/font][font=宋体]③进行凝胶过滤[/font][font=宋体]④无菌过滤[/font][font=宋体] [/font][font=宋体][font=Calibri]3[/font][font=宋体]、经纯化的蛋白[/font][/font][font=宋体] [/font][font=宋体][b]包涵体蛋白的折叠与纯化[/b][/font][font=宋体]在大肠杆菌中表达的重组蛋白位于细胞裂解后低速颗粒部分,它们高度聚集。包涵体通常来自于细胞质(或细胞周质,如使用了分泌载体)中的蛋白聚集。如前所述,由于与细菌核酸的相互作用,蛋白也可以位于低速或高速颗粒部分中。[/font][font=宋体] [/font][font=宋体][font=宋体]采用蛋白变性剂提取蛋白,如盐酸胍[/font][font=Calibri](Gu[/font][font=宋体][/font][font=Calibri]HCl)[/font][font=宋体]、尿素或有机酸。使用还原剂二硫苏糖醇[/font][font=Calibri](DTT)[/font][font=宋体]防止人工二硫键形成(尤其是分子间键)。变性后的蛋白可以通过各种方法纯化后再折叠,也可以直接折叠。通常建议在折叠前进行一些纯化(如[/font][font=Calibri]Gu[/font][font=宋体][/font][font=Calibri]HCl[/font][font=宋体]中的凝胶过滤),因为这往往会带来更高的折叠产率。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]原文转载:[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/protein-purification-protocol[/font][/font]
[font=宋体]蛋白纯化介质主要应用于研究目的蛋白的结构、功用以及相互作用的和过程中。比如:在蛋白纯化过程中,由于[url=https://cn.sinobiological.com/resource/protein-review/protein-purification-by-ac][b]亲和层析法[/b][/url]的选择性和结合力较强,分辨率也高。所以,亲和层析法是一种常用的蛋白、抗体纯化方法,天地人和生物多种简单易用的亲和纯化介质,适用于批量或利用重力进行纯化,可以高效、便捷、可靠地从品中分离蛋白和抗体,为下游应用提供有力保证。[/font][font=宋体][b]亲和层析法的原理:[/b][/font][font=宋体][font=宋体]亲和层析是应用生物高分子与配基可逆结合的原理,将配基通过共价键牢固结合于载体上而制得的层析系统。这种可逆结合的作用主要是靠生物高分子对它的配基的空间结构的识别。常用的生物亲和关系有酶[/font][font=Calibri]-[/font][font=宋体]底物、底物类似物、抑制剂、激活剂、辅因子,抗体[/font][font=Calibri]-[/font][font=宋体]抗原,激素[/font][font=Calibri]-[/font][font=宋体]受体蛋白、载体蛋白,外源凝集素[/font][font=Calibri]-[/font][font=宋体]多糖、糖蛋白、细胞表面受体,核酸[/font][font=Calibri]-[/font][font=宋体]互补核苷酸序列、组蛋白、核酸结合蛋白等,具有高效、简单、快速的优点,是当前最为理想的分离纯化蛋白的方法。[/font][/font][b][font=宋体][font=宋体]亲和层析的操作步骤[/font][font=Calibri]:[/font][/font][/b][font=宋体] [/font][font=宋体][font=宋体]在亲和层析中,蛋白在影响蛋白[/font][font=Calibri]([/font][font=宋体]或标签[/font][font=Calibri])[/font][font=宋体]与其配体之间结合的条件下被加载到柱子上。在不破坏特定相互作用但能破坏污染蛋白与固定相之间任何非特异性相互作用的条件下洗涤结合的蛋白。然后用含有竞争性分子的缓冲液或破坏所有蛋白[/font][font=Calibri]/[/font][font=宋体]蛋白相互作用的条件洗脱结合的蛋白。竞争分子与配体结合,取代目标蛋白,这种竞争分子通常通过另一种色谱流程或透析法从目标蛋白中去除。[/font][/font][font=宋体] [/font][table][tr][td][b][font=微软雅黑][color=#232323]亲和层析配体和洗脱条件[/color][/font][/b][/td][td][font=微软雅黑] [/font][/td][td][font=微软雅黑] [/font][/td][/tr][tr][td][b][font=微软雅黑][color=#232323]需纯化的蛋白[/color][/font][/b][/td][td][b][font=微软雅黑][color=#232323]配体[/color][/font][/b][/td][td][b][font=微软雅黑][color=#232323]洗脱条件[/color][/font][/b][/td][/tr][tr][td][font=微软雅黑][color=#232323]抗体(抗原特异性)[/color][/font][/td][td][font=微软雅黑][color=#232323]抗原肽[/color][/font][/td][td][font=微软雅黑][color=#232323]游离肽[/color][/font][/td][/tr][tr][td][font=微软雅黑][color=#232323]多聚组氨酸标签蛋白[/color][/font][/td][td][font=微软雅黑][color=#232323]Ni2+或Co2+[/color][/font][/td][td][font=微软雅黑][color=#232323]咪唑或游离组氨酸[/color][/font][/td][/tr][tr][td][font=微软雅黑][color=#232323]FLAG标签蛋白[/color][/font][/td][td][font=微软雅黑][color=#232323]FLAG特异性抗体[/color][/font][/td][td][font=微软雅黑][color=#232323]FLAG肽或低pH值[/color][/font][/td][/tr][tr][td][font=微软雅黑][color=#232323]GST标签蛋白[/color][/font][/td][td][font=微软雅黑][color=#232323]还原型谷胱甘肽[/color][/font][/td][td][font=微软雅黑][color=#232323]游离谷胱甘肽[/color][/font][/td][/tr][tr][td][font=微软雅黑][color=#232323]Myc标签蛋白[/color][/font][/td][td][font=微软雅黑][color=#232323]Myc特异性抗体[/color][/font][/td][td][font=微软雅黑][color=#232323][font=微软雅黑]低[/font][font=微软雅黑]pH[/font][/color][/font][/td][/tr][tr][td][font=微软雅黑][color=#232323]抗体(类特异性)[/color][/font][/td][td][font=微软雅黑][color=#232323][font=微软雅黑]蛋白[/font][font=微软雅黑]A、G和L或精蛋白[/font][/color][/font][/td][td][font=微软雅黑][color=#232323]pH极端值[/color][/font][/td][/tr][tr][td][font=微软雅黑][color=#232323]DNA结合蛋白[/color][/font][/td][td][font=微软雅黑][color=#232323]肝素[/color][/font][/td][td][font=微软雅黑][color=#232323]高离子强度[/color][/font][/td][/tr][/table][font=宋体][font=宋体]更多详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/protein-purification-by-ac[/font][/font]
国外的核酸蛋白检测仪比较起来哪个厂家的比较好,给推荐几个,价位又是什么样的,谢谢