凝胶色谱法GPC[b]分析原理:[/b]样品通过凝胶柱时,按分子的流体力学体积不同进行分离,大分子先流出[b]谱图的表示方法:[/b]柱后流出物浓度随保留值的变化[b]提供的信息:[/b]高聚物的平均分子量及其分布根据所用凝胶的性质,可以分为使用水溶液的凝胶过滤色谱法(GFC)和使用有机溶剂的凝胶渗透色谱法(GPC)。
我们学习分离血红蛋白时,书上提到凝胶色谱法分离蛋白质原理是蛋白质分子量大小不同导致有些蛋白质能进入凝胶颗粒,另一些不能,所以迁移速度不同,将分子量不同的蛋白质分离。既然这样,那为什么不是因为蛋白质分子大小不同呢? [b]问题补充:[/b]关键在于为什么是根据蛋白质分子量大小而不是蛋白质分子大小(所占空间)分离呢 小分子蛋白可以在小孔内穿过 从而增加了分离时所走的路程 最后被分离。大分子蛋白主要是通过凝胶颗粒之间的空隙通过 因此路线相对较短最先被分离。 只是做题时这一题选分子量而不选分子大小
凝胶色谱法开关电源1.2 分离纯化蛋白质的原理与方法──凝胶色谱法(分子筛效应)凝胶是一些由多糖类化合物构成的多孔球体,当相对分子质量不同的蛋白质通过凝胶时,相对分子质量较小的蛋白质直径小于凝胶网孔,由于静电吸附和扩散作用容易进入凝胶内部的通道,可以自由地进入凝胶颗粒的网孔,在向下移动的过程中,它们从凝胶颗粒的网孔扩散到凝胶颗粒间的孔隙,再进入另一凝胶颗粒的网孔,如此不断地进出,使流程增长,而最后流出层析柱。而相对分子质量较大的蛋白质无法进入凝胶颗粒的网孔,只能沿着凝胶颗粒间的孔隙,随着洗脱液流动,流程较短,因此首先流出层析柱。分子量介于二者之间的物质,虽然能够进入凝胶网孔,但比小分子难,因此进入凝胶网孔的几率比小分子小,向下移动的速度比小分子快,而比大分子慢。相对分子质量不同的蛋白质分子因此得以分离。需要注意的是,有部分小分子蛋白质未进入凝胶内部,而在外部移动,因此,如果需要得到纯度更高的蛋白质分子,可将色谱柱中的凝胶溶液进行平衡后进行再次冼脱和分离。1.3 鉴定蛋白质纯度的原理与方法──电泳蛋白质分子的基本单位是氨基酸,氨基酸的一些基团在一定的pH下会发生水解或电离从而带有电荷。但总的来说蛋白质分子一般带有负电。在电场的作用下,带电的蛋白质分子会向着电泳槽中的正极方向移动。由于样品中各种蛋白质分子净电荷的量的差异以及蛋白质分子本身的大小等因素,使蛋白质分子产生不同的迁移速率,从而将样品中各种蛋白质分子分离开。由于蛋白质分子带电电荷比较复杂,净电荷总量与蛋白质分子的质量不成正比,而蛋白质分子的质量又是衡定的,电泳时在带电量和分子质量两种因素的作用下会产生迁移速率的复杂化,不能正确地将分子质量不同的蛋白质分子分离开,因此,实际操作中,一般会将蛋白质分子与SDS(十二烷基硫酸钠)发生反应形成蛋白质—SDS复合物,由于SDS所带负电荷的量大大超过蛋白质分子原有的电荷量,因此掩盖了不同种蛋白质间的电荷差异,使蛋白质的迁移率完全取决于蛋白质分子质量的大小。在电场条件下,分子量大的蛋白质迁移率慢,离前沿较远,而分子量小的蛋白质迁移快,离前沿较近。这样,不同分子量大小的蛋白质得到了分离。如果蛋白质的纯度高,迁移率一致,就会形成前沿整齐、清晰的条带。www.peakoil.com.cn
凝胶色谱法介绍
凝胶色谱法又叫凝胶色谱技术,是六十年代初发展起来的一种快速而又简单的分离分析技术,由于设备简单、操作方便,不需要[url=http://baike.baidu.com/view/435064.htm]有机溶剂[/url],对高分子物质有很高的分离效果。凝胶色谱法又称[url=http://baike.baidu.com/view/1395520.htm]分子排阻色谱法[/url]。凝胶色谱法主要用于[url=http://baike.baidu.com/view/328669.htm]高聚物[/url]的相对分子质量分级分析以及相对分子质量分布测试。根据分离的对象是水溶性的化合物还是有机溶剂可溶物,又可分为凝胶过滤色谱(GFC)和[url=http://baike.baidu.com/view/1966792.htm]凝胶渗透色谱[/url](GPC)。 GFC一般用于分离水溶性的大分子,如[url=http://baike.baidu.com/view/728282.htm]多糖类[/url]化合物。凝胶的代表是葡萄糖系列,洗脱溶剂主要是水。凝胶渗透色谱法主要用于有 机溶剂中可溶的高聚物 ([url=http://baike.baidu.com/view/237319.htm]聚苯乙烯[/url]、聚氯已烯、[url=http://baike.baidu.com/view/11277.htm]聚乙烯[/url]、[url=http://baike.baidu.com/view/591731.htm]聚甲基丙烯酸甲酯[/url]等)相对分子质量分布分析及分离,常用的[url=http://baike.baidu.com/view/65842.htm]凝胶[/url]为交联聚苯乙烯凝胶,洗脱溶剂为四氢呋喃等有机溶剂。凝胶色谱不但可以用于分离测定高聚物的相对分子质量和相对分子质量分布,同时根据所用凝胶填料不同,可分离油溶性和水溶 性物质,分离相对分子质量的范围从几百万到100以下。近年来,凝胶色谱也广泛用于分离小分子化合物。化学结构不同但相对分子质量相近的物质,不可能通过凝胶色谱法达到完全的分离纯化的目的。凝胶色谱主要用于高聚物的相对分子质量分级分析以及相对勿子质量分布测试。目前已经被[url=http://baike.baidu.com/view/24503.htm]生物化学[/url]、[url=http://baike.baidu.com/view/2461.htm]分子生物学[/url]、[url=http://baike.baidu.com/view/264316.htm]生物工程学[/url]、[url=http://baike.baidu.com/view/2011973.htm]分子免疫学[/url]以及[url=http://baike.baidu.com/view/7490.htm]医学[/url]等有关领域广泛采用,不但应用于科学实验研究,而且已经大规模地用于工业生产。
[color=#444444]凝胶色谱法中相同高分子量的高分子支链多的先出来还是少的先出来[/color]
谁有施良和编的《凝胶色谱法》?在其他网上看到有 但是没有积分下不了![em09509]
某凝胶色谱法分离抗生素聚合物,要求kav0.3的不超过2%,而kav0.1的不超过0.5%,流速为0.8ml/min,柱子Tosoh taskkav0.3的峰有1个,而kav0.1的没有。我的问题是如果改成流速0.5ml/min,可以分离出更多的峰,kav0.3的峰有3个,而kav0.1的没有。那么这样做有意义吗?Kav受流速的影响吗?
请教如何用凝胶色谱法进行食品多农残样品处理?
谁能提供给我一些关于凝胶色谱法测定高分子物质多糖的例子,谢谢了另外凝胶色谱法测定多糖的流动相和凝胶选用什么比较合适,谢谢!
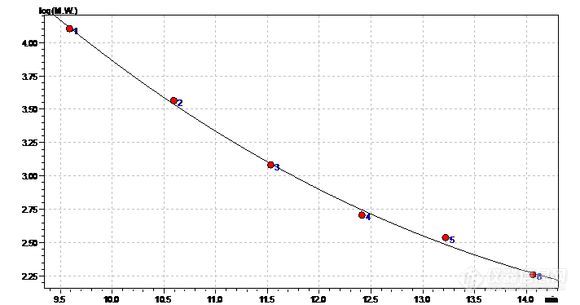
[color=#333333]用岛津的凝胶渗透色谱(色谱柱 TSK-gel GW PWXL2500)和软件,算酶解寡糖分子的分子量, 结果相差很大,用其他方法算, 大约1000-2000Da(数均),而用凝胶色谱法大约只有200-300。几乎就是差一个数量级。 但是,多个样品之间的变化规律,两种方法测是一致的,( 哪个大,哪个小,大多少,算出来都一样)。怀疑是软件计算出了什么问题,但是我找不出来。[/color][color=#333333]我用的是右旋糖酐做分子量标准,是个比较通用的标准了, 使用的方法,是测别的糖的方法,和文献里优化的方法不同,但是感觉应该还能用,最主要的几个峰还是有的。[/color][color=#333333]在此请问大家出的是什么问题,谢谢大家了。 [/color][color=#333333][img=,580,305]https://ng1.17img.cn/bbsfiles/images/2019/05/201905081545541636_4140_1849104_3.jpg!w580x305.jpg[/img][img=,580,148]https://ng1.17img.cn/bbsfiles/images/2019/05/201905081545545297_131_1849104_3.jpg!w580x148.jpg[/img][img=,580,148]https://ng1.17img.cn/bbsfiles/images/2019/05/201905081545548297_2890_1849104_3.jpg!w580x148.jpg[/img][/color]
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=42615]凝胶色谱法简介[/url]
凝胶色谱法的基本理论简介:凝胶色谱技术是六十年代初发展起来的一种快速而又简单的分离分技术,由于设备简单、操作方便,不需要有机溶剂,对高分子物质有很高的分离效果。内容: 目前已经被生物化学、分子生物学、生物工程学、分子免疫学以及医学等有关领域广泛采用,不但应用于科学实验研究,而且已经大规模地用于工业生产。基本理论(一) 分子筛效益 一个含有各种分子的样品溶液缓慢地流经凝胶色谱柱时,各分子在柱内同时进行着两种不同的运动:垂直向下的移动和无定向的扩散运动。大分子物质由于直径较大,不易进入凝胶颗粒的微孔,而只能分布颗粒之间,所以在洗脱时向下移动的速度较快。小分子物质除了可在凝胶颗粒间隙中扩散外,还可以进入凝胶颗粒的微孔中,即进入凝胶相内,在向下移动的过程中,从一个凝胶内扩散到颗粒间隙后再进入另一凝胶颗粒,如此不断地进入和扩散,小分子物质的下移速度落后于大分子物质,从而使样品中分子大的先流出色谱柱,中等分子的后流出,分子最小的最后流出,这种现象叫分子筛效应。 具有多孔的凝胶就是分子筛。各种分子筛的孔隙大小分布有一定范围,有最大极限和最小极限。分子直径比凝胶最大孔隙直径大的,就会全部被排阻在凝胶颗粒之外,这种情况叫全排阻。两种全排阻的分子即使大小不同,也不能有分离效果。直径比凝胶最小孔直径小的分子能进入凝胶的全部孔隙。如果两种分子都能全部进入凝胶孔隙,即使它们的大小有差别,也不会有好的分离效果。因此,一定的分子筛有它一定的使用范围。综上所述,在凝胶色谱中会有三种情况,一是分子很小,能进入分子筛全部的内孔隙;二是分子很大,完全不能进入凝胶的任何内孔隙;三是分子大小适中,能进入凝胶的内孔隙中孔径大小相应的部分。大、中、小三类分子彼此间较易分开,但每种凝胶分离范围之外的分子,在不改变凝胶种类的情况下是很难分离的。 对于分子大小不同,但同属于凝胶分离范围内各种分子,在凝胶床中的分布情况是不同的:分子较大的只能进入孔径较大的那一部分凝胶孔隙内,而分子的可进入较多的凝胶颗粒内,这样分子较大的在凝胶床内移动距离较短,分子较小的移动距离较长。于是分子较大的先通过凝胶床而分子较小的后通过凝胶床,这样就利用分子筛可将分子量不同的物质分离。另外,凝胶本身具有三维网状结构,大的分子在通过这种网状结构上的孔隙时阻力较大,小分子通过时阻力较小。分子量大小不同的多种成份在通过凝胶床时,按照分子量大小“排队,凝胶表现分子筛效应。(二) 色谱柱的重要参数⑴柱体积:柱体积是指凝胶装柱后,从柱的底板到凝胶沉积表面的体积。在色谱柱中充满凝胶的部分称为凝胶床,因引柱体积又称“床”体积,常用Vt 表示。⑵外水体积:色谱柱内凝胶颗粒间隙,这部分体积称外水体积,亦称间隙体积,常用Vo表示。⑶内水体积:因为凝胶为三维网状结构,颗粒内部仍有空间,液体可进入颗粒内部,这就分间隙的总和为内水体积,又称定相体积,常用Vi表示。 不包括固体支持物的体积(Vg)。⑷峰洗脱体积:是指被分离物质通过凝胶柱所需洗脱液有体积,常用Ve 表示。当使用样品的体积很少时,(与洗脱体积比较可以忽略不计),在洗脱图中,从加样到峰顶位置所用洗脱液体积为Ve。 当样品体积与洗脱体积比较不能忽略时,洗脱体积计算可以从样品体积的一半到峰顶位置。当样品很大时,洗脱体积计算可以从应用样品开始到洗脱峰升高的弯曲点(或半高处)。
看了本版上传的凝胶色谱法方面的书籍,如凝胶色谱法 施良和编 科学出版社 1980 O657.7/0832 纸版 ,凝胶渗透色谱法的进展及其应用 成跃祖编 中国石化出版社 1993 O658.9/5363 纸版 ,时间都比较老了,大家能否推荐几本最新出版的、比较好的凝胶色谱法方面的书籍?
如题,请问凝胶色谱的原理是什么?
凝胶色谱的原理是什么?
请问哪位做过Sephadex LH-20凝胶色谱法分离高分子物质。本人想利用此凝胶,希望得到帮助,哪位用过请留个联系QQ。谢谢。
凝胶色谱法简介 凝胶色谱技术是六十年代初发展起来的一种快速而又简单的分离分技术,由于设备简单、操作方便,不需要有机溶剂,对高分子物质有很高的分离效果。目前已经被生物化学、分子生物学、生物工程学、分子免疫学以及医学等有关领域广泛采用,不但应用于科学实验研究,而且已经大规模地用于工业生产。 一、基本理论 (一) 分子筛效益 一个含有各种分子的样品溶液缓慢地流经凝胶色谱柱时,各分子在柱内同时进行着两种不同的运动:垂直向下的移动和无定向的扩散运动。大分子物质由于直径较大,不易进入凝胶颗粒的微孔,而只能分布颗粒之间,所以在洗脱时向下移动的速度较快。小分子物质除了可在凝胶颗粒间隙中扩散外,还可以进入凝胶颗粒的微孔中,即进入凝胶相内,在向下移动的过程中,从一个凝胶内扩散到颗粒间隙后再进入另一凝胶颗粒,如此不断地进入和扩散,小分子物质的下移速度落后于大分子物质,从而使样品中分子大的先流出色谱柱,中等分子的后流出,分子最小的最后流出,这种现象叫分子筛效应。具有多孔的凝胶就是分子筛。各种分子筛的孔隙大小分布有一定范围,有最大极限和最小极限。分子直径比凝胶最大孔隙直径大的,就会全部被排阻在凝胶颗粒之外,这种情况叫全排阻。两种全排阻的分子即使大小不同,也不能有分离效果。直径比凝胶最小孔直径小的分子能进入凝胶的全部孔隙。如果两种分子都能全部进入凝胶孔隙,即使它们的大小有差别,也不会有好的分离效果。因此,一定的分子筛有它一定的使用范围。综上所述,在凝胶色谱中会有三种情况,一是分子很小,能进入分子筛全部的内孔隙;二是分子很大,完全不能进入凝胶的任何内孔隙;三是分子大小适中,能进入凝胶的内孔隙中孔径大小相应的部分。大、中、小三类分子彼此间较易分开,但每种凝胶分离范围之外的分子,在不改变凝胶种类的情况下是很难分离的。对于分子大小不同,但同属于凝胶分离范围内各种分子,在凝胶床中的分布情况是不同的:分子较大的只能进入孔径较大的那一部分凝胶孔隙内,而分子的可进入较多的凝胶颗粒内,这样分子较大的在凝胶床内移动距离较短,分子较小的移动距离较长。于是分子较大的先通过凝胶床而分子较小的后通过凝胶床,这样就利用分子筛可将分子量不同的物质分离。另外,凝胶本身具有三维网状结构,大的分子在通过这种网状结构上的孔隙时阻力较大,小分子通过时阻力较小。分子量大小不同的多种成份在通过凝胶床时,按照分子量大小“排队,凝胶表现分子筛效应。 二)色谱柱的重要参数 ⑴柱体积:柱体积是指凝胶装柱后,从柱的底板到凝胶沉积表面的体积。在色谱柱中充满凝胶的部分称为凝胶床,因引柱体积又称“床”体积,常用Vt 表示。 ⑵外水体积:色谱柱内凝胶颗粒间隙,这部分体积称外水体积,亦称间隙体积,常用Vo表示。 ⑶内水体积:因为凝胶为三维网状结构,颗粒内部仍有空间,液体可进入颗粒内部,这就分间隙的总和为内水体积,又称定相体积,常用Vi表示。 不包括固体支持物的体积(Vg)。 ⑷峰洗脱体积:是指被分离物质通过凝胶柱所需洗脱液有体积,常用Ve 表示。当使用样品的体积很少时,(与洗脱体积比较可以忽略不计),在洗脱图中,从加样到峰顶位置所用洗脱液体积为Ve。 当样品体积与洗脱体积比较不能忽略时,洗脱体积计算可以从样品体积的一半到峰顶位置。当样品很大时,洗脱体积计算可以从应用样品开始到洗脱峰升高的弯曲点(或半高处)。 二、凝胶的种类及性质 (一) 交联葡聚糖凝胶 ⑴Sephadex G交联葡聚糖的商品名为Sephndex,不同规格型号的葡聚糖用英文字母G表示,G后面的阿拉伯数为凝胶得水值的10倍。例如,G-25为每克凝胶膨胀时吸水2.5克,同样G-200克每克千胶吸水20克。交联葡聚糖凝胶的种类有G-10,G-15,G-25,G-50,G-75,G-100,G-150,和G-200。因此,“G”反映,凝胶的交联程度,膨胀程度及分部范围。 ⑵Sephadex LH-20,是─Sephadex G-25的羧丙基衍生物, 能溶于水及亲脂溶剂,用于分离不溶于水的物质。 (二) 琼脂糖凝胶: 商品名很多,常见的有,Sepharose(瑞典,pharmacia ),Bio-Gel-A(美国Bio-Rad)等。琼脂糖凝胶是依靠糖链之间的次级链如氢键来维持网状结构,网状结构的疏密依靠琼脂糖的浓度。一般情况下,它的结构是稳定的,可以在许多条件下使用(如水,pH4-9范围内的盐溶液)。琼脂糖凝胶在40℃以上开始融化,也不能高压消毒,可用化学灭菌活处理。 (三)聚丙烯酰胺凝胶:是一种人工合成凝胶,是以丙烯酰胺为单位, 由甲叉双丙烯酰胺交联成的,经干燥粉碎或加工成形制成粒状,控制交联剂的用量可制成各种型号的凝胶。交联剂越多,孔隙越小。聚丙烯酰胺凝胶的商品为生物胶-P (Bio-Gel P),由美国Bio-Rod厂生产,型号很多,从P-2至P-300共10种,P 后面的数字再乘1000就相当于该凝胶的排阻限度。 (四)聚苯乙烯凝胶商品为Styrogel , 具有大网孔结构, 可用于分离分子量1600到40,000,000的生物大分子,适用于有机多聚物,分子量测定和脂溶性天然物的分级,凝胶机械强度好,洗脱剂可用甲基亚砜。 三、实验技术 (一)层析柱 层析柱是凝胶层析技术中的主体,一般用玻璃管或有机玻璃管。层析柱的直径大小不影响分离度,样品用量大,可加大柱的直径,一般制备用凝胶柱,直径大于2厘米,但在加样时应将样品均匀分布于凝胶柱床面上。此外, 直径加大,洗脱液体体积增大,样品稀释度大。分离度取决于柱高,为分离不同组分,凝胶柱床必须有适宜的高度,分离度与柱高的平方根相关,但由于软凝胶柱过高挤压变形阻塞,一般不超过1米。分族分离时用短柱,一般凝胶柱长20-30厘米,柱高与直径的比较5:1─10:1,凝胶床体积为样品溶液体积的4-10倍。 分级分离时柱高与直径之线为20:1─100:1,常用凝胶柱有50×25厘米,10×25厘米。层析柱滤板下的死体积应尽可能的小,如果支掌滤板下的死体积大,被分离组分之间重新混合的可能性就大,其结果是影响洗脱峰形,出现拖尾出象,降低分辩力。在精确分离时,死体积不能超过总床体积的1/1000。 (二)凝胶的选择 根据所需凝胶体积,估计所需干胶的量。 一般葡聚糖凝胶吸水后的凝胶体积约为其吸水量的2倍,例如Sephadex G-20的吸水量为20,1 克Sephadex G─200吸水后形成的凝胶体积约40ml。凝胶的粒度也可影响层析分离效果。粒度细胞分离效果好,但阻力大,流速慢。一般实验室分离蛋白质采用100-200号筛目的的Sephadex G-200效果好, 脱盐用Sephadex G-25、G-50,用粗粒,短柱,流速快。 (三)凝胶的制备 商品凝胶是干燥的颗粒使用前需直接在欲使用的洗脱液中膨胀。为了加速膨胀,可用加热法,即在沸水浴中将湿凝胶逐渐升温至近沸,这样可大大中速膨胀,通常在1-2小时内即可完成。特别是在使用软胶时, 自然膨胀需24小时至数天,而用加热法在几小时内就可完成。这种方法不但节约时间,而且还可消毒,除去凝胶中污染的细菌和排除胶内的空气。 (四)样品溶液的处理 样品溶液如有沉淀应过滤或离心除去,如含脂类可高速离心或通过Sephadex G-15短柱除去。样品的粘度不可大,含蛋白为超过4%,粘度高影响分离效果。上柱样品液的体积根据凝胶床体积的分离要求确定。分离蛋白质样品的体积为凝胶床的1-4%(一般约0.5-2ml),进行分族分离时样品液可为凝胶床的10%,在蛋白质溶液除盐时,样品可达凝胶床的20-30%。 分级分离样品体积要小,使样品层尽可能窄,洗脱出的峰形较好。 (五)防止微生物的污染 交联葡聚糖和琼脂糖都是多糖类物质,防止微生物的生长,在凝胶层析中十分重要,常用的抑菌剂有: ⑴叠氨钠(NaN3)在凝胶层析中只要用0.02%叠氮钠已足够防止微生物的生长,叠氮钠易溶一水,在20℃时约为40%;它不与蛋白质或碳水化合物相互作用,因此叠氮钠不影响抗体活力;不会改变蛋白质和碳水化合物的层析我特性。叠氮钠可干扰荧光标记蛋白质。⑵可乐酮[Cl3C-C(OH)(CH3)2]在凝胶层析中使用浓度为0.01-0.02%。在微酸性溶液中它的杀菌效果最佳,在强碱性溶液中或温度高于60℃时易引起分解而失效。⑶乙基汞代巯基水杨酸钠 在凝胶层析中作为抑菌剂使用浓度为0.05-0. 01%。在微酸性溶液中最为有效。重金属离子可使乙基代巯基的物质结合,因而包含疏基的蛋白质可在不同程度上降低它的抑菌效果。⑷苯基汞代盐 在凝胶层析中使用浓度为0.001-0.01%。在微碱性溶液中抑效果最佳,长时间放置时可与卤素、硝酸根离子作用而产生沉淀;还原剂可引起此化合物分解;含疏基的物质亦可降低或抑制它的抑菌作用。 百特纯大分子(武汉)科技提供葡聚糖GPC标样
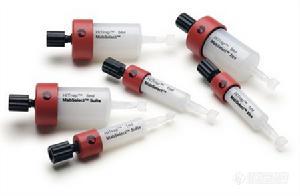
凝胶色谱技术是六十年代初发展起来的一种快速而又简单的分离分析技术,由于设备简单、操作方便,不需要有机溶剂,对高分子物质有很高的分离效果。凝胶色谱法又称分子排阻色谱法。凝胶色谱主要用于高聚物的相对分子质量分级分析以及相对分子质量分布测试。目前已经被生物化学、分子生物学、生物工程学、分子免疫学以及医学等有关领域广泛采用,不但应用于科学实验研究,而且已经大规模地用于工业生产。[B]凝胶色谱-分类[/B]根据分离的对象是水溶性的化合物还是有机溶剂可溶物,凝胶色谱又可分为凝胶过滤色谱(GFC)和凝胶渗透色谱(GPC)。凝胶过滤色谱一般用于分离水溶性的大分子, [img]http://ng1.17img.cn/bbsfiles/images/2009/03/200903190825_139314_1608025_3.jpg[/img]凝胶过滤色谱柱 如多糖类化合物。凝胶的代表是葡萄糖系列,洗脱溶剂主要是水。凝胶渗透色谱法主要用于有机溶剂中可溶的高聚物 (聚苯乙烯、聚氯已烯、聚乙烯、聚甲基丙烯酸甲酯等) 相对分子质量分布分析及分离,常用的凝胶为交联聚苯乙烯凝胶,洗脱溶剂为四氢呋喃等有机溶剂。凝胶色谱不但可以用于分离测定高聚物的相对分子质量和相对分子质量分布,同时根据所用凝胶填料不同,可分离油溶性和水溶性物质,分离相对分子质量的范围从几百万到100以下。近年来,凝胶色谱也广泛用于分离小分子化合物。化学结构不同但相对分子质量相近的物质,不可能通过凝胶色谱法达到完全的分离纯化的目的。[B]凝胶色谱-分子筛效益[/B]一个含有各种分子的样品溶液缓慢地流经凝胶色谱柱时,各分子在柱内同时进行着两种不同的运动:垂直向下的移动和无定向的扩散运动。大分子物质由于直径较大,不易进入凝胶颗粒的微孔,而只能分布颗粒之间,所以在洗脱时向下移动的速度较快。小分子物质除了可在凝胶颗粒间隙中扩散外,还可以进入凝胶颗粒的微孔中,即进入凝胶相内,在向下移动的过程中,从一个凝胶内扩散到颗粒间隙后再进入另一凝胶颗粒,如此不断地进入和扩散,小分子物质的下移速度落后于大分子物质,从而使样品中分子大的先流出色谱柱,中等分子的后流出,分子最小的最后流出,这种现象叫分子筛效应。具有多孔的凝胶就是分子筛。各种分子筛的孔隙大小分布有一定范围,有最大极限和最小极限。分子直径比凝胶最大孔隙直径大的,就会全部被排阻在凝胶颗粒之外,这种情况叫全排阻。两种全排阻的分子即使大小不同,也不能有分离效果。直径比凝胶最小孔直径小的分子能进入凝胶的全部孔隙。如果两种分子都能全部进入凝胶孔隙,即使它们的大小有差别,也不会有好的分离效果。因此,一定的分子筛有它一定的使用范围。 [img]http://ng1.17img.cn/bbsfiles/images/2009/03/200903190826_139315_1608025_3.jpg[/img]凝胶色谱法原理 在凝胶色谱中会有三种情况,一是分子很小,能进入分子筛全部的内孔隙;二是分子很大,完全不能进入凝胶的任何内孔隙;三是分子大小适中,能进入凝胶的内孔隙中孔径大小相应的部分。大、中、小三类分子彼此间较易分开,但每种凝胶分离范围之外的分子,在不改变凝胶种类的情况下是很难分离的。对于分子大小不同,但同属于凝胶分离范围内各种分子,在凝胶床中的分布情况是不同的:分子较大的只能进入孔径较大的那一部分凝胶孔隙内,而分子较小的可进入较多的凝胶颗粒内,这样分子较大的在凝胶床内移动距离较短,分子较小的移动距离较长。于是分子较大的先通过凝胶床而分子较小的后通过凝胶床,这样就利用分子筛可将分子量不同的物质分离。另外,凝胶本身具有三维网状结构,大的分子在通过这种网状结构上的孔隙时阻力较大,小分子通过时阻力较小。分子量大小不同的多种成份在通过凝胶床时,按照分子量大小排队,凝胶表现分子筛效应。
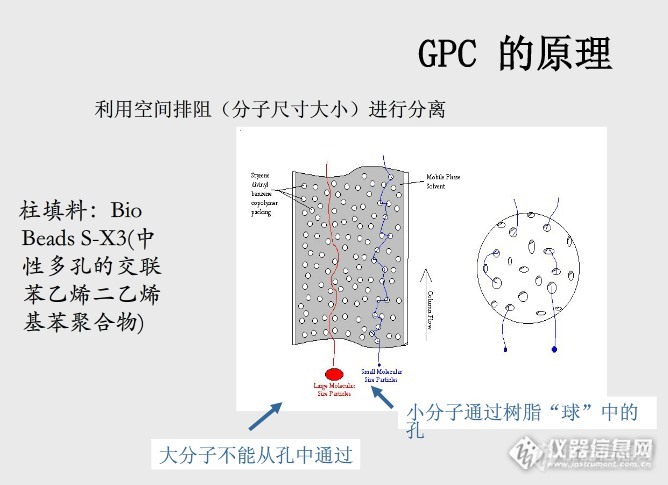
凝胶色谱是根据多孔凝胶对不同大小分子的排助效应进行分离。 样品在多孔凝胶柱中随着流动相的移动,待分离的组分沿凝胶颗粒间的孔隙移动,大分子移动路径较短,先流出色谱柱,小分子由于扩散进入凝胶颗粒内部,迁移路径长,后流出色谱柱,实现分离。看下面一个图,就能懂得凝胶色谱的原理:http://ng1.17img.cn/bbsfiles/images/2015/05/201505041629_544714_2984502_3.png 小伙伴儿们,你看懂了吗?
本人凝胶色谱新手,在做一个项目,需要用凝胶色谱。美国药典论坛上已有方法,重复了人家方法发现有些地方不对,撇开这些不谈,先说说我的疑问吧!1 美国药典上的流动相加了0.1M的硝酸钾,我试了一针加的,一针不加的,发现不加盐峰会前沿,加盐的峰很对称,请问在凝胶色谱里加盐的目的除了改善峰形还有什么作用吗?我更好奇的是盐是通过什么原理来改善峰形的?2 还有一个很奇怪的现象,我的样品和两个杂质出峰时间重叠,即专属性不合格,这三种物质虽然都是钠盐,但大家请注意样品的分子量范围是1000-2000,而两个杂质的分子量一个是100多,一个是300多,就是说在分离原理为分子排阻的凝胶色谱里,分子量1000多的和100,300的一起出峰,改变流动相(换过纯水,也试过加大有机相比例)变化并不明显,这是为什么呢?难道现在的凝胶色谱已经不是单纯的分子排阻原理了,还是说样品的出峰时间除了和分子量有关,还和他们的水溶性有关?这两个问题快把我折磨疯了,请高手解答!
我先把本板快的知识与大家的问题归归类,大家看看那些是需要留住让后来人看看学习的。大家认为没有必要留驻的帖子(连接),用站内短消息与我联系。[b]另外如果大家发现有我整理的内容里有任何问题,都可以用站内短消息与我联系。另外如果大家对凝胶色谱版块的建设有任何建议或意见可以发新帖或跟帖[/b][url=http://www.instrument.com.cn/bbs/shtml/20060912/552188/]真希望凝胶版可以旺起来![/url][b]我都会根据情况给予一定的奖励。[/b]谢谢大家!![b]整理一下本板块的知识点:[/b]如何学习凝胶色谱啊?[url]http://www.instrument.com.cn/bbs/shtml/20050228/129987/[/url]凝胶色谱技术:[url]http://www.instrument.com.cn/bbs/shtml/20031110/18764/[/url]凝胶层析法技术简介:[url]http://www.instrument.com.cn/bbs/shtml/20060421/401834/[/url]凝胶层析的知识(基本原理,凝胶类型与选择,凝胶的处理):[url]http://www.instrument.com.cn/bbs/shtml/20070110/704521/[/url]《色谱法》电子书:[url]http://www.instrument.com.cn/bbs/shtml/20050105/114592/[/url]《仪器分析》课件--色谱法:[url]http://www.instrument.com.cn/bbs/shtml/20040508/46902/[/url]色谱中的一些符号:[url]http://www.instrument.com.cn/bbs/shtml/20040107/24878/[/url]色谱术语:[url]http://www.instrument.com.cn/bbs/shtml/20041012/84241/[/url]凝胶色谱(电子书):[url]http://www.instrument.com.cn/bbs/shtml/20060416/396030/[/url]凝胶色谱手册(英文著作,515页):[url]http://www.instrument.com.cn/bbs/shtml/20051220/305998/[/url]凝胶色谱的讲义第一章(1):[url]http://www.instrument.com.cn/bbs/shtml/20051102/265886/[/url]凝胶色谱(GPC)电子教材:[url]http://www.instrument.com.cn/bbs/shtml/20041220/109533/[/url]GPC操作规程:[url]http://www.instrument.com.cn/bbs/shtml/20060328/376128/[/url]凝胶色谱仪检定方法:[url]http://www.instrument.com.cn/bbs/shtml/20050928/245321/[/url]GPC是指凝胶色谱仪?[url]http://www.instrument.com.cn/bbs/shtml/20060919/560251/[/url]高温GPC:[url]http://www.instrument.com.cn/bbs/shtml/20060605/448959/[/url]GPC软件-现场培训教材:[url]http://www.instrument.com.cn/bbs/shtml/20061120/634044/[/url]需要介绍GPC组成方面的资料:[url]http://www.instrument.com.cn/bbs/shtml/20061106/617390/[/url][em61]
想问一下大家有没有谁用凝胶色谱法测定过地表水的分子量分布,在测定过程中,如何用标准物质对色谱柱进行标定,标准物质的浓度应该怎么确定啊 ,我是刚刚做,想请教一下专家
[b]凝胶色谱的应用[/b]:1、[b]分子量的测定[/b]根据凝胶色谱的原理,样品物质在凝胶色谱柱中的洗脱性质与该物质的分子大小有关。因此选用不同的凝胶色谱柱后,能方便地测定物质的分子量。用此法测定分子量时,可以在各种PH值、离子强度和温度条件下进行。所测定的物质可以是天然状态,也可以是变性后的。实际应用中,可先选用一系列已知分子量的标准样品在同一色谱条件下进行色谱分离分析,并以保留体积(或保留时间)对分子量的对数作图,在一定分子量范围内得到一直线(标准曲线),而后根据待测定物在同一条件下的保留体积(或保留时间),从标准曲线上查得/计算出其分子量。目前用本法测定分子量的应用范围非常广泛。[u]高分子物质的分子量及其分布的测定[/u]:特别是近年来,随着各种高分子材料的问世,人们对高分子科学的不断探索,高聚物的分子量及其分布的测定显得尤为重要,成为科研和生产中不可缺少的测试项目之一。例如:常见的聚苯乙烯塑料制品,其分子量为十几万,如果聚苯乙烯的分子量低至几千,就不能成型;相反,当分子量大到几百万,甚至几千万,它又难以加工,失去了实用意义。科研和生产上通过控制高聚物的分子量及其分布宽度指数D(D=Mw/Mn)、分子量微分分布曲线、分子量积分分布曲线来生产出性能最佳的高聚物产品。同样,除了快速测定分子量及其分布以外,凝胶渗透色谱还广泛被用于研究高聚物的支化度,共聚物的组成分布及高聚物中微量添加剂的分析等方面。如果配以在线的绝对分子量检测器(如:LALLS、Multi-Angle LS、Dual-Angle LS等),凝胶渗透色谱可以测定高聚物的绝对分子量。[u]蛋白质分子量的测定[/u]:现代蛋白质药物的研究中,凝胶色谱法测定分子量是蛋白质分子量的快速测定方法之一。一般选用标准分子量蛋白质(如:铁蛋白、醛缩酶、牛血清白蛋白、卵清蛋白、胃蛋白酶、核糖核酸酶,这就是一组分子量从300KD到14KD的标准品)。
凝胶色谱的资料又积攒了不少,接力前辈,汇总一下,方便查找。要注意帖子的回复,里面也有宝藏哦~~【原创】凝胶色谱的应用 http://bbs.instrument.com.cn/shtml/20061228/685978/【资料】GPC分析的聚合物可以选择的良溶剂方案 http://bbs.instrument.com.cn/shtml/20101214/2999859/【资料】最近凝胶色谱相关的文献资料http://bbs.instrument.com.cn/shtml/20100401/2476606/ 【资料】GPC高级课程培训-柱选择 http://bbs.instrument.com.cn/shtml/20110519/3315288/【资料】《凝胶渗透色谱操作手册》北京大学化学院 http://bbs.instrument.com.cn/shtml/20101228/3045365/【分享】凝胶色谱的讲义 http://bbs.instrument.com.cn/shtml/20101106/2908677/【资料】凝胶色谱柱操作 http://bbs.instrument.com.cn/shtml/20101105/2907744/【分享】凝胶色谱仪标准操作规程(SOP) http://bbs.instrument.com.cn/shtml/20101012/2855479/【原创】多功能凝胶色谱仪(GPC)测聚合物分子量分布 http://bbs.instrument.com.cn/shtml/20100510/2546330/【资料】凝胶色谱法的基本理论 http://bbs.instrument.com.cn/shtml/20100406/2483413/下面是前辈整理的资料:2010.4【资料】凝胶色谱 和 超临界流体色谱 资料汇总http://bbs.instrument.com.cn/shtml/20100411/2493256/2006年【公告】凝胶色谱版的知识点汇总! http://bbs.instrument.com.cn/shtml/20061215/669019/
SEC/GPC凝胶渗透色谱分析的工作原理[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=91284]SEC/GPC凝胶渗透色谱分析的工作原理[/url]
求GB/T21863-2008凝胶渗透色谱法(GPC) 用四氢呋喃做淋洗液谢谢
请教本人想用凝胶色谱法分析褐藻胶(褐藻酸钠)的分子量,据说褐藻胶对凝胶柱损伤大,做十几个样品柱子基本就废了,是这样吗?请高人指点!
本人凝胶色谱新手,在做一个项目,需要用凝胶色谱。美国药典论坛上已有方法,重复了人家方法发现有些地方不对,撇开这些不谈,先说说我的疑问吧!1 美国药典上的流动相加了0.1M的硝酸钾,我试了一针加的,一针不加的,发现不加盐峰会前沿,加盐的峰很对称,请问在凝胶色谱里加盐的目的除了改善峰形还有什么作用吗?我更好奇的是盐是通过什么原理来改善峰形的?2 还有一个很奇怪的现象,我的样品和两个杂质出峰时间重叠,即专属性不合格,这三种物质虽然都是钠盐,但大家请注意样品的分子量范围是1000-2000,而两个杂质的分子量一个是100多,一个是300多,就是说在分离原理为分子排阻的凝胶色谱里,分子量1000多的和100,300的一起出峰,改变流动相(换过纯水,也试过加大有机相比例)变化并不明显,这是为什么呢?难道现在的凝胶色谱已经不是单纯的分子排阻原理了,还是说样品的出峰时间除了和分子量有关,还和他们的水溶性有关?3 还有一个现象我不能理解,就是走空白,也就是流动相的时候会出现一些溶剂峰,走样品的时候也会出现溶剂峰,但是样品中的溶剂峰的响应要比溶剂峰里的高多了,这是怎么回事呢?这几个问题快把我折磨疯了,请高手解答!!
不知道那位前辈有“GB/T 21863-2008 凝胶渗透色谱法(GPC) 用四氢呋喃做淋洗液”的电子版啊!可否上传一份给小弟啊!不胜感激!!!