在下从事医疗器械研发工作,想了解一下医疗器械相关的检测机构有哪些,最好是有联系方式,恳请各位朋友指点一二,不胜感激
《CNAS-CL12 实验室认可准则在医疗器械检测实验室的应用说明》5.2.1条要求“实验室应确保所有与检测质量有关的人员受过医疗器械相关法律、法规的培训”。我看了下,跟检测实验室有关的医疗器械法律法规好像没什么内容啊?有哪些法律法规相关的呢?
YYT 0681.11-2014 无菌医疗器械包装试验方法 第11部分:目力检测医用包装密封完整性
附件:医疗器械检测机构资格认可管理办法(征求意见稿)第一章总则第一条 为了保证医疗器械检测机构工作的规范性、公正性和科学性,依据《医疗器械监督管理条例》的规定,制定本办法。第二条 国家食品药品监督管理局负责医疗器械检测机构资格的认可工作和监督管理工作。第三条 国家食品药品监督管理局依据GB/T15481-2000《校准和检验实验室能力的通用要求》及本办法的《医疗器械检测机构评审细则表》对医疗器械检测机构的质量体系和运行能力进行认可。第四条 国家食品药品监督管理局根据《医疗器械监督管理条例》、及相关配套规章、医疗器械通用和专用安全要求标准以及产品标准认可医疗器械检测机构的医疗器械受检目录。各医疗器械检测机构应在认可的医疗器械受检目录范围内开展检测工作。第五条 国家食品药品监督管理局的职责:(一)组织对医疗器械检测机构资格认可评审员的培训及资格评定,建立医疗器械检测机构资格认可评审员库。(二)受理医疗器械检测机构资格认可申请。组织对申请资格认可的医疗器械检测机构进行评审。(三)组织对资格认可后的医疗器械检测机构进行监督和复审。根据监督或复审结果做出维持认可、限期改正、撤销认可或变更认可范围的决定。(四)受理对医疗器械检测机构资格认可工作的申诉。第二章认可条件第六条 医疗器械检测机构资格认可条件:(一)医疗器械检测机构应是具有法人资格的专职检测机构。(二)已获得计量认证证书。具有按GB/T15481-2000《校准和检验实验室能力的通用要求》进行质量体系运行的能力。(三)具备受检目录内医疗器械的检测能力,检测设备配备率不低于95%,并按标准或相应的指导检测实施的技术性文件,作模拟运转,建立并保存原始记录和检验报告。(四)符合《医疗器械检测机构评审细则表》(附后)的要求。(五)遵守本办法中的有关规定。第三章申请和认可程序第七条 申请资格认可的医疗器械检测机构(以下简称申请方)可向国家食品药品监督管理局提交意向申请并可咨询有关认可事宜。国家药品监督管理局向申请方提供最新版本的认可规则和其他有关认可要求的文件。申请方办理正式申请手续时,应填写国家药品监督管理局提供的正式申请书和调查表,连同最新版本的质量手册及相有关资料一并提交国家食品药品监督管理局。第八条 国家食品药品监督管理局对审查申请方提交资料的完整性进行审查,发现资料不符合要求时,当日应书面通知申请方。第九条资料审查符合要求后,由国家食品药品监督管理局应当日出具受理通知书,并与申请方商定现场评审时间。国家食品药品监督管理局组织评审员和有关专家组成现场评审组,并将组成人员名单通知申请方。如申请方对评审人员有异议时,应及时告知国家食品药品监督管理局,由国家食品药品监督管理局决定是否调整。国家食品药品监督管理局将调整后的执行现场评审人员名单、评审日期及有关事宜通知申请方。第十条 评审组依据《医疗器械检测机构现场评审核查表》评审细则和有关标准对医疗器械检测机构申请认可范围内的技术能力和质量管理进行现场评审,审查应于3个工作日内完成。。评审组实行组长负责制。第十一条 现场评审结束后,评审组应在5个工作日内将现场评审的不符合项目书面告知申请方,同时向国家食品药品监督管理局提交评审报告。第十二条 国家食品药品监督管理局将经审查的评审报告通知申请方。第十三条 国家食品药品监督管理局在20个工作日内批准经评审合格的申请方或在国家食品药品监督管理局同意的期限内实施纠正措施、并经跟踪评审合格的申请方,向其颁发资格认可证书。医疗器械检测机构资格认可证书有效期为5年。对经评审不合格的申
请教大家,有做医疗器械检测行业的老师吗?医疗器械检测标准(电气检测、电磁兼容检测、医疗器械生物学评价检测)国家CMA和CNAS扩项评审时需不需要进行方法验证并形成验证报告?医疗器械生物学评价项目需要用到动物,还牵扯到动物福利问题。所以不知道到底要不要做?
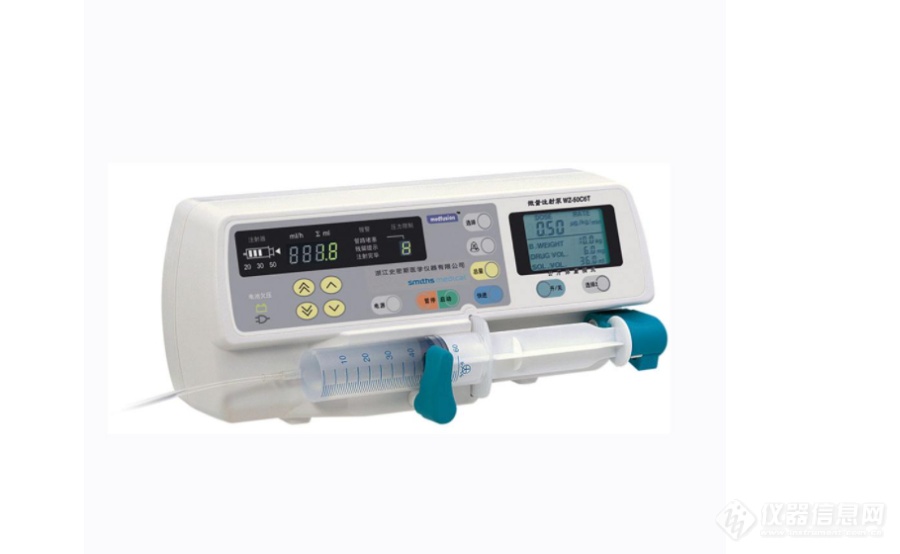
市场背景为了推进医疗器械强制性行业标准规范,国家药监局最近再次发布了一条“进一步加强医疗器械强制性行业标 准管理有关事项”的通知。这无疑更加说明了国家对医疗器械行业的要求越来越严格,越来越趋同于药品生产的要求。https://ng1.17img.cn/bbsfiles/images/2021/07/202107091820375261_2058_5319121_3.png!w690x424.jpg为什么医疗器械法规要求会越来越高呢?1. 中国医疗改革的需要根据国务院印发的《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,直至今,国家不断发布了很多相关改革,例如“4+7”带量采购、《中国药品管理法》、《中国疫苗管理法》、新《药典》等。为了跟进此次改革,各种医疗器械指导原则频繁被推出来规范行业。2. 医药行业的法规环境越来越规范为了跟进医药的法规情况,在2020年上半年,NMPA发布相关的法规文件和公告指令等总数差不多等同于2019年的全年相关发布量,这也促进医疗器械的法规更加成熟和规范。医疗器械过检难题解决很多的医疗产品公司开发一款产品时都会遇到过检不通过的原因,往往不是产品的主要医疗功能不过,更多是一些附属的功能,如医疗报警音的要求,但是这个今天我的方案让你解决这个问题,不再是难点了1.图片上面的方案就是YY0709标准的二类医疗器械的报警要求,对声音和语音芯片的要求比较高,因为输出的声音脉冲不圆润的话,容易误导检测员的判断,导致你的检测不过关,所以我们也是经过多年的调试,开发出了过检的方案,现在被客户广泛运用在制氧机,呼吸机,注射泵等二类医疗器械。2.运用到的就是我们的NVC芯片加一个模拟的功放芯片就能实现,最重要的就是我们的这个语音芯片的稳定性,接下来就介绍一下我们这个芯片的特性。功能特点☆OTP存储格式,生产周期快,最快仅需一天,下单无最小量限制;☆灵活的多种按键操作模式以及电平输出方式供选择(边沿按键触发、电平触发、随机按键播放、顺序按键播放);☆简单方便的一线MCU串口控制方式,用户主控MCU可控制任意段语音的触发播放及停止;☆语音时长20秒、40秒、80秒、180秒;☆内置一组PWM输出器可直推0.5W喇叭,支持13bit的DAC输出,可外接模拟功放;☆灵活的放音操作,通过组合可节省语音空间,最多可播放220个语音组合;☆音质优美,性能稳定,物美价廉;☆内置LVR自复位电路,保证芯片正常工作;☆DIP8,SOP8,SOP24以及COB多种封装可供选择,使用方便,应用灵活;☆支持和弦MIDI播放,音质非常优美;☆外围电路简单,仅需一耦合电容;☆工作电压范围:2V~4.5V;☆静态电流:小于2uA;
请教各位,有没有医疗器械累生物相容性检测、微生物检测、性能检测等可以参加的能力验证的机构,请大家帮忙推荐几家。谢谢!
YYT 0681.5-2010无菌医疗器械包装试验方法 第5部分:内压法检测粗大泄露(气包法)
关于初次申请医疗器械资质,体系是要运行一年以上才能申请吗?是不是要做了内审和管评才能申请呢?然后是每个项目都要做验证试验吗,还有不确定度报告有要求吗?哪些专业的技术人员能直接考核后上岗检测医疗器械?
质量体系对医疗器械标签、说明书和包装的探究见附件
需要对医疗器械的EO和ECH进行残留检测,现有一台GC2014C,0.53um安捷伦柱子,进样口150,柱温60,检测口200,试过EO和ECH各加100uL的标液浓度为10ug/mL到一个顶空瓶,两个标定物的峰共用一个,分不开,大佬有啥法子嘛
之前一直是外包,现在想自己弄一台来检测,想请大家大家推荐一款性价比高的,主要用于检测医疗器械EO灭菌后的环氧残留,谢谢大家。
求医疗器械检验所的检测设备清单,要建实验室 QQ:931118572
求推荐比较好发的核心期刊 有关化学的或药的 医疗器械类的 药品包装材料类的 口腔材料检测类的或者有关健康的 都可以 最好的能在几个月之内发表的 发表周期短 再推荐一下相对好发的中文核心吧
YYT 0681.18-2020 无菌医疗器械包装试验方法 第18部分:用真空衰减法无损检验包装泄漏
第三方检测公司申请医疗器械CMA,为省运费,想外省建立分场所,是否可行?分场所和分公司的两种适用区别?注意事项哪些?请求大神指教。
医疗器械唯一标识中的产品标识(DI)是特定于某种规格型号和包装的医疗器械唯一代码,医疗器械唯一标识中的生产标识(PI)由医疗器械生产过程相关信息的代码组成,根据监管和实际应用需求,可包含医疗器械序列号、生产批号、生产日期、失效日期等。

各位大神,很久不见,应该有6-7年没有上来了,如题求成立关于医疗器械方面检测中心实验室的申请报告,类似下面的文本,求医疗器械方面分享,谢谢![img=,585,639]https://ng1.17img.cn/bbsfiles/images/2021/03/202103111431168656_8396_2258796_3.png!w585x639.jpg[/img]
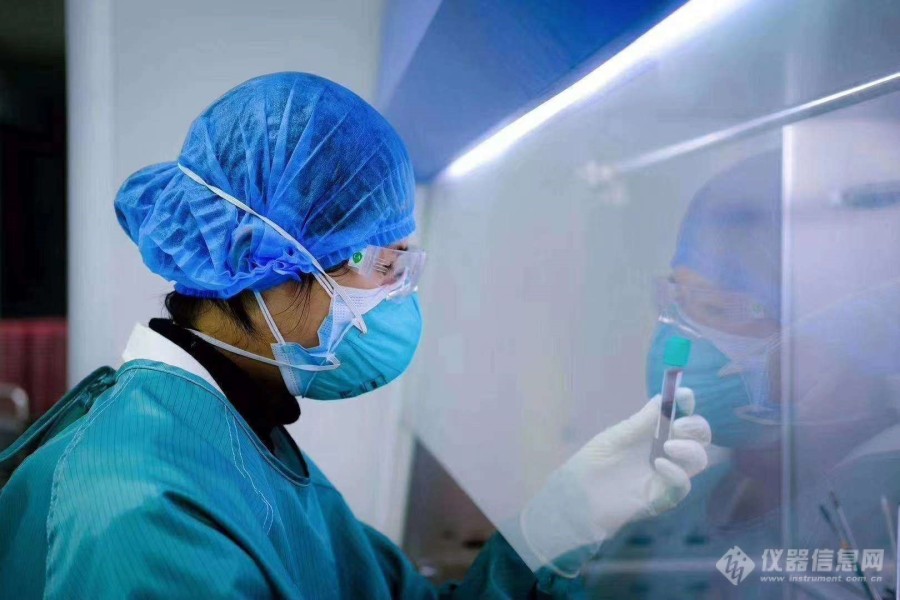
[align=center][b][size=24px]医疗器械环氧乙烷灭菌残留快速检测[/size][/b][/align][img=,690,460]https://ng1.17img.cn/bbsfiles/images/2020/02/202002162131118294_7217_1871535_3.jpg!w690x460.jpg[/img]新型冠状病毒(2019-nCoV)肺炎疫情牵动着祖国亿万人民的心。面对此次突如其来的疫 情,南京科捷分析仪器有限公司利用在医疗用品灭菌残留快检方面的优势,开展医疗卫生用 品环氧乙烷灭菌残留快速检测相关工作,整理出检测方案,为需要的厂家和单位提供充足的 设备和技术支持,全力抗击疫情。 一.环氧乙烷的危害和限量 环氧乙烷是一种可刺激体表并引起强烈反应的易燃性气体。在很多情况下,环氧乙烷具有 致突变 性、胎儿毒性和致畸特性,对睾丸功能具有不良作用,并能对体内的多个器官系统产生 损害。在动物致 癌研究中,吸入 EO 可产生几种致瘤性变化,包括白血病、脑肿瘤和乳房肿瘤, 而食入或皮下注射 EO 仅 在接触部位形成肿瘤。1994 年,国际癌症研究机构( IARC)依据 EO 的作用机理,重新将其划分为人类致癌物质(一类)。[img=,690,595]https://ng1.17img.cn/bbsfiles/images/2020/02/202002162131520854_8773_1871535_3.png!w690x595.jpg[/img]国标 GB/T16886.7-2015 医疗器械生物学评价 第 7 部分和 ISO 10993-7 对于环氧乙烷 (EO)残留限量提出如下要求: [img=,690,277]https://ng1.17img.cn/bbsfiles/images/2020/02/202002162132206083_6393_1871535_3.png!w690x277.jpg[/img]二.检测适用范围 南京科捷环氧乙烷残留快速测定仪主要用于快速检测一次性医用口罩、手套、防护服、医疗 用品包装材料等医疗用品。产品操作简单、结果可靠,已经市场销售多年,客户反馈口碑良 好。适合用户:各种医疗器械、药厂、药检、商检及质检等。 三. 检测指标:环氧乙烷(EO) 四. 试剂:环氧乙烷(EO)标准溶液 五、医疗设备中残留环氧乙烷分析[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]分析流程图示: 样品制备――顶空进样器进样――[url=https://insevent.instrument.com.cn/t/Mp]gc[/url] 分析――色谱工作站――数据输出 六、医疗设备中残氧乙烷残留分析[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]配置:[img=,690,437]https://ng1.17img.cn/bbsfiles/images/2020/02/202002162133000122_4620_1871535_3.png!w690x437.jpg[/img]七、医疗器械中环氧乙烷测定条件(极限浸提法) 色谱柱: 30m*0.32mm*0.25μm 色谱仪柱温:60℃ 汽化室:150℃ FID:200℃ 顶空进样器:样品加热 60℃,阀箱 80℃,管路 120℃。 附 1 标准曲线溶液浓度:1 至 10 ug/mL, 附 2 样品处理:取产品上与人体接触的 EO 相对残留含量最高的部件进行试验。截为 5mm 厂碎片,称取 1.0g 放入 20mL 萃取容器中,精密加入 5mL 水,密封,60℃温度下平衡 40mi 八. 仪器外观:[img=,690,250]https://ng1.17img.cn/bbsfiles/images/2020/02/202002162133446337_3354_1871535_3.jpg!w690x250.jpg[/img]九.图谱及其线性: [img=,690,371]https://ng1.17img.cn/bbsfiles/images/2020/02/202002162134150457_4745_1871535_3.jpg!w690x371.jpg[/img][img=,690,420]https://ng1.17img.cn/bbsfiles/images/2020/02/202002162134159748_3281_1871535_3.jpg!w690x420.jpg[/img]十. 参考依据:GBT 16886.7-2015 医疗器械生物学评价 第 7 部分:环氧乙烷灭菌残留量.
笔者近日了解到:韩国2009年11 月9 日发布通报,韩国食品药品管理局拟修订医疗器械标准规范提案。本提案草案规定了诸如“焊接的金属”和“金属烤瓷修复体金属”中铍、镍、镉和铅等有害元素的含量标准。镉、铍和铅的含量应当最高不超过0.02wt%。镍超过0.1wt%应当在包装上用0.1wt%的单位显示。针对韩国拟修订医疗器械标准规范提案,笔者联系到了著名检测机构——PONY谱尼测试集团的消费品检测专家进行了咨询。PONY谱尼测试的专家表示:铍、镍、镉和铅有害物质现在被很多法规、指令限制,比如欧盟RoHS指令、中国RoHS指令等。因此韩国此番修订医疗器械标准规范提案,我们企业不必过度紧张,只要企业在生产过程中注意这些有害物质的含量,并从原材料采购初期就开始管控,确保产品的环保性,就可跨跃此法案造成的贸易壁垒。同时,PONY谱尼测试的专家也强调,由于在整个供应链过程中,不能保证对有害物质的百分百管控。因此谱尼测试专家建议企业在产品出口销售前,可前往有资质的第三方检测机构,就产品的有害物质含量进行检测,确保预销售的产品符合有害物质的限制。除了对有害元素的含量和化学合成物必须标示。本修正案同样还规定了“矫形外科丙烯酸水泥”的物理/化学/性能测试的标准和规范。
YYT 0681.1-2009 无菌医疗器械包装试验方法 第1部分:加速老化试验指南
[color=#00008B][size=4]爱心捐助 我本来是想悬赏的,可是我的分数才6分,[em0804] !!!我想问的是 医疗器械产品灭菌后的无菌检测用不用按药典的要求做方法验证试验,以验证其无抑菌性?那个阴性对照还用不用做?培养基的灵敏度试验用不用做,如果做的话是按要点要求的6种菌都做,还是只选最常用的金黄色葡萄球菌啊?[/size][/color]在两周之内,只要能够较好回答楼主问题的回帖,除获得版主加分奖励之外,将会得到额外的应助奖励。--jun来也于2008.07.31
YYT 0681.15-2019 无菌医疗器械包装试验方法 第15部分运输容器和系统的性能试验
仪器岛津GC-2014C,进样口150℃。柱温60℃,检测器200℃,安捷伦柱子0.53um,想能同时检测医疗器械中残留的EO和ECH,但检测结果显示两者共用一个峰,改变色谱条件也做不到分离。大佬们又懂的吗
医疗器械实验室需要按照RB/T217-2017运行三年才能够申请吗?在RB/T217-2017 4.1.2中明确提出:医疗器械检验机构所申请开展的医疗器械检验活动应用具三年以上的相关领域(专业)的检验经历。如果按这个说法,那机构成立三年,进行检验又不能出具报告,还不得饿死呀?
随着医疗事业的发展,同时,因为生活观念的转变,家用医疗器械运用市场快速增长,原因在于: 1、家用医疗器械以其功能齐全、无副作用、使用方便绝对优势赢得了广大消费者的青睐。 2、医疗费用越来越高,服务质量却令人不满意,给家用医疗器械创造空间,家用医疗器械售价只有千元左右,可以用10~20年,可大大降低医药费用。 3、中国病患群体在很大程度依然相信中医,随着中医类家用医疗器械的发展,特别是:针灸、按摩、拔火罐、刮痧等理疗家用器械的成功研发,更是获得了市场的一致青睐。 4、个人健康意识增强,性能良好、使用方便的用于社区、家庭和个人的治疗设备、预防及健身的设备、健康自我检测设备将成为家庭中新的“家电”和“家私”。 5、近年来,家用医疗器械已经悄然成为最时尚的礼物之一。哈慈五行针、周林频谱仪、祝强将压仪、利德治疗仪、氧立得、紫环颈椎治疗仪等,都没有每天高喊着“送礼、送礼、送礼”的口号,但我们进行消费者行为分析时,都会看都一个自然形成的、巨大的“礼品市场”的存在。
各省、自治区、直辖市食品药品监督管理局: 为做好医疗器械产品注册检验工作,根据《医疗器械注册管理办法》(国家食品药品监督管理总局令第4号)和《体外诊断试剂注册管理办法》(国家食品药品监督管理总局令第5号),总局组织制定了《医疗器械检验机构开展医疗器械产品技术要求预评价工作规定》,现予印发,自2014年10月1日起施行。 国家食品药品监督管理总局 2014年8月21日
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=50400]ASTM F 1980-2002 无菌医疗器械包装加速老化试验 CHN.doc[/url][img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=50401]ASTM F 1980-2002 无菌医疗器械包装加速老化试验(EN).pdf[/url]
YYT 0681.7-2011 无菌医疗器械包装试验方法 第7部分:用胶带评价软包装材料上印墨或涂
YYT 0681.6-2011 无菌医疗器械包装试验方法 第6部分 软包装材料上印墨和涂层抗化学性评价