盐含量测定仪是应用微库仑分析技术,采用计算机控制微库仑滴定的最新的测定盐含量的新一代产品,具有性能稳定、操作方便、分析数据重复性好、便于安装等特点。 盐含量测定仪可用于重油、渣油,炼油厂及油田和各种工业用水及排放水中的盐含量的测定,同时还适用于上述各种样品中无机氯离子的测定,测量结果符合SY/T-0536-94及国际通用方法的要求,是当前电脱盐工艺控制盐含量的理想仪器。 盐含量测定仪是应用微库仑滴定原理,由零平衡工作方式设计的库仑放大器与滴定池和适宜的电解液组成了一种闭环负反馈系统。其数据的采集、处理由单片机控制,并以串行通信的方式与计算机相连,从而实现自动控制。
大家好!我是个新手,有谁知道这个问题请联系我!硫酸新霉素的硫酸盐的含量测定原理,怎么计算?
各位大侠能帮我详细分析一下下面的含量测定反应原理吗?拜谢了!!!取麝香草酚约0.1g,精密称定,置250ml碘瓶中,加入25ml1mol/LNaOH溶液。加入20ML热的稀盐酸(1→2),立即用溴滴定液(0.05mol/L)滴定至计算终点1到2之内。加热溶液至70~80℃,加2滴甲基橙指示液,继续缓慢滴定,每次滴加后,用力振摇。当甲基橙的颜色消失时,加2滴溴滴定液(0.05mol/L),振摇10秒钟,加1滴甲基橙指示剂,并用力振荡。如果溶液显红色,继续逐滴滴加,边加边振荡,直到颜色消失。重复交替滴加滴定液与甲基橙指示液直到在加入指示液后不显红色。每1ml溴滴定液(0.05mol/L)相当于3.755mg的C10H14O。
求助2010版中国药典氧化镁含量测定的原理及计算公式
请问各位专家,朱砂中硫化汞的含量测定的原理是什么,及所有各试剂的作用,最后的现象是什么?以下是2005版药典一部中关于朱砂含量测定的操作步骤:取本品粉末约0.3g,精密称定,置锥形瓶中,加硫酸10ml与硝酸钾1.5g,加热使溶解,放冷,加水50ml,并加1%高锰酸钾溶液至显粉红色,再滴加2%硫酸亚铁溶液至红色消失后,加硫酸铁铵指示液2ml,用硫氰酸铵滴定液(0.1mol/L)滴定。每1ml硫氰酸铵滴定液(0.1mol/L)相当于11.63mg的硫化汞。
尿素含量测定时空白消耗量一般是多少?尿素含量测定原理可否详细介绍下
国标检测甘氨酸含量的原理是什么国标中,检测甘氨酸含量是用高氯酸标准溶液非水滴定的,用的是结晶紫指示剂,请问,原理是什么呢?国标中没有提到~~氮基乙酸含量的测定检测方法提要:试样以甲酸为助溶剂,以冰乙酸为溶剂,以结晶紫为指示剂,用高氯酸标准滴定溶液滴定,根据消耗高氯酸标准滴定溶液的体积,计算氨基乙酸的含量。
求助在钨精矿的钼含量测定中,柠檬酸铵屏蔽钨的原理,对于60-70品位的钨需要多少柠檬酸铵屏蔽?在加了2毫升50%柠檬酸,5毫升的样液与加了4毫升50%柠檬酸,10毫升样液的读数不一致,差别很大,其中5毫升的读数比10毫升的读数高,样液中钨的含量在50左右,请问这是为啥啊,求好心的哥哥姐姐帮偶啊
火焰[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收光谱[/color][/url]法测定头发中微量元素的含量的方法原理
三氯化六氨合钴的制备及钴含量的测定实验原理,所需滴定剂,指示剂,其他试剂及其配制方法,所需仪器,实验步骤,需记录数据及处理方法
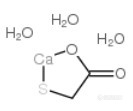
巯基乙酸钙盐三水合物 CAS号:5793-98-6 分子式:C2H8CaO5S 分子量 184 结构式http://ng1.17img.cn/bbsfiles/images/2017/10/2016042817011772_01_1490617_3.png 《化妆品安全技术规范》(2015年版)当中,3.9巯基乙酸第三法——化学滴定法的反应方程如下:https://ng1.17img.cn/bbsfiles/images/2017/01/201701191701_670059_1490617_3.png 原理是https://ng1.17img.cn/bbsfiles/images/2016/04/201604281715_591808_1490617_3.png 该方法的适用范围中这样描述:本方法适用于脱毛类、烫发类和其他发用类化妆品中巯基乙酸及其盐类和酯类含量的测定。客户委托了一款产品,要求按照巯基乙酸钙含量出报告,含量计算公式中有一个系数0.184,描述是1mmol碘溶液相当于巯基乙酸钙的克数,这样显然其指的巯基乙酸钙不是CAS:814-71-1 分子式C4H6CaO4S2(分子量222.3),不知道巯基乙酸钙盐三水合物是否依然按照上述原理与碘反应。 求高手指教,前辈指点!谢谢
近日在做甲酸钾珠含量的测定时,发生了奇怪的现象。原理是用定量的高锰酸钾(足量)氧化后,加等量的草酸钠,再用高锰酸钾反滴,推算出甲酸钾的含量。但在做的时候很奇怪,取1g样品和5g样品做出来的值差了30%,取1g时做出来是96%,取5g时做出来是65%,做了多次都是这样,为什么?另:用IC测阴离子,折算出来甲酸钾含量在65%,cl离子1%,SO4检不出。又另:因为其方法及原理与CODmn相近,故放在水质版来求助。
国标检测甘氨酸含量的原理是什么国标中,检测甘氨酸含量是用高氯酸标准溶液非水滴定的,用的是结晶紫指示剂,请问,原理是什么呢?国标中没有提到~~氮基乙酸含量的测定检测方法提要:试样以甲酸为助溶剂,以冰乙酸为溶剂,以结晶紫为指示剂,用高氯酸标准滴定溶液滴定,根据消耗高氯酸标准滴定溶液的体积,计算氨基乙酸的含量。
Folin-Ciocalteu 方法测定检品总多酚含量步驟為分别于 96 孔微量盘中加入 20 μL 的不同浓度 catechin 标准品溶液及不同苦瓜检品,再加入 200 μL 蒸馏水及 40 μL 的 Folin-Ciocalteu phenol reagent 混合,于室温下反应 5 分钟,再加入 40 μL 的 20% sodium carbonate 混合后,将 96 孔微量盘置于微量盘分光光谱仪测量 OD680 之吸光值结果以换算每克萃取物中所含 catechin 的毫克数(mg catechin equivalent/g extract)表示。請問Folin-Ciocalteu 方法测定检品总多酚含量的原理
[color=#444444]原理上味精谷氨酸钠含量测定可以和酱油氨基酸态氮的测定方法一样,实际上甲醛法就是同一个方法。现在我们用测酱油的比色法测味精含量,结果却差的很离谱。测到味精含量在[/color][color=#444444]2900[/color][color=#444444]%,大了很多,感觉不知道出错在哪里。哪位高手指点下啦[/color]
一、实验目的掌握旋光法测定谷氨酸单钠的原理,熟悉旋光法测定谷氨酸单钠含量的方法。二、实验原理谷氨酸单钠分子结构中含有一个不对称碳原子,具有光学活性,能使偏振光面旋转一定角度,所以,可用旋光仪测定其旋光度,并根据旋光度换算成谷氨酸单钠的含量。三、仪器与试材1.仪器与器材旋光仪(精度±0.010),带有钠光谱D线589.3nm的钠光灯。2.试剂除特别说明外,实验中所用试剂均为分析纯,水为去离子水或蒸馏水。常规试剂:HCl。3.实验材料2~3种味精(纯度大于99%),各50g。四、实验步骤1.样品处理(1)称取样品10.0000g,加少量水溶解并全部移入100mL容量瓶中。(2)加20mILHCl,混匀,冷却至20℃后,补加水至刻度,摇匀。2.测定在20℃恒温室中,先用标准旋光角校正仪器。然后,将上述试液置于旋光管中(注意不能产生气泡),观测其旋光度,同时记录旋光管中溶液的温度。3.计算样品中谷氨酸单钠的含量按下式计算:a/LcX=─────────×10025.16+0.047×(20-t)式中,X为样品中谷氨酸钠的含量,%;a为实测试液的旋光度;L为旋光管的长度(即液层厚度),·dm;c为1mL试液中含谷氨酸钠的质量,g/mL;25.16为谷氨酸钠的比旋光度苫;t为溶液的温度,℃;0.047为温度校正系数。
130 油含量的测定甲 红处分光光度法本方法适用于循环冷却水中油含量的测定,测定范围为0.01~2mg/L。1.原理油中甲基、次甲基团在3.4μm波长处有明显的吸收,且在一定范围内,吸收峰峰高与水中含量成正比。2.试剂2.1 1+2硫酸溶液。2.2 无水硫酸钠。2.3 标准油样吸取65mL正十六烷,25mL异辛烷、10mL苯混合,摇匀,即标准油。再称取此油样,用四氯化碳稀释,配成20mg/L的标准油样。3.仪器3.1 红处油份分析器:波长1.4μm,范围0~50mg/L,精度1mg/L。3.2 分液漏斗:1000mL。3.3 砂芯漏斗:G3。4.分析步骤 4.1 用玻璃瓶取3000~4000mL水样,摇匀后,注入1000mL分液漏斗(漏斗标有800mL的标记)于标记处,加1+1硫酸溶液调至pH小于1。4.2 加25mL四氯化碳,剧烈振荡2分钟,并不断开启活塞排气,静置分层。以G3玻璃砂芯漏斗(或快速定性滤纸放入适量无水硫酸钠)将四氯化碳滤入50mL容量瓶中。4.3 重复4.2步骤一次,四氯化碳抽出液也收集于上述50mL容量瓶中,摇匀。4.4 按仪器使用说明书要求,调整零点,用20mg/L油标准液调满刻度,测定四氯化碳抽出液中油含量。5.分析结果的计算水样中油含量X(毫克/升),按下式计算: 式中:A——仪器测量值,毫克/升; VW——水样体积,毫升。50——抽取水中油用四氯化碳的体积,毫升。6.注释 6.1 禁止用塑料器皿取水样,因塑料器皿吸附油。6.2 如用滤纸过滤,均用统一规格的滤纸、漏斗。7.允许差油含量在2mg/L以下时,平行测定两结果差不大于0.04mg/L。8.结果表示取平行测定两结果的算术平均值,作为水样中油的含量。乙 紫外分光光度法本方法适用于循环冷却水和天然水中微量石油类化合物的测定。测定范围0~10mg/L。1.原理循环冷却水中含有在紫外光区有特征吸收的芳烃化合物,可借助于测定该物质的含量来确定相应的油含量。以60~90℃石油醚作溶剂从水中抽出油品,在波长为225nm处测其吸光度。2.试剂2.1 1+3硫酸溶液。2.2 石油醚:30~60℃,60~90℃。2.3 无水硫酸钠。2.4 细孔硅胶:80~100目(或13×分子筛)。2.5 硫酸、甲醛试剂。在50mL浓硫酸中,逐滴加入2.5mL甲醛。2.6 精制石油醚当60~90℃石油醚的透光率低于60%时,需要进行精制。预先将细孔硅胶或13×分子筛在150℃烘箱中活化4小时,冷后装入直径为5cm,高为250 cm的吸附柱中,使60~90℃石油醚通过该吸附柱,以除去其中的芳烃。用硫酸、甲醛试剂检查流出来的石油醚,应不呈黄色,于225nm处以水为参比,测其透光率,精制后石油醚其透光率不得少于60%。2.7 油标准样品在酸性条件下,用30~60℃石油醚萃取循环水中油类物质,然后经无水硫酸钠脱水,过滤后,置于80℃水浴上蒸去大部分石油醚,再置于70℃烘箱内,蒸尽石油醚,即得标准油样。3.仪器3.1 紫外分光光度计。3.2 分液漏斗:500mL。3.3 漏斗:¢60mm。3.4 容量瓶:50mL。4.分析步骤4.1 标准曲线的绘制4.1.1 准确称取100mg标准油样,用60~90℃石油醚将其移入100mL容量瓶中,并稀释至刻度。得到1mL含1mg的标准油样,再稀释5倍,得1mL含0.2mg的标准油样。4.1.2 分别取1mL含0.2mg的标准油样1、2、4、6、8、10mL于6只50mL容量瓶中,用石油醚稀释至刻度,摇匀。4.1.3 于225nm处用1cm石英比色皿,以石油醚作空白,测其吸光度。4.1.4 以吸光度为纵坐标,油的毫克数为横坐标,绘制标准曲线。4.2 水样的测定4.2.1 量取150~200mL水样移入分液漏斗中,加入5mL1+3硫酸溶液。4.2.2 加入20mL石油醚,依次洗涤采样瓶、量筒,然后倾入分液漏斗中,剧烈振荡2~3分钟,并不断开启活塞排气,静置2~3分钟分层,将下层水样放入原采样瓶内。4.2.3 在放有滤纸的漏斗中放入1/3高度的无水硫酸钠,将石油醚抽出物滤入50mL容量瓶内。4.2.4 将水样再一次移回分液漏斗,按本方法第4.2.2,4.2.3条规定重复一次,然后加10mL石油醚洗涤漏斗及滤瓶,石油醚抽出液均收集于同一容量瓶中,用石油醚稀释至刻度,摇匀。4.2.5 按本方法第4.1.3条测其吸光度。5.分析结果的计算水样中油含量X(毫克/升),按下式计算: 式中:A——与吸光度相对应的油含量,毫克; VW——水样体积,毫升。7.允许差含油量小于5mg/L时,平行测定两结果差不大于较小结果的20%;含油量在5~10mg/L时,平行测定两结果差不大于较小结果的15%。8.结果表示取平行测定两结果的算术平均值,作为水样中油的含量。
一、概述 1.定义:非水溶液滴定法即在非水溶剂中进行的滴定分析方法。一些很弱的酸或碱以及某些盐类,在水溶液中进行滴定时,没有明显的滴定突跃,难于掌握滴定终点;另外还有一些有机化合物,在水中溶解度很小,因此,以水作溶剂的滴定分析受到一定的限制。 所以,滴定分析法逐渐采用了各种非水溶剂(包括有机溶剂与不含水的无机溶剂)作为滴定分析的介质,不仅能增大有机化合物的溶解度,而且能改变物质的化学性质(例如酸碱性及其强度),使在水中不能进行完全的滴定反应能够顺利进行。 2.分类 非水溶液滴定法除有酸碱滴定外,尚有氧化还原滴定、络合滴定及沉淀滴定等,而在药物分析中,以非水溶液酸碱滴定分析法用得最为广泛。 3.非水溶液酸碱滴定法:是利用非水溶剂的特点来改变物质的酸碱相对强度,即在水溶液中呈弱酸性或弱碱性的化合物,由于酸碱度太弱,不可能得到滴定的终点。如果选择某些适当的非水溶剂为溶剂使化合物增加相对的酸度成为强酸,或者增加相对的碱度成为强碱,就可以顺利地进行滴定的分析方法。 4.应用:本法主要用来测定有机碱及其氢卤酸盐、磷酸盐、硫酸盐或有机酸盐以及有机酸碱金属盐类药物的含量,也用于测定某些有机弱酸含量。 二、原理:酸碱质子理论 (一)有关酸碱的定义有三种学说 1.Arrhenius 的电离学说 凡化合物溶于水中能电离生成H+离子的是酸,能电离生成OH-离子的是碱。 H+ + OH- === H2O 酸碱反应即为中和,这种学说在水溶液中很适用,但在非水溶液中考虑离子平衡问题就受到限制。 2.刘易斯(Lewis)的电子理论 把酸碱反应看成是电子对转移共享的反应,认为酸是一个电子对的接受者,它接受一对电子以构成配位鍵;碱是一个电子对的供给者,它供给酸一对电子以构成配位鍵。 A + :B → A:B 任何物质,凡能从其它的分子或离子接受电子对组成一个安定生成物的,都是酸。 任何物质,凡能供给它种分子或离子以电子对而组成一个安定生成物的,都是碱。 中和反应是酸和碱形成配位鍵的反应。 电子理论从物质的本身去了解物质的酸碱性质,不依靠溶剂来说明。在非水溶液滴定中应用惰性溶剂(非极性溶剂)时,即以此学说为基础。 3.劳莱-勃伦斯(Lowry-Bronsted)的质子理论 (1)定义:凡能给出质子的物质是酸 凡能接受质子的物质是碱 表示方程:HA === A- + H+ 从这个方程式可以知道:酸和碱既可以是中性分子,也可以是阴离子或阳离子 (2)共轭酸碱对 一种酸给出质子后,所余的部分即是该酸的共轭碱 一种碱接受质子以后,即成为该碱的共轭酸 HA === A- + H+ HA和A-称为共轭酸碱对。 (3)强度定义 越容易给出质子的物质酸性越强,越容易接受质子的物质碱性越强。 强酸的共轭碱是弱碱,而强碱的共轭酸必定是弱酸。 如: HCl是一强酸,它的共轭碱Cl-则为弱碱。 (二)相对酸碱度 任何一种溶质溶于给定的溶剂中,其酸碱性都将受到溶剂的离解程度、溶剂的酸碱性及溶剂的极性等因素的影响。 所以,酸碱强弱不仅决定于物质本身的酸碱性,也决定于溶剂的性质。不同的酸溶解在相同的溶剂中,供给质子能力愈大的,显的酸性越强;一种酸在不同的溶剂中,溶剂接受质子能力愈强的,显的酸性愈强。因此,某些物质在水溶液中,其酸性或碱性很弱,不能进行滴定,便选择适当的碱性(或酸性)溶剂以增强其酸性(或碱性)来进行滴定。 例如:可以把在水溶液中显弱碱性的胺类溶于冰醋酸中,以增强其相对碱性,然后可用高氯酸滴定液滴定。 同样在水中呈弱酸性的物质,可以选择适当的碱性溶剂。如乙二胺或甲醇使其酸性增强后,用标准碱溶液甲醇钠滴定。 总之,酸碱强弱不能脱离溶剂而言。溶剂对酸碱的强弱影响很大,一个弱酸溶解在碱性溶液中,可以增强其酸性,一个弱碱溶解在酸性溶剂中,可以增强其碱性。非水溶液中的酸碱滴定即是利用这一事实,使原来在水溶液中不能滴定的弱酸弱碱,在选择适当的溶剂增强其酸碱性后,就可以滴定了。 (三)溶剂合质子 在水溶液中,H+离子不能单独存在,它与溶剂水分子结合成水合质子(H3O+),习惯上以H+表示。 在非水溶液中,游离的质子(H+)也不能单独存在,而是与溶剂分子结合成溶剂合质子。 (四)酸碱反应的实质 酸碱中和反应的实质是质子的转移,而质子转移是通过溶剂合质子实现的。按质子论的酸碱中和反应并无盐的生成。 在非水溶剂中,酸碱反应可用下式表示: 三、碱的滴定 (一)适用范围:.非水溶液滴定法,主要用来测定有机碱及其氢卤酸盐、磷酸盐、硫酸盐或有机酸盐,以及有机酸碱金属盐类药物的含量,也用于测定某些有机弱酸的含量。非水溶液滴定法,大多用于原料药品的含量测定。 (二)方法 1.滴定系统:一般,弱碱性化合物在酸性溶剂中能增强其碱性,即可用强酸进行滴定。上述各类药物多半可以在冰醋酸或醋酐中进行滴定,有时也可在一些惰性溶剂(苯、四氯化碳、氯仿等)或在能影响溶质的解离情况和能显著影响酸碱度的溶剂(硝基甲烷、二氧六环、丙酮等)中进行滴定。 滴定液多采用高氯酸的冰醋酸溶液。 2.指示终点的方法:电位法和指示剂法,一般按电位法指示终点,如采用指示剂时,终点颜色的变化应以电位法终点时指示剂的颜色的变化为准。实际操作中多用指示剂法。 以冰醋酸作溶剂,用酸滴定液滴定碱时,最常用的指示剂为结晶紫,还有α-萘酚苯甲醇(0.2%冰醋酸溶液,其碱式色为黄色,酸式色为绿色)和喹哪啶红(0.1%甲醇液,其碱式色为红色,酸式色为无色) 结晶紫指示液(0.5%冰醋酸溶液):其碱式色为紫色,酸式色为黄色。在不同的酸度下变色较为复杂,由碱区到酸区的颜色变化有: 紫色→蓝色→蓝绿色→绿色→黄绿色→黄色 在滴定不同的碱时,终点颜色变化不同: (1)滴定较强的碱时,应以蓝色或蓝绿色为终点; (2)滴定较弱的碱时,应以蓝绿色或绿色为终点。 在非水溶液酸碱滴定中,除用指示剂指示终点外,电位滴定法是测定终点的基本方法。因为在非水溶液滴定中,有许多物质的滴定,目前还没有找到合适的指示剂,而且在选择指示剂和确定指示剂终点颜色时都需要以电位滴定法作为对照。 (三) 酸根对于碱滴定的影响 由HClO4滴定碱的反应式可知,滴定有机酸的盐生成相应的酸HA。当滴定生成的酸HA比HClO4的酸性强度差的越远,反应就越易进行。根据实验知道,某些强的无机酸(冰醋酸溶液)比较其酸性强度为: HClO4HBrH2SO4HClHNO3其他酸 所以HClO4在冰醋酸中是很强的酸。有机碱的氢卤酸盐则由于HX在冰醋酸中酸性比较强,反应不能进行完全,所以不能直接滴定,可加入过量的醋酸汞试液所以HClO4在冰醋酸中是很强的酸,使与有机碱的氢卤酸盐发生复分解反应。 2BHX + Hg(Ac)2 → 2BHAc + HgX2 HgX2和Hg(Ac)2都是络合物,而HgX2 比Hg(Ac)2更加稳定,难于电离,所以这时即可用HClO4直接去滴定。其反应式可综合如下: 2BHX + Hg(Ac)2 → 2BHAc + HgX2 HClO4 + HAc → H2Ac+ + ClO4- H2Ac+ +BHAc→BH++ 2 HAc HClO4 + BHAc → BH+ + ClO4- + HAc 滴定生成的HAc比HClO4的酸度要弱得多,故反应可进行完全。如:盐酸环丙沙星、盐酸左旋咪唑原料的含量测定方法,即以上述方法排除氢卤酸盐的影响。
请教一下各位:目前执行的国家标准GB/T 21918-2008,是硼砂硼酸测定的标准,该标准的检测原理是测定样品中硼元素的含量后按照比例转换为相应的硼酸和硼砂,这样就可以进行报告,请问这样的换算科学吗?食品中的硼元素一定是以硼酸或者硼砂的形式存在的吗?硼元素在食品当中没有其他的的存在方式吗?
现在需要测定定锂离子电池正极材料中的粘结剂PVDF(聚偏二氟乙烯)的含量,不知能否用DSC测定。如果能测定,请说明一下测定原理。[em01]
红外测油仪测水中油含量的原理是什么?

水质中氮磷含量的测定方法一、前言根据单位领导要求尝试做一下水质中氮磷含量的测定,借助以前现有的检测方法,例如肥料或者土壤中氮磷的检测方法。二、检测原理2.1氮的检测原理:采用纳氏比色法,无论是肥料还是以前的土壤中氮的检测都是一样的试剂,包括加的滴数都一样。2.2磷的检测原理:肥料中的是采用的磷钼黄法,土壤中的采用的是磷钼蓝法。两种方法的试剂有区别,进行了分别实验。三、实验所用试剂及仪器3.1试剂:土壤肥料铵态氮试剂全套肥料磷显色剂土壤有效磷试剂全套水解氮水解剂硝态氮助掩剂硫酸土壤标准储备液PH试纸3.2仪器及玻璃器皿:YN—2001型土壤养分速测仪;电陶炉50ml闭塞管,250ml三角瓶、移液管(1.0ml、2.0ml、5.0ml)、玻璃棒、玻璃珠、比色皿、量筒四、实验前处理4.1浓缩4.1.1第一次前处理量取200ml自来水样品于250ml三角瓶中,加入0.5ml浓硫酸和4粒玻璃珠,摇匀,放到电陶炉上加热浓缩至约10ml左右;同时做空白(量取200ml蒸馏水做空白)、标准(标准是在空白的基础上添加0.25ml土壤标准储备液)和样品添加(样品添加是在样品的基础上添加0.25ml土壤标准储备液);同时做平行试验4.1.2第二次前处理根绝第一次前处理后检测的结果,样品经过浓缩8倍后仍检测不出来,所以本次前处理采用在样品中添加不同含量土壤标准储备液,处理过程同“4.1第一次前处理”一样,分别添加了0.1ml、0.25ml、0.35ml、0.5ml土壤标准储备
激光粒子计数器能不能测定胶体的颗粒含量?因为胶体有丁达尔现象 这与粒子计数器的原理相悖吗?因为我测了很多组数据 好像不太适合,所以请教各位高手。 仪器型号:cls-700 有知道的麻烦回复或发到我的邮箱:zoufengpingok@163.com 谢谢了
石灰石中钙、镁含量的测定目的原理实验目的1. 练习酸溶法的溶样方法;2. 掌握络合滴定法测定石灰石或白云石中钙、镁含量的方法和原理;3. 了解沉淀分离法在本测定中的应用;4. 练习沉淀分离中的一些基本操作技术,如沉淀、过滤、洗涤等。实验原理石灰石、白云石的主要成分为CaCO3和MgCO3,此外,还常常含有其他碳酸盐、石英、FeS2、粘土、硅酸盐和磷酸盐等。石灰石、白云石中钙、镁含量测定的原理如下:1.试样的溶解:一般的石灰石、白云石,用盐酸就能使其溶解,其中钙、镁等以Ca2+、Mg2+等离子形式转入溶液中。有些试样经盐酸处理后仍不能全部溶解,则需以碳酸钠熔融,或用高氯酸处理,也可将试样先在950-1050℃的高温下灼烧成氧化物,这样就易被酸分解(在灼烧中粘土和其他难于被酸分解的硅酸盐会变为可被酸分解的硅酸钙和硅酸镁等)。2.干扰的除去:白云石、石灰石试样中常含有铁、铝等干扰元素,但其量不多,可在pH值为5.5-6.5的条件下使之沉淀为氢氧化物而除去。在这样的条件下,由于沉淀少,因此吸咐现象极微,不致影响分析结果。3.钙、镁含量的测定:将白云石、石灰石溶解并除去干扰元素后,调节溶液酸度至pH≥12,以钙指示剂指示终点,用EDTA标准溶液滴定,即得到钙量。再取一份试液,调节其酸度至pH≈10,以铬黑T(或K-B指示剂)作指示剂,用EDTA标准溶液滴定,此时得到钙、镁的总量。由此二量相减即得镁量,其原理与EDTA溶液之标定相同,此处从略。仪器药品0.02mol/dm3EDTA标准溶液、1+1HCl溶液、1+1氨水、NH3-NH4Cl缓冲液(pH≈10)、10%NaOH溶液、钙指示剂、铬黑T指示剂、K-B指示剂、0.2%甲基红指示剂、镁溶液、1+1三乙醇胺溶液。过程步骤一、试液的制备准确称取石灰石或白云石试样0.5~0.7g,放入250ml烧杯中,徐徐加入8-10ml 1+1HCl溶液,盖上表面皿,用小火加热至近沸,待作用停止,再用1+1HCl溶液检查试样溶解是否完全?(怎样判断?)如已完全溶解,移开表面皿,并用水吹洗表面皿。加水50ml,加入1-2滴甲基红指示剂,用1+1的氨水中和至溶液刚刚呈现黄色。(为什么?) (在教学时数允许时,除去Fe3+、Al3+等干扰离子可采用分离的方法,这样可以对沉淀、分离、洗涤等操作再进行一次训练。时数不足时,可以采用加掩蔽剂的方法,即在石灰石、白云石试样经酸溶解完全后,用容量瓶稀释至250ml。然后在测定钙量和钙、镁合量时吸出25ml溶液中加1+1三乙醇胺溶液3ml,其他步骤不变。)煮沸1~2min,趁热过滤于250ml容量瓶中,用热水洗涤7~8次。冷却滤液,加水稀释至刻度,摇匀,待用。二、钙量的滴定先进行一次初步滴定,(进行初步滴定的目的是为了便于在临近终点时才加入NaOH溶液,这样可以减少Mg(OH)2对Ca2+离子的吸附作用,以防止终点的提前到达。)吸取25ml试液,以25ml水稀释,加4ml 10%NaOH溶液,摇匀,使溶液pH达12-14左右,再加约0.01g钙指示剂(用试剂勺小头取一勺即可),用EDTA标准溶液滴定至溶液呈蓝色(在快到终点时,必须充分振摇),记录所用EDTA溶液的体积。然后作正式滴定:吸取25ml试液,以25ml水稀释,加入比初步滴定时所用约少1ml的EDTA溶液,再加入4ml10%NaOH溶液,然后再加入0.01g钙指示剂,继续以EDTA滴定至终点,记下滴定所用去的体积V1。三、钙、镁总量的滴定吸取试液25ml,以25ml水稀释,加入5ml NH3-NH4Cl缓冲溶液,使溶液酸度保持在pH = 10左右,摇匀,再加入0.01g铬黑T指示剂 (或K-B指示剂),以EDTA标准溶液滴定至终点,记下滴定所用去的体积V2。分析思考 1.络合滴定法测定石灰石或白云石中钙、镁含量的原理是什么?这时钙、镁共存,相互有无妨碍?为什么?2.怎样分解石灰石或白云石试样?用酸溶解时,应注意什么?怎样知道试样溶解已经完全?3.用1+1氨水中和溶液至刚刚使甲基红指示剂呈现黄色时溶液的pH值为多少?4.本法测定钙、镁含量时,试样中存在的少量铁、铝等物质有干扰吗?用什么方法可以除去铁、铝的干扰?
[em0801]红外光谱测定地产小麦维生素E含量 这个我没弄懂它的原理,还不确定检测它的方法,所以在此发出求助的帖子,希望高手指导,小妹谢拉!!
甲醛法测试高氯酸铵含量测试原理有人知道么?
维权声明:本文为abcdefghijkl123原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现的,均属侵权违法行为,我们将追究法律责任。 面制品中铝含量的测定1.原理 在pH6.7~7.0范围内,铝在聚乙二醇辛基苯醚和溴代十六烷基吡啶的存在下与铬天菁S反应生成了蓝绿色的四元胶束,比定定量。2原因:面制品中铝含量的测定国标是用GB/T5009.182-2003法测定,测定面包中的铝含量铬天菁-S法的操作关键点是控制反应液的pH值。GB/T5009.182-2003法规定样品消化处理后待测样液应保证试样溶液中含有1%硫酸。这给操作不熟练者带来了一定的难度,因为消化处理和样品稀释过程中,赶酸的程度存在差异,不易于控制待测液的pH值。而样品经消化处理后样液依据GB/T5750.6-2006铬天菁-S法测定铝含量,该法待测液的pH容易控制,准确度与重现性高,且该法灵敏度更高,检测限可达0.2μg。3.两种方法比对:抽取了4个不同含量的面制品样品用两种方法检测,检测数据记录见下表13.1两种方法工作曲线的绘制:第一法:GB/T5009.182-2003标样浓度(μg)ABS000.50.0521.00.0842.00.1563.00.2304.00.289波长:640nm比色皿:1cm[

[b]饲料水分仪在水产饲料中的控制及应用[/b] 颗粒饲料的水分含量是一项非常重要的质量指标,它直接影响到颗粒饲料的品质和饲料企业的经济效益,对其进行有效控制是保证饲料产品质量安全的关键技术之一。水分含量超过规定的标准,颗粒饲料容易发霉变质,不利于保存,还会使营养成分的含量相对减少;但如果产品水分含量过低,对企业又造成了不必要的损失,而且高低不均的水分含量,还造成产品质量的不稳定,影响到产品的品牌声誉。在饲料加工过程中,适宜的水分含量有利于制粒,降低能耗、提高生产。因此,在配合饲料的生产过程中,要使生产更顺利地进行,能耗更低,颗粒更光洁均匀,最终产品又符合规定的水分含量标准,就必须进行生产全过程的水分控制。大部分客户目前都在使用深圳冠亚生产制造的[b]SFY系列快速水分测定仪[/b],仪器方便快捷,测量准确高,是一款理想的水分检测设备。水分控制,就是在生产的整个过程中根据不同的情况综合控制各种因素,使产品的最终水分含量达到生产者的预期目标。影响饲料产品最终水分含量的主要因素有:饲料原料本身的水分含量、粉碎阶段的水分变化、混合阶段的液体添加量、蒸汽的水分含量、调质水平、压模的模孔大小及其厚度、冷却器的风量及风干时间、包装质量管理、不同气候环境因素的影响等。[img=饲料水分检测仪,690,312]http://ng1.17img.cn/bbsfiles/images/2017/09/201709011422_01_2233_3.jpg[/img][b] 一、饲料原料的水分控制[/b] 1、原料接收过程中的水分控制关键在于准确检测原料样品中的水分含量 抽样必需代表整批原料的综合情况,按取样标准抽取样品,防止漏抽,同时在抽样过程中感观检测原料水分的高低。原料水分检测过程中要保证准确,为减小误差,可以作两到三个平行样品的检测,求取平均值作为检测值。 2、做好易吸水的原料(米糠、麦麸等)的管理和存贮 易吸水的原料一次性进货无需太多,同时避免靠墙堆码,注意仓库管理,防潮,潮湿天气防止湿气入仓。应根据正常生产条件下的原料用量进料,原料出库遵循“先进先出”原则,尽量缩短原料的库存期。经检测,入库水分为10%以上的棉菜粕,库存六个月后,水分损失约为1%。[img=颗粒饲料水分检测仪,400,500]http://ng1.17img.cn/bbsfiles/images/2017/09/201709011423_01_2233_3.jpg[/img] [b] 二、粉碎阶段中的水分控制[/b] 粉碎工艺是饲料产品加工过程的关键环节,水分在粉碎过程中的损失不容忽视。通过对不同孔径的粉碎机筛片,粉碎前后物料水分含量进行对比检测分析发现,随着物料粉碎粒度的减小,水分损耗明显增加。同样对不同梯度水分含量的物料,作粉碎前后物料水分含量对比检测分析发现,随着物料水分含量的增加,粉碎后粉料的水分损耗增加,水分的最大损耗接近1%,粉碎效率显着降低,能耗明显增加。虾料超微粉碎后,粒度98%能过80目。鱼料目前使用较多的是水滴型的锤片粉碎机,筛网的粒径在1.0~1.5毫米。对配有负压吸风并有风门调节装置的粉碎机,可调节风量的大小。对粉碎前后物料水分损耗作对比检测发现,风量的大小对生产效率影响较显着,而水分损耗没有显着影响,但随着风量的增加,水分损耗仍有增加的趋势。玉米粉碎后用机械运输水分损耗为0.22%,用气力运输损耗为0.95%。虾料大多用的是无网的超微粉碎,是使用吸风的气力运输,鱼料大多是粉碎后使用绞龙做机械运输。 [b] 三、混合过程中的水分控制[/b] 当混合后粉料的水分含量远低于12.5%时,可考虑在混合时喷加雾化水。但目前这方面存在很多问题:不能超过2%;保水性能差,添加2%的水仅有40~50%的保水率;最好是使用热水,防霉;要考虑混合时间和水分添加时间(一起喷完)的一致;为保证均匀,调整喷头的位置和喷水口大小;需要加防霉剂;要注意清理混合机的内壁。诸多因素限制了在混合机加水,而且加的游离水会使成品料的潜在发霉机会增加。[img=饲料水分检测仪,690,412]http://ng1.17img.cn/bbsfiles/images/2017/09/201709011423_02_2233_3.png[/img] [b]SFY系列快速水分测定仪[/b]是针对粮食(饲料)深加工过程中水分检测而研发的一款第五代高性能全自动水分检测设备,该水分仪采用国际烘箱原理。按照国家标准取样X克,均匀的放置称量盘上,其环状的卤素加热器确保样品在测试过程中均匀受热,使样品表面不易受损,按测试键,仪器开始测量。水分仪持续测量并即时显示样品丢失的水分含量%,干燥程序完成后,最终测定的水分含量值被锁定显示。快速水分测定仪与国际烘箱加热法相比,其检测结果与国标玉米中水分的测定GB/T 1353-2009(105℃恒重法)检测结果具有良好的一致性,并有可替代性,且检测效率远远高于烘箱法(105℃恒重法)。一般样品只需几分钟即可完成测定。适用范围:花生,小麦,玉米,谷物,水稻,高粱,大豆,芝麻,绿豆等.
[color=#333333][font=&][color=#333333]总氮是各种无机态氮(硝酸盐氮、亚硝酸盐氮、氨氮)和有机态氮(蛋白质、氨基酸、有机胺)的总量,它是衡量水质的重要指标。[/color][/font][font=&][color=#333333]目前,比较常用的总氮检验方法是碱性过硫酸钾消解紫外分光光度法(HJ636-2012)。[/color][/font][font=&][color=#333333]但很多水友反应该方法不好做,其中代表性问题有:[/color][/font][font=&][color=#333333]氨氮高于总氮的测定结果;[/color][/font][/color][font=&][color=#333333]按道理来说,氨氮包含于无机氮,而无机氮包含于总氮中。[/color][/font][font=&][color=#333333]但在实际测定中,氨氮总氮的情况还是很常见的。[/color][/font][font=&][color=#333333]对于这种现象来说,一般看法是样品中氨氮含量较高时,加入碱性过硫酸钾,在碱性条件下形成氨水,氨水挥发生成氨气,从比色管中释放出来,导致测定的总氮量只包含了部分氨氮,从而低于氨氮含量。[/color][/font][font=&][color=#333333]因此,利用碱性过硫酸钾消解紫外分光光度法处理样品时,可以在所有样品都加入过硫酸钾溶液后,统一加盖。这样就给氨氮含量较高的样品中氨氮以氨气形式挥发出来创造了时间。[/color][/font][font=&][color=#333333]当然,也有操作人员采用双管消解法。即将样品加入比色管用无氨水稀释至10mL后,将碱性过硫酸钾加入另一小试管中,再将装有碱性过硫酸钾的小试管放入比色管中,小试管顶部的高度应超出比色管中的试样液面以避免样品处于碱性环境,盖上比色管盖后,再进行比色管内两种液体的混合。[/color][/font][font=&][color=#333333]但双管法在实际操作过程中过于繁琐,测试结果也不是很理想。[/color][/font][font=&][color=#333333]其实,针对氨氮总氮这个问题应该如HJ636-2012的征求意见稿所说,“不应该仅仅停留在总氮测定本身上,而是应该从测定总氮和氨氮两者之间存在的一些联系上查找原因”,“在不断完善总氮测定的过程中,还应同步完善氨氮测定中包括实验用水、器皿、试剂和实验环境,使两者同步远离氮的污染,才能保证测定结果的正确性。”转自食品伙伴网[/color][/font]
实验方法原理 DNA 在酸性条件下加热,其嘌呤碱与脱氧核糖间的糖苷键断裂,生成嘌呤碱、脱氧核糖和脱氧嘧啶核苷酸,而2-脱氧核糖在酸性环境中加热脱水生成ω-羟基-γ-酮基戊糖,与二苯胺试剂反应生成蓝色物质,在595nm 波长处有最大吸收。DNA 在40-400μg 范围内,光吸收与DNA的浓度成正比。在反应液中加入少量乙醛,可以提高反应灵敏度。实验材料 DNA样品试剂、试剂盒 DNA 钠盐 NaOH 溶液 二苯胺 冰乙酸 过氯酸 乙醛仪器、耗材 分光光度计 水浴锅实验步骤 1. 制作DNA 标准曲线:取12 支洁净干燥试管加入DNA标准溶液,加完各试剂后,充分混匀。于60℃水浴中保温1h,冷却后于595nm 波长处以1,2 管为空白调零,测定各管光密度(OD595nm)。取两管的平均值,以DNA 的含量为横坐标,光密度为纵坐标,绘制标准曲线。2. 样品DNA 含量测定:取2 支干净试管 加入样品试剂,其它操作同上。待测溶液中的DNA 含量应调整至标准曲线的可读范围内。3. DNA 含量计算:以样品的光密度,从标准曲线上查出相对应DNA 含量,计算出样品中DNA 的百分含量。注意事项 二苯胺试剂具有腐蚀性,且二苯胺反应产生的蓝色不易褪色,操作中应防止洒出,比色时,比色杯外面一定要擦干净。其他 二苯胺主要用于合成橡胶的防老剂、燃料和医药中间体,润滑油抗氧剂,也是火药的稳定剂。硝酸盐、氯酸盐和其他氧化性物质的检定。铱的催化测定。硝酸盐的光度测定。氧化还原指示剂。单倍体育种培养基。制造染料。是硝化纤维素、炸药、火棉的稳定剂。