[size=18px]检验检测机构在运用计算机信息系统实施检验检测、数据传输或者对检验检测数据和相关信息进行管理时,应当具有保障安全性、完整性、正确性措施。1.检验检测机构在利用计算机信息系统对检验检测数据进行采集处理、记录、报告、存储或者检索时,检验检测机构的管理体系文件应包含保护数据完整性、安全性和不可伪造篡改的内容,防止未经授权的访问,确保检验检测数据、结果不被篡改、不丢失、可追溯。2.检验检测机构应当对所使用的自动化软件的正确性进行验证并保留相关活动记录,自动化软件包括但不限于信息化管理系统、数据采集系统、数据处理系统。3.检验检测机构管理体系应包含计算机信息系统的数据保护、电子存储和传输结果的规定。[/size]
[b][url=http://www.f-lab.cn/cell-analyzers/wga-dna.html]DNA完整性检测试剂[/url][/b]是为[b]DNA完整性检测[/b]和[b]全基因组扩增WGA[/b]质量检测控制而设计的[b]PCR检测器[/b]具,它采用PCR技术,非常适合[b]WGA染色[/b]应用等[b]WGA质量检测[/b]。一瓶DNA完整性检测试剂可检测10个DNA片段.[img=DNA完整性检测试剂]http://www.f-lab.cn/Upload/WGA-DNA-integrity.JPG[/img]DNA完整性检测试剂:[url]http://www.f-lab.cn/cell-analyzers/wga-dna.html[/url]
各有关单位: 根据《天津市环境影响评价协会团体标准管理办法(试行)》的相关要求,天津市环境影响评价协会秘书处对《工业水处理系统膜组件完整性光谱法检测技术规程》团体标准组织召开了立项专家审查会,经技术专家认真研究与审核,该项团体标准编制技术路线合理、方案可行,同意该团体标准立项申请。该项团体标准符合立项条件,现批准立项。 请该项团体标准立项申请单位严格把控标准编制质量和水平,增加标准的实用性,尽快组织完成标准编写工作。 天津市环境影响评价协会2024年10月24日 https://www.ttbz.org.cn/ueditor/dialogs/attachment/fileTypeImages/icon_pdf.gif天津市环境影响评价协会关于《工业水处理系统膜组件完整性光谱法检测技术规程》团体标准立项的公告.pdf
质量控制是每个实验室必须做的一个工作,不论是外来的原辅料还是企业内部生产的中间品、成品都必须经过实验室的检测。对实验室检测而言,结果报告是实验室的最终产品。结果报告的准确性和可靠性,直接关系到公司的切身利益,也关系到实验室的形象和信誉。为保证实验室质量控制的有效性,首先应保证实验室数据的完整性。数据完整性是指应能保证在整过生命周期内,所有数据均完全一致和准确。实验室由于其涉及的数据信息量大,首当其冲成为数据完整性的重灾区。从国家局发布的飞行检查数据显示自2015年12月1日计算机化系统生效以来,12家问题企业涉及实验室数据完整性缺陷的有6家,占总数的50%,而自2016年发布的5家问题企业有4家涉及。通过以上不难看出实验室是GMP检查的一个重点区域,而实验室的数据完整性又是一个重中之重。实验室的主要工作是完成对样品的检测,发出检测报告书,因此检测过程中原始数据和原始记录是非常重要的,这些数据和记录是检测过程中的基础信息来源,也是结果报告的重要依据。随着检验用仪器设备日新月异的发展以及仪器设备使用的商业计算机软件的开发,现代化仪器设备为我们检测工作提供了极大的方便同时提高我们的工作效率为保证实验室数据的完整性检验人员需要做到以下几点:1、标准品的配制、溶解、流动相等数据记录和维护应确保可追溯使用的具体物料、称量、混合时间等,包括发生的日期,时间及操作人员。2、必须关注所有决定成品放行的数据。不符合规定的数据应该展开调查。3液相应安装审计追踪功能,并设置三级权限管理,只允许相关人员通过其单独的用户名和密码进入系统并浏览或编辑其相应工作项下的数据。4、原始数据的原件和复印件应保持一致,并清晰可见。5、检验记录或其它相关记录应受控,实验室不允许出现没有编号或受控号的记录。6、HPLC或其它设备不允许样品或标准品试进样;不允许与样品图谱相近的试样,与SOP操作一致性,不允许SOP没的有规定的操作。8标准品和样品应使用始终如一的积分参数,并附在检验记录中。9以前批次的色谱图不得重复打印、命名为当前批次。实验室质量控制应该是严谨的操作、即使的记录、准确的分析。做检测就像是当审判官,你的一举一动关乎着他人的安微,因为质量是药品的生命而检测就是质量的生命。
YYT 0681.11-2014 无菌医疗器械包装试验方法 第11部分:目力检测医用包装密封完整性
现在对于滤芯、滤膜完整性测试的要求越来越严,有谁了解这方面的工作?采用哪种仪器?采用哪种方法?完整性测试的传统方法包括:气泡点测试法、扩散流测试法,这些测试方法都要求使用合适的湿润剂将被测滤膜彻底湿润。对于疏水性滤膜,采用上述方法测试前,必须使用表面张力比滤膜材质本身表面张力小的润湿剂,实际应用中采用如醇类或醇水混合液等有机溶剂作为湿润剂,来保证滤膜充分湿润。当过滤系统是生物反应器或发酵罐的无菌空气过滤器和呼吸器时,经测试过程而残留在滤膜的有机溶剂会对料液产生危害。同时,从操作的安全性考虑,使用有机溶剂时,对相应的生产设备必须进行防燃和防爆等保护措施,并且还有避免有机溶剂污染产品,最后,使用前干燥滤器的方法也相当复杂。此外,在线测试滤器完整性的同时,还必须测定滤器的安全密封性。而滤器在经过在线蒸汽灭菌后,就不能在使用有机溶剂湿润滤器来进行完整性测试。
随着检验用仪器设备日新月异的发展以及仪器设备使用的商业计算机软件的开发,现代化仪器设备为我们检测工作提供了极大的方便同时提高我们的工作效率为保证实验室数据的完整性检验人员需要做到以下几点:1、标准品的配制、溶解、流动相等数据记录和维护应确保可追溯使用的具体物料、称量、混合时间等,包括发生的日期,时间及操作人员。2、必须关注所有决定成品放行的数据。
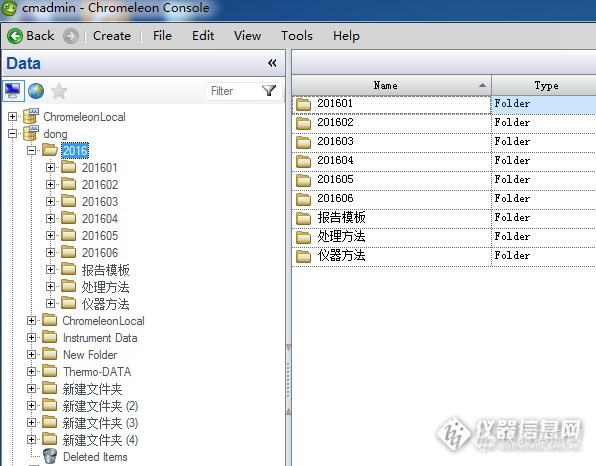
确保变色龙客户端数据备份完整性使用thermo变色龙软件的用户,在仪器运行一段时间后,会产生大量的数据,包括序列表、审计追踪、仪器方法、处理方法、报告模板,这些数据都是用户积累的宝贵财富,如何正确有效的保证数据完整的长期保存下去变得非常重要,下面就此问题提供几个建议。用户在建立序列、仪器方法的时候通常会建立不同的文件夹,当然本人也建议这么去操作,方便之后的数据管理,有的用户会按年月份来建立数据存放文件夹,如图一,有的用户按检测目标物的种类建立数据存放文件夹,如图二,等等。接下来我就以按日期建立文件夹举例分析。图一:http://ng1.17img.cn/bbsfiles/images/2017/01/201701191701_669157_3139210_3.png图二:http://ng1.17img.cn/bbsfiles/images/2016/09/201609301000_612941_3139210_3.png按如上方式建立文件夹不仅有利于数据查找,对之后的数据备份也有好处,数据备份时,先在桌面建立一个文件夹,可以以数据备份时的日期命名,让后右击201601文件夹,点击复制或发送到,如图三,将数据粘贴到您刚建立的文件夹内,依次操作剩余的文件夹,在这里不建议直接将2016文件夹整个复制,这在之后的数据恢复时遇到报错时很那处理,因为这个文件夹包含的内容比较多,当恢复数据出现错误,如图四,就很难确定是哪个子文件的问题,不利于数据的完整性。图三:http://ng1.17img.cn/bbsfiles/images/2016/09/201609301003_612943_3139210_3.jpg图四:http://ng1.17img.cn/bbsfiles/images/2016/09/201609301003_612944_3139210_3.jpg将数据成功导出到指定文件夹后,可以在变色龙软件数据管理界面新建一个文件夹,将备份的数据导入(图五)此文件夹,来确认导出的数据完整性,这样就能确保数据的完好保存了。图五:http://ng1.17img.cn/bbsfiles/images/2016/09/201609301004_612945_3139210_3.jpg
最近一个客户参观向我们提出了分析样品的完整性的概念,我们非常迷惑,样品的完整性包括哪几方面的内容呢?向各位大侠求救了~~~[em0812] [em0812] [em0812]
看到的关于数据完整性和审计追踪的一段话,分享下:“现在数据完整性已经引起了FDA,欧盟GMP检察官的高度重视,特别是印度和中国的药企,查的最多,FDA在中国的检察官已经增加到20人左右(以前就几个人)。他们查电子版的数据查的特别严格,专门比对电子版数据和纸质版数据是否一致。FDA还特别请安捷伦工程师给他们培训服务器和审计追踪。HPLC和GC不连服务器,不开审计追踪,或者工作站的使用权限没分开(管理者和分析员,即便最高管理者也不应有删除数据的权限),都会有恶意篡改数据的嫌疑,HPLC和GC的电脑不设置开机和锁屏密码、工作站一定时间不操作自动锁定不设置,或者FDA官员检查时,你输入工作站密码不加遮挡,都会被怀疑数据完整性或者缺陷。现在更是连天平、PH计、水分测定仪也有这方面要求的趋势。”液相做的少,这两个怎么理解的”不设置锁屏密码、工作站一定时间不操作自动锁定不设置“?
[color=#333333]点击链接查看更多:[url]https://www.woyaoce.cn/service/info-39732.html[/url][font=&][size=16px]服务背景[/size][/font][font=&][color=#333333][/color][/font]富士康华南检测中心SI实验室,专业信号质量测试、信号完整性分析第三方检测实验室,拥有26余年信号眼图测试经验,提供元器件性能验证,元器件系统可靠性验证,信号完整性测试,元器件标杆比对分析,元器件/系统失效分析,帮助对元器件进行评估筛选,风险预警。可帮助供应商搜寻开发,以及供应商风险能力评估,更多信息,可联系博主交流[font=&][size=16px]检测内容[/size][/font][font=&][color=#333333][/color][/font]l SB2.0接口为什么要做信号完整性测试?USB2.0数据线目前应用较为广泛,USB传输信号质量稳定性与可靠性,需要实验室功能测试和安全测试来评估,业内常用的方案大多为信号完整性测试。USB2.0串行总线使用四条线:VBUS主机Host或集线器hub电源线、D-传送数据线、D+传送数据线和接地线。在信号质量都有规定的速率等级和上升时间,USB2.0是否合规,并获得认证资质的关键评判因素就是信号质量稳定性。[/color][table][tr][td]类型[/td][td]数据速率[/td][td]上升时间[/td][/tr][tr][td]低速[/td][td]1.5Mbps[/td][td]75-300纳秒[/td][/tr][tr][td]全速[/td][td]12Mbps[/td][td]4-20纳秒[/td][/tr][tr][td]高速[/td][td]480Mbps[/td][td]500皮秒[/td][/tr][/table]l USB2.0信号质量测试项目眼图测试信号速率涨落时间JK抖动KJ抖动连续抖动数据包结束宽度单调测试,适用于高速交叉电压范围,适用于低速和全速信号眼图测试报告[table][tr][td]No.[/td][td]Test Item[/td][td]Test result[/td][/tr][tr][td]1[/td][td]Signal quality[/td][td]Pass[/td][/tr][tr][td]2[/td][td]Packet parameter[/td][td]Pass[/td][/tr][tr][td]3[/td][td]Resume measurement[/td][td]Pass[/td][/tr][tr][td]4[/td][td]Reset from suspend[/td][td]Pass[/td][/tr][tr][td]5[/td][td]Suspend[/td][td]Pass[/td][/tr][tr][td]6[/td][td]Reset from high speed[/td][td]Pass[/td][/tr][tr][td]7[/td][td]Chirp[/td][td]Pass[/td][/tr][tr][td]8[/td][td]J/K,SE0_NAK[/td][td]Pass[/td][/tr][tr][td]9[/td][td]Receiver sensitivity[/td][td]Pass[/td][/tr][/table][font=&][size=16px][color=#333333]检测标准[/color][/size][/font][font=&][color=#333333][/color][/font][table][tr][td]产品名称[/td][td]检测项目[/td][td]检测标准[/td][/tr][tr][td]USB2.0[/td][td]信号完整性测试[/td][td]实验室标准[/td][/tr][/table][font=&][size=16px][color=#333333]我们的优势[/color][/size][/font][font=&][color=#333333][/color][/font]优尔鸿信总部富士康华南检测中心针对USB2.0信号质量测试,主要基于Tektronix的USB2.0 发送端,加上软件TDSUSB2,支持Embed嵌入、De-embed去嵌入功能,内置Host和Device的一致性通道传递函数,可以嵌入一致性通道模型,面向Host端的产品、Device端产品,均可完成一致性测试规范要求。
Academy of Management Journal编辑部发表了系列文章,谈论文写作要注意什么问题。该刊2012年第1期由Yan(Anthea)Zhang和Jason D. Shaw合写的文章属于这个系列的第5部分,专门讨论“方法”与“结果”两小节的写作。我觉得,文章所谈的内容不仅适用于管理学论文,而且具有超出管理学学科的一定的普遍意义,故简要介绍其观点。两位作者对该刊保存的大量拒稿信档案进行了考察,看看被拒文稿有什么共同问题,结果发现,它们主要在completeness(完整性)、clarity(清晰性)和credibility(可信性)这3C中的至少一方面出了问题。“方法”小节的3C完整性“方法”小节要实现3个目标,每个目标都涉及完整性的问题。1.要交代研究过程的how、what和why。比如,论文涉及的所有测度值如果能放在附录中就很好。2.使得读者读完论文后,能够就本文的优点与缺点作出评价。3.提供充分的信息,让人家有可能重复本项研究,得出同样的结果。清晰性作者在清晰性方面经常出问题,比如,说本文所用的指标是对原有指标做了改进,却没讲清楚到底是怎么改动的,改动的依据是否充分。可信性1.一定要交代为什么选取某个样本。2.最好简要小结一下本文采用的构念(Construct)的定义,然后再描述相关构念的测度指标。3.说清为什么要进行某种操作。比如,有多种可供选择的指标时,应说明本文除了最后选定的指标外,还考察过哪些其他指标,为什么弃用那些指标。4.一定要就模型设定和数据分析方法展开一些论证,比如同样对于面板数据,是采用固定效应模型还是采用随机效应模型?“结果”小节的3C完整性文章采用的分析单位、样本规模、模型的变量等,一定要阐述清楚。清晰性常见的问题是,有的作者没有把研究发现与起初的研究假设关联起来。有时候,你得出的结果不能支持假设,但是,不具有显著统计意义的结果,与期望值符号相反的结果,也是同等重要的。有的作者喜欢将这些不太理想的结果给隐藏起来,反而被审稿者逮个正着。另外,对于不同的变量,这一段是按这个次序叙述的,下一段也按这个次序来叙述,也有助于文章的清晰性。可信性1.要回答,为什么自己对结果的阐释是合适的。2.如果存在着多种指标、方法和模型设定方式,而作者只选了一种,就可能被批评为“摘樱桃”――挑选有利的结果来支持自己的假设。因此,最好要提供补充性的分析和稳健性检验。3.即使所得结果具有显著的统计意义,读者仍会问:那又怎么样?具有显著统计意义的效应未必是实际意义重大的效应。因此,可以做一些追加分析来表明研究结果确实具有实际意义。
2008年8月13日,欧盟化学品管理局(ECHA)发布了IUCLID 5的新插件——PPORD通报完整性检查工具。根据REACH法规条款,当制造/进口的物质用于以产品和制程为导向的研发(即PPORD)时,可以通过通报免除注册义务,这可以看作是REACH法规鼓励创新的一个侧面。当通报人完成通报文件的编辑之后,就可以使用此完整性检查工具,对文件自行进行完整性检查,检查完成后,再行进行提交,从而避免因卷宗不完整带来重复提交的局面。点击下载:[url=http://echa.europa.eu/iuclid]PPORD通报完整性检查工具[/url]ECHA的这一举动,使我们有理由相信,为注册及其他提交ECHA的卷宗发布完整性检查的工具,应当已进入议事日程!
[align=center][b][size=14.0pt]数据完整性在细胞计数中的要求[/size][/b][/align][align=center][size=11.0pt]会议时间:2020年3月20日14:00[/size][/align][b][size=12.0pt]内容介绍:[/size][/b]GMP体系中数据完整性的基本要求,不同大小的细胞计数的不同要求以及vicell的技术优势和数据完整性介绍。[b][size=12.0pt]讲师介绍:[/size] [size=11.0pt]丁华平:[/size][/b][size=11.0pt]10[/size][size=11.0pt]年以上的重组蛋白/抗体的细胞培养和纯化工艺开发和工艺放大研究和管理工作经验,包括CHO、大肠杆菌;有CMC技术转移和200L/250L/2000L工艺放大经验,熟悉并了解cGMP、PAT、QbD和NDA的要求; CMC项目管理经验丰富; 在培养基开发、细胞培养平台技术开发、工艺过程控制和工艺放大至200L/250L/2000L生物反应器方面经验丰富。[/size]报名地址:[url]https://www.instrument.com.cn/webinar/meeting_10387.html[/url]
在对质量管理体系的变更进行策划和实施时,保持质量管理体系的完整性.,采取何种措施来保证体系的完整性??
请问 作为企业内部实验室,会出现ABCD部门,对于同一产品,A部门只要求A方面数据,B部门只要求B方面数据,现在我们的做法是单独出具报告,cl01要求报告的完整性,即不能只出部分数据。像我们实验室如何能满足准则要求又便于各部门操作?
最近有在寻求些有关于农药毒性报告的完整性资料,可有用的资料真的很少,现在真的不知道该怎么办了?

【液相色谱之家】你们的仪器数据完整性都恁上了吗 来自微友:药品检测-蕾微A:数据恢复卡—DRC。所有的信号,图谱和数据都缓存于高容量的植入式的压缩闪存卡。仪器和计算机故障时,防止数据丢失,一旦暂时通讯失败,自动进行恢复,一旦一直通讯失败,在软件 计算机 或仪器重启后,手动进行恢复。http://ng1.17img.cn/bbsfiles/images/2016/03/201603151202_587033_2960432_3.jpg微B:我们是要买网络版的软件,用不到DRC了吧!微C:网络版也要尽量配上,还是S家好,自带的恢复,A家网络版,是运行整个序列,然后打包上传,中间断电就没有数据了。那么数据收集卡是如何工作的呢? 所有的LC检测器都使用恒定频率传输数据,然而,计算机软件是成间隔的收集数据,这就需要运行过程中进行一个最小的数据缓冲以保证不损失数据,如果LC检测器中没有足够的空间来缓存原始数据,这样便会导致一旦仪器和计算机之间通讯中断,运行的数据便会被破坏或完全丢失,使用默认的数据恢复卡能够缓存运行的所有数据(包括所有信号,完整的图谱信息和原始数据)。数据从二级管阵列检测器到数据恢复卡,然后,从数据恢复卡传输到计算机软件中。如果产生暂时的网络连接失败或计算机不能持续连接数据,当网络恢复正常或计算机可以接受数据时,储存的数据便会自动传输到工作站。如果网络长时间中断,在网络恢复正常之后,运行恢复对话框可以将DRC中储存的完整数据恢复到计算机的数据目录中。这样无论段短时间的通讯失败还是需要重启软件,或者计算机及仪器长时间通讯失败,都不会损失任何数据。
怎样理解:具备相应的职责和权利,对测试结果的完整性和准确性负责?
怎样理解“具有相应的职责和权利,对测试结果的完整性和准确性负责”?
请教各位老师关于法规要求色谱类仪器数据完整性的问题,都是怎么做的?是购买的单机版合规软件还是网络版软件?向我们这种有不同品牌的色谱的话怎么办?
a 相应的职责是指对本单位的技术能力的有效性和检测结果的完整性的准确性负有责任,对检测报告承担相应的技术责任和民事责任。b 权力是指有权中止违反有效性、准确性和真实性的检测活动;有权抵制违反公正性和质量方针的不恰当干预。c 具体地讲可以从以下各方面了解本单位的相关技术能力。人员技术水平,学历资历和技术资格证书情况 实验设施和环境条件 检测设备配置情况,设备的完好性、量值溯源的有效性、正确的使用维护和有效运行及运行状态检查;技术标准、技术规范和检测方法的有效性;实验消耗材料的质量控制;抽样和样品管理的规范性;本单位的质量控制状况,能力验证和实验室之间比对情况;分包检测情况及变化。
新人一个,在编程序文件,《保护数据完整性和安全性的程序》没有头绪,求高人指点!
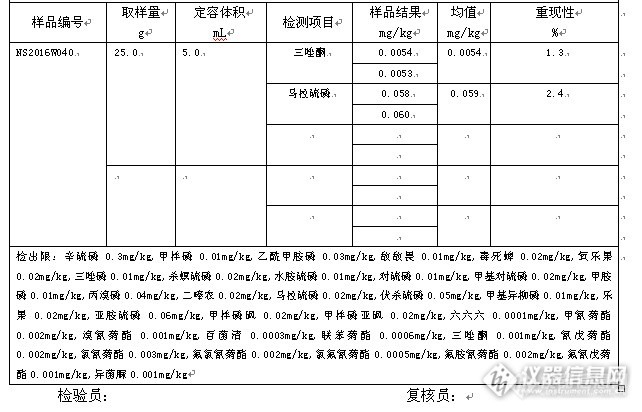
监督评审时提出的检验记录的完整性问题 2016年检验检测机构资质认定专项监督检查现场正式启动,现场检查是由省质监抽查被检单位,组织评审专家前往现场检查,我单位为我市第一家被抽查的实验室,监督评审时提出的其中一个问题是“编号NS2016W040的检验记录信息不全,缺标准物质信息。检验记录没编页码”。 一、不完整的检验报告 我们的检验记录由以下6部分组成:①检验报告、②检验结果报告书、③样品检验流转单、④气相色谱测定原始记录、⑤标液模板图、⑥样品色谱图等。http://ng1.17img.cn/bbsfiles/images/2016/07/201607171559_600822_1645480_3.jpg蔬菜样品编号NS2016W040的检验报告封皮。http://ng1.17img.cn/bbsfiles/images/2016/07/201607171559_600828_1645480_3.jpg检验报告的内容包括样品名称、受检单位、样品数量、抽样人、检验依据、样品编号等。http://ng1.17img.cn/bbsfiles/images/2016/07/201607171559_600823_1645480_3.jpg检验结果报告书包括检验项目、标准要求、检验结果、单项结论等。http://ng1.17img.cn/bbsfiles/images/2016/07/201607171559_600824_1645480_3.jpg样品检验流转单包括样品名称、样品状态、下达任务、发放样品、接受检验任务、返回样品、汇总结果、编制检验报告人等。http://ng1.17img.cn/bbsfiles/images/2016/07/201607171559_600825_1645480_3.jpg气相色谱仪测定原始记录包括样品编号、检测日期、执行标准、检测项目、气相条件、计算公式、取样量、定容体积、检测项目、样品结果、均值等。http://ng1.17img.cn/bbsfiles/images/2016/07/201607171559_600827_1645480_3.jpg有机磷与有机氯标液32种的色谱图,包括保留时间、峰面积、浓度等。http://ng1.17img.cn/bbsfiles/images/2016/07/201607171559_600826_1645480_3.jpg样品的检验结果色谱图。 二、新增的记录 监督评审时提出,色谱图张数较多,没有编页码,如果整理过程丢失一页,很难发现,应在软件上设置图谱的页码,如果软件上没有此功能,可手工在色谱图上编写页码。 标准物质有32种标液的模板色谱图,但没有标准物质的详细信息,比如标准物质的证书编号,有效期,如何配制等,要求在气相色谱原始记录上加入该信息,想着信息量太大,就另外设计一表,专门填写标准物质的详细信息见下表。将它附在气相色谱原始记录后面,这样就成为一份完整的检验报告了。http://ng1.17img.cn/bbsfiles/images/2016/07/201607171603_600832_1645480_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/07/201607171603_600833_1645480_3.jpg 这是样品的原始记录表http://ng1.17img.cn/bbsfiles/images/2016/07/201607171559_600830_1645480_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/07/201607171559_600831_1645480_3.jpg这是标准溶剂的记录表。三、结论 样品检测结果出来后,要填写检验报告,一份完整的检验报告会包括以下内容,样品结果判定单、样品检验流转单、样品的原始记录、标液模板色谱图、样品色谱图等,这其中重要一点是标准物质的信息,以往的样品检验报告,我们都缺少这一项,这次监督评审时,评审老师提出来,补充标准物质详细信息,有利于标准物质的可追溯性,使样品档案更加完整,所以每次评审都是一次学习机会,不断改进与完善质量体系,可以保证实验室的质量体系有效运行,有利于提高监管水平,做好我们的每一项工作。
完整性测试仪的IQ、OQ方案[~95087~]

http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_646706_2507958_3.gif除菌过滤器完整性测试的基本原理和常见问题活动时间:2014年 5月29日 14:30 主讲人: 何燕娜 何燕娜,拥有生物化工专业的硕士学位。现任默克密理博生物制药工艺部门高级技术服务代表,是自动化完整性测试操作的认证培训师http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_646706_2507958_3.gif【简介】 对于关键的除菌级过滤工艺而言,完整性测试是一种必要的手段,以确保过滤工艺的安全性。通过完整性测试,可以确定过滤器自身的完整性及正确安装,可以确保工艺中安装了正确的过滤器,可以确定所安装的过滤器符合制造商提供的标准,还可以确保过滤系统的密闭性等等。同时,进行完整性测试也是各国法规和审计的要求。这次讲座的目的是让大家了解完整性测试的各种方法和基本原理,并且能够基本解决测试过程中的常见问题。http://ng1.17img.cn/bbsfiles/images/2014/03/201403211104_493852_2507958_3.jpghttp://ng1.17img.cn/bbsfiles/images/2014/03/201403211104_493853_2507958_3.jpghttp://ng1.17img.cn/bbsfiles/images/2014/03/201403211104_493854_2507958_3.jpg-------------------------------------------------------------------------------1、报名条件:只要您是仪器网注册用户均可报名参加。2、参加及审核人数限制:限制报名人数为120人,审核人数100人。3、报名截止时间:2014年5 月29 日 14 :00 4、报名参会:http://simg.instrument.com.cn/meeting/images/20100414/baoming.jpg5、参与互动: *参会期间您还可以将有疑问的数据通过上传的形式给老师予以展示,并寻求解答*6、环境配置:只要您有电脑、外加一个耳麦就能参加。建议使用IE浏览器进入会场。7、提问时间:现在就可以在此帖提问啦,截至2014年 5月 29 日8、会议进入:2014年5月29日 14:00 就可以进入会议室9、特别说明:报名并通过审核将会收到1 封电子邮件通知函(您已注册培训课程),请注意查收,并按提示进入会议室 ! 为了使您的报名申请顺利通过,请填写完整而正确的信息哦~http://simg.instrument.com.cn/webinar/20110223/images/zb_11.gif注意:由于参会名额有限,如您通过审核,请您珍惜宝贵的学习交流机会,按时参加会议。如您临时有事无法参会,请您进入报名页面请假。无故不参会将会影响您下一次的参会报名。快来参加吧:我要报名》》》

http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_646712_2507958_3.gif除菌过滤器完整性测试的基本原理和常见问题活动时间:2014年 5月29日 14:30 主讲人: 何燕娜 何燕娜,拥有生物化工专业的硕士学位。现任默克密理博生物制药工艺部门高级技术服务代表,是自动化完整性测试操作的认证培训师http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_646712_2507958_3.gif【简介】 对于关键的除菌级过滤工艺而言,完整性测试是一种必要的手段,以确保过滤工艺的安全性。通过完整性测试,可以确定过滤器自身的完整性及正确安装,可以确保工艺中安装了正确的过滤器,可以确定所安装的过滤器符合制造商提供的标准,还可以确保过滤系统的密闭性等等。同时,进行完整性测试也是各国法规和审计的要求。这次讲座的目的是让大家了解完整性测试的各种方法和基本原理,并且能够基本解决测试过程中的常见问题。http://ng1.17img.cn/bbsfiles/images/2014/03/201403211104_493852_2507958_3.jpghttp://ng1.17img.cn/bbsfiles/images/2014/03/201403211104_493853_2507958_3.jpghttp://ng1.17img.cn/bbsfiles/images/2014/03/201403211104_493854_2507958_3.jpg-------------------------------------------------------------------------------1、报名条件:只要您是仪器网注册用户均可报名参加。2、参加及审核人数限制:限制报名人数为120人,审核人数100人。3、报名截止时间:2014年5 月29 日 14 :00 4、报名参会:http://simg.instrument.com.cn/meeting/images/20100414/baoming.jpg5、参与互动: *参会期间您还可以将有疑问的数据通过上传的形式给老师予以展示,并寻求解答*6、环境配置:只要您有电脑、外加一个耳麦就能参加。建议使用IE浏览器进入会场。7、提问时间:现在就可以在此帖提问啦,截至2014年 5月 29 日8、会议进入:2014年5月29日 14:00 就可以进入会议室9、特别说明:报名并通过审核将会收到1 封电子邮件通知函(您已注册培训课程),请注意查收,并按提示进入会议室 ! 为了使您的报名申请顺利通过,请填写完整而正确的信息哦~http://simg.instrument.com.cn/webinar/20110223/images/zb_11.gif注意:由于参会名额有限,如您通过审核,请您珍惜宝贵的学习交流机会,按时参加会议。如您临时有事无法参会,请您进入报名页面请假。无故不参会将会影响您下一次的参会报名。快来参加吧:我要报名》》》
最高管理者如何确保保持管理体系的完整性?如何具体实施?是指文件评审?还是指相应改动的地方要及时通知到相应岗位部门,做到及时有效?
近期准备FDA检查准备,FDA要求色谱数据等要有审计追踪,确保数据完整性,咨询了Agilengt公司,他们说需要把单机版软件换成网络版才能符合要求 ,一个小网络版也要40万左右,这是真的吗? FDA它的要求给如何理解?
过滤器完整性验证包括哪些方面?我们怎么没有做过这个验证呢?[em52]