推荐厂家
暂无
暂无



 400-807-5250
400-807-5250
 留言咨询
留言咨询

 400-617-6366
400-617-6366
 留言咨询
留言咨询

 400-617-6366
400-617-6366
 留言咨询
留言咨询



请问有哪位大侠做植酸酶活力测试的吗?小弟按照国标GBT 18634-2009方法做的,吸光度值刚开始比较低,到后来越来越高,到10次后才稳定下来!请问大家碰到过这样的问题吗?
请教关于酶活力测定过程中加福林试剂后出现沉淀问题在用福林法测定酱油大曲酶活力过程中,在最后一步加入福林试剂后出现白色沉淀,这白色沉淀能自动慢慢沉淀下来。那位高手能指点一下这是那方面出现问题?
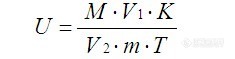
酶活力的测定方法(1)葡萄糖标准曲线的绘制取8只洗净烘干的20 mL具塞刻度试管,编号后分别吸取0.0 mL ~ 1.4 mL葡萄糖标液用蒸馏水定容至2 mL,配置成一系列不同浓度的葡萄糖溶液。充分摇匀后,向各试管中加入1.5 mLDNS溶液,摇匀后沸水浴5 min,取出冷却后用蒸馏水定容至20 mL,充分混匀。在540 nm波长下,以1号试管溶液作为空白对照,调零点,测定其它各管溶液的吸光度值并记录结果。以葡萄糖含量为横坐标,以对应的吸光度值为纵坐标,绘制出葡萄糖标准曲线。(2)滤纸酶活力的测定取4支洗净烘干的20 mL具塞刻度试管,编号后各加入0.5 mL酶液和1.5 mL 0.05 mol/L pH 4.5的柠檬酸缓冲液,向1号试管中加入1.5 mL DNS溶液以钝化酶活性,作为空白对照,比色时调零用。将4支试管同时在50℃水浴中预热5 min ~ 10 min,再各加入滤纸条50 mg(定量滤纸,约1 cm × 6 cm),50℃水浴中保温1 h后取出立即向2、3、4号试管中各加入1.5 mL DNS溶液以终止酶反应,充分摇匀后沸水浴5 min,取出冷却后用蒸馏水定容至20 mL,充分混匀。以1号试管溶液为空白对照调零点,在540 nm波长下测定2、3、4号试管液的吸光度值并记录结果。根据3个重复吸光度的平均值,在标准曲线上查出对应的葡萄糖含量,按下式计算出滤纸酶活力(U/g)。在上述条件下,每小时由底物生成1 μmol葡萄糖所需的酶量定义为一个酶活力单位(U)。 http://ng1.17img.cn/bbsfiles/images/2014/10/201410171615_518835_2770543_3.jpg 式中:U—滤纸酶活力(U/g); M—葡萄糖含量(mg);V1—酶液定容总体积(mL); K—5.56[font=宋体


