推荐厂家
暂无
暂无




 400-860-5168转4226
400-860-5168转4226
 留言咨询
留言咨询

 400-860-5168转4226
400-860-5168转4226
 留言咨询
留言咨询

 400-860-5168转4226
400-860-5168转4226
 留言咨询
留言咨询



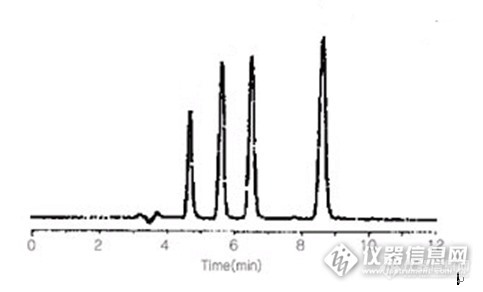
生育酚分析http://ng1.17img.cn/bbsfiles/images/2015/05/201505121416_545699_2452211_3.png生育酚共有α、β、γ、δ四种,分子结构包括苯并杂环、一个较长的碳链,其差别仅在苯环上甲基的数量和位置,其中α-生育酚具有三个甲基,β-、γ-生育酚具有两个甲基、互为同分异构体,而δ-生育酚有一个甲基。极性较弱,属脂溶性物质,同时又能溶于甲醇/水,分子量小于500,所以选色谱柱时也许有两种选择:正相柱和反相柱。填料孔径则可锁定在100Å左右。在实际分析中,反相C18柱仅能分出三个峰(如图一):δ峰、γ和β共同出的峰、α峰。γ和β生育酚的差别仅在于苯环上甲基的位置不同,以“分配作用”为作用模式的C18对它们选择性基本没有差异,而所用的流动相为95%以上的甲醇水溶液(甲醇含量太低时,保留时间太长),这种溶剂体系对这两种生育酚的溶解性也基本没有差异,所以γ-和β-生育酚在反相模式下无法分离。http://ng1.17img.cn/bbsfiles/images/2015/05/201505121417_545701_2452211_3.png正相的Silica柱和氨基柱则对化合物上的基团具有选择性,像γ-和β-生育酚结构上这样细小的差别就能被分辨,从而达到分离。http://ng1.17img.cn/bbsfiles/images/2015/05/201505121419_545702_2452211_3.png在实际分析中,C18柱常常用于常规生育酚总量测定,因为总量测定时并不需要分开γ和β生育酚;而正相柱则常用于生育酚组成的测定。
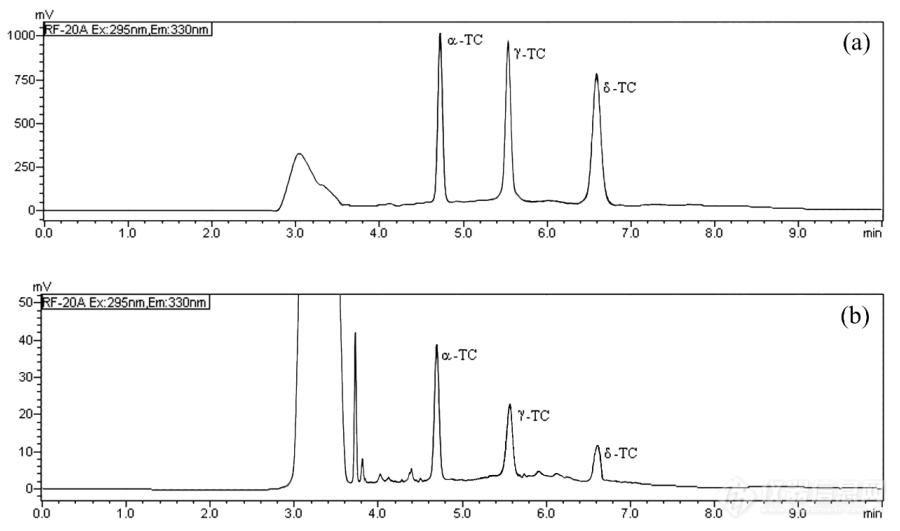
正相[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]条件下分析三种生育酚。色谱柱为:LiChrosorb Si 60 (5 μm) 色谱柱 (4.6 mm ID × 250 mm),柱温 40 °C 等度条件,流动相由正己烷/乙酸乙酯 (90:10 v / v ) 组成。进样量为 20 μL,流速为 0.8 mL min -1. 荧光激发和发射波长分别为 295 nm 和 330 nm。牛奶样品前处理过程:将 2 mL 牛奶的等分试样倒入 10 mL 深色螺旋杯容器中(以保护 TOC 免受潜在的氧化),加入 2 mL n加入正己烷,加盖并在室温下混合 10 秒。然后,进一步添加 2 mL 甲醇 KOH (2 N),并通过用氮气吹扫空气空间从容器中除去氧气。立即将容器盖上盖子并再次在室温下混合 10 秒。最终溶液在 20 °C 下超声处理 10 分钟。详见[url]https://doi.org/10.3390/molecules26154645[/url][img=,690,407]https://ng1.17img.cn/bbsfiles/images/2022/09/202209231500475476_5272_2641053_3.png!w690x407.jpg[/img]
混合检测目前有国标[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]检测法但矫正因子是按照α生育酚计算,但实际上混合生育酚主要成分有四种,它们的相对矫正因子应当是不一样的,我们用液相外标法计算时原先也用α生育酚做定量矫正因子,后来发现用δ生育酚做定量矫正因子时与α生育酚做定量矫正因子有很大的误差,论坛里有专业做生育酚检测的朋友吗,你们平时的检测是按照什么方法,欢迎生育酚生产厂家参加讨论


