推荐厂家
暂无
暂无
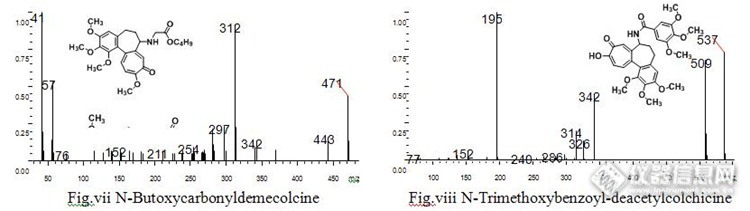
秋水仙碱类生物碱的质谱裂解规律探究摘要:采用气相色谱质谱(GC/MS)研究了八种秋水仙碱类生物碱化合物的质谱裂解途径和机理。发现部分碎片离子一致,其主要的裂解途径是通过四元环过渡态氢重排失去侧链生成离子m/z340,由于结构中的七元环上有羰基,而七元环相对来讲没有六元环稳定,所以其会进一步失去羰基的CO生成离子m/z 312,保持了较高的稳定性,所以在质谱图上表现出较高的丰度,同时化合物还通过失去甲氧基自由基及甲基自由基得到其他对应的碎片离子峰。关键词:秋水仙碱;裂解规律;气质联用;生物碱秋水仙碱类生物碱是一类很重要的有机化合物,秋水仙碱是1820年于百合科植物秋水仙中发现的一种重要的卓酚酮类生物碱(1)。由于秋水仙碱及其类似物的特殊生理活性和药用价值,它们一直受到广泛的关注。因其特殊的结构和强抗癌活性,近几年有关秋水仙碱作用机制的研究异常活跃。临床上常作为痛风性关节炎急性发作和某些癌症治疗的首选药(2-5)。当秋水仙碱的摄入量过多将会导致死亡,所以也受到司法鉴定的关注。同时秋水仙碱在生物学上更重要的用途是作为多倍体诱导剂诱导多倍体的发生(6-10)。目前关于秋水仙碱的检测方法已有较多报道(11-14)。色谱质谱法由于其特异性,具有较好的分离度以及较高的灵敏度且能提供更多的样品信息而被广泛应用,对于生物碱类化合物的质谱裂解规律及机理已有较多的文献报道(15-21)。而关于秋水仙碱类生物碱的质谱裂解机理和规律还未见相关报道,电子轰击离子源由于具有较高的电离能,能够获得更加丰富的质谱信息而被广泛应用,所以本文通过气相色谱质谱联用法对多种秋水仙碱类化合物在电子轰击离子源下的质谱裂解途径和规律做以阐释总结,旨在为此类化合物的组分鉴定,结构确认提供理论指导依据。1试验部分1.1 仪器与试剂GCMS-QP2010UItra(日本Shimadzu公司);Demecolcine、Deacetylcolchicine、2-Demethylthiodemecolcine、N-Butoxycarbonyldemecolcine、N-Deacetylisocolchicine、N-Acetylcolchamine、N-Trifluoroacetyldemecolcine标准品2.2 仪器条件1.2.1 色谱条件 色谱柱:Agilent DB-1MS弹性石英毛细管柱(30m*0.32mm*0.25um);载气:He(纯度99.999%);恒压模式:48.0kPa;初始温度100℃,以10℃/min的速率升至300℃恒温10min;分流进样,分流比10:1;进样量0.2ul,进样口温度300℃,接口温度300℃。1.2.2 质谱条件 离子化方式:EI(电子轰击离子源),离子化电压70ev,离子源温度250℃,离子扫描范围:m/z 32~600。1.2 实验方法称取0.25mg标准品用1ml甲苯溶解,分别进行GC/MS全扫描,获得八种化合物EI离子源下的质谱图。八种化合物及其对应的质谱图如下:http://ng1.17img.cn/bbsfiles/images/2015/08/201508211541_562003_2359621_3.jpghttp://ng1.17img.cn/bbsfiles/images/2015/08/201508211541_562004_2359621_3.jpghttp://ng1.17img.cn/bbsfiles/images/2015/08/201508211541_562005_2359621_3.jpghttp://ng1.17img.cn/bbsfiles/images/2015/08/201508211541_562006_2359621_3.jpg2 结果与讨论2.1 Deacetylcolchicine的质谱裂解途径去乙酰秋水仙碱Deacetylcolchicine的质谱图见图Fig.i,谱图中基峰为分子离子峰m/z 357,表明其分子结构具有较高的稳定性。谱图中有明显的m/z 340碎片离子,其生成是由于氨基具有较强的质子亲合能,β位的氢通过四元环过渡态重排到氨基上,然后脱去中性分子NH3,两个孤电子成对生成烯键得到碎片离子m/z 340。由于分子结构中具有环庚三烯酮结构,所以其可以发生进一步的裂解失去CO中性分子,而形成六元环稳定结构,得到碎片离子m/z 312,为奇电子离子,具有较高的丰度。由分子离子峰可直接失去CO中性分子得到碎片离子m/z 329,当苯环上的一对π电子被电离后,离子m/z 329可以发生α断裂,失去甲基自由基,得到离子m/z 314,该离子通过氢过渡态重排失去NH3得到离子m/z 297(其生成也有可能是m/z 312失去甲基自由基)。该离子失去中性分子CO后生成离子m/z 269,该离子再失去甲基自由基后得到碎片离子m/z 254,该离子可进一步失去甲基自由基生成离子m/z 239,后失去一分子CO得到离子m/z 211,再失去一分子CO得到离子m/z 183。游离基中心定域在氨基上,游离基中心孤电子强的配对倾向诱导发生α断裂失去氢自由基得到碎片离子m/z 328。由分子离子峰可以失去甲氧基得到碎片离子m/z 326,该离子进一步失去CO得到离子m/z 298具有较高的丰度,后失去甲基自由基生成离子m/z 281。可能的质谱裂解途径见Fig. 1http://ng1.17img.cn/bbsfiles/images/2015/08/201508211451_561952_2359621_3.jpg图1 Deacetylcolchicine的质谱裂解可能的质谱裂解途径Fig. 1 Possible cleavage pathways of Deacetylcolchicine2.2 N-Deacetylisocolchicine的质谱裂解途径去乙酰异秋水仙碱N-Deacetylisocolchicine的质谱图见图Fig.ii,其结构上与去乙酰秋水仙碱有细微的差异,仅是甲氧基取代基与羰基的位置发生了互换,其质谱图中基峰为分子离子峰m/z 357,分子离子峰失去甲基自由基,生成碎片离子m/z 342,该碎片离子失去中性分子CO后生成离子m/z 314,后通过四元环过渡态β位氢重排失去小分子NH3生成离子m/z 297,由分子离子失去中性分子CO后生成离子m/z 329,当游离基中心定域在氨基上自由基强烈的配对倾向诱导发生α断裂失去氢自由基生成碎片离子m/z 328。由分子离子还可直接失去甲氧基自由基生成碎片离子m/z 326,其可以失去CO得到离子m/z 298,具有较高丰度,分子内氢重排失去甲醛后生成离子m/z 268。当分子离子经过四元环过渡态氢重排后失去NH3可生成离子m/z340,该离子进一步裂解失去CO中性分子得到离子m/z 312,稳定的六元环结构提高了离子的稳定性,所以具有较高的丰度,该离子失去甲氧基后生成离子m/z 281,可进一步裂解得到离子m/z 266,或者通过氢重排失去甲醛生成离子m/z 282,可进一步裂解生成离子m/z 267。m/z 312亦可失去甲基自由基得到离子m/z
求助标准谱图,秋水仙碱。哪位大虾有电子版的红外光谱集啊?
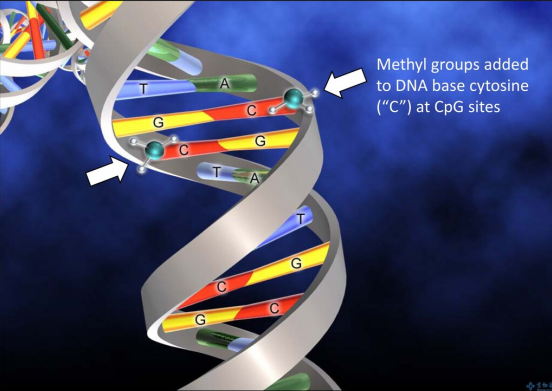
(一)烷化剂 是栽培作物诱发突变的最重要的一类诱变剂。药剂带有一个或多个活泼的烷基。通过烷基置换,取代其它分子的氢原子称为"烷化作用"所以这类物质称烷化剂。 烷化剂分为以下几类: 1. 烷基磺酸盐和烷基硫酸盐 代表药剂:甲基磺酸乙酯(EMS)、硫酸二乙酯(DES) 2. 亚硝基烷基化合物 代表药剂:亚硝基乙基脲(NEH)、N-亚硝基-N-乙基脲烷(NEU) 3. 次乙胺和环氧乙烷类 代表药剂:乙烯亚胺(EI) 4. 芥子气类 氮芥类、硫芥类 烷化剂的作用机制--烷化作用 作用重点是核酸,导致DNA断裂、缺失或修补。 (二)核酸碱基类似物 这类化合物具有与DNA碱基类似的结构。 代表药剂: 5-溴尿嘧啶(BU)、5-溴去氧尿核苷(BudR) 为胸腺嘧啶(T)的类似物 2-氨基嘌呤(AP) 为腺嘌呤(A)的类似物 马来酰肼(MH) 为尿嘧啶(U)的异构体 作用机制:作为DNA的成份而渗入到DNA分子中去,使DNA复制时发生配对错误,从而引起有机体变异。 (三)其它诱变剂 亚硝酸 能使嘌呤或嘧啶脱氨,改变核酸结构和性质,造成DNA复制紊乱。HNO2还能造成DNA双链间的交联而引起遗传效应。 叠氮化钠(NaN3) 是一种呼吸抑制剂,能引起基因突变,可获得较高的突变频率,而且无残毒。 用秋水仙素诱导多倍体。 秋水仙素是从百合科植物秋水仙的器官和种子中提取出来的一种剧毒的植物碱。纯品为无色或淡黄色针状结晶,熔点155℃,有苦味,易溶于冷水、酒精、氯仿和甲醛。通常用水或酒精作溶媒。 (1)秋水仙素诱导多倍体的原理 秋水仙素与正在分裂的细胞接触后,可抑制微管的聚合过程,不能形成纺锤丝,使染色体无法分向两极,从而产生染色体加倍的核。 适宜浓度的秋水仙素溶液,能阻碍纺锤丝的形成,但对染色体结构无明显影响。处理的细胞在一定时间内可恢复正常,重新进行分裂。 (2)秋水仙诱导多倍体应注意的问题 ①注意诱变材料的选择 选主要经济性状优良的品种; 选染色体组数少的品种因为倍性高的种在进化过程中已经利用了它的多倍性。 最好选能单性结实的品种因为染色体多倍化后,常会使育性降低。 尽量选多个品种处理因为不同的种、品种、类型遗传基础不同,多倍化后的表现也不同。 ②注意处理部位的选择 处理的组织应该是旺盛分裂的组织。如萌动的种子、正在膨大的芽、根尖、幼苗、嫩枝生长点、花蕾等。 ③注意药剂浓度和处理时间的选择 溶液的浓度不宜过高或过低。过高,会引起伤害,以至致死;过低,又不起作用。一般采用临界范围内的高浓度、短时间处理。 医学教.育网搜集整理 通常,草本浓度较低,木本浓度较高。 果树、树木:1-1.5%蔬菜、草本花卉:0.01-0.2% 王鸣等(1960)在甘蓝、白菜、南瓜、萝卜上试验表明,在0.01-0.2%的范围内,随浓度增高,引变的百分率也显著提高。 处理时间以细胞分裂周期为转换。 ④注意被处理植物的生长条件 处理后,用清水冲洗,除去残留药物,并为植株生长提供良好的条件,便于植株恢复生长。 外部条件中最重要的是温度,一般25-30℃。 (3)诱导方法 ①浸渍法 可用溶液浸渍幼苗、新梢、插条、接穗、种子及球根类蔬菜、花卉等材料。为避免蒸发,宜加盖,避光。 一般发芽种子处理数小时至3d或多至10d左右。秋水仙碱能阻碍根系的发育,处理后要用清水洗净后再播种。发芽种子的胚根,处理后往往受到抑制,发根较慢,为利于根的生长,可在药液中添加适当生长素。 处理插条、接穗一般1-2d。处理后也要用清水洗干净。 处理幼苗时,为避免根系受害,可将盆钵架起来倒置,使茎端生长点浸入秋水仙碱溶液中。 ②涂抹法 把秋水仙碱按一定浓度配成乳剂,涂抹在幼苗或枝条的顶端,处理部位要适当遮盖,以减少蒸发和避免雨水冲洗。 ③滴液法 对较大植株的顶芽、腋芽处理时可采用此法。常用的水溶液浓度为0.1%~0.4%,每日滴一至数次,反复处理数日,使溶液透过表皮渗入组织内部。如溶液在上面停不住时,可将小片脱脂棉包裹幼芽,再滴加溶液,浸湿棉花。 ④套罩法 保留新梢的顶芽,除去顶芽下面的几片叶,套上一个防水的胶囊,内盛有含1%秋水仙碱的0.65%的琼脂,经24h即可去掉胶囊。这种方法的优点是不需加甘油,可避免甘油引起药害。 医.学教育网搜集整理 ⑤毛细管法 将植株的顶芽、腋芽用脱脂棉或纱布包裹后,将脱脂棉与纱布的另一端浸在盛有秋水仙碱溶液的小瓶中,小瓶置于植株旁,利用毛细管吸水作用逐渐把芽浸透,此法一般多用于大植株上芽的处理。 此外,还有注射法、喷雾法等。 秋水仙素诱导也与物理辐射等方法结合使用。如山川邦夫(1973)报道,将好望角苣苔属中的一些种用秋水仙碱处理11d,再用0.05Gy的X射线照射可提高加倍株的出现率。在单独用秋水仙碱处理时为30%,而兼用X射线照射时可提高到60%,并且在取得的多倍体植株中发现有两株变成八倍体。他们认为,这是由于秋水仙碱的处理,使多倍体混杂于二倍体性细胞群中,二倍体细胞由于先开始分裂,所以就被X射线淘汰了。 秋水仙素诱导只能产生偶数多倍体,且为同源多倍体。 有性杂交可产生奇数多倍体、异源多倍体。异源多倍体具有更高的杂合性、育性;二倍体基因渗入,创造遗传多样性,得到杂合多倍性群体。





 400-860-5168转0812
400-860-5168转0812
 留言咨询
留言咨询

 留言咨询
留言咨询

 400-860-5586
400-860-5586
 留言咨询
留言咨询


